文档内容
第 35 讲 分子的性质 配合物与超分子
[复习目标] 1.理解分子的极性。2.掌握范德华力的含义及对物质性质的影响。 3.理解氢键
的含义, 能列举存在氢键的物质, 并能解释氢键对物质性质的影响。4.理解配位键的含义。
5.了解超分子的概念。
考点一 键的极性与分子极性
1.键的极性
(1)极性键与非极性键的比较
极性键 非极性键
成键原子 ________种元素的原子间 ________元素的原子间
电子对 ________偏移(电荷分布不均匀) ________偏移(电荷分布均匀)
成键原子的电性 H—Cl 呈电中性
思考 如何判断共价键极性的强弱?
_______________________________________________________________________________
(2)键的极性对化学性质的影响
键的极性对羧酸酸性大小的影响实质是通过改变羧基中羟基的______而实现的,羧基中羟基
的极性越大,越__________________,则羧酸的酸性越强。
①与羧基相邻的共价键的极性越大,羧基中____________________,则羧酸的酸性越强。
②烷基是推电子基团,从而减小羧基中羟基的________,导致羧酸的酸性减小。一般地,烷
基越长,推电子效应________,羧酸的酸性_________________________________________。
2.极性分子和非极性分子
(1)概念
极性分子:分子的正电中心和负电中心______,键的极性的向量和________零。
非极性分子:分子的正电中心和负电中心________,键的极性的向量和________零。
(2)极性分子和非极性分子的判断方法
①A—A型分子一定是非极性分子、A—B型分子一定是极性分子。
②判断AB 型分子极性的两条经验规律
n
a.中心原子A化合价的绝对值等于该元素原子最外层电子数,则为非极性分子,反之则为
极性分子。b.中心原子A没有孤电子对,则为非极性分子,反之则为极性分子。
一、有关羧酸酸性强弱的判断及归因分析
1.试比较下列有机酸的酸性强弱。
①CFCOOH ②CCl COOH ③CHCl COOH ④CHClCOOH ⑤CHCOOH
3 3 2 2 3
⑥CHCHCOOH
3 2
_______________________________________________________________________________
2.酸性:氟乙酸大于氯乙酸的原因是______________________________________________
_______________________________________________________________________________
_______________________________________________________________________________
。
3.酸性:甲酸大于乙酸的原因是__________________________________________________
_______________________________________________________________________________
。
二、分子极性的判断
4.下列分子P 、C 、 Cl 、NO、HO 、NO 、SO 、CHCl 、CS 、C H 、SO 、 BF 、
4 60 2 2 2 2 2 2 2 2 2 2 3 3
HCN 、 HCHO 、 PCl 、 PCl 属 于 极 性 分 子 的 是
5 3
_____________________________________________ ; 属 于 非 极 性 分 子 的 是
_____________________________________________________________
_______________________________________________________________________________
。
考点二 分子间作用力
1.分子间作用力
(1)范德华力、氢键的对比
范德华力 氢键
H与N、O、F等电负性很
作用微粒 分子或原子(稀有气体分子)
大的原子
分类 - 分子内氢键和分子间氢键
特征 ____方向性和饱和性 ____饱和性和方向性
强度 共价键>________>____________
影响其强度的因素 ①组成和结构相似的物质,相对分 X—H…Y强弱与X和Y子质量________,范德华力越大;
②分子的极性______,范德华力越 的电负性有关
大
对物质性质的影响 主要影响物理性质(如熔、沸点)
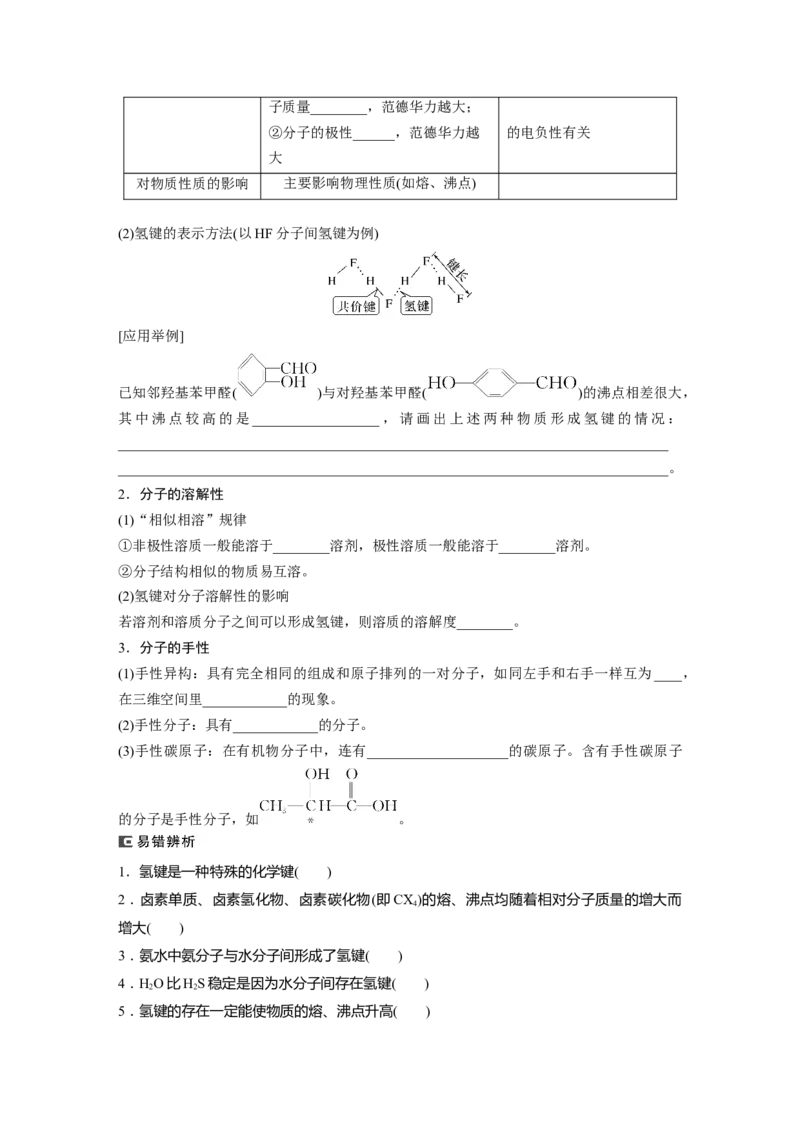
(2)氢键的表示方法(以HF分子间氢键为例)
[应用举例]
已知邻羟基苯甲醛( )与对羟基苯甲醛( )的沸点相差很大,
其中沸点较高的是__________________,请画出上述两种物质形成氢键的情况:
______________________________________________________________________________
______________________________________________________________________________。
2.分子的溶解性
(1)“相似相溶”规律
①非极性溶质一般能溶于________溶剂,极性溶质一般能溶于________溶剂。
②分子结构相似的物质易互溶。
(2)氢键对分子溶解性的影响
若溶剂和溶质分子之间可以形成氢键,则溶质的溶解度________。
3.分子的手性
(1)手性异构:具有完全相同的组成和原子排列的一对分子,如同左手和右手一样互为____,
在三维空间里____________的现象。
(2)手性分子:具有____________的分子。
(3)手性碳原子:在有机物分子中,连有____________________的碳原子。含有手性碳原子
的分子是手性分子,如 。
1.氢键是一种特殊的化学键( )
2.卤素单质、卤素氢化物、卤素碳化物(即CX)的熔、沸点均随着相对分子质量的增大而
4
增大( )
3.氨水中氨分子与水分子间形成了氢键( )
4.HO比HS稳定是因为水分子间存在氢键( )
2 2
5.氢键的存在一定能使物质的熔、沸点升高( )一、分子间作用力与物质性质原因分析
1.下列说法正确的是( )
A.可燃冰(CH·8H O)中甲烷分子与水分子间形成了氢键
4 2
B.“X—H…Y”三原子不在一条直线上时,不可能形成氢键
C.萃取剂CCl 的沸点高于CH 的沸点
4 4
D.卤素单质、碱金属单质的熔、沸点均随着摩尔质量的增大而升高
2.下列关于氢键的说法正确的是( )
A.每一个水分子内含有两个氢键
B.冰和干冰分子间都存在氢键
C.DNA中的碱基互补配对是通过氢键来实现的
D.HO是一种非常稳定的化合物是因为水分子间可以形成氢键
2
3.有关分子的溶解性,解答下列各题:
(1)H O 难溶于CS,简要说明理由_______________________________________________
2 2 2
______________________________________________________________________________。
(2)NH 、CHCHOH、CHCHO都极易溶于水的原因是______________________________
3 3 2 3
______________________________________________________________________________。
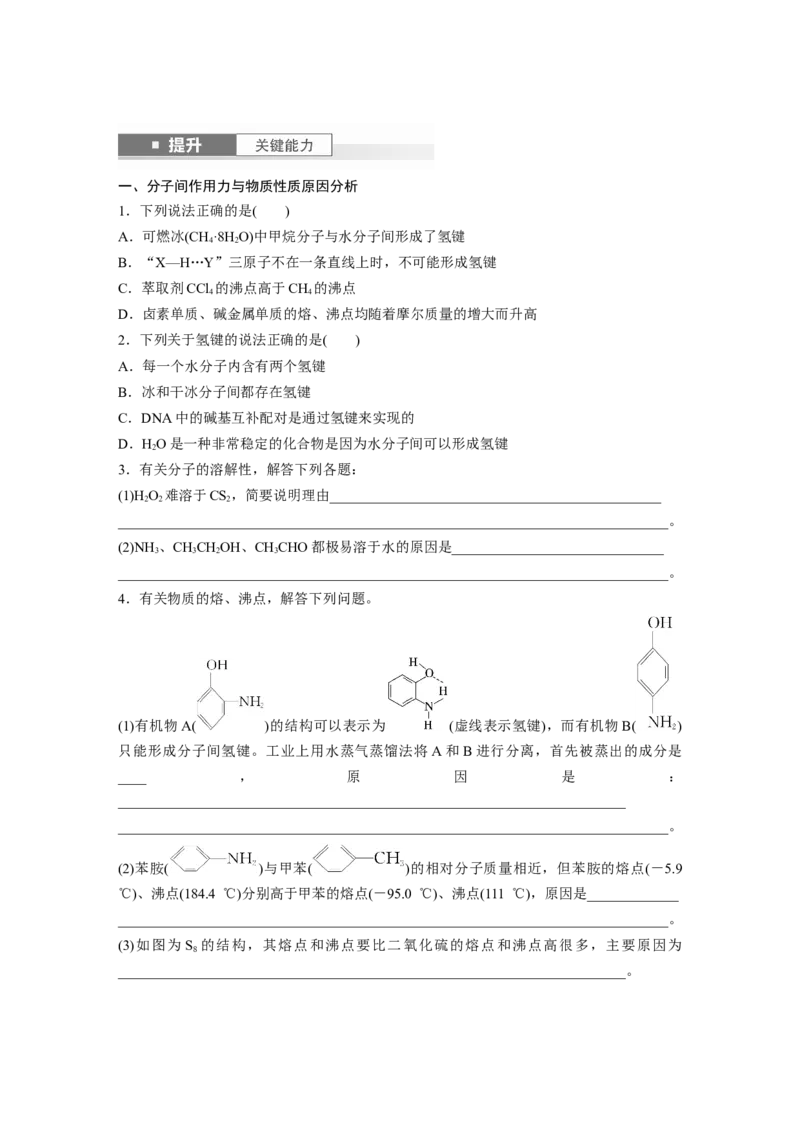
4.有关物质的熔、沸点,解答下列问题。
(1)有机物A( )的结构可以表示为 (虚线表示氢键),而有机物B( )
只能形成分子间氢键。工业上用水蒸气蒸馏法将A和B进行分离,首先被蒸出的成分是
____ , 原 因 是 :
________________________________________________________________________
______________________________________________________________________________。
(2)苯胺( )与甲苯( )的相对分子质量相近,但苯胺的熔点(-5.9
℃)、沸点(184.4 ℃)分别高于甲苯的熔点(-95.0 ℃)、沸点(111 ℃),原因是_____________
______________________________________________________________________________。
(3)如图为 S 的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为
8
________________________________________________________________________。(4)在CO 低压合成甲醇反应(CO +3H===CHOH+HO)所涉及的4种物质中,沸点从高到
2 2 2 3 2
低的顺序为____________________________________________________________________,
原因是________________________________________________________________________
______________________________________________________________________________。
二、手性碳的判断
5.(2023·海南,12改编) 闭花耳草是海南传统药材,具有消炎功效。车叶草苷酸是其活性
成分之一,结构简式如图所示。用“*”标出分子中的手性碳原子。
考点三 配合物、超分子
1.配位键
(1)形成:由一个原子单方面提供____________而另一个原子接受孤电子对形成的共价键,
即“电子对给予—接受”键被称为________。
(2)表示方法:常用“____”来表示配位键,箭头指向接受孤电子对的原子,如NH可表示
为________________,在NH中,虽然有一个N—H形成过程与其他3个N—H形成过程不
同,但是一旦形成之后,4个共价键就完全________。
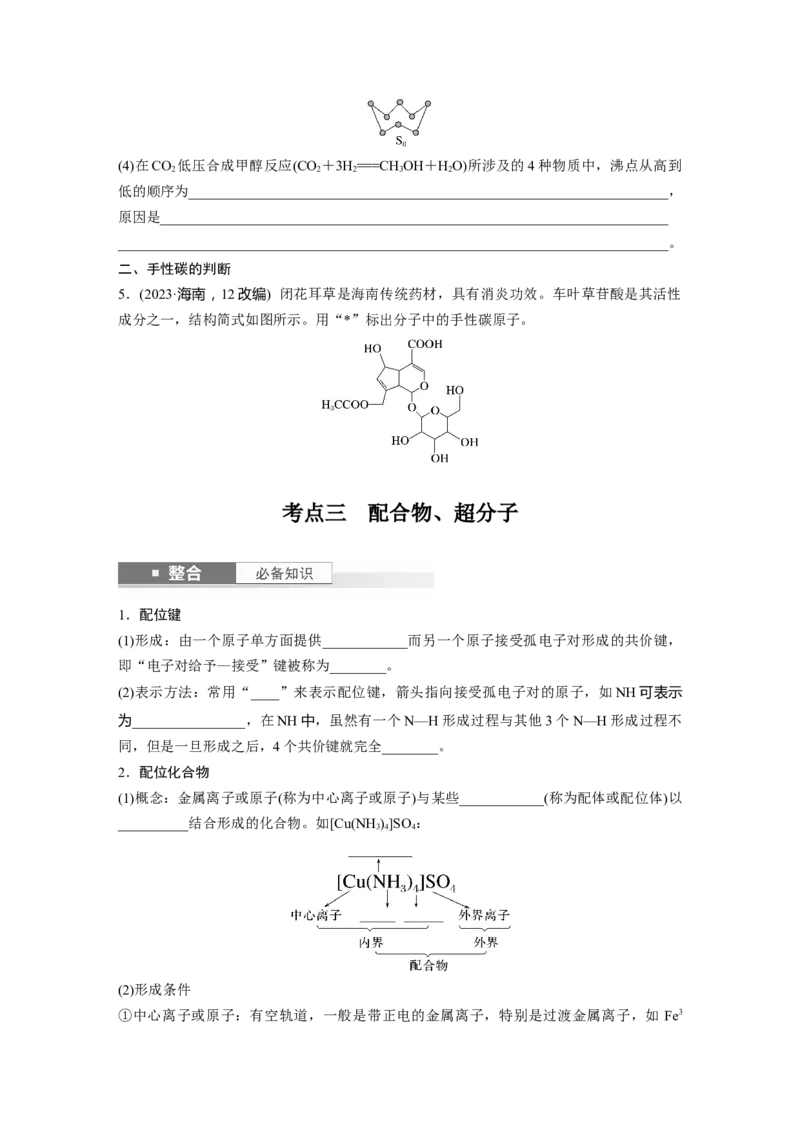
2.配位化合物
(1)概念:金属离子或原子(称为中心离子或原子)与某些____________(称为配体或配位体)以
__________结合形成的化合物。如[Cu(NH )]SO :
3 4 4
(2)形成条件
①中心离子或原子:有空轨道,一般是带正电的金属离子,特别是过渡金属离子,如 Fe3+、Cu2+、Zn2+、Ag+等,但也有电中性的原子等。
②配位体:其中的配位原子(配位体中直接同中心离子或原子配合的原子)有孤电子对。配位
体可以是分子,如CO、NH 、HO等,也可以是离子,如F-、Cl-、Br-、I-、CN-、SCN
3 2
-、OH-等。
(3)配位原子及配位数
①配位原子:配位体中提供孤对电子的原子叫配位原子,如:HO中的O原子,NH 中的N
2 3
原子。
②配位数:作为配位体直接与中心原子结合的离子或分子的数目,即形成的配位键的数目称
为配位数。如:[Cu(NH )]2+的配位数为4,[Ag(NH)]+的配位数为2。
3 4 3 2
(4)内界和外界:配合物分为内界和外界,其中中心离子或原子与配位体组成的部分称为内
界,与内界发生电性匹配的阳离子(或阴离子)称为外界,如:[Cu(NH )]SO 的内界是
3 4 4
[Cu(NH )]2+,外界是SO,配合物在水溶液中电离成内界和外界两部分。
3 4
即:[Cu(NH )]SO ===[Cu(NH )]2++SO,而内界很难电离,其电离程度很小,[Cu(NH )]2+
3 4 4 3 4 3 4
Cu2++4NH 。
3
3.超分子
(1)概念
超分子是由__________________的分子通过________________形成的分子聚集体。
(2)超分子内分子间的作用力
多数人认为,超分子内部分子之间通过非共价键相结合,包括氢键、静电作用、疏水作用以
及一些分子与金属离子形成的弱配位键等。
(3)超分子的两个重要特征是____________和________。
(4)超分子的应用
在分子水平上进行分子设计,有序组装甚至复制出一些新型的分子材料。
1.配位键实质上是一种特殊的共价键( )
2.提供孤电子对的微粒既可以是分子,也可以是离子( )
3.有配位键的化合物就是配位化合物( )
4.配位化合物都很稳定( )
5.在配合物[Co(NH )Cl]Cl 中的Cl-均可与AgNO 反应生成AgCl沉淀( )
3 5 2 3
6.Ni(CO) 是配合物,它是由中心原子与配体构成的( )
4
一、配合物
1.关于化学式为[TiCl(H O) ]Cl ·H O的配合物,下列说法正确的是( )
2 5 2 2
A.配位体是Cl-和HO,配位数是8
2
B.中心离子是Ti4+,配离子是[TiCl(H O) ]2+
2 5C.内界和外界中Cl-的数目比是1∶2
D.在1 mol该配合物中加入足量AgNO 溶液,可以得到3 mol AgCl沉淀
3
2.(2023·烟台模拟)过渡金属配合物的一些特有性质的研究正受到许多研究人员的关注,因为
这方面的研究无论是理论上还是工业应用上都有重要意义。氯化铁溶液用于检验食用香精乙
酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示。下列有关该配离子的说法正确
的是( )
A.1 mol该配离子中含有π键的个数是6×6.02×1023
B.该配离子中碳原子的杂化类型均为sp2杂化
C.该配离子含有的非金属元素中电负性最大的是碳
D.该配离子中含有的化学键有离子键、共价键、配位键
3.回答下列问题:
(1)将白色CuSO 粉末溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配位数是4的
4
配 离 子 , 请 写 出 生 成 此 配 离 子 的 离 子 方 程 式 :
_________________________________________,
蓝色溶液中的阳离子内存在的全部化学键类型有________________。1 mol该阳离子中含σ
键个数为________。
(2)CuSO ·5H O(胆矾)中含有水合铜离子而呈蓝色,写出胆矾晶体中水合铜离子的结构简式
4 2
(必须将配位键表示出来):________________________________________________________。
(3)向CuSO 溶液中滴加氨水会生成蓝色沉淀,再滴加氨水到沉淀刚好全部溶解可得到深蓝
4
色溶液,继续向其中加入极性较小的乙醇可以析出深蓝色的[Cu(NH )]SO ·H O晶体。下列
3 4 4 2
说法不正确的是_________(填字母)。
a.[Cu(NH )]SO 的组成元素中电负性最大的是N元素
3 4 4
b.CuSO 晶体及[Cu(NH )]SO ·H O中S原子的杂化方式均为sp3
4 3 4 4 2
c.[Cu(NH )]SO 所含有的化学键有离子键、共价键和配位键
3 4 4
d.NH 分子内的H—N—H键角大于HO分子内的H—O—H 键角
3 2
e.SO的空间结构为正四面体形
f.[Cu(NH )]2+中,N原子是配位原子
3 4
g.NH 分子中氮原子的杂化轨道类型为sp2
3
二、超分子
4.冠醚是皇冠状的分子,它能否适配碱金属离子与其空腔直径和离子直径有关。二苯
并-18-冠-6与K+形成的配离子的结构如图所示。下列说法错误的是( )冠醚 冠醚空腔直径/pm 适合的粒子(直径/pm)
15-冠-5 170~220 Na+(204)
18-冠-6 260~320 K+(276)、Rb+(304)
21-冠-7 340~430 Cs+(334)
A.冠醚可以用来识别碱金属离子
B.二苯并-18-冠-6也能适配Li+
C.该冠醚分子中碳原子杂化方式有2种
D.一个配离子中配位键的数目为6
5.利用超分子可分离C 和C 。将C 、C 混合物加入一种空腔大小适配C 的“杯酚”中
60 70 60 70 60
进行分离的流程如图。下列说法错误的是( )
A.第二电离能:C