文档内容
第 29 讲 非金属及其化合物拓展创新
[复习目标] 1.了解第ⅥA族元素硒、碲的性质及应用。2.了解第ⅤA族元素磷、砷的性质
及应用。
考点一 氧族元素——硒、碲
1.氧族元素概述
(1)主要包括氧(O)、硫(S)、硒(Se)、碲(Te)、钋(Po),价层电子排布为ns2np4。
(2)硫、硒、碲与大多数金属元素形成共价化合物。硒、碲在自然界无单质存在,常存在于
重金属硫化物矿中。少量硒对人体新陈代谢起调节作用,过量则有毒;有光电性质,用于电
影传真和制造光电管。
2.硒及其化合物的性质
(1)单质硒及其氢化物在空气中燃烧可得到SeO。
2
(2)SeO 的氧化性比SO 强,属于中等强度的氧化剂,可氧化HS、NH 等,化学方程式分别
2 2 2 3
为SeO+2HS===Se+2S+2HO、3SeO+4NH ===3Se+2N+6HO。
2 2 2 2 3 2 2
(3)亚硒酸可作氧化剂 ,能氧化SO ,反应为HSeO +2SO +HO===2HSO +Se↓,但遇
2 2 3 2 2 2 4
到强氧化剂时表现还原性,可被氧化成硒酸,反应为HSeO+Cl+HO===HSeO+2HCl。
2 3 2 2 2 4
3.碲及其化合物的性质
(1)碲在空气或纯氧中燃烧生成TeO 。
2
(2)TeO 是不挥发的白色固体,微溶于水,可溶于强酸、强碱,如 TeO +2NaOH===NaTeO
2 2 2 3
+HO。
2
(3)H TeO 具有氧化性和还原性,如
2 3
HTeO +2SO +HO===2HSO +Te,
2 3 2 2 2 4
HTeO +Cl+HO===HTeO +2HCl。
2 3 2 2 2 4
1.硒(34Se)元素及其化合物与人体健康、工业生产密切相关。某科研小组以阳极泥(主要成
分是Se,含有CuSe、Ag Se等杂质)为原料,提炼硒的流程如下:
2
请回答下列问题:(1)基态硒原子的价层电子排布式为________,与硒同主族相邻元素是________(填元素名称)。
(2)已知滤液 A 中主要成分是 NaSeO ,可用于治疗克山病,则 NaSeO 的化学名称为
2 3 2 3
________;滤液C中主要成分是NaSe,则NaSe的电子式为________。
2 2
(3)上述流程图中的括号内,按操作先后顺序依次填写的内容是________、________。
(4)写出高温下用焦炭还原固体B的化学方程式:_____________________________________。
(5)滤液C中析出硒的离子方程式为________________________。
答案 (1)4s24p4 硫、碲 (2)亚硒酸钠 (3)粉碎 过滤 (4)Na SeO
2 4
+4C=====NaSe+4CO↑ (5)2Se2-+O +2CO===2Se↓+2CO(或 2Se2-+O +4CO +
2 2 2 2 2
2HO===2Se↓+4HCO)
2
2.(2023·长沙一中高三段考)碲及其化合物具有许多优良性能,被广泛用于冶金、化工、医
药卫生等工业领域。工业上用铜阳极泥(主要成分除含Cu Te、TeO 外,还有少量Ag和Au)
2 2
经如下工艺流程得到粗碲。
已知:TeO 是两性氧化物,TeOSO 为正盐。
2 4
(1)已知此工艺中“加压硫酸浸出”过程中会发生以下化学反应:Cu Te+2O===2CuO+
2 2
TeO ;TeO +HSO ===TeOSO +HO。“含碲浸出液”的溶质成分除了TeOSO 外,主要是
2 2 2 4 4 2 4
__________(填化学式)。
(2)操作Ⅰ的分离方法是__________________;从浸出渣中分离出 Au 的方法是
_____________
_______________________________________________________________________________
。
(3)“电解沉积除铜”目的是除去溶液中的 Cu2+,电解初级阶段阴极的主要电极反应是
______________。
(4)向“含碲硫酸铜母液”中通入SO 并加入NaCl反应一段时间后,Te(Ⅳ)浓度从6.72 g·L-1
2
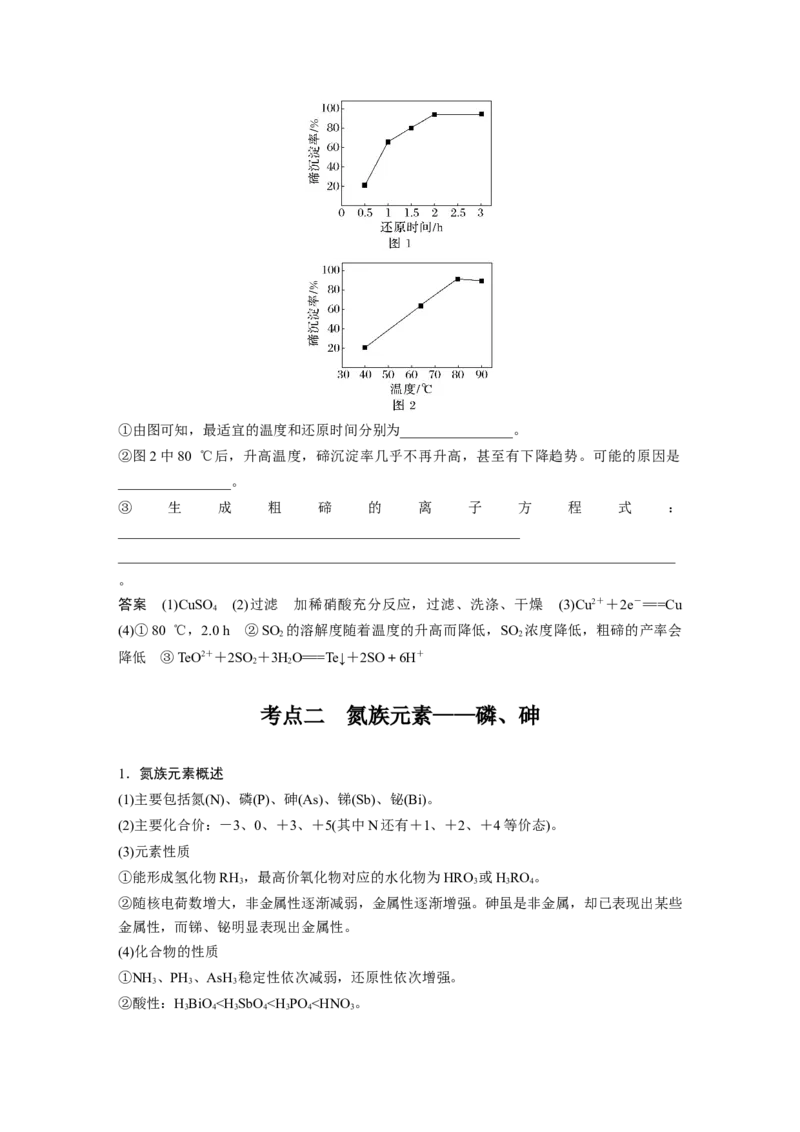
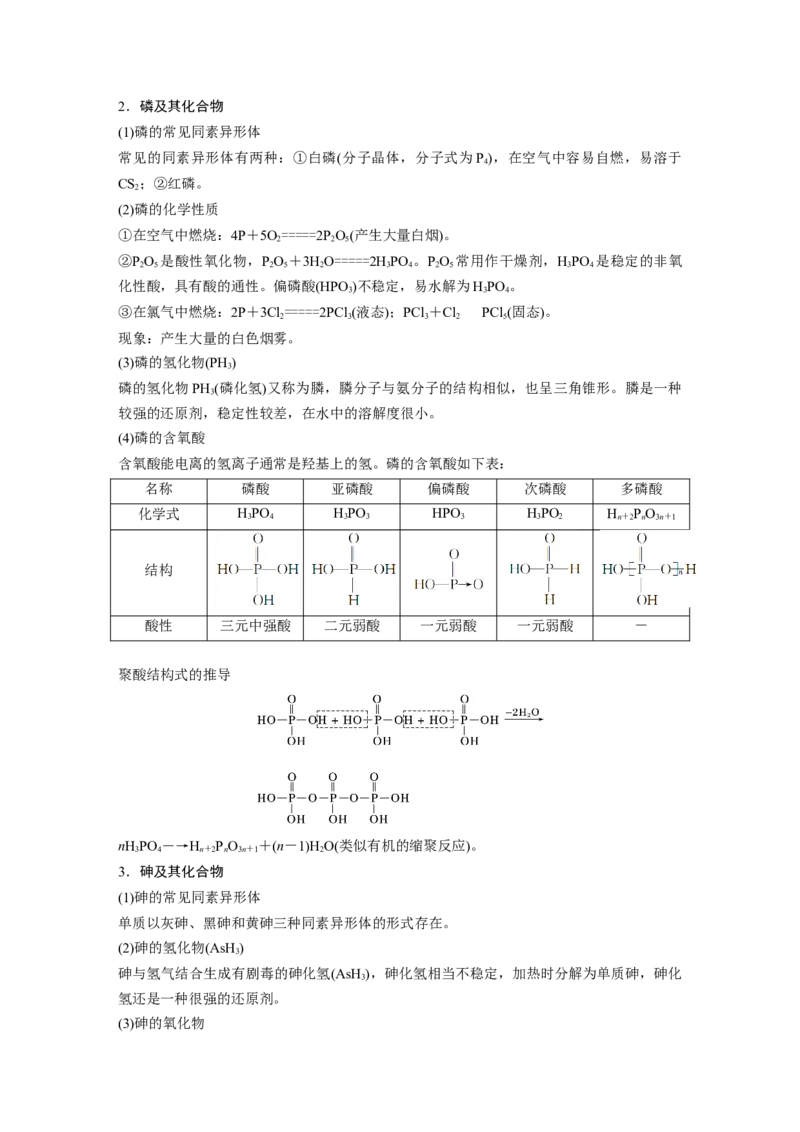
下降到0.10 g·L-1,在一定条件下,碲沉淀率与还原时间、温度的变化曲线分别如图1、图2
所示:①由图可知,最适宜的温度和还原时间分别为________________。
②图2中80 ℃后,升高温度,碲沉淀率几乎不再升高,甚至有下降趋势。可能的原因是
________________。
③ 生 成 粗 碲 的 离 子 方 程 式 :
_________________________________________________________
_______________________________________________________________________________
。
答案 (1)CuSO (2)过滤 加稀硝酸充分反应,过滤、洗涤、干燥 (3)Cu2++2e-===Cu
4
(4)①80 ℃,2.0 h ②SO 的溶解度随着温度的升高而降低,SO 浓度降低,粗碲的产率会
2 2
降低 ③TeO2++2SO +3HO===Te↓+2SO+6H+
2 2
考点二 氮族元素——磷、砷
1.氮族元素概述
(1)主要包括氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi)。
(2)主要化合价:-3、0、+3、+5(其中N还有+1、+2、+4等价态)。
(3)元素性质
①能形成氢化物RH,最高价氧化物对应的水化物为HRO 或HRO。
3 3 3 4
②随核电荷数增大,非金属性逐渐减弱,金属性逐渐增强。砷虽是非金属,却已表现出某些
金属性,而锑、铋明显表现出金属性。
(4)化合物的性质
①NH 、PH 、AsH 稳定性依次减弱,还原性依次增强。
3 3 3
②酸性:HBiO K (AgSCN),可知在水溶液中部分氯化银可以转化为AgSCN,使得实验中生成的
sp sp
AgSCN偏多,测定结果将偏小;n(Cl)=0.100 0 mol·L-1×20.00×10-3 L-cV×10-3 mol=
(2.0-cV)×10-3 mol,则m(Cl)=35.5×(2.0-cV)×10-3 g,所测Cl元素含量为×100%。
7.NaSbF (六氟锑酸钠)是光化学反应的催化剂。我国科学家开发一种以锑矿(主要含
6
Sb O、Sb S,还含少量Sb O、Fe O、CuO等)为原料制备NaSbF 的工艺流程如图所示。
2 3 2 3 2 5 2 3 6
已知:
①Sb的氧化物及氢氧化物的性质与Al的类似,Sb S 溶于NaOH浓溶液;
2 3
②NaSbO ·3H O难溶于水,NaSbF 易溶于水;
3 2 6
③常温下,K (CuS)=6.0×10-36。
sp
回答下列问题:
(1)NaSbF 的组成元素中第一电离能最大的是______(填元素符号)。
6
(2)“碱浸”前,先将锑矿粉碎过筛的目的是____________________。
(3)“除杂”时生成CuS的化学方程式为____________________________,“除杂”结束后
溶液中c(S2-)=1×10-6mol·L-1,此时溶液中c(Cu2+)=______mol·L-1。
(4)“转化”中HO 与NaSbO 溶液发生反应,该反应中氧化剂与还原剂的物质的量之比为
2 2 2
__________________;分离出NaSbO ·3H O的操作是______________(填名称);“转化”时
3 2
适当加热可提高反应速率,但是温度过高,转化效率降低,其主要原因是
_________________。
(5)“氟化”中加入氢氟酸,“氟化”不能使用陶瓷容器,其主要原因是________________。答案 (1)F (2)增大固体和液体接触面积 (3)Na S+CuSO ===CuS↓+NaSO 6.0×10-30
2 4 2 4
(4)1∶1 过滤 温度过高,双氧水分解加快,反应物浓度降低 (5)陶瓷的主要成分是硅酸
盐,HF与硅酸盐反应
解析 锑矿(主要含Sb O 、Sb S ,还含有少量Sb O 、Fe O 、CuO等)加NaOH浓溶液、
2 3 2 3 2 5 2 3
NaSO 溶液进行碱浸、还原,过滤除去不溶的Fe O 、CuO,Sb O 、Sb S 与NaOH溶液反
2 2 3 2 3 2 3 2 3
应最终转化为 NaSbO 、NaS,Sb O 、NaOH 溶液与 NaSO 溶液反应生成 NaSbO 、
2 2 2 5 2 2 3 2
NaSO ;含NaSbO 、NaS的溶液加硫酸铜将硫离子转化为CuS,将过量的氢氧根离子转化
2 4 2 2
为氢氧化铜除去,得到主要溶质为NaSbO 的溶液,NaSbO 溶液加过氧化氢、浓NaOH转化
2 2
得到NaSbO ·3H O,再用HF进行氟化得到NaSbF 。(3)“除杂”时NaS和CuSO 反应生成
3 2 6 2 4
CuS沉淀,化学方程式为Na S+CuSO ===CuS↓+Na SO ,“除杂”结束后溶液中c(S2
2 4 2 4
-)=1×10-6mol·L-1,此时溶液中c(Cu2+)=mol·L-1=6.0×10-30mol·L-1。