文档内容
第 51 讲 弱电解质的电离平衡
[复习目标] 1.理解弱电解质在水溶液中的电离平衡。2.理解电离常数的含义,掌握电离常
数的应用并能进行相关计算。
考点一 弱电解质的电离平衡及影响因素
1.电离平衡的建立
在一定条件下(如温度、压强等),当弱电解质分子电离产生离子的速率和离子结合成分子的
速率相等时,电离过程达到了平衡。
平衡建立过程如图所示:
2.外因对电离平衡的影响
(1)浓度:在一定温度下,同一弱电解质溶液,浓度越小,越易电离。
(2)温度:温度越高,电离程度越大。
(3)同离子效应:加入与弱电解质具有相同离子的电解质时,可使电离平衡向结合成弱电解
质分子的方向移动。
(4)化学反应:加入能与弱电解质电离出的离子反应的物质时,可使电离平衡向电离方向移
动。
1.强电解质稀溶液中不存在溶质分子,弱电解质稀溶液中存在溶质分子( )
2.弱电解质溶液中至少存在两种共价化合物分子( )3.氨气溶于水,当NH ·H O电离出的c(OH-)=c(NH)时,表明NH ·H O电离处于平衡状态
3 2 3 2
( )
4.一元弱碱BOH的电离方程式为BOH===B++OH-( )
5.NaSO 溶液与NaHSO 溶液中所含微粒的种类相同( )
2 3 3
6.电离平衡向右移动,弱电解质分子的浓度一定减小( )
7.25 ℃时,0.1 mol·L-1的氨水加水稀释,各离子浓度均减小( )
答案 1.√ 2.√ 3.× 4.× 5.√ 6.× 7.×
一、外因对电离平衡移动结果的判断
1.以0.1 mol·L-1 CHCOOH溶液为例,只改变一种条件对CHCOOH(aq)CHCOO-(aq)
3 3 3
+H+(aq) ΔH>0的影响,完成下表:
改变条件 平衡移动方向 n(H+) c(H+) 导电能力
加水稀释 向右 增大 减小 减弱
加入少量冰醋酸 向右 增大 增大 增强
通入HCl(g) 向左 增大 增大 增强
加NaOH(s) 向右 减小 减小 增强
加CHCOONa(s) 向左 减小 减小 增强
3
升高温度 向右 增大 增大 增强
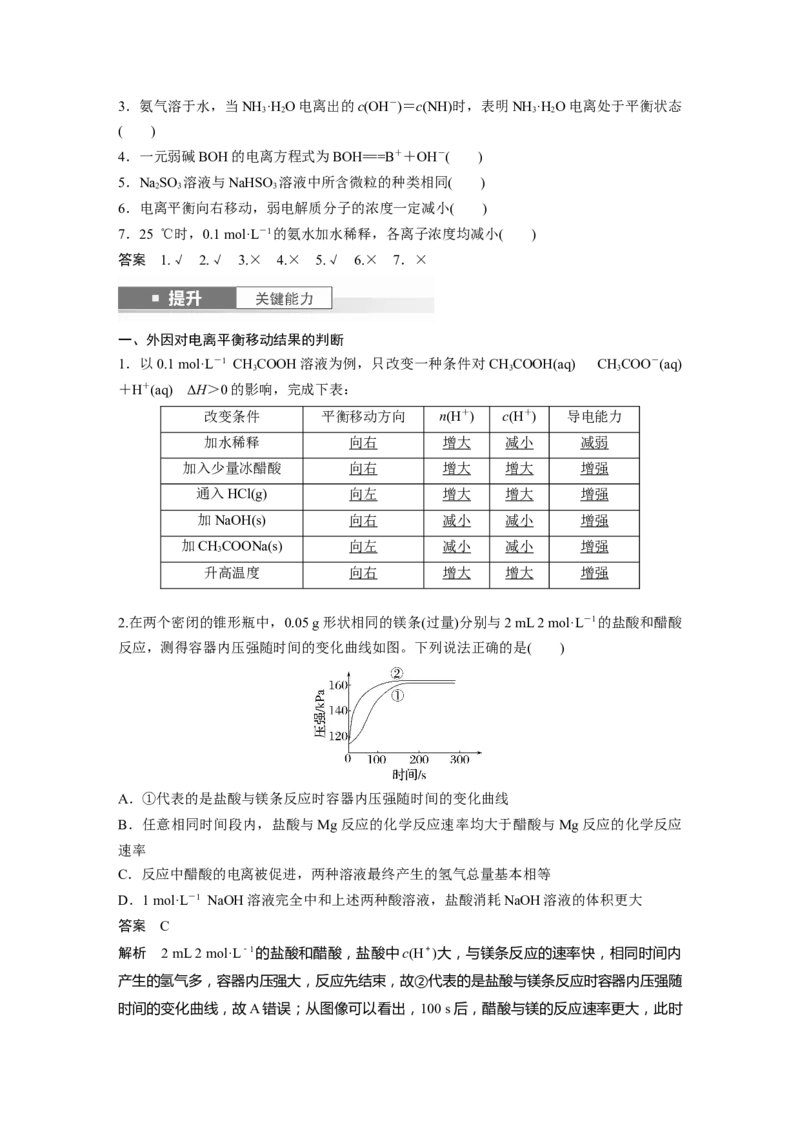
2.在两个密闭的锥形瓶中,0.05 g形状相同的镁条(过量)分别与2 mL 2 mol·L-1的盐酸和醋酸
反应,测得容器内压强随时间的变化曲线如图。下列说法正确的是( )
A.①代表的是盐酸与镁条反应时容器内压强随时间的变化曲线
B.任意相同时间段内,盐酸与Mg反应的化学反应速率均大于醋酸与Mg反应的化学反应
速率
C.反应中醋酸的电离被促进,两种溶液最终产生的氢气总量基本相等
D.1 mol·L-1 NaOH溶液完全中和上述两种酸溶液,盐酸消耗NaOH溶液的体积更大
答案 C
解析 2 mL 2 mol·L-1的盐酸和醋酸,盐酸中c(H+)大,与镁条反应的速率快,相同时间内
产生的氢气多,容器内压强大,反应先结束,故②代表的是盐酸与镁条反应时容器内压强随
时间的变化曲线,故A错误;从图像可以看出,100 s后,醋酸与镁的反应速率更大,此时盐酸与镁已接近反应结束,c(H+)较小,反应速率较小,故B错误;由于盐酸和醋酸的浓度
和体积均相同,则二者物质的量相同,故反应结束时,产生的氢气总量基本相等,用 1
mol·L-1 NaOH溶液完全中和上述两种酸溶液时,盐酸与醋酸消耗NaOH溶液的体积相等,
故C正确、D错误。
一强一弱的比较
(1)相同浓度、相同体积的一元强酸与一元弱酸与金属或碱反应特点分析
项目 与足量Mg反应
中和碱的能力 与足量Mg反应过程中的速率
酸 产生H 的量
2
一元强酸 开始时强酸的反应速率大,一
相同 相同
一元弱酸 段时间后弱酸的反应速率大
(2)相同pH、相同体积的一元强酸与一元弱酸与金属或碱反应特点分析
项目 与足量Mg反
中和碱的能力 与足量Mg反应过程中的速率
酸 应产生H 的量
2
一元强酸 小 少 开始时二者相同,一段时间后弱
一元弱酸 大 多 酸的速率保持较大
二、多角度证明弱电解质
3.能证明蚁酸(HCOOH)是弱酸的实验事实是( )
A.HCOOH溶液与Zn反应放出H
2
B.0.1 mol·L-1 HCOOH溶液可使紫色石蕊溶液变红
C.HCOOH溶液与NaCO 反应生成CO
2 3 2
D.常温时0.1 mol·L-1 HCOOH溶液的pH=2.3
答案 D
解析 A、B项,只能证明蚁酸具有酸性,不能证明其酸性强弱,错误;C项,只能证明蚁
酸的酸性比碳酸强,错误;D项,溶液的pH=2.3,说明HCOOH未完全电离,正确。
4.某同学拟用pH计测定溶液pH以探究某酸HR是否为弱电解质。下列说法正确的是(
)
A.25 ℃时,若测得0.01 mol·L-1 HR溶液pH>2,则HR是弱酸
B.25 ℃时,若测得0.01 mol·L-1和0.1 mol·L-1 HR溶液的pH差值等于1,则HR是弱酸
C.25 ℃时,若测得0.01 mol·L-1 NaR溶液pH=7,则HR是弱酸
D.25 ℃时,若测得NaR溶液pH=a,将该溶液升温至50 ℃,测得pH=b,a>b,则HR
是弱酸
答案 A
解析 25 ℃时,若测得0.01 mol·L-1 HR溶液pH>2,说明HR在水溶液中部分电离,溶液中存在电离平衡,则HR是弱酸,故A正确;25 ℃时,若测得0.01 mol·L-1和0.1 mol·L-1
HR溶液的pH差值等于1,说明稀释十倍,H+的物质的量没有变化,HR完全电离,是强酸,
故B错误;25 ℃时,若测得0.01 mol·L-1 NaR溶液pH=7,说明溶液呈中性,NaR为强酸
强碱盐,HR为强酸,故C错误;若HR为强酸,NaR溶液呈中性,升高温度,促进水的电
离,pH减小,则a>b,若HR是弱酸,R-水解溶液呈碱性,加热,促进盐的水解,碱性增
强,则aK (填“>”或“<”)
a1 a2
2.电离常数的影响因素
(1)内因:相同温度下,电解质越弱,其电离常数越小,反之,电离常数越大。
(2)外因:电离平衡常数与温度有关,与浓度无关,升高温度,K增大。
3.电离常数的意义
(1)反映弱电解质的相对强弱,电离平衡常数越大,弱电解质的电离能力越强。
(2)多元弱酸的各步电离常数的大小关系是K >K >K ……,当K ≫K 时,计算多元弱酸中
a1 a2 a3 a1 a2
的c(H+)或比较多元弱酸酸性的相对强弱时,通常只考虑第一步电离。1.同一弱电解质,浓度不同其电离常数一定不同( )
2.弱电解质的电离平衡右移,电离常数一定增大( )
3.某一弱电解质,电离度越大,电离常数就越大( )
4.常温下,依据K (H CO)>K (H PO ),可知碳酸的酸性比磷酸强( )
a1 2 3 a2 3 4
答案 1.× 2.× 3.× 4.×
一、弱电解质相对强弱的比较
1.(2022·湖北,12)根据酸碱质子理论,给出质子(H+)的物质是酸,给出质子的能力越强,
酸性越强。已知:NH+NH ===NH+NH ,NH +CHCOOH===NH+CHCOO-,下列酸
2 3 2 4 2 4 3 2 3
性强弱顺序正确的是( )
A.NH>N H>NH
2 2 4
B.NH>CH COOH>NH
2 3
C.NH >N H>CH COO-
3 2 4 3
D.CHCOOH>N H>NH
3 2
答案 D
解析 根据复分解反应的规律,强酸能制得弱酸,根据酸碱质子理论,给出质子(H+)的物质
是酸,则反应NH +CHCOOH===NH+CHCOO-中,酸性:CHCOOH>NH,反应NH
2 4 3 2 3 3 2 2
+NH ===NH+NH 中,酸性:NH>NH,故酸性:CHCOOH>N H>NH。
3 2 4 2 3 2
2.下列事实中,不能比较氢硫酸与亚硫酸的酸性强弱的是( )
A.氢硫酸不能与碳酸氢钠溶液反应,而亚硫酸可以
B.氢硫酸的导电能力低于相同浓度的亚硫酸
C.0.10 mol·L-1的氢硫酸和亚硫酸的pH分别为4.5和2.1
D.氢硫酸的还原性强于亚硫酸
答案 D
3.部分弱酸的电离平衡常数如下表:
弱酸 HCOOH HS HCO HClO
2 2 3
电离平衡常 K =1.1×10-7 K =4.5×10-7 K=
a1 a1 a
K=1.77×10-4
a
数(25 ℃) K =1.3×10-13 K =4.7×10-11 4.0×10-8
a2 a2
按要求回答下列问题:
(1)HCOOH、HS、HCO、HClO的酸性由强到弱的顺序为____________________。
2 2 3
(2)相同浓度的HCOO-、HS-、S2-、HCO、CO、ClO-结合H+的能力由强到弱的顺序为
________________________________________________________________________________________________________________________________________________。
(3)运用上述电离常数及物质的特性判断下列化学方程式不正确的是________(填序号)。
①次氯酸与NaHCO 溶液的反应:HClO+HCO===ClO-+HO+CO↑
3 2 2
②少量CO 通入NaClO溶液中:CO+HO+2ClO-===CO+2HClO
2 2 2
③少量CO 通入NaClO溶液中:CO+HO+ClO-===HCO+HClO
2 2 2
④硫化氢通入NaClO溶液中:HS+ClO-===HS-+HClO
2
⑤碳酸钠滴入足量甲酸溶液中:2HCOOH+CO===2HCOO-+CO↑+HO
2 2
答案 (1)HCOOH>HCO>HS>HClO
2 3 2
(2)S2->CO>ClO->HS->HCO>HCOO-
(3)①②④
二、微粒浓度比值判断
4.常温下,将0.1 mol·L-1的CHCOOH溶液加水稀释,请填写下列表达式中的数据变化情
3
况(填“变大”“变小”或“不变”)。
(1)________;
(2)________;
(3)________;
(4)________;
(5)________。
答案 (1)变小 (2)变大 (3)变小 (4)不变
(5)不变
解析 (1)将该式变为=或稀释时醋酸的电离平衡正向移动,n(CHCOOH)减小,n(H+)增大,
3
因此其比值变小。
(2)将该式变为=或稀释时醋酸的电离平衡正向移动,n(CHCOOH)减小,n(CHCOO-)增大,
3 3
因此其比值变大。
(5)将该式变为=,故其比值不变。
判断溶液中微粒浓度比值的三种方法
(1)将浓度之比转化为物质的量之比进行比较,这样分析起来可以忽略溶液体积的变化,只
需分析微粒数目的变化即可。
(2)“假设法”,如上述问题(3),假设无限稀释,c(CHCOO-)趋近于0,c(H+)趋于10-
3
7mol·L-1,故比值变小。
(3)“凑常数”,解题时将某些粒子的浓度比值乘以或除以某种粒子的浓度,转化为一个常
数与某种粒子浓度的乘积或相除的关系。1.(2020·北京,11)室温下,对于1 L 0.1 mol·L-1醋酸溶液。下列判断正确的是( )
A.该溶液中CHCOO-的粒子数为6.02×1022
3
B.加入少量CHCOONa固体后,溶液的pH降低
3
C.滴加NaOH溶液过程中,n(CHCOO-)与n(CHCOOH)之和始终为0.1 mol
3 3
D.与NaCO 溶液反应的离子方程式为CO+2H+===HO+CO↑
2 3 2 2
答案 C
解析 醋酸属于弱电解质,则含0.1 mol醋酸的溶液中CHCOO-的粒子数小于6.02×1022,
3
A错误;加入少量CHCOONa固体,抑制醋酸的电离,溶液的pH升高,故B错误;根据元
3
素守恒,n(CHCOO-)+n(CHCOOH)=0.1 mol,故C正确;醋酸的酸性强于碳酸,则根据
3 3
强酸制取弱酸,醋酸与NaCO 溶液反应生成醋酸钠、二氧化碳和水,醋酸是弱电解质,离
2 3
子反应中不能拆写,故D错误。
2.(2022·全国乙卷,13)常温下,一元酸HA的K(HA)=1.0×10-3。在某体系中,H+与A-
a
不能穿过隔膜,未电离的HA可自由穿过该膜(如图所示)。
设溶液中c (HA)=c(HA)+c(A-),当达到平衡时,下列叙述正确的是( )
总
A.溶液Ⅰ中c(H+)=c(OH-)+c(A-)
B.溶液Ⅱ中的HA的电离度[]为
C.溶液Ⅰ和Ⅱ中的c(HA)不相等
D.溶液Ⅰ和Ⅱ中的c (HA)之比为10-4
总
答案 B
解析 常温下,溶液Ⅰ的pH=7.0,则溶液Ⅰ中c(H+)=c(OH-)=1×10-7 mol·L-1,c(H+)
<c(OH-)+c(A-),A错误;常温下,溶液Ⅱ的pH=1.0,溶液中c(H+)=0.1 mol·L-1,
K(HA)==1.0×10-3,c (HA)=c(HA)+c(A-),则=1.0×10-3,解得=,B正确;常温下,
a 总
溶液Ⅰ的pH=7.0,溶液Ⅰ中c(H+)=1×10-7 mol·L-1,K(HA)==1.0×10-3,c (HA)=
a 总
c(HA)+c(A-),=1.0×10-3,溶液Ⅰ中c (HA)=(104+1)c(HA);溶液Ⅱ中,由B项解析可
总
知c (HA)=1.01c(HA),未电离的HA可自由穿过隔膜,故溶液Ⅰ和Ⅱ中的c(HA)相等,溶
总
液Ⅰ和Ⅱ中c (HA)之比为[(104+1)c(HA)]∶[1.01c(HA)]=(104+1)∶1.01≈104,C、D错误。
总
3.[2020·天津,16(5)节选]已知 25 ℃碳酸电离常数为 K 、K ,当溶液 pH=12 时,
a1 a2
c(H CO)∶c(HCO)∶c(CO)=1∶________∶______________________。
2 3
答案 1012·K 1024·K ·K
a1 a1 a2
解析 HCO 是二元弱酸,分步发生电离:HCOHCO+H+、HCOCO+H+,则有
2 3 2 3
K =、K =,从而可得K ·K =。当溶液pH=12时,c(H+)=10-12 mol·L-1,代入K 、
a1 a2 a1 a2 a1
K ·K 可得c(H CO)∶c(HCO)=1∶(1012·K ),c(H CO)∶c(CO)=1∶(1024·K ·K ),综合可
a1 a2 2 3 a1 2 3 a1 a2得c(H CO)∶c(HCO)∶c(CO)=1∶(1012·K )∶(1024·K ·K )。
2 3 a1 a1 a2
课时精练
1.氢氰酸(HCN)是一种弱酸,在水溶液中存在电离平衡:HCNH++CN-,常温下电离
常数为K。下列说法正确的是( )
a
A.0.1 mol·L-1 HCN溶液的pH<1
B.增大HCN溶液浓度,其电离程度减小
C.升高HCN溶液温度,平衡逆向移动
D.加入少量NaOH溶液,会使K 增大
a
答案 B
解析 氢氰酸(HCN)是一种弱酸,在水溶液中部分电离,因此0.1 mol·L-1 HCN溶液中c(H
+)<0.1 mol·L-1,pH>1,故A错误;氢氰酸为弱电解质,增大HCN溶液浓度,其电离程
度减小,故B正确;弱电解质的电离是吸热过程,升高温度,平衡正向移动,故 C错误;
加入少量NaOH溶液,电离平衡正向移动,但溶液的温度不变,电离平衡常数不变,故D
错误。
2.饱和氨水中存在化学平衡和电离平衡:NH +HONH ·H ONH+OH-。下列有关
3 2 3 2
说法正确的是( )
A.常温下饱和氨水的pH<7
B.向氨水中滴加过量硫酸,上述平衡均正向移动,pH增大
C.电离是吸热过程,升高温度,上述平衡均正向移动
D.向氨水中加入少量NaOH固体,上述平衡均逆向移动,有NH 放出
3
答案 D
解析 常温下饱和氨水呈碱性,pH>7,A项错误;加入过量硫酸,H+浓度增大,pH减小,
B项错误;升温会使NH 逸出,NH +HONH ·H O平衡逆向移动,C项错误;加入少量
3 3 2 3 2
NaOH固体,OH-浓度增大,平衡向生成NH 的方向移动,有NH 放出,D项正确。
3 3
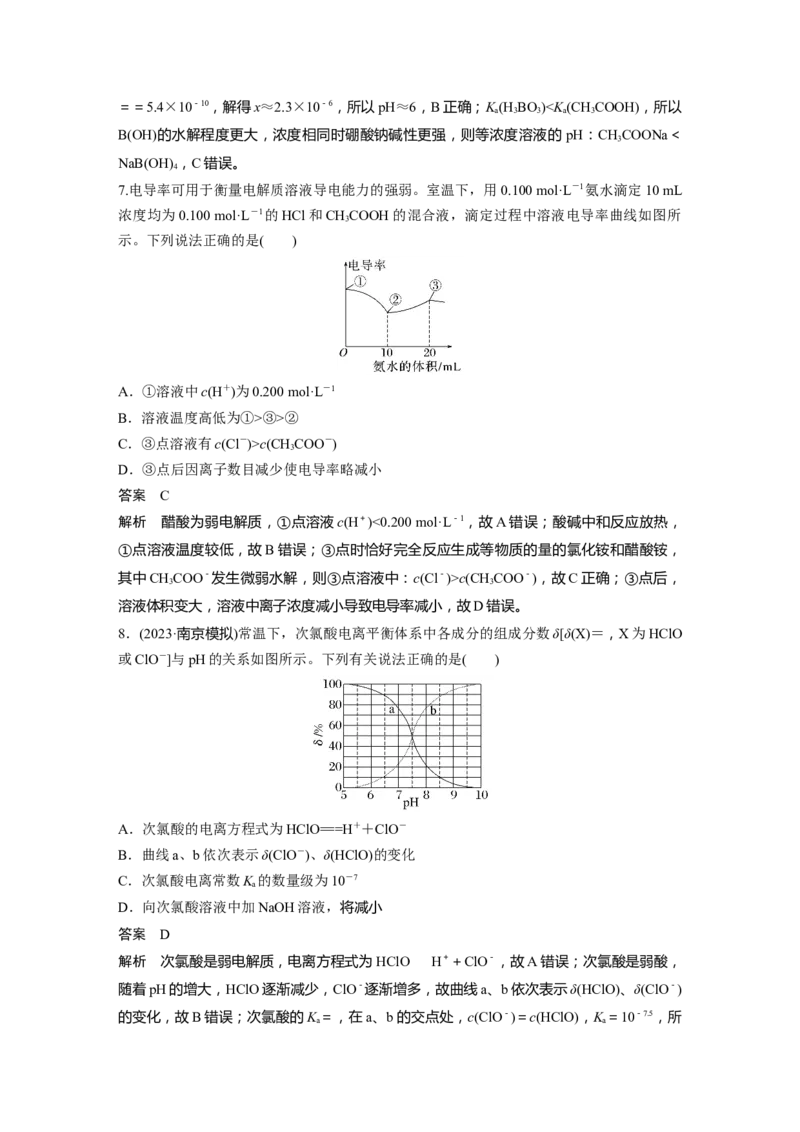
3.一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下
列说法正确的是( )
A.a、b、c三点溶液的pH:c1
3
D.相同物质的量浓度、相同体积的CHCOOH溶液和盐酸分别与足量的活泼金属反应,消
3
耗金属的量相同
答案 D
解析 相同浓度和体积的两溶液中溶质物质的量相同,消耗的金属的量相同,不能说明二者
的酸性强弱。
5.已知数据:7.2×10-4、4.6×10-4、4.9×10-10分别是三种酸的电离平衡常数,若已知这
些酸可发生如下反应:①NaCN+HNO===HCN+NaNO ,②NaCN+HF===HCN+NaF,
2 2
③NaNO +HF===HNO+NaF,由此可判断下列叙述中不正确的是( )
2 2
A.HF的电离平衡常数为7.2×10-4
B.HNO 的电离平衡常数为4.9×10-10
2
C.根据①③两个反应即可知三种酸的相对强弱
D.HNO 的电离平衡常数比HCN大,比HF小
2
答案 B
解析 反应①说明酸性:HNO>HCN,反应③说明酸性:HF>HNO。
2 2
6.硼酸(H BO)的电离方程式为 HBO +HOB(OH)+H+。已知常温下,K(H BO)=
3 3 3 3 2 a 3 3
5.4×10-10、K(CHCOOH)=1.75×10-5。下列说法错误的是( )
a 3
A.HBO 为一元酸
3 3
B.0.01 mol·L-1 HBO 溶液的pH≈6
3 3
C.常温下,等浓度溶液的pH:CHCOONa>NaB(OH)
3 4
D.NaOH溶液溅到皮肤时,可用大量水冲洗,再涂上硼酸溶液
答案 C
解析 根据题意可知HBO 只存在一步电离,所以为一元酸,A正确;设0.01 mol·L-1
3 3
HBO 溶液中c(H+)=x mol·L-1,则c[B(OH)]也可近似认为等于x mol·L-1,则有K(H BO)
3 3 a 3 3==5.4×10-10,解得x≈2.3×10-6,所以pH≈6,B正确;K(H BO)③>②
C.③点溶液有c(Cl-)>c(CHCOO-)
3
D.③点后因离子数目减少使电导率略减小
答案 C
解析 醋酸为弱电解质,①点溶液c(H+)<0.200 mol·L-1,故A错误;酸碱中和反应放热,
①点溶液温度较低,故B错误;③点时恰好完全反应生成等物质的量的氯化铵和醋酸铵,
其中CHCOO-发生微弱水解,则③点溶液中:c(Cl-)>c(CHCOO-),故C正确;③点后,
3 3
溶液体积变大,溶液中离子浓度减小导致电导率减小,故D错误。
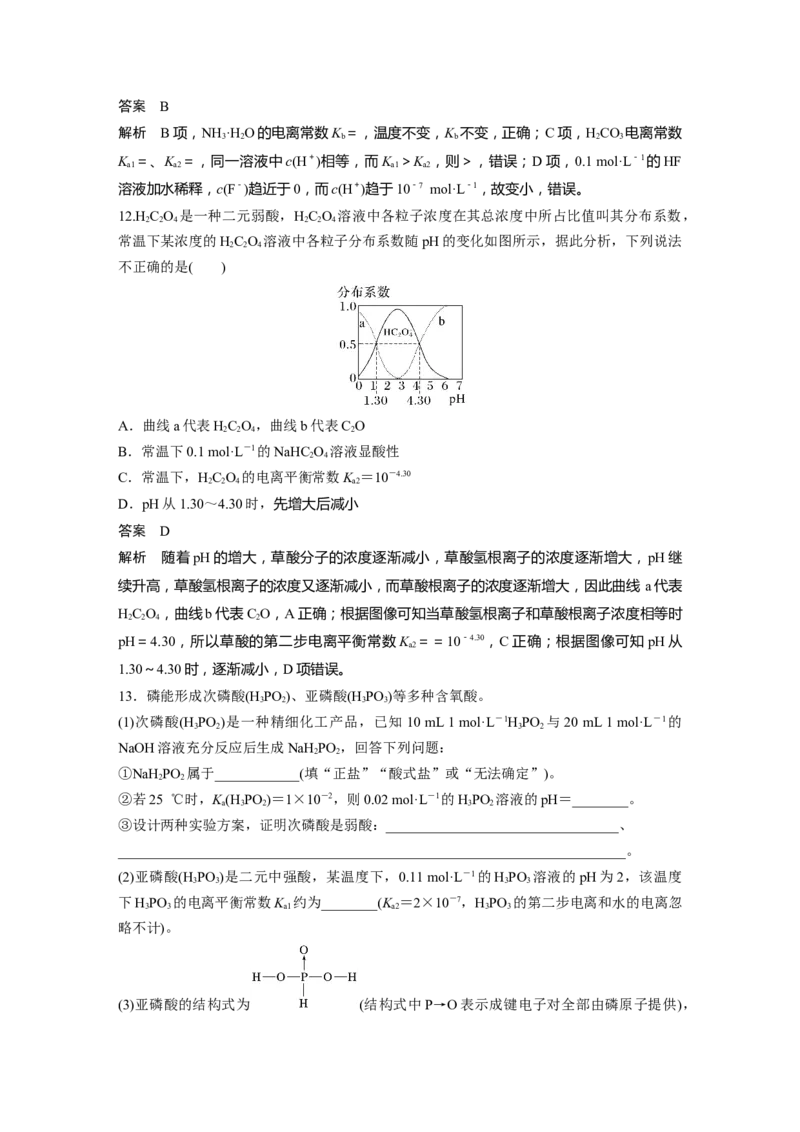
8.(2023·南京模拟)常温下,次氯酸电离平衡体系中各成分的组成分数δ[δ(X)=,X为HClO
或ClO-]与pH的关系如图所示。下列有关说法正确的是( )
A.次氯酸的电离方程式为HClO===H++ClO-
B.曲线a、b依次表示δ(ClO-)、δ(HClO)的变化
C.次氯酸电离常数K 的数量级为10-7
a
D.向次氯酸溶液中加NaOH溶液,将减小
答案 D
解析 次氯酸是弱电解质,电离方程式为HClOH++ClO-,故A错误;次氯酸是弱酸,
随着pH的增大,HClO逐渐减少,ClO-逐渐增多,故曲线a、b依次表示δ(HClO)、δ(ClO-)
的变化,故B错误;次氯酸的K=,在a、b的交点处,c(ClO-)=c(HClO),K=10-7.5,所
a a以K 的数量级为10-8,故C错误;向次氯酸溶液中加NaOH溶液,随着碱性增强,HClO逐
a
渐减少,ClO-逐渐增多,故将减小,故D正确。
9.下列酸碱溶液恰好完全中和,如图所示,则下列叙述正确的是( )
A.因为两种酸溶液的pH相等,故V 一定等于V
1 2
B.若V>V,则说明HA为强酸,HB为弱酸
1 2
C.若实验①中,V=V,则混合溶液中c(Na+)=c(A-)
1
D.实验②的混合溶液,可能pH<7
答案 C
解析 因为不知道两种酸的酸性强弱关系,所以不能判断V 与V 的相对大小,故A错误;
1 2
若V>V ,说明HA的酸性比HB的酸性强,但无法说明HA是强酸,故B错误;若实验①
1 2
中,V=V ,则HA的物质的量浓度也为0.01 mol·L-1,HA溶液pH=2,则HA为强酸,反
1
应后溶液显中性,故混合溶液中c(Na+)=c(A-),故C正确;恰好完全中和后实验②的混合
溶液中溶质为强碱弱酸盐或强酸强碱盐,溶液的pH≥7,故D错误。
10.25 ℃时,几种弱酸的电离平衡常数如表所示。下列说法正确的是( )
HCOOH HCO HCN
2 3
K =4.5×10-7
a1
K=1.8×10-4 K=6.2×10-10
a a
K =4.7×10-11
a2
A.HCO 溶液和NaCN溶液反应的离子方程式为HCO+CN-===HCO+HCN
2 3 2 3
B.HCOOH的电离平衡常数表达式为K=
a
C.物质的量浓度均为0.1 mol·L-1的HCOONa溶液和NaCN溶液,pH前者大
D.酸性强弱顺序是HCOOH>HCN>H CO
2 3
答案 A
11.下列关于电解质的说法正确的是( )
A.向0.1 mol·L-1 CHCOOH溶液中加入少量水,溶液中减小
3
B.室温下向10 mL 0.1 mol·L-1的氨水中加水稀释后,溶液中不变
C.等体积、等物质的量浓度的NaCO 和NaHCO 溶液混合:<
2 3 3
D.将浓度为0.1 mol·L-1 HF溶液加水不断稀释过程中,电离平衡常数K(HF)保持不变,始
a
终增大答案 B
解析 B项,NH ·H O的电离常数K =,温度不变,K 不变,正确;C项,HCO 电离常数
3 2 b b 2 3
K =、K =,同一溶液中c(H+)相等,而K >K ,则>,错误;D项,0.1 mol·L-1的HF
a1 a2 a1 a2
溶液加水稀释,c(F-)趋近于0,而c(H+)趋于10-7 mol·L-1,故变小,错误。
12.H C O 是一种二元弱酸,HC O 溶液中各粒子浓度在其总浓度中所占比值叫其分布系数,
2 2 4 2 2 4
常温下某浓度的HC O 溶液中各粒子分布系数随pH的变化如图所示,据此分析,下列说法
2 2 4
不正确的是( )
A.曲线a代表HC O,曲线b代表C O
2 2 4 2
B.常温下0.1 mol·L-1的NaHC O 溶液显酸性
2 4
C.常温下,HC O 的电离平衡常数K =10-4.30
2 2 4 a2
D.pH从1.30~4.30时,先增大后减小
答案 D
解析 随着pH的增大,草酸分子的浓度逐渐减小,草酸氢根离子的浓度逐渐增大,pH继
续升高,草酸氢根离子的浓度又逐渐减小,而草酸根离子的浓度逐渐增大,因此曲线 a代表
HC O ,曲线b代表C O,A正确;根据图像可知当草酸氢根离子和草酸根离子浓度相等时
2 2 4 2
pH=4.30,所以草酸的第二步电离平衡常数K ==10-4.30,C正确;根据图像可知pH从
a2
1.30~4.30时,逐渐减小,D项错误。
13.磷能形成次磷酸(H PO )、亚磷酸(H PO )等多种含氧酸。
3 2 3 3
(1)次磷酸(H PO )是一种精细化工产品,已知10 mL 1 mol·L-1HPO 与20 mL 1 mol·L-1的
3 2 3 2
NaOH溶液充分反应后生成NaH PO ,回答下列问题:
2 2
①NaH PO 属于____________(填“正盐”“酸式盐”或“无法确定”)。
2 2
②若25 ℃时,K(H PO )=1×10-2,则0.02 mol·L-1的HPO 溶液的pH=________。
a 3 2 3 2
③设计两种实验方案,证明次磷酸是弱酸:_________________________________、
________________________________________________________________________。
(2)亚磷酸(H PO )是二元中强酸,某温度下,0.11 mol·L-1的HPO 溶液的pH为2,该温度
3 3 3 3
下HPO 的电离平衡常数K 约为________(K =2×10-7,HPO 的第二步电离和水的电离忽
3 3 a1 a2 3 3
略不计)。
(3)亚磷酸的结构式为 (结构式中P→O表示成键电子对全部由磷原子提供),含有两个“—OH”,分子中有两个可电离的H+,因而是二元酸,由此类推次磷酸分子中含
有__________个“O—H”。
(4)向HPO 溶液中滴加NaOH溶液恰好中和生成NaHPO 时,所得溶液的pH__________(填
3 3 2 3
“>”“<”或“=”)7。
答案 (1)①正盐 ②2 ③测NaH PO 溶液的pH,若pH>7,则证明次磷酸为弱酸 向等
2 2
物质的量浓度的盐酸、次磷酸溶液中各滴入2滴石蕊溶液,若次磷酸溶液中红色浅一些,则
说明次磷酸为弱酸 (2)1×10-3 (3)1 (4)>
解析 (1)①NaOH过量,只生成NaH PO ,说明次磷酸中只有一个可电离出的氢离子,因而
2 2
NaH PO 是正盐。②设溶液中的H+浓度为x mol·L-1。
2 2
HPO H++HPO
3 2 2
初始/(mol·L-1) 0.02 0 0
平衡/(mol·L-1) 0.02-x x x
K(H PO )==1×10-2[注意由于K(H PO )比较大,不能近似计算],解得x=0.01,故pH=
a 3 2 a 3 2
-lg 0.01=2。(2)忽略HPO 的第二步电离和水的电离,则溶液中c(H PO)≈c(H+)=1×10-2
3 3 2
mol·L-1,c(H PO )=(0.11-1×10-2) mol·L-1=0.1 mol·L-1,HPO 的电离平衡常数K =
3 3 3 3 a1
==1×10-3。(4)Na HPO 溶液中,HPO水解,溶液呈碱性。
2 3
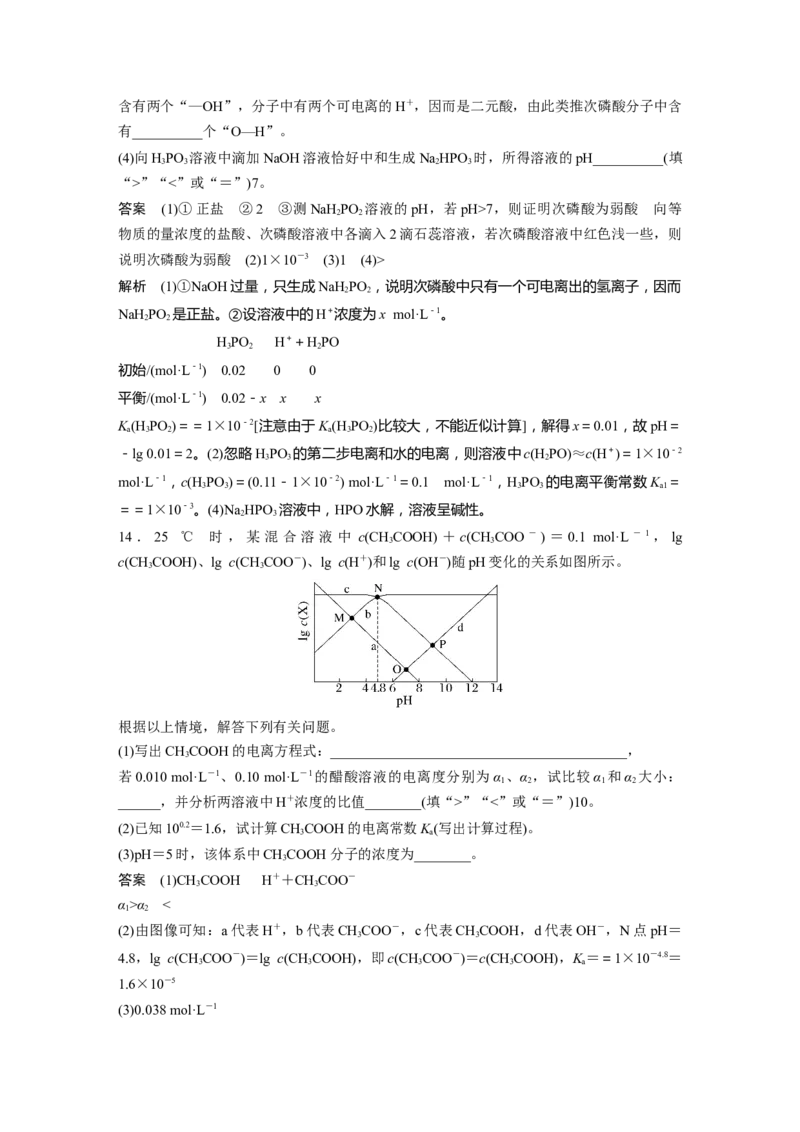
14 . 25 ℃ 时 , 某 混 合 溶 液 中 c(CHCOOH) + c(CHCOO - ) = 0.1 mol·L - 1 , lg
3 3
c(CHCOOH)、lg c(CHCOO-)、lg c(H+)和lg c(OH-)随pH变化的关系如图所示。
3 3
根据以上情境,解答下列有关问题。
(1)写出CHCOOH的电离方程式:__________________________________________,
3
若0.010 mol·L-1、0.10 mol·L-1的醋酸溶液的电离度分别为 α 、α ,试比较α 和α 大小:
1 2 1 2
______,并分析两溶液中H+浓度的比值________(填“>”“<”或“=”)10。
(2)已知100.2=1.6,试计算CHCOOH的电离常数K(写出计算过程)。
3 a
(3)pH=5时,该体系中CHCOOH分子的浓度为________。
3
答案 (1)CH COOHH++CHCOO-
3 3
α>α <
1 2
(2)由图像可知:a代表H+,b代表CHCOO-,c代表CHCOOH,d代表OH-,N点pH=
3 3
4.8,lg c(CHCOO-)=lg c(CHCOOH),即c(CHCOO-)=c(CHCOOH),K==1×10-4.8=
3 3 3 3 a
1.6×10-5
(3)0.038 mol·L-1解析 (3)pH=5时c(H+)=1×10-5 mol·L-1,相同温度下电离常数不变,K==10-4.8,=
a
=100.2=1.6,由于 c(CHCOO-)+c(CHCOOH)=0.1 mol·L-1,解得 c(CHCOOH)≈0.038
3 3 3
mol·L-1。