文档内容
第 56 讲 溶液中的粒子平衡曲线分类突破
[复习目标] 1.能正确识别图像,能从图像中找到曲线指代、趋势、关键点。2.利用溶液中
的平衡关系,学会分析不同类型图像中各粒子浓度之间的关系。
类型一 中和反应进程中pH变化曲线
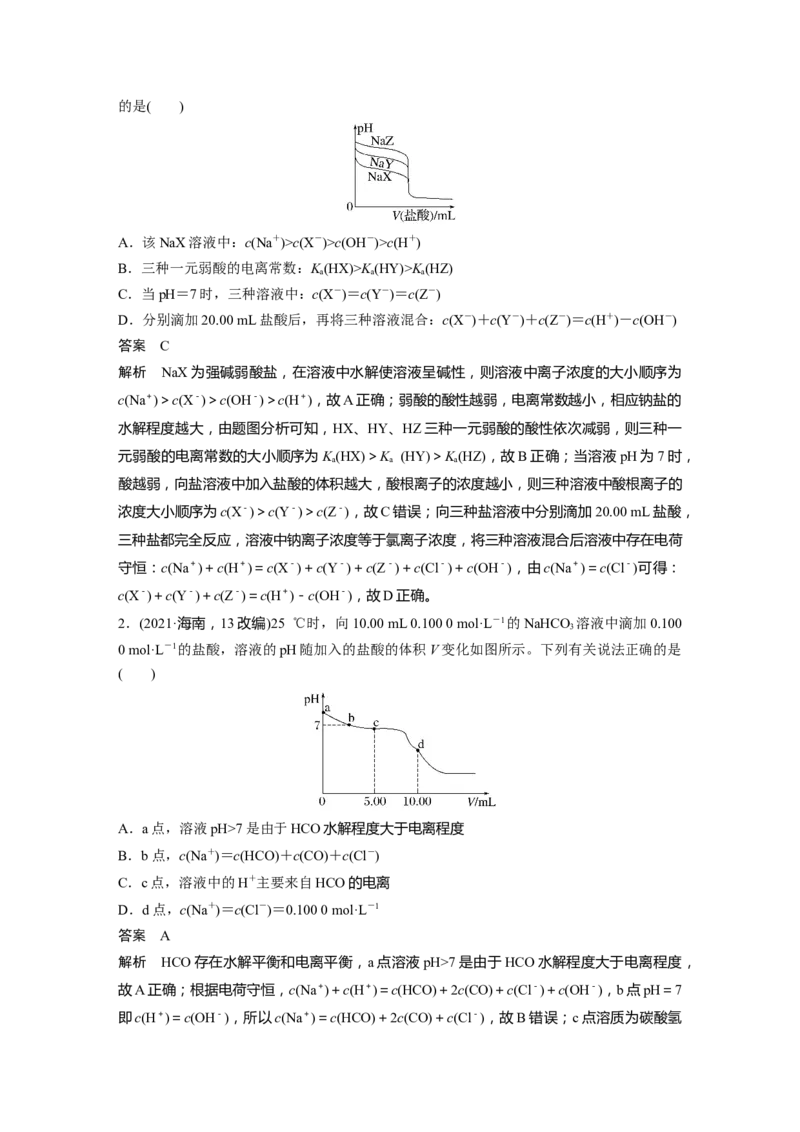
解决酸碱中和滴定曲线类问题的关键是巧抓“5点”,即曲线的起点、反应一半点、中性点、
恰好反应点和过量点,先判断出各点中的溶质及溶液的酸碱性。以室温时用 0.1 mol·L-
1NaOH溶液滴定20 mL 0.1 mol·L-1 CHCOOH溶液为例(如图),总结如何抓住滴定曲线的5
3
个关键点。
(1)起点
V(NaOH)=0(0 点):溶质是 CHCOOH,粒子浓度大小关系: c (CH COOH) > c (H + ) >
3 3
c (CH COO - ) > c (OH - ) 。
3
(2)一半点
V(NaOH)=10 mL(点①):溶质是等物质的量的CHCOOH 和CHCOONa,粒子浓度大小关
3 3
系: c (CH COO - ) > c (Na + ) > c (CH COOH) > c (H + ) > c (OH - ) ;元素守恒:c(CHCOOH)+
3 3 3
c(CHCOO-)= 2 c (Na + ) 。
3
(3)中性点
pH=7(点②):溶质是 CHCOONa 和少量的 CHCOOH,粒子浓度大小关系: c (Na + ) =
3 3
c (CH COO - ) > c (H + ) = c (OH - ) 。
3
(4)恰好反应点
V(NaOH)=20 mL(点③):溶质是CHCOONa,粒子浓度大小关系: c (Na + ) > c (CH COO - ) >
3 3
c (OH - ) > c (H + ) 。
(5)过量1倍点
V(NaOH)=40 mL:溶质是等物质的量的CHCOONa 和NaOH,粒子浓度大小关系: c (Na + )
3
> c (OH - ) > c (CH COO - ) > c (H + ) 。
3
1.(2021·湖南,9)常温下,用0.100 0 mol·L-1的盐酸分别滴定 20.00 mL浓度均为0.100 0
mol·L-1的三种一元弱酸的钠盐(NaX、NaY、NaZ)溶液,滴定曲线如图所示。下列判断错误的是( )
A.该NaX溶液中:c(Na+)>c(X-)>c(OH-)>c(H+)
B.三种一元弱酸的电离常数:K(HX)>K(HY)>K(HZ)
a a a
C.当pH=7时,三种溶液中:c(X-)=c(Y-)=c(Z-)
D.分别滴加20.00 mL盐酸后,再将三种溶液混合:c(X-)+c(Y-)+c(Z-)=c(H+)-c(OH-)
答案 C
解析 NaX为强碱弱酸盐,在溶液中水解使溶液呈碱性,则溶液中离子浓度的大小顺序为
c(Na+)>c(X-)>c(OH-)>c(H+),故A正确;弱酸的酸性越弱,电离常数越小,相应钠盐的
水解程度越大,由题图分析可知,HX、HY、HZ三种一元弱酸的酸性依次减弱,则三种一
元弱酸的电离常数的大小顺序为K(HX)>K (HY)>K(HZ),故B正确;当溶液pH为7时,
a a a
酸越弱,向盐溶液中加入盐酸的体积越大,酸根离子的浓度越小,则三种溶液中酸根离子的
浓度大小顺序为c(X-)>c(Y-)>c(Z-),故C错误;向三种盐溶液中分别滴加20.00 mL盐酸,
三种盐都完全反应,溶液中钠离子浓度等于氯离子浓度,将三种溶液混合后溶液中存在电荷
守恒:c(Na+)+c(H+)=c(X-)+c(Y-)+c(Z-)+c(Cl-)+c(OH-),由c(Na+)=c(Cl-)可得:
c(X-)+c(Y-)+c(Z-)=c(H+)-c(OH-),故D正确。
2.(2021·海南,13改编)25 ℃时,向10.00 mL 0.100 0 mol·L-1的NaHCO 溶液中滴加0.100
3
0 mol·L-1的盐酸,溶液的pH随加入的盐酸的体积V变化如图所示。下列有关说法正确的是
( )
A.a点,溶液pH>7是由于HCO水解程度大于电离程度
B.b点,c(Na+)=c(HCO)+c(CO)+c(Cl-)
C.c点,溶液中的H+主要来自HCO的电离
D.d点,c(Na+)=c(Cl-)=0.100 0 mol·L-1
答案 A
解析 HCO存在水解平衡和电离平衡,a点溶液pH>7是由于HCO水解程度大于电离程度,
故A正确;根据电荷守恒,c(Na+)+c(H+)=c(HCO)+2c(CO)+c(Cl-)+c(OH-),b点pH=7
即c(H+)=c(OH-),所以c(Na+)=c(HCO)+2c(CO)+c(Cl-),故B错误;c点溶质为碳酸氢钠、氯化钠、碳酸,溶液中的H+主要来自HCO 的电离,故C错误;d点,碳酸氢钠和盐
2 3
酸恰好反应,c(Na+)=c(Cl-)=0.050 0 mol·L-1,故D错误。
3.已知pK =-lg K 25 ℃时,HSO 的pK =1.85,pK =7.19。常温下,用 0.1 mol·L-
a a, 2 3 a1 a2
1NaOH溶液滴定20 mL 0.1 mol·L-1HSO 溶液的滴定曲线如图所示。下列说法不正确的是(
2 3
)
A.a点所得溶液中:2c(H SO )+c(SO)<0.1 mol·L-1
2 3
B.b点所得溶液中:c(H SO )+c(H+)=c(SO)+c(OH-)
2 3
C.c点所得溶液中:c(Na+)>3c(HSO)
D.d点所得溶液中:c(Na+)>c(HSO)>c(SO)
答案 D
解析 滴定过程中发生反应:NaOH+HSO ===NaHSO +HO、NaHSO +NaOH===NaSO
2 3 3 2 3 2 3
+HO。a点溶液中的溶质为NaHSO 和HSO ,根据元素守恒得出,c(H SO )+c(HSO)+
2 3 2 3 2 3
c(SO)<0.1 mol·L-1,根据电离常数 K =,此时溶液的 pH=1.85,可推出 c(HSO)=
a1
c(H SO ),代入上式得出,2c(H SO )+c(SO)<0.1 mol·L-1,故 A 正确;b 点加入 20 mL
2 3 2 3
NaOH溶液,NaOH和HSO 恰好完全反应生成NaHSO ,即溶质为NaHSO ,根据质子守恒
2 3 3 3
得c(H SO )+c(H+)=c(SO)+c(OH-),故B正确;c点溶质为NaSO 和NaHSO ,溶液显碱
2 3 2 3 3
性,SO+HOHSO+OH-,根据水解平衡常数K (SO)==,c(OH-)=,推出c(HSO)=
2 h
c(SO)①,根据电荷守恒:c(Na+)+c(H+)=2c(SO)+c(HSO)+c(OH-)②,将①代入②得c(Na
+)+c(H+)=3c(HSO)+c(OH-),c点溶液显碱性,c(OH-)>c(H+),显然:c(Na+)>3c(HSO),
故C正确;d点溶质为NaSO ,溶液中离子浓度c(Na+)>c(SO)>c(HSO),故D错误。
2 3
类型二 分布系数曲线
1.认识分布系数δ(X)与pH曲线
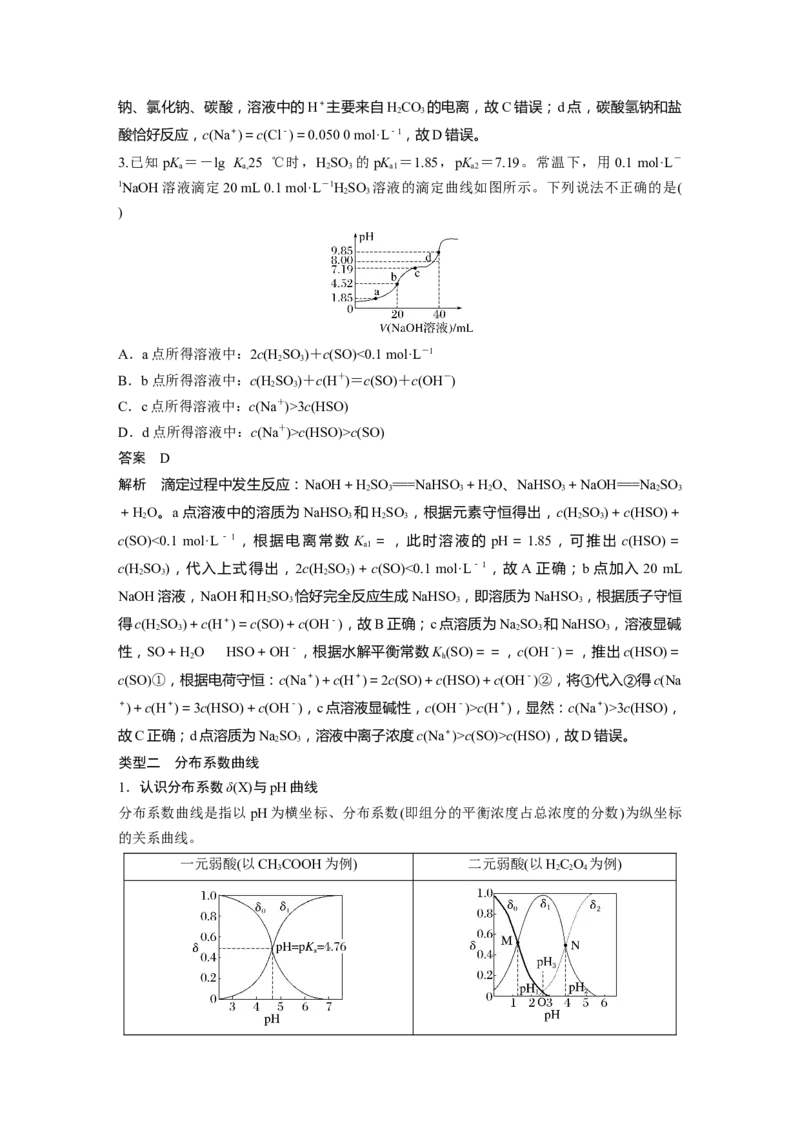
分布系数曲线是指以pH为横坐标、分布系数(即组分的平衡浓度占总浓度的分数)为纵坐标
的关系曲线。
一元弱酸(以CHCOOH为例) 二元弱酸(以HC O 为例)
3 2 2 4注:pK 为电离常数的负对数
a
δ 为CHCOOH的分布系数,δ 为CHCOO- δ 为HC O 的分布系数,δ 为HC O的
0 3 1 3 0 2 2 4 1 2
的分布系数 分布系数,δ 为C O的分布系数
2 2
2.读图解题要领
(1)读“曲线”——每条曲线所代表的粒子及变化趋势(以上图中HC O 为例)随pH增大,δ
2 2 4
只减不增的为HC O 曲线,δ先增后减的为HC O曲线,δ只增不减的为C O曲线。
2 2 4 2 2
(2)“用交点”——交点是某两种粒子浓度相等的点,可计算电离常数K:
①图中M点:c(HC O)=c(H C O),其pH为pH,K (H C O)== 。
2 2 2 4 1 a1 2 2 4
②同理图中N点:c(HC O)=c(C O),对应pH为pH,K = 。
2 2 2 a2
③图中O点,c(H C O)=c(C O),此时c(HC O)最大,其溶液pH为pH,则pH=。
2 2 4 2 2 3 3
思考 请根据HC O 的两级电离常数,推理论证上述③中结论。
2 2 4
提示 HC OH++HC O,HC OH++C O,K ·K =,由于交点O时,c(H C O)=
2 2 4 2 2 2 a1 a2 2 2 4
c(C O),c2(H+)=K ·K = · ,两边取负对数,即可得,pH=。
2 a1 a2 3
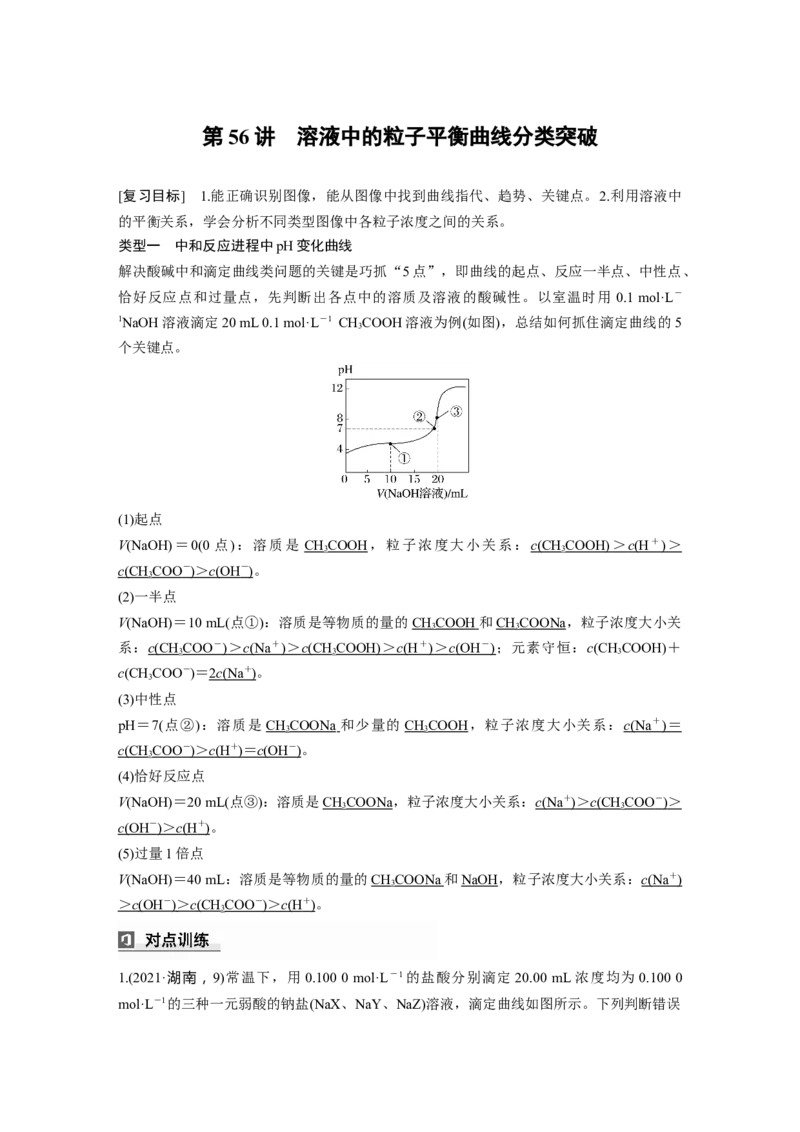
1.(2020·海南,12)某弱酸HA溶液中主要成分的分布分数随pH的变化如图所示。下列说法
错误的是( )
A.该酸-lg K ≈4.7
a
B.NaA的水解平衡常数K =
h
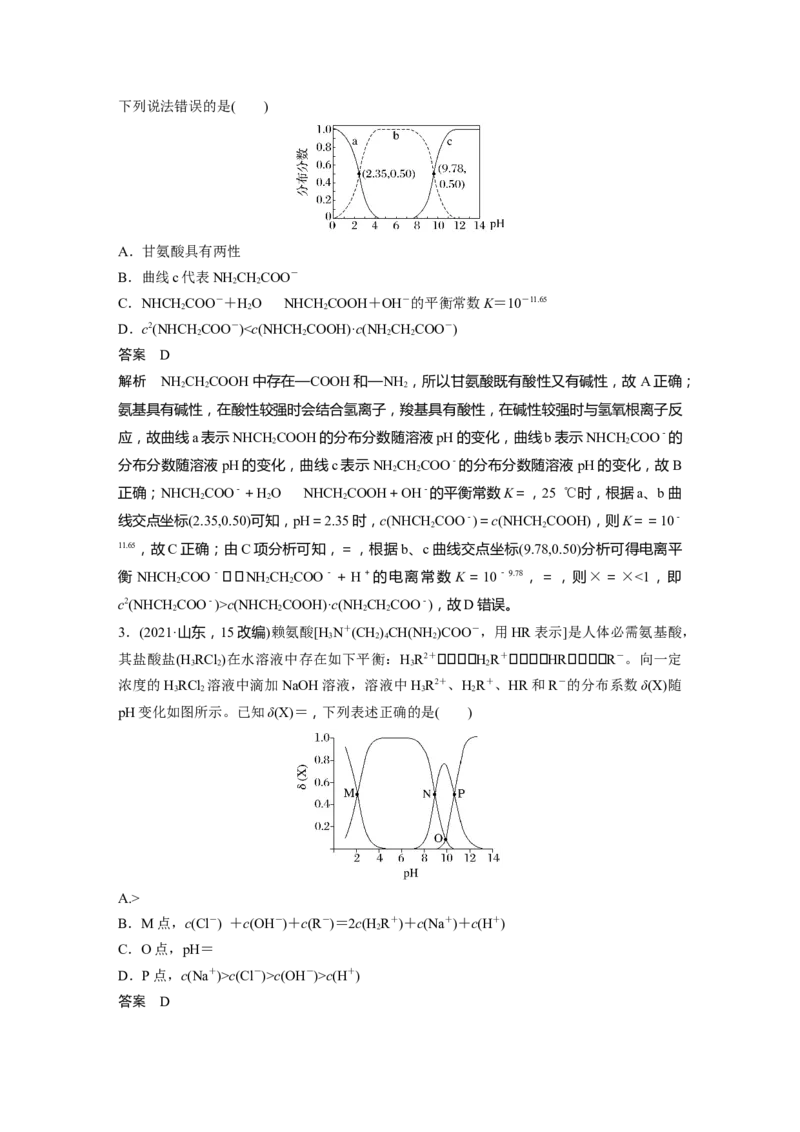
C.当该溶液的pH=7.0时,c(HA)c(NHCHCOOH)·c(NH CHCOO-),故D错误。
2 2 2 2
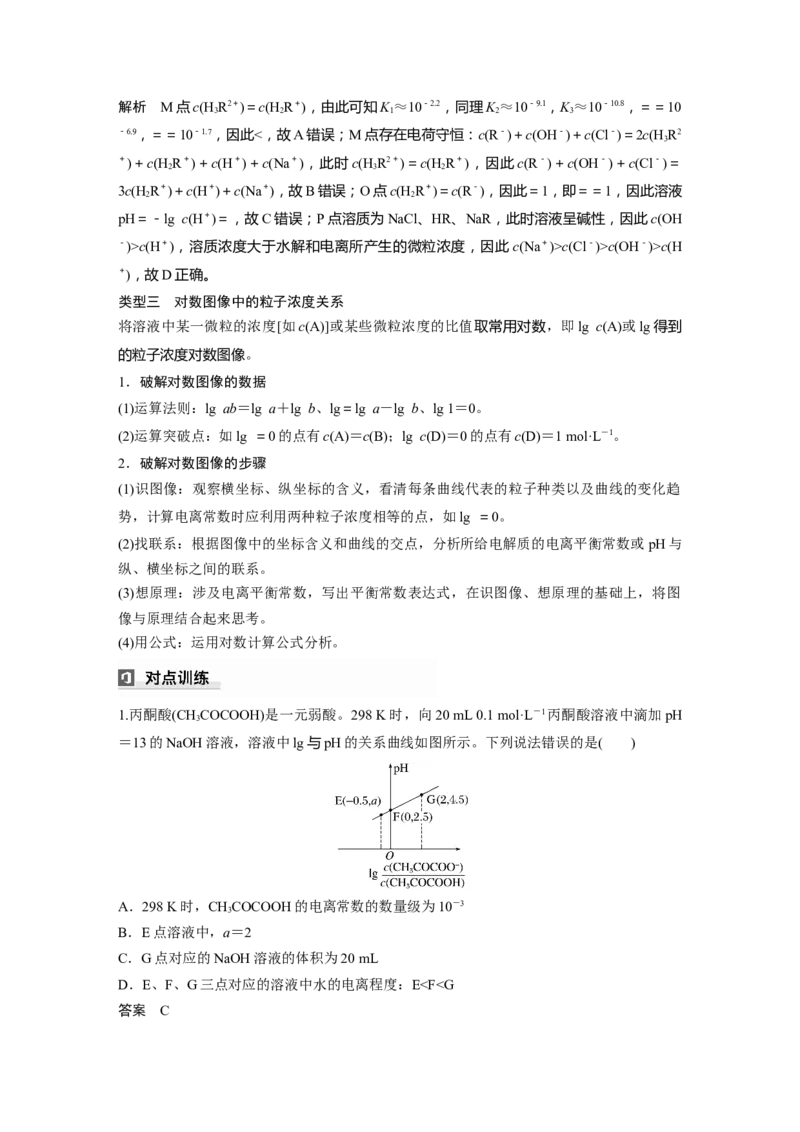
3.(2021·山东,15改编)赖氨酸[H N+(CH)CH(NH)COO-,用HR表示]是人体必需氨基酸,
3 2 4 2
其盐酸盐(H RCl )在水溶液中存在如下平衡:HR2+HR+HRR-。向一定
3 2 3 2
浓度的HRCl 溶液中滴加NaOH溶液,溶液中HR2+、HR+、HR和R-的分布系数δ(X)随
3 2 3 2
pH变化如图所示。已知δ(X)=,下列表述正确的是( )
A.>
B.M点,c(Cl-) +c(OH-)+c(R-)=2c(H R+)+c(Na+)+c(H+)
2
C.O点,pH=
D.P点,c(Na+)>c(Cl-)>c(OH-)>c(H+)
答案 D解析 M点c(H R2+)=c(H R+),由此可知K ≈10-2.2,同理K ≈10-9.1,K ≈10-10.8,==10
3 2 1 2 3
-6.9,==10-1.7,因此<,故A错误;M点存在电荷守恒:c(R-)+c(OH-)+c(Cl-)=2c(H R2
3
+)+c(H R+)+c(H+)+c(Na+),此时c(H R2+)=c(H R+),因此c(R-)+c(OH-)+c(Cl-)=
2 3 2
3c(H R+)+c(H+)+c(Na+),故B错误;O点c(H R+)=c(R-),因此=1,即==1,因此溶液
2 2
pH=-lg c(H+)=,故C错误;P点溶质为NaCl、HR、NaR,此时溶液呈碱性,因此c(OH
-)>c(H+),溶质浓度大于水解和电离所产生的微粒浓度,因此 c(Na+)>c(Cl-)>c(OH-)>c(H
+),故D正确。
类型三 对数图像中的粒子浓度关系
将溶液中某一微粒的浓度[如c(A)]或某些微粒浓度的比值取常用对数,即lg c(A)或lg得到
的粒子浓度对数图像。
1.破解对数图像的数据
(1)运算法则:lg ab=lg a+lg b、lg=lg a-lg b、lg 1=0。
(2)运算突破点:如lg =0的点有c(A)=c(B);lg c(D)=0的点有c(D)=1 mol·L-1。
2.破解对数图像的步骤
(1)识图像:观察横坐标、纵坐标的含义,看清每条曲线代表的粒子种类以及曲线的变化趋
势,计算电离常数时应利用两种粒子浓度相等的点,如lg =0。
(2)找联系:根据图像中的坐标含义和曲线的交点,分析所给电解质的电离平衡常数或pH与
纵、横坐标之间的联系。
(3)想原理:涉及电离平衡常数,写出平衡常数表达式,在识图像、想原理的基础上,将图
像与原理结合起来思考。
(4)用公式:运用对数计算公式分析。
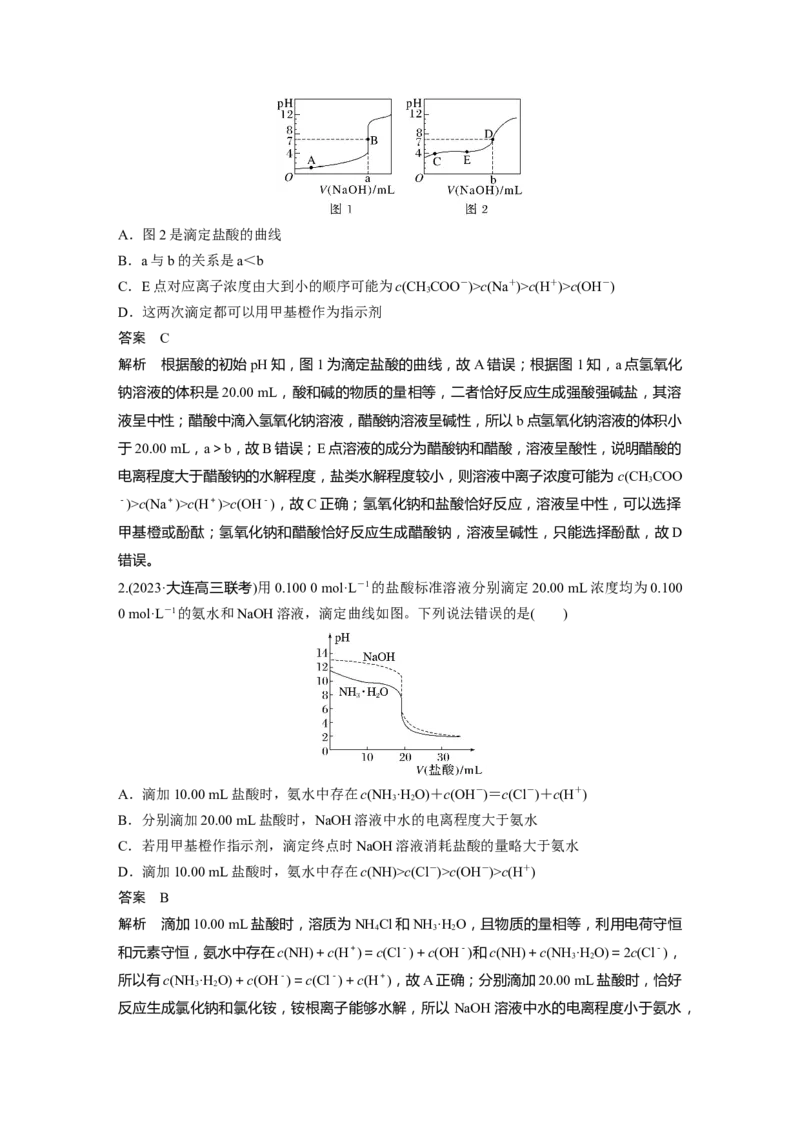
1.丙酮酸(CHCOCOOH)是一元弱酸。298 K时,向20 mL 0.1 mol·L-1丙酮酸溶液中滴加pH
3
=13的NaOH溶液,溶液中lg与pH的关系曲线如图所示。下列说法错误的是( )
A.298 K时,CHCOCOOH的电离常数的数量级为10-3
3
B.E点溶液中,a=2
C.G点对应的NaOH溶液的体积为20 mL
D.E、F、G三点对应的溶液中水的电离程度:Ec(OH-)
D.当混合溶液呈中性时,c(Na+)>c(HX-)>c(X2-)>c(OH-)=c(H+)
答案 D
解析 横坐标取0时,曲线M对应pH约为5.4,曲线N对应pH约为4.4,因为是NaOH滴
定HX溶液,所以在酸性较强的溶液中会存在 c(HX-)=c(H X),所以曲线N表示pH与lg
2 2
的变化关系,B正确;=1时,即lg=0,pH≈5.4,c(H+)=1×10-5.4 mol·L-1,K ==1×10
a2
-5.4,A正确;NaHX溶液中,c(HX-)>c(X2-),即<1,lg <0,此时溶液呈酸性,C正确;当
溶液呈中性时,由曲线M可知lg >0,>1,即c(X2-)>c(HX-),D错误。
课时精练
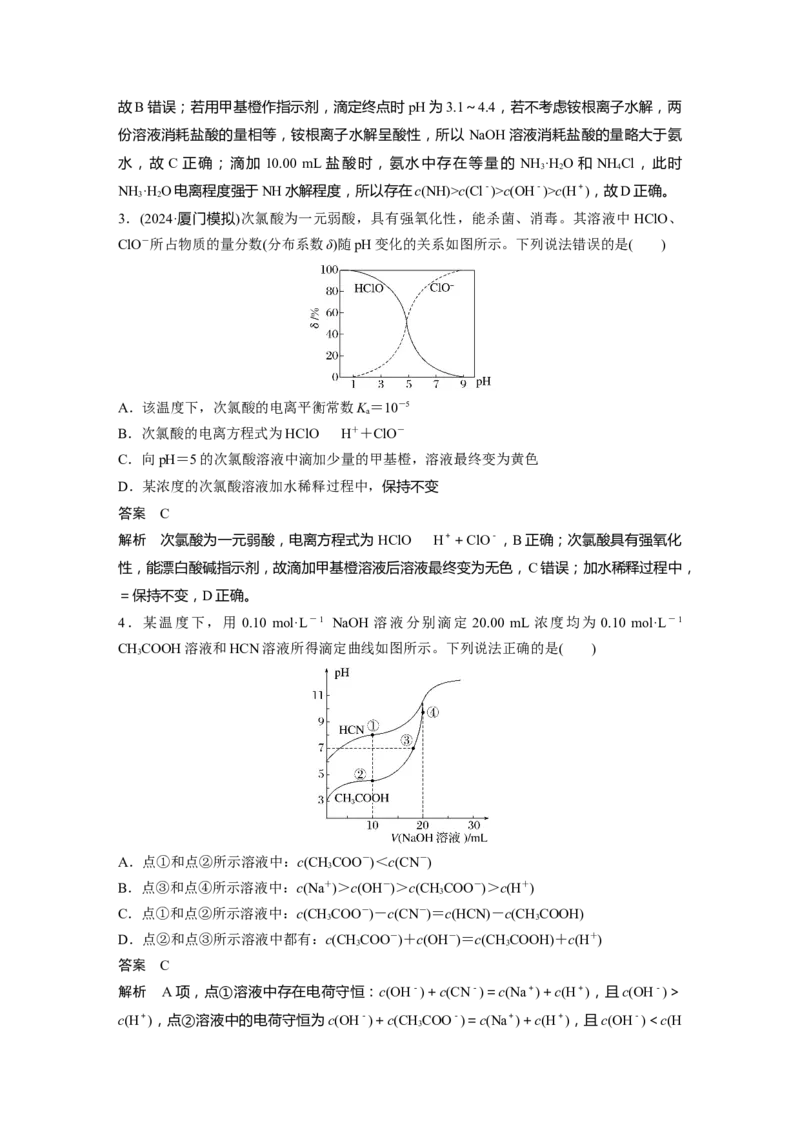
1.常温下,用0.10 mol·L-1 NaOH溶液分别滴定20.00 mL 0.10 mol·L-1盐酸和20.00 mL
0.10 mol·L-1 CHCOOH溶液,得到两条滴定曲线,如图所示,则下列说法正确的是( )
3A.图2是滴定盐酸的曲线
B.a与b的关系是a<b
C.E点对应离子浓度由大到小的顺序可能为c(CHCOO-)>c(Na+)>c(H+)>c(OH-)
3
D.这两次滴定都可以用甲基橙作为指示剂
答案 C
解析 根据酸的初始pH知,图1为滴定盐酸的曲线,故A错误;根据图1知,a点氢氧化
钠溶液的体积是20.00 mL,酸和碱的物质的量相等,二者恰好反应生成强酸强碱盐,其溶
液呈中性;醋酸中滴入氢氧化钠溶液,醋酸钠溶液呈碱性,所以b点氢氧化钠溶液的体积小
于20.00 mL,a>b,故B错误;E点溶液的成分为醋酸钠和醋酸,溶液呈酸性,说明醋酸的
电离程度大于醋酸钠的水解程度,盐类水解程度较小,则溶液中离子浓度可能为 c(CHCOO
3
-)>c(Na+)>c(H+)>c(OH-),故C正确;氢氧化钠和盐酸恰好反应,溶液呈中性,可以选择
甲基橙或酚酞;氢氧化钠和醋酸恰好反应生成醋酸钠,溶液呈碱性,只能选择酚酞,故D
错误。
2.(2023·大连高三联考)用0.100 0 mol·L-1的盐酸标准溶液分别滴定20.00 mL浓度均为0.100
0 mol·L-1的氨水和NaOH溶液,滴定曲线如图。下列说法错误的是( )
A.滴加10.00 mL盐酸时,氨水中存在c(NH ·H O)+c(OH-)=c(Cl-)+c(H+)
3 2
B.分别滴加20.00 mL盐酸时,NaOH溶液中水的电离程度大于氨水
C.若用甲基橙作指示剂,滴定终点时NaOH溶液消耗盐酸的量略大于氨水
D.滴加10.00 mL盐酸时,氨水中存在c(NH)>c(Cl-)>c(OH-)>c(H+)
答案 B
解析 滴加10.00 mL盐酸时,溶质为NH Cl和NH ·H O,且物质的量相等,利用电荷守恒
4 3 2
和元素守恒,氨水中存在c(NH)+c(H+)=c(Cl-)+c(OH-)和c(NH)+c(NH ·H O)=2c(Cl-),
3 2
所以有c(NH ·H O)+c(OH-)=c(Cl-)+c(H+),故A正确;分别滴加20.00 mL盐酸时,恰好
3 2
反应生成氯化钠和氯化铵,铵根离子能够水解,所以 NaOH溶液中水的电离程度小于氨水,故B错误;若用甲基橙作指示剂,滴定终点时pH为3.1~4.4,若不考虑铵根离子水解,两
份溶液消耗盐酸的量相等,铵根离子水解呈酸性,所以 NaOH溶液消耗盐酸的量略大于氨
水,故 C 正确;滴加 10.00 mL 盐酸时,氨水中存在等量的 NH ·H O 和 NH Cl,此时
3 2 4
NH ·H O电离程度强于NH水解程度,所以存在c(NH)>c(Cl-)>c(OH-)>c(H+),故D正确。
3 2
3.(2024·厦门模拟)次氯酸为一元弱酸,具有强氧化性,能杀菌、消毒。其溶液中HClO、
ClO-所占物质的量分数(分布系数δ)随pH变化的关系如图所示。下列说法错误的是( )
A.该温度下,次氯酸的电离平衡常数K=10-5
a
B.次氯酸的电离方程式为HClOH++ClO-
C.向pH=5的次氯酸溶液中滴加少量的甲基橙,溶液最终变为黄色
D.某浓度的次氯酸溶液加水稀释过程中,保持不变
答案 C
解析 次氯酸为一元弱酸,电离方程式为HClOH++ClO-,B正确;次氯酸具有强氧化
性,能漂白酸碱指示剂,故滴加甲基橙溶液后溶液最终变为无色,C错误;加水稀释过程中,
=保持不变,D正确。
4.某温度下,用 0.10 mol·L-1 NaOH 溶液分别滴定 20.00 mL 浓度均为 0.10 mol·L-1
CHCOOH溶液和HCN溶液所得滴定曲线如图所示。下列说法正确的是( )
3
A.点①和点②所示溶液中:c(CHCOO-)<c(CN-)
3
B.点③和点④所示溶液中:c(Na+)>c(OH-)>c(CHCOO-)>c(H+)
3
C.点①和点②所示溶液中:c(CHCOO-)-c(CN-)=c(HCN)-c(CHCOOH)
3 3
D.点②和点③所示溶液中都有:c(CHCOO-)+c(OH-)=c(CHCOOH)+c(H+)
3 3
答案 C
解析 A项,点①溶液中存在电荷守恒:c(OH-)+c(CN-)=c(Na+)+c(H+),且c(OH-)>
c(H+),点②溶液中的电荷守恒为c(OH-)+c(CHCOO-)=c(Na+)+c(H+),且c(OH-)<c(H
3+),二者中钠离子浓度相同,所以c(CHCOO-)>c(CN-),错误;B项,点③溶液pH=7,
3
则c(OH-)=c(H+),则点③溶液中c(Na+)=c(CHCOO-)>c(H+)=c(OH-),错误;C项,点
3
①所示的溶液中存在元素守恒:c(HCN)+c(CN-)=2c(Na+),点②所示的溶液中存在元素守
恒:c(CHCOOH)+c(CHCOO-)=2c(Na+),二者中钠离子浓度相同,则c(HCN)+c(CN-)=
3 3
c(CHCOOH)+c(CHCOO-),即c(CHCOO-)-c(CN-)=c(HCN)-c(CHCOOH),正确。
3 3 3 3
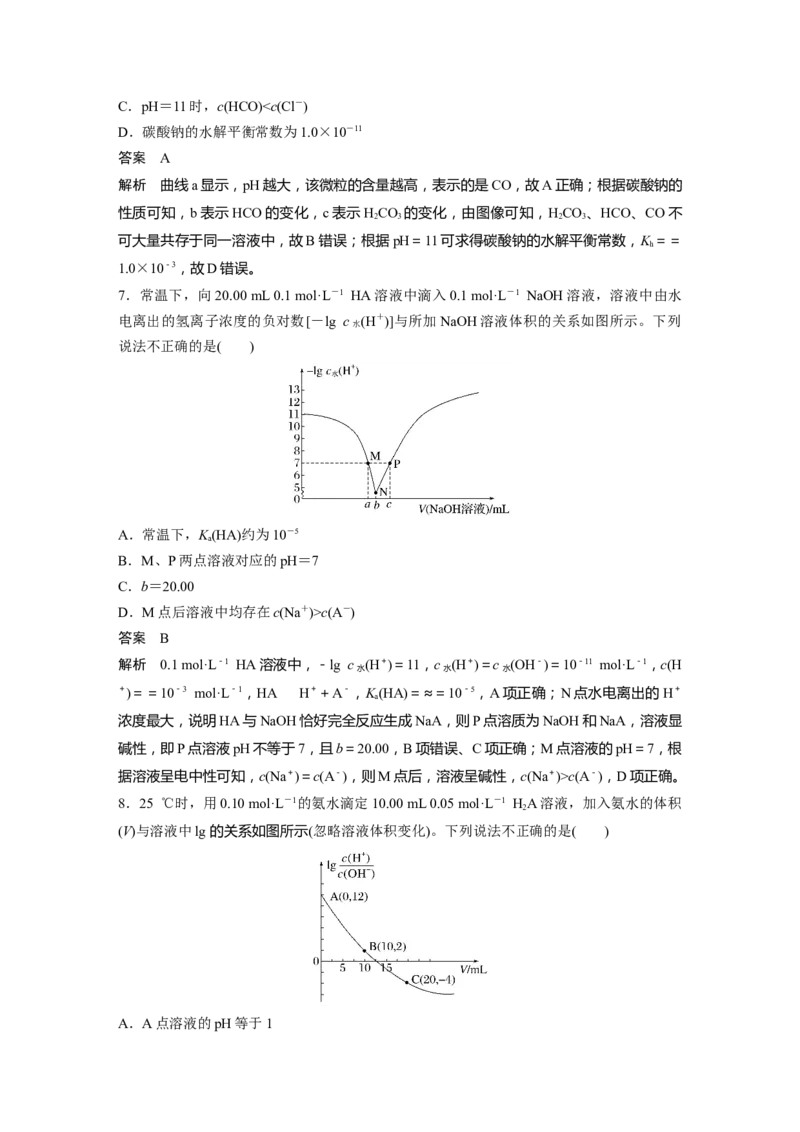
5.(2021·浙江6月选考,23)取两份10 mL 0.05 mol·L-1的NaHCO 溶液,一份滴加 0.05
3
mol·L-1的盐酸,另一份滴加0.05 mol·L-1 NaOH溶液,溶液的pH随加入酸(或碱)体积的变
化如图,下列说法不正确的是( )
A.由a点可知:NaHCO 溶液中HCO的水解程度大于电离程度
3
B.a→b→c过程中:c(HCO)+2c(CO)+c(OH-)逐渐减小
C.a→d→e过程中:c(Na+)y
答案 C
解析 a点溶质为NaHCO ,此时溶液呈碱性,由此可知,NaHCO 溶液中HCO的水解程度
3 3
大于电离程度,故A正确;由电荷守恒可知,a→b→c过程溶液中c(HCO)+2c(CO)+c(OH
-)=c(H+)+c(Na+),滴加NaOH溶液的过程中c(Na+)保持不变,c(H+)逐渐减小,因此
c(HCO)+2c(CO)+c(OH-)逐渐减小,故B正确;由元素守恒可知,a点溶液中c(Na+)=
c(HCO)+c(CO)+c(H CO),向NaHCO 溶液中滴加盐酸过程中有 CO 逸出,因此a→d→e
2 3 3 2
过程中c(Na+)>c(HCO)+c(CO)+c(H CO),故C错误;c点溶液中c(Na+)+c(H+)=(0.05+
2 3
10-11.3)mol·L-1,e点溶液体积增大1倍,此时溶液中c(Na+)+c(H+)=(0.025+10-4.3)mol·L-
1,因此x>y,故D正确。
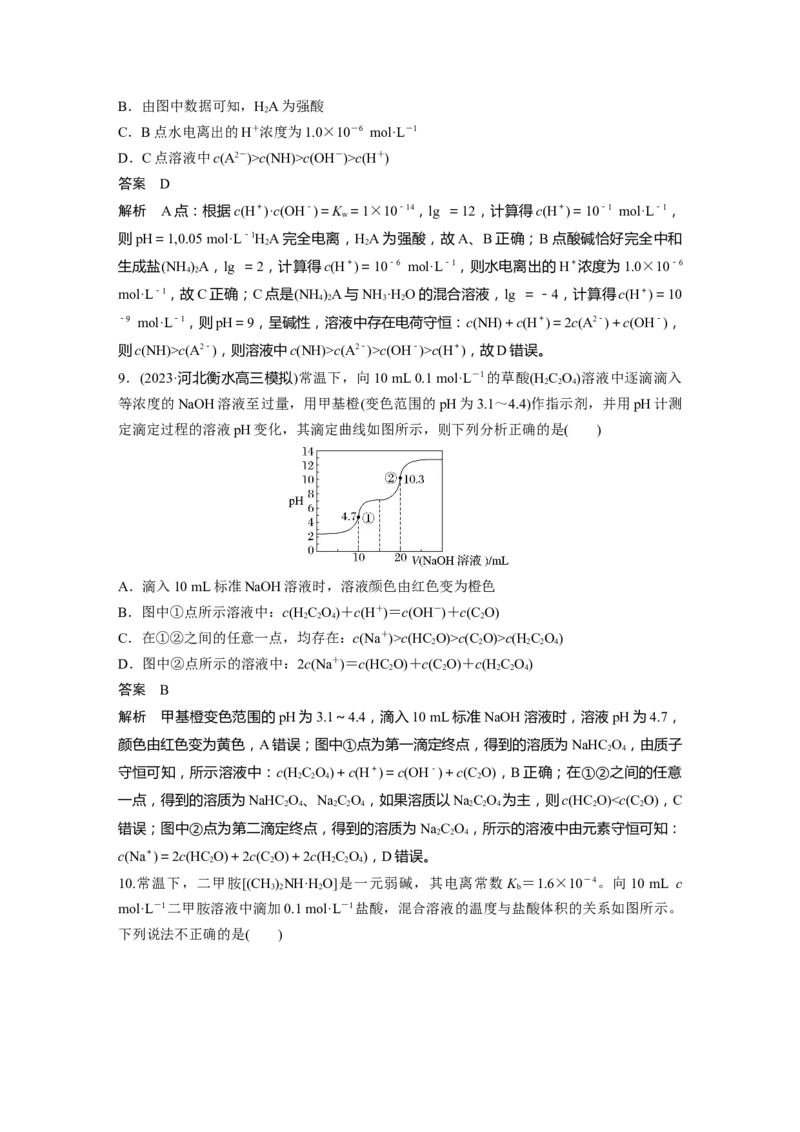
6.常温下,在20 mL 0.1 mol·L-1 Na CO 溶液中逐滴加入40 mL 0.1 mol·L-1稀盐酸,溶液中
2 3
含碳元素各种微粒(CO 因逸出未画出)的物质的量分数(纵轴)随溶液pH变化的部分情况如图
2
所示。下列说法正确的是( )
A.曲线a表示CO的变化曲线
B.HCO、HCO、CO可大量共存于同一溶液中
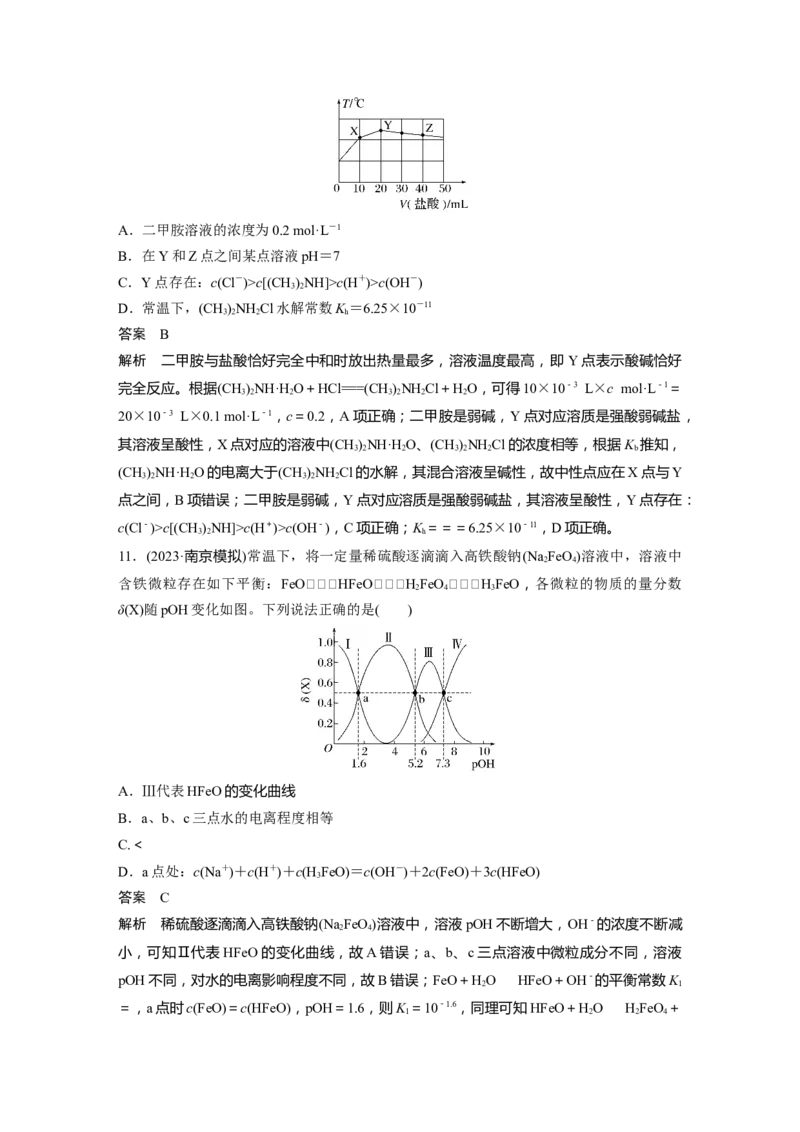
2 3C.pH=11时,c(HCO)c(A-)
答案 B
解析 0.1 mol·L-1 HA溶液中,-lg c (H+)=11,c (H+)=c (OH-)=10-11 mol·L-1,c(H
水 水 水
+)==10-3 mol·L-1,HAH++A-,K(HA)=≈=10-5,A项正确;N点水电离出的H+
a
浓度最大,说明HA与NaOH恰好完全反应生成NaA,则P点溶质为NaOH和NaA,溶液显
碱性,即P点溶液pH不等于7,且b=20.00,B项错误、C项正确;M点溶液的pH=7,根
据溶液呈电中性可知,c(Na+)=c(A-),则M点后,溶液呈碱性,c(Na+)>c(A-),D项正确。
8.25 ℃时,用0.10 mol·L-1的氨水滴定10.00 mL 0.05 mol·L-1 HA溶液,加入氨水的体积
2
(V)与溶液中lg 的关系如图所示(忽略溶液体积变化)。下列说法不正确的是( )
A.A点溶液的pH等于1B.由图中数据可知,HA为强酸
2
C.B点水电离出的H+浓度为1.0×10-6 mol·L-1
D.C点溶液中c(A2-)>c(NH)>c(OH-)>c(H+)
答案 D
解析 A点:根据c(H+)·c(OH-)=K =1×10-14,lg =12,计算得c(H+)=10-1 mol·L-1,
w
则pH=1,0.05 mol·L-1HA完全电离,HA为强酸,故A、B正确;B点酸碱恰好完全中和
2 2
生成盐(NH )A,lg =2,计算得c(H+)=10-6 mol·L-1,则水电离出的H+浓度为1.0×10-6
4 2
mol·L-1,故C正确;C点是(NH )A与NH ·H O的混合溶液,lg =-4,计算得c(H+)=10
4 2 3 2
-9 mol·L-1,则pH=9,呈碱性,溶液中存在电荷守恒:c(NH)+c(H+)=2c(A2-)+c(OH-),
则c(NH)>c(A2-),则溶液中c(NH)>c(A2-)>c(OH-)>c(H+),故D错误。
9.(2023·河北衡水高三模拟)常温下,向10 mL 0.1 mol·L-1的草酸(H C O)溶液中逐滴滴入
2 2 4
等浓度的NaOH溶液至过量,用甲基橙(变色范围的pH为3.1~4.4)作指示剂,并用pH计测
定滴定过程的溶液pH变化,其滴定曲线如图所示,则下列分析正确的是( )
A.滴入10 mL标准NaOH溶液时,溶液颜色由红色变为橙色
B.图中①点所示溶液中:c(H C O)+c(H+)=c(OH-)+c(C O)
2 2 4 2
C.在①②之间的任意一点,均存在:c(Na+)>c(HC O)>c(C O)>c(H C O)
2 2 2 2 4
D.图中②点所示的溶液中:2c(Na+)=c(HC O)+c(C O)+c(H C O)
2 2 2 2 4
答案 B
解析 甲基橙变色范围的pH为3.1~4.4,滴入10 mL标准NaOH溶液时,溶液pH为4.7,
颜色由红色变为黄色,A错误;图中①点为第一滴定终点,得到的溶质为NaHC O,由质子
2 4
守恒可知,所示溶液中:c(H C O)+c(H+)=c(OH-)+c(C O),B正确;在①②之间的任意
2 2 4 2
一点,得到的溶质为NaHC O 、NaC O ,如果溶质以NaC O 为主,则c(HC O)c[(CH )NH]>c(H+)>c(OH-)
3 2
D.常温下,(CH)NH Cl水解常数K =6.25×10-11
3 2 2 h
答案 B
解析 二甲胺与盐酸恰好完全中和时放出热量最多,溶液温度最高,即 Y点表示酸碱恰好
完全反应。根据(CH)NH·HO+HCl===(CH)NH Cl+HO,可得10×10-3 L×c mol·L-1=
3 2 2 3 2 2 2
20×10-3 L×0.1 mol·L-1,c=0.2,A项正确;二甲胺是弱碱,Y点对应溶质是强酸弱碱盐,
其溶液呈酸性,X点对应的溶液中(CH)NH·HO、(CH)NH Cl的浓度相等,根据K 推知,
3 2 2 3 2 2 b
(CH)NH·HO的电离大于(CH)NH Cl的水解,其混合溶液呈碱性,故中性点应在X点与Y
3 2 2 3 2 2
点之间,B项错误;二甲胺是弱碱,Y点对应溶质是强酸弱碱盐,其溶液呈酸性,Y点存在:
c(Cl-)>c[(CH )NH]>c(H+)>c(OH-),C项正确;K ===6.25×10-11,D项正确。
3 2 h
11.(2023·南京模拟)常温下,将一定量稀硫酸逐滴滴入高铁酸钠(Na FeO)溶液中,溶液中
2 4
含铁微粒存在如下平衡:FeOHFeOHFeOHFeO,各微粒的物质的量分数
2 4 3
δ(X)随pOH变化如图。下列说法正确的是( )
A.Ⅲ代表HFeO的变化曲线
B.a、b、c三点水的电离程度相等
C.<
D.a点处:c(Na+)+c(H+)+c(H FeO)=c(OH-)+2c(FeO)+3c(HFeO)
3
答案 C
解析 稀硫酸逐滴滴入高铁酸钠(Na FeO)溶液中,溶液pOH不断增大,OH-的浓度不断减
2 4
小,可知Ⅱ代表HFeO的变化曲线,故A错误;a、b、c三点溶液中微粒成分不同,溶液
pOH不同,对水的电离影响程度不同,故B错误;FeO+HOHFeO+OH-的平衡常数K
2 1
=,a点时c(FeO)=c(HFeO),pOH=1.6,则K =10-1.6,同理可知HFeO+HOHFeO +
1 2 2 4OH-的平衡常数K =10-5.2,HFeO+HOHFeO+OH-的平衡常数K =10-7.3,由此推出
2 2 4 2 3 3
<,故 C 正确;a点溶液中 c(FeO)=c(HFeO),溶液中存在电荷守恒:c(Na+)+c(H+)+
c(H FeO)=c(OH-)+2c(FeO)+c(HFeO)+2c(SO),从O到a点溶液中发生反应:2NaFeO +
3 2 4
HSO ===2NaHFeO +NaSO ,溶液中 c(SO)≠c(HFeO),则 a 点溶液中 c(Na+)+c(H+)+
2 4 4 2 4
c(H FeO)≠c(OH-)+2c(FeO)+3c(HFeO),故D错误。
3
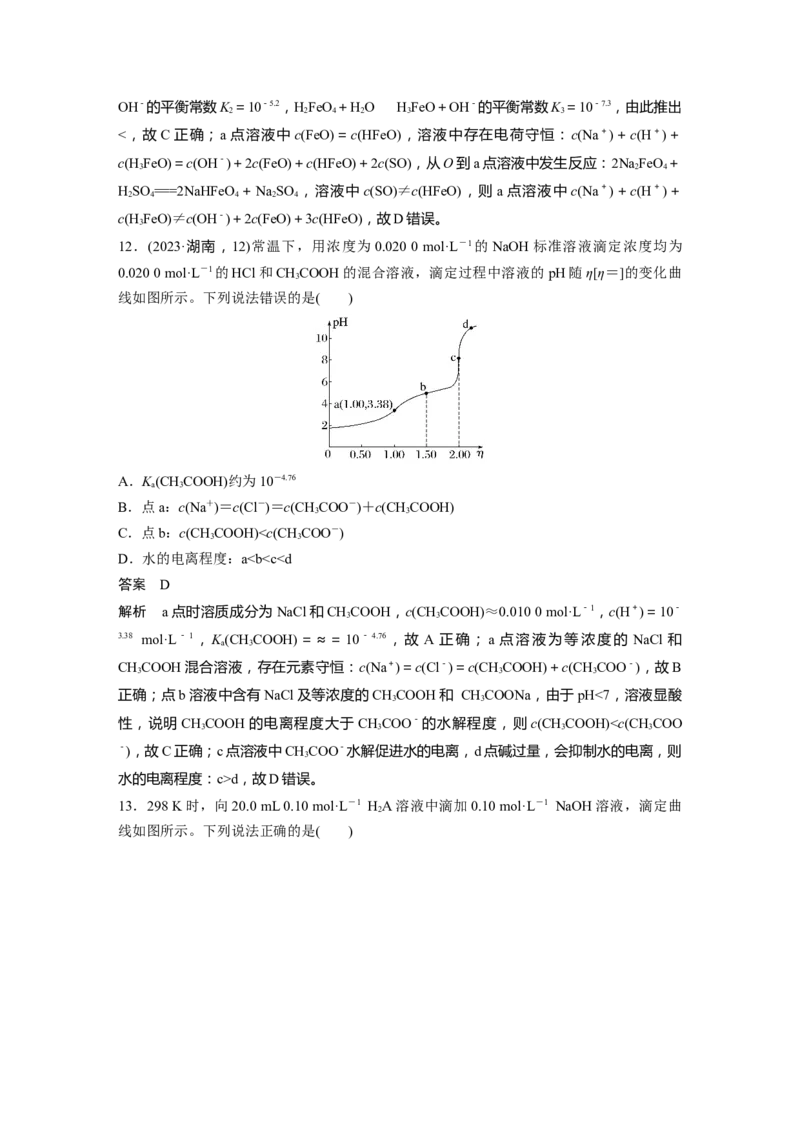
12.(2023·湖南,12)常温下,用浓度为0.020 0 mol·L-1的NaOH标准溶液滴定浓度均为
0.020 0 mol·L-1的HCl和CHCOOH的混合溶液,滴定过程中溶液的pH随η[η=]的变化曲
3
线如图所示。下列说法错误的是( )
A.K(CHCOOH)约为10-4.76
a 3
B.点a:c(Na+)=c(Cl-)=c(CHCOO-)+c(CHCOOH)
3 3
C.点b:c(CHCOOH)d,故D错误。
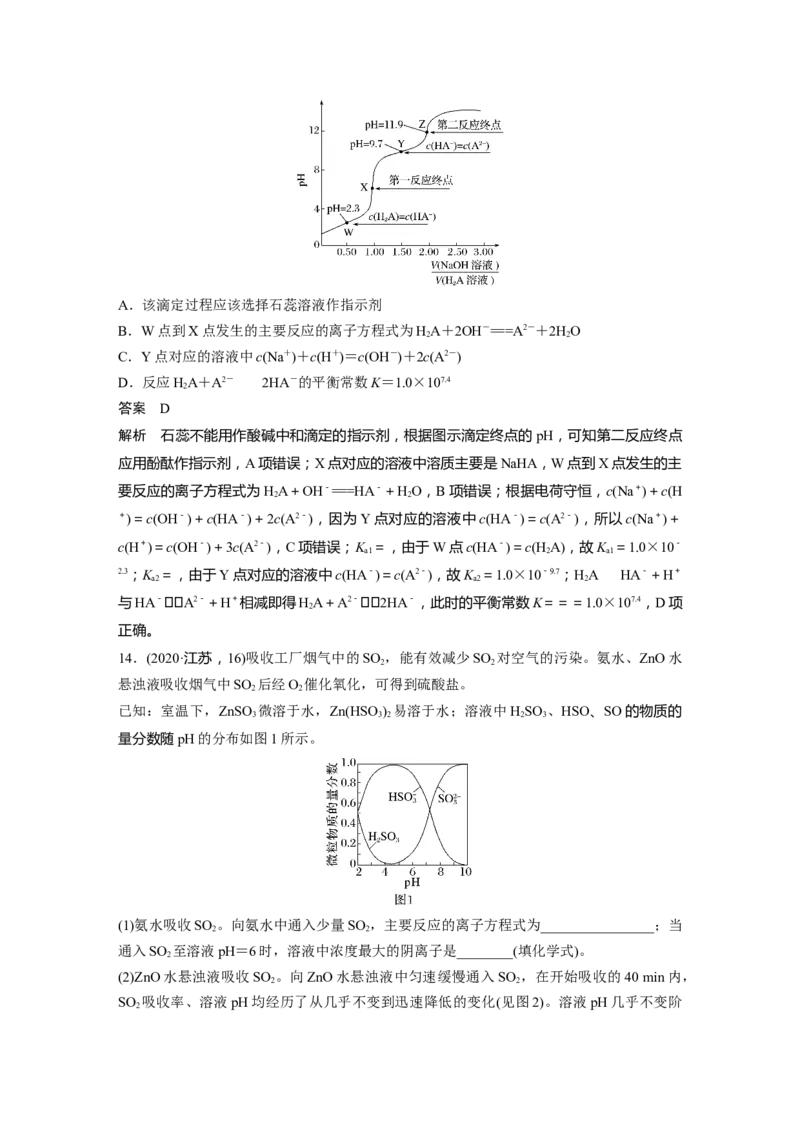
13.298 K时,向20.0 mL 0.10 mol·L-1 HA溶液中滴加0.10 mol·L-1 NaOH溶液,滴定曲
2
线如图所示。下列说法正确的是( )A.该滴定过程应该选择石蕊溶液作指示剂
B.W点到X点发生的主要反应的离子方程式为HA+2OH-===A2-+2HO
2 2
C.Y点对应的溶液中c(Na+)+c(H+)=c(OH-)+2c(A2-)
D.反应HA+A2-2HA-的平衡常数K=1.0×107.4
2
答案 D
解析 石蕊不能用作酸碱中和滴定的指示剂,根据图示滴定终点的pH,可知第二反应终点
应用酚酞作指示剂,A项错误;X点对应的溶液中溶质主要是NaHA,W点到X点发生的主
要反应的离子方程式为HA+OH-===HA-+HO,B项错误;根据电荷守恒,c(Na+)+c(H
2 2
+)=c(OH-)+c(HA-)+2c(A2-),因为Y点对应的溶液中c(HA-)=c(A2-),所以c(Na+)+
c(H+)=c(OH-)+3c(A2-),C项错误;K =,由于W点c(HA-)=c(H A),故K =1.0×10-
a1 2 a1
2.3;K =,由于Y点对应的溶液中c(HA-)=c(A2-),故K =1.0×10-9.7;HAHA-+H+
a2 a2 2
与HA-A2-+H+相减即得HA+A2-2HA-,此时的平衡常数K===1.0×107.4,D项
2
正确。
14.(2020·江苏,16)吸收工厂烟气中的SO ,能有效减少SO 对空气的污染。氨水、ZnO水
2 2
悬浊液吸收烟气中SO 后经O 催化氧化,可得到硫酸盐。
2 2
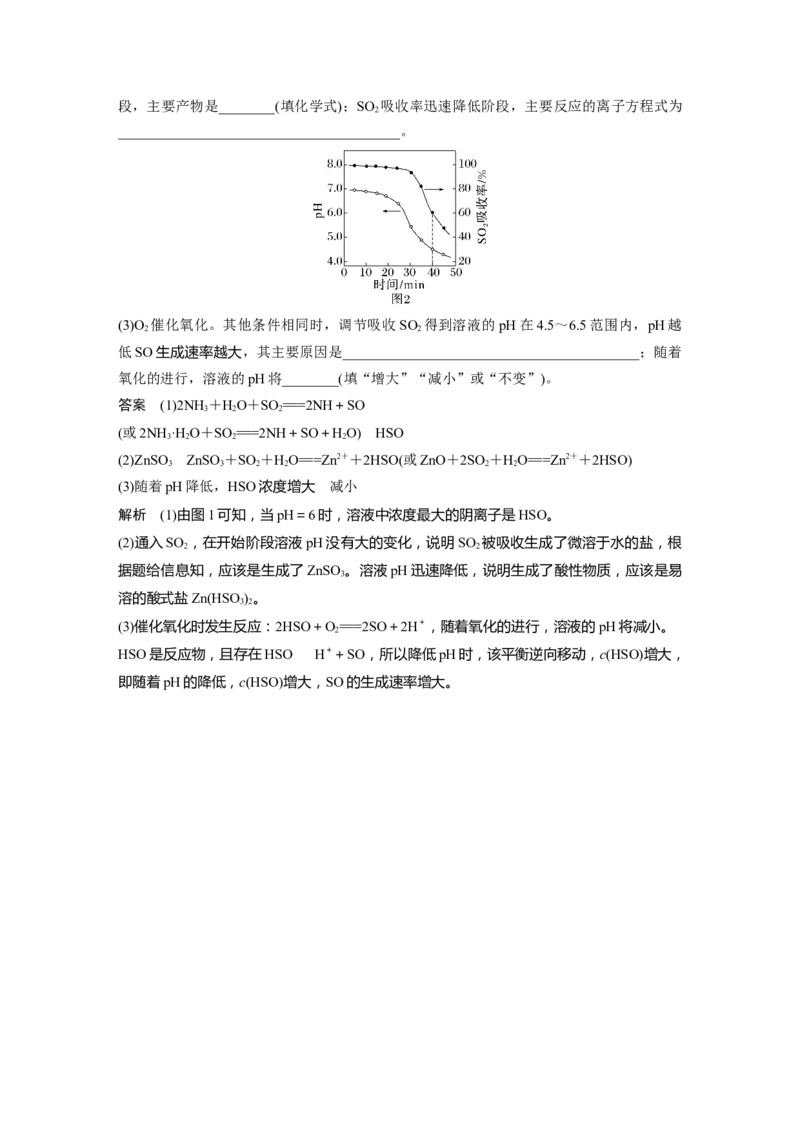
已知:室温下,ZnSO 微溶于水,Zn(HSO ) 易溶于水;溶液中HSO 、HSO、SO的物质的
3 3 2 2 3
量分数随pH的分布如图1所示。
(1)氨水吸收SO 。向氨水中通入少量SO ,主要反应的离子方程式为________________;当
2 2
通入SO 至溶液pH=6时,溶液中浓度最大的阴离子是________(填化学式)。
2
(2)ZnO水悬浊液吸收SO 。向ZnO水悬浊液中匀速缓慢通入SO ,在开始吸收的40 min内,
2 2
SO 吸收率、溶液pH均经历了从几乎不变到迅速降低的变化(见图2)。溶液pH几乎不变阶
2段,主要产物是________(填化学式);SO 吸收率迅速降低阶段,主要反应的离子方程式为
2
________________________________________。
(3)O 催化氧化。其他条件相同时,调节吸收SO 得到溶液的pH在4.5~6.5范围内,pH越
2 2
低SO生成速率越大,其主要原因是__________________________________________;随着
氧化的进行,溶液的pH将________(填“增大”“减小”或“不变”)。
答案 (1)2NH +HO+SO ===2NH+SO
3 2 2
(或2NH ·H O+SO ===2NH+SO+HO) HSO
3 2 2 2
(2)ZnSO ZnSO+SO +HO===Zn2++2HSO(或ZnO+2SO +HO===Zn2++2HSO)
3 3 2 2 2 2
(3)随着pH降低,HSO浓度增大 减小
解析 (1)由图1可知,当pH=6时,溶液中浓度最大的阴离子是HSO。
(2)通入SO ,在开始阶段溶液pH没有大的变化,说明SO 被吸收生成了微溶于水的盐,根
2 2
据题给信息知,应该是生成了ZnSO 。溶液pH迅速降低,说明生成了酸性物质,应该是易
3
溶的酸式盐Zn(HSO )。
3 2
(3)催化氧化时发生反应:2HSO+O===2SO+2H+,随着氧化的进行,溶液的pH将减小。
2
HSO是反应物,且存在HSOH++SO,所以降低pH时,该平衡逆向移动,c(HSO)增大,
即随着pH的降低,c(HSO)增大,SO的生成速率增大。