文档内容
第 57 讲 难溶电解质的沉淀溶解平衡
[复习目标] 1.了解难溶电解质的沉淀溶解平衡。2.理解溶度积(K )的含义,并能进行相关计
sp
算。3.了解沉淀的生成、溶解与转化,并能应用化学平衡原理解释。
考点一 沉淀溶解平衡 溶度积
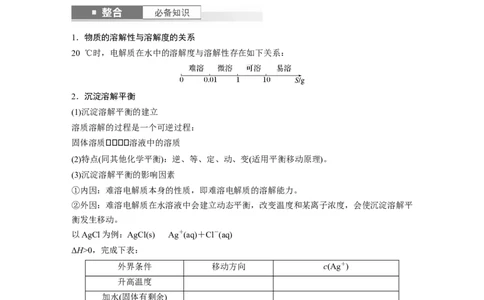
1.物质的溶解性与溶解度的关系
20 ℃时,电解质在水中的溶解度与溶解性存在如下关系:
2.沉淀溶解平衡
(1)沉淀溶解平衡的建立
溶质溶解的过程是一个可逆过程:
固体溶质溶液中的溶质
(2)特点(同其他化学平衡):逆、等、定、动、变(适用平衡移动原理)。
(3)沉淀溶解平衡的影响因素
①内因:难溶电解质本身的性质,即难溶电解质的溶解能力。
②外因:难溶电解质在水溶液中会建立动态平衡,改变温度和某离子浓度,会使沉淀溶解平
衡发生移动。
以AgCl为例:AgCl(s)Ag+(aq)+Cl-(aq)
ΔH>0,完成下表:
外界条件 移动方向 c(Ag+)
升高温度
加水(固体有剩余)
加入少量AgNO(s)
3
加入NaS(s)
2
通入HCl
通入NH
3
[应用举例]
将足量BaCO 固体分别加入:①30 mL水;②10 mL 0.2 mol·L-1NaCO 溶液;③50 mL 0.01
3 2 3mol·
L-1 BaCl 溶液;④100 mL 0.01 mol·L-1盐酸中溶解至溶液饱和。
2
所得溶液中c(Ba2+)由大到小的顺序为____________________________。
3.溶度积常数
(1)溶度积常数和离子积比较
以A B (s)mAn+(aq)+nBm-(aq)为例:
m n
溶度积(K ) 离子积(Q)
sp
含义 沉淀溶解平衡的平衡常数 溶液中有关离子浓度幂的乘积
K (A B )= Q(A B )=
sp m n m n
表达式 ________________________,式中的浓 __________________,式中的浓
度是平衡浓度 度是任意浓度
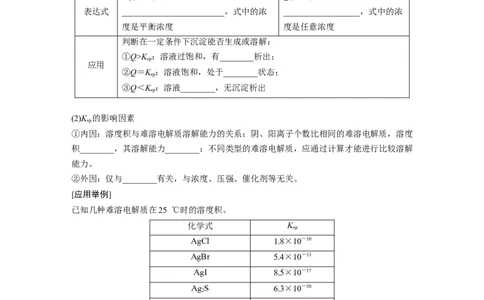
判断在一定条件下沉淀能否生成或溶解:
①Q>K :溶液过饱和,有________析出;
sp
应用
②Q=K :溶液饱和,处于________状态;
sp
③Q<K :溶液________,无沉淀析出
sp
(2)K 的影响因素
sp
①内因:溶度积与难溶电解质溶解能力的关系:阴、阳离子个数比相同的难溶电解质,溶度
积________,其溶解能力________;不同类型的难溶电解质,应通过计算才能进行比较溶解
能力。
②外因:仅与________有关,与浓度、压强、催化剂等无关。
[应用举例]
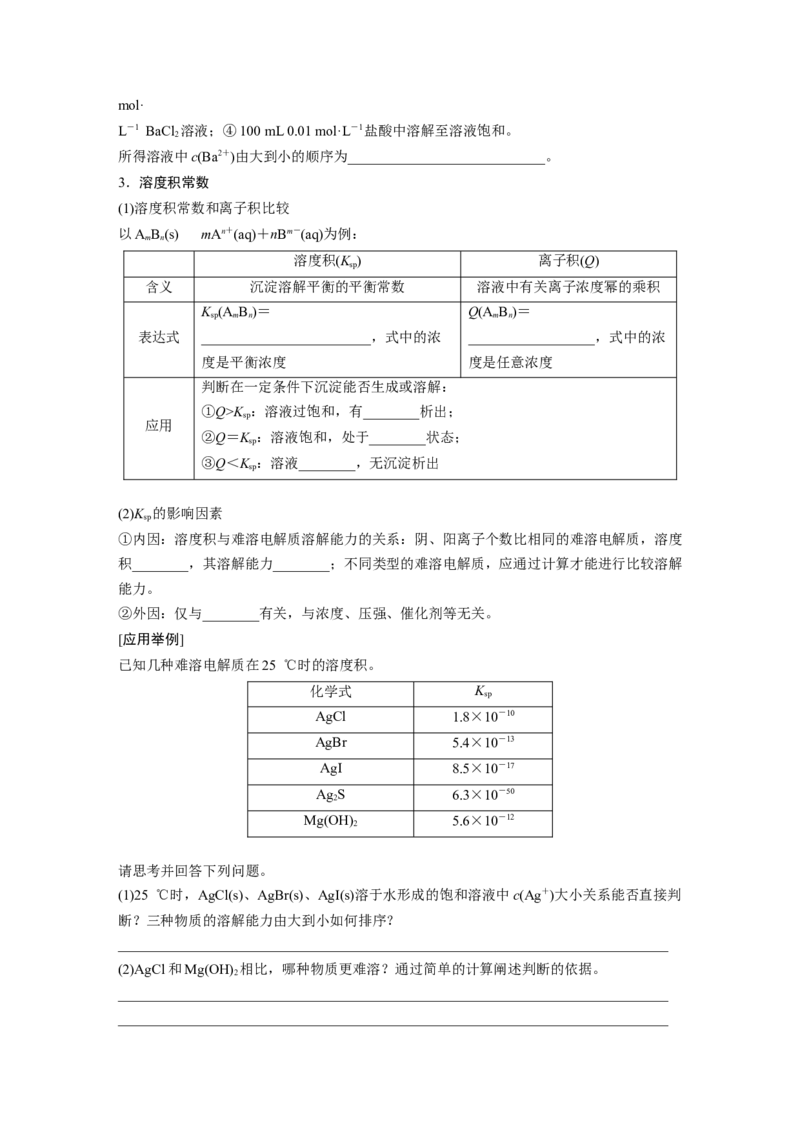
已知几种难溶电解质在25 ℃时的溶度积。
化学式 K
sp
AgCl 1.8×10-10
AgBr 5.4×10-13
AgI 8.5×10-17
Ag S 6.3×10-50
2
Mg(OH) 5.6×10-12
2
请思考并回答下列问题。
(1)25 ℃时,AgCl(s)、AgBr(s)、AgI(s)溶于水形成的饱和溶液中c(Ag+)大小关系能否直接判
断?三种物质的溶解能力由大到小如何排序?
______________________________________________________________________________
(2)AgCl和Mg(OH) 相比,哪种物质更难溶?通过简单的计算阐述判断的依据。
2
______________________________________________________________________________
______________________________________________________________________________一、沉淀溶解平衡移动
1.已知溶液中存在平衡:Ca(OH) (s)Ca2+(aq)+2OH-(aq) ΔH<0,下列有关该平衡体
2
系的说法不正确的是______________(填序号)。
①升高温度,平衡逆向移动
②向溶液中加入少量碳酸钠粉末能增大钙离子的浓度
③除去氯化钠溶液中混有的少量钙离子,可以向溶液中加入适量的NaOH溶液
④恒温下,向溶液中加入CaO,溶液的pH升高
⑤给溶液加热,溶液的pH升高
⑥向溶液中加入NaCO 溶液,其中固体质量增加
2 3
⑦向溶液中加入少量NaOH固体,Ca(OH) 固体质量不变
2
2.(2023·青海海东统考模拟)将足量AgCl(s)溶解在水中,形成悬浊液。已知:AgCl(s)Ag
+(aq)+Cl-(aq) ΔH>0,下列叙述错误的是( )
A.加热悬浊液,使其温度升高,则K (AgCl)增大
sp
B.加少量水稀释,上述平衡正向移动,c(Ag+)不变
C.向悬浊液中通入少量氨气,Q(AgCl)K 。
sp
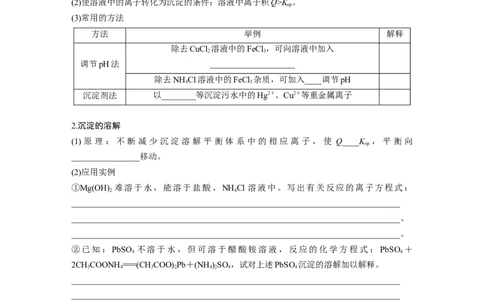
(3)常用的方法
方法 举例 解释
除去CuCl 溶液中的FeCl ,可向溶液中加入
2 3
调节pH法 ____________________
除去NH Cl溶液中的FeCl 杂质,可加入____调节pH
4 3
沉淀剂法 以________等沉淀污水中的Hg2+、Cu2+等重金属离子
2.沉淀的溶解
(1)原理:不断减少沉淀溶解平衡体系中的相应离子,使 Q____K ,平衡向
sp
________________移动。
(2)应用实例
①Mg(OH) 难溶于水,能溶于盐酸、NH Cl 溶液中。写出有关反应的离子方程式:
2 4
_____________________________________________________________________________
_____________________________________________________________________________、
_____________________________________________________________________________。
②已知:PbSO 不溶于水,但可溶于醋酸铵溶液,反应的化学方程式:PbSO +
4 4
2CHCOONH===(CHCOO) Pb+(NH )SO ,试对上述PbSO 沉淀的溶解加以解释。
3 4 3 2 4 2 4 4
_____________________________________________________________________________
_____________________________________________________________________________
特别提醒 利用氧化还原反应、形成配合物也可以降低难溶电解质沉淀溶解平衡中的某种离
子,使难溶电解质向溶解的方向移动。
3.沉淀的转化
(1)原理:由一种沉淀转化为另一种沉淀的过程,实质是____________________。
(2)沉淀转化规律
①一般来说,溶解度小的沉淀转化为溶解度更小的沉淀容易实现。
如,AgNO 溶液――→________――→AgI,K (AgCl)____K (AgI)。
3 sp sp
②一定条件下溶解度小的沉淀也可以转化成溶解度相对较大的沉淀。重晶石[BaSO(s)]―――――――→BaCO (s),但K (BaSO)____K (BaCO)。
4 3 sp 4 sp 3
(3)实际应用
① 锅 炉 除 垢 : 水 垢 中 的 CaSO(s)― ― ― ― ―Ca→CO (s)― ― →Ca2 + (aq) 。 离 子 方 程 式 为
4 3
______________________________________________________________________________
______________________________________________________________________________。
②矿物转化:原生铜的硫化物――――→CuSO 溶液――――――――→铜蓝(CuS)。
4
ZnS转化为CuS的离子方程式为__________________________________________________
______________________________________________________________________________。
PbS转化为CuS的离子方程式为__________________________________________________
______________________________________________________________________________。
一、实验探究沉淀的生成、溶解与转化
1.(2023·天津模拟)取1 mL 0.1 mol·L-1 AgNO 溶液进行如下实验(实验中所用试剂浓度均为
3
0.1 mol·L-1),下列说法不正确的是( )
A.实验①白色沉淀是难溶的AgCl
B.若按②①顺序实验,能看到白色沉淀
C.若按①③顺序实验,能看到黑色沉淀
D.由实验②说明AgI比AgCl更难溶
2.某同学设计实验探究影响沉淀溶解平衡的因素,有关实验操作如下:
ⅰ.取规格相同的两支试管①和②,先向试管①中加入少量PbI 黄色固体,并插入电导率测
2
试仪,然后分别加入等体积PbI 饱和溶液;
2
ⅱ.向试管①和②中分别滴入1滴0.1 mol·L-1 KI溶液,观察沉淀变化情况,一段时间后向①
中滴入少量蒸馏水,测得溶液电导率变化如图2所示。下列说法错误的是( )
A.滴加KI溶液①②中产生PbI 固体
2
B.b到c过程中①中固体质量减小
C.c点时溶液中c(Pb2+):①=②
D.b点:c(Pb2+)·c2(I-)”或“<”)K (Ag S)。
sp sp 2
3.[2022·重庆,15(2)]25 ℃时相关的溶度积见表。
化学式 Fe(OH) Cu(OH)
3 2
溶度积 4×10-38 2.5×10-20
①在某滤液中Fe3+和Cu2+的浓度相近,加入NaOH溶液,先得到的沉淀是__________。
②25 ℃时,为了使Cu2+沉淀完全,需调节溶液H+浓度不大于__________ mol·L-1。
4.[2022·全国乙卷,26(1)(2)]废旧铅蓄电池的铅膏中主要含有PbSO 、PbO 、PbO和Pb,还
4 2
有少量Ba、Fe、Al的盐或氧化物等,为了保护环境、充分利用铅资源,通过下图流程实现
铅的回收。
一些难溶电解质的溶度积常数如下表:
难溶电解质 PbSO PbCO BaSO BaCO
4 3 4 3
K 2.5×10-8 7.4×10-14 1.1×10-10 2.6×10-9
sp
(1)在“脱硫”中PbSO 转化反应的离子方程式为___________________________________,
4
用沉淀溶解平衡原理解释选择NaCO 的原因:_____________________________________
2 3
______________________________________________________________________________。
(2)在“脱硫”中,加入NaCO 不能使铅膏中BaSO 完全转化,原因是________________
2 3 4
______________________________________________________________________________。