文档内容
第 40 讲 原电池 常见化学电源
[复习目标] 1.理解原电池的工作原理。2.了解常见化学电源的种类及其工作原理。3.能够书
写常见化学电源的电极反应式和总反应方程式。
考点一 原电池的工作原理
1.概念
原电池是把________能转化为____能的装置。
2.构成条件
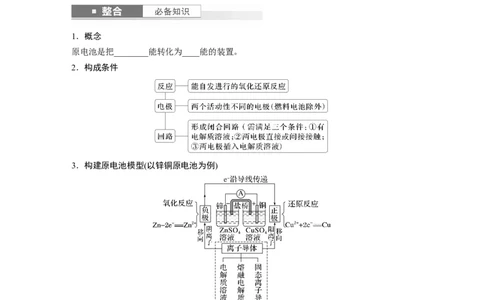
3.构建原电池模型(以锌铜原电池为例)
盐桥的组成和作用
(1)盐桥中装有含KCl饱和溶液的琼脂,离子可在其中自由移动。
(2)盐桥的作用:a.连接内电路,__________________________________________________;
b.____________,使原电池不断产生电流。
(3)盐桥中离子移向:阴离子移向______,阳离子移向______。1.盐桥是所有原电池构成的必要条件( )
2.原电池内部电解质中的阴离子一定移向负极,阳离子一定移向正极( )
3.构成原电池两极的电极材料一定是活泼性不同的金属( )
4.原电池中负极失去电子的总数一定等于正极得到电子的总数( )
5.使用盐桥可以提高电池的效率( )
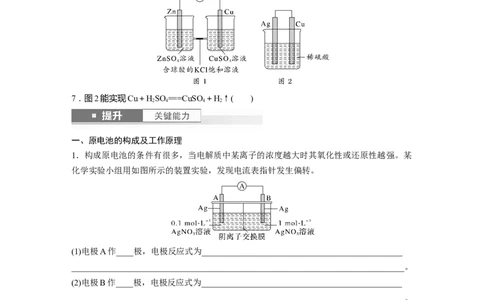
6.图1能验证锌与硫酸铜反应过程中有电子转移( )
7.图2能实现Cu+HSO ===CuSO +H↑( )
2 4 4 2
一、原电池的构成及工作原理
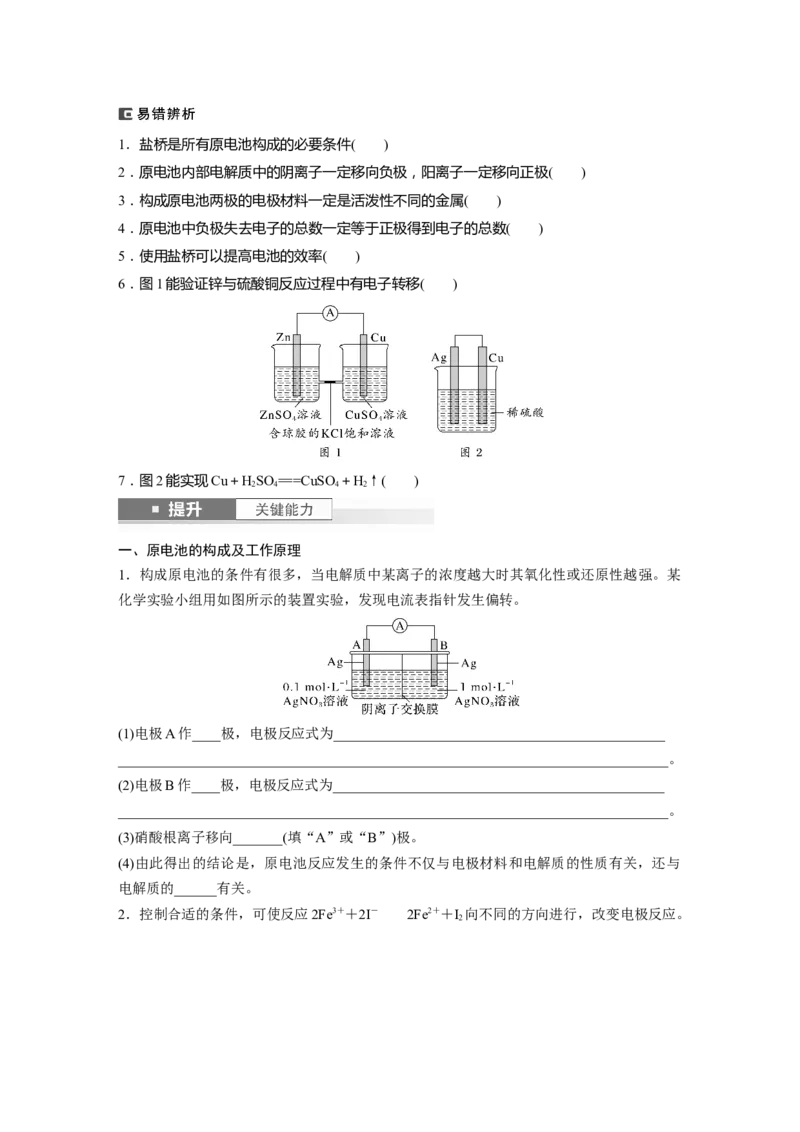
1.构成原电池的条件有很多,当电解质中某离子的浓度越大时其氧化性或还原性越强。某
化学实验小组用如图所示的装置实验,发现电流表指针发生偏转。
(1)电极A作____极,电极反应式为_______________________________________________
______________________________________________________________________________。
(2)电极B作____极,电极反应式为_______________________________________________
______________________________________________________________________________。
(3)硝酸根离子移向_______(填“A”或“B”)极。
(4)由此得出的结论是,原电池反应发生的条件不仅与电极材料和电解质的性质有关,还与
电解质的______有关。
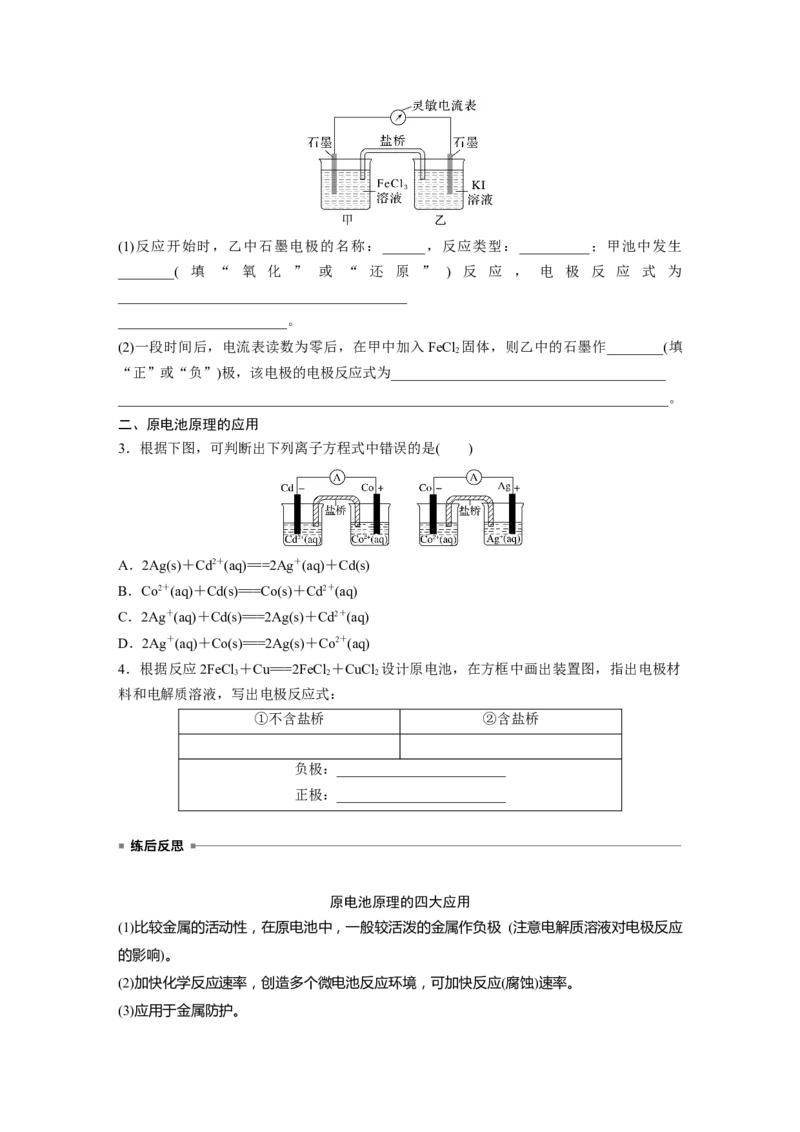
2.控制合适的条件,可使反应2Fe3++2I-2Fe2++I 向不同的方向进行,改变电极反应。
2(1)反应开始时,乙中石墨电极的名称:______,反应类型:__________;甲池中发生
________( 填 “ 氧 化 ” 或 “ 还 原 ” ) 反 应 , 电 极 反 应 式 为
_________________________________________
________________________。
(2)一段时间后,电流表读数为零后,在甲中加入FeCl 固体,则乙中的石墨作________(填
2
“正”或“负”)极,该电极的电极反应式为_______________________________________
______________________________________________________________________________。
二、原电池原理的应用
3.根据下图,可判断出下列离子方程式中错误的是( )
A.2Ag(s)+Cd2+(aq)===2Ag+(aq)+Cd(s)
B.Co2+(aq)+Cd(s)===Co(s)+Cd2+(aq)
C.2Ag+(aq)+Cd(s)===2Ag(s)+Cd2+(aq)
D.2Ag+(aq)+Co(s)===2Ag(s)+Co2+(aq)
4.根据反应2FeCl +Cu===2FeCl +CuCl 设计原电池,在方框中画出装置图,指出电极材
3 2 2
料和电解质溶液,写出电极反应式:
①不含盐桥 ②含盐桥
负极:________________________
正极:________________________
原电池原理的四大应用
(1)比较金属的活动性,在原电池中,一般较活泼的金属作负极 (注意电解质溶液对电极反应
的影响)。
(2)加快化学反应速率,创造多个微电池反应环境,可加快反应(腐蚀)速率。
(3)应用于金属防护。(4)设计原电池。
①首先将氧化还原反应分成两个半反应。
②根据原电池反应的特点,结合两个半反应找出正、负极材料和电解质溶液。
考点二 常见化学电源
1.一次电池
负极反应式:
_______________________________________;
正极反应式:
______________________________________;
总反应:Zn+2MnO +2HO===2MnO(OH)+Zn(OH)
2 2 2
负极反应式:
_______________________________________;
正极反应式:
______________________________________;
总反应:Zn+Ag O===ZnO+2Ag
2
2.二次电池
铅酸蓄电池是最常见的二次电池,总反应:Pb+PbO +2HSO 2PbSO +2HO。
2 2 4 4 2
(1)放电时:
负极反应式:____________________________________________________________;
正极反应式:____________________________________________________________。
放电时,当外电路上有2 mol e-通过时,溶液中消耗HSO ____ mol。
2 4
(2)充电时:
阴极反应式:____________________________________________________________;
阳极反应式:____________________________________________________________。
充电一段时间电解质溶液的pH__________(填“增大”“减小”或“不变”)。
提醒 充电时电极的连接,负接负作阴极,正接正作阳极。
3.燃料电池(1)氢氧燃料电池是目前最成熟的燃料电池,常见的燃料除 H 外,还有CO、水煤气(CO和
2
H)、烃类(如CH)、醇类(如CHOH)、醚类(如CHOCH )、氨(NH )、肼(H N—NH)等。如
2 4 3 3 3 3 2 2
无特别提示,燃料电池反应原理类似于燃料的燃烧。
(2)燃料电池的电解质常有四种类型:酸性条件、碱性条件、固体电解质(可传导O2-)、熔融
碳酸盐,不同电解质会对总反应式、电极反应式有影响。
(3)以甲醇为燃料,写出下列介质中的电极反应式。
①酸性溶液(或含质子交换膜)
正极:________________________________________________________________________,
负极:________________________________________________________________________。
②碱性溶液
正极:________________________________________________________________________,
负极:________________________________________________________________________。
③固体氧化物(其中O2-可以在固体介质中自由移动)
正极:________________________________________________________________________,
负极:________________________________________________________________________。
④熔融碳酸盐(CO)
正极(通入CO):______________________________________________________________,
2
负极:________________________________________________________________________。
1.干电池根据电池内的电解质分为酸性电池和碱性电池( )
2.手机、电脑中使用的锂离子电池属于一次电池( )
3.镍镉电池不能随意丢弃的主要原因是镍、镉的资源有限,价格昂贵( )
4.铅酸蓄电池放电时,正极与负极质量均增加( )
5.二次电池充电时,阴极连接电源的负极,发生还原反应( )
6.铅酸蓄电池放电时的负极和充电时的阳极均发生还原反应( )
7.燃料电池工作时燃料在电池中燃烧,然后热能转化为电能( )
8.在原电池中,正极本身一定不参与电极反应,负极本身一定发生氧化反应( )
一、多样化的燃料电池
1.燃料电池是燃料(如CO、H 、CH 、C H 等)与氧气(或空气)反应将化学能转变为电能的
2 4 2 6
装置,若电解质溶液是强碱溶液,下列关于乙烷(C H)燃料电池的说法正确的是( )
2 6
A.通入5.6 L O 完全反应后,有1 mol电子发生转移
2
B.负极反应式:C H+18OH-+14e-===2CO+12HO
2 6 2
C.该电池工作时,正极附近溶液的碱性增强
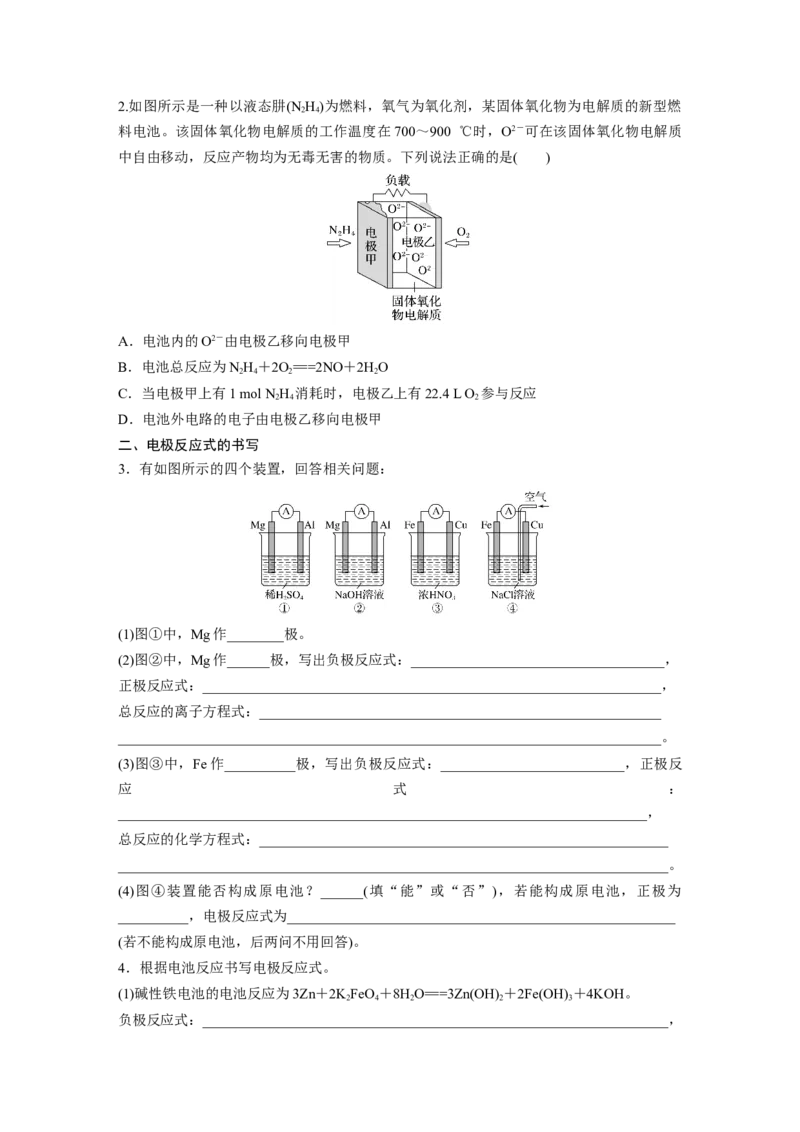
D.燃料电池的优点之一是燃料反应时化学能全部转化为电能2.如图所示是一种以液态肼(N H)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃
2 4
料电池。该固体氧化物电解质的工作温度在700~900 ℃时,O2-可在该固体氧化物电解质
中自由移动,反应产物均为无毒无害的物质。下列说法正确的是( )
A.电池内的O2-由电极乙移向电极甲
B.电池总反应为NH+2O===2NO+2HO
2 4 2 2
C.当电极甲上有1 mol N H 消耗时,电极乙上有22.4 L O 参与反应
2 4 2
D.电池外电路的电子由电极乙移向电极甲
二、电极反应式的书写
3.有如图所示的四个装置,回答相关问题:
(1)图①中,Mg作________极。
(2)图②中,Mg作______极,写出负极反应式:____________________________________,
正极反应式:_________________________________________________________________,
总反应的离子方程式:_________________________________________________________
_____________________________________________________________________________。
(3)图③中,Fe作__________极,写出负极反应式:__________________________,正极反
应 式 :
___________________________________________________________________________,
总反应的化学方程式:__________________________________________________________
______________________________________________________________________________。
(4)图④装置能否构成原电池?______(填“能”或“否”),若能构成原电池,正极为
__________,电极反应式为_______________________________________________________
(若不能构成原电池,后两问不用回答)。
4.根据电池反应书写电极反应式。
(1)碱性铁电池的电池反应为3Zn+2KFeO+8HO===3Zn(OH) +2Fe(OH) +4KOH。
2 4 2 2 3
负极反应式:__________________________________________________________________,正极反应式:__________________________________________________________________。
(2)一种锂电池的反应为CoO+LiC ===LiCoO +C ,Li原子嵌入电池负极材料碳(C )中。
2 6 2 6 6
负极反应式:__________________________________________________________________,
正极反应式:__________________________________________________________________。
(3)Mg-AgCl 电池是一种能被海水激活的一次性贮备电池,电池反应方程式:2AgCl+
Mg===Mg2++2Ag+2Cl-。
负极反应式:__________________________________________________________________,
正极反应式:__________________________________________________________________。
(1)电极反应式书写的一般方法
(2)已知总反应式的复杂电极反应式的书写方法
①首先写出较简单的电极反应式。
②复杂电极反应式=总反应式-简单电极反应式。
③注意电子守恒。
1.(2023·海南,8)利用金属Al、海水及其中的溶解氧可组成电池,如图所示。下列说法正确
的是( )
A.b电极为电池正极
B.电池工作时,海水中的Na+向a电极移动
C.电池工作时,紧邻a电极区域的海水呈强碱性
D.每消耗1 kg Al,电池最多向外提供37 mol电子的电量
2.(2023·广东,6)负载有Pt和Ag的活性炭,可选择性去除Cl-实现废酸的纯化,其工作原理
如图。下列说法正确的是( )A.Ag作原电池正极
B.电子由Ag经活性炭流向Pt
C.Pt表面发生的电极反应:O+2HO+4e-===4OH-
2 2
D.每消耗标准状况下11.2 L的O,最多去除1 mol Cl-
2
3.(2021·重庆,12)CO 电化学传感器是将环境中CO 浓度转变为电信号的装置,工作原理
2 2
如图所示,其中YSZ是固体电解质,当传感器在一定温度下工作时,在熔融 LiCO 和YSZ
2 3
之间的界面X会生成固体LiO。下列说法错误的是( )
2
A.CO迁移方向为界面X―→电极b
B.电极a上消耗的O 和电极b上产生的CO 的物质的量之比为1∶1
2 2
C.电极b为负极,发生的电极反应为2CO-4e-===O↑+2CO↑
2 2
D.电池总反应为LiCO===LiO+CO↑
2 3 2 2
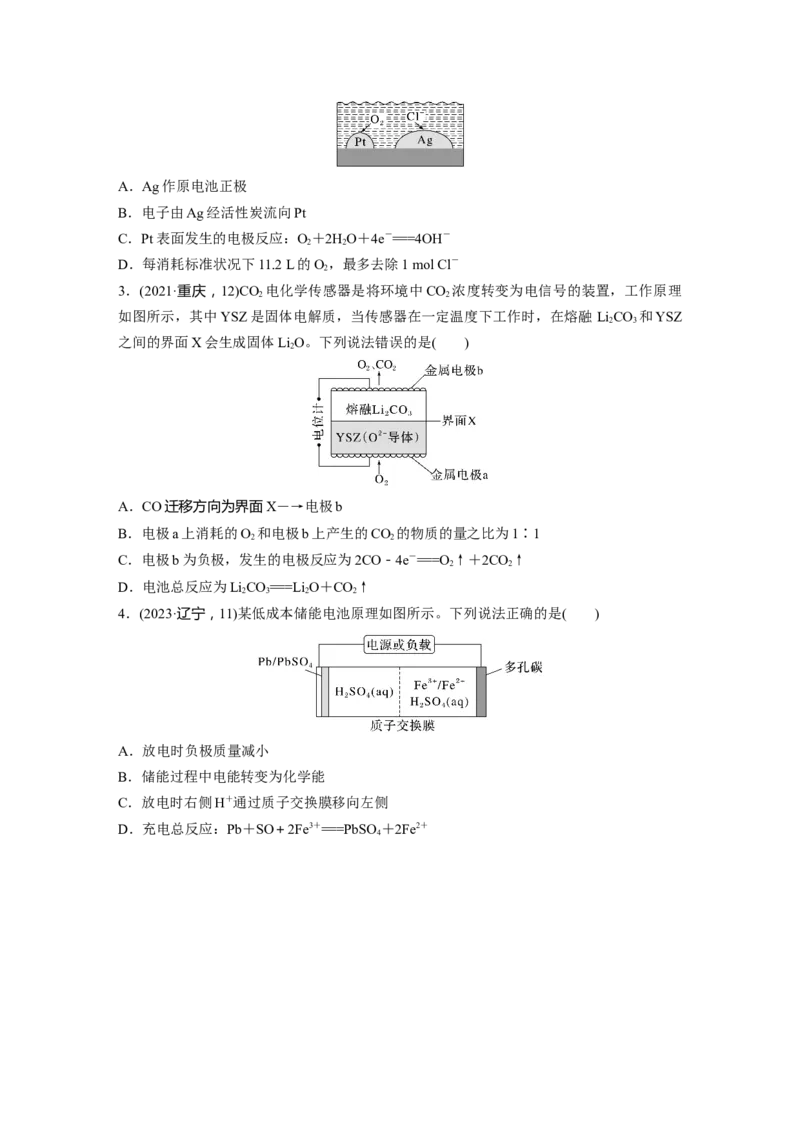
4.(2023·辽宁,11)某低成本储能电池原理如图所示。下列说法正确的是( )
A.放电时负极质量减小
B.储能过程中电能转变为化学能
C.放电时右侧H+通过质子交换膜移向左侧
D.充电总反应:Pb+SO+2Fe3+===PbSO +2Fe2+
4