文档内容
第 41 讲 新型化学电源分类突破
[复习目标] 1.熟悉常考新型化学电源的类型及考查方式。2.会分析新型化学电源的工作原
理,能正确书写新型化学电源的电极反应式。
类型一 固体电解质电池
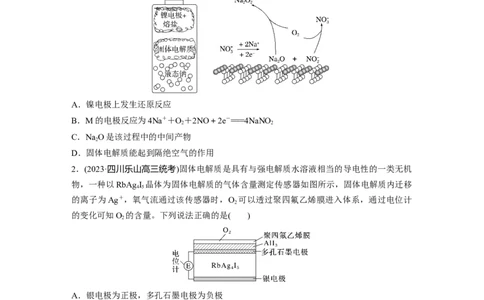
1.以硝酸盐为离子导体的Na-O 电池装置与其某一电极M附近的反应机理如图所示。下列
2
说法错误的是( )
A.镍电极上发生还原反应
B.M的电极反应为4Na++O+2NO+2e-===4NaNO
2 2
C.NaO是该过程中的中间产物
2
D.固体电解质能起到隔绝空气的作用
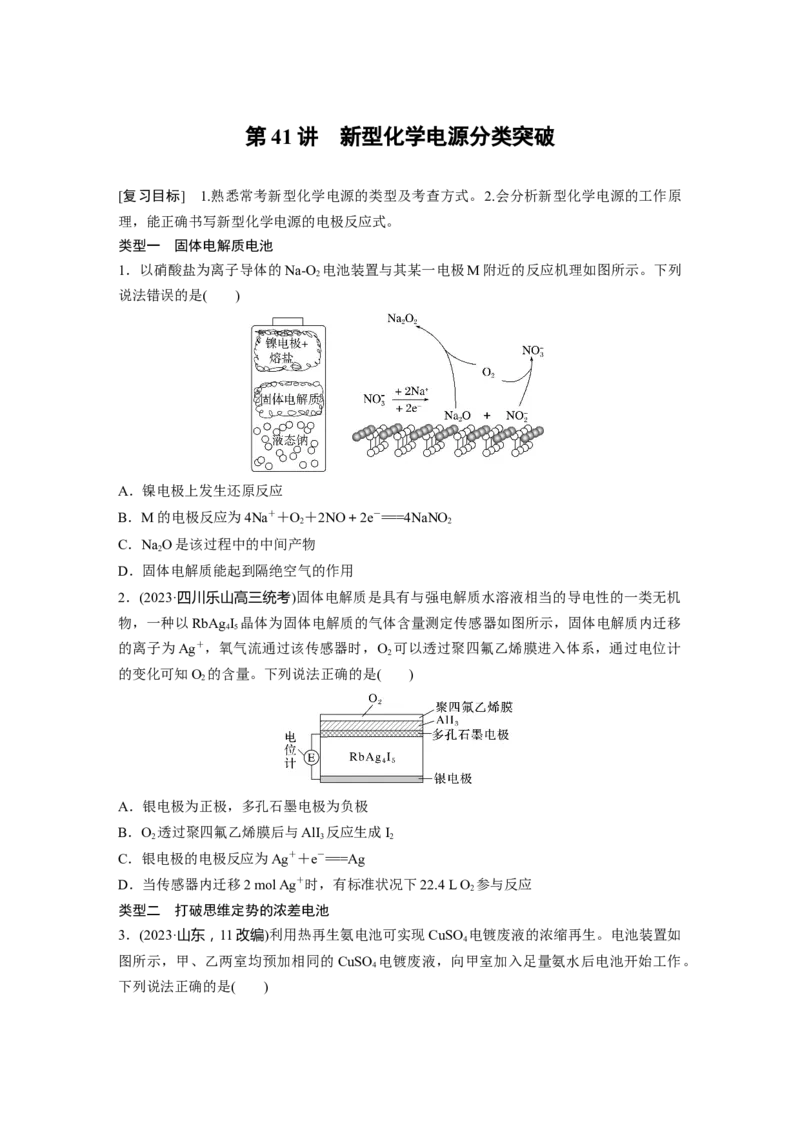
2.(2023·四川乐山高三统考)固体电解质是具有与强电解质水溶液相当的导电性的一类无机
物,一种以RbAg I 晶体为固体电解质的气体含量测定传感器如图所示,固体电解质内迁移
4 5
的离子为Ag+,氧气流通过该传感器时,O 可以透过聚四氟乙烯膜进入体系,通过电位计
2
的变化可知O 的含量。下列说法正确的是( )
2
A.银电极为正极,多孔石墨电极为负极
B.O 透过聚四氟乙烯膜后与AlI 反应生成I
2 3 2
C.银电极的电极反应为Ag++e-===Ag
D.当传感器内迁移2 mol Ag+时,有标准状况下22.4 L O 参与反应
2
类型二 打破思维定势的浓差电池
3.(2023·山东,11改编)利用热再生氨电池可实现CuSO 电镀废液的浓缩再生。电池装置如
4
图所示,甲、乙两室均预加相同的CuSO 电镀废液,向甲室加入足量氨水后电池开始工作。
4
下列说法正确的是( )A.甲室Cu电极为正极
B.隔膜为阳离子膜
C.电池总反应:Cu2++4NH ===[Cu(NH )]2+
3 3 4
D.NH 扩散到乙室不会对电池电动势产生影响
3
4.(2022·浙江1月选考,21)pH计是一种采用原电池原理测量溶液pH的仪器。如图所示,
以玻璃电极(在特制玻璃薄膜球内放置已知浓度的 HCl溶液,并插入Ag-AgCl电极)和另一
Ag-AgCl电极插入待测溶液中组成电池,pH与电池的电动势E存在关系:pH=。下列说法
正确的是( )
A.如果玻璃薄膜球内电极的电势低,则该电极反应式为:AgCl(s)+e-===Ag(s)+Cl-(0.1
mol·L-1)
B.玻璃膜内外氢离子浓度的差异不会引起电动势的变化
C.分别测定含已知pH的标准溶液和未知溶液的电池的电动势,可得出未知溶液的pH
D.pH计工作时,电能转化为化学能
(1)浓差电池是仅由一种物质由高浓度向低浓度扩散而引发的一类电池。电池内部,当某种
电解质离子或分子浓度越大时,其氧化性或还原性越强。
(2)“浓差电池”的分析方法
浓差电池是利用物质的浓度差产生电势的一种装置。两侧半电池中的特定物质有浓度差,离
子均是由“高浓度”移向“低浓度”,依据阳离子移向正极区域、阴离子移向负极区域判断
电池的正、负极,这是解题的关键。
类型三 基于废物利用的微生物燃料电池
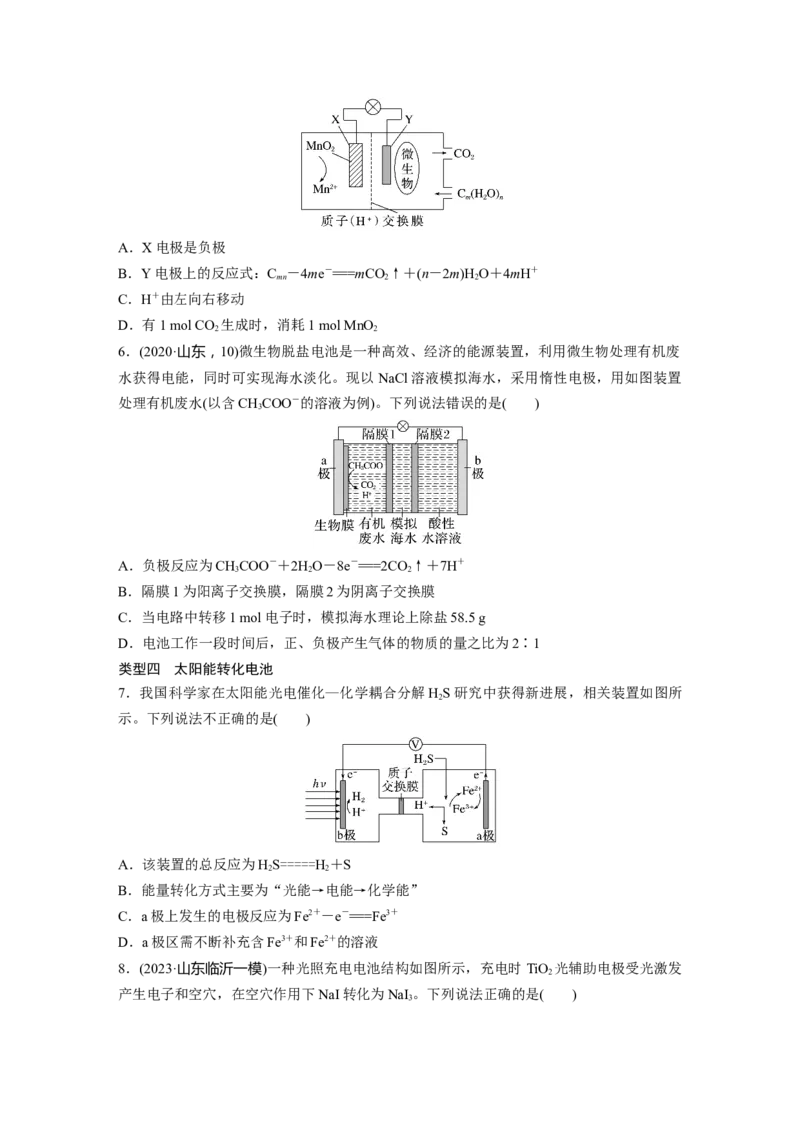
5.利用某新型微生物电池可消除水中碳水化合物的污染,其工作原理如图所示,下列有关
说法正确的是( )A.X电极是负极
B.Y电极上的反应式:C -4me-===mCO↑+(n-2m)H O+4mH+
mn 2 2
C.H+由左向右移动
D.有1 mol CO 生成时,消耗1 mol MnO
2 2
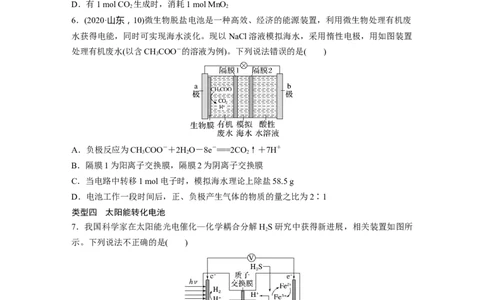
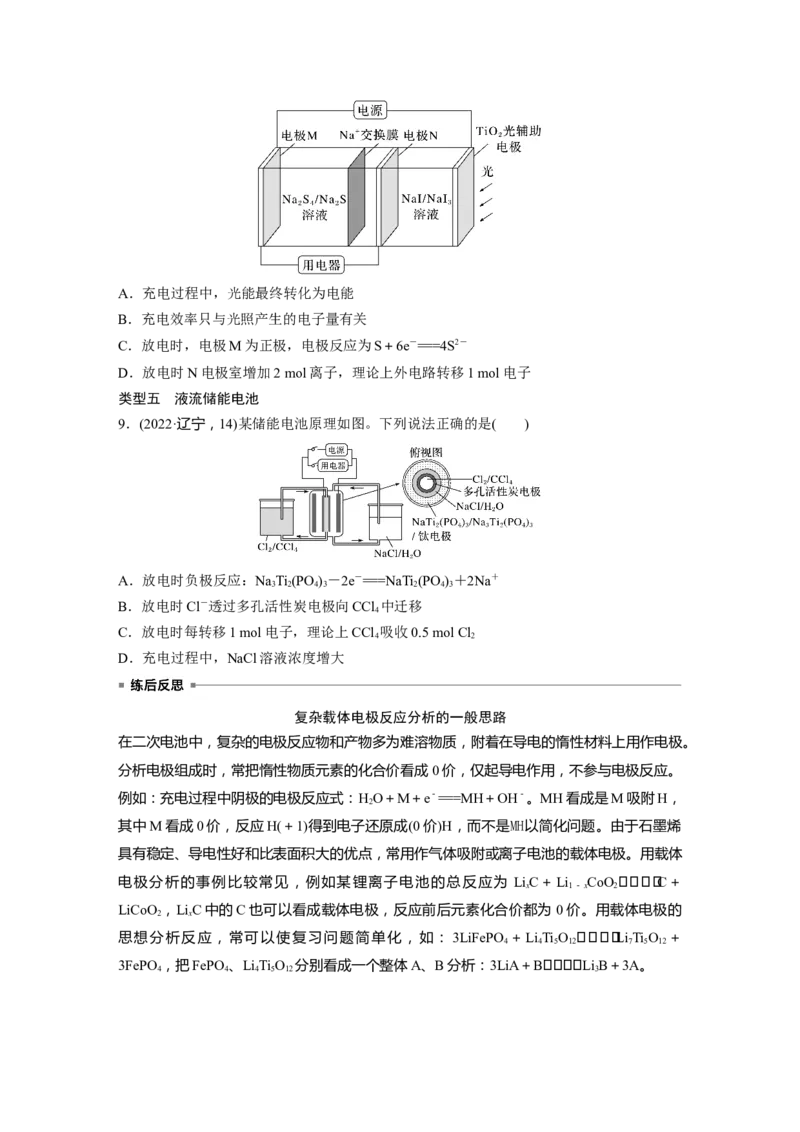
6.(2020·山东,10)微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废
水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用如图装置
处理有机废水(以含CHCOO-的溶液为例)。下列说法错误的是( )
3
A.负极反应为CHCOO-+2HO-8e-===2CO↑+7H+
3 2 2
B.隔膜1为阳离子交换膜,隔膜2为阴离子交换膜
C.当电路中转移1 mol电子时,模拟海水理论上除盐58.5 g
D.电池工作一段时间后,正、负极产生气体的物质的量之比为2∶1
类型四 太阳能转化电池
7.我国科学家在太阳能光电催化—化学耦合分解HS研究中获得新进展,相关装置如图所
2
示。下列说法不正确的是( )
A.该装置的总反应为HS=====H+S
2 2
B.能量转化方式主要为“光能→电能→化学能”
C.a极上发生的电极反应为Fe2+-e-===Fe3+
D.a极区需不断补充含Fe3+和Fe2+的溶液
8.(2023·山东临沂一模)一种光照充电电池结构如图所示,充电时TiO 光辅助电极受光激发
2
产生电子和空穴,在空穴作用下NaI转化为NaI 。下列说法正确的是( )
3A.充电过程中,光能最终转化为电能
B.充电效率只与光照产生的电子量有关
C.放电时,电极M为正极,电极反应为S+6e-===4S2-
D.放电时N电极室增加2 mol离子,理论上外电路转移1 mol电子
类型五 液流储能电池
9.(2022·辽宁,14)某储能电池原理如图。下列说法正确的是( )
A.放电时负极反应:NaTi (PO )-2e-===NaTi (PO )+2Na+
3 2 4 3 2 4 3
B.放电时Cl-透过多孔活性炭电极向CCl 中迁移
4
C.放电时每转移1 mol电子,理论上CCl 吸收0.5 mol Cl
4 2
D.充电过程中,NaCl溶液浓度增大
复杂载体电极反应分析的一般思路
在二次电池中,复杂的电极反应物和产物多为难溶物质,附着在导电的惰性材料上用作电极。
分析电极组成时,常把惰性物质元素的化合价看成0价,仅起导电作用,不参与电极反应。
例如:充电过程中阴极的电极反应式:HO+M+e-===MH+OH-。MH看成是M吸附H,
2
其中M看成0价,反应H(+1)得到电子还原成(0价)H,而不是MH以简化问题。由于石墨烯
具有稳定、导电性好和比表面积大的优点,常用作气体吸附或离子电池的载体电极。用载体
电极分析的事例比较常见,例如某锂离子电池的总反应为 LiC+Li CoOC+
x 1-x 2
LiCoO ,LiC中的C也可以看成载体电极,反应前后元素化合价都为 0价。用载体电极的
2 x
思想分析反应,常可以使复习问题简单化,如:3LiFePO +LiTi O LiTi O +
4 4 5 12 7 5 12
3FePO ,把FePO 、LiTi O 分别看成一个整体A、B分析:3LiA+BLiB+3A。
4 4 4 5 12 3