文档内容
第 41 讲 新型化学电源分类突破
[复习目标] 1.熟悉常考新型化学电源的类型及考查方式。2.会分析新型化学电源的工作原
理,能正确书写新型化学电源的电极反应式。
类型一 固体电解质电池
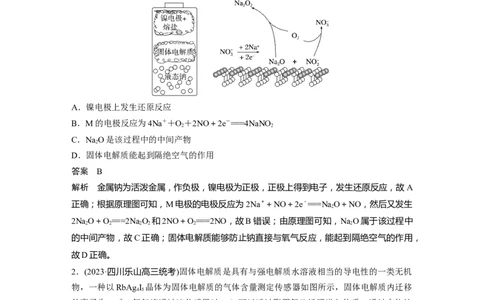
1.以硝酸盐为离子导体的Na-O 电池装置与其某一电极M附近的反应机理如图所示。下列
2
说法错误的是( )
A.镍电极上发生还原反应
B.M的电极反应为4Na++O+2NO+2e-===4NaNO
2 2
C.NaO是该过程中的中间产物
2
D.固体电解质能起到隔绝空气的作用
答案 B
解析 金属钠为活泼金属,作负极,镍电极为正极,正极上得到电子,发生还原反应,故A
正确;根据原理图可知,M电极的电极反应为2Na++NO+2e-===NaO+NO,然后又发生
2
2NaO+O===2NaO 和2NO+O===2NO,故B错误;由原理图可知,NaO属于该过程中
2 2 2 2 2 2
的中间产物,故C正确;固体电解质能够防止钠直接与氧气反应,能起到隔绝空气的作用,
故D正确。
2.(2023·四川乐山高三统考)固体电解质是具有与强电解质水溶液相当的导电性的一类无机
物,一种以RbAg I 晶体为固体电解质的气体含量测定传感器如图所示,固体电解质内迁移
4 5
的离子为Ag+,氧气流通过该传感器时,O 可以透过聚四氟乙烯膜进入体系,通过电位计
2
的变化可知O 的含量。下列说法正确的是( )
2
A.银电极为正极,多孔石墨电极为负极
B.O 透过聚四氟乙烯膜后与AlI 反应生成I
2 3 2C.银电极的电极反应为Ag++e-===Ag
D.当传感器内迁移2 mol Ag+时,有标准状况下22.4 L O 参与反应
2
答案 B
解析 传感器中发生反应4AlI +3O===2Al O +6I ,所以O 透过聚四氟乙烯膜后与AlI 反
3 2 2 3 2 2 3
应生成I ,故B正确;银电极的电极反应为Ag-e-===Ag+,故C错误;由关系式4Ag~
2
O,可知迁移2 mol Ag+时,有标准状况下11.2 L O 参与反应,故D错误。
2 2
类型二 打破思维定势的浓差电池
3.(2023·山东,11改编)利用热再生氨电池可实现CuSO 电镀废液的浓缩再生。电池装置如
4
图所示,甲、乙两室均预加相同的CuSO 电镀废液,向甲室加入足量氨水后电池开始工作。
4
下列说法正确的是( )
A.甲室Cu电极为正极
B.隔膜为阳离子膜
C.电池总反应:Cu2++4NH ===[Cu(NH )]2+
3 3 4
D.NH 扩散到乙室不会对电池电动势产生影响
3
答案 C
解析 向甲室加入足量氨水后电池开始工作,则甲室Cu电极溶解,变为铜离子与氨气形成
[Cu(NH )]2+,因此甲室Cu电极为负极,故A错误;原电池内电路中阳离子向正极移动,
3 4
若隔膜为阳离子膜,电极溶解生成的铜离子要向右侧移动,通入氨气要消耗铜离子,显然左
侧阳离子不断减小,明显不利于电池反应正向进行,故 B错误;负极反应是 Cu-2e-+
4NH ===[Cu(NH )]2+,正极反应是 Cu2++2e-===Cu,则电池总反应为 Cu2++
3 3 4
4NH ===[Cu(NH )]2+,故C正确;NH 扩散到乙室会与铜离子反应生成[Cu(NH )]2+,铜离
3 3 4 3 3 4
子浓度降低,铜离子得电子能力减弱,因此将对电池电动势产生影响,故D错误。
4.(2022·浙江1月选考,21)pH计是一种采用原电池原理测量溶液pH的仪器。如图所示,
以玻璃电极(在特制玻璃薄膜球内放置已知浓度的 HCl溶液,并插入Ag-AgCl电极)和另一
Ag-AgCl电极插入待测溶液中组成电池,pH与电池的电动势E存在关系:pH=。下列说法
正确的是( )A.如果玻璃薄膜球内电极的电势低,则该电极反应式为:AgCl(s)+e-===Ag(s)+Cl-(0.1
mol·L-1)
B.玻璃膜内外氢离子浓度的差异不会引起电动势的变化
C.分别测定含已知pH的标准溶液和未知溶液的电池的电动势,可得出未知溶液的pH
D.pH计工作时,电能转化为化学能
答案 C
解析 如果玻璃薄膜球内电极的电势低,则该电极为负极,负极发生氧化反应而不是还原反
应,A错误;pH与电池的电动势E存在关系:pH=,则玻璃膜内外氢离子浓度的差异会引
起电动势的变化,B错误;pH与电池的电动势E存在关系:pH=,则分别测定含已知pH
的标准溶液和未知溶液的电池的电动势,可得出未知溶液的 pH,C正确;pH计工作时,利
用原电池原理,则化学能转化为电能,D错误。
(1)浓差电池是仅由一种物质由高浓度向低浓度扩散而引发的一类电池。电池内部,当某种
电解质离子或分子浓度越大时,其氧化性或还原性越强。
(2)“浓差电池”的分析方法
浓差电池是利用物质的浓度差产生电势的一种装置。两侧半电池中的特定物质有浓度差,离
子均是由“高浓度”移向“低浓度”,依据阳离子移向正极区域、阴离子移向负极区域判断
电池的正、负极,这是解题的关键。
类型三 基于废物利用的微生物燃料电池
5.利用某新型微生物电池可消除水中碳水化合物的污染,其工作原理如图所示,下列有关
说法正确的是( )
A.X电极是负极
B.Y电极上的反应式:C -4me-===mCO↑+(n-2m)H O+4mH+
mn 2 2
C.H+由左向右移动D.有1 mol CO 生成时,消耗1 mol MnO
2 2
答案 B
解析 根据装置图,X电极上MnO 转化成Mn2+,化合价降低,发生还原反应,作正极,A
2
错误;Y电极为负极,C (H O) 中C的平均化合价由 0价升高为+4价,电极反应式为
m 2 n
C (H O) -4me-===mCO↑+(n-2m)H O+4mH+,B正确;根据原电池工作原理,阳离子
m 2 n 2 2
由负极向正极移动,即H+由右向左移动,C错误;正极反应式为MnO +2e-+4H+===Mn2
2
++2HO,建立关系式为2mMnO ~4me-~mCO,有1 mol CO 生成时,消耗2 mol MnO ,
2 2 2 2 2
D错误。
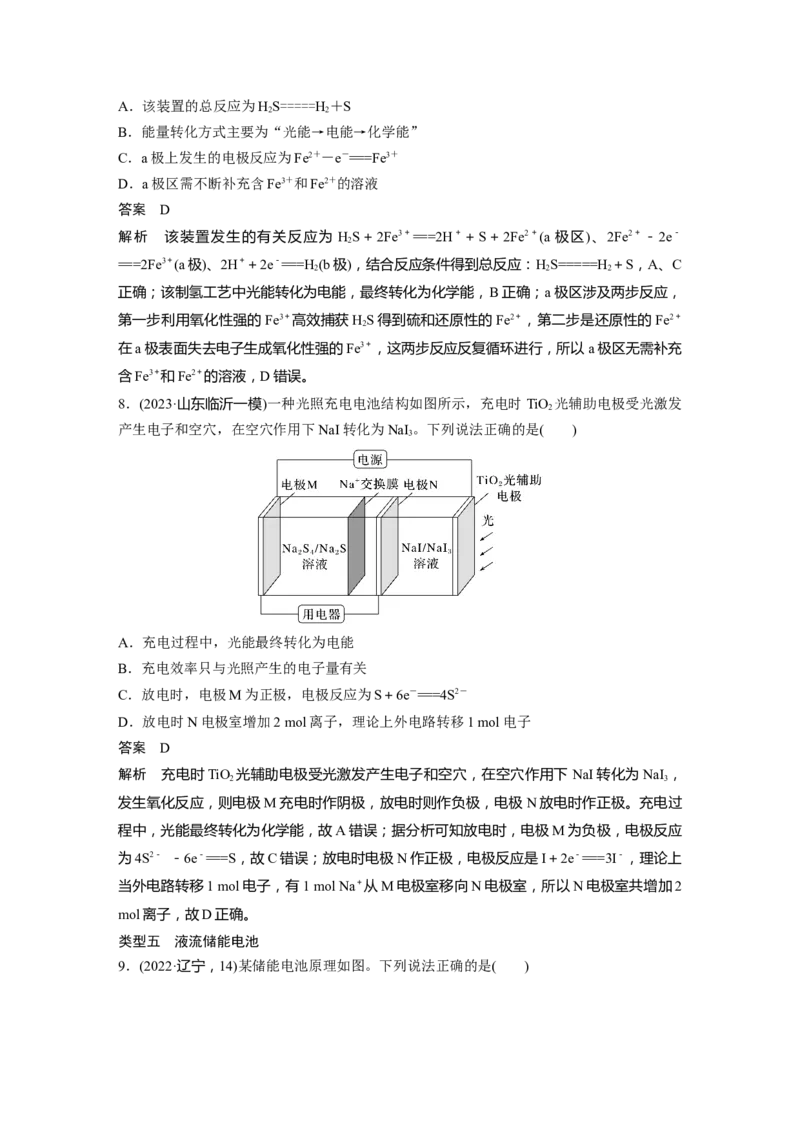
6.(2020·山东,10)微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废
水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用如图装置
处理有机废水(以含CHCOO-的溶液为例)。下列说法错误的是( )
3
A.负极反应为CHCOO-+2HO-8e-===2CO↑+7H+
3 2 2
B.隔膜1为阳离子交换膜,隔膜2为阴离子交换膜
C.当电路中转移1 mol电子时,模拟海水理论上除盐58.5 g
D.电池工作一段时间后,正、负极产生气体的物质的量之比为2∶1
答案 B
解析 由题图可知,a极为负极,b极为正极,则隔膜1为阴离子交换膜,隔膜2为阳离子
交换膜,才能使模拟海水中的氯离子移向负极,钠离子移向正极,达到海水淡化的目的,B
项错误;电路中有1 mol电子通过时,则电解质溶液中有1 mol钠离子移向正极,1 mol氯离
子移向负极,C项正确;负极反应:CHCOO-+2HO-8e-===2CO↑+7H+,正极反应:
3 2 2
2H++2e-===H↑,根据电荷守恒,正、负极产生气体的物质的量之比为2∶1,A、D项正
2
确。
类型四 太阳能转化电池
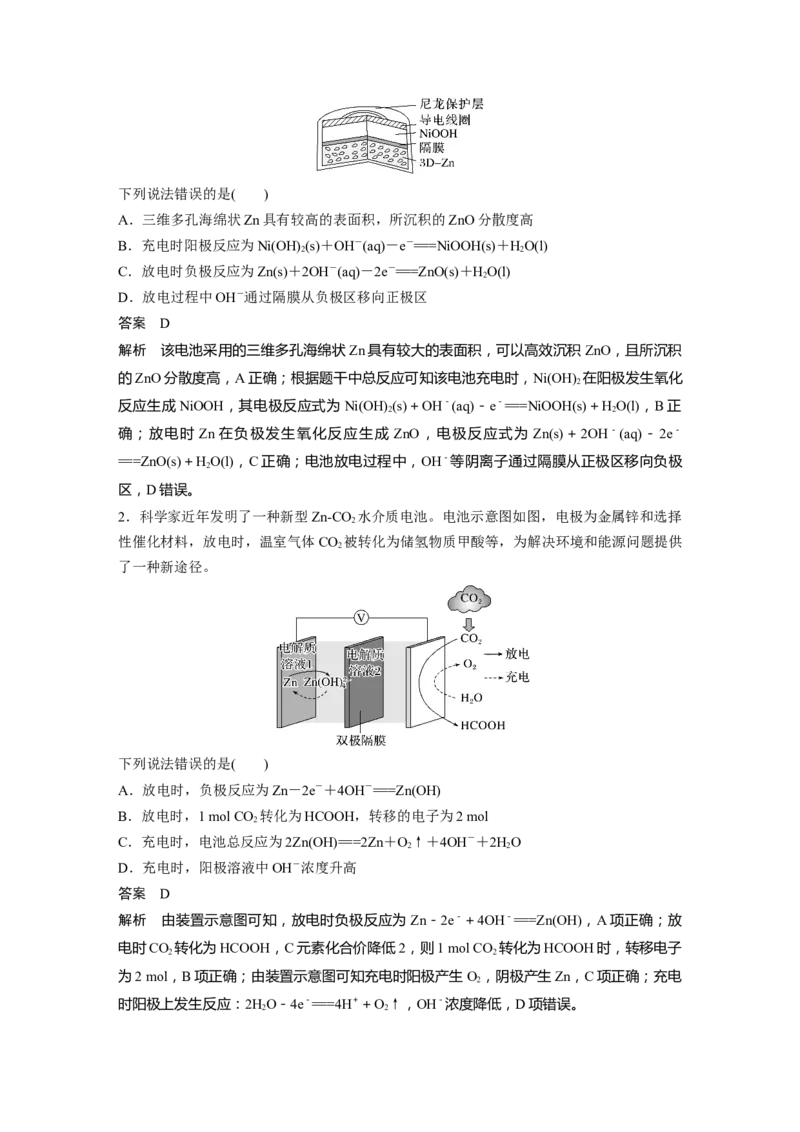
7.我国科学家在太阳能光电催化—化学耦合分解HS研究中获得新进展,相关装置如图所
2
示。下列说法不正确的是( )A.该装置的总反应为HS=====H+S
2 2
B.能量转化方式主要为“光能→电能→化学能”
C.a极上发生的电极反应为Fe2+-e-===Fe3+
D.a极区需不断补充含Fe3+和Fe2+的溶液
答案 D
解析 该装置发生的有关反应为 HS+2Fe3+===2H++S+2Fe2+(a 极区)、2Fe2+-2e-
2
===2Fe3+(a极)、2H++2e-===H(b极),结合反应条件得到总反应:HS=====H+S,A、C
2 2 2
正确;该制氢工艺中光能转化为电能,最终转化为化学能,B正确;a极区涉及两步反应,
第一步利用氧化性强的Fe3+高效捕获HS得到硫和还原性的Fe2+,第二步是还原性的Fe2+
2
在a极表面失去电子生成氧化性强的Fe3+,这两步反应反复循环进行,所以a极区无需补充
含Fe3+和Fe2+的溶液,D错误。
8.(2023·山东临沂一模)一种光照充电电池结构如图所示,充电时TiO 光辅助电极受光激发
2
产生电子和空穴,在空穴作用下NaI转化为NaI 。下列说法正确的是( )
3
A.充电过程中,光能最终转化为电能
B.充电效率只与光照产生的电子量有关
C.放电时,电极M为正极,电极反应为S+6e-===4S2-
D.放电时N电极室增加2 mol离子,理论上外电路转移1 mol电子
答案 D
解析 充电时TiO 光辅助电极受光激发产生电子和空穴,在空穴作用下 NaI转化为NaI ,
2 3
发生氧化反应,则电极M充电时作阴极,放电时则作负极,电极N放电时作正极。充电过
程中,光能最终转化为化学能,故A错误;据分析可知放电时,电极M为负极,电极反应
为4S2- -6e-===S,故C错误;放电时电极N作正极,电极反应是I+2e-===3I-,理论上
当外电路转移1 mol电子,有1 mol Na+从M电极室移向N电极室,所以N电极室共增加2
mol离子,故D正确。
类型五 液流储能电池
9.(2022·辽宁,14)某储能电池原理如图。下列说法正确的是( )A.放电时负极反应:NaTi (PO )-2e-===NaTi (PO )+2Na+
3 2 4 3 2 4 3
B.放电时Cl-透过多孔活性炭电极向CCl 中迁移
4
C.放电时每转移1 mol电子,理论上CCl 吸收0.5 mol Cl
4 2
D.充电过程中,NaCl溶液浓度增大
答案 A
解析 放电时负极失电子,发生氧化反应,电极反应:NaTi (PO ) -2e-===NaTi (PO ) +
3 2 4 3 2 4 3
2Na+,故A正确;放电时,阴离子移向负极,则放电时Cl-透过多孔活性炭电极向NaCl中
迁移,故B错误;正极电极反应:Cl +2e-===2Cl-,放电时每转移1 mol电子,理论上
2
CCl 释放0.5 mol Cl ,故C错误;充电过程中,阳极电极反应:2Cl--2e-===Cl ↑,消耗
4 2 2
氯离子,阴极消耗Na+,NaCl溶液浓度减小,故D错误。
复杂载体电极反应分析的一般思路
在二次电池中,复杂的电极反应物和产物多为难溶物质,附着在导电的惰性材料上用作电极。
分析电极组成时,常把惰性物质元素的化合价看成0价,仅起导电作用,不参与电极反应。
例如:充电过程中阴极的电极反应式:HO+M+e-===MH+OH-。MH看成是M吸附H,
2
其中M看成0价,反应H(+1)得到电子还原成(0价)H,而不是MH以简化问题。由于石墨烯
具有稳定、导电性好和比表面积大的优点,常用作气体吸附或离子电池的载体电极。用载体
电极分析的事例比较常见,例如某锂离子电池的总反应为 LiC+Li CoOC+
x 1-x 2
LiCoO ,LiC中的C也可以看成载体电极,反应前后元素化合价都为 0价。用载体电极的
2 x
思想分析反应,常可以使复习问题简单化,如:3LiFePO +LiTi O LiTi O +
4 4 5 12 7 5 12
3FePO ,把FePO 、LiTi O 分别看成一个整体A、B分析:3LiA+BLiB+3A。
4 4 4 5 12 3
课时精练
1.(2019·全国卷Ⅲ,13)为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状
Zn(3D-Zn)可以高效沉积ZnO的特点,设计了采用强碱性电解质的3D-Zn-NiOOH二次
电池,结构如图所示。电池反应为Zn(s)+2NiOOH(s)+HO(l)ZnO(s)+2Ni(OH) (s)。
2 2下列说法错误的是( )
A.三维多孔海绵状Zn具有较高的表面积,所沉积的ZnO分散度高
B.充电时阳极反应为Ni(OH) (s)+OH-(aq)-e-===NiOOH(s)+HO(l)
2 2
C.放电时负极反应为Zn(s)+2OH-(aq)-2e-===ZnO(s)+HO(l)
2
D.放电过程中OH-通过隔膜从负极区移向正极区
答案 D
解析 该电池采用的三维多孔海绵状Zn具有较大的表面积,可以高效沉积ZnO,且所沉积
的ZnO分散度高,A正确;根据题干中总反应可知该电池充电时,Ni(OH) 在阳极发生氧化
2
反应生成NiOOH,其电极反应式为Ni(OH) (s)+OH-(aq)-e-===NiOOH(s)+HO(l),B正
2 2
确;放电时 Zn 在负极发生氧化反应生成 ZnO,电极反应式为 Zn(s)+2OH-(aq)-2e-
===ZnO(s)+HO(l),C正确;电池放电过程中,OH-等阴离子通过隔膜从正极区移向负极
2
区,D错误。
2.科学家近年发明了一种新型Zn-CO 水介质电池。电池示意图如图,电极为金属锌和选择
2
性催化材料,放电时,温室气体CO 被转化为储氢物质甲酸等,为解决环境和能源问题提供
2
了一种新途径。
下列说法错误的是( )
A.放电时,负极反应为Zn-2e-+4OH-===Zn(OH)
B.放电时,1 mol CO 转化为HCOOH,转移的电子为2 mol
2
C.充电时,电池总反应为2Zn(OH)===2Zn+O↑+4OH-+2HO
2 2
D.充电时,阳极溶液中OH-浓度升高
答案 D
解析 由装置示意图可知,放电时负极反应为Zn-2e-+4OH-===Zn(OH),A项正确;放
电时CO 转化为HCOOH,C元素化合价降低2,则1 mol CO 转化为HCOOH时,转移电子
2 2
为2 mol,B项正确;由装置示意图可知充电时阳极产生O ,阴极产生Zn,C项正确;充电
2
时阳极上发生反应:2HO-4e-===4H++O↑,OH-浓度降低,D项错误。
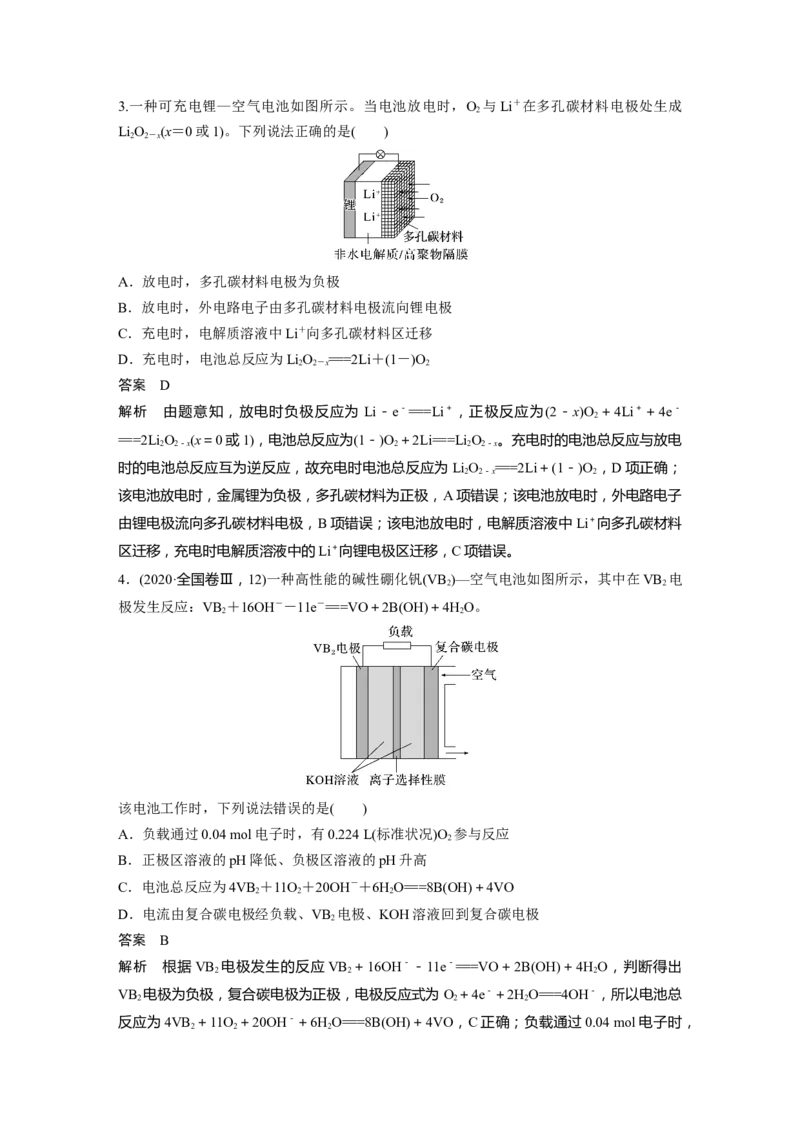
2 23.一种可充电锂—空气电池如图所示。当电池放电时,O 与Li+在多孔碳材料电极处生成
2
LiO (x=0或1)。下列说法正确的是( )
2 2-x
A.放电时,多孔碳材料电极为负极
B.放电时,外电路电子由多孔碳材料电极流向锂电极
C.充电时,电解质溶液中Li+向多孔碳材料区迁移
D.充电时,电池总反应为LiO ===2Li+(1-)O
2 2-x 2
答案 D
解析 由题意知,放电时负极反应为 Li-e-===Li+,正极反应为(2-x)O +4Li++4e-
2
===2LiO (x=0或1),电池总反应为(1-)O +2Li===LiO 。充电时的电池总反应与放电
2 2-x 2 2 2-x
时的电池总反应互为逆反应,故充电时电池总反应为LiO ===2Li+(1-)O ,D项正确;
2 2-x 2
该电池放电时,金属锂为负极,多孔碳材料为正极,A项错误;该电池放电时,外电路电子
由锂电极流向多孔碳材料电极,B项错误;该电池放电时,电解质溶液中Li+向多孔碳材料
区迁移,充电时电解质溶液中的Li+向锂电极区迁移,C项错误。
4.(2020·全国卷Ⅲ,12)一种高性能的碱性硼化钒(VB )—空气电池如图所示,其中在VB 电
2 2
极发生反应:VB +16OH--11e-===VO+2B(OH)+4HO。
2 2
该电池工作时,下列说法错误的是( )
A.负载通过0.04 mol电子时,有0.224 L(标准状况)O 参与反应
2
B.正极区溶液的pH降低、负极区溶液的pH升高
C.电池总反应为4VB +11O+20OH-+6HO===8B(OH)+4VO
2 2 2
D.电流由复合碳电极经负载、VB 电极、KOH溶液回到复合碳电极
2
答案 B
解析 根据VB 电极发生的反应VB +16OH--11e-===VO+2B(OH)+4HO,判断得出
2 2 2
VB 电极为负极,复合碳电极为正极,电极反应式为O+4e-+2HO===4OH-,所以电池总
2 2 2
反应为4VB +11O +20OH-+6HO===8B(OH)+4VO,C正确;负载通过0.04 mol电子时,
2 2 2有0.01 mol氧气参与反应,即标准状况下有0.224 L氧气参与反应,A正确;负极区消耗
OH-,溶液的pH降低,正极区生成OH-,溶液的pH升高,B错误。
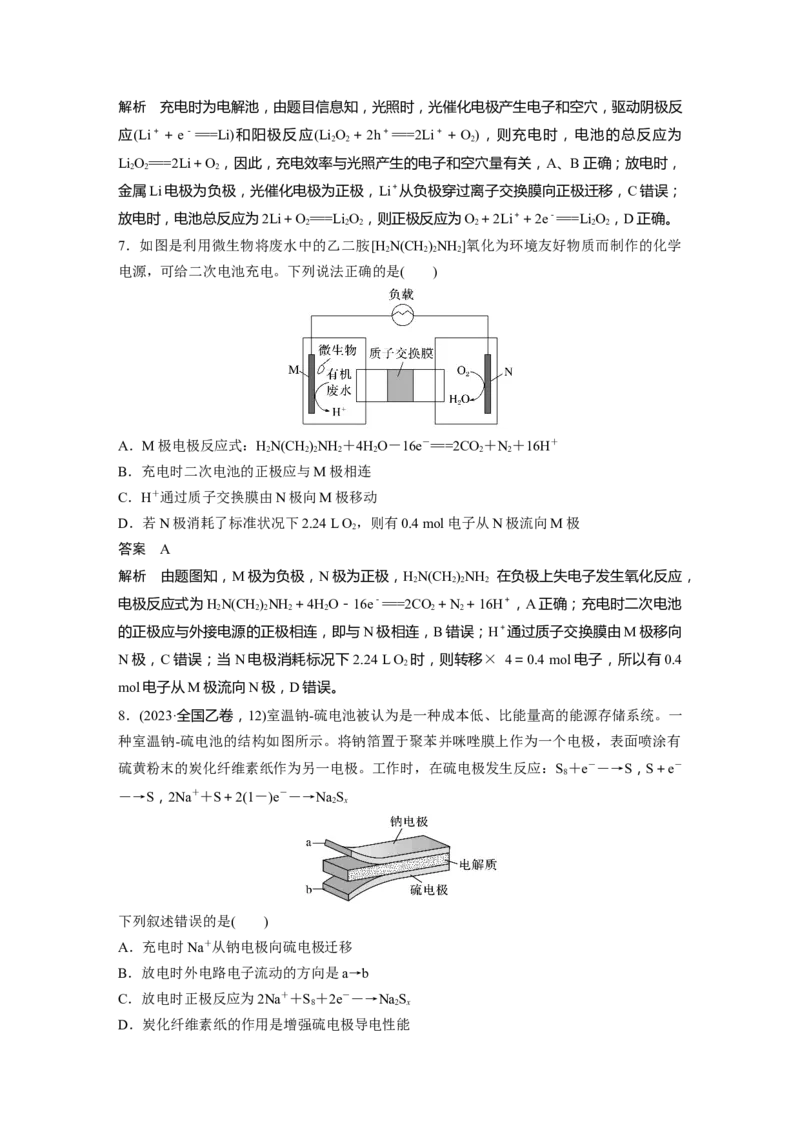
5.浓差电池是利用物质的浓度差产生电势的一种装置。将两个完全相同的电极浸入两个溶
质相同但浓度不同的电解质溶液中构成的浓差电池,称为双液浓差电池。模拟工业上电渗析
法实现海水(用氯化钠溶液代替)淡化的装置如图所示。下列说法错误的是( )
A.SO向Cu(1)极区域迁移
B.C(2)极发生还原反应
C.膜1为阳离子交换膜
D.C(2)极反应:2HO+2e-===2OH-+H↑
2 2
答案 C
解析 为使交换膜两侧硫酸铜溶液的浓度相等,即阴离子交换膜左侧溶液 c(CuSO )增大,
4
右侧溶液c(CuSO )减小,又因为只允许阴离子迁移,故交换膜左侧铜电极溶解,c(Cu2+)增
4
大;交换膜右侧铜电极上析出铜,c(Cu2+)减小,即Cu(1)极为负极,发生氧化反应:Cu-2e
-===Cu2+;Cu(2)极为正极,发生还原反应:Cu2++2e-===Cu,SO由阴离子交换膜右侧向
左侧迁移。
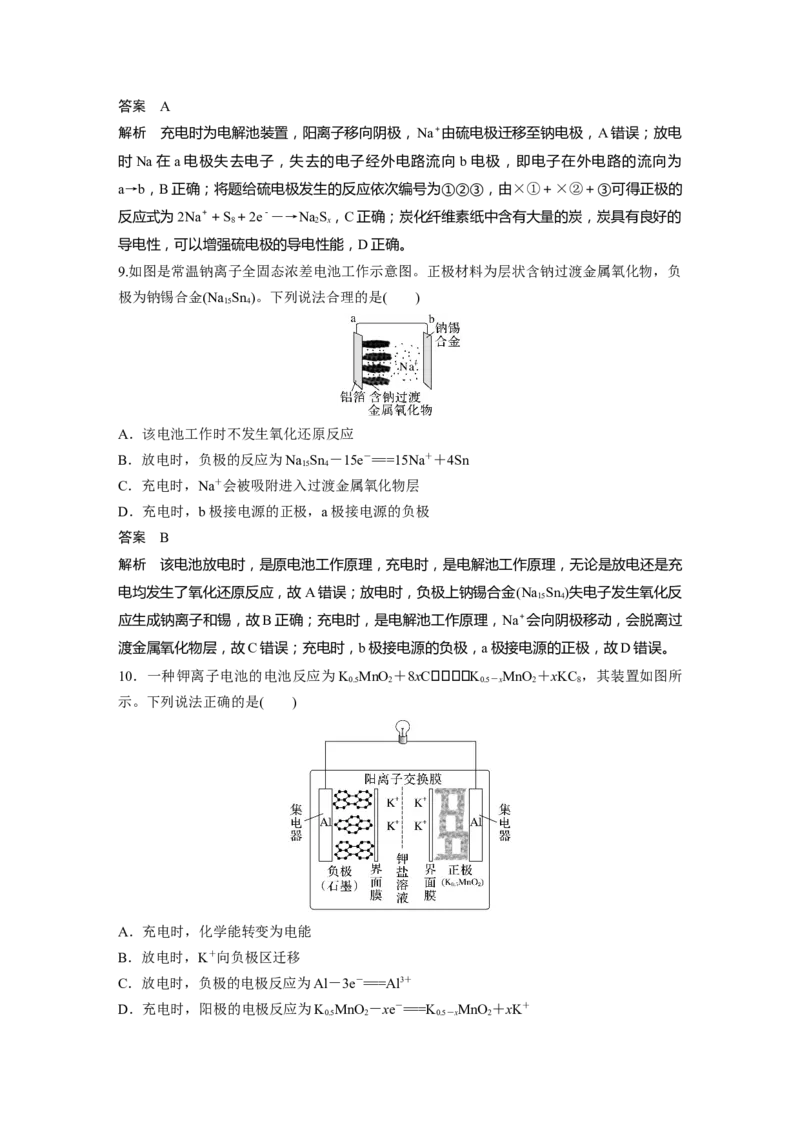
6.(2022·全国乙卷,12)Li-O 电池比能量高,在汽车、航天等领域具有良好的应用前景。近
2
年来,科学家研究了一种光照充电Li-O 电池(如图所示)。光照时,光催化电极产生电子(e-)
2
和空穴(h+),驱动阴极反应(Li++e-===Li)和阳极反应(Li O +2h+===2Li++O)对电池进行
2 2 2
充电。下列叙述错误的是( )
A.充电时,电池的总反应为LiO===2Li+O
2 2 2
B.充电效率与光照产生的电子和空穴量有关
C.放电时,Li+从正极穿过离子交换膜向负极迁移
D.放电时,正极发生反应:O+2Li++2e-===LiO
2 2 2
答案 C解析 充电时为电解池,由题目信息知,光照时,光催化电极产生电子和空穴,驱动阴极反
应(Li++e-===Li)和阳极反应(Li O +2h+===2Li++O),则充电时,电池的总反应为
2 2 2
LiO===2Li+O ,因此,充电效率与光照产生的电子和空穴量有关,A、B正确;放电时,
2 2 2
金属Li电极为负极,光催化电极为正极,Li+从负极穿过离子交换膜向正极迁移,C错误;
放电时,电池总反应为2Li+O===LiO,则正极反应为O+2Li++2e-===LiO,D正确。
2 2 2 2 2 2
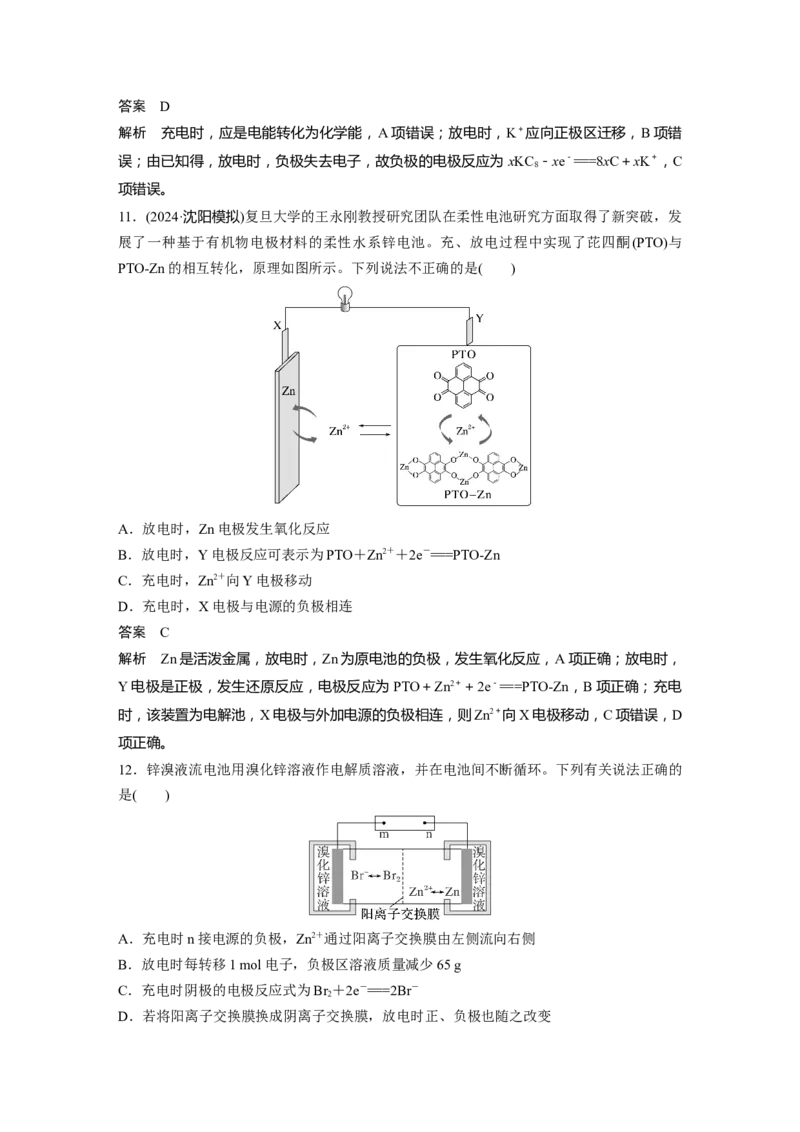
7.如图是利用微生物将废水中的乙二胺[H N(CH )NH ]氧化为环境友好物质而制作的化学
2 2 2 2
电源,可给二次电池充电。下列说法正确的是( )
A.M极电极反应式:HN(CH )NH +4HO-16e-===2CO+N+16H+
2 2 2 2 2 2 2
B.充电时二次电池的正极应与M极相连
C.H+通过质子交换膜由N极向M极移动
D.若N极消耗了标准状况下2.24 L O ,则有0.4 mol电子从N极流向M极
2
答案 A
解析 由题图知,M极为负极,N极为正极,HN(CH )NH 在负极上失电子发生氧化反应,
2 2 2 2
电极反应式为HN(CH )NH +4HO-16e-===2CO +N +16H+,A正确;充电时二次电池
2 2 2 2 2 2 2
的正极应与外接电源的正极相连,即与N极相连,B错误;H+通过质子交换膜由M极移向
N极,C错误;当N电极消耗标况下2.24 L O 时,则转移× 4=0.4 mol电子,所以有0.4
2
mol电子从M极流向N极,D错误。
8.(2023·全国乙卷,12)室温钠-硫电池被认为是一种成本低、比能量高的能源存储系统。一
种室温钠-硫电池的结构如图所示。将钠箔置于聚苯并咪唑膜上作为一个电极,表面喷涂有
硫黄粉末的炭化纤维素纸作为另一电极。工作时,在硫电极发生反应:S+e-―→S,S+e-
8
―→S,2Na++S+2(1-)e-―→NaS
2 x
下列叙述错误的是( )
A.充电时Na+从钠电极向硫电极迁移
B.放电时外电路电子流动的方向是a→b
C.放电时正极反应为2Na++S+2e-―→NaS
8 2 x
D.炭化纤维素纸的作用是增强硫电极导电性能答案 A
解析 充电时为电解池装置,阳离子移向阴极,Na+由硫电极迁移至钠电极,A错误;放电
时Na在a电极失去电子,失去的电子经外电路流向 b电极,即电子在外电路的流向为
a→b,B正确;将题给硫电极发生的反应依次编号为①②③,由×①+×②+③可得正极的
反应式为2Na++S+2e-―→NaS,C正确;炭化纤维素纸中含有大量的炭,炭具有良好的
8 2 x
导电性,可以增强硫电极的导电性能,D正确。
9.如图是常温钠离子全固态浓差电池工作示意图。正极材料为层状含钠过渡金属氧化物,负
极为钠锡合金(Na Sn )。下列说法合理的是( )
15 4
A.该电池工作时不发生氧化还原反应
B.放电时,负极的反应为Na Sn -15e-===15Na++4Sn
15 4
C.充电时,Na+会被吸附进入过渡金属氧化物层
D.充电时,b极接电源的正极,a极接电源的负极
答案 B
解析 该电池放电时,是原电池工作原理,充电时,是电解池工作原理,无论是放电还是充
电均发生了氧化还原反应,故A错误;放电时,负极上钠锡合金(Na Sn )失电子发生氧化反
15 4
应生成钠离子和锡,故B正确;充电时,是电解池工作原理,Na+会向阴极移动,会脱离过
渡金属氧化物层,故C错误;充电时,b极接电源的负极,a极接电源的正极,故D错误。
10.一种钾离子电池的电池反应为K MnO +8xCK MnO +xKC ,其装置如图所
0.5 2 0.5-x 2 8
示。下列说法正确的是( )
A.充电时,化学能转变为电能
B.放电时,K+向负极区迁移
C.放电时,负极的电极反应为Al-3e-===Al3+
D.充电时,阳极的电极反应为K MnO -xe-===K MnO +xK+
0.5 2 0.5-x 2答案 D
解析 充电时,应是电能转化为化学能,A项错误;放电时,K+应向正极区迁移,B项错
误;由已知得,放电时,负极失去电子,故负极的电极反应为 xKC -xe-===8xC+xK+,C
8
项错误。
11.(2024·沈阳模拟)复旦大学的王永刚教授研究团队在柔性电池研究方面取得了新突破,发
展了一种基于有机物电极材料的柔性水系锌电池。充、放电过程中实现了芘四酮(PTO)与
PTO-Zn的相互转化,原理如图所示。下列说法不正确的是( )
A.放电时,Zn电极发生氧化反应
B.放电时,Y电极反应可表示为PTO+Zn2++2e-===PTO-Zn
C.充电时,Zn2+向Y电极移动
D.充电时,X电极与电源的负极相连
答案 C
解析 Zn是活泼金属,放电时,Zn为原电池的负极,发生氧化反应,A项正确;放电时,
Y电极是正极,发生还原反应,电极反应为PTO+Zn2++2e-===PTO-Zn,B项正确;充电
时,该装置为电解池,X电极与外加电源的负极相连,则Zn2+向X电极移动,C项错误,D
项正确。
12.锌溴液流电池用溴化锌溶液作电解质溶液,并在电池间不断循环。下列有关说法正确的
是( )
A.充电时n接电源的负极,Zn2+通过阳离子交换膜由左侧流向右侧
B.放电时每转移1 mol电子,负极区溶液质量减少65 g
C.充电时阴极的电极反应式为Br +2e-===2Br-
2
D.若将阳离子交换膜换成阴离子交换膜,放电时正、负极也随之改变答案 A
解析 充电时n接电源的负极,作电解池的阴极,Zn2+通过阳离子交换膜向阴极定向迁移,
故由左侧流向右侧,A正确;放电时,负极Zn溶解生成Zn2+,Zn2+通过阳离子交换膜向正
极定向迁移,故负极区溶液质量不变,B错误;充电时阴极的电极反应式为 Zn2++2e-
===Zn,C错误;若将阳离子交换膜换成阴离子交换膜,放电时正、负极不会改变,D错误。
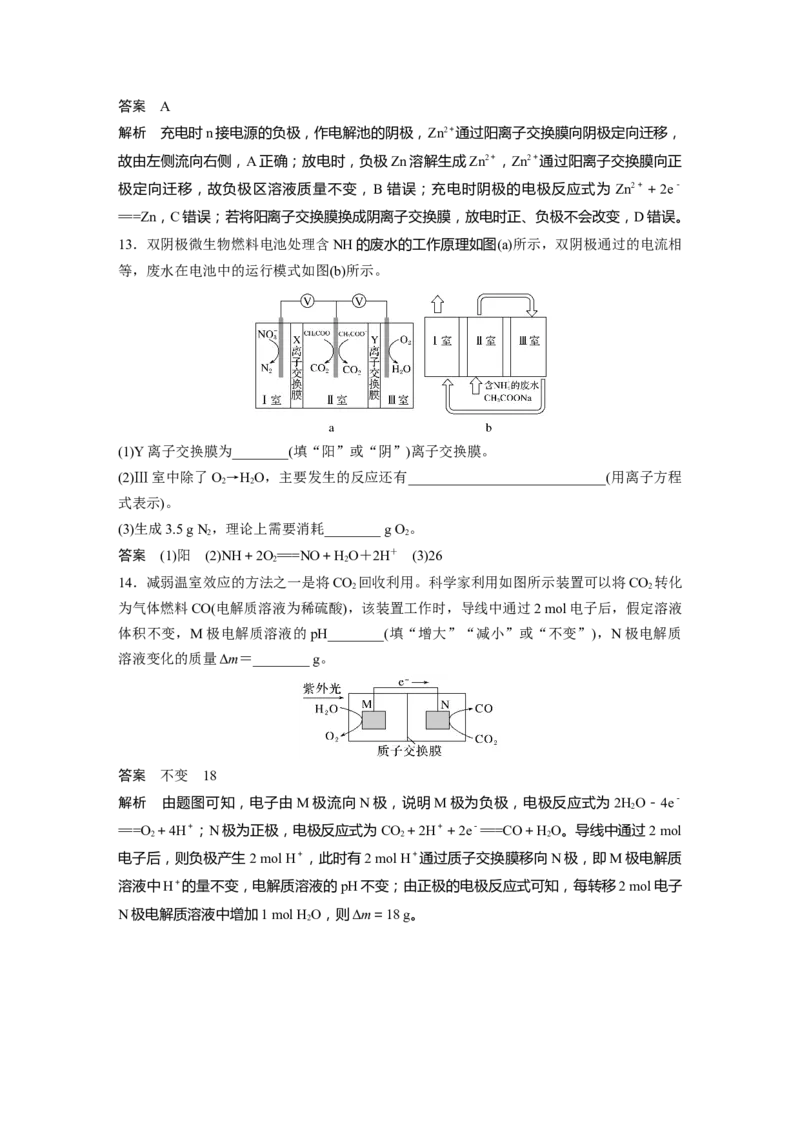
13.双阴极微生物燃料电池处理含NH的废水的工作原理如图(a)所示,双阴极通过的电流相
等,废水在电池中的运行模式如图(b)所示。
(1)Y离子交换膜为________(填“阳”或“阴”)离子交换膜。
(2)Ⅲ室中除了O→HO,主要发生的反应还有____________________________(用离子方程
2 2
式表示)。
(3)生成3.5 g N ,理论上需要消耗________ g O。
2 2
答案 (1)阳 (2)NH+2O===NO+HO+2H+ (3)26
2 2
14.减弱温室效应的方法之一是将CO 回收利用。科学家利用如图所示装置可以将CO 转化
2 2
为气体燃料CO(电解质溶液为稀硫酸),该装置工作时,导线中通过2 mol电子后,假定溶液
体积不变,M极电解质溶液的pH________(填“增大”“减小”或“不变”),N极电解质
溶液变化的质量Δm=________ g。
答案 不变 18
解析 由题图可知,电子由M极流向N极,说明M极为负极,电极反应式为2HO-4e-
2
===O +4H+;N极为正极,电极反应式为CO +2H++2e-===CO+HO。导线中通过2 mol
2 2 2
电子后,则负极产生2 mol H+,此时有2 mol H+通过质子交换膜移向N极,即M极电解质
溶液中H+的量不变,电解质溶液的pH不变;由正极的电极反应式可知,每转移2 mol电子
N极电解质溶液中增加1 mol H O,则Δm=18 g。
2