文档内容
专项训练 工业流程题
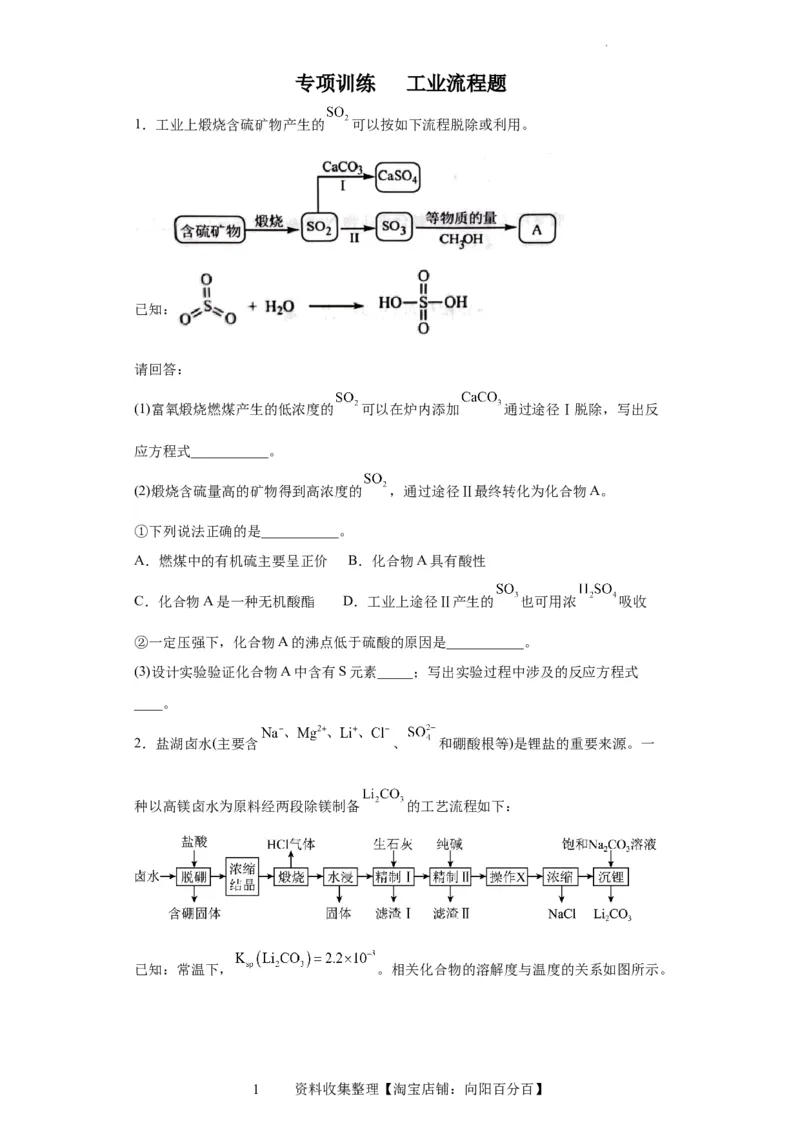
1.工业上煅烧含硫矿物产生的 可以按如下流程脱除或利用。
已知:
请回答:
(1)富氧煅烧燃煤产生的低浓度的 可以在炉内添加 通过途径Ⅰ脱除,写出反
应方程式___________。
(2)煅烧含硫量高的矿物得到高浓度的 ,通过途径Ⅱ最终转化为化合物A。
①下列说法正确的是___________。
A.燃煤中的有机硫主要呈正价 B.化合物A具有酸性
C.化合物A是一种无机酸酯 D.工业上途径Ⅱ产生的 也可用浓 吸收
②一定压强下,化合物A的沸点低于硫酸的原因是___________。
(3)设计实验验证化合物A中含有S元素_____;写出实验过程中涉及的反应方程式
____。
2.盐湖卤水(主要含 、 和硼酸根等)是锂盐的重要来源。一
种以高镁卤水为原料经两段除镁制备 的工艺流程如下:
已知:常温下, 。相关化合物的溶解度与温度的关系如图所示。
1 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司回答下列问题:
(1)含硼固体中的 在水中存在平衡: (常温下,
); 与 溶液反应可制备硼砂 。常温下,
在 硼砂溶液中, 水解生成等物质的量浓度的 和
,该水解反应的离子方程式为_____,该溶液 _____。
(2)滤渣Ⅰ的主要成分是_____(填化学式);精制Ⅰ后溶液中 的浓度为 ,则
常温下精制Ⅱ过程中 浓度应控制在_____ 以下。若脱硼后直接进行精制Ⅰ,
除无法回收 外,还将增加_____的用量(填化学式)。
(3)精制Ⅱ的目的是_____;进行操作 时应选择的试剂是_____,若不进行该操作而直
接浓缩,将导致_____。
3.超纯 是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者
开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯 方面取
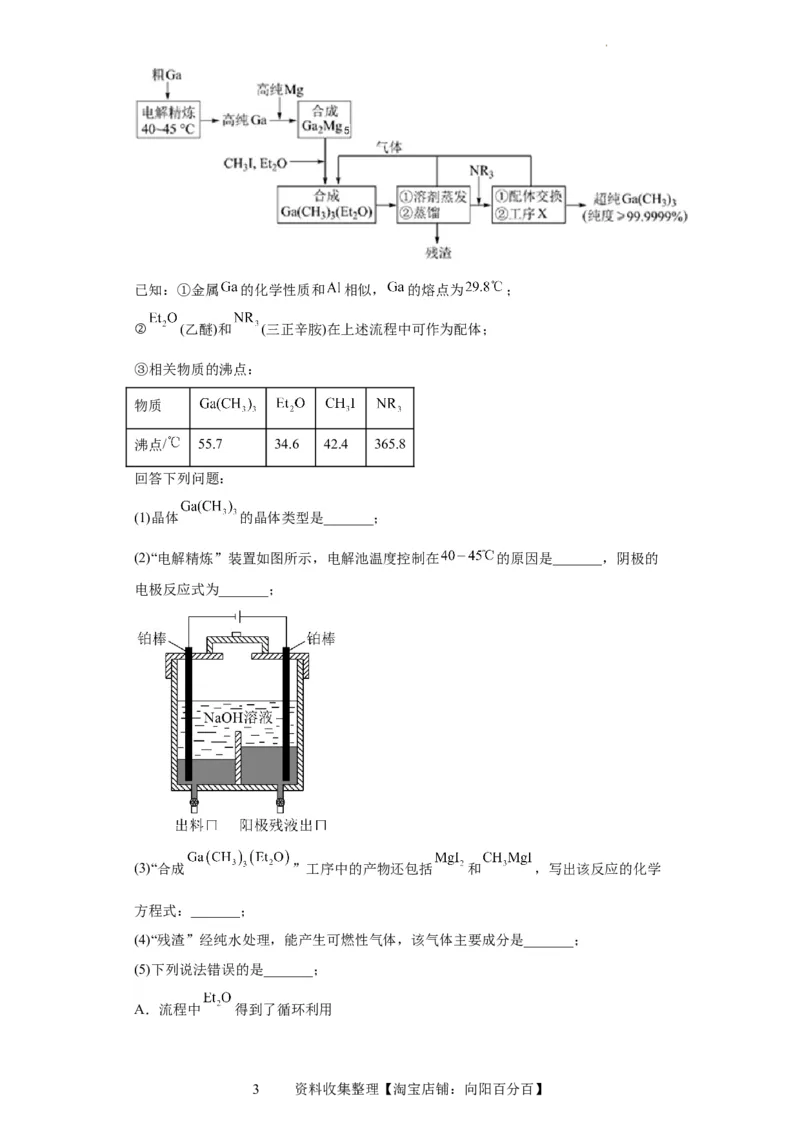
得了显著成果,工业上以粗镓为原料,制备超纯 的工艺流程如下:
试卷第2页,共13页已知:①金属 的化学性质和 相似, 的熔点为 ;
② (乙醚)和 (三正辛胺)在上述流程中可作为配体;
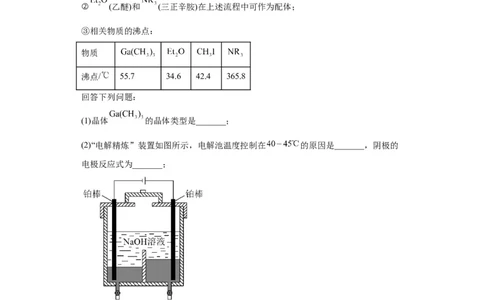
③相关物质的沸点:
物质
沸点/ 55.7 34.6 42.4 365.8
回答下列问题:
(1)晶体 的晶体类型是_______;
(2)“电解精炼”装置如图所示,电解池温度控制在 的原因是_______,阴极的
电极反应式为_______;
(3)“合成 ”工序中的产物还包括 和 ,写出该反应的化学
方程式:_______;
(4)“残渣”经纯水处理,能产生可燃性气体,该气体主要成分是_______;
(5)下列说法错误的是_______;
A.流程中 得到了循环利用
3 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司B.流程中,“合成 ”至“工序X”需在无水无氧的条件下进行
C.“工序X”的作用是解配 ,并蒸出
D.用核磁共振氢谱不能区分 和
(6)直接分解 不能制备超纯 ,而本流程采用“配体交换”工
艺制备超纯 的理由是_______;
(7)比较分子中的 键角大小: _______ (填“>”“<”
或“=”),其原因是_______。
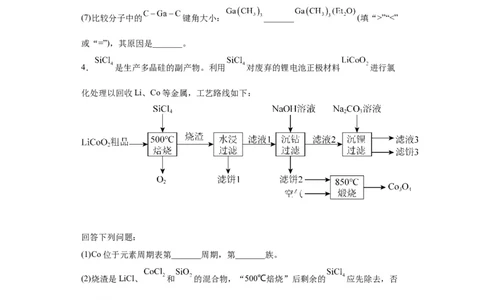
4. 是生产多晶硅的副产物。利用 对废弃的锂电池正极材料 进行氯
化处理以回收Li、Co等金属,工艺路线如下:
回答下列问题:
(1)Co位于元素周期表第_______周期,第_______族。
(2)烧渣是LiCl、 和 的混合物,“500℃焙烧”后剩余的 应先除去,否
则水浸时会产生大量烟雾,用化学方程式表示其原因_______。
(3)鉴别洗净的“滤饼3”和固体 常用方法的名称是_______。
(4)已知 ,若“沉钴过滤”的pH控制为10.0,则溶液中
浓度为_______ 。“850℃煅烧”时的化学方程式为_______。
(5)导致 比 易水解的因素有_______(填标号)。
试卷第4页,共13页a.Si-Cl键极性更大 b.Si的原子半径更大
c.Si-Cl键键能更大 d.Si有更多的价层轨道
5.某工厂采用如下工艺处理镍钴矿硫酸浸取液含( 和
)。实现镍、钴、镁元素的回收。
已知:
物质
回答下列问题:
(1)用硫酸浸取镍钴矿时,提高浸取速率的方法为_______(答出一条即可)。
(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸 ,
中过氧键的数目为_______。
(3)“氧化”中,用石灰乳调节 , 被 氧化为 ,该反应的离子方
程式为_______( 的电离第一步完全,第二步微弱);滤渣的成分为 、
_______(填化学式)。
(4)“氧化”中保持空气通入速率不变, (Ⅱ)氧化率与时间的关系如下。 体积分
数为_______时, (Ⅱ)氧化速率最大;继续增大 体积分数时, (Ⅱ)氧化速率
减小的原因是_______。
5 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司(5)“沉钴镍”中得到的 (Ⅱ)在空气中可被氧化成 ,该反应的化学方程式为
_______。
(6)“沉镁”中为使 沉淀完全 ,需控制 不低于_______(精确至0.1)。
6.LiMn O 作为一种新型锂电池正极材料受到广泛关注。由菱锰矿(MnCO ,含有少
2 4 3
量Si、Fe、Ni、Al等元素)制备LiMn O 的流程如下:
2 4
已知:K [Fe(OH) ]=2.8×10-39,K [Al(OH) ]=1.3×10-33,K [Ni(OH) ]=5.5×10-16。
sp 3 sp 3 sp 2
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为_______。为提高溶矿速率,可采取的措施
_______(举1例)。
(2)加入少量MnO 的作用是_______。不宜使用HO 替代MnO ,原因是_______。
2 2 2 2
(3)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)=_______mol·L-1;用石灰乳调节
至pH≈7,除去的金属离子是_______。
(4)加入少量BaS溶液除去Ni2+,生成的沉淀有_______。
(5)在电解槽中,发生电解反应的离子方程式为_______。随着电解反应进行,为保持电
解液成分稳定,应不断_______。电解废液可在反应器中循环利用。
(6)煅烧窑中,生成LiMn O 反应的化学方程式是_______。
2 4
7.铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、
铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:
试卷第6页,共13页已知:最高价铬酸根在酸性介质中以Cr O 存在,在碱性介质中以CrO 存在。
2
回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为
___________(填化学式)。
(2)水浸渣中主要有SiO 和___________。
2
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是___________。
(4)“除硅磷”步骤中,使硅、磷分别以MgSiO 和MgNH PO 的形式沉淀,该步需要控
3 4 4
制溶液的pH≈9以达到最好的除杂效果,若pH<9时,会导致___________;pH>9时,
会导致___________。
(5)“分离钒”步骤中,将溶液pH调到1.8左右得到VO 沉淀,VO 在pH<1时,溶解
2 5 2 5
为VO 或VO3+在碱性条件下,溶解为VO 或VO ,上述性质说明VO 具有
2 5
___________(填标号)。
A.酸性 B.碱性 C.两性
(6)“还原”步骤中加入焦亚硫酸钠(Na SO)溶液,反应的离子方程式为___________。
2 2 5
8. 是一种压电材料。以 为原料,采用下列路线可制备粉状 。
回答下列问题:
(1)“焙烧”步骤中碳粉的主要作用是_______。
(2)“焙烧”后固体产物有 、易溶于水的 和微溶于水的 。“浸取”时主要
7 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司反应的离子方程式为_______。
(3)“酸化”步骤应选用的酸是_______(填标号)。
a.稀硫酸 b.浓硫酸 c.盐酸 d.磷酸
(4)如果焙烧后的产物直接用酸浸取,是否可行?_______,其原因是_______。
(5)“沉淀”步骤中生成 的化学方程式为_______。
(6)“热分解”生成粉状钛酸钡,产生的 _______。
9.金属镍广泛应用于制造记忆合金、储氢合金以及用作加氢反应的催化剂,是重要的
战略物资,但资源匮乏。从某废镍渣(含NiFe O、NiO、FeO、Al O)中回收镍并转化
2 4 2 3
为NiSO 的流程如图所示:
4
回答下列问题:
(1)“碱浸”时发生反应的离子方程式为___________。
(2)“焙烧”后金属元素以硫酸盐的形式存在,写出NiO与(NH )SO 反应的化学方程式
4 2 4
___________。
(3)使用95℃热水“溶解”后过滤,所得滤渣的主要成分的化学式是___________。
(4)①“萃取”时发生反应 (Mn+为金属离子,RH为萃取剂),萃
取率与 的关系如下表所示,当 时,水层中主要的阳离子为
___________。
萃取率/% 0.1 0.15 0.2 0.25 0.3 0.35 0.4
Ni2+ 55% 68% 80% 99% 99.5% 99.8% 99.9%
Fe2+ 2% 2% 4% 5% 8% 30% 58%
②物质X的化学式为___________。
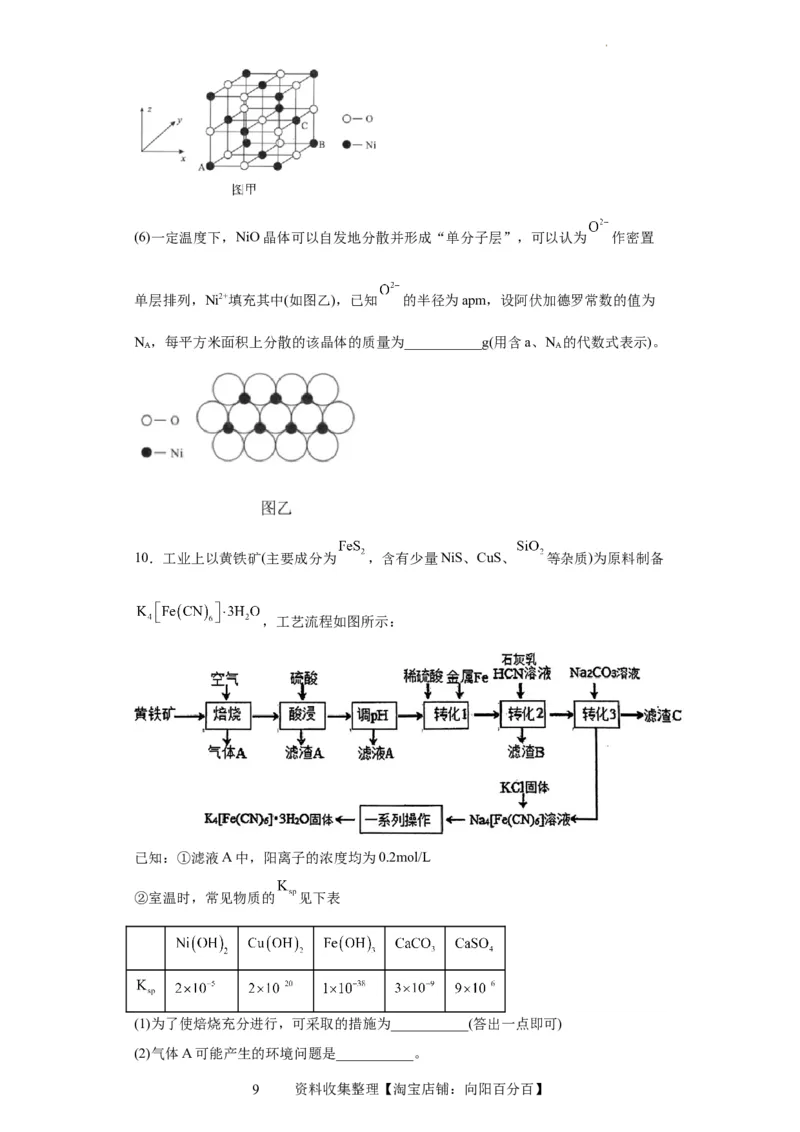
(5)碳酸镍受热可分解为NiO,NiO的晶体结构如图甲所示,其中离子坐标参数A为
(0,0,0),B为(1,1,0),则C离子坐标参数为___________。
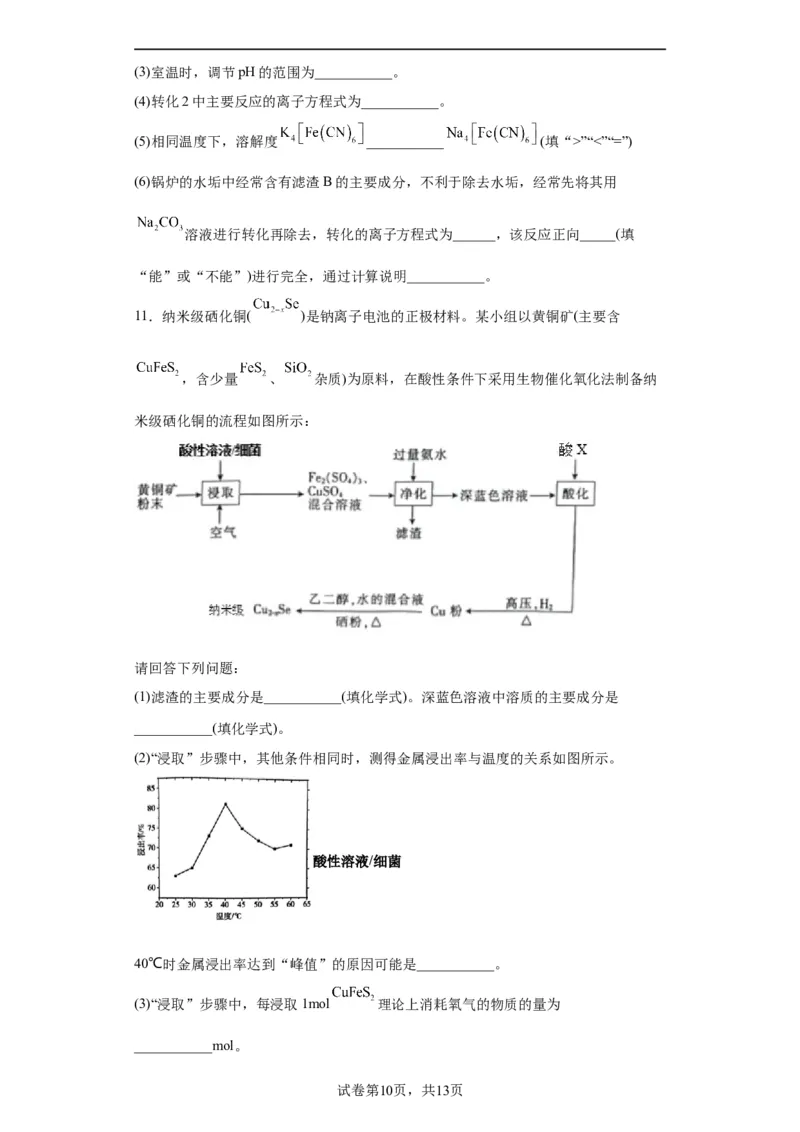
试卷第8页,共13页(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为 作密置
单层排列,Ni2+填充其中(如图乙),已知 的半径为apm,设阿伏加德罗常数的值为
N ,每平方米面积上分散的该晶体的质量为___________g(用含a、N 的代数式表示)。
A A
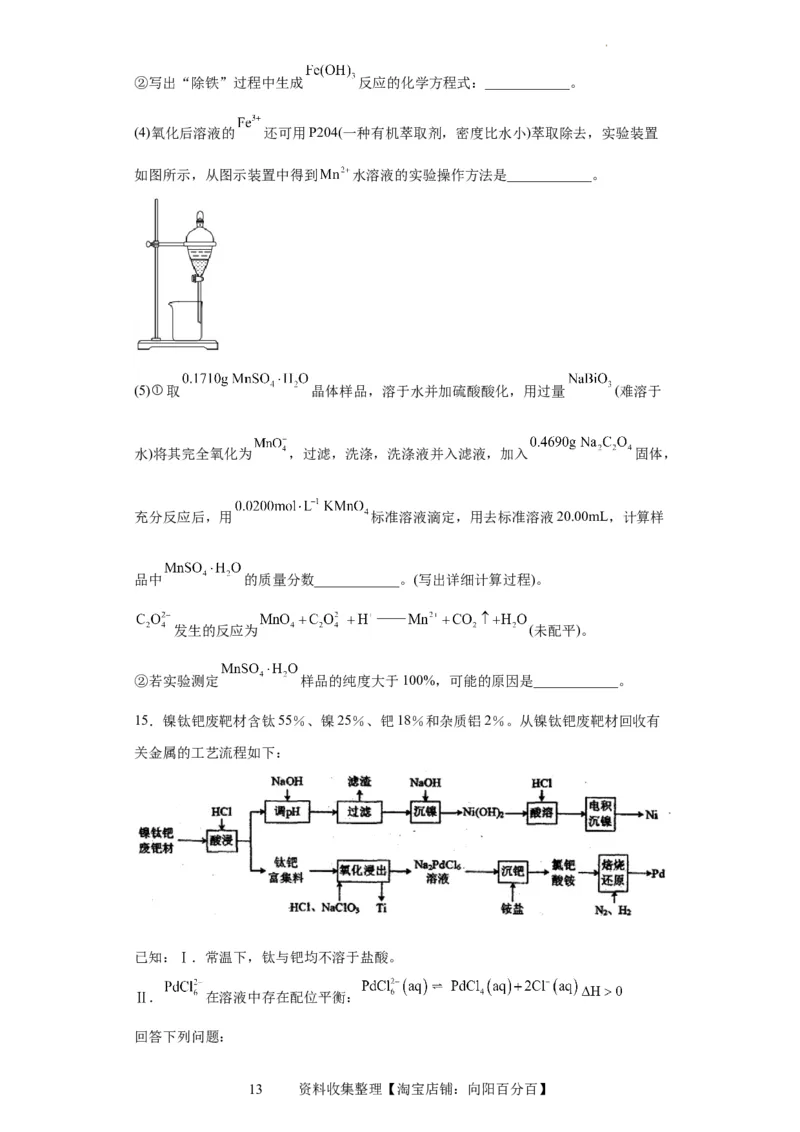
10.工业上以黄铁矿(主要成分为 ,含有少量NiS、CuS、 等杂质)为原料制备
,工艺流程如图所示:
已知:①滤液A中,阳离子的浓度均为0.2mol/L
②室温时,常见物质的 见下表
(1)为了使焙烧充分进行,可采取的措施为___________(答出一点即可)
(2)气体A可能产生的环境问题是___________。
9 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司(3)室温时,调节pH的范围为___________。
(4)转化2中主要反应的离子方程式为___________。
(5)相同温度下,溶解度 ___________ (填“>”“<”“=”)
(6)锅炉的水垢中经常含有滤渣B的主要成分,不利于除去水垢,经常先将其用
溶液进行转化再除去,转化的离子方程式为______,该反应正向_____(填
“能”或“不能”)进行完全,通过计算说明___________。
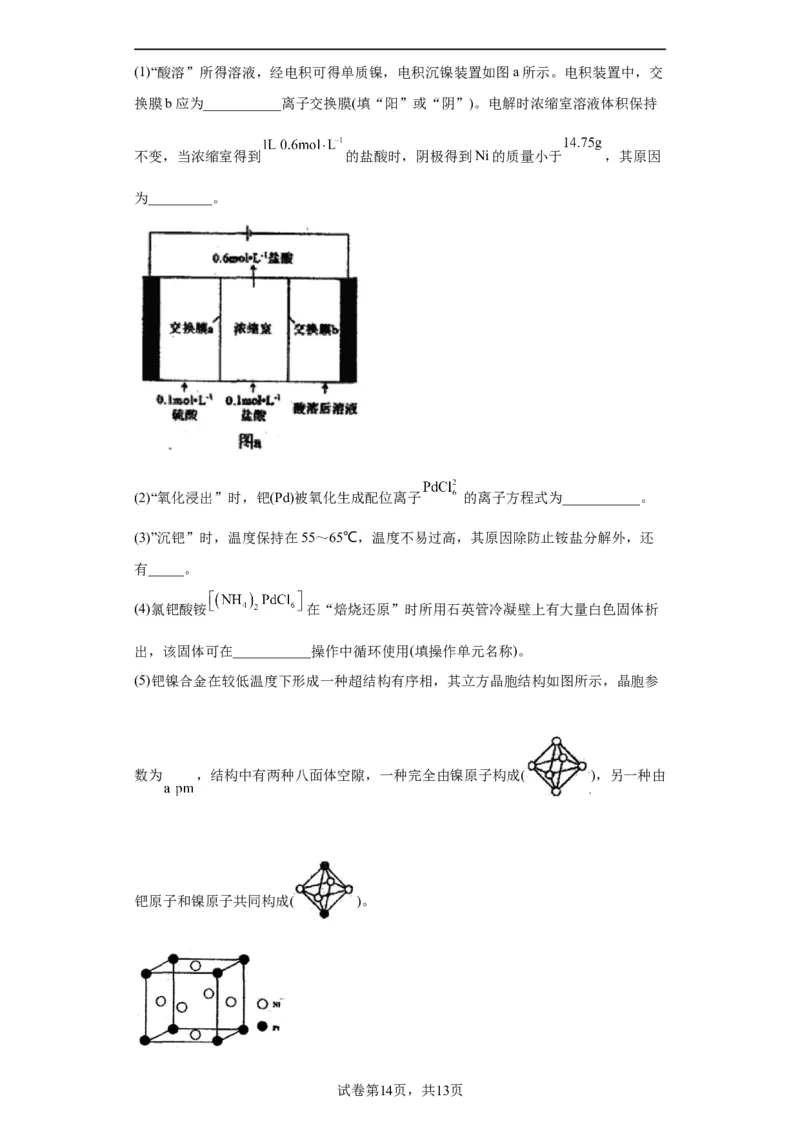
11.纳米级硒化铜( )是钠离子电池的正极材料。某小组以黄铜矿(主要含
,含少量 、 杂质)为原料,在酸性条件下采用生物催化氧化法制备纳
米级硒化铜的流程如图所示:
请回答下列问题:
(1)滤渣的主要成分是___________(填化学式)。深蓝色溶液中溶质的主要成分是
___________(填化学式)。
(2)“浸取”步骤中,其他条件相同时,测得金属浸出率与温度的关系如图所示。
酸性溶液/细菌
40℃时金属浸出率达到“峰值”的原因可能是___________。
(3)“浸取”步骤中,每浸取1mol 理论上消耗氧气的物质的量为
___________mol。
试卷第10页,共13页(4)用CuO或 替代氨水可以达到相同的目的,其可能原因是___________。
12.以废锌电池预处理物(主要成分为ZnO,另含少量 、CuO、 、MnO等)为
原料可生产草酸锌晶体( )、生产流程如下图所示。
已知:常温下,溶度积常数 ; 。
回答问题:
(1)“酸浸”后所得“滤渣A”的主要成分为_______。
(2)“除锰”时,反应的离子方程式为_______。
(3)“除铁”时,加入ZnO的目的是_______。
(4)“除铜”后要求溶液中 mol·L ,若溶液中 浓度为0.1 mol·L
试列式计算说明溶液能否达到“除铜”要求_______。
(5)“沉淀”后,需经过滤、洗涤、干燥系列操作分离出草酸锌晶体,检验沉淀是否洗净
的操作为_______。
(6)在通风橱中,将草酸锌晶体置于陶瓷仪器_______(填仪器名称)中加热分解可制得
ZnO。
13.在镀镍生产过程中,产生的硫酸镍废料(含Cu2+ 、Fe3+、Ca2+、Mg2+、Zn2+等杂质
离子)是一种宝贵的可再生资源,某实验小组用粗硫酸镍废料制备硫酸镍
(NiSO ·6H O),其流程如图所示:
4 2
11 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司(1)“滤渣1”的主要成分是___________ (写化学式), 中S原子采用___________
杂化。
(2)基态Ni2+的价电子排布式为___________。
(3)写出“硫化”过程中Fe3+与HS反应的离子方程式:___________。
2
(4)“氟化”的目的是除去Ca2+、Mg2+ ,已知25℃时, K (CaF )=3.95× 10-11 ;K
sp 2 sp
(MgF )=6.40×10-9。当Mg2+刚好完全沉淀(浓度小于等于10-5 mol·L-1 )时,Ca2+的浓度为
2
___________(保留两位有效数字)mol· L-1。氟化钙的晶胞结构如图所示,该晶体属于
___________ (填“离子”或“ 共价”)晶体,每个Ca2+周围距离最近且等距的F- 有
___________个。
14.用废锰渣(主要成分为 、MgO和 )和硫铁矿(主要成分 )制取
的工艺流程如下:
(1) 较易被氧化成 ,请从原子结构的角度分析其可能的原因:____________。
(2)“酸溶”后需“过滤”的目的是:①防止将 等杂质离子带入还原反应液中,简
化除杂操作:②____________。
(3)已知:室温下 , ,
,“氧化”后溶液中 。
①欲使溶液中 ,“除铁”过程需控制溶液pH的范围是
____________。
试卷第12页,共13页②写出“除铁”过程中生成 反应的化学方程式:____________。
(4)氧化后溶液的 还可用P204(一种有机萃取剂,密度比水小)萃取除去,实验装置
如图所示,从图示装置中得到 水溶液的实验操作方法是____________。
(5)①取 晶体样品,溶于水并加硫酸酸化,用过量 (难溶于
水)将其完全氧化为 ,过滤,洗涤,洗涤液并入滤液,加入 固体,
充分反应后,用 标准溶液滴定,用去标准溶液20.00mL,计算样
品中 的质量分数____________。(写出详细计算过程)。
发生的反应为 (未配平)。
②若实验测定 样品的纯度大于100%,可能的原因是____________。
15.镍钛钯废靶材含钛55%、镍25%、钯18%和杂质铝2%。从镍钛钯废靶材回收有
关金属的工艺流程如下:
已知:Ⅰ.常温下,钛与钯均不溶于盐酸。
Ⅱ. 在溶液中存在配位平衡:
回答下列问题:
13 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司(1)“酸溶”所得溶液,经电积可得单质镍,电积沉镍装置如图a所示。电积装置中,交
换膜b应为___________离子交换膜(填“阳”或“阴”)。电解时浓缩室溶液体积保持
不变,当浓缩室得到 的盐酸时,阴极得到Ni的质量小于 ,其原因
为_________。
(2)“氧化浸出”时,钯(Pd)被氧化生成配位离子 的离子方程式为___________。
(3)”沉钯”时,温度保持在55~65℃,温度不易过高,其原因除防止铵盐分解外,还
有_____。
(4)氯钯酸铵 在“焙烧还原”时所用石英管冷凝壁上有大量白色固体析
出,该固体可在___________操作中循环使用(填操作单元名称)。
(5)钯镍合金在较低温度下形成一种超结构有序相,其立方晶胞结构如图所示,晶胞参
数为 ,结构中有两种八面体空隙,一种完全由镍原子构成( ),另一种由
钯原子和镍原子共同构成( )。
试卷第14页,共13页①该晶体的化学式为___________。
②两种八面体空隙中心的最近距离为___________。
15 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司