文档内容
珠海市教研联盟校 2023 届高三联考
化学试题
满分100分,考试用时75分钟。
可能用到的相对原子质量:H-1 C-12 O-16 Na-23
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小
题4分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1. 《医学入门》中记载我国传统中医提纯铜绿的方法:“水洗净,细研水飞,去石澄清,慢火熬干,”其中
未涉及的操作是
A. 洗涤 B. 粉碎 C. 萃取 D. 蒸发
2. 化学与生产、生活、科技、医药等密切相关。下列说法错误的是
A. 冬奥会使用的二氧化碳跨临界制冰技术,与传统制冷剂氟利昂相比更加环保
B. 新冠疫苗使用的中硼硅玻璃瓶含有的 是一种复杂的氧化物
C. “天宫二号”空间站的太阳能电池帆板,其主要材料含有晶体硅
D. C919国产大飞机风挡结构部分使用的有机玻璃属于有机高分子材料
3. 下列化学用语描述或图示表达正确的是
A. 原子结构示意图 ,可以表示 和
B. 中子数为127的碘原子:
C. 过氧化氢 比例模型:
的
D. NaClO的电子式:
4. 图为酸雨形成的示意图。下列说法正确的是A. 空气中的 溶于水也会形成酸雨
B. 易溶于水,并在雨水中转化为
C. 含 的雨水在空气中放置其pH可能会降低
D. 硝酸型酸雨会腐蚀石灰岩建筑,而硫酸型酸雨不能
5. 某无色透明溶液中加入 后,有无色无味气体产生,同时产生沉淀。则原溶液中可能含有的离子
是
A. B. C. D.
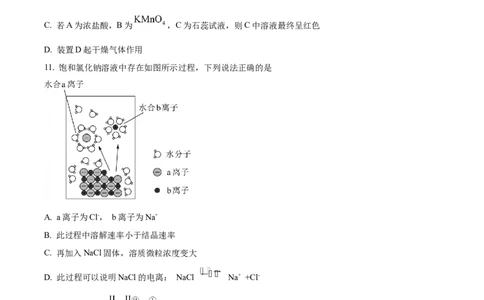
6. 实验室用氯化铵和氢氧化钙反应制取氨气,按照制备、收集、性质检验及尾气处理的顺序进行实验,下
列装置(“→”表示气流方向)不能达到实验目的的是
A. B. C.
D.
7. 几种物质的转化关系如图所示。下列说法正确的是A. 反应1中 是还原产物
B. 反应2中 得电子
C. 反应2的离子方程式为
D. 能和 大量共存
8. 某药物的一种成分均由短周期主族元素组成,其结构如图所示。元素X、Y、Z、W、E的原子序数依次
增大,X与其它几种元素不同周期,W与E原子的基态价电子排布均为 。下列说法中错误的是
A. 原子半径:W<E B. 简单氢化物的沸点:Z>Y
C. 第一电离能:Z>W D. 最高价氧化物对应的水化物的酸性:E>Y
化学试题 第2页(共8页)
9. 化学创造美好生活。下列生产活动中,没有运用相应化学原理的是
选
生产活动 化学原理
项
A 环保工程师用熟石灰处理酸性废水 熟石灰具有碱性
B 利用便携式电池为手机提供能量 原电池将化学能转化为电能
C 利用黄铁矿制备硫酸 黄铁矿中硫元素可被氧化
D 利用焦炭和石英砂制取粗硅 二氧化硅具有很好的光学性能
A. A B. B C. C D. D
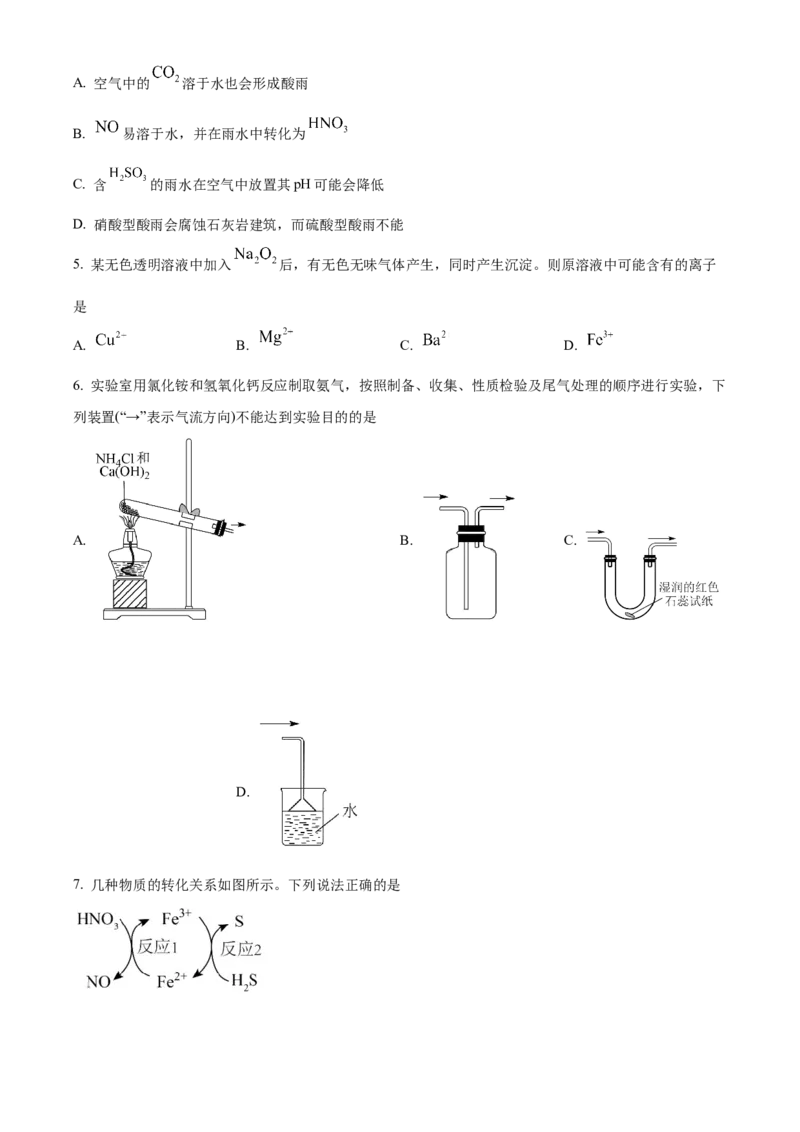
10. 用如图装置进行实验前将液体A逐滴加入到固体B中,下列叙述正确的是A. 若A为浓盐酸,B为 ,C为 溶液,可证明酸性:
B. 若A为70%的硫酸,B为 固体,C为 溶液,则C中溶液变浑浊
C. 若A为浓盐酸,B为 ,C为石蕊试液,则C中溶液最终呈红色
D. 装置D起干燥气体作用
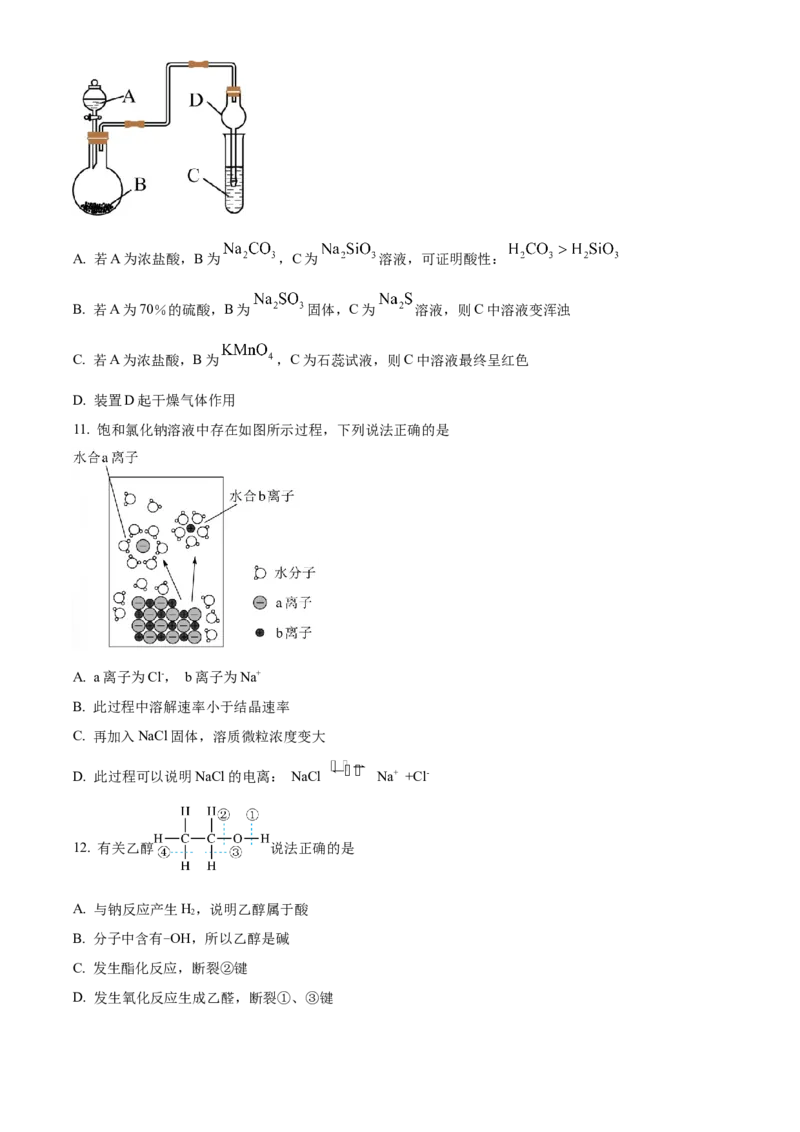
11. 饱和氯化钠溶液中存在如图所示过程,下列说法正确的是
A. a离子为Cl-, b离子为Na+
B. 此过程中溶解速率小于结晶速率
C. 再加入NaCl固体,溶质微粒浓度变大
D. 此过程可以说明NaCl的电离: NaCl Na+ +Cl-
12. 有关乙醇 说法正确的是
A. 与钠反应产生H,说明乙醇属于酸
2
B. 分子中含有-OH,所以乙醇是碱
C. 发生酯化反应,断裂②键
D. 发生氧化反应生成乙醛,断裂①、③键13. 下图是试剂标签上的部分内容。据此,下列说法错误的是
硫酸 化学纯
CP500mL
品名:硫酸
化学式:
相对分子质量:98
密度:
质量分数:98%
A. 该硫酸物质的量浓度为
的
B. 100mL该硫酸中,氧原子 数目大于7.36N
A
的
C. 取100mL该硫酸与足量铜反应,产生 分子数小于0.92N
A
D. 将该硫酸稀释至 ,溶液中 的数目为0.1 N
A
14. 下列离子方程式书写正确的是
A. 往KBr溶液中通入少量 :
B. 少量金属钠投入 溶液中:
C. 氢氧化钡溶液与稀硫酸混合:
D. 铁片投入稀硫酸中:
15. 下列由相关实验现象所得出的结论中,正确的是
A. 能使湿润的淀粉KI试纸变蓝的物质一定是
B. 滴加硝酸酸化的 溶液后有白色沉淀生成,说明溶液中一定含有
C. Zn粒分别放入稀盐酸和稀硝酸均产生气泡,说明Zn与两种酸均发生置换反应
D. 向溶液中先加氯水,再滴加KSCN溶液,溶液显红色,不能说明溶液一定含
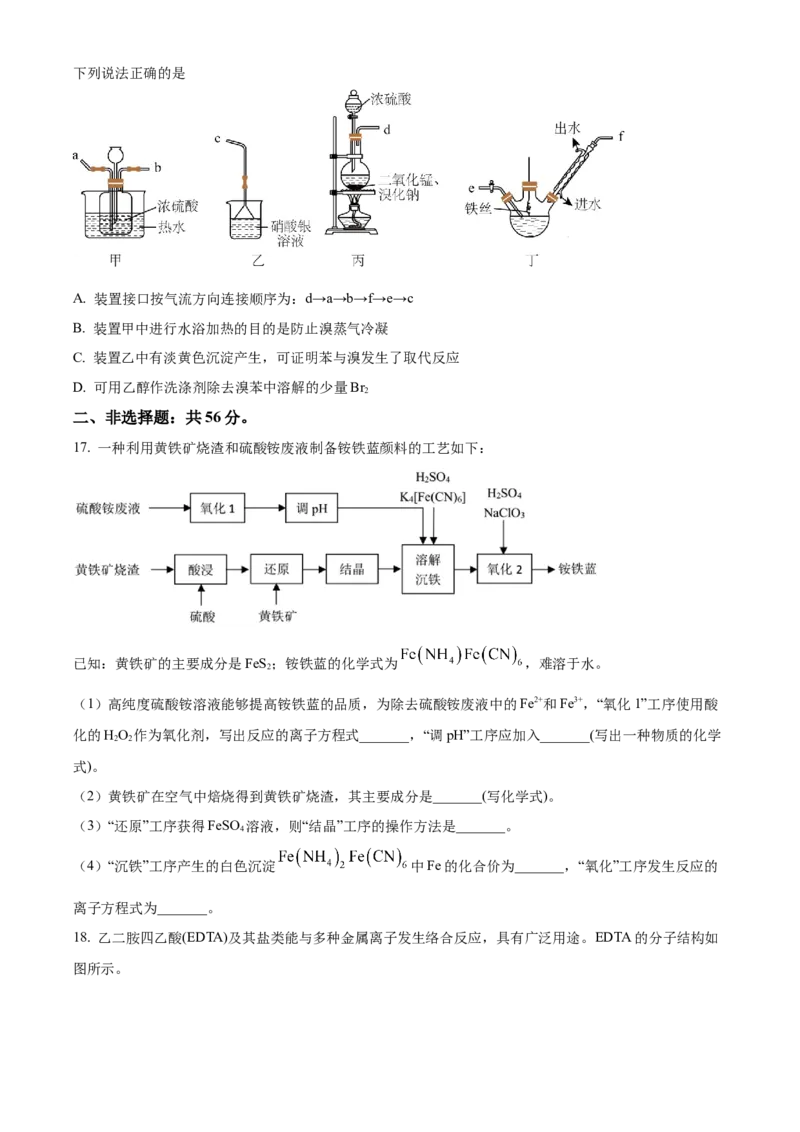
16. 已知:MnO +2NaBr+2H SO MnSO +Na SO +Br ↑+2H O,实验室利用如下图所示的装置制备溴苯。
2 2 4 4 2 4 2 2下列说法正确的是
A. 装置接口按气流方向连接顺序为:d→a→b→f→e→c
B. 装置甲中进行水浴加热的目的是防止溴蒸气冷凝
C. 装置乙中有淡黄色沉淀产生,可证明苯与溴发生了取代反应
D. 可用乙醇作洗涤剂除去溴苯中溶解的少量Br
2
二、非选择题:共56分。
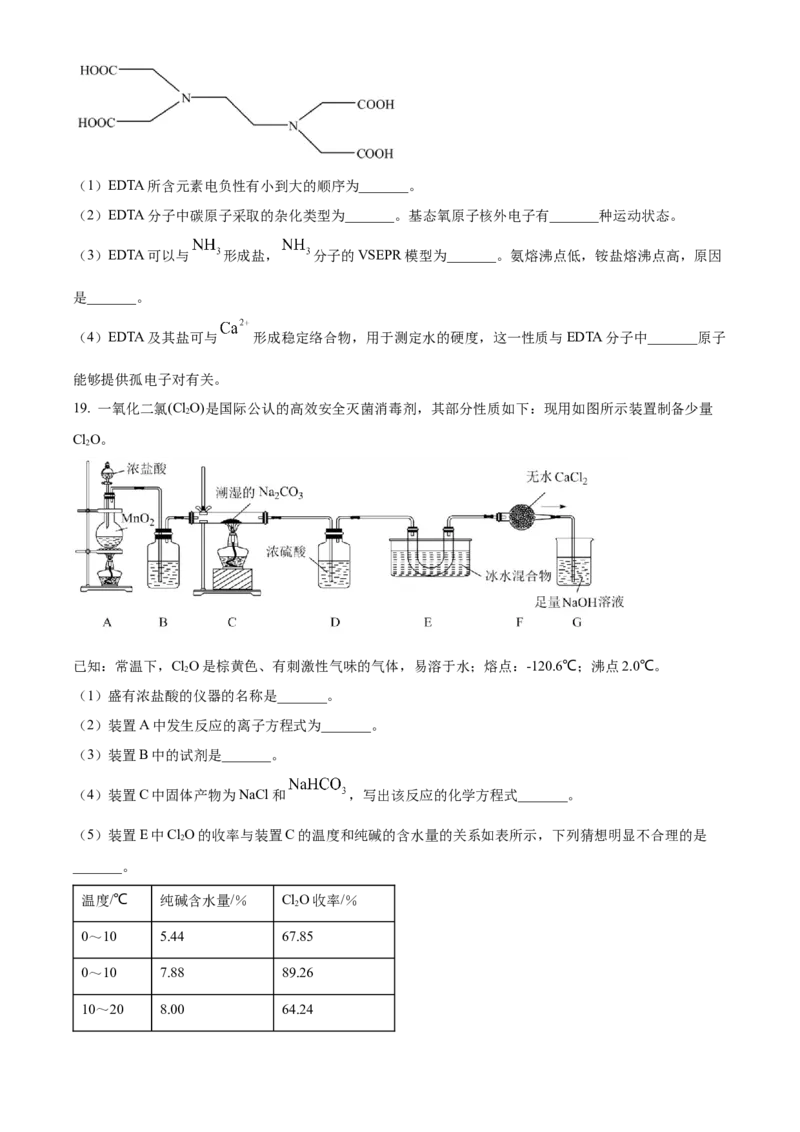
17. 一种利用黄铁矿烧渣和硫酸铵废液制备铵铁蓝颜料的工艺如下:
已知:黄铁矿的主要成分是FeS;铵铁蓝的化学式为 ,难溶于水。
2
(1)高纯度硫酸铵溶液能够提高铵铁蓝的品质,为除去硫酸铵废液中的Fe2+和Fe3+,“氧化1”工序使用酸
化的HO 作为氧化剂,写出反应的离子方程式_______,“调pH”工序应加入_______(写出一种物质的化学
2 2
式)。
(2)黄铁矿在空气中焙烧得到黄铁矿烧渣,其主要成分是_______(写化学式)。
(3)“还原”工序获得FeSO 溶液,则“结晶”工序的操作方法是_______。
4
(4)“沉铁”工序产生的白色沉淀 中Fe的化合价为_______,“氧化”工序发生反应的
离子方程式为_______。
18. 乙二胺四乙酸(EDTA)及其盐类能与多种金属离子发生络合反应,具有广泛用途。EDTA的分子结构如
图所示。(1)EDTA所含元素电负性有小到大的顺序为_______。
(2)EDTA分子中碳原子采取的杂化类型为_______。基态氧原子核外电子有_______种运动状态。
(3)EDTA可以与 形成盐, 分子的VSEPR模型为_______。氨熔沸点低,铵盐熔沸点高,原因
是_______。
(4)EDTA及其盐可与 形成稳定络合物,用于测定水的硬度,这一性质与EDTA分子中_______原子
能够提供孤电子对有关。
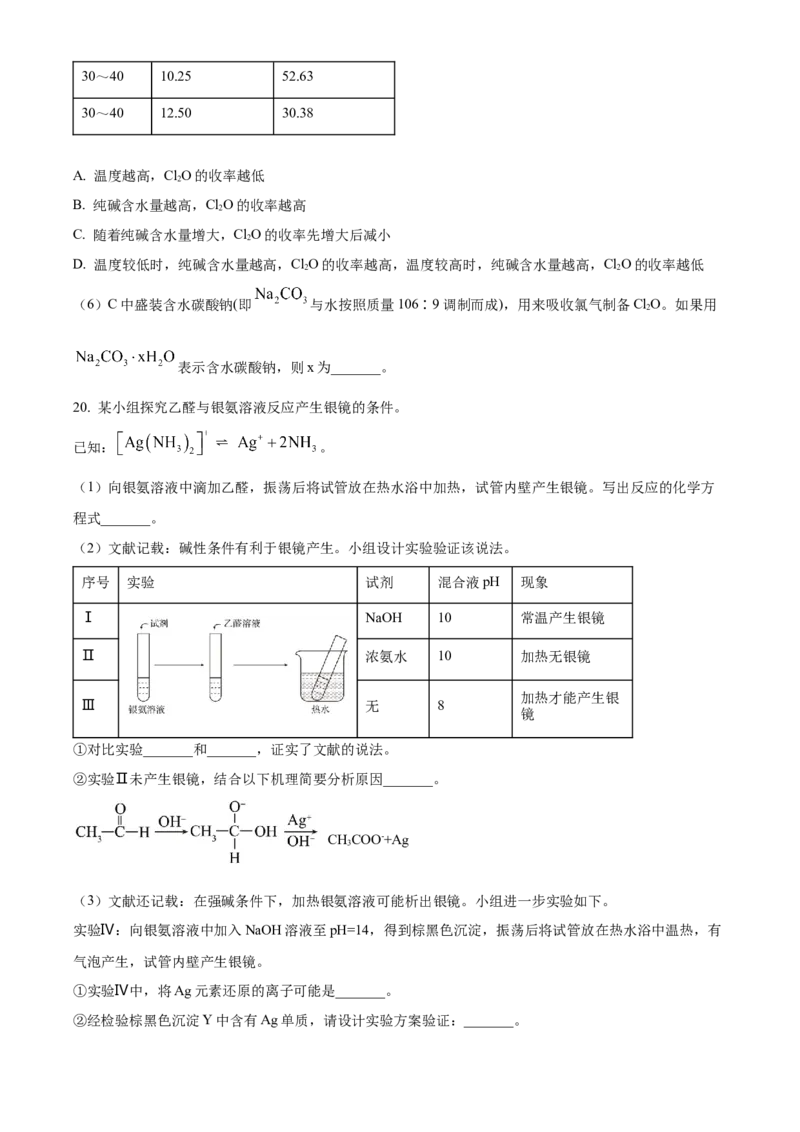
19. 一氧化二氯(Cl O)是国际公认的高效安全灭菌消毒剂,其部分性质如下:现用如图所示装置制备少量
2
ClO。
2
已知:常温下,ClO是棕黄色、有刺激性气味的气体,易溶于水;熔点:-120.6℃;沸点2.0℃。
2
(1)盛有浓盐酸的仪器的名称是_______。
(2)装置A中发生反应的离子方程式为_______。
(3)装置B中的试剂是_______。
(4)装置C中固体产物为NaCl和 ,写出该反应的化学方程式_______。
(5)装置E中ClO的收率与装置C的温度和纯碱的含水量的关系如表所示,下列猜想明显不合理的是
2
_______。
温度/℃ 纯碱含水量/% ClO收率/%
2
0~10 5.44 67.85
0~10 7.88 89.26
10~20 8.00 64.2430~40 10.25 52.63
30~40 12.50 30.38
A. 温度越高,ClO的收率越低
2
B. 纯碱含水量越高,ClO的收率越高
2
C. 随着纯碱含水量增大,ClO的收率先增大后减小
2
D. 温度较低时,纯碱含水量越高,ClO的收率越高,温度较高时,纯碱含水量越高,ClO的收率越低
2 2
(6)C中盛装含水碳酸钠(即 与水按照质量106∶9调制而成),用来吸收氯气制备ClO。如果用
2
表示含水碳酸钠,则x为_______。
20. 某小组探究乙醛与银氨溶液反应产生银镜的条件。
已知: 。
(1)向银氨溶液中滴加乙醛,振荡后将试管放在热水浴中加热,试管内壁产生银镜。写出反应的化学方
程式_______。
(2)文献记载:碱性条件有利于银镜产生。小组设计实验验证该说法。
序号 实验 试剂 混合液pH 现象
Ⅰ NaOH 10 常温产生银镜
Ⅱ 浓氨水 10 加热无银镜
加热才能产生银
Ⅲ 无 8
镜
①对比实验_______和_______,证实了文献的说法。
②实验Ⅱ未产生银镜,结合以下机理简要分析原因_______。
CHCOO-+Ag
3
(3)文献还记载:在强碱条件下,加热银氨溶液可能析出银镜。小组进一步实验如下。
实验Ⅳ:向银氨溶液中加入NaOH溶液至pH=14,得到棕黑色沉淀,振荡后将试管放在热水浴中温热,有
气泡产生,试管内壁产生银镜。
①实验Ⅳ中,将Ag元素还原的离子可能是_______。
②经检验棕黑色沉淀Y中含有Ag单质,请设计实验方案验证:_______。的
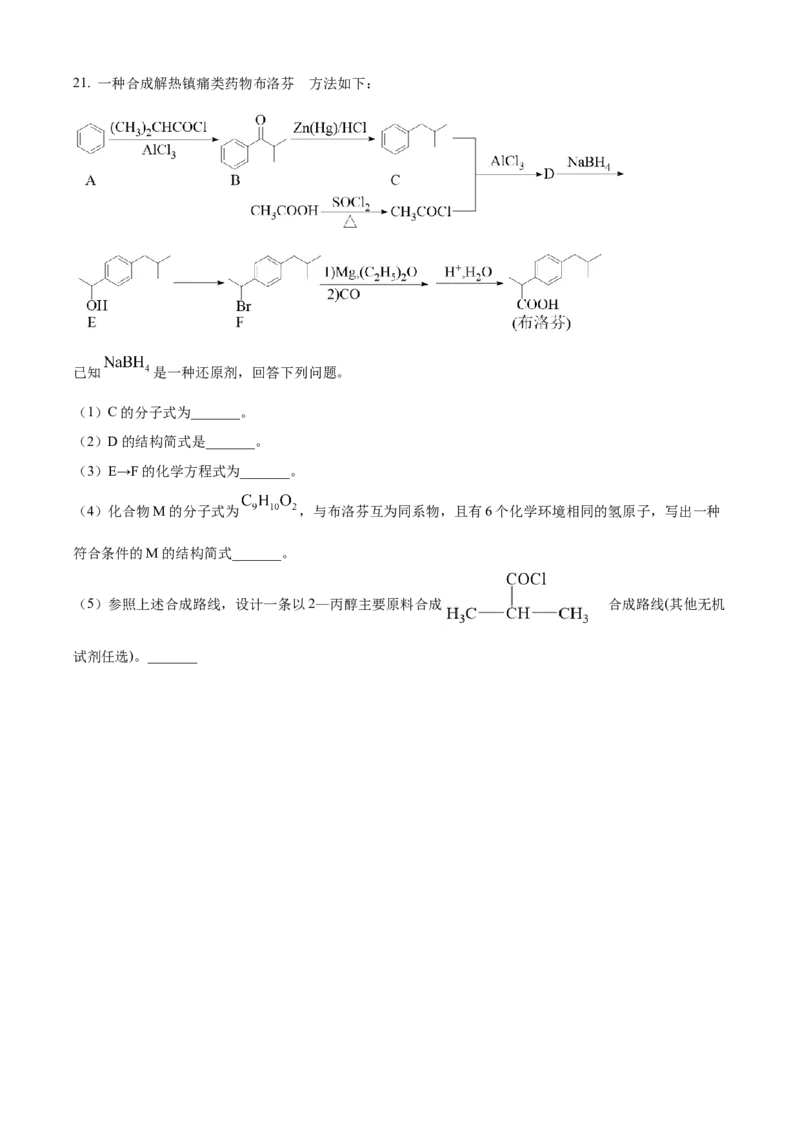
21. 一种合成解热镇痛类药物布洛芬 方法如下:
已知 是一种还原剂,回答下列问题。
(1)C的分子式为_______。
(2)D的结构简式是_______。
(3)E→F的化学方程式为_______。
(4)化合物M的分子式为 ,与布洛芬互为同系物,且有6个化学环境相同的氢原子,写出一种
符合条件的M的结构简式_______。
(5)参照上述合成路线,设计一条以2—丙醇主要原料合成 合成路线(其他无机
的
试剂任选)。_______珠海市教研联盟校 2023 届高三联考
化学试题
满分100分,考试用时75分钟。
可能用到的相对原子质量:H-1 C-12 O-16 Na-23
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小
题4分。在每小题给出的四个选项中,只有一项是符合题目要求的。
【1题答案】
【答案】C
【2题答案】
【答案】B
【3题答案】
【答案】A
【4题答案】
【答案】C
【5题答案】
【答案】B
【6题答案】
【答案】B
【7题答案】
【答案】C
【8题答案】
【答案】C
化学试题 第2页(共8页)
【9题答案】
【答案】D
【10题答案】
【答案】B
【11题答案】
【答案】A
【12题答案】
【答案】D【13题答案】
【答案】D
【14题答案】
【答案】A
【15题答案】
【答案】D
【16题答案】
【答案】B
二、非选择题:共56分。
【17题答案】
【答案】(1) ①. ②. 或
(2)Fe O (3)蒸发浓缩、冷却结晶
2 3
(4) ①. +2 ②.
【18题答案】
【答案】(1)H、C、N、O或H<C<N<O
(2) ①. 、 ②. 8
(3) ①. 四面体 ②. 氨是分子晶体,相邻分子靠分子间作用力相互吸引,铵盐是离子晶体,离子
间存在离子键,离子键的相互作用比分子间作用力强,所以熔沸点高
(4)N、O
【19题答案】
【答案】(1)分液漏斗
(2)
(3)饱和食盐水 (4) (5)B
(6)0.5
【20题答案】
【答案】(1)CHCHO+2Ag(NH )OH CHCOONH+2Ag↓+3NH+H O
3 3 2 3 4 3 2(2) ①. Ⅰ ②. Ⅲ ③. Ag+浓度小或氨水浓度大, 逆向移动,
Ag+浓度减小
(3) ①. OH- ②. 取棕黑色沉淀,加入稀硝酸溶液,产生无色气泡,气泡接触空气变为红棕色,
说明存在Ag
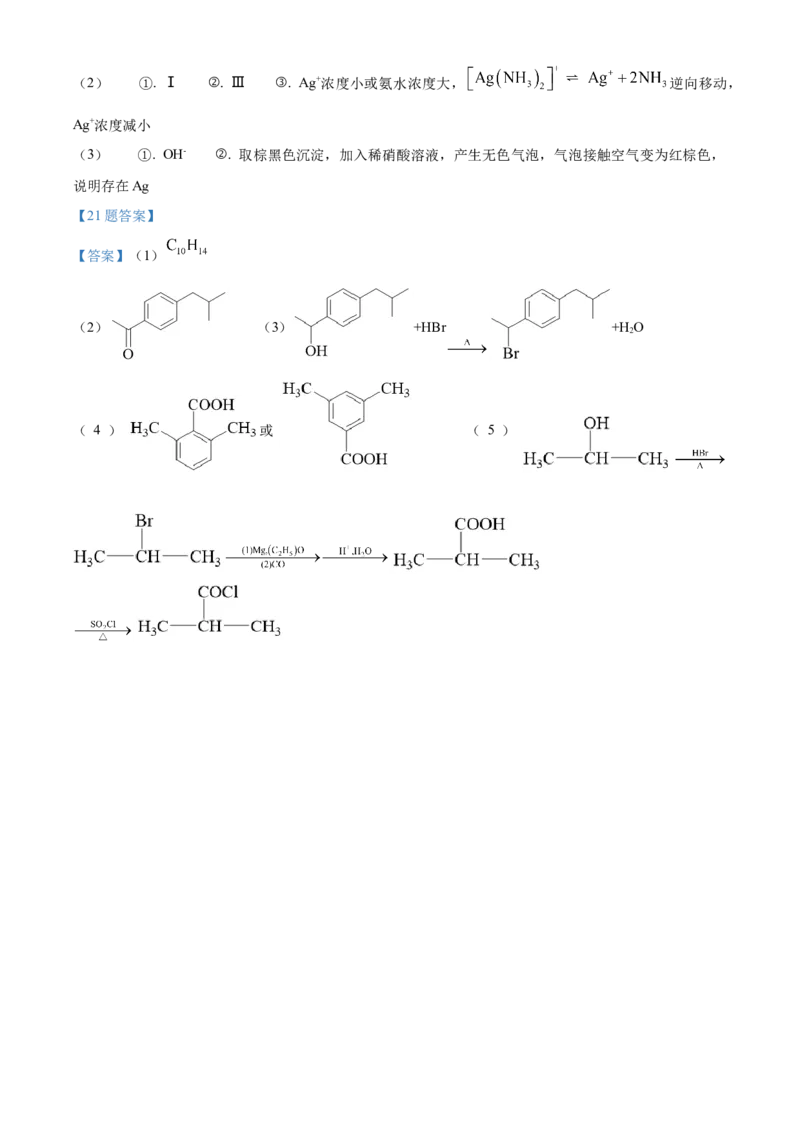
【21题答案】
【答案】(1)
(2) (3) +HBr +H O
2
( 4 ) 或 ( 5 )