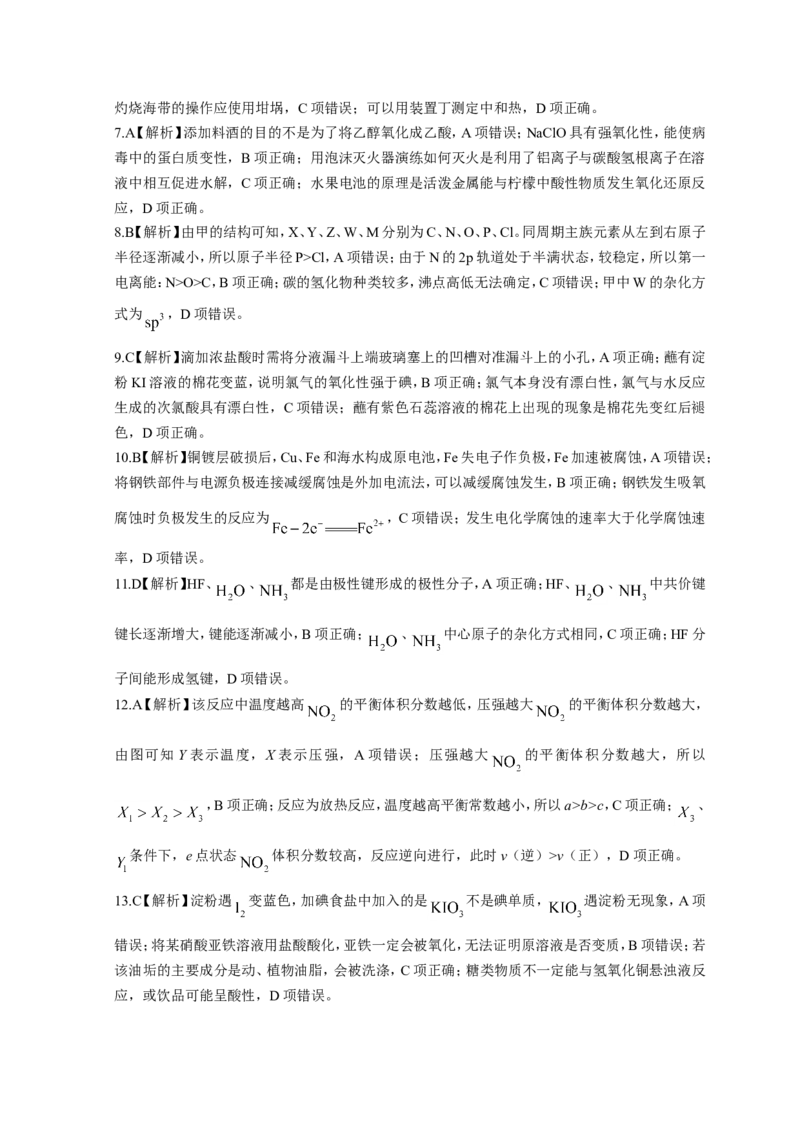文档内容
保密★启用前
2022-2023 学年光明区第一次高三模拟考试
化学试卷
2022.8
注意事项:
1.答题前,学生务必将自己的姓名、准考证号填写在相应的位置。
2.考试时间75分钟,满分100分。
3.全部答案在答题卡上完成,答在本试卷上无效。
可能用到的相对原子质量:H1C12 O 16K39Cu64 I 127
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小
题4分。在每小题给出的四个选项中,只有一项是符合题目要求的。
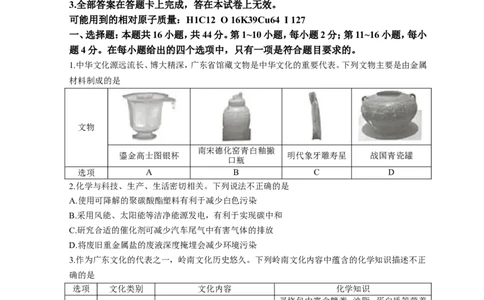
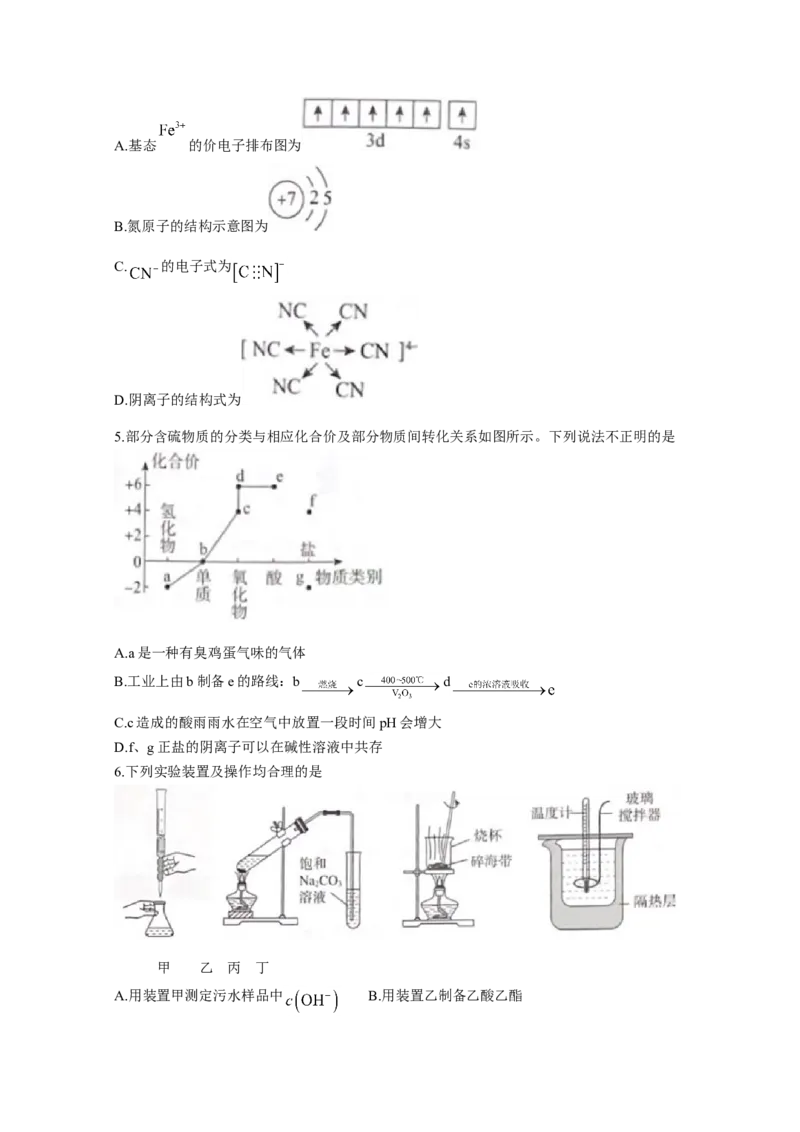
1.中华文化源远流长、博大精深,广东省馆藏文物是中华文化的重要代表。下列文物主要是由金属
材料制成的是
文物
南宋德化窑青白釉撇
鎏金高士图银杯 明代象牙雕寿星 战国青瓷罐
口瓶
选项 A B C D
2.化学与科技、生产、生活密切相关。下列说法不正确的是
A.使用可降解的聚碳酸酯塑料有利于减少白色污染
B.采用风能、太阳能等洁净能源发电,有利于实现碳中和
C.研究合适的催化剂可减少汽车尾气中有害气体的排放
D.将废旧重金属盐的废液深度掩埋会减少环境污染
3.作为广东文化的代表之一,岭南文化历史悠久。下列岭南文化内容中蕴含的化学知识描述不正
确的是
选项 文化类别 文化内容 化学知识
叉烧包中富含糖类、油脂、蛋白质等营养
A 饮食文化 早茶文化中的叉烧包
物质
婚礼流程中“敬茶”环节所
B 嫁娶文化 陶瓷茶具的主要成分为硅酸盐
用陶瓷茶具
C 服饰文化 “丝中贵族”香云纱 鉴别丝和棉花可以用灼烧的方法
烟花利用了“焰色试验”原理,该原理
D 节日文化 烟花舞龙
属于化学变化
4.亚铁氰化铁又名普鲁士蓝,化学式为 ,是一种配位化合物,可以用来上釉、用作
油画染料等。下列有关普鲁士蓝构成微粒的符号表征正确的是A.基态 的价电子排布图为
B.氮原子的结构示意图为
C. 的电子式为
D.阴离子的结构式为
5.部分含硫物质的分类与相应化合价及部分物质间转化关系如图所示。下列说法不正明的是
A.a是一种有臭鸡蛋气味的气体
B.工业上由b制备e的路线:b c d
C.c造成的酸雨雨水在空气中放置一段时间pH会增大
D.f、g正盐的阴离子可以在碱性溶液中共存
6.下列实验装置及操作均合理的是
甲 乙 丙 丁
A.用装置甲测定污水样品中 B.用装置乙制备乙酸乙酯C.用装置丙灼烧海带 D.用装置丁测定中和热
7.劳动成就梦想。下列劳动项目与所述的化学知识没有关联的是
选项 劳动项目 化学知识
A 厨房帮厨:炒菜时,时常会添加料酒 将乙醇氧化为可调昧的乙酸
工厂消毒:向各个办公场所喷洒“84”消毒 NaClO具有强氧化性,能使蛋白质变性
B
液 杀灭病毒
铝离子与碳酸氢根离子在溶液中相互促
C 社区服务:用泡沫灭火器演练如何灭火
进水解
自主探究:锌、铜和柠檬为原料制作水果电 锌能与柠檬中酸性物质发生氧化还原反
D
池 应
8.已知X、Y、Z、W、M为原子序数依次递增的短周期元素,其中X、Y、Z元素同周期,
Y与W元素同主族,它们可以形成一种重要化合物甲.其结构如图所示。下列说法正确的是
A.原子半径:M>W>Z B.第一电离能:Y>Z>X
C.氢化物的沸点:Z>Y>X D.甲中W的杂化方式为
9.某实验小组利用下图装置进行实验。下列说法不正确的是
A.滴加浓盐酸时需将分液漏斗上端玻璃塞上的凹槽对准漏斗上的小孔
B.蘸有淀粉KI溶液的棉花变蓝,说明氯气的氧化性强于碘
C.蘸有品红溶液的棉花褪色,说明氯气具有漂白性
D.蘸有紫色石蕊溶液的棉花上出现的现象是棉花先变红后褪色
10.我国有着丰富的海风资源,在海水中建立风电设备,防腐蚀是一个突出问题。下列说法正确的
是
A.钢铁构件表面的镀铜破损后依然会保护内部钢铁不被腐蚀B.可将钢铁构件与电源负极连接臧缓腐蚀发生
C.钢铁发生吸氧腐蚀时负极发生的反应为
D.海水中发生化学腐蚀的速率大于电化学腐蚀速率
11.下列关于HF、 、 的说法不正确的是
A.HF、 、 都是由极性键形成的极性分子
B.HF、 、 中共价键键长逐渐增大,键能逐渐减小
C. 、 的中心原子杂化方式相同
D. 比HF的沸点高是由于HF分子间不能形成氢键
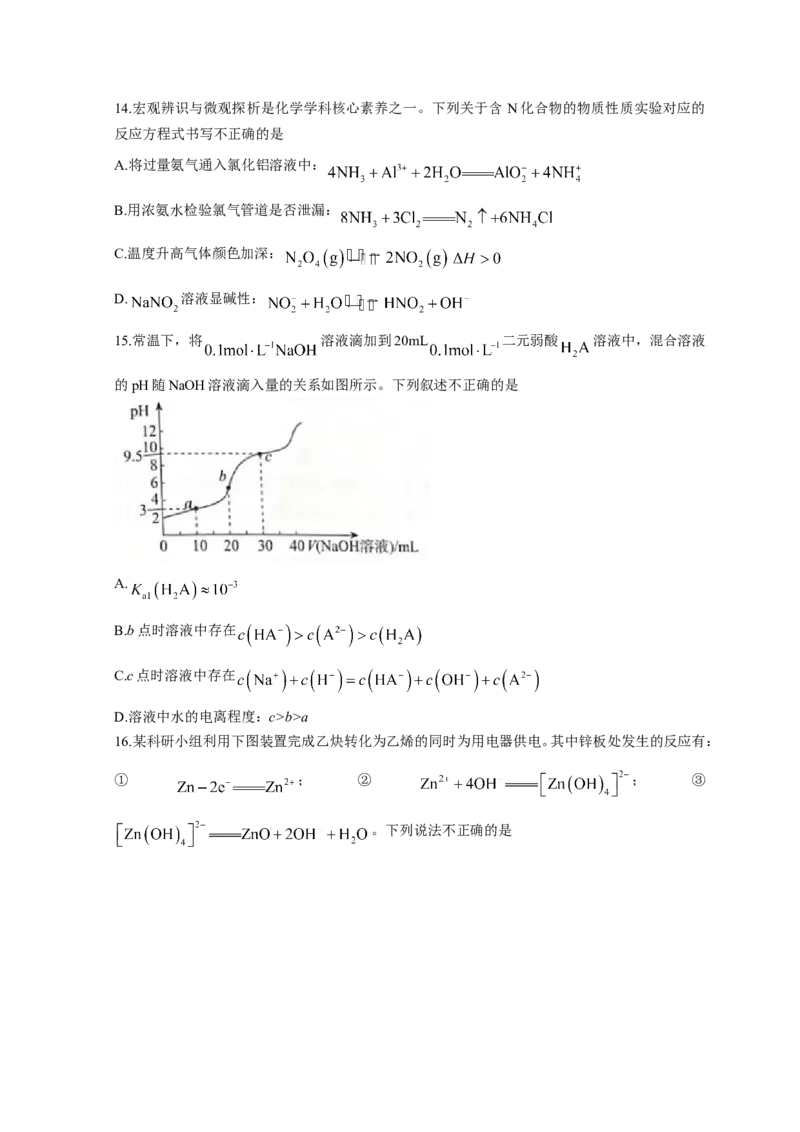
12.工业上制备硝酸过程中涉及反应: 。某
实验小组测得不同条件下反应平衡时 的体积分数变化如下图(图中X、Y分别代表温度或压
强),下列说法不正确的是
A.图中X表示温度,Y表示压强
B.
C.对应条件下的平衡常数:a>b>c
D. 、 条件下,e点对应状态时v(逆)>v(正)
13.由下列实验及现象推出的相应结论正确的是
选项 实验 现象 结论
A 向某食盐溶液中滴加淀粉溶液 溶液颜色不变 该食盐属于无碘盐
将某硝酸亚铁溶液用盐酸酸化,并 该硝酸亚铁溶液已变
B 溶液变红
滴加少量KSCN溶液 质
用热碳酸钠溶液清洗铁钉表面上油 该油垢的主要成分不
C 油垢无明显变化
垢 是动、植物油脂
将新制的氢氧化铜悬浊液与某饮品
D 未出现砖红色沉淀 该饮品不含糖
混合,加热14.宏观辨识与微观探析是化学学科核心素养之一。下列关于含 N化合物的物质性质实验对应的
反应方程式书写不正确的是
A.将过量氨气通入氯化铝溶液中:
B.用浓氨水检验氯气管道是否泄漏:
C.温度升高气体颜色加深:
D. 溶液显碱性:
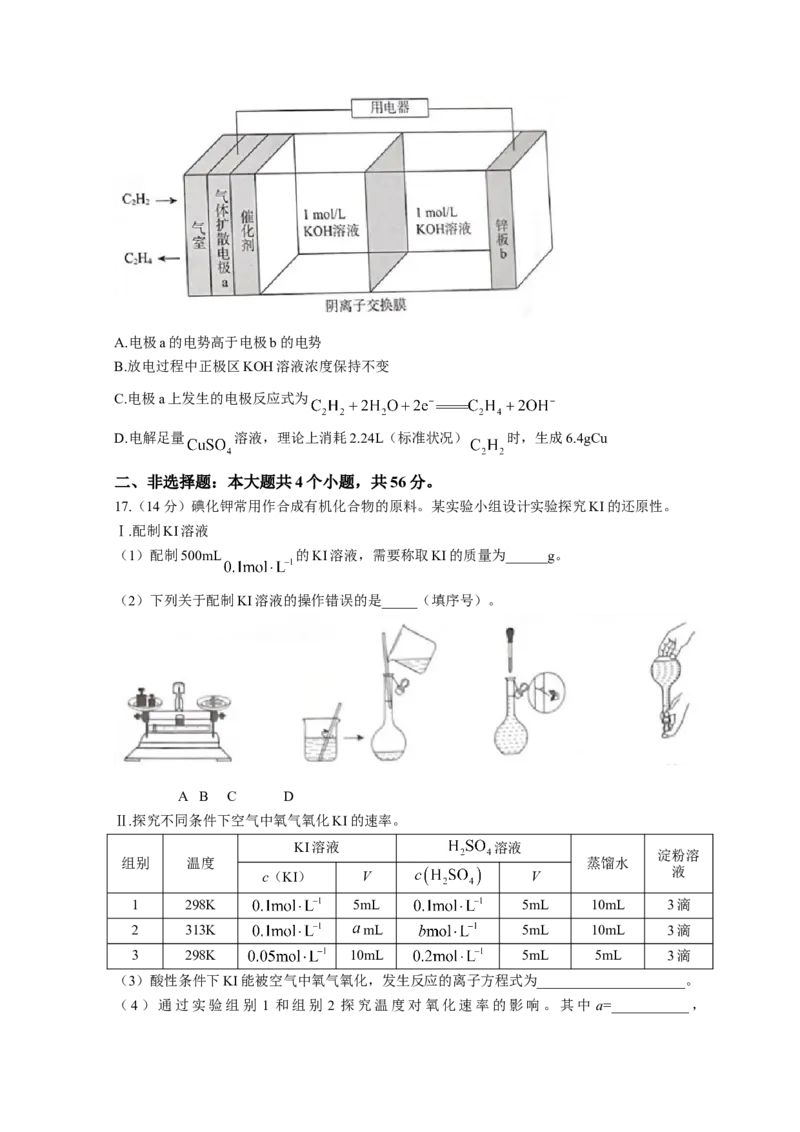
15.常温下,将 溶液滴加到20mL 二元弱酸 溶液中,混合溶液
的pH随NaOH溶液滴入量的关系如图所示。下列叙述不正确的是
A.
B.b点时溶液中存在
C.c点时溶液中存在
D.溶液中水的电离程度:c>b>a
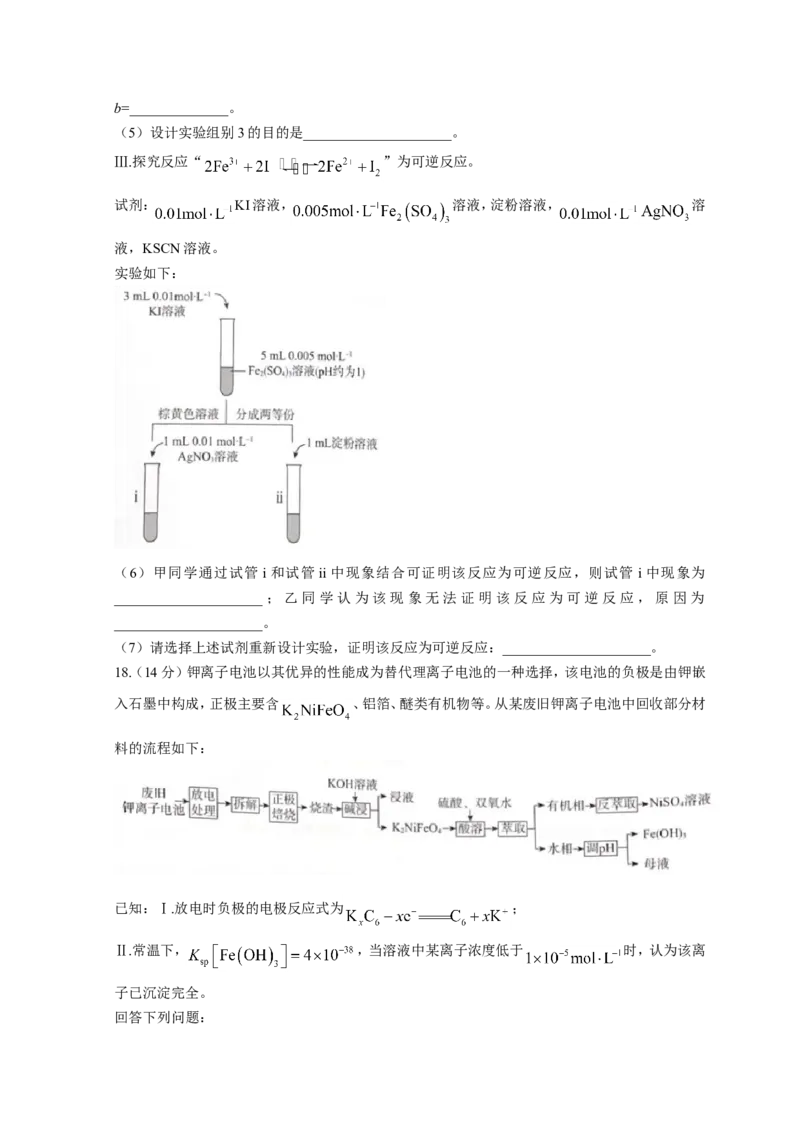
16.某科研小组利用下图装置完成乙炔转化为乙烯的同时为用电器供电。其中锌板处发生的反应有:
① ; ② ; ③
。下列说法不正确的是A.电极a的电势高于电极b的电势
B.放电过程中正极区KOH溶液浓度保持不变
C.电极a上发生的电极反应式为
D.电解足量 溶液,理论上消耗2.24L(标准状况) 时,生成6.4gCu
二、非选择题:本大题共4个小题,共56分。
17.(14分)碘化钾常用作合成有机化合物的原料。某实验小组设计实验探究KI的还原性。
Ⅰ.配制KI溶液
(1)配制500mL 的KI溶液,需要称取KI的质量为______g。
(2)下列关于配制KI溶液的操作错误的是_____(填序号)。
A B C D
Ⅱ.探究不同条件下空气中氧气氧化KI的速率。
KI溶液 溶液
淀粉溶
组别 温度 蒸馏水
液
c(KI) V V
1 298K 5mL 5mL 10mL 3滴
2 313K mL 5mL 10mL 3滴
3 298K 10mL 5mL 5mL 3滴
(3)酸性条件下KI能被空气中氧气氧化,发生反应的离子方程式为_____________________。
(4)通过实验组别 1 和组别 2 探究温度对氧化速率的影响。其中 a=___________,b=______________。
(5)设计实验组别3的目的是_____________________。
Ⅲ.探究反应“ ”为可逆反应。
试剂: KI溶液, 溶液,淀粉溶液, 溶
液,KSCN溶液。
实验如下:
(6)甲同学通过试管 i和试管ii中现象结合可证明该反应为可逆反应,则试管 i中现象为
_____________________;乙同学认为该现象无法证明该反应为可逆反应,原因为
_____________________。
(7)请选择上述试剂重新设计实验,证明该反应为可逆反应:_____________________。
18.(14分)钾离子电池以其优异的性能成为替代理离子电池的一种选择,该电池的负极是由钾嵌
入石墨中构成,正极主要含 、铝箔、醚类有机物等。从某废旧钾离子电池中回收部分材
料的流程如下:
已知:Ⅰ.放电时负极的电极反应式为 ;
Ⅱ.常温下, ,当溶液中某离子浓度低于 时,认为该离
子已沉淀完全。
回答下列问题:(1)废旧电池放电处理的原因为_____________________。
(2)“碱浸”时发生的化学反应方程式为_____________________。
(3)已 知 中的 铁为+3 价,则“酸 溶”时主要 反应的 离子方程式为
_____________________;该工序中温度需控制在40℃的原因为_____________________。
(4)若最终调节pH=3,则所得母液中的 ___________(填“已”或“未”)沉淀完全。
(5)实验室中从“反萃取”所得混合液中分离出 溶液的操作名称为______。
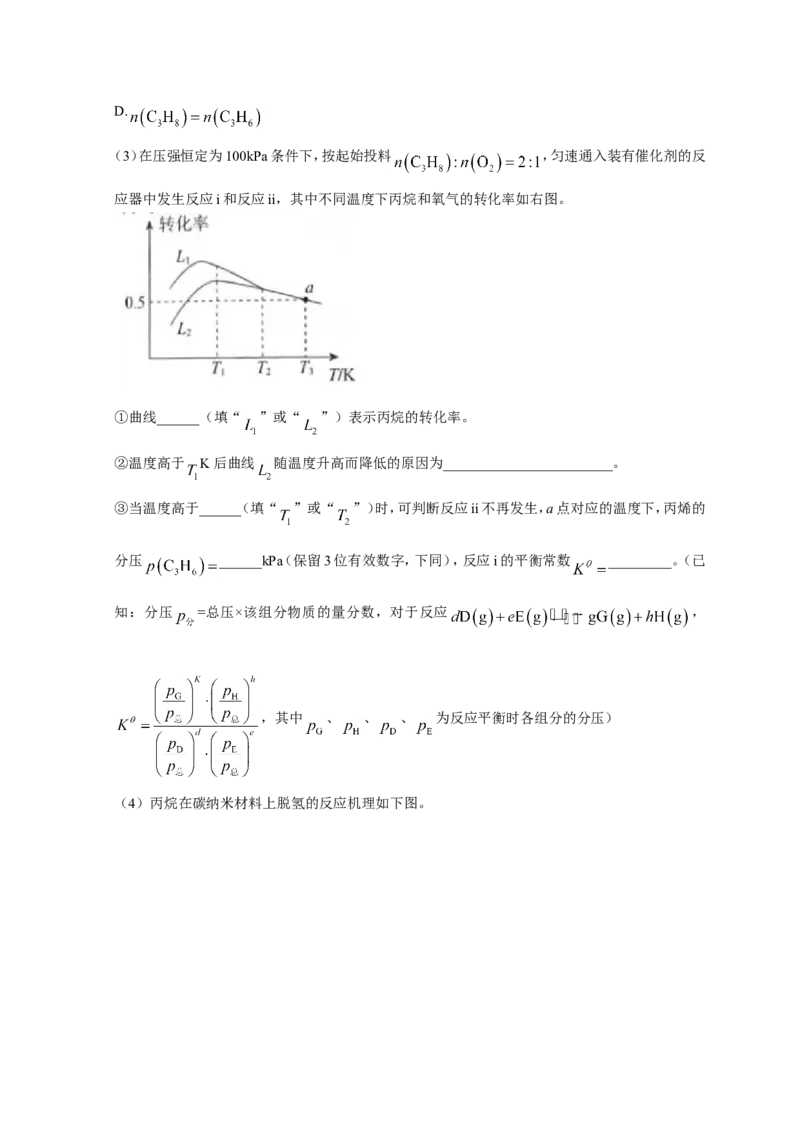
(6)废旧钾离子电池放电处理并拆解后,从负极得到石墨,其结构如下图。石墨两层之间最近碳原
子间距远大于层内最近碳原子间距的原因为__________________;设阿伏加德罗常数的值为 ,
则石墨晶体密度为______ (列式即可)。
19(. 14分)丙烯是重要的有机合成原料。由丙烷制备丙烯是近年来研究的热点,主要涉及如下反应。
反应i:
反应ii:
回答下列问题:
(1)反应: ______。
(2)在刚性绝热容器中发生反应i,下列能说明已达到平衡状态的有______(填标号)。
A.每断裂1molO=O键,同时生成4molO—H键
B.容器内温度不再变化
C.混合气体的密度不再变化D.
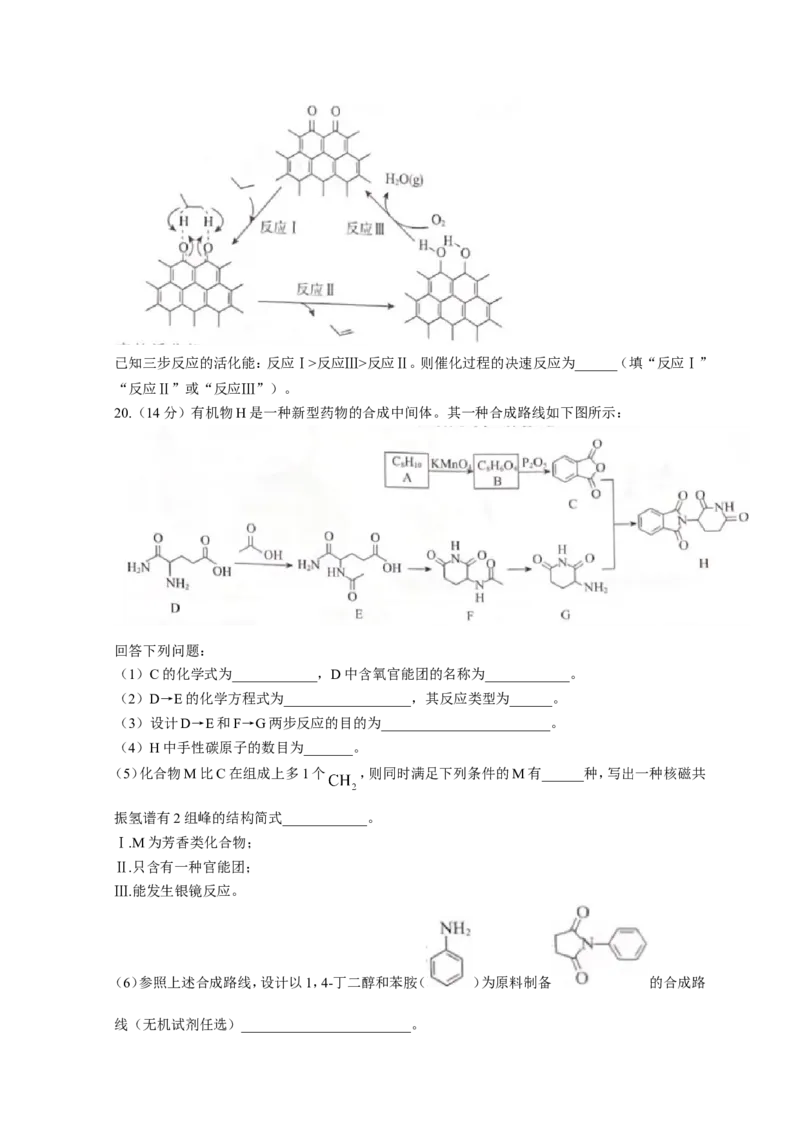
(3)在压强恒定为100kPa条件下,按起始投料 ,匀速通入装有催化剂的反
应器中发生反应i和反应ii,其中不同温度下丙烷和氧气的转化率如右图。
①曲线______(填“ ”或“ ”)表示丙烷的转化率。
②温度高于 K后曲线 随温度升高而降低的原因为________________________。
③当温度高于______(填“ ”或“ ”)时,可判断反应ii不再发生,a点对应的温度下,丙烯的
分压 ______kPa(保留3位有效数字,下同),反应i的平衡常数 _________。(已
知:分压 =总压×该组分物质的量分数,对于反应 ,
,其中 、 、 、 为反应平衡时各组分的分压)
(4)丙烷在碳纳米材料上脱氢的反应机理如下图。已知三步反应的活化能:反应Ⅰ>反应Ⅲ>反应Ⅱ。则催化过程的决速反应为______(填“反应Ⅰ”
“反应Ⅱ”或“反应Ⅲ”)。
20.(14分)有机物H是一种新型药物的合成中间体。其一种合成路线如下图所示:
回答下列问题:
(1)C的化学式为____________,D中含氧官能团的名称为____________。
(2)D→E的化学方程式为__________________,其反应类型为______。
(3)设计D→E和F→G两步反应的目的为________________________。
(4)H中手性碳原子的数目为_______。
(5)化合物M比C在组成上多1个 ,则同时满足下列条件的M有______种,写出一种核磁共
振氢谱有2组峰的结构简式____________。
Ⅰ.M为芳香类化合物;
Ⅱ.只含有一种官能团;
Ⅲ.能发生银镜反应。
(6)参照上述合成路线,设计以1,4-丁二醇和苯胺( )为原料制备 的合成路
线(无机试剂任选)________________________。2022-2023 学年光明区第一次高三模拟考试
化学试卷参考答案及评分标准
2022.8
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小
题4分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.A【解析】鎏金高士图银杯是由金属材料制成,A项正确。
2.D【解析】可降解的聚碳酸酯塑料在自然环境中快速降解成无害物质,使用这种塑料有利于减少
白色污染,A项正确;风能、太阳能等洁净能源发电,有利于实现碳中和,B项正确;合适的催化剂
可将汽车尾气中的NO和CO快速转化为无毒气体 和 ,减少有害气体的排放,C项正确;
重金属盐掩埋会造成环境污染,D项错误。
3.D【解析】叉烧包面皮中富含糖类,馅料肉中富含蛋白质和油脂,A项正确;陶瓷的主要成分为硅
酸盐,B项正确;可以用灼烧的方法鉴别丝和棉花,C项正确;焰色试验属于物理变化,D项错误。
4.B【解析】基态 的价电子排布图为 ,A项错误;氮原子结构示意图:
,B项正确; 的电子式为 ,C项错误;配位键箭头指向错误,D项错误。
5.C【解析】 是一种有臭鸡蛋气味的气体,A项正确;工业上由硫黄制备硫酸的路线为硫黄
,B项正确; 溶于水生成 ,会
被空气氧化生成硫酸,pH降低,C项错误; 与 在碱性溶液中不发生反应,D项正确。
6.D【解析】用装置甲测定污水样品中 时,应使用酸式滴定管盛放标准酸溶液,A项错误;
用装置乙制备乙酸乙酯时,导气管不应插人饱和 的液面以下,以免发生倒吸,B项错误;灼烧海带的操作应使用坩埚,C项错误;可以用装置丁测定中和热,D项正确。
7.A【解析】添加料酒的目的不是为了将乙醇氧化成乙酸,A项错误;NaClO具有强氧化性,能使病
毒中的蛋白质变性,B项正确;用泡沫灭火器演练如何灭火是利用了铝离子与碳酸氢根离子在溶
液中相互促进水解,C项正确;水果电池的原理是活泼金属能与柠檬中酸性物质发生氧化还原反
应,D项正确。
8.B【解析】由甲的结构可知,X、Y、Z、W、M分别为C、N、O、P、Cl。同周期主族元素从左到右原子
半径逐渐减小,所以原子半径P>Cl,A项错误;由于N的2p轨道处于半满状态,较稳定,所以第一
电离能:N>O>C,B项正确;碳的氢化物种类较多,沸点高低无法确定,C项错误;甲中W的杂化方
式为 ,D项错误。
9.C【解析】滴加浓盐酸时需将分液漏斗上端玻璃塞上的凹槽对准漏斗上的小孔,A项正确;蘸有淀
粉KI溶液的棉花变蓝,说明氯气的氧化性强于碘,B项正确;氯气本身没有漂白性,氯气与水反应
生成的次氯酸具有漂白性,C项错误;蘸有紫色石蕊溶液的棉花上出现的现象是棉花先变红后褪
色,D项正确。
10.B【解析】铜镀层破损后,Cu、Fe和海水构成原电池,Fe失电子作负极,Fe加速被腐蚀,A项错误;
将钢铁部件与电源负极连接减缓腐蚀是外加电流法,可以减缓腐蚀发生,B项正确;钢铁发生吸氧
腐蚀时负极发生的反应为 ,C项错误;发生电化学腐蚀的速率大于化学腐蚀速
率,D项错误。
11.D【解析】HF、 、 都是由极性键形成的极性分子,A项正确;HF、 、 中共价键
键长逐渐增大,键能逐渐减小,B项正确; 、 中心原子的杂化方式相同,C项正确;HF分
子间能形成氢键,D项错误。
12.A【解析】该反应中温度越高 的平衡体积分数越低,压强越大 的平衡体积分数越大,
由图可知Y表示温度,X表示压强,A项错误;压强越大 的平衡体积分数越大,所以
,B项正确;反应为放热反应,温度越高平衡常数越小,所以a>b>c,C项正确; 、
条件下,e点状态 体积分数较高,反应逆向进行,此时v(逆)>v(正),D项正确。
13.C【解析】淀粉遇 变蓝色,加碘食盐中加入的是 不是碘单质, 遇淀粉无现象,A项
错误;将某硝酸亚铁溶液用盐酸酸化,亚铁一定会被氧化,无法证明原溶液是否变质,B项错误;若
该油垢的主要成分是动、植物油脂,会被洗涤,C项正确;糖类物质不一定能与氢氧化铜悬浊液反
应,或饮品可能呈酸性,D项错误。14.A【解析】氨气无法溶解 沉淀,A项错误。
15.C【解析】a 点时 pH≈3,加入 10mLNaOH 溶液,此时 ,可知,
,A 项正确; ,由 c 点
pH=9.5可知 ,b点时溶液为NaHA,则 的电离程度大于水解程度,溶液中
, B 项 正 确 ; 由 电 荷 守 恒 可 知 , c 点 时 溶 液 中
,C项错误;a点为 与NaHA混合溶液,b
点为NaHA,c点为NaHA与 混合溶液,溶液中水的电离程度:c>b>a,D项正确。
16.B【解析】由图可知锌板为负极,所以电极a的电势高于电极b的电势,A项正确;放电过程中正
极区消耗水,导致 KOH 溶液浓度增大,B 项错误;电极 a 上发生的电极反应式为
,C 项正确;电解硫酸铜时,生成铜的电极反应为
,理论上消耗2.24L (标准状况),即0.1mol,对应电子转移0.2mol,可生
成铜6.4g,D项正确。
二、非选择题:本大题共4个小题,共56分。
17.(14分)(1)8.3(1分)(2)AC(2分)
(3) (2分)
(4)5(1分)0.1(1分)
(5)探究硫酸的浓度对氧化速率的影响(2分)
(6)产生黄色沉淀(1分)含 的溶液中加入 也能产生黄色沉淀(2分,答案合理即可)
(7)向5mL(过量) 溶液中加入3mL(少量) 溶液,再向
其中加入KSCN溶液,溶液变红,说明含有过量 的溶液中存在 ,即可证明该反应为可逆反
应(2分,合理答案即可)
【 解 析 】 ( 1 ) 配 制 500mL 的 KI 溶 液 , 需 要 称 取 KI 的 质 量。
(2)使用托盘天平时,应左盘盛放药品,右盘盛放砝码,A项错误,向容量瓶转移液体时,用玻璃棒
引流,玻璃棒下端位于刻度线以下,同时玻璃棒不能接触容量瓶瓶口,B项正确;定容时视线应平
视溶液凹液面,C项错误;定容完成后,盖好瓶塞,将容量瓶来回颠倒,将溶液摇匀,颠倒过程左手
食指抵住瓶塞,右手扶住容量瓶底部,D项正确。
( 3 ) 酸 性 条 件 下 KI 能 被 空 气 中 氧 气 氧 化 , 发 生 反 应 的 离 子 方 程 式 为
。
(4)根据控制单一变量的思想可知a=5,b=0.1。
(5)设计实验组别3的目的是为了与组别1对比,从而探究硫酸的浓度对氧化速率的影响。
(6)由题意可知实验i中现象为产生黄色沉淀;乙同学认为该现象无法证明该反应为可逆反应,原
因为含 的溶液中加入 也能产生黄色沉淀。
(7)向5mL 溶液中加入3mL(少量) 溶液,再向其中加
入KSCN溶液,溶液变红,说明含有过量 的溶液中存在 ,即可证明该反应为可逆反应【或向
溶液中加入5mL(过量) 溶液,再向其中加入
KSCN溶液,溶液变红,说明含有过量 的溶液中存在 ,即可证明该反应为可逆反应】
18(. 14分)(1)将正负极材料分离提高回收率并防止拆解过程和焙烧过程中发生危险(2分,答案
合理即可)
(2) (2分)
(3) (2分)低于40℃,反
应速率慢,高于40℃, 的分解速度太快(2分)
(4)未(1分)
(5)分液(1分)
(6)层内相邻碳原子采用共价键相连,层与层之间碳原子之间的作用力为范德华力(2分)
(2分)
【解析】(1)废旧电池放电处理的原因为通过放电将正负极材料分离,提高回收率并防止拆解过程和焙烧过程中漏电。
(2)“正极焙烧”除去正极材料中的醚类有机物,并将铝箔转化为 ,“碱浸"时发生的化学
反应方程式为 。
( 3 ) “ 酸 溶 ” 时 发 生 反 应 的 离 子 方 程 式 为
;该工序中温度需控制
在40℃的原因为低于40℃,反应速率慢,高于40℃, 的分解速度太快。
( 4 ) , 若 最 终 调 节 pH=3 , 则
, 所 得 母 液 中
,所以 尚未沉淀完全。
(5)实验室中从“反萃取”所得混合液中分离出 溶液的操作名称为分液。
(6)石墨两层之间最近碳原子间距远大于层内最近碳原子间距的原因为层内相邻碳原子采用共价
键 相 连 , 层 与 层 之 间 碳 原 子 之 间 的 作 用 力 为 范 德 华 力 ; 由 图 可 知 , 晶 胞 中
有个碳原子,则石墨的密度为 。
19.(14分)(1) (2分)
(2)B(2分)
(3)① (2分)
②放热反应,温度升高平衡逆向移动(2分)
③ (1分)28.6(2分)0.571(2分,若答 可酌情给分)
(4)反应I(1分)
【解析】(1)根据信息可知, 。
(2)在刚性绝热容器中发生反应i,反应时每断裂1molO=O键,必然同时生成4molO—H键,不能
说明反应达到平衡,A项错误;放热反应,容器内温度不再发生变化,可以说明反应达到平衡,B项
正确;反应物与生成物均为气体,混合气体密度不再变化,不能说明反应达到平衡,C项错误;时不能说明反应达到平衡,D项错误。
(3)①通过两反应方程式系数可知,丙烷转化率低于氧气,所以曲线 表示丙烷的转化率。
②由于 K后反应达到平衡,两个反应均为放热反应,温度升高平衡逆向移动。
③当温度达到 时, 与丙烷的转化率相同,且起始投料比 ,可以判断
温度达到 后反应ii不再发生, K时只发生反应i。设 的起始量为2, 的起始量为1,
K下,根据图中数据可知:
起始量 2 1 0 0
反应量 1 0.5 1 1
剩余量 1 0.5 1 1
丙 烯 的 分 压 , 反 应 i 的 平 衡 常 数
。
(4)活化能越大,速率越慢,慢反应为决速反应,所以催化过程的决速反应为反应I。
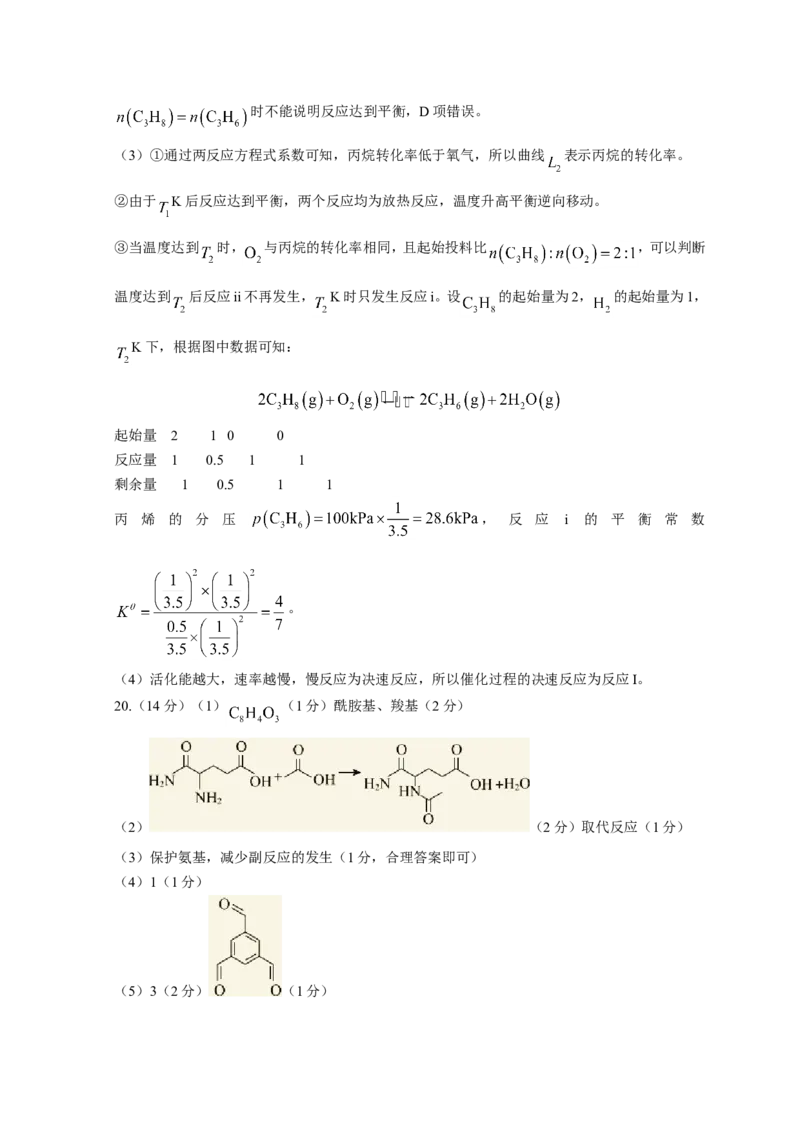
20.(14分)(1) (1分)酰胺基、羧基(2分)
(2) (2分)取代反应(1分)
(3)保护氨基,减少副反应的发生(1分,合理答案即可)
(4)1(1分)
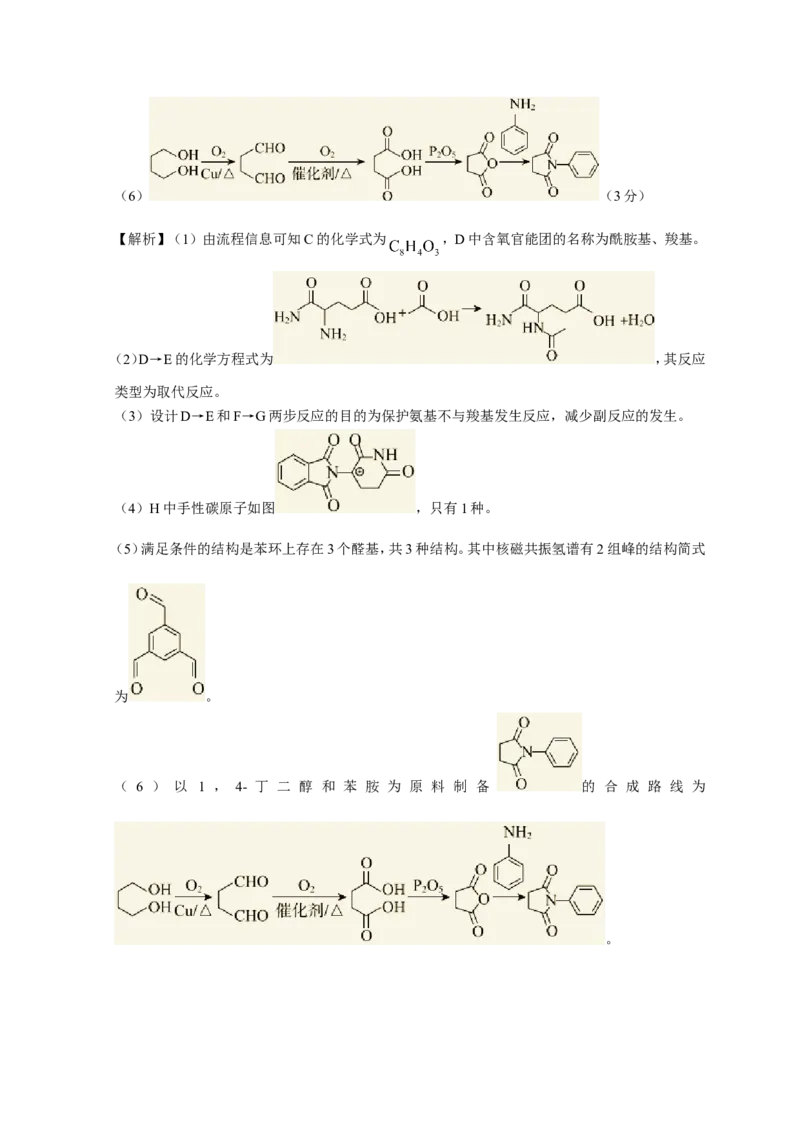
(5)3(2分) (1分)(6) (3分)
【解析】(1)由流程信息可知C的化学式为 ,D中含氧官能团的名称为酰胺基、羧基。
(2)D→E的化学方程式为 ,其反应
类型为取代反应。
(3)设计D→E和F→G两步反应的目的为保护氨基不与羧基发生反应,减少副反应的发生。
(4)H中手性碳原子如图 ,只有1种。
(5)满足条件的结构是苯环上存在3个醛基,共3种结构。其中核磁共振氢谱有2组峰的结构简式
为 。
( 6 ) 以 1 , 4- 丁 二 醇 和 苯 胺 为 原 料 制 备 的 合 成 路 线 为
。