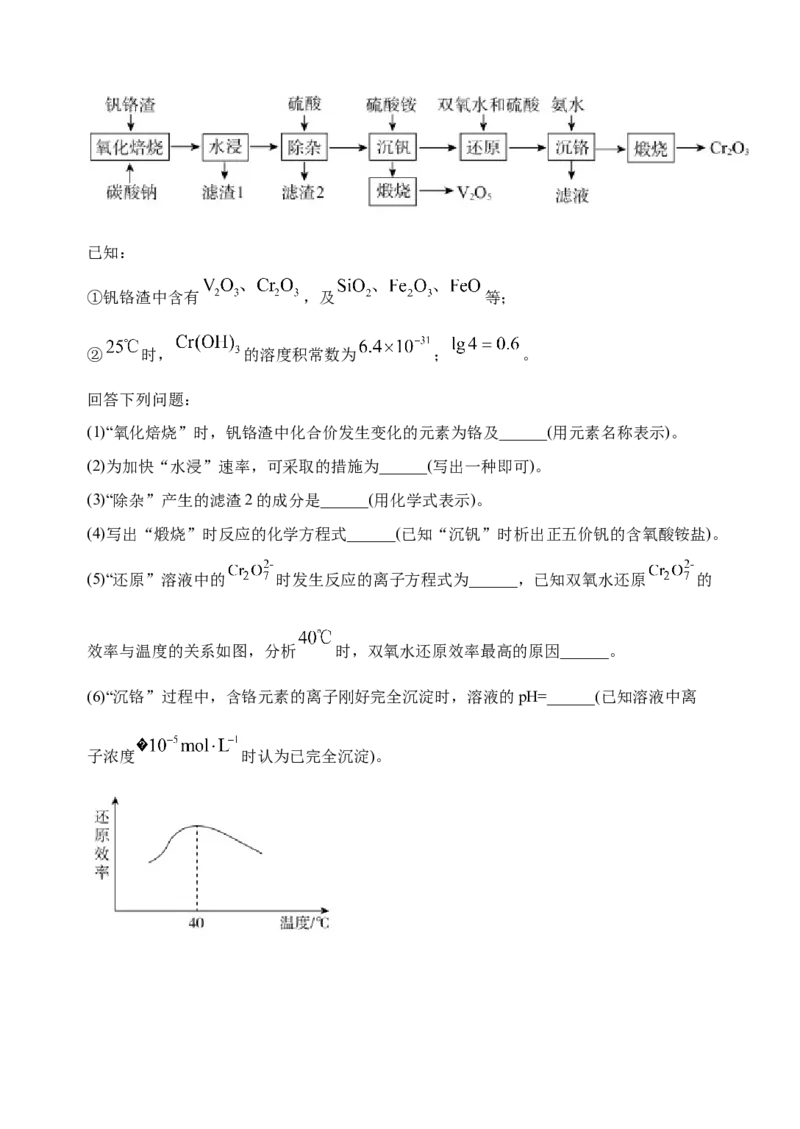
文档内容
微专题18 金属及其化合物制备流程(V)
钒:元素符号V,原子序数23,原子量50.94,外围电子排布3d34s2,位于第四周期VB族。
一、物理性质:
银白色金属,有良好的延展性。密度 5.96克/厘米3,熔点 1890±10℃,沸点3380℃,主
要化合价+2、+3、+4、+5。
二、化学性质:
常温下化学性质不活动,有较强的耐腐蚀性,不与空气、水反应,也不和非氧化性酸及
强碱溶液反应。能溶于氢氟酸、硝酸和王水。高温条件下,钒和氧、氮、碳能反应。
三、用途:
主要用于制合金钠和催化剂。1830年瑞典的塞夫斯唐姆发现了钒。主要矿物有钒酸钾铀
矿、铅钒矿等。用钙还原五氧化二钒或用镁还原三氯化钒制得。
四、五氧化二钒提取工艺
传统工艺
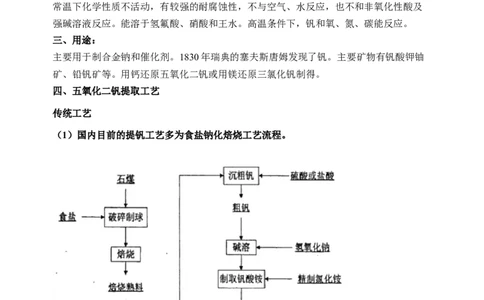
(1)国内目前的提钒工艺多为食盐钠化焙烧工艺流程。
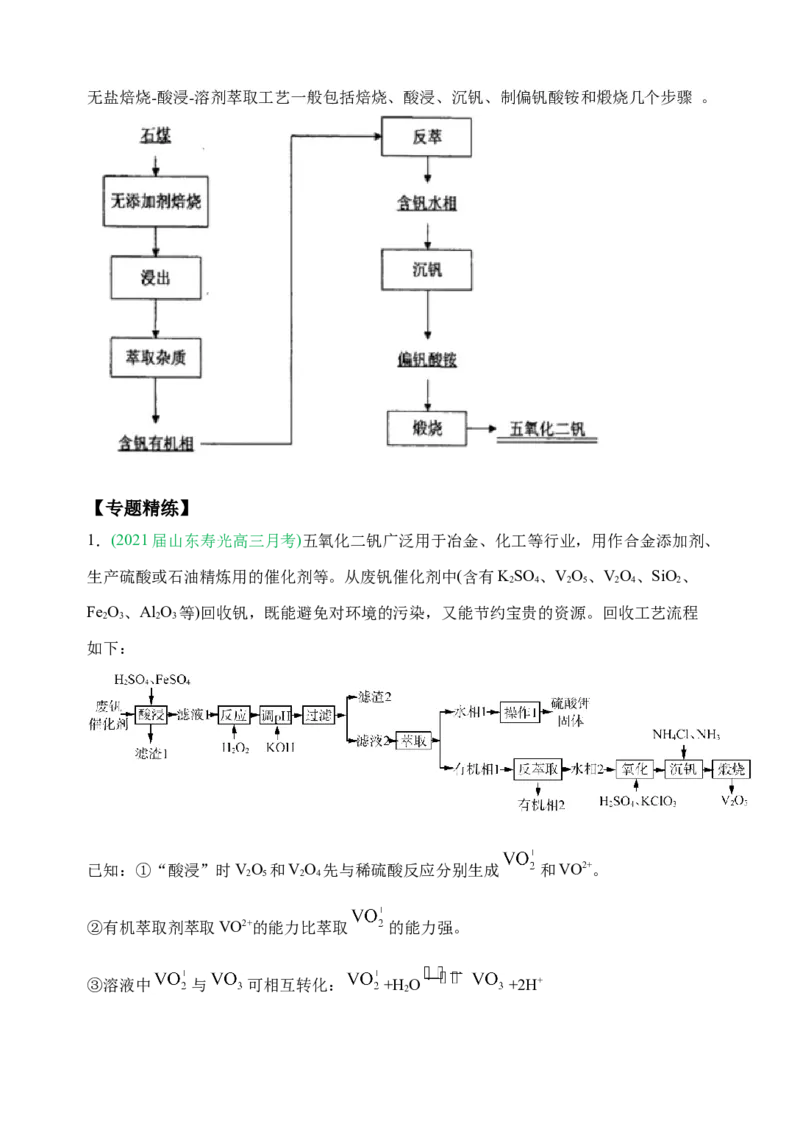
(2)无盐焙烧-酸浸-溶剂萃取工艺:无盐焙烧-酸浸-溶剂萃取工艺一般包括焙烧、酸浸、沉钒、制偏钒酸铵和煅烧几个步骤 。
【专题精练】
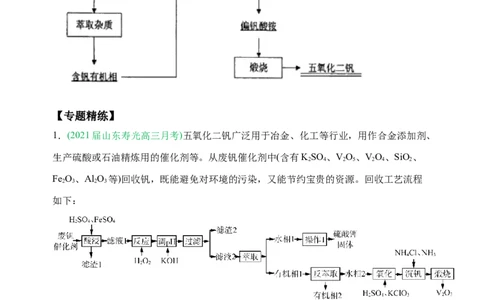
1.(2021届山东寿光高三月考)五氧化二钒广泛用于冶金、化工等行业,用作合金添加剂、
生产硫酸或石油精炼用的催化剂等。从废钒催化剂中(含有KSO 、VO、VO、SiO、
2 4 2 5 2 4 2
Fe O、Al O 等)回收钒,既能避免对环境的污染,又能节约宝贵的资源。回收工艺流程
2 3 2 3
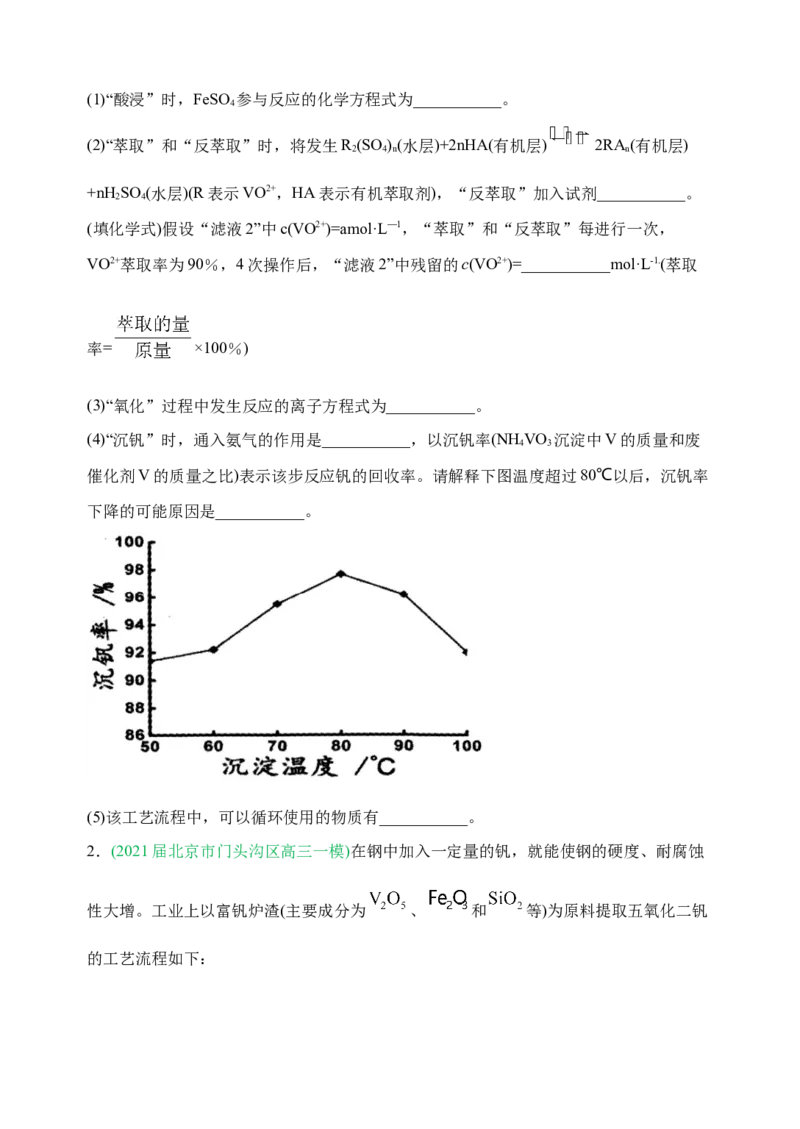
如下:
已知:①“酸浸”时VO 和VO 先与稀硫酸反应分别生成 和VO2+。
2 5 2 4
②有机萃取剂萃取VO2+的能力比萃取 的能力强。
③溶液中 与 可相互转化: +H O +2H+
2(1)“酸浸”时,FeSO 参与反应的化学方程式为___________。
4
(2)“萃取”和“反萃取”时,将发生R (SO )(水层)+2nHA(有机层) 2RA(有机层)
2 4 n n
+nH SO (水层)(R表示VO2+,HA表示有机萃取剂),“反萃取”加入试剂___________。
2 4
(填化学式)假设“滤液2”中c(VO2+)=amol·L—1,“萃取”和“反萃取”每进行一次,
VO2+萃取率为90%,4次操作后,“滤液2”中残留的c(VO2+)=___________mol·L-1.(萃取
率= ×100%)
(3)“氧化”过程中发生反应的离子方程式为___________。
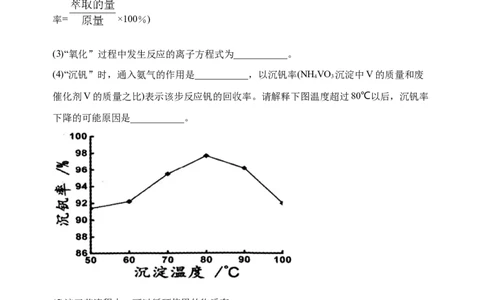
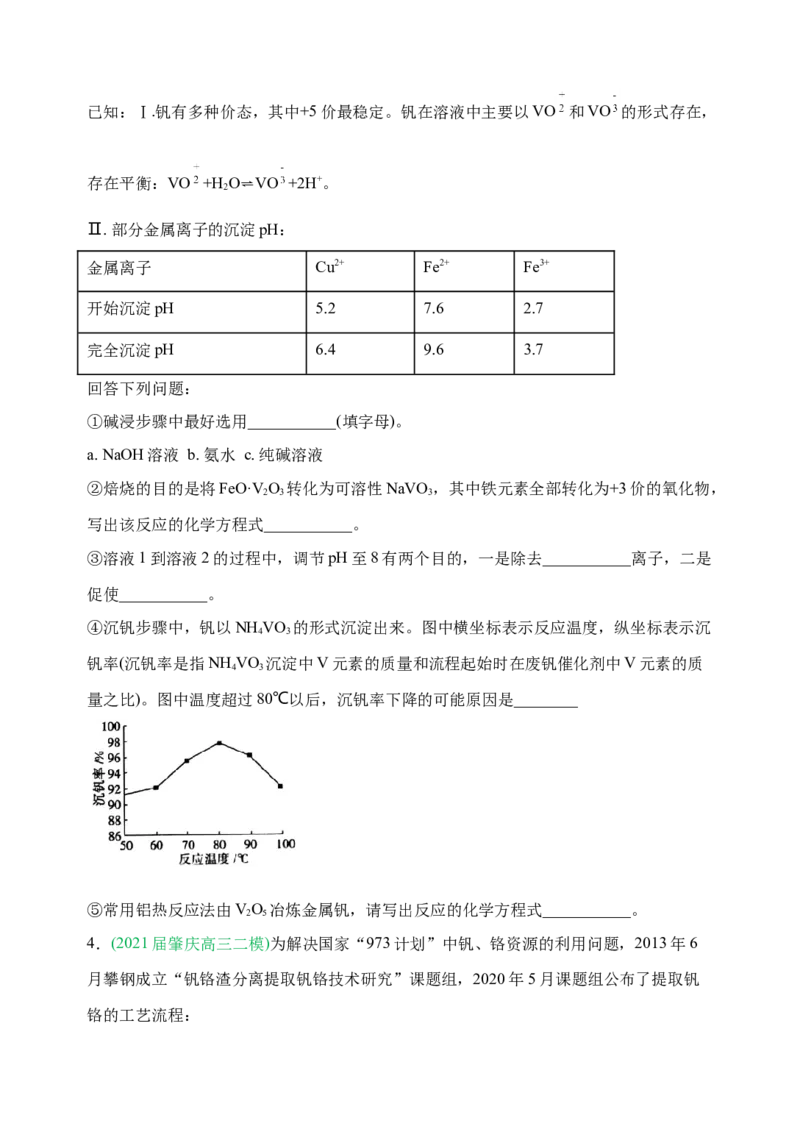
(4)“沉钒”时,通入氨气的作用是___________,以沉钒率(NH VO 沉淀中V的质量和废
4 3
催化剂V的质量之比)表示该步反应钒的回收率。请解释下图温度超过80℃以后,沉钒率
下降的可能原因是___________。
(5)该工艺流程中,可以循环使用的物质有___________。
2.(2021届北京市门头沟区高三一模)在钢中加入一定量的钒,就能使钢的硬度、耐腐蚀
性大增。工业上以富钒炉渣(主要成分为 、 和 等)为原料提取五氧化二钒
的工艺流程如下:(1)在第—步操作焙烧过程中 转化为可溶性 ,该反应的化学方程式为
___________。
(2)焙烧炉中可用 代替NaCl与富钒炉渣焙烧制得偏钒酸钠。用 代替
NaCl的优点是___________。
(3)以上流程中应用过滤操作的有___________,在第三步操作后加入氯化铵得到偏钒酸铵
,为使钒元素的沉降率达到98%,要加入较多的 ,从平衡角度分析
原因___________。
(4)产品纯度测定:将mg产品溶于足量稀硫酸配成 溶液。取20.00mL
该溶液于锥形瓶中,用 标准溶液进行滴定,经过三次滴定,达到滴定
终点时平均消耗标准溶液的体积为20.00mL。
资料:钒的盐类的颜色五光十色,有绿的、红的、黑的、黄的,绿的碧如翡翠,黑的犹
如浓墨。这些色彩缤纷的钒的化合物,常被制成鲜艳的颜料。如: 溶液为黄色,
溶液为蓝色,而五氧化二钒则是红色的。
①完成下列滴定过程的离子方程式。
,_____________
②该滴定实验不需要另外加入指示剂,达到滴定终点的现象是___________。
③产品的纯度为___________。(用质量分数表示)已知相对分子质量: ;
。
3.(2021届福建高三12月联考)钒(V)为过渡元素,可形成多价态化合物。
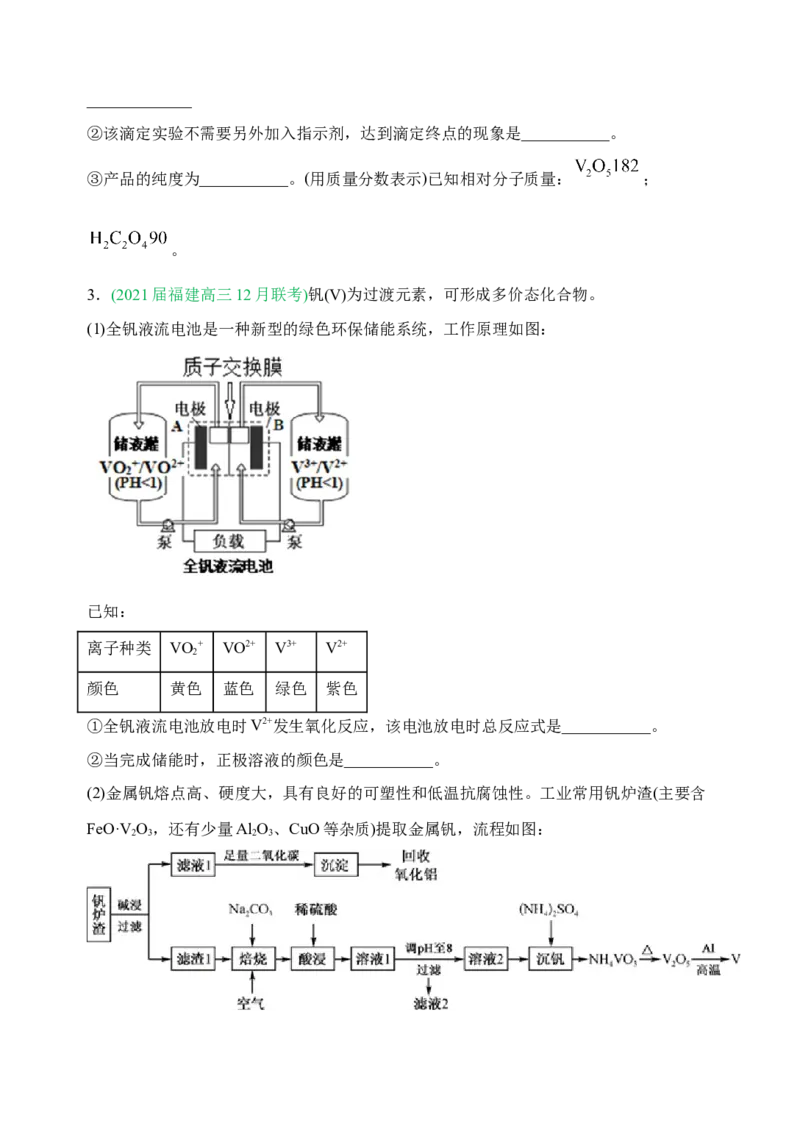
(1)全钒液流电池是一种新型的绿色环保储能系统,工作原理如图:
已知:
离子种类 VO + VO2+ V3+ V2+
2
颜色 黄色 蓝色 绿色 紫色
①全钒液流电池放电时V2+发生氧化反应,该电池放电时总反应式是___________。
②当完成储能时,正极溶液的颜色是___________。
(2)金属钒熔点高、硬度大,具有良好的可塑性和低温抗腐蚀性。工业常用钒炉渣(主要含
FeO·V O,还有少量Al O、CuO等杂质)提取金属钒,流程如图:
2 3 2 3已知:Ⅰ.钒有多种价态,其中+5价最稳定。钒在溶液中主要以VO 和VO 的形式存在,
存在平衡:VO +H
2
O⇌VO +2H+。
Ⅱ. 部分金属离子的沉淀pH:
金属离子 Cu2+ Fe2+ Fe3+
开始沉淀pH 5.2 7.6 2.7
完全沉淀pH 6.4 9.6 3.7
回答下列问题:
①碱浸步骤中最好选用___________(填字母)。
a. NaOH溶液 b. 氨水 c. 纯碱溶液
②焙烧的目的是将FeO·V O 转化为可溶性NaVO ,其中铁元素全部转化为+3价的氧化物,
2 3 3
写出该反应的化学方程式___________。
③溶液1到溶液2的过程中,调节pH至8有两个目的,一是除去___________离子,二是
促使___________。
④沉钒步骤中,钒以NH VO 的形式沉淀出来。图中横坐标表示反应温度,纵坐标表示沉
4 3
钒率(沉钒率是指NH VO 沉淀中V元素的质量和流程起始时在废钒催化剂中V元素的质
4 3
量之比)。图中温度超过80℃以后,沉钒率下降的可能原因是________
⑤常用铝热反应法由VO 冶炼金属钒,请写出反应的化学方程式___________。
2 5
4.(2021届肇庆高三二模)为解决国家“973计划”中钒、铬资源的利用问题,2013年6
月攀钢成立“钒铬渣分离提取钒铬技术研究”课题组,2020年5月课题组公布了提取钒
铬的工艺流程:已知:
①钒铬渣中含有 ,及 等;
② 时, 的溶度积常数为 ; 。
回答下列问题:
(1)“氧化焙烧”时,钒铬渣中化合价发生变化的元素为铬及______(用元素名称表示)。
(2)为加快“水浸”速率,可采取的措施为______(写出一种即可)。
(3)“除杂”产生的滤渣2的成分是______(用化学式表示)。
(4)写出“煅烧”时反应的化学方程式______(已知“沉钒”时析出正五价钒的含氧酸铵盐)。
(5)“还原”溶液中的 时发生反应的离子方程式为______,已知双氧水还原 的
效率与温度的关系如图,分析 时,双氧水还原效率最高的原因______。
(6)“沉铬”过程中,含铬元素的离子刚好完全沉淀时,溶液的pH=______(已知溶液中离
子浓度 时认为已完全沉淀)。【五氧化二钒】化学式VO。黄色正交晶体。微溶于水,能溶于酸或碱溶液。在有机合
2 5
成和硫酸工业上用它做催化剂。灼烧钒酸铵制得。