文档内容
微专题突破4 物质结构与性质二
一、选择题
1.(2024·海南省海口市摸底)氧和硫是元素周期表中第ⅥA族元素。下列说法正确的是
A.电负性:O<S B.沸点:HO<HS
2 2
C.SO 是极性分子 D.SO2-空间构型为平面三角形
2 3
2.(2024·广西北海市一模)Fe(NH )[Fe(CN)](俗称铵铁蓝)是一种蓝色的无机颜料。下列有关该
4 6
物质的说法错误的是
A.电负性:N>C>H
B.铵铁蓝中铁元素有两种化合价
C.NH中H-N-H的键角比NH 中的H-N-H的键角大
3
D.铵铁蓝中的配体是 ,该配体中σ键与π键的数目之比是2∶1
3.(2025·江苏苏州市开学考)[Cu(NH )]SO 常用作杀虫剂、媒染剂。下列说法正确的是
3 4 4
A.原子半径:r(N)>r(O)>r(S)
B.沸点:HS>HO>NH
2 2 3
C.第一电离能:I(N)>I(O)>I(S)
1 1 1
D.电负性:χ(N)>χ(O)>χ(Cu)
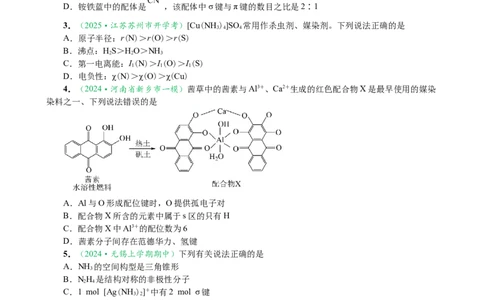
4.(2024·河南省新乡市一模)茜草中的茜素与Al3+、Ca2+生成的红色配合物X是最早使用的媒染
染料之一、下列说法错误的是
A.Al与O形成配位键时,O提供孤电子对
B.配合物X所含的元素中属于s区的只有H
C.配合物X中Al3+的配位数为6
D.茜素分子间存在范德华力、氢键
5.(2024·无锡上学期期中)下列有关说法正确的是
A.NH 的空间构型是三角锥形
3
B.NH 是结构对称的非极性分子
2 4
C.1 mol [Ag(NH)]+中有2 mol σ键
3 2
D.[Ag(NH)]+和NH 中N-H键角相等
3 2 3
6.(2025·连云港市上学期期中)摩尔盐[(NH )Fe(SO )•6H O]可以用于配制标准溶液。下列说
4 2 4 2 2
法正确的是
A.半径:r(O2-)>r(S2-)
B.第一电离能:I(N)>I(O)
1 1
C.电负性:χ(Fe)>χ(H)
D.热稳定性:HS>HO
2 2
7.(2024·苏锡常镇二模)周期表中ⅦA族元素及其化合物应用广泛。电解KHF 与HF的混合物时,
2
HF2-转化为F ;加热NaCl与浓HSO 的混合物,可制得HCl。氯还可形成HClO 、HClO 、HClO 等多
2 2 4 2 3 4
种含氧酸。ClO 是Al级高效安全灭菌消毒剂;Cl 与CH 反应可制备有机溶剂CCl。在照相底片的定影过
2 2 4 4
程中,底片上未曝光的AgBr浸入NaSO 溶液转变成[Ag(SO)]3-而溶解。氯化碘(ICl)性质与卤素单质
2 2 3 2 3 2微专题突破4 物质结构与性质二
相似,常用作分析化学试剂。下列说法正确的是
A.基态F原子的核外电子排布式为2s22p5
B.KHF 中既含有离子键,又含有共价键
2
C.ClO2-、ClO -和ClO -中O-Cl-O键角依次逐渐减小
3 4
D.SO2-(结构如图 )中两个S原子均可作配位原子
2 3
8.(2024·江苏盐城市高三期中)元素镓( Ga)、锗( Ge)、砷( As)位于周期表中第四周期。下列
31 32 33
说法不正确的是
A.原子半径:r(Ga)>r(Ge)>r(As)
B.电负性:χ(Ga)<χ(Ge)<χ(As)
C.Ge、Ga、As都具有半导体性能
D.第一电离能:I(Ga)<I(As)<I(Ge)
1 1 1
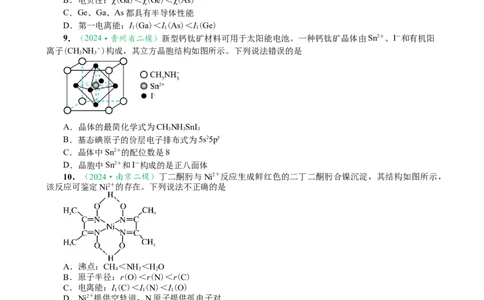
9.(2024·贵州省二模)新型钙钛矿材料可用于太阳能电池。一种钙钛矿晶体由Sn2+、I-和有机阳
离子(CHNH +)构成,其立方晶胞结构如图所示。下列说法错误的是
3 3
A.晶体的最简化学式为CHNH SnI
3 3 3
B.基态碘原子的价层电子排布式为5s25p5
C.晶体中Sn2+的配位数是8
D.晶胞中Sn2+和I-构成的是正八面体
10.(2024·南京二模)丁二酮肟与Ni2+反应生成鲜红色的二丁二酮肟合镍沉淀,其结构如图所示,
该反应可鉴定Ni2+的存在。下列说法不正确的是
A.沸点:CH<NH <HO
4 3 2
B.原子半径:r(O)<r(N)<r(C)
C.电离能:I(C)<I(N)<I(O)
1 1 1
D.Ni2+提供空轨道,N原子提供孤电子对
11.(2025·江苏苏州市开学考)VA族元素及其化合物应用广泛。NH 催化氧化生成NO,NO继续
3
被氧化为NO ,将NO 通入水中可制得HNO;肼(NH)常温下为液态,燃烧热为(642 kJ·mol-1),产
2 2 3 2 4
物无污染,常用作火箭燃料:白磷(P)为正四面体结构,常用来制烟雾弹、燃烧弹;雄黄(As S)具有解
4 4 4
毒、杀虫功效,燃烧后生成砒霜(As O)和一种具有刺激性气味的气体;锑是一种银白色金属,其氧化物
2 3
Sb O 可用于制造颜料,铅锑合金可用作铅蓄电池的电极材料。
2 3
下列说法正确的是
A.NH 分子中既有极性键,又有非极性键
2 4
B.NH 中键角比P 中键角小
3 4
C.1 mol白磷含有4 mol P-P键
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找D.As基态原子核外电子排布式为[Ar]4s24p3
12.(2023·苏州上学期期末)含锂物质在能源方面有重要应用。锂在氧气中燃烧与Mg相似,其燃
烧热为299 kJ·mol-1。锂与氮气反应得到的LiN可用作储氨材料。锂-空气电池是一种二次电池,放电
3
时主要产物为LiO ,充电时阴极产物易形成固态枝晶,导致电池短路。目前应用广泛的是锂离子电池,
2 2
例如,磷酸铁锂电池充电时锂离子由LiFePO 电极迁移至石墨电极形成LiC,LiFePO 的前体FePO 可由
4 x 4 4
NH HPO 、FeSO 、HO 在pH=12的条件下反应制得。下列物质结构与性质或物质性质与用途具有对应
4 2 4 4 2 2
关系的是
A.Mg有强还原性,可用于钢铁的电化学防护
B.LiOH可溶于水,可用作宇宙飞船中CO 吸收剂
2
C.石墨晶体层间存在范德华力,石墨易导电
D.HO 是极性分子,HO 有强氧化性
2 2 2 2
13.(2024·南通市如皋2月)NH
3
中的一个H原子被-OH取代可形成羟胺(NH
2
OH),被-NH
2
取代
可形成肼(NH),-OH吸电子能力比-NH 强。下列说法正确的是
2 4 2
A.NH 的键角比HO小
3 2
B.1 mol [Cu(NH )]2+中含12 mol σ键
3 4
C.NH OH难溶于水
2
D.NH OH中N结合H+的能力比NH 弱
2 2 4
的
14.(2025·连云港市上学期期中)铜及其重要化合物在生产中有着重要 应用。Cu在O 存在下能
2
与氨水反应生成[Cu(NH )]2+。单质铜作催化剂可以将CHCHOH氧化为CHCHO。Cu O是一种良好的
3 4 3 2 3 2
离子型半导体,加入稀硫酸中,溶液变蓝色并有紫红色固体产生。Cu S高温下可以被O 氧化为Cu和
2 2
SO ,将制得的粗铜通过电解精炼得铜。CuCl的盐酸溶液能吸收CO形成配合物Cu(CO)Cl•HO,结构如
2 2
图所示。
下列有关说法正确的是
A.CHCHOH和CHCHO中碳原子杂化类型均为sp3
3 2 3
B.Cu2+与NH 形成[Cu(NH )]2+,Cu2+提供孤对电子
3 3 4
C.1 mol Cu(CO)Cl•HO中含有σ键的数目为7 mol
2
D.CHCHOH、SO 、Cu(NO ) 三者晶体的类型相同
3 2 2 3 2
二、填空题
15.(2025·南通市开学考)脱除和利用SO 具有重要意义。
2
(4)一种回收利用SO 的方法:将SO 转化为SO ,再将SO 与等物质的量的甲醇反应转化为化合物
2 2 3 3
A。
已知:
①写出化合物A的结构简式:______________________。
② 一 定 压 强 下 , 化 合 物 A 的 沸 点 低 于 硫 酸 的 原 因 是
____________________________________________
__________________________________________________________________________________________
。
16.(2025·南通市如东县第一次调研)实验室以碳酸锰矿(含MnCO 及少量Fe、Al、Si等氧化物)
3
为原料可制得高纯MnCO。
3微专题突破4 物质结构与性质二
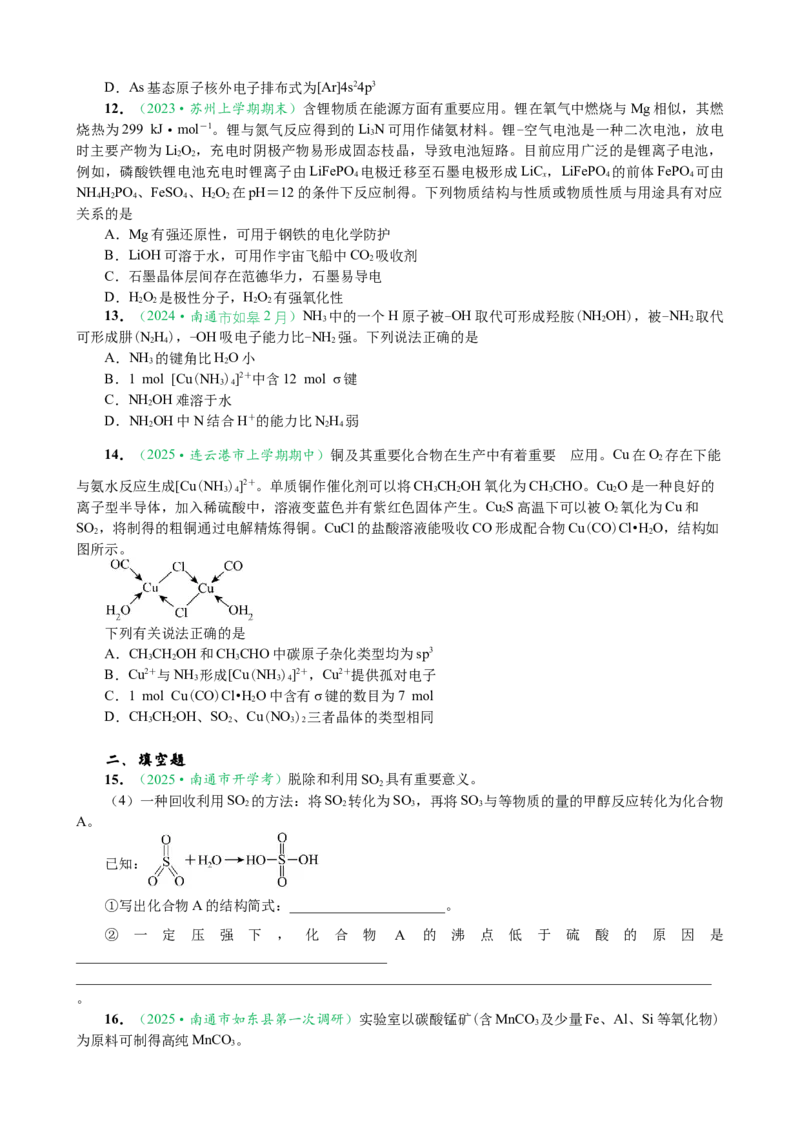
MnCO 在空气流中热解得到不同价态锰的氧化物,其固体残留率随温度的变化图-1所示。
3
(3)①770℃时,剩余固体中n(Mn)∶n(O)为___________。
(写出计算过程,Mn的相对原子质量为55)
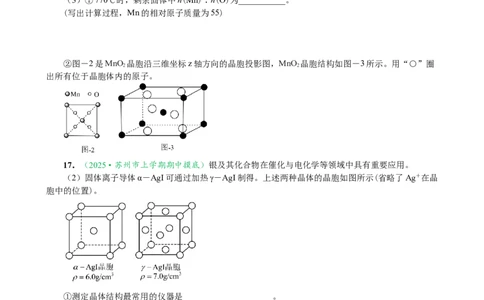
②图-2是MnO 晶胞沿三维坐标z轴方向的晶胞投影图,MnO 晶胞结构如图-3所示。用“○”圈
2 2
出所有位于晶胞体内的原子。
17.(2025·苏州市上学期期中摸底)银及其化合物在催化与电化学等领域中具有重要应用。
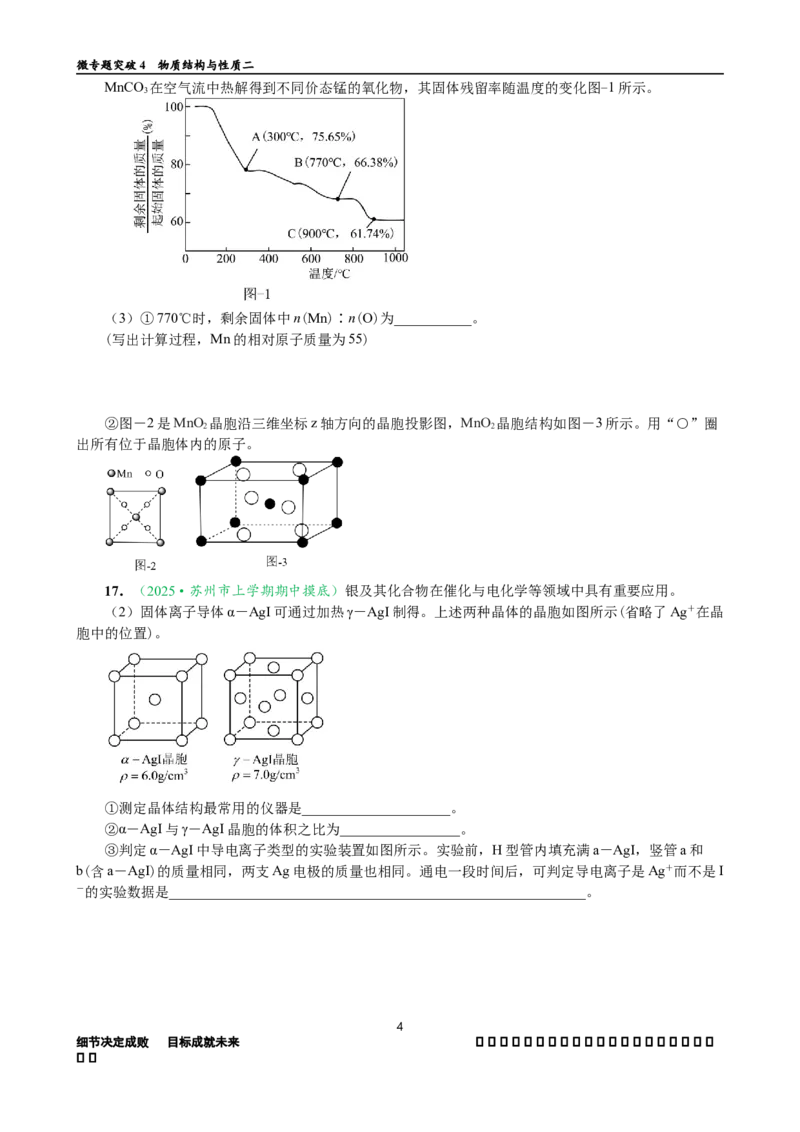
(2)固体离子导体α-AgI可通过加热γ-AgI制得。上述两种晶体的晶胞如图所示(省略了Ag+在晶
胞中的位置)。
①测定晶体结构最常用的仪器是_____________________。
②α-AgI与γ-AgI晶胞的体积之比为_________________。
③判定α-AgI中导电离子类型的实验装置如图所示。实验前,H型管内填充满a-AgI,竖管a和
b(含a-AgI)的质量相同,两支Ag电极的质量也相同。通电一段时间后,可判定导电离子是Ag+而不是I
-的实验数据是___________________________________________________________。
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找