文档内容
微专题突破5 无机物的性质、转化与应用二
一、选择题
1.(2024·浙江省宁波市上学期模拟)物质的性质决定用途,下列两者关系对应不正确的是
A.铝合金质量轻、强度大,可用作制造飞机和宇宙飞船的材料
B.FeCl 溶液呈酸性,可腐蚀覆铜板制作印刷电路板
3
C.CuS、HgS极难溶,可用NaS作沉淀剂除去废水中的Cu2+和Hg2+
2
D.碳化硅硬度大,可用作砂纸、砂轮的磨料
【答案】B
【解析】A项,合金的密度比成分金属一般较小,硬度一般比成分金属要大,故铝合金质量轻、强
度大,决定其可用作制造飞机和宇宙飞船的材料,不合题意;B项,用FeCl 溶液腐蚀覆铜板制作印刷电
3
路板的原理为:Cu+2FeCl =CuCl +2FeCl ,反应中FeCl 作氧化剂,与其溶液呈酸性无关,符合题意;
3 2 2 3
C项,由于CuS、HgS极难溶,故可用NaS作沉淀剂除去废水中的Cu2+和Hg2+,不合题意;D项,碳化
2
硅硬度大,可用作砂纸、砂轮的磨料,不合题意。
2.(2025·辽宁省丹东市上学期月考)下列物质的性质、用途及其分类均正确的是
选项 物质 性质 用途 分类
A 碳酸氢钠 细小白色晶体 用于纺织、玻璃 酸式盐
B 磁性氧化铁 黑色 用作油漆、涂料和橡胶的染料 碱性氧化物
C 聚乙烯 无色,耐腐蚀 用作食品、药物的包装材料 纯净物
D 次氯酸钙 强氧化性 用作漂白、杀菌消毒 正盐
A.A B.B C.C D.D
【答案】D
【解析】A项,碳酸氢钠是细小白色晶体,可用于治疗胃酸过多,制发酵粉,属于酸式盐,碳酸钠
可用于纺织、玻璃,错误;B项,磁性氧化铁是四氧化三铁,黑色固体,是复杂氧化物,可用作红色油漆
和涂料和橡胶的染料的是红色氧化铁,错误;C项,聚乙烯为有机高分子化合物,可用作食品、药物的包
装材料,由于n不同,不属于纯净物,错误;D项,次氯酸钙具有强氧化性,可以使蛋白质变性,可用于
消毒杀菌,属于正盐,正确。
3.(2024·江苏省南通市三模)下列物质结构与性质或物质性质与用途具有对应关系的是
A.键能:H-F>H-Cl,HF的沸点比HCl的高
B.乙酸中-CH 使羟基的极性减小,乙酸的酸性比甲酸的弱
3
C.HClO具有弱酸性,可用于杀菌消毒
D.KAl(SO )•12HO能与NaOH溶液反应,可用作净水剂
4 2 2
【答案】B
【解析】A项,HF的沸点比HCl的高是因为HF分子间存在氢键,HCl分子间不存在氢键,与键能
大小无关,错误;B项,乙酸中-CH 是推电子基团,推电子效应使羧基中羟基极性变小,羟酸的酸性越
3
弱,所以乙酸的酸性比甲酸的弱,正确;C项,HClO具有强氧化性,能使蛋白质变性,可作杀菌消毒剂,
与其具有酸性无关,错误;D项,KAl(SO )•12HO溶于水时电离的Al3+水解生成吸附性强的氢氧化铝
4 2 2
胶体,可吸附水中悬浮物形成沉淀,可作净水剂,和 KAl(SO )•12HO能与NaOH溶液反应的性质无关,
4 2 2
错误。
4.(2024·南通市如皋二模)下列含氮化合物的结构与性质或性质与用途具有对应关系的是
A.NH 中N存在孤电子对,NH 可用作配体
3 3
B.GaN硬度大,可用作半导体材料
C.HNO 具有氧化性,可用于制备NH NO
3 4 3
D.NH 分子间存在氢键,NH 热稳定性高
3 3
【答案】A
【解析】A项,NH 中N存在1对孤电子对,NH 可用作配体,正确;B项,GaN可用作半导体材料
3 3
是因为能导电而作半导体,与硬度大小无关,错误;C项,HNO 具有酸性,可用于制备NH NO ,错误;
3 4 3微专题突破5 无机物的性质、转化与应用二
D项,NH 分子间存在氢键,NH 熔沸点较高,NH 热稳定性与氢键无关,错误。
3 3 3
5.(2025·苏州市上学期期中摸底)元素及其化合物的转化在工业生产中具有极其重要的用途。下
列物质间转化能实现的是
A.工业制取漂白粉:饱和食盐水通电—\s\up 4()Cl 澄清石\s\up 4()漂白粉
—→ 2灰水—
B.工业制取镁:MgCl 溶液蒸干—\s\up 4()无水MgCl 电解—熔 Mg
2 —→ 2 —→ 融
C.工业制取硫酸:S过
2—
量
—
O点
燃
SO
3
水
—
—
→
\s\up 4()H
2
SO
4
D.工业制取纯碱:饱和食盐水NaHCO ①过量②过量固体Δ—\s\up 4()NaCO 固体
3NH3CO2 —→ 2 3
【答案】D
【解析】A项,工业制取漂白粉是将Cl 通入石灰乳中制得,不合题意;B项,由于MgCl 水解生成
2 2
Mg(OH) 和HCl,HCl易挥发,故直接蒸干MgCl 溶液得不到无水MgCl ,不合题意;C项,硫与过量的
2 2 2
O 燃烧只能生成SO ,SO 经催化氧化才能制得SO ,且工业上制备硫酸是煅烧含硫矿物来制得SO ,不
2 2 2 3 2
合题意;D项,向饱和食盐水中先通入NH ,后通入CO ,可以制得NaHCO 固体此为侯氏制碱法,然后
3 2 3
NaHCO 受热分解得到纯碱,符合题意。
3
的
6.(2024·江苏盐城市高三期中)氯及其化合物 转化具有重要应用。下列说法正确的是
A.用Fe制取FeCl 3 :Fe(s)H (a C q l\s\up 4()FeCl 3 蒸 — 发 → —\s\up 4()FeCl 3 •6H 2 OΔ — — → \s\up 4()FeCl 3 (s)
B.工业制取苯酚:NaCl电 — 解 → —\s\up 4()Cl 2 (g)苯 — — → 铁 C 6 H 5 Cl浓 — 硫 — 酸 — Δ C 6 H 5 OH
C.实验室制取Cl:MnO +4H++2Cl-====Mn2++Cl↑+2HO
2 2 2 2
D.工业制取漂白粉:Cl+Ca(OH)=Ca(ClO)+H↑
2 2 2 2
【答案】C
【解析】A项,Fe与HCl反应生成氯化亚铁,错误;B项,苯生成氯苯应与液氯反应,错误;C项,
实验室用二氧化锰与浓盐酸加热制备氯气,方程式为:MnO +4H++2Cl-====Mn2++Cl↑+2HO,正
2 2 2
确;D项,工业用氯气与石灰乳反应制备漂白粉,方程式为:2Cl +2Ca(OH) =Ca(ClO) +CaCl +
2 2 2 2
2HO,错误。
2
7.(2025·南通市海安市开学考)硫及其化合物的转化具有重要的应用。下列说法正确的是
A.FeS 2O — 2 → —高 温 SO 2 浓 SO H2 4 \s\up 4()SO 3
B.浓硫酸C u Δ SO 2 足 水 量 — 氨 — \s\up 4()(NH 4 ) 2 SO 3
C.硫化亚铁与稀硫酸混合:S2-+2H+=HS↑
2
D.SO 通入Ca(ClO) 溶液中:Ca2++2ClO-+SO +HO=CaSO↓+2HClO
2 2 2 2 3
【答案】B
【解析】A项,硫化亚铁在空气中煅烧,生成二氧化硫和三氧化二铁,二氧化硫与氧气反应生成三
氧化硫,错误;B项,铜和浓硫酸反应生成二氧化硫,二氧化硫与足量氨水反应生成亚硫酸氨和水,正确;
C项,硫化亚铁与稀硫酸反应生成硫化氢和硫酸亚铁,离子方程式为:FeS+2H+=HS↑+Fe2+,错误;
2
D项,Ca(ClO) 中通入SO ,两者反应生成硫酸钙、次氯酸和氯离子,正确的离子方程式为:Ca2++
2 2
3ClO-+SO +HO=CaSO↓+2HClO+Cl-(SO 少量),错误。
2 2 4 2
8.(2024·南通市如皋 2 月)NH 的燃烧热为 622 kJ·mol-1,具有强还原性,可由尿素
2 4
CO(NH )、NaClO和NaOH溶液一起反应制得。下列化学反应的表示正确的是
2 2
A.金属钠和液氨反应:NH +Na=NaNH +H↑
3 2 2
B.过量氨水和SO 反应:SO +2NH ·HO=(NH )SO +HO
2 2 3 2 4 2 3 2
C.尿素、NaClO、NaOH溶液制取NH 的离子方程式:CO(NH )+ClO-=CO↑+NH+Cl-
2 4 2 2 2 2 4
D.肼燃烧的热化学方程式:NH(l)+O(g)=N(g)+2HO(g) ∆H=-622 kJ·mol-1
2 4 2 2 2
【答案】B
【解析】A项,金属钠和液氨反应生成NaNH 和H ,反应的方程式为:2NH +2Na=2NaNH +
2 2 3 2
H↑,错误;B 项,过量氨水吸收工业尾气中的 SO ,生成(NH )SO 和水:SO +2NH ·HO=
2 2 4 2 3 2 3 2
(NH )SO +HO,正确;C项,尿素和NaClO溶液在碱性条件下反应生成NH 、NaCO 和NaCl,反应
4 2 3 2 2 4 2 3
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找的离子方程式为:CO(NH ) +ClO-+2OH-=CO2-+NH +Cl-+HO,错误;D项,肼燃烧的热化学
2 2 3 2 4 2
方程式中HO应为液态,错误。
2
9.(2024·南京、盐城二模)碳元素在自然界分布很广。游离态的碳有金刚石、石墨、C 等,化合
60
态的碳存在形式更为多样。碳单质是重要的还原剂,工业上用焦炭还原石英砂可制得粗硅。CO能将溶液
中的Pd2+还原为Pd,生成黑色沉淀,该反应可用于检验CO。燃煤烟气中的CO 可用NaCO 饱和溶液进
2 2 3
行捕集。一定温度和压强下,CO 可转化为具有良好溶解能力和流动性能的超临界流体。C H 在氧气中燃
2 2 2
烧放出大量的热,常用来切割金属。下列化学反应表示正确的是
A.焦炭与石英砂反应:C+SiO====CO↑+Si
2 2
B.CO与酸性PdCl 溶液反应:CO+Pd2++2OH-=CO+Pd↓+HO
2 2 2
C.CO2-的水解反应:CO2-+2HO HCO+2OH-
3 3 2 2 3
D.NaCO 饱和溶液与足量CO 反应:2Na++CO2-+CO+HO=2NaHCO ↓
2 3 2 3 2 2 3
【答案】D
【解析】焦炭与石英砂在高温下反应生成粗硅和CO,化学方程式为2C+SiO====Si+2CO↑,错误;
2
由题意知,将CO通入氯化钯(PdCl )溶液中,CO能将溶液中的Pd2+还原为Pd,生成黑色沉淀,根据
2
氧化还原反应原理及元素守恒,可知反应产物中还应该有CO 和HCl,该反应的化学方程式为CO+PdCl
2 2
+HO=CO+Pd↓+2HCl(注意:酸性溶液中,不能有氢氧根离子参加反应),错误;多元弱酸根离
2 2
子的水解分步进行,故CO2-的水解反应为CO2-+HO HCO -+OH-、HCO -+HO HCO+
3 3 2 3 3 2 2 3
OH-(以第一步为主),错误;NaCO 饱和溶液与足量CO 反应生成碳酸氢钠,相同条件下碳酸氢钠的
2 3 2
溶解度小于碳酸钠,故有碳酸氢钠固体析出,离子方程式为2Na++CO2-+CO+HO=2NaHCO ↓,
3 2 2 3
正确。
10.(2024·苏州调研期初)铁及其化合物转化具有重要应用,铁及其化合物应用广泛。纳米铁粉
可用于处理水中污染物,一定条件下,向FeSO 溶液中滴加碱性NaBH 溶液,生成纳米铁粉、H 和
4 4 2
B(OH) -;Fe O 可用作锂离子电池的电极材料,电池工作时有 Li+嵌入其中生成 LiFe O ;铁氰化钾
4 3 4 3 4
{K [Fe(CN)]}遇Fe2+发生反应生成深蓝色沉淀{Fe [Fe(CN)]};常用于检验Fe2+。下列表述不正确的是
3 6 3 6 2
A.制备纳米铁粉的离子反应:2Fe2++BH-+4OH-=2Fe↓+2H↑+B(OH)-
4 2 4
B.FeS 2 制硫酸过程中物质转化:FeS 2 (g)O g— 2 — (高 温 SO 2 (g)H (l 2 — O\s\up 4()H 2 SO 4 (aq)
C.Fe O 晶体中嵌入Li+形成LiFe O 时,部分Fe3+转化为Fe2+
3 4 3 4
D.铁氰化钾检验Fe2+的离子反应:3Fe2++2[Fe(CN)]3-=Fe [Fe(CN)]↓
6 3 6 2
【答案】B
【解析】A项,一定条件下,向FeSO 溶液中滴加碱性NaBH 溶液,生成纳米铁粉、H 和B(OH)
4 4 2 4
-,对应的离子方程式为:2Fe2++BH -+4OH-=2Fe↓+2H↑+B(OH) -,正确;B项,FeS 制硫酸
4 2 4 2
过程,即FeS 与氧气反应生成氧化铁和二氧化硫,二氧化硫在五氧化二钒作催化剂且加热的条件下被氧
2
气氧化为三氧化硫,三氧化硫与水(实际用的是浓硫酸)反应得硫酸,错误;C项,Fe O 晶体中嵌入Li+
3 4
形成LiFe O 时,锂离子带正电荷,因此部分Fe3+转化为Fe2+,正确;D项,铁氰化钾检验Fe2+是利用了
3 4
亚铁离子与[Fe(CN)]3-能生成蓝色沉淀,对应的离子反应方程式为:3Fe2++2[Fe(CN)]3-=
6 6
Fe [Fe(CN)]↓,正确。
3 6 2
11.(2024·江苏盐城市高三期中)碳元素及其化合物在自然界广泛存在且具有重要应用。12C、
13C、14C是碳元素的3种核素,碳元素不仅可以形成金刚石等单质,还能形成CO、CH、CHOH、
2 4 3
CHCHOH、HCOONa、NaHCO 等重要化合物。CH 具有较大的燃烧热(890.3 kJ·mol-1),是常见燃料。
3 2 3 4
用NaOH溶液吸收CO 生成NaHCO 溶液是CO“固定”再利用的方法之一、电解NaHCO 溶液可获得
2 3 2 3
CH;向NaHCO 溶液中加入铁粉,反应初期产生H 并生成FeCO,FeCO 迅速转化为活性Fe O-x,活
4 3 2 3 3 3 4
性Fe O-x催化HCO -加氢生成HCOO-。“侯氏制碱法”是以CO、NH 、NaCl为原料制备NaCO。下
3 4 3 2 3 2 3
列化学反应表示正确的是
A.甲烷的燃烧:CH(g)+2O(g)=CO(g)+2HO(g) ∆H=-890.3 kJ·mol-1
4 2 2 2
B.铁粉和NaHCO 溶液反应制H:Fe+HCO -+HO=FeCO↓+H↑+OH-
3 2 3 2 3 2
C.CO 通入氨的饱和食盐水中:2NaCl+2NH +CO+HO=NaCO↓+2NH Cl
2 3 2 2 2 3 4
D.催化电解HCO -生成CH 的阳极反应式:HCO -+8e—+9H+=CH+3HO
3 4 3 4 2
【答案】B
【解析】A项,燃烧热是在101 kPa时,1 mol物质完全燃烧生成稳定的氧化物时所放出的热量,应该微专题突破5 无机物的性质、转化与应用二
生成液态水,错误;B项,由题意可知,向NaHCO 溶液中加入铁粉,反应初期产生H 并生成FeCO ,
3 2 3
反应中铁化合价升高发生氧化反应、水中氢元素化合价降低发生还原反应,反应为 Fe+HCO -+HO=
3 2
FeCO↓+H↑+OH-,正确;C项,CO 通入氨的饱和食盐水中生成溶解度较小的碳酸氢钠,同时生成
3 2 2
氯化铵:NaCl+NH +CO +HO=NaHCO↓+NH Cl,错误;D项,由题意可知,电解NaHCO 溶液可
3 2 2 3 4 3
获得CH,反应中碳元素得到电子在弱碱性条件下发生还原反应生成甲烷,反应在阴极进行:HCO -+8e
4 3
—+6HO=CH+9OH-,错误。
2 4
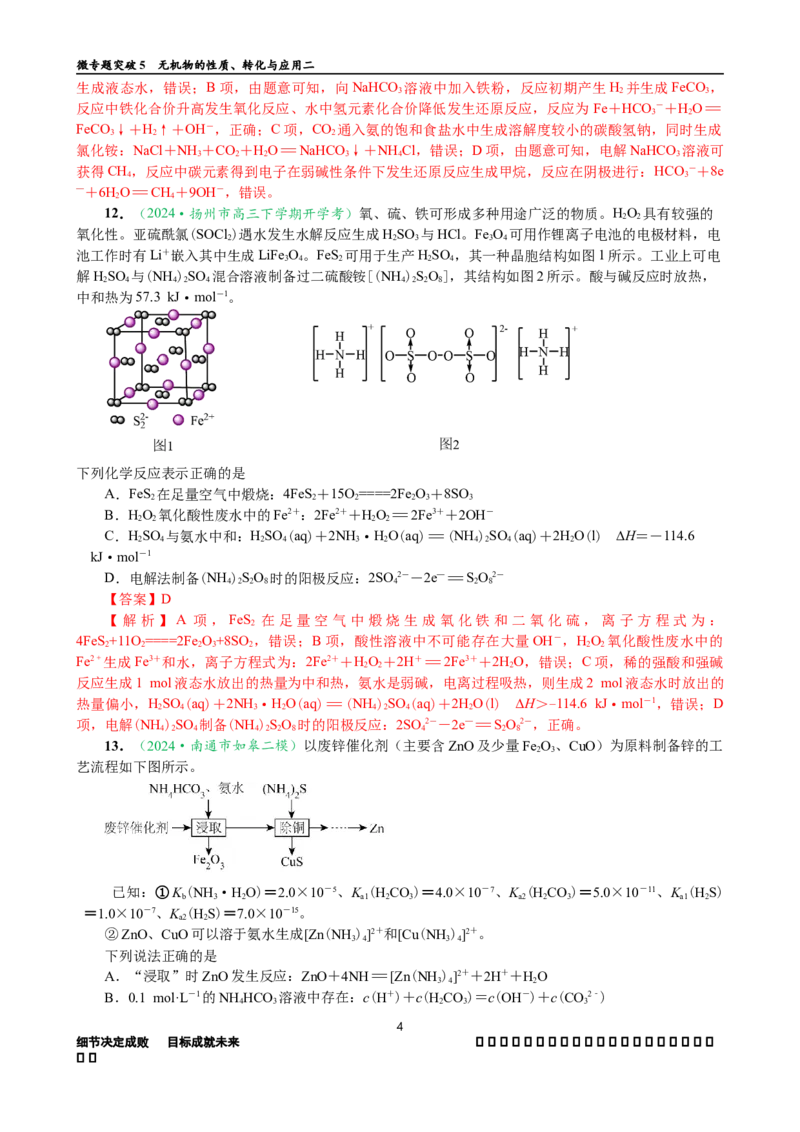
12.(2024·扬州市高三下学期开学考)氧、硫、铁可形成多种用途广泛的物质。HO 具有较强的
2 2
氧化性。亚硫酰氯(SOCl )遇水发生水解反应生成HSO 与HCl。Fe O 可用作锂离子电池的电极材料,电
2 2 3 3 4
池工作时有Li+嵌入其中生成LiFe O。FeS 可用于生产HSO ,其一种晶胞结构如图1所示。工业上可电
3 4 2 2 4
解HSO 与(NH )SO 混合溶液制备过二硫酸铵[(NH )SO],其结构如图2所示。酸与碱反应时放热,
2 4 4 2 4 4 2 2 8
中和热为57.3 kJ·mol-1。
下列化学反应表示正确的是
A.FeS 在足量空气中煅烧:4FeS+15O====2Fe O+8SO
2 2 2 2 3 3
B.HO 氧化酸性废水中的Fe2+:2Fe2++HO=2Fe3++2OH-
2 2 2 2
C.HSO 与氨水中和:HSO (aq)+2NH ·HO(aq)=(NH )SO (aq)+2HO(l) ∆H=-114.6
2 4 2 4 3 2 4 2 4 2
kJ·mol-1
D.电解法制备(NH )SO 时的阳极反应:2SO 2--2e—=SO2-
4 2 2 8 4 2 8
【答案】D
【解析】A 项,FeS 在足量空气中煅烧生成氧化铁和二氧化硫,离子方程式为:
2
4FeS+11O====2Fe O+8SO ,错误;B项,酸性溶液中不可能存在大量OH-,HO 氧化酸性废水中的
2 2 2 3 2 2 2
Fe2+生成Fe3+和水,离子方程式为:2Fe2++HO +2H+=2Fe3++2HO,错误;C项,稀的强酸和强碱
2 2 2
反应生成1 mol液态水放出的热量为中和热,氨水是弱碱,电离过程吸热,则生成2 mol液态水时放出的
热量偏小,HSO (aq)+2NH ·HO(aq)=(NH )SO (aq)+2HO(l) ∆H>-114.6 kJ·mol-1,错误;D
2 4 3 2 4 2 4 2
项,电解(NH )SO 制备(NH )SO 时的阳极反应:2SO 2--2e—=SO2-,正确。
4 2 4 4 2 2 8 4 2 8
13.(2024·南通市如皋二模)以废锌催化剂(主要含ZnO及少量Fe O 、CuO)为原料制备锌的工
2 3
艺流程如下图所示。
已知:①K (NH ·HO)=2.0×10-5、K (HCO)=4.0×10-7、K (HCO)=5.0×10-11、K (HS)
b 3 2 a1 2 3 a2 2 3 a1 2
=1.0×10-7、K (HS)=7.0×10-15。
a2 2
②ZnO、CuO可以溶于氨水生成[Zn(NH )]2+和[Cu(NH )]2+。
3 4 3 4
下列说法正确的是
A.“浸取”时ZnO发生反应:ZnO+4NH=[Zn(NH )]2++2H++HO
3 4 2
B.0.1 mol·L-1的NH HCO 溶液中存在:c(H+)+c(HCO)=c(OH-)+c(CO2-)
4 3 2 3 3
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找C.“除铜”所得上层清液中存在<
D.ZnS、CuS均不能溶于氨水生成[Zn(NH )]2+和[Cu(NH )]2+
3 4 3 4
【答案】C
【解析】A项,根据已知②,“浸取”时ZnO发生反应:ZnO+2NH+2NH ·HO=[Zn(NH )]2+
3 2 3 4
+3HO,错误;B项,0.1 mol·L-1的NH HCO 溶液中存在质子守恒:c(H+)+c(HCO)=c(OH-)+
2 4 3 2 3
c(CO2-)+c(NH ·HO),错误;C项,“除铜”所得上层清液中锌离子没有沉淀,溶液中存在c(Zn2
3 3 2
+)•c(S2-)<K (ZnS),c(Cu2+)•c(S2-)=K (CuS),故存在<,正确;D项,除铜步骤中[Cu(NH )]2++
sp sp 3 4
S2-=CuS↓+4NH ,说明氨不易与CuS反应生成配离子四氨合铜离子,同理[Zn(NH )]2+不能和S2-反
3 3 4
应生成四氨合铜离子离子,说明ZnS能溶于氨水生成配离子[Zn(NH )]2+,错误。
3 4
14.(2024·浙江省嘉兴12月)一水硫酸四氨合铜(Ⅱ)的化学式为[Cu(NH )]SO •HO是一种重要
3 4 4 2
的染料及农药中间体。某学习小组以废铜料(含少量铁及难溶性杂质)为主要原料合成该物质,合成路线
如下:
下列说法不正确的是
A.操作I中发生的主要反应为:2Fe2++HO+2H+=2Fe3++2HO
2 2 2
B.操作II中趁热过滤除去的是难溶性杂质和氢氧化铁
C.操作III中洗涤可用乙醇和水的混合液,干燥可采用减压干燥方式
D.设计操作IV的目的是为了提高乙醇的利用率
【答案】A
【解析】含铜废料加硫酸和双氧水,铜被氧化为硫酸铜,铁被氧化为硫酸铁,加氧化铜调节 pH=4
生成氢氧化铁沉淀除去铁,滤液得硫酸铜溶液,滤液中加氨水生成深蓝色硫酸四氨合铜溶液,加入乙醇
硫酸四氨合铜溶解度降低,析出[Cu(NH )]SO •HO。
3 4 4 2
A项,操作I中铜被氧化为硫酸铜,发生的主要反应为:Cu+HO+2H+=Cu2++2HO,错误;B
2 2 2
项,加氧化铜调节pH=4生成氢氧化铁沉淀,操作II中趁热过滤除去的是难溶性杂质和氢氧化铁,正确;
C项,硫酸四氨合铜在乙醇中的溶解度远小于在水中的溶解度,操作III中洗涤可用乙醇和水的混合液,
干燥可采用减压干燥方式,正确;D项,设计操作IV,乙醇循环利用,目的是为了提高乙醇的利用率,
正确。
15.(2024·南通市二模)第四周期过渡元素形成的化合物具有重要作用。黄铜(CuFeS)用
2
Fe (SO ) 溶液浸泡后生成单质硫,所得 CuSO 溶液可用于制取纳米 Cu O,Cu O能与酸发生反应。
2 4 3 4 2 2
CuO-TiO 可用于低温下催化氧化HCHO:HCHO(g)+O(g)==========CO(g)+HO(l)。CoCl 具有强
x 2 2 2 2 3
氧化性,可与盐酸反应生成氯气。由 NaNO 、Co(NO ) 、HO 和 CHCOOH 反应制备的配合物
2 3 2 2 2 3
Na[Co(NO )]可应用于K+的鉴定。下列化学反应表示正确的是
3 2 6
A.Cu O与稀硫酸反应:Cu O+2H+=2Cu2++HO
2 2 2
B.Fe (SO ) 溶液和CuFeS 反应:CuFeS+4Fe3+=5Fe2++Cu2++2S
2 4 3 2 2
C.Co(OH) 与足量盐酸反应:Co(OH)+3HCl=CoCl +3HO
3 3 3 2
D.制备Na[Co(NO )]的反应:12NO2-+2Co2++HO+2H+=2Na[Co(NO )]3-+2HO
3 2 6 2 2 3 2 6 2
【答案】B
【解析】A项,Cu O与稀硫酸发生歧化反应,离子方程式为Cu O+2H+=Cu2++Cu+HO,错误;
2 2 2
B项,Fe (SO ) 溶液和CuFeS 反应,生成Fe2+和单质S,离子方程式为:CuFeS +4Fe3+=5Fe2++Cu2+
2 4 3 2 2
+2S,正确;C项,CoCl 具有强氧化性,可与盐酸反应生成氯气,故Co(OH) 与足量盐酸反应生成Cl
3 3 2
和Co2+,化学方程式为:2Co(OH) +6HCl=2CoCl +Cl↑+3HO,错误;D项,制备Na[Co(NO )]
3 2 2 2 3 2 6
时的离子方程式,醋酸要保留化学式,离子方程式为 12NO2-+2Co2++HO +2CHCOOH=
2 2 3微专题突破5 无机物的性质、转化与应用二
2Na[Co(NO )]3-+2HO+2CHCOO-,错误。
3 2 6 2 3
16.(2024·湖北卷)结构决定性质,性质决定用途。下列事实解释错误的是
事实 解释
A 甘油是黏稠液体 甘油分子间的氢键较强
B 王水溶解铂 浓盐酸增强了浓硝酸的氧化性
C 冰的密度小于干冰 冰晶体中水分子的空间利用率相对较低
D 石墨能导电 未杂化的p轨道重叠使电子可在整个碳原子平面内运动
A.A B.B C.C D.D
【答案】B
【解析】A项,甘油分子中有3个羟基,分子间可以形成更多的氢键,且O元素的电负性较大,故
其分子间形成的氢键较强,因此甘油是黏稠液体,正确;B项,王水溶解铂,是因为浓盐酸提供的Cl-能
与被硝酸氧化产生的高价态的铂离子形成稳定的配合物从而促进铂的溶解,在这个过程中浓盐酸没有增
强浓硝酸的氧化性,而是通过形成配合物增强了铂的还原性,不正确;C项,冰晶体中水分子间形成较多
的氢键,由于氢键具有方向性,因此,水分子间形成氢键后空隙变大,冰晶体中水分子的空间利用率相
对较低,冰的密度小于干冰,正确;D项,石墨属于混合型晶体,在石墨的二维结构平面内,每个碳原
子以C—C键与相邻的3个碳原子结合,形成六元环层。碳原子有4个价电子,而每个碳原子仅用3个价
电子通过sp2杂化轨道与相邻的碳原子形成共价键,还有1个电子处于碳原子的未杂化的2p轨道上,层内
碳原子的这些p轨道相互平行,相邻碳原子p轨道相互重叠形成大π键,这些p轨道的电子可以在整个层
内运动,因此石墨能导电,正确。
二、填空题
17.(2024·江苏盐城市高三期中)二氧化氯(ClO)是一种高效消毒剂,易溶于水,沸点为
2
11.0℃,浓度高时极易爆炸。
(1)实验室在60℃的条件下用闪锌矿(主要成份ZnS)与NaClO 溶液、HSO 溶液制备二氧化氯,同
3 2 4
时生成硫酸锌。
①写出反应的离子方程式:_____________________________________________________。
②用如图所示的装置制备二氧化氯。则闪锌矿、NaClO 溶液、HSO 溶液三种反应物的加料方式是
3 2 4
__________________________________________________________________________。
③若闪锌矿加料过量太多,生成ClO 的量明显减少的原因是
2
___________________________________________________________________________________________
。
④反应过程中通入N 的作用是_____________________________________________________________
2
___________________________________________________。
【答案】(1)①ZnS+8ClO -+8H+=====ClO +Zn2++4HO+SO 2- ②将粉碎的闪锌矿和NaClO
3 2 2 4 3
混合加入三颈烧瓶中,通过滴液漏斗缓慢滴加HSO 溶液 ③ZnS具有还原性,过量的ZnS能与ClO 发
2 4 2
生氧化还原反应,导致ClO 被消耗 ④既能将生成的ClO 排出;又由于二氧化氯浓度高时极易爆炸,通
2 2
入N 可降低二氧化氯浓度,防止发生爆炸
2
【解析】(1)在60℃的条件下用闪锌矿(主要成份ZnS)与NaClO 溶液、HSO 溶液制备二氧化氯,同
3 2 4
6
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找时生成硫酸锌:①反应的离子方程式:ZnS+8ClO -+8H+=====ClO +Zn2++4HO+SO 2-;②加料方式:
3 2 2 4
将粉碎的闪锌矿和NaClO 混合加入三颈烧瓶中,通过滴液漏斗缓慢滴加HSO 溶液;③若闪锌矿加料过
3 2 4
量太多,生成ClO 的量明显减少的原因:ZnS具有还原性,过量的ZnS能与ClO 发生氧化还原反应,导
2 2
致ClO 被消耗;④反应过程中通入N 的作用:既能将生成的ClO 排出;又由于二氧化氯(ClO)浓度高时
2 2 2 2
极易爆炸,通入N 可降低(ClO)浓度,防止发生爆炸。
2 2