文档内容
微专题突破6 无机化工流程题透视
知之者不如好之者,好之者不如乐之者——孔子
目标定位
1.知道化工生产术语及意义,了解流程题构成特点,会分析各步操作的作用。
2.能解释物质制备中反应条件控制的目的、会对混合物进行分离提纯。
3.能根据有关原理解释图像曲线变化的原因。
【规律点和易错点】
孙猴子七十二般变化,都逃不出你的手心
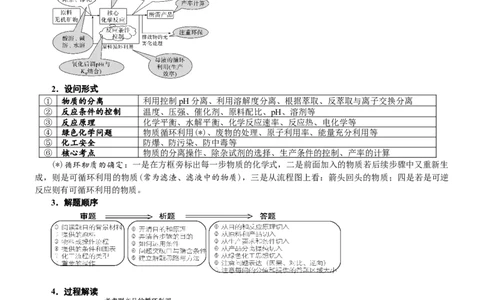
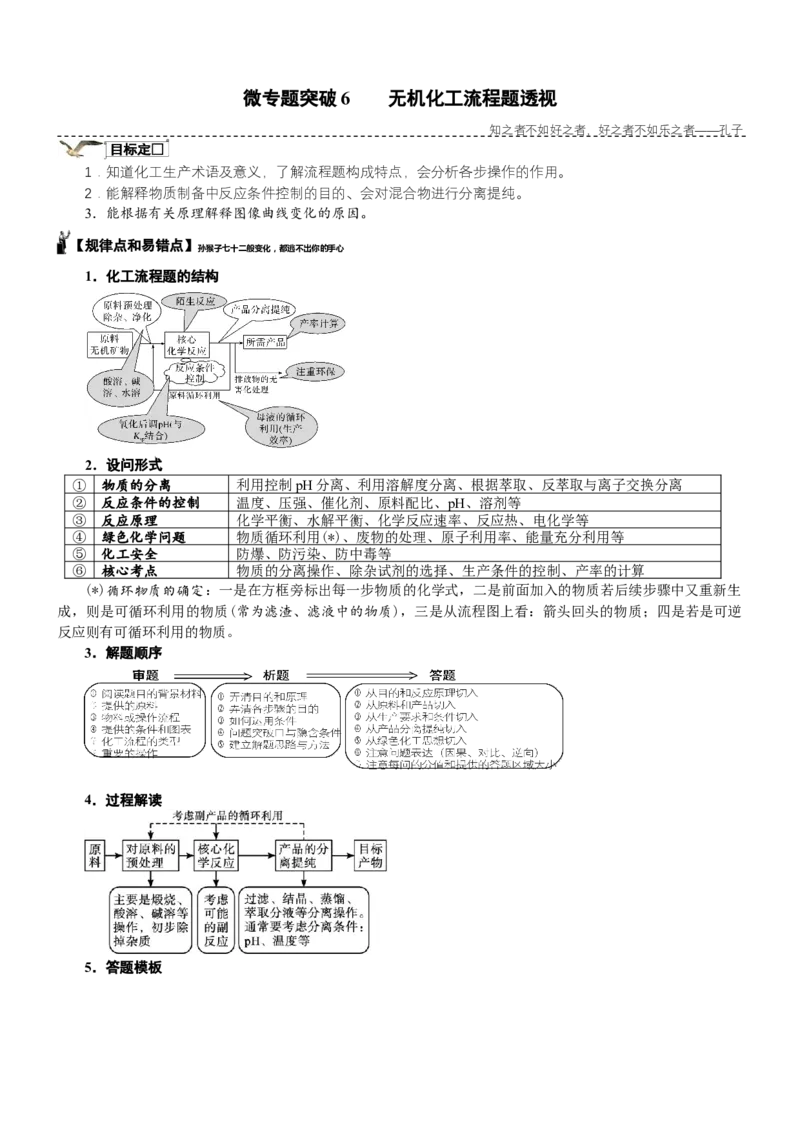
1.化工流程题的结构
2.设问形式
① 物质的分离 利用控制pH分离、利用溶解度分离、根据萃取、反萃取与离子交换分离
② 反应条件的控制 温度、压强、催化剂、原料配比、pH、溶剂等
③ 反应原理 化学平衡、水解平衡、化学反应速率、反应热、电化学等
④ 绿色化学问题 物质循环利用(*)、废物的处理、原子利用率、能量充分利用等
⑤ 化工安全 防爆、防污染、防中毒等
⑥ 核心考点 物质的分离操作、除杂试剂的选择、生产条件的控制、产率的计算
(*)循环物质的确定:一是在方框旁标出每一步物质的化学式,二是前面加入的物质若后续步骤中又重新生
成,则是可循环利用的物质(常为滤渣、滤液中的物质),三是从流程图上看:箭头回头的物质;四是若是可逆
反应则有可循环利用的物质。
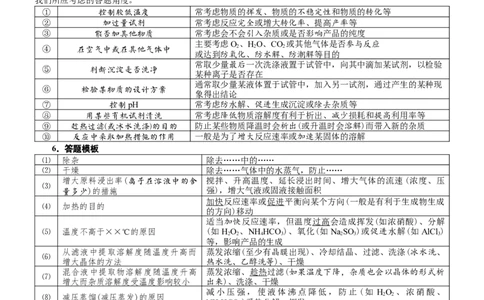
3.解题顺序
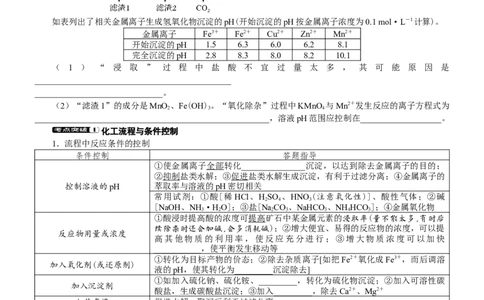
4.过程解读
5.答题模板微专题突破6 无机化工流程题透视 问题的态度:问则少;辩则明
5.表述性词汇“十大答题方向”
化工生产流程和综合实验题中经常会出现一些表述性词语,这些表述性词语就是隐性的信息,它可以暗示
我们所应考虑的答题角度。
① 控制较低温度 常考虑物质的挥发、物质的不稳定性和物质的转化等
② 加过量试剂 常考虑反应完全或增大转化率、提高产率等
③ 能否加其他物质 常考虑会不会引入杂质或是否影响产品的纯度
主要考虑O、HO、CO 或其他气体是否参与反应
④ 在空气中或在其他气体中 2 2 2
或达到防氧化、防水解、防潮解等目的
常取少量最后一次洗涤液置于试管中,向其中滴加某试剂,以检验
⑤ 判断沉淀是否洗净
某种离子是否存在
通常取少量某液体置于试管中,加入另一试剂,通过产生的某种现
⑥ 检验某物质的设计方案
象得出结论
⑦ 控制pH 常考虑防水解、促进生成沉淀或除去杂质等
⑧ 用某些有机试剂清洗 常考虑降低物质溶解度有利于析出、减少损耗和提高利用率等
⑨ 趁热过滤(或冰水洗涤)的目的 防止某些物质降温时会析出(或升温时会溶解)而带入新的杂质
⑩ 反应中采取加热措施的作用 一般是为了增大反应速率或加速某固体的溶解
6.答题模板
⑴ 除杂 除去……中的……
⑵ 干燥 除去……气体中的水蒸气,防止……
增大原料浸出率(离子在溶液中的含 搅拌、升高温度、延长浸出时间、增大气体的流速(浓度、压
⑶
量多少)的措施 强),增大气液或固液接触面积
加快反应速率或促进平衡向某个方向(一般是有利于生成物生成
⑷ 加热的目的
的方向)移动
适当加快反应速率,但温度过高会造成挥发(如浓硝酸)、分解
⑸ 温度不高于××℃的原因 (如HO 、NH HCO )、氧化(如NaSO )或促进水解(如AlCl )
2 2 4 3 2 3 3
等,影响产品的生成
从滤液中提取溶解度随温度升高而 蒸发浓缩(至少有晶膜出现)、冷却结晶、过滤、洗涤(冰水洗、
⑹
增大晶体的方法 热水洗、乙醇洗等)、干燥
混合液中提取物溶解度随温度升高 蒸发浓缩、趁热过滤(如果温度下降,杂质也会以晶体的形式析
⑺
增大而杂质溶解度受温度影响较小 出来)、洗涤、干燥
减小压强,使液体沸点降低,防止(如 HO 、浓硝酸、
⑻ 减压蒸馏(减压蒸发)的原因 2 2
NH HCO )受热分解、挥发
4 3
检验溶液中离子是否沉淀完全的方 将溶液静置一段时间后,向上层清液中滴入沉淀剂,若无沉淀
⑼
法 生成,则离子沉淀完全
沿玻璃棒往漏斗中加蒸馏水至液面浸没沉淀,待水自然流下
⑽ 洗涤沉淀
后,重复操作2~3次
取少量最后一次的洗涤液于试管中,向其中滴入某试剂,若未
⑾ 检验沉淀是否洗涤干净的方法
出现特征反应现象,则沉淀洗涤干净
⑿ 洗涤沉淀的目的 除掉附着在沉淀表面的可溶性杂质
洗去晶体表面的杂质离子并降低被洗涤物质的溶解度,减少其
⒀ 冰水洗涤的目的
在洗涤过程中的溶解损耗
降低被洗涤物质的溶解度,减少其在洗涤过程中的溶解损耗,
⒁ 乙醇洗涤的目的
得到较干燥的产物(乙醇易挥发,可迅速干燥)
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找抑制某离子的水解,如加热蒸发AlCl 溶液时为获得AlCl 需在
⒂ 蒸发、反应时的气体氛围 3 3
HCl气流中进行
⒃ 事先煮沸溶液的原因 除去溶解在溶液中的氧化性气体(如氧气),防止某物质被氧化
⒄ 沉淀时pH范围的确定 pH过小导致某离子沉淀不完全,pH过大导致主要离子开始沉淀
7.常考试剂的作用
类别 物质 作用
HO、HNO、空气、次氯酸
氧化剂 2 2 3 氧化某些还原性物质,便于后续分离,如氧化Fe2+、Co2+等
盐、KMnO 、MnO 等
4 2
还原剂SO 、NaSO 、I-、金属单质等 还原某些氧化性物质,便于后续分离,如还原Fe3+等
2 2 3
溶解金属和金属氧化物,调节pH促进水解(沉淀),HSO 可提供SO 2-
酸 HCl、HSO 、HNO 等 2 4 4
2 4 3 作沉淀剂
去除油污;调节pH促进水解(沉淀);NaOH溶液可溶解氧化铝、铝、
碱 NaOH、NH ·HO等
3 2 二氧化硅
调节pH使某些离子沉淀;提供CO2-使某些离子(如Cu2+①、Ca2+、
碳酸盐 NaCO、(NH )CO 等 3
2 3 4 2 3 Pb2+、Ba2+等)沉淀
调pH使某些离子沉淀;提供HCO -使某些离子{如[Al(OH)]-]、Fe3+
碳酸 3 4
NaHCO 、NH HCO ③、Al3+、Cr3+、Fe2+④、Mg2+、Mn2+、Co2+等}沉淀;相对于碳酸盐,
氢盐 3 4 3
碳酸氢盐可避免溶液碱性过强而使金属离子转化为氢氧化物
草酸盐 NaC O 沉淀某些离子,如Ba2+、Ca2+等
2 2 4
硫化物 HS、NaS、(NH )S等 沉淀某些离子,如Cu2+、Pb2+、Ag+、Sn2+等
2 2 4 2
氟化物 HF、NaF 沉淀某些离子,如Ba2+、Ca2+、Mg2+等
注:①发生反应:2Cu2++2CO2-+HO=Cu (OH)CO↓+CO↑;②发生反应:[Al(OH)]-+HCO -
3 2 2 2 3 2 4 3
=Al(OH)↓+CO2-+HO;③发生反应:Fe3++3HCO -=Fe(OH)↓+3CO↑;④发生反应:Fe2++
3 3 2 3 3 2
2HCO -=FeCO↓+CO↑+HO。
3 3 2 2
8.创新考查——萃取与反萃取
萃取则是利用物质性质由一个液相转移到另一个液相的分离方法。萃取的作用是:从矿石的浸出
萃取原理
液中,提取和富集有价值金属,分离化学性质相近的金属离子
萃取的操作步骤一般是首先将水溶液(料液)与有机溶剂(或溶液)充分混合,然后利用两相的密度
萃取步骤 不同静置分相。分出的称为萃取液,有机相称为负载有机相,被萃入到有机相中去的物质称为被
萃取物(起富集或分离作用)
被萃取物萃入有机相后,一般需要使其重新返回水相,此时把负载有机相与反萃剂(一般为无机
反萃取 酸或碱的水溶液,也可以是纯水)接触,使被萃取物转入水相,这一过程相当于萃取的逆过程,
故称为反萃取
9.工业流程常见专业术语
浸出 固体加水(酸)溶解得到离子
浸出率 固体溶解后,离子在溶液中的含量的多少
酸浸 在酸溶液中反应使可溶性金属离子进入溶液,不溶物通过过滤除去的溶解过程
通常为除去水溶性杂质(滤液淋洗——减少沉淀的溶解;冷水洗涤——减少沉淀的溶解;酒精洗
水洗
涤——减少晶体溶解,得到较干燥的沉淀)
水浸 与水接触反应或溶解
提高“浸出率 ①将矿石粉碎;②适当加热;③充分搅拌;④适当提高浸取液的浓度;⑤适当延长浸取时间等
考考位位位
(2023·江苏)实验室模拟“镁法工业烟气脱硫”并制备MgSO ·HO,其实验过程可表示为
4 2
(1)在搅拌下向氧化镁浆料中匀速缓慢通入SO 气体,生成MgSO ,反应为Mg(OH) +HSO =MgSO
2 3 2 2 3 3
+2HO,其平衡常数 K 与 K [Mg(OH)]、K (MgSO )、K (HSO )、K (HSO )的代数关系式为 K=
2 sp 2 sp 3 a1 2 3 a2 2 3
____________________________________________________;下列实验操作一定能提高氧化镁浆料吸收SO 效
2
率的有________________(填序号)。
A.水浴加热氧化镁浆料
B.加快搅拌速率
C.降低通入SO 气体的速率
2微专题突破6 无机化工流程题透视 问题的态度:问则少;辩则明
D.通过多孔球泡向氧化镁浆料中通SO
2
(2)在催化剂作用下MgSO 被O 氧化为MgSO 。已知MgSO 的溶解度为0.57 g (20℃),O 氧化溶液中
3 2 4 3 2
SO的离子方程式为__________________________________;在其他条件相同时,以负载钴的分子筛为催化剂,
浆料中MgSO 被O 氧化的速率随pH的变化如图甲所示。在pH=6~8范围内,pH增大,浆料中MgSO 的氧化
3 2 3
速率增大,其主要原因是__________________________________________________________
____________________________________。
【问题解决1】
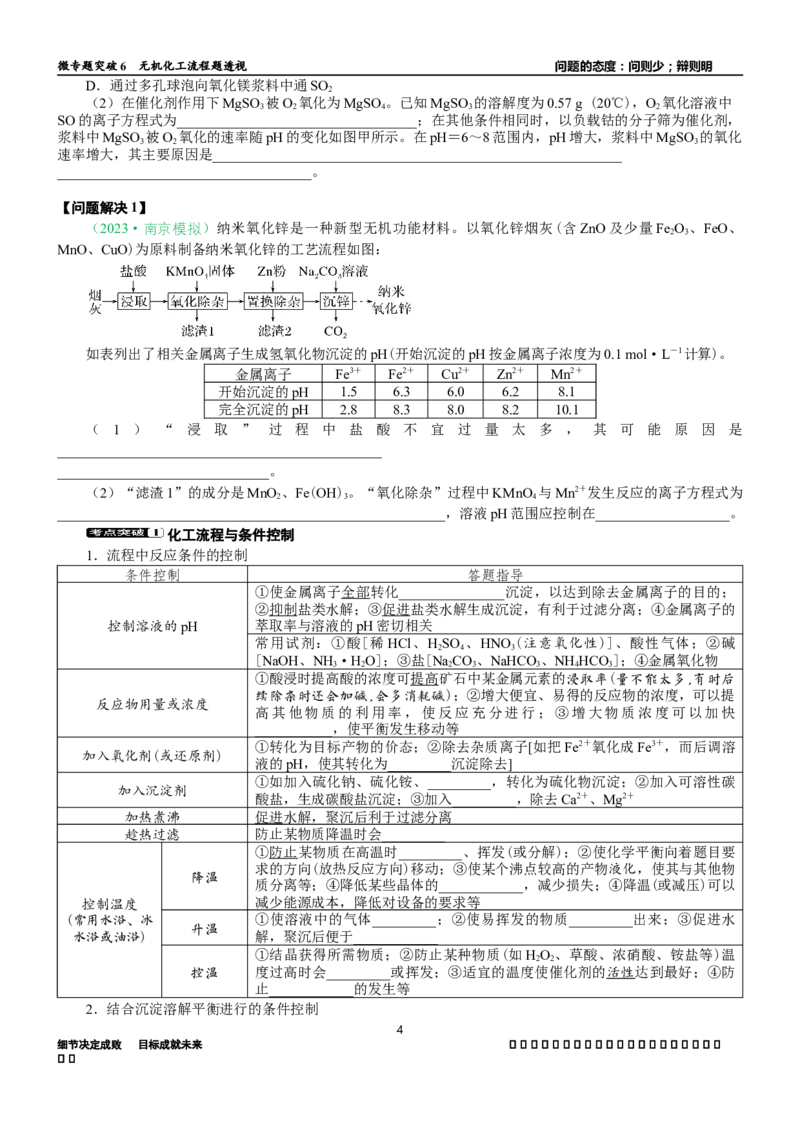
(2023·南京模拟)纳米氧化锌是一种新型无机功能材料。以氧化锌烟灰(含ZnO及少量Fe O 、FeO、
2 3
MnO、CuO)为原料制备纳米氧化锌的工艺流程如图:
如表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1 mol·L-1计算)。
金属离子 Fe3+ Fe2+ Cu2+ Zn2+ Mn2+
开始沉淀的pH 1.5 6.3 6.0 6.2 8.1
完全沉淀的pH 2.8 8.3 8.0 8.2 10.1
( 1 ) “ 浸 取 ” 过 程 中 盐 酸 不 宜 过 量 太 多 , 其 可 能 原 因 是
______________________________________________
______________________________。
(2)“滤渣1”的成分是MnO 、Fe(OH) 。“氧化除杂”过程中KMnO 与Mn2+发生反应的离子方程式为
2 3 4
_______________________________________________________,溶液pH范围应控制在___________________。
化工流程与条件控制
1.流程中反应条件的控制
条件控制 答题指导
①使金属离子全部转化_______________沉淀,以达到除去金属离子的目的;
②抑制盐类水解;③促进盐类水解生成沉淀,有利于过滤分离;④金属离子的
控制溶液的pH 萃取率与溶液的pH密切相关
常用试剂:①酸[稀HCl、HSO 、HNO(注意氧化性)]、酸性气体;②碱
2 4 3
[NaOH、NH ·HO];③盐[NaCO、NaHCO 、NH HCO ];④金属氧化物
3 2 2 3 3 4 3
①酸浸时提高酸的浓度可提高矿石中某金属元素的浸取率(量不能太多,有时后
续除杂时还会加碱,会多消耗碱);②增大便宜、易得的反应物的浓度,可以提
反应物用量或浓度
高其他物质的利用率,使反应充分进行;③增大物质浓度可以加快
___________,使平衡发生移动等
①转化为目标产物的价态;②除去杂质离子[如把Fe2+氧化成Fe3+,而后调溶
加入氧化剂(或还原剂)
液的pH,使其转化为_________沉淀除去]
①如加入硫化钠、硫化铵、_________,转化为硫化物沉淀;②加入可溶性碳
加入沉淀剂
酸盐,生成碳酸盐沉淀;③加入_________,除去Ca2+、Mg2+
加热煮沸 促进水解,聚沉后利于过滤分离
趁热过滤 防止某物质降温时会_________
①防止某物质在高温时_________、挥发(或分解);②使化学平衡向着题目要
求的方向(放热反应方向)移动;③使某个沸点较高的产物液化,使其与其他物
降温
质分离等;④降低某些晶体的____________,减少损失;④降温(或减压)可以
控制温度 减少能源成本,降低对设备的要求等
(常用水浴、冰 ①使溶液中的气体_________;②使易挥发的物质_________出来;③促进水
升温
水浴或油浴) 解,聚沉后便于____________
①结晶获得所需物质;②防止某种物质(如HO 、草酸、浓硝酸、铵盐等)温
2 2
控温 度过高时会_________或挥发;③适宜的温度使催化剂的活性达到最好;④防
止____________的发生等
2.结合沉淀溶解平衡进行的条件控制
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找①运用K 计算反应所需要的pH条件。
sp
②根据题目要求计算某条件下的离子浓度、需要加入的试剂量等。
考点精练
温度的控制
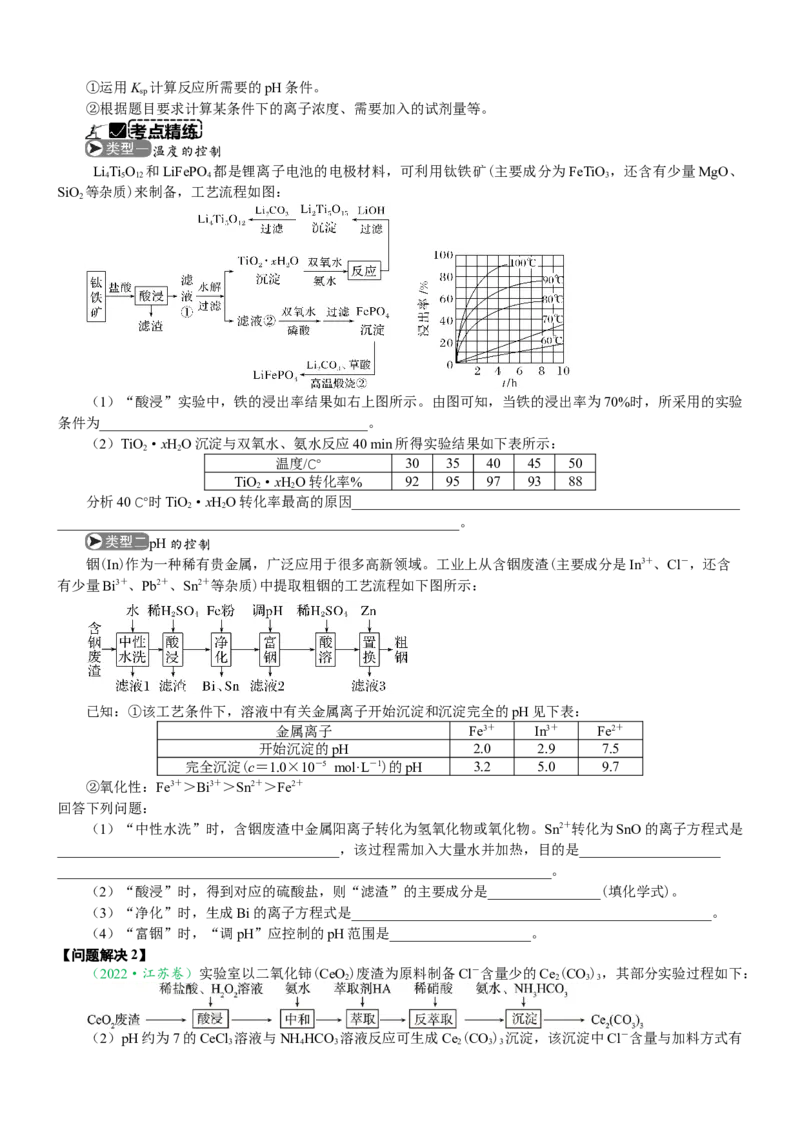
LiTi O 和LiFePO 都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO ,还含有少量MgO、
4 5 12 4 3
SiO 等杂质)来制备,工艺流程如图:
2
(1)“酸浸”实验中,铁的浸出率结果如右上图所示。由图可知,当铁的浸出率为70%时,所采用的实验
条件为______________________________________。
(2)TiO·xHO沉淀与双氧水、氨水反应40 min所得实验结果如下表所示:
2 2
温度/℃ 30 35 40 45 50
TiO·xHO转化率% 92 95 97 93 88
2 2
分析40 ℃时TiO·xHO转化率最高的原因_______________________________________________________
2 2
_________________________________________________________。
pH的控制
铟(In)作为一种稀有贵金属,广泛应用于很多高新领域。工业上从含铟废渣(主要成分是In3+、Cl-,还含
有少量Bi3+、Pb2+、Sn2+等杂质)中提取粗铟的工艺流程如下图所示:
已知:①该工艺条件下,溶液中有关金属离子开始沉淀和沉淀完全的pH见下表:
金属离子 Fe3+ In3+ Fe2+
开始沉淀的pH 2.0 2.9 7.5
完全沉淀(c=1.0×10-5 mol·L-1)的pH 3.2 5.0 9.7
②氧化性:Fe3+>Bi3+>Sn2+>Fe2+
回答下列问题:
(1)“中性水洗”时,含铟废渣中金属阳离子转化为氢氧化物或氧化物。Sn2+转化为SnO的离子方程式是
________________________________________,该过程需加入大量水并加热,目的是____________________
______________________________________________________________________。
(2)“酸浸”时,得到对应的硫酸盐,则“滤渣”的主要成分是________________(填化学式)。
(3)“净化”时,生成Bi的离子方程式是___________________________________________________。
(4)“富铟”时,“调pH”应控制的pH范围是____________________。
【问题解决2】
(2022·江苏卷)实验室以二氧化铈(CeO)废渣为原料制备Cl-含量少的Ce (CO) ,其部分实验过程如下:
2 2 3 3
(2)pH约为7的CeCl 溶液与NH HCO 溶液反应可生成Ce (CO) 沉淀,该沉淀中Cl-含量与加料方式有
3 4 3 2 3 3微专题突破6 无机化工流程题透视 问题的态度:问则少;辩则明
关。得到含Cl-量较少的Ce (CO) 的加料方式为__________(填序号)。
2 3 3
A.将NH HCO 溶液滴加到CeCl 溶液中
4 3 3
B.将CeCl 溶液滴加到NH HCO 溶液中
3 4 3
(3)通过中和、萃取、反萃取、沉淀等过程,可制备Cl-含量少的Ce (CO) 。已知Ce3+能被有机萃取剂
2 3 3
(简称HA)萃取,其萃取原理可表示为Ce3+(水层)+3HA(有机层) CeA(有机层)+3H+(水层)
3
①加氨水“中和”去除过量盐酸,使溶液接近中性。去除过量盐酸的目的是___________________________
____________________________________________________________________。
②反萃取的目的是将有机层Ce3+转移到水层。为使Ce3+尽可能多地发生上述转移,应选择的实验条件或采
取的实验操作有_____________________________________________________________________(填两项)。
③与“反萃取”得到的水溶液比较,过滤 Ce (CO) 溶液的滤液中,物质的量减小的离子有
2 3 3
_________________(填化学式)。
化工流程与反应原理
1.原理型化工流程题是以物质制备流程为主线,主要考查考生运用化学平衡原理、化学反应与能量变化、
电化学等知识来解决化工生产中实际问题的能力。
2.解答此类型题目的基本步骤是:(1)从题干中获取有用信息,了解生产的产品;(2)分析流程中的每
一步骤,如:每一步骤中反应物是什么,发生了什么反应,该反应造成了什么后果,对制取产品有什么作用;
(3)从题中获取信息,运用化学反应原理分析制备产品的最佳条件,帮助解题。
3.化学工艺流程图题常考查的主要化学反应原理
① 沉淀溶解平衡的相关应用 ①沉淀的最小浓度控制;②沉淀的转化条件;③不同离子的分步沉淀
反应速率及化学平衡理论在 ①反应速率的控制(如温度等);②化学平衡的移动(如浓度、温度
②
实际生产中的应用 等);③化学平衡常数的计算与应用;④反应条件的控制
③ 盐类水解的具体应用 ①抑制盐的水解;②水解反应的规律;③水解反应的控制
氧化还原反应规律及其运用 ① 反应的________规律;②反应的________规律;③反应
④
的选择规律
4.试题中会出现一些化工术语如水(或酸)浸、苛化、煅烧、脱硫、提取、热过滤、水热处理、表面处理等,
实际考查的是化学反应原理(包括化学平衡原理、水解原理)或相关实验操作,以及绿色化学观念和从经济的视
角分析实际生产中各种问题的能力。因此试题的解答始于对各阶段流程的化学原理的分析。图示如下:
考点精练
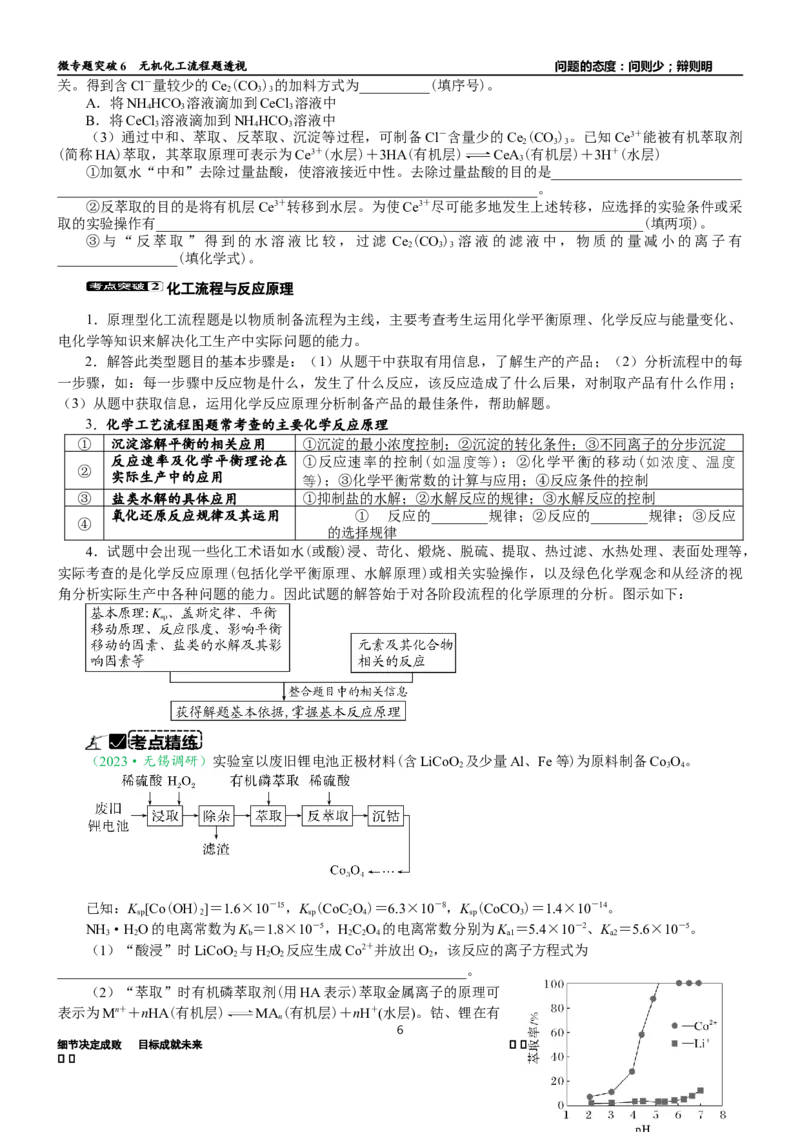
(2023·无锡调研)实验室以废旧锂电池正极材料(含LiCoO 及少量Al、Fe等)为原料制备Co O。
2 3 4
已知:K [Co(OH)]=1.6×10-15,K (CoC O)=6.3×10-8,K (CoCO)=1.4×10-14。
sp 2 sp 2 4 sp 3
NH ·HO的电离常数为K =1.8×10-5,HC O 的电离常数分别为K =5.4×10-2、K =5.6×10-5。
3 2 b 2 2 4 a1 a2
(1)“酸浸”时LiCoO 与HO 反应生成Co2+并放出O,该反应的离子方程式为
2 2 2 2
__________________________________________________________。
(2)“萃取”时有机磷萃取剂(用HA表示)萃取金属离子的原理可
表示为Mn++nHA(有机层) MA (有机层)+nH+(水层)。钴、锂在有
n
6
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找机磷萃取剂中的萃取率与pH的关系如图所示。随pH的升高,Co2+在有机磷萃取剂中萃取率增大的原因是
________________________________
_______________________________________________________。
(3)“反萃取”的目的是将有机层中Co2+转移到水层。使Co2+尽可能多地发生上述转移,应选择的实验
条件或采取的实验操作有
__________________________________________________________________________________(填两项)。
(4)“沉钴”时,可加入HC O 溶液或(NH )C O 溶液反应制得CoC O。
2 2 4 4 2 2 4 2 4
①若用HC O 溶液作沉淀剂,反应Co2++HC O CoC O+2H+的平衡常数K的数值为________。
2 2 4 2 2 4 2 4
②不能用NaC O 溶液代替(NH )C O 溶液的原因是
2 2 4 4 2 2 4
_______________________________________________________________。
【问题解决3】
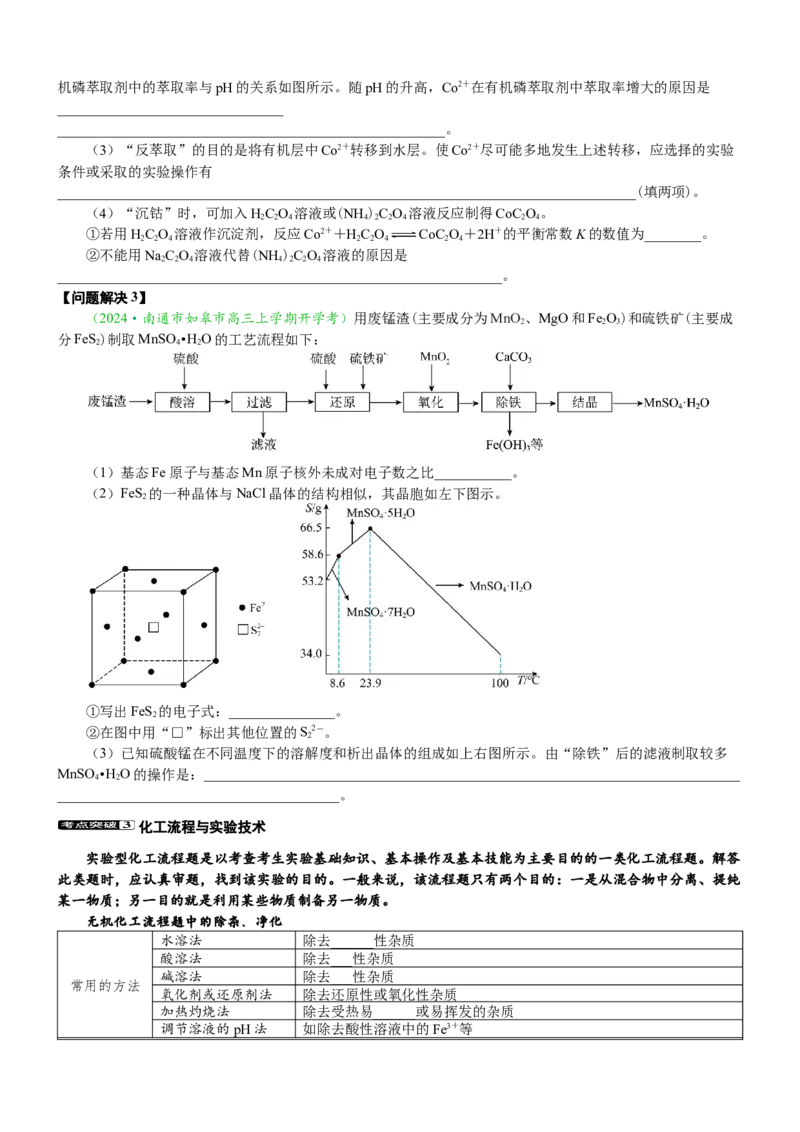
(2024·南通市如皋市高三上学期开学考)用废锰渣(主要成分为MnO 、MgO和Fe O)和硫铁矿(主要成
2 2 3
分FeS)制取MnSO •HO的工艺流程如下:
2 4 2
(1)基态Fe原子与基态Mn原子核外未成对电子数之比___________。
(2)FeS 的一种晶体与NaCl晶体的结构相似,其晶胞如左下图示。
2
①写出FeS 的电子式:_______________。
2
②在图中用“□”标出其他位置的S2-。
2
(3)已知硫酸锰在不同温度下的溶解度和析出晶体的组成如上右图所示。由“除铁”后的滤液制取较多
MnSO •HO的操作是:____________________________________________________________________________
4 2
________________________________________。
化工流程与实验技术
实验型化工流程题是以考查考生实验基础知识、基本操作及基本技能为主要目的的一类化工流程题。解答
此类题时,应认真审题,找到该实验的目的。一般来说,该流程题只有两个目的:一是从混合物中分离、提纯
某一物质;另一目的就是利用某些物质制备另一物质。
无机化工流程题中的除杂、净化
水溶法 除去______性杂质
酸溶法 除去___性杂质
碱溶法 除去___性杂质
常用的方法
氧化剂或还原剂法 除去还原性或氧化性杂质
加热灼烧法 除去受热易______或易挥发的杂质
调节溶液的pH法 如除去酸性溶液中的Fe3+等微专题突破6 无机化工流程题透视 问题的态度:问则少;辩则明
过滤(热滤或抽滤) 分离难溶物和易溶物,根据特殊需要采用______过滤或者______等方
法
利用溶质在互不相溶的溶剂里的溶解度不同提取分离物质,如用CCl
萃取和分液 4
或苯萃取溴水中的溴
蒸发结晶 提取溶解度随温度变化______的溶质,如从溶液中提取NaCl
常用的操作
提取溶解度随温度变化______的溶质、易水解的溶质或结晶水合物,
冷却结晶
如KNO、FeCl 、CuCl 、CuSO ·5HO、FeSO ·7HO等
3 3 2 4 2 4 2
蒸馏或分馏 分离______不同且互溶的液体混合物,如分离乙醇或甘油
利用气体易液化的特点分离气体,如合成氨工业采用冷却法分离平衡
冷却法
混合气体中的氨气
考点精练
(2022·湖北卷)全球对锂资源的需求不断增长,“盐湖提锂”越来越受到重视。某兴趣小组取盐湖水进
行浓缩和初步除杂后,得到浓缩卤水(含有Na+、Li+、Cl-和少量Mg2+、Ca2+),并设计了以下流程通过制备碳
酸锂来提取锂。
25 ℃时相关物质的参数如下:
LiOH的溶解度:12.4 g/100 g H O
2
化合物 K
sp
Mg(OH) 5.6×10-12
2
Ca(OH) 5.5×10-6
2
CaCO 2.8×10-9
3
LiCO 2.5×10-2
2 3
回答下列问题:
(1)“沉淀1”为_______________。
( 2 ) 向 “ 滤 液 1” 中 加 入 适 量 固 体 LiCO 的 目 的 是
2 3
_________________________________________________。
(3)为提高LiCO 的析出量和纯度,“操作A”依次为________________、________________、洗涤。
2 3
(4)有同学建议用“侯氏制碱法”的原理制备LiCO。查阅资料后,发现文献对常温下的LiHCO 有不同
2 3 3
的描述:①是白色固体;②尚未从溶液中分离出来。为探究LiHCO 的性质,将饱和LiCl溶液与饱和NaHCO
3 3
溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。上述现象说明,在
该实验条件下LiHCO ____________(填“稳定”或“不稳定”),有关反应的离子方程式为
3
_____________________________________________________________________________________。
(5)他们结合(4)的探究结果,拟将原流程中向“滤液2”加入NaCO 改为通入CO 。这一改动能否达
2 3 2
到相同的效果,作出你的判断并给出理由_____________________________________________________________
______________________________________________________________________________________。
【问题解决4】
8
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
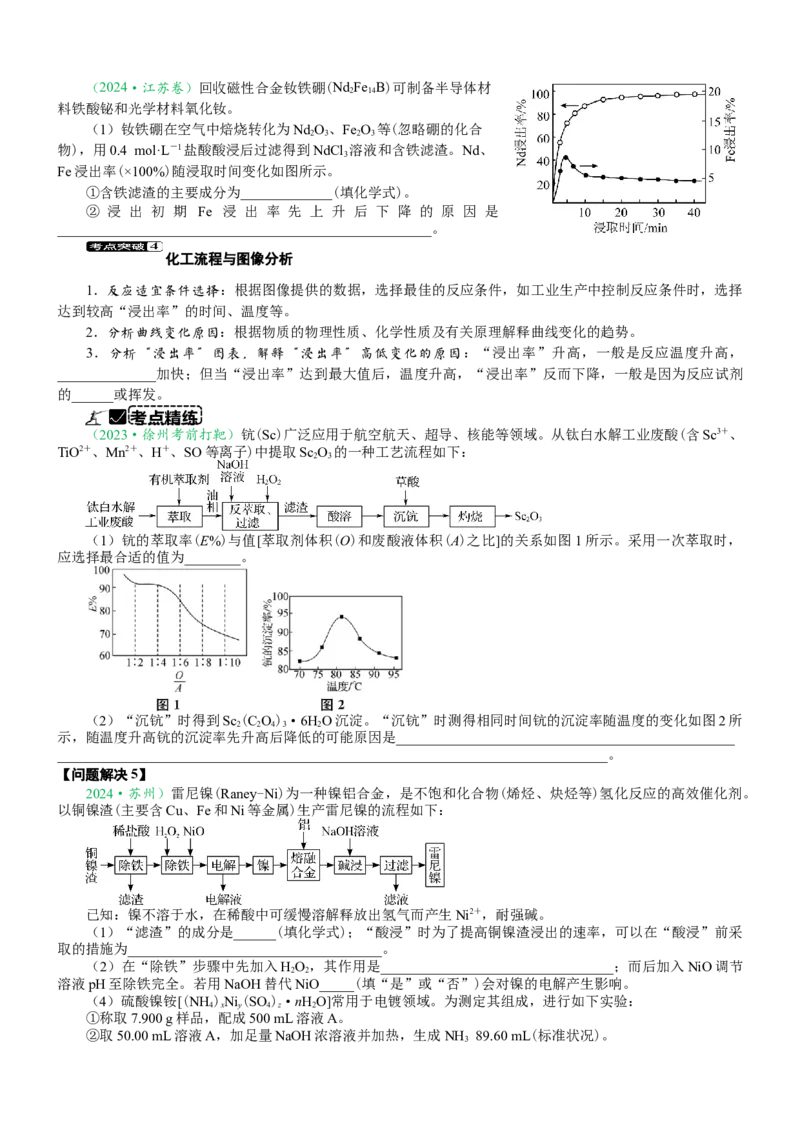
找找(2024·江苏卷)回收磁性合金钕铁硼(Nd Fe B)可制备半导体材
2 14
料铁酸铋和光学材料氧化钕。
(1)钕铁硼在空气中焙烧转化为Nd O、Fe O 等(忽略硼的化合
2 3 2 3
物),用0.4 mol·L-1盐酸酸浸后过滤得到NdCl 溶液和含铁滤渣。Nd、
3
Fe浸出率(×100%)随浸取时间变化如图所示。
①含铁滤渣的主要成分为_____________(填化学式)。
② 浸 出 初 期 Fe 浸 出 率 先 上 升 后 下 降 的 原 因 是
_____________________________________________________。
化工流程与图像分析
1.反应适宜条件选择:根据图像提供的数据,选择最佳的反应条件,如工业生产中控制反应条件时,选择
达到较高“浸出率”的时间、温度等。
2.分析曲线变化原因:根据物质的物理性质、化学性质及有关原理解释曲线变化的趋势。
3.分析“浸出率”图表,解释“浸出率”高低变化的原因:“浸出率”升高,一般是反应温度升高,
______________加快;但当“浸出率”达到最大值后,温度升高,“浸出率”反而下降,一般是因为反应试剂
的______或挥发。
考点精练
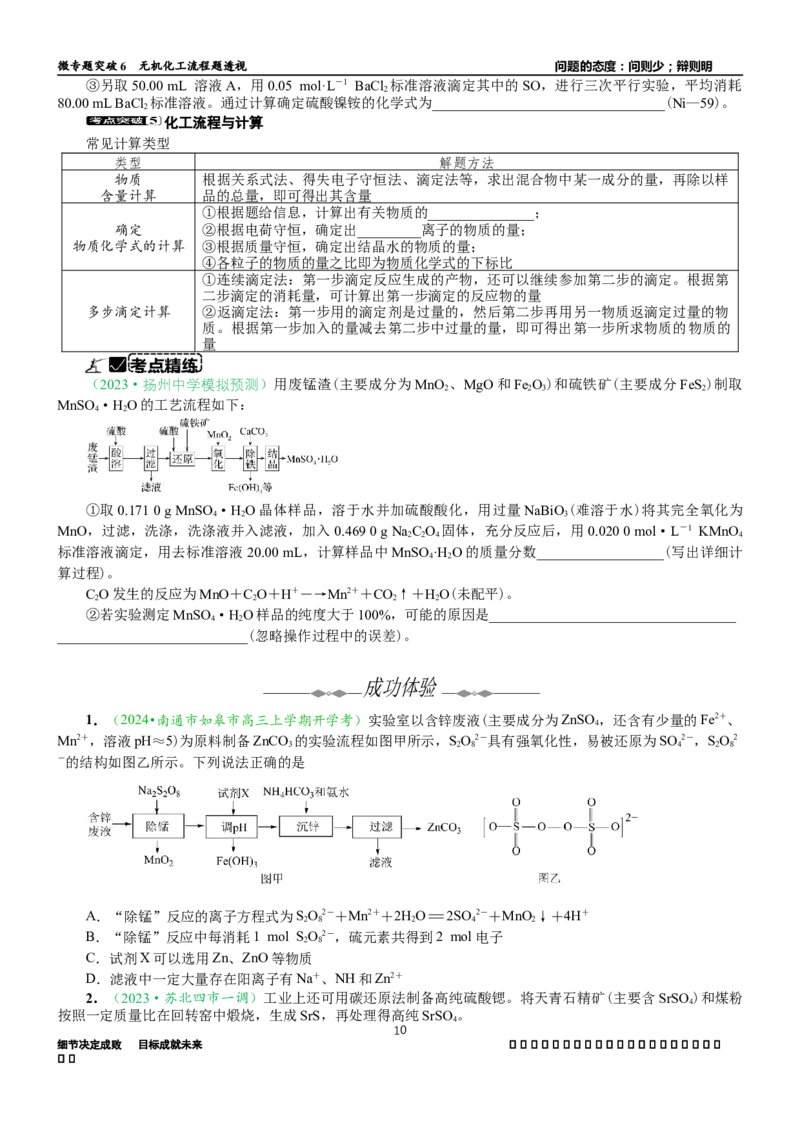
(2023·徐州考前打靶)钪(Sc)广泛应用于航空航天、超导、核能等领域。从钛白水解工业废酸(含Sc3+、
TiO2+、Mn2+、H+、SO等离子)中提取Sc O 的一种工艺流程如下:
2 3
(1)钪的萃取率(E%)与值[萃取剂体积(O)和废酸液体积(A)之比]的关系如图1所示。采用一次萃取时,
应选择最合适的值为________。
(2)“沉钪”时得到Sc (C O)·6HO沉淀。“沉钪”时测得相同时间钪的沉淀率随温度的变化如图2所
2 2 4 3 2
示,随温度升高钪的沉淀率先升高后降低的可能原因是________________________________________________
______________________________________________________________________________。
【问题解决5】
2024·苏州)雷尼镍(Raney-Ni)为一种镍铝合金,是不饱和化合物(烯烃、炔烃等)氢化反应的高效催化剂。
以铜镍渣(主要含Cu、Fe和Ni等金属)生产雷尼镍的流程如下:
已知:镍不溶于水,在稀酸中可缓慢溶解释放出氢气而产生Ni2+,耐强碱。
(1)“滤渣”的成分是______(填化学式);“酸浸”时为了提高铜镍渣浸出的速率,可以在“酸浸”前采
取的措施为____________________________________。
(2)在“除铁”步骤中先加入HO ,其作用是_________________________________;而后加入NiO调节
2 2
溶液pH至除铁完全。若用NaOH替代NiO_____(填“是”或“否”)会对镍的电解产生影响。
(4)硫酸镍铵[(NH )Ni(SO )·nHO]常用于电镀领域。为测定其组成,进行如下实验:
4 x y 4 z 2
①称取7.900 g样品,配成500 mL溶液A。
②取50.00 mL溶液A,加足量NaOH浓溶液并加热,生成NH 89.60 mL(标准状况)。
3微专题突破6 无机化工流程题透视 问题的态度:问则少;辩则明
③另取50.00 mL 溶液A,用0.05 mol·L-1 BaCl 标准溶液滴定其中的SO,进行三次平行实验,平均消耗
2
80.00 mL BaCl 标准溶液。通过计算确定硫酸镍铵的化学式为_________________________________(Ni—59)。
2
化工流程与计算
常见计算类型
类型 解题方法
物质 根据关系式法、得失电子守恒法、滴定法等,求出混合物中某一成分的量,再除以样
含量计算 品的总量,即可得出其含量
①根据题给信息,计算出有关物质的_______________;
确定 ②根据电荷守恒,确定出_________离子的物质的量;
物质化学式的计算 ③根据质量守恒,确定出结晶水的物质的量;
④各粒子的物质的量之比即为物质化学式的下标比
①连续滴定法:第一步滴定反应生成的产物,还可以继续参加第二步的滴定。根据第
二步滴定的消耗量,可计算出第一步滴定的反应物的量
多步滴定计算 ②返滴定法:第一步用的滴定剂是过量的,然后第二步再用另一物质返滴定过量的物
质。根据第一步加入的量减去第二步中过量的量,即可得出第一步所求物质的物质的
量
考点精练
(2023·扬州中学模拟预测)用废锰渣(主要成分为MnO 、MgO和Fe O)和硫铁矿(主要成分FeS)制取
2 2 3 2
MnSO ·HO的工艺流程如下:
4 2
①取0.171 0 g MnSO ·HO晶体样品,溶于水并加硫酸酸化,用过量NaBiO(难溶于水)将其完全氧化为
4 2 3
MnO,过滤,洗涤,洗涤液并入滤液,加入0.469 0 g Na C O 固体,充分反应后,用0.020 0 mol·L-1 KMnO
2 2 4 4
标准溶液滴定,用去标准溶液20.00 mL,计算样品中MnSO ·H O的质量分数__________________(写出详细计
4 2
算过程)。
C O发生的反应为MnO+C O+H+―→Mn2++CO↑+HO(未配平)。
2 2 2 2
②若实验测定MnSO ·HO样品的纯度大于100%,可能的原因是___________________________________
4 2
___________________________(忽略操作过程中的误差)。
成功体验
1.(2024•南通市如皋市高三上学期开学考)实验室以含锌废液(主要成分为ZnSO,还含有少量的Fe2+、
4
Mn2+,溶液pH≈5)为原料制备ZnCO 的实验流程如图甲所示,SO2-具有强氧化性,易被还原为SO 2-,SO2
3 2 8 4 2 8
-的结构如图乙所示。下列说法正确的是
A.“除锰”反应的离子方程式为SO2-+Mn2++2HO=2SO 2-+MnO ↓+4H+
2 8 2 4 2
B.“除锰”反应中每消耗1 mol SO2-,硫元素共得到2 mol电子
2 8
C.试剂X可以选用Zn、ZnO等物质
D.滤液中一定大量存在阳离子有Na+、NH和Zn2+
2.(2023·苏北四市一调)工业上还可用碳还原法制备高纯硫酸锶。将天青石精矿(主要含SrSO )和煤粉
4
按照一定质量比在回转窑中煅烧,生成SrS,再处理得高纯SrSO 。
4
10
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
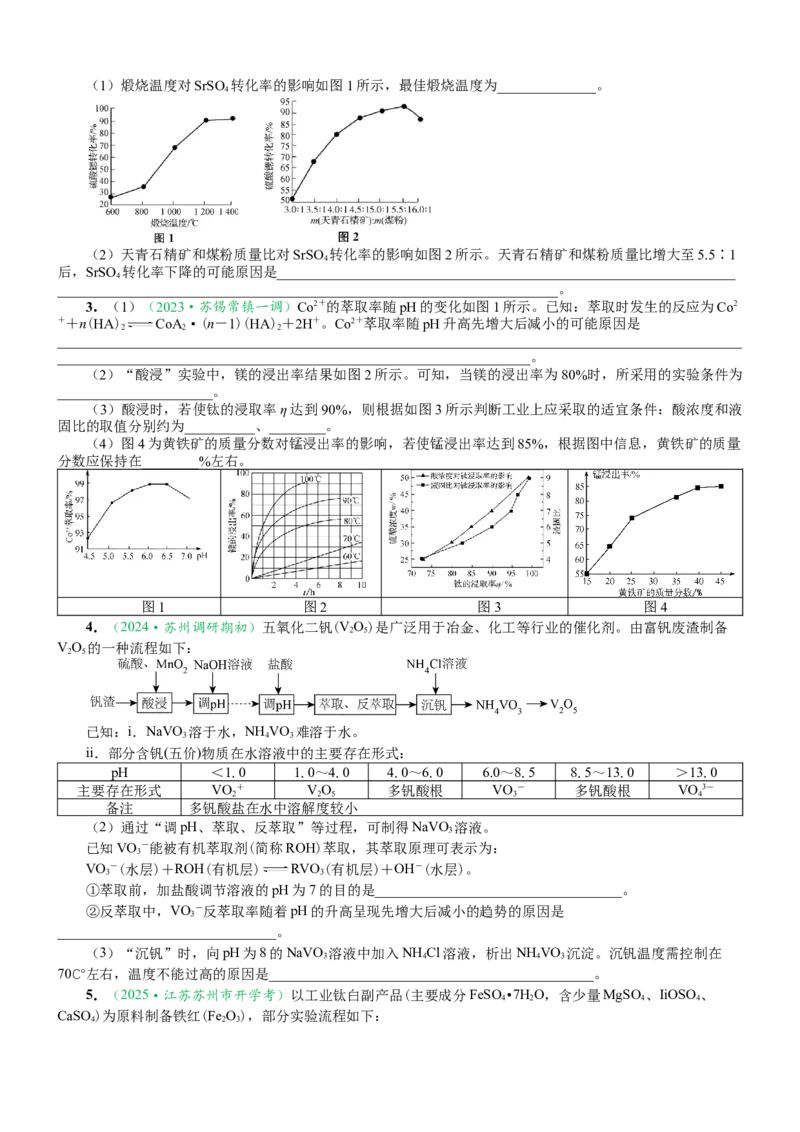
找找(1)煅烧温度对SrSO 转化率的影响如图1所示,最佳煅烧温度为______________。
4
(2)天青石精矿和煤粉质量比对SrSO 转化率的影响如图2所示。天青石精矿和煤粉质量比增大至5.5∶1
4
后,SrSO 转化率下降的可能原因是_________________________________________________________________
4
_______________________________________________________________________。
3.(1)(2023·苏锡常镇一调)Co2+的萃取率随pH的变化如图1所示。已知:萃取时发生的反应为Co2
++n(HA) CoA·(n-1)(HA)+2H+。Co2+萃取率随pH升高先增大后减小的可能原因是
2 2 2
_________________________________________________________________________________________________
___________________________________________________________________。
(2)“酸浸”实验中,镁的浸出率结果如图2所示。可知,当镁的浸出率为80%时,所采用的实验条件为
______________________。
(3)酸浸时,若使钛的浸取率η达到90%,则根据如图3所示判断工业上应采取的适宜条件:酸浓度和液
固比的取值分别约为__________、________。
(4)图4为黄铁矿的质量分数对锰浸出率的影响,若使锰浸出率达到85%,根据图中信息,黄铁矿的质量
分数应保持在________%左右。
图1 图2 图3 图4
4.(2024·苏州调研期初)五氧化二钒(VO)是广泛用于冶金、化工等行业的催化剂。由富钒废渣制备
2 5
VO 的一种流程如下:
2 5
已知:i.NaVO 溶于水,NH VO 难溶于水。
3 4 3
ii.部分含钒(五价)物质在水溶液中的主要存在形式:
pH <1.0 1.0~4.0 4.0~6.0 6.0~8.5 8.5~13.0 >13.0
主要存在形式 VO + VO 多钒酸根 VO - 多钒酸根 VO3-
2 2 5 3 4
备注 多钒酸盐在水中溶解度较小
(2)通过“调pH、萃取、反萃取”等过程,可制得NaVO 溶液。
3
已知VO -能被有机萃取剂(简称ROH)萃取,其萃取原理可表示为:
3
VO -(水层)+ROH(有机层) RVO (有机层)+OH-(水层)。
3 3
①萃取前,加盐酸调节溶液的pH为7的目的是___________________________________。
②反萃取中,VO -反萃取率随着pH的升高呈现先增大后减小的趋势的原因是
3
_______________________________。
(3)“沉钒”时,向pH为8的NaVO 溶液中加入NH Cl溶液,析出NH VO 沉淀。沉钒温度需控制在
3 4 4 3
70℃左右,温度不能过高的原因是______________________________________________。
5.(2025·江苏苏州市开学考)以工业钛白副产品(主要成分FeSO •7HO,含少量MgSO 、IiOSO 、
4 2 4 4
CaSO)为原料制备铁红(Fe O),部分实验流程如下:
4 2 3微专题突破6 无机化工流程题透视 问题的态度:问则少;辩则明
I.精制FeSO
4
(1)“除钛”时,利用TiOSO 电离出的TiO2+水解,生成HTiO 沉淀。
4 2 3
①TiO2+水解的离子方程式为____________________________________。
②加入Fe粉的作用是___________________________________。
(2)“除镁钙”时,当溶液中Mg2+和Ca2+沉淀完全时,溶液中F-浓度最小值为___________mol·L-1。
[已知:K (CaF)=1.0×10-10,K (MgF)=7.5×10-11;当离子浓度≤10-5 mol·L-1认为沉淀完全]
sp 2 sp 2
Ⅱ.制铁红(Fe O)
2 3
方法一:FeSO 精制液与NH HCO 溶液反应生成FeCO 沉淀,再用O 将FeCO 氧化为铁红。
4 4 3 3 2 3
(3)补充完成由FeSO 精制液制备FeCO 的实验方案:70℃下将精制液浓缩成饱和溶液,___________,
4 3
干燥,得到FeCO。[FeCO 沉淀需“洗涤完全”,Fe(OH) 开始沉淀的pH=6.5]
3 3 2
(4)70℃时,O 将FeCO 的化学方程式为_______________________________________。
2 3
方法二:精制液与NaNO 、HSO 、O 反应生成铁黄(FeOOH),再由铁黄制取铁红。
2 2 4 2
(5)NaNO 、HSO 产生的NO 作催化剂,使精制FeSO 溶液被O 氧化为铁黄。其中NO作催化剂时分两
2 2 4 x 4 2
步进行:第一步反应为Fe2++NO=Fe(NO)2+,第二步反应的离子方程式为
_______________________________________________________________________________。
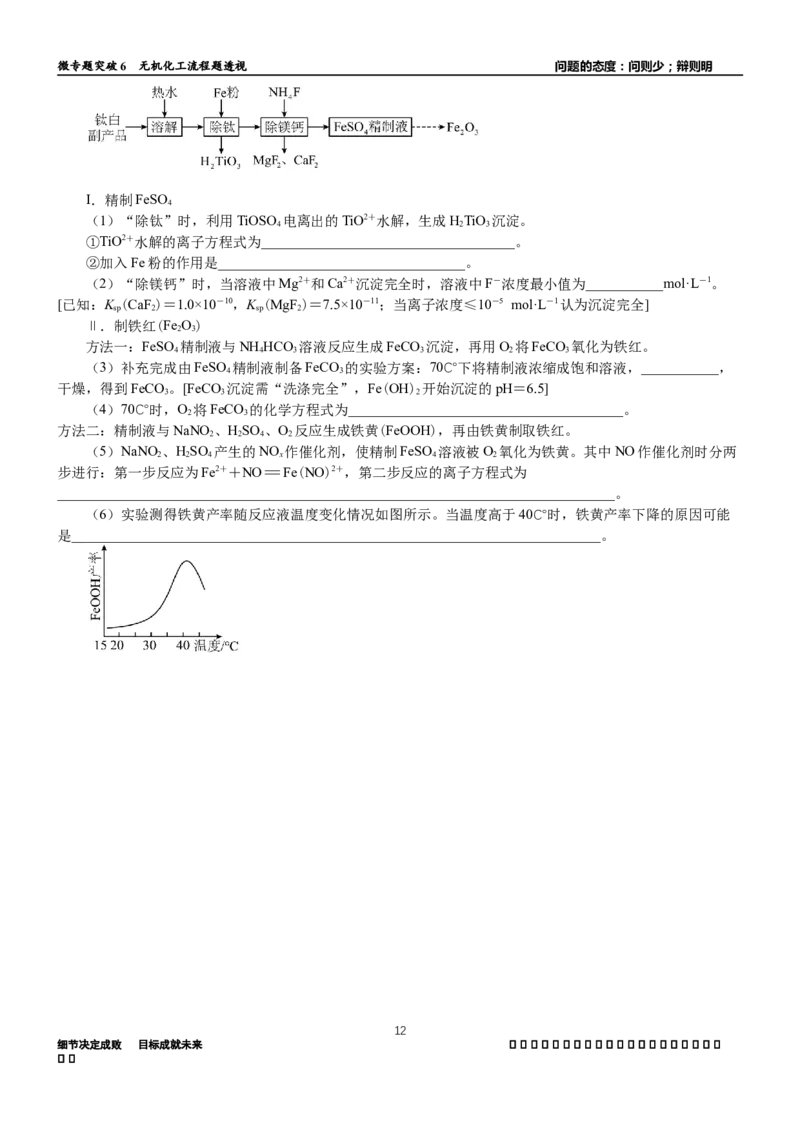
(6)实验测得铁黄产率随反应液温度变化情况如图所示。当温度高于40℃时,铁黄产率下降的原因可能
是___________________________________________________________________________。
12
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找