文档内容
微考点 电解质溶液的图像分析
目录
.............................................................................................................................................1
1.高考真题考点分布...................................................................................................................................1
2.命题规律及备考策略...............................................................................................................................1
.............................................................................................................................................2
考法01 电解质溶液微粒变化图像...........................................................................................................2
考法02 沉淀溶解平衡图像.......................................................................................................................9
...........................................................................................................................................15
1.高考真题考点分布
考点内容 考点分布
电解质溶液微粒变 2023湖南卷,3分;2022河北卷,3分;2022浙江卷,2分;2022福建卷,4分;
化图像 2022浙江卷,2分;2021浙江卷,2分;2021浙江卷,2分;2021湖南卷,3分;
沉淀溶解平衡图像 2024·辽宁卷,3分;2024·浙江卷,3分;2024·湖北卷,3分;2024·全国甲卷,6
分;2023辽宁卷,3分;2023全国甲卷,6分;2023新课标卷,6分;2023山东
卷,4分;2023北京卷,3分;2022福建卷,4分;2022湖南卷,3分;2022山东
卷,4分;
2022海南卷,4分;
2.命题规律及备考策略
【命题规律】
高频考点从近几年全国高考试题来看,酸碱中和滴定、沉淀滴定、沉淀溶解平衡曲线、中和滴定曲线、对
数曲线等仍是高考命题的热点。
【备考策略】【命题预测】
预计2025年高考会以新的情境载体考查沉淀溶解平衡曲线、中和滴定曲线、对数曲线、分布曲线等知识,
考查数形结合能力、信息整合能力,题目难度一般较大。
考法01 电解质溶液微粒变化图像
1.滴定曲线特殊点的分析
(1)强酸与强碱滴定过程中pH曲线
(以0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1盐酸为例)
(2)强酸(碱)滴定弱碱(酸)pH曲线比较
盐酸滴定等浓度等体积的氢氧化钠、氨水的滴定曲
氢氧化钠滴定等浓度等体积的盐酸、醋酸的滴定曲线
线
曲线起点不同:强碱滴定强酸、弱酸的曲线,强酸起点低;强酸滴定强碱、弱碱的曲线,强碱起点高
突跃点变化范围不同:强碱与强酸反应(强酸与强碱反应)的突跃点变化范围大于强碱与弱酸反应(强酸与弱
碱反应)
案例:常温下,用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1 CHCOOH溶液所得滴定曲线
3
如图:(3)pH—V图 各特殊点粒子大小关系及变化趋势
点 溶质 离子浓度大小比较
A CHCOOH
3
B(1∶1) CHCOOH、HCOONa
3 3
C(pH=7) CHCOOH、CHCOONa
3 3
D CHCOONa
3
E(2∶1) CHCOONa、NaOH
3
F(1∶1) CHCOONa、NaOH
3
(4)各特殊点对水电离程度的影响
点 溶质 水的电离情况 pH—V图
A CHCOOH 抑制
3
B CHCOOH、CHCOONa 抑制
3 3
C CHCOOH、CHCOONa 正常电离
3 3
D CHCOONa 只促进
3
E CHCOONa、NaOH 抑制
3
F CHCOONa、NaOH 抑制
3
结论:水的电离程度大小顺序为:
2.分布曲线
分布系数图及分析【分布曲线是指以pH为横坐标、分布系数(即组分的平衡浓度占总浓度的分数)为纵坐标
的关系曲线】
一元弱酸(以CHCOOH为例) 二元弱酸(以草酸HC O 为例)
3 2 2 4
δ 为CHCOOH分布系数,δ 为CHCOO-分 δ 为HC O 分布系数、δ 为HC O分布系数、δ 为C O分布
0 3 1 3 0 2 2 4 1 2 2 2
布系数 系数
1.随着pH增大,溶质分子浓度不断减小,离子浓度逐渐增大,酸根离子增多。根据分布系数可以书写一
定pH时所发生反应的离子方程式
2.同一pH条件下可以存在多种溶质微粒。根据在一定pH的微粒分布系数和酸的浓度,就可以计算各成分在该pH时的平衡浓度
3.坐标为对数或负对数的图像分析
(1)pC:类比pH,即为C离子浓度的负对数,规律是pC越大,C离子浓度越小。
(2)pK:平衡常数的负对数,规律是pK越大,平衡常数越小,对于一元弱酸(HX):pK=pH-lg ,lg 越
a
大,HX的电离程度越大。
(3)AG=lg,氢离子浓度与氢氧根离子浓度比的对数;规律是:AG越大,酸性越强,中性时AG=0。
【图像示例】
(1)pOH—pH曲线
(2)常温下,二元弱酸HY溶液中滴加NaOH溶液,所得混合溶液的pH与离子浓度变化的关系如图所示:
2
(3)常温下将KOH溶液滴加到二元弱酸(H X)溶液中,混合溶液的pH与离子浓度变化的关系图:
2
考向01 考查滴定曲线
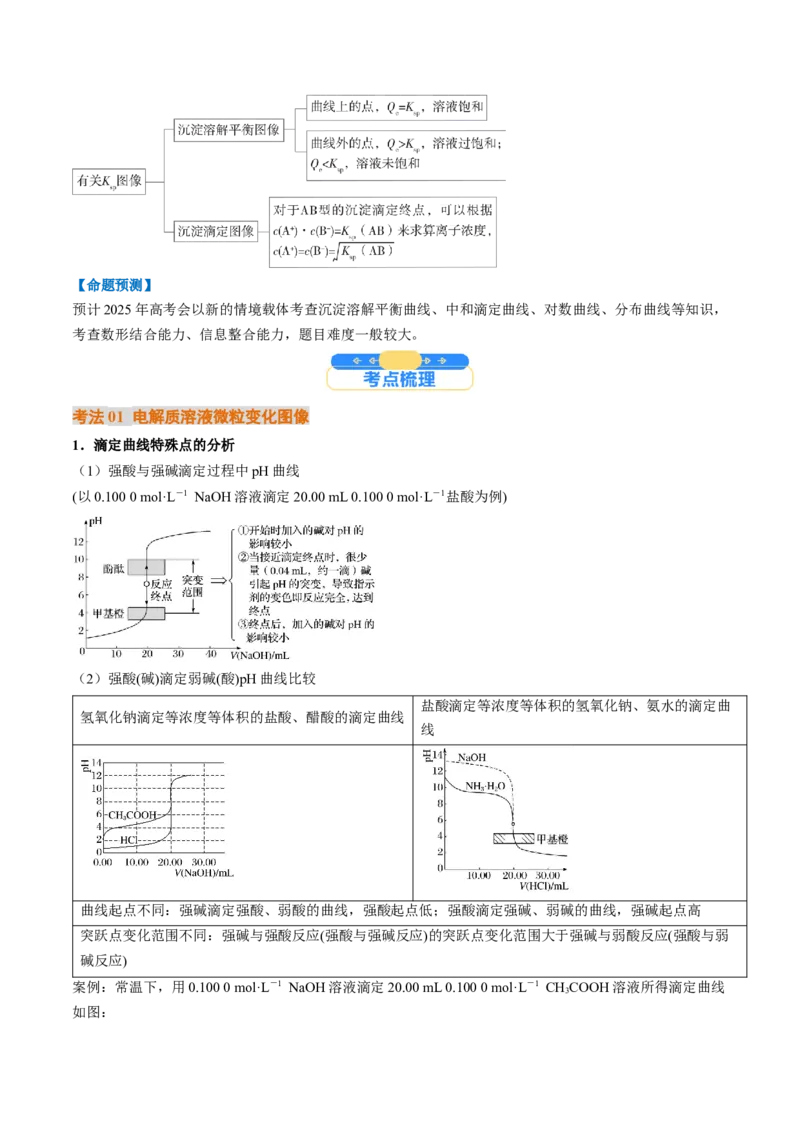
【例1】(2024·陕西商洛·模拟预测)室温下,用 的二甲胺 溶液(二甲胺在水中的电
离与一水合氨相似)滴定 盐酸溶液。溶液 随加入二甲胺溶液体积变化曲线如图所示(忽
略溶液混合时的体积变化)。下列说法正确的是A.x=1,y=7
B.a、b两点的溶液中, 不相等
C.本实验应该选择酚酞作指示剂
D.b点溶液中存在:
考向02 考查分布曲线图像
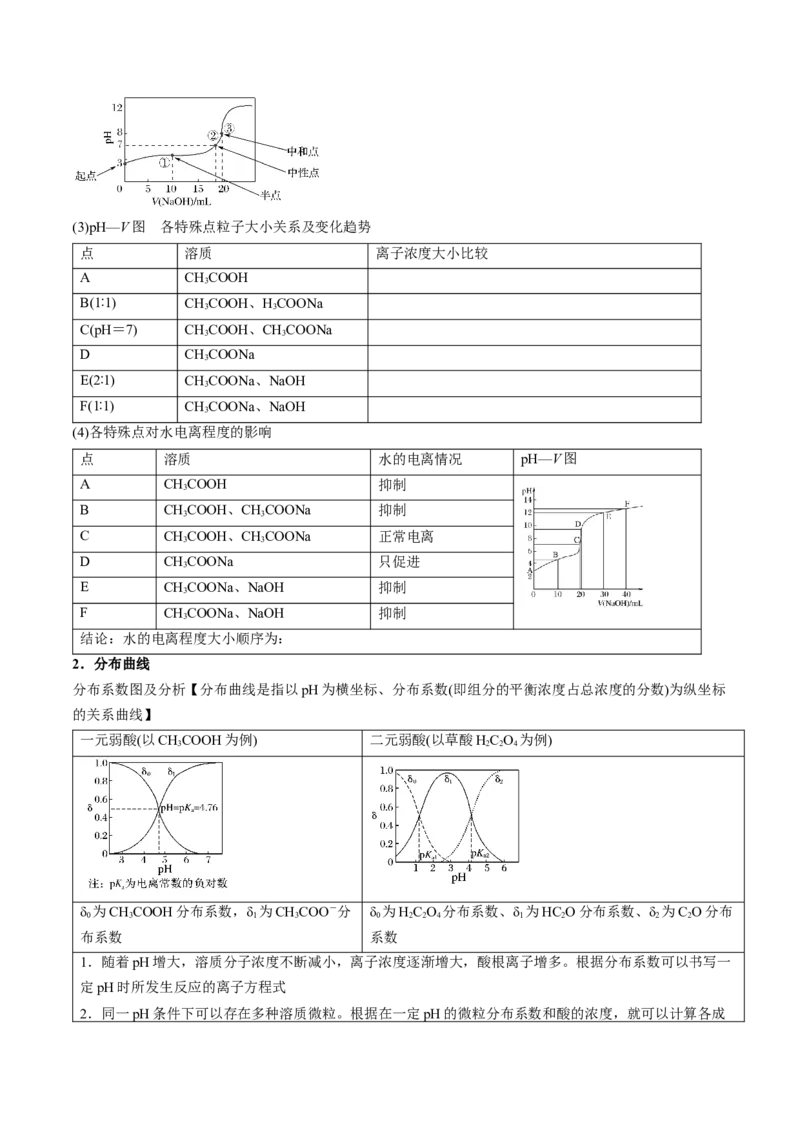
【例2】(2024·江苏苏州·模拟)HC O 为二元弱酸,20 ℃时,配制一组c(H C O)+c(HC O)+c(C O)=
2 2 4 2 2 4 2 2
0.1 mol ·L-1的HC O 和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下
2 2 4
列指定溶液中微粒的物质的量浓度关系一定正确的是( )
A.pH=2.5的溶液中:c(H C O)+c(C O)>c(HC O)
2 2 4 2 2
B.pH=7的溶液中,c(Na+)=2c(C O)
2
C.c(HC O)=c(C O)的溶液中:c(Na+)>0.1+c(HC O)
2 2 2
D.c(Na+)=0.1 mol ·L-1的溶液中:c(H+)+c(H C O)=c(OH-)+c(C O)
2 2 4 2
考向03 考查坐标为对数或负对数的图像
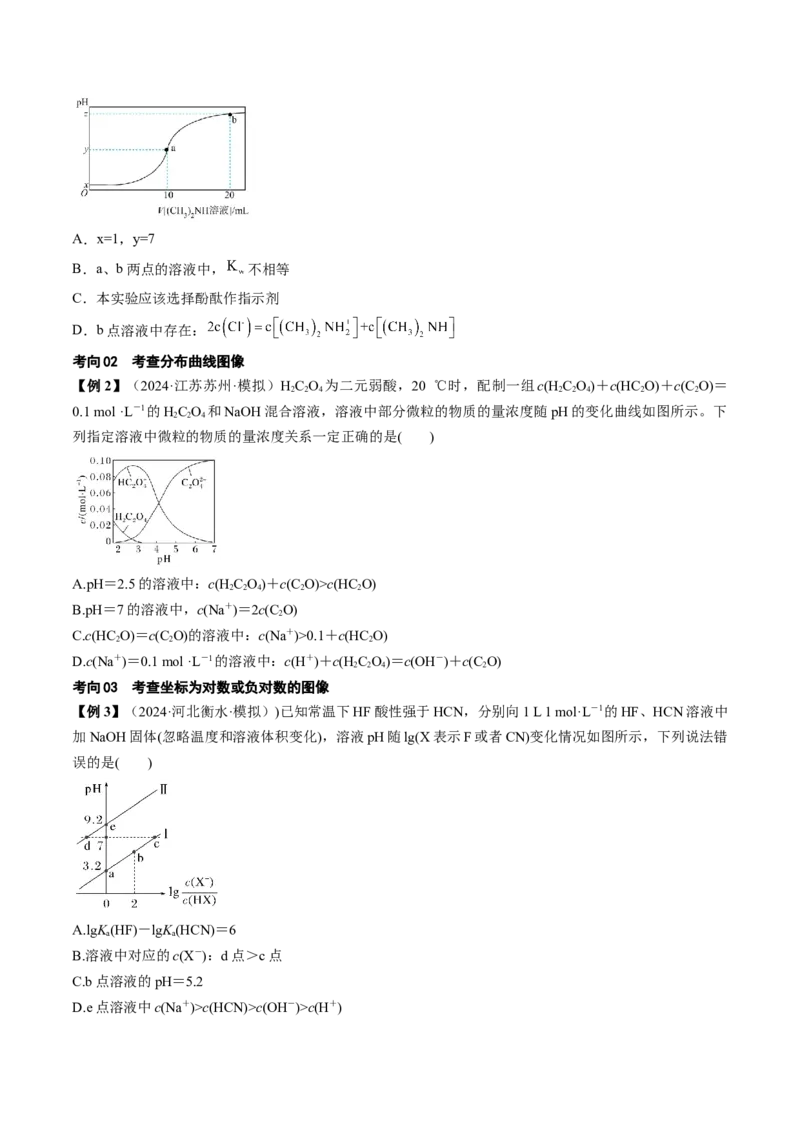
【例3】(2024·河北衡水·模拟))已知常温下HF酸性强于HCN,分别向1 L 1 mol·L-1的HF、HCN溶液中
加NaOH固体(忽略温度和溶液体积变化),溶液pH随lg(X表示F或者CN)变化情况如图所示,下列说法错
误的是( )
A.lgK(HF)-lgK(HCN)=6
a a
B.溶液中对应的c(X-):d点>c点
C.b点溶液的pH=5.2
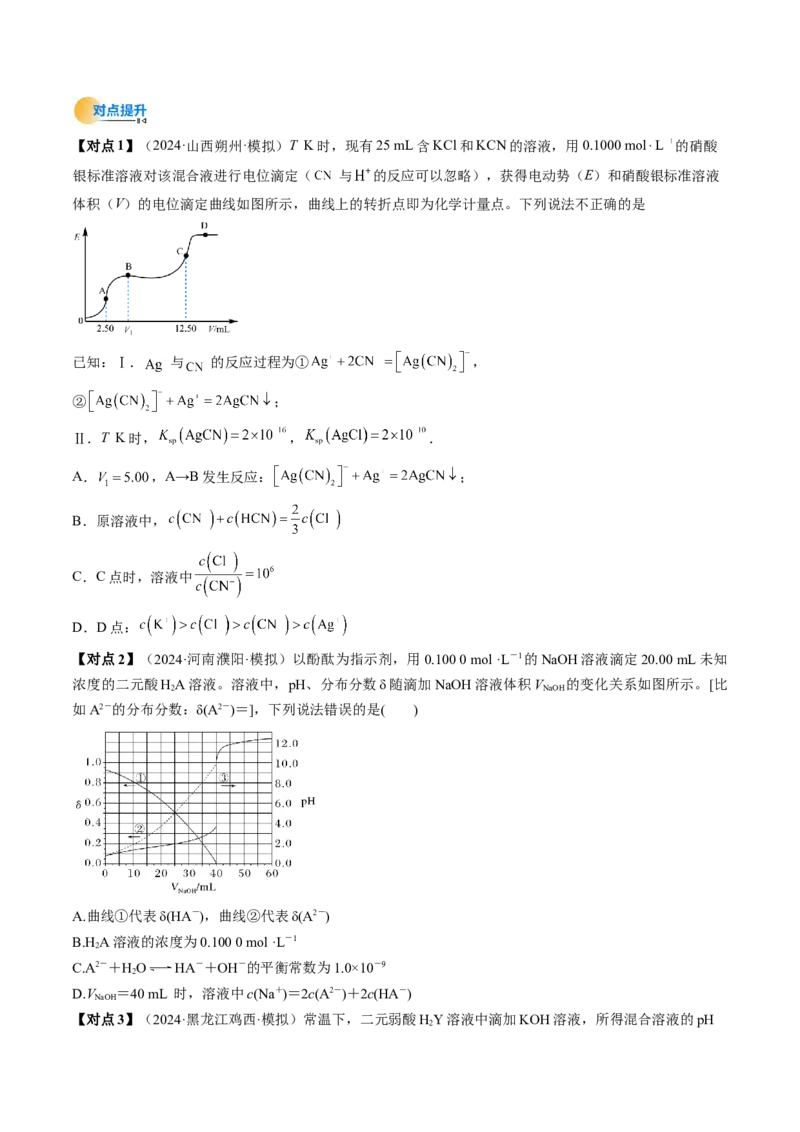
D.e点溶液中c(Na+)>c(HCN)>c(OH-)>c(H+)【对点1】(2024·山西朔州·模拟)T K时,现有25 mL含KCl和KCN的溶液,用0.1000 mol⋅L 的硝酸
银标准溶液对该混合液进行电位滴定( 与 的反应可以忽略),获得电动势(E)和硝酸银标准溶液
体积(V)的电位滴定曲线如图所示,曲线上的转折点即为化学计量点。下列说法不正确的是
已知:Ⅰ. 与 的反应过程为① ,
② ;
Ⅱ.T K时, , .
A. ,A→B发生反应: ;
B.原溶液中,
C.C点时,溶液中
D.D点:
【对点2】(2024·河南濮阳·模拟)以酚酞为指示剂,用0.100 0 mol ·L-1的NaOH溶液滴定20.00 mL未知
浓度的二元酸HA溶液。溶液中,pH、分布分数δ随滴加NaOH溶液体积V 的变化关系如图所示。[比
2 NaOH
如A2-的分布分数:δ(A2-)=],下列说法错误的是( )
A.曲线①代表δ(HA-),曲线②代表δ(A2-)
B.H A溶液的浓度为0.100 0 mol ·L-1
2
C.A2-+HO HA-+OH-的平衡常数为1.0×10-9
2
D.V =40 mL 时,溶液中c(Na+)=2c(A2-)+2c(HA-)
NaOH
【对点3】(2024·黑龙江鸡西·模拟)常温下,二元弱酸HY溶液中滴加KOH溶液,所得混合溶液的pH
2与离子浓度变化的关系如图所示,下列说法错误的是( )
A.曲线M表示pH与lg的变化关系
B.K (H Y)=10-4.3
a2 2
C.a点溶液中:c(H+)-c(OH-)=2c(Y2-)+c(HY-)-c(K+)
D.交点c的溶液中:c(H Y)=c(Y2-)>c(HY-)>c(H+)
2
考法02 沉淀溶解平衡图像
一、沉淀溶解平衡K 曲线的分析
sp
1.阳离子—阴离子单曲线
以“BaSO(s) Ba2+(aq)+SO(aq)”为例
4
图像展示
a→c 在曲线上变化,增大c(SO)
b→c 加入1×10-5 mol·L-1 Na SO 溶液(加水不可以)
2 4
点的变化
d→c 加入BaCl 固体(忽略溶液的体积变化)
2
c→a 在曲线上变化,增大c(Ba2+)
溶液蒸发时,离
原溶液不饱和时,离子浓度都增大;原溶液饱和时,离子浓度都不变
子浓度的变化
溶度积常数只是温度的函数,与溶液中溶质的离子浓度无关,在同一曲线上的点,溶度积常数相同
2.阴、阳离子浓度——温度双曲线图
以“Ba
SO ”为
4
例
曲线可
①曲线上各点的意义:每条曲线上任一点都表示饱和溶液,曲线上方的任一点均表示过饱和溶
知信息液,此时有沉淀析出,曲线下方的任一点均表示不饱和溶液
T 曲线:a、b点都表示饱和溶液,c点表示过饱和溶液
1
T 曲线:a、b、c点都表示不饱和溶液
2
②计算K :由a或b点可以计算出T 温度下的K
sp 1 sp
③比较T 和T 大小:因BaSO 沉淀溶解平衡吸热,可知:TK (CuS)
sp sp sp
3.负对数[-lg c(M+)~-lg c(R-)]曲线
图像
展示
关系 函数关系:随着CO浓度增大,Ca2+浓度减小
①横坐标数值越大,CO越小;纵坐标数值越小,c(M)越大
曲线 ②直线上各点的意义:直线上的任何一点为饱和溶液;直线上方的点为不饱和溶液;直线下方
可知 的点为过饱和溶液,有沉淀生成
信息 如:c点,相对于MgCO 来说,处于直线上方,为不饱和溶液;相对于CaCO 来说,处于直线
3 3
下方,为过饱和溶液,此时有CaCO 沉淀生成
3③计算K :由曲线上面给定数据可以计算出相应的K
sp sp
④比较K 大小:K (MgCO )>K (CaCO)>K (MnCO )
sp sp 3 sp 3 sp 3
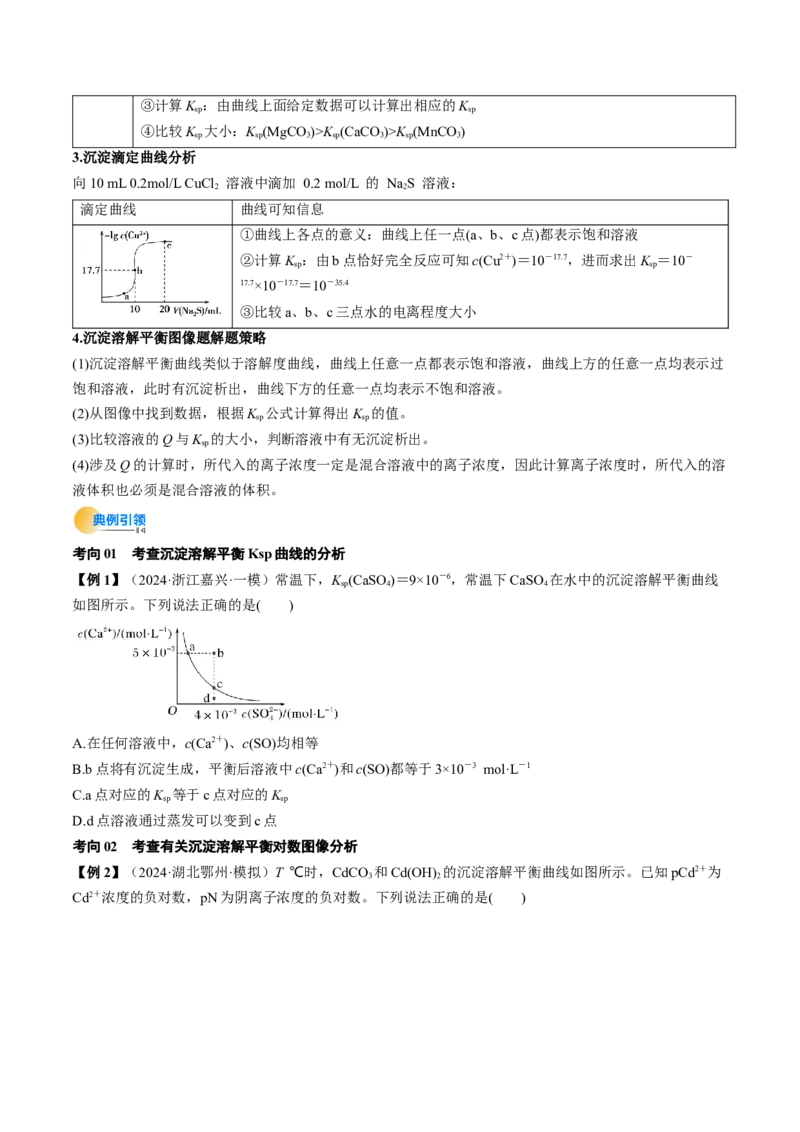
3.沉淀滴定曲线分析
向10 mL 0.2mol/L CuCl 溶液中滴加 0.2 mol/L 的 NaS 溶液:
2 2
滴定曲线 曲线可知信息
①曲线上各点的意义:曲线上任一点(a、b、c点)都表示饱和溶液
②计算K :由b点恰好完全反应可知c(Cu2+)=10-17.7,进而求出K =10-
sp sp
17.7×10-17.7=10-35.4
③比较a、b、c三点水的电离程度大小
4.沉淀溶解平衡图像题解题策略
(1)沉淀溶解平衡曲线类似于溶解度曲线,曲线上任意一点都表示饱和溶液,曲线上方的任意一点均表示过
饱和溶液,此时有沉淀析出,曲线下方的任意一点均表示不饱和溶液。
(2)从图像中找到数据,根据K 公式计算得出K 的值。
sp sp
(3)比较溶液的Q与K 的大小,判断溶液中有无沉淀析出。
sp
(4)涉及Q的计算时,所代入的离子浓度一定是混合溶液中的离子浓度,因此计算离子浓度时,所代入的溶
液体积也必须是混合溶液的体积。
考向01 考查沉淀溶解平衡Ksp曲线的分析
【例1】(2024·浙江嘉兴·一模)常温下,K (CaSO)=9×10-6,常温下CaSO 在水中的沉淀溶解平衡曲线
sp 4 4
如图所示。下列说法正确的是( )
A.在任何溶液中,c(Ca2+)、c(SO)均相等
B.b点将有沉淀生成,平衡后溶液中c(Ca2+)和c(SO)都等于3×10-3 mol·L-1
C.a点对应的K 等于c点对应的K
sp sp
D.d点溶液通过蒸发可以变到c点
考向02 考查有关沉淀溶解平衡对数图像分析
【例2】(2024·湖北鄂州·模拟)T ℃时,CdCO 和Cd(OH) 的沉淀溶解平衡曲线如图所示。已知pCd2+为
3 2
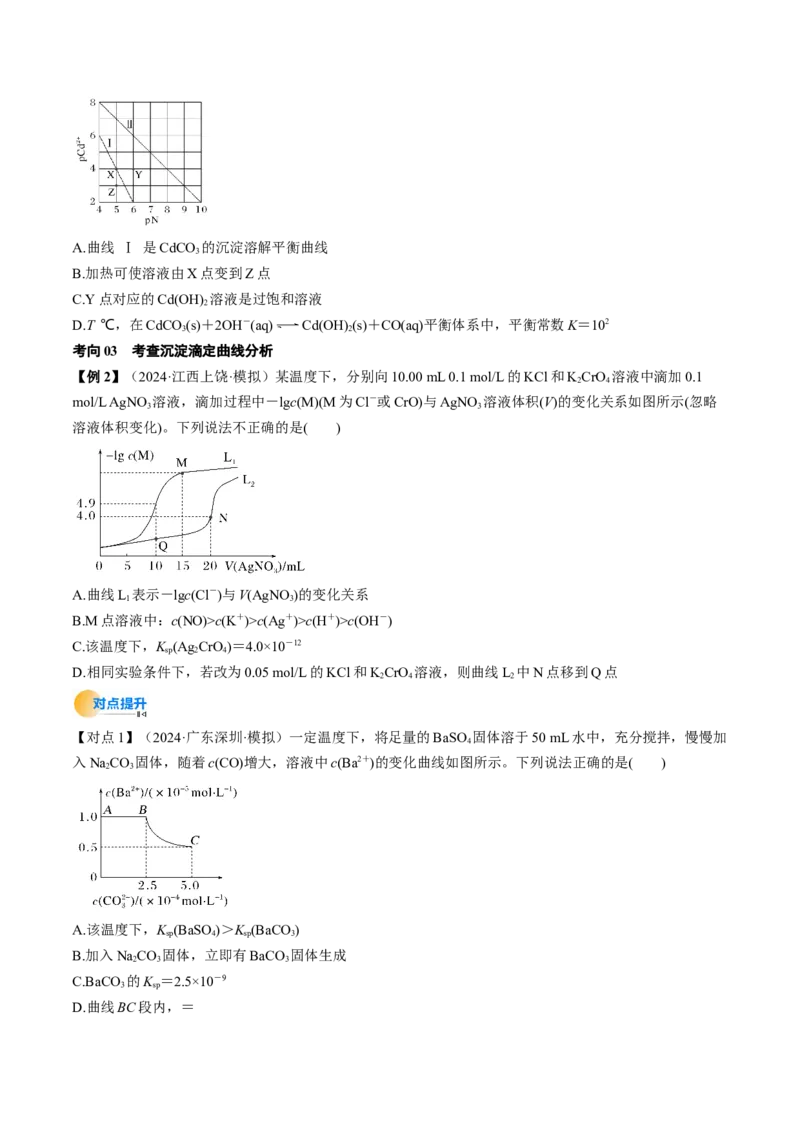
Cd2+浓度的负对数,pN为阴离子浓度的负对数。下列说法正确的是( )A.曲线 Ⅰ 是CdCO 的沉淀溶解平衡曲线
3
B.加热可使溶液由X点变到Z点
C.Y点对应的Cd(OH) 溶液是过饱和溶液
2
D.T ℃,在CdCO(s)+2OH-(aq) Cd(OH) (s)+CO(aq)平衡体系中,平衡常数K=102
3 2
考向03 考查沉淀滴定曲线分析
【例2】(2024·江西上饶·模拟)某温度下,分别向10.00 mL 0.1 mol/L的KCl和KCrO 溶液中滴加0.1
2 4
mol/L AgNO 溶液,滴加过程中-lgc(M)(M为Cl-或CrO)与AgNO 溶液体积(V)的变化关系如图所示(忽略
3 3
溶液体积变化)。下列说法不正确的是( )
A.曲线L 表示-lgc(Cl-)与V(AgNO)的变化关系
1 3
B.M点溶液中:c(NO)>c(K+)>c(Ag+)>c(H+)>c(OH-)
C.该温度下,K (Ag CrO)=4.0×10-12
sp 2 4
D.相同实验条件下,若改为0.05 mol/L的KCl和KCrO 溶液,则曲线L 中N点移到Q点
2 4 2
【对点1】(2024·广东深圳·模拟)一定温度下,将足量的BaSO 固体溶于50 mL水中,充分搅拌,慢慢加
4
入NaCO 固体,随着c(CO)增大,溶液中c(Ba2+)的变化曲线如图所示。下列说法正确的是( )
2 3
A.该温度下,K (BaSO)>K (BaCO)
sp 4 sp 3
B.加入NaCO 固体,立即有BaCO 固体生成
2 3 3
C.BaCO 的K =2.5×10-9
3 sp
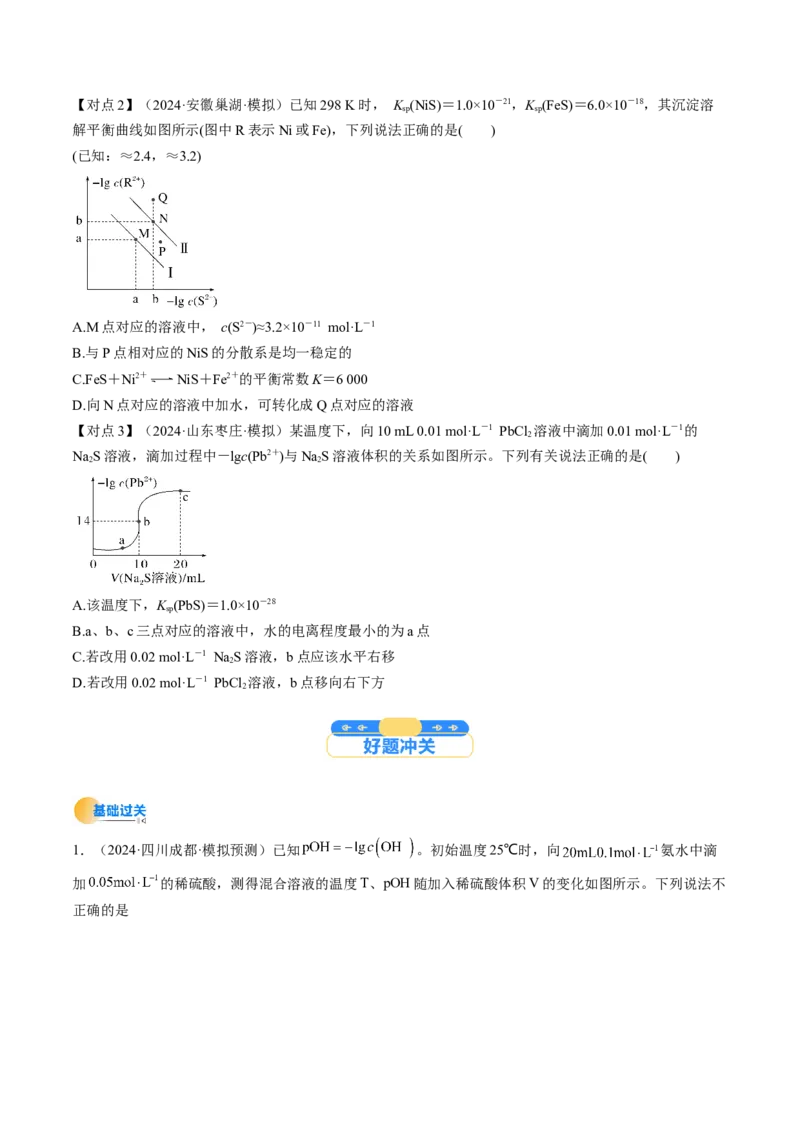
D.曲线BC段内,=【对点2】(2024·安徽巢湖·模拟)已知298 K时, K (NiS)=1.0×10-21,K (FeS)=6.0×10-18,其沉淀溶
sp sp
解平衡曲线如图所示(图中R表示Ni或Fe),下列说法正确的是( )
(已知:≈2.4,≈3.2)
A.M点对应的溶液中, c(S2-)≈3.2×10-11 mol·L-1
B.与P点相对应的NiS的分散系是均一稳定的
C.FeS+Ni2+ NiS+Fe2+的平衡常数K=6 000
D.向N点对应的溶液中加水,可转化成Q点对应的溶液
【对点3】(2024·山东枣庄·模拟)某温度下,向10 mL 0.01 mol·L-1 PbCl 溶液中滴加0.01 mol·L-1的
2
NaS溶液,滴加过程中-lgc(Pb2+)与NaS溶液体积的关系如图所示。下列有关说法正确的是( )
2 2
A.该温度下,K (PbS)=1.0×10-28
sp
B.a、b、c三点对应的溶液中,水的电离程度最小的为a点
C.若改用0.02 mol·L-1 Na S溶液,b点应该水平右移
2
D.若改用0.02 mol·L-1 PbCl 溶液,b点移向右下方
2
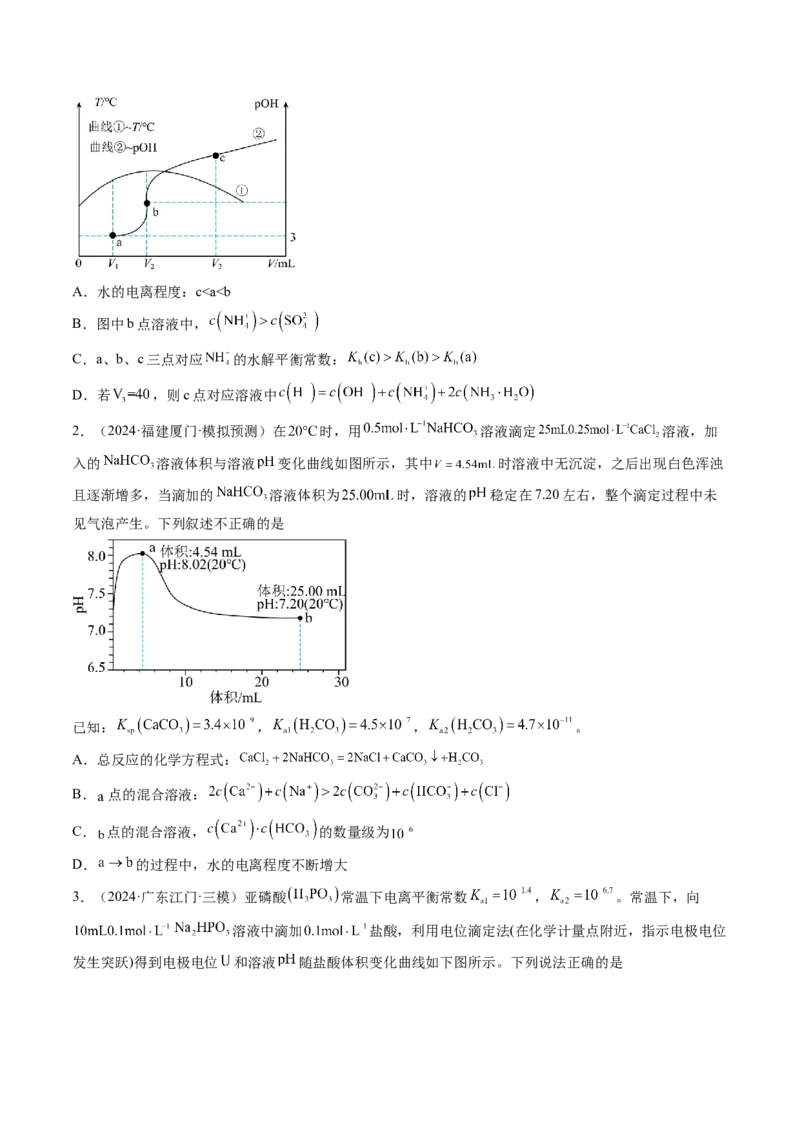
1.(2024·四川成都·模拟预测)已知 。初始温度25℃时,向 氨水中滴
加 的稀硫酸,测得混合溶液的温度T、pOH随加入稀硫酸体积V的变化如图所示。下列说法不
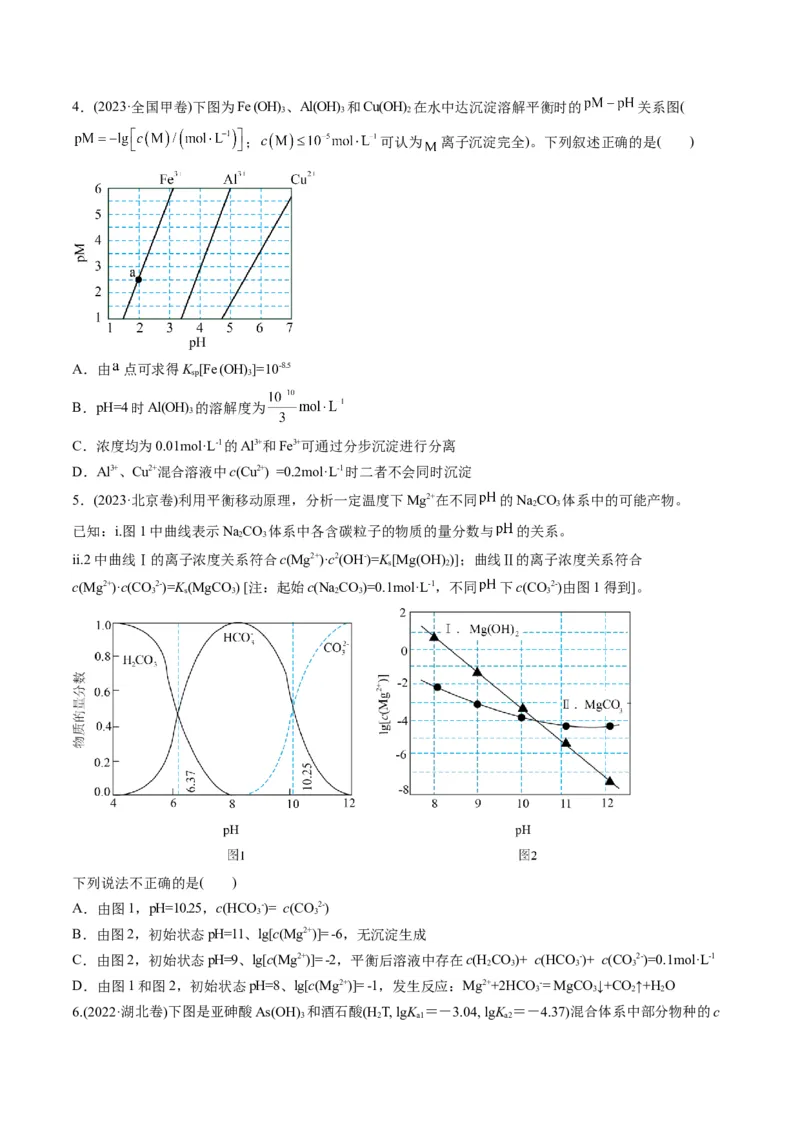
正确的是A.水的电离程度:c 。下列叙述正确的是
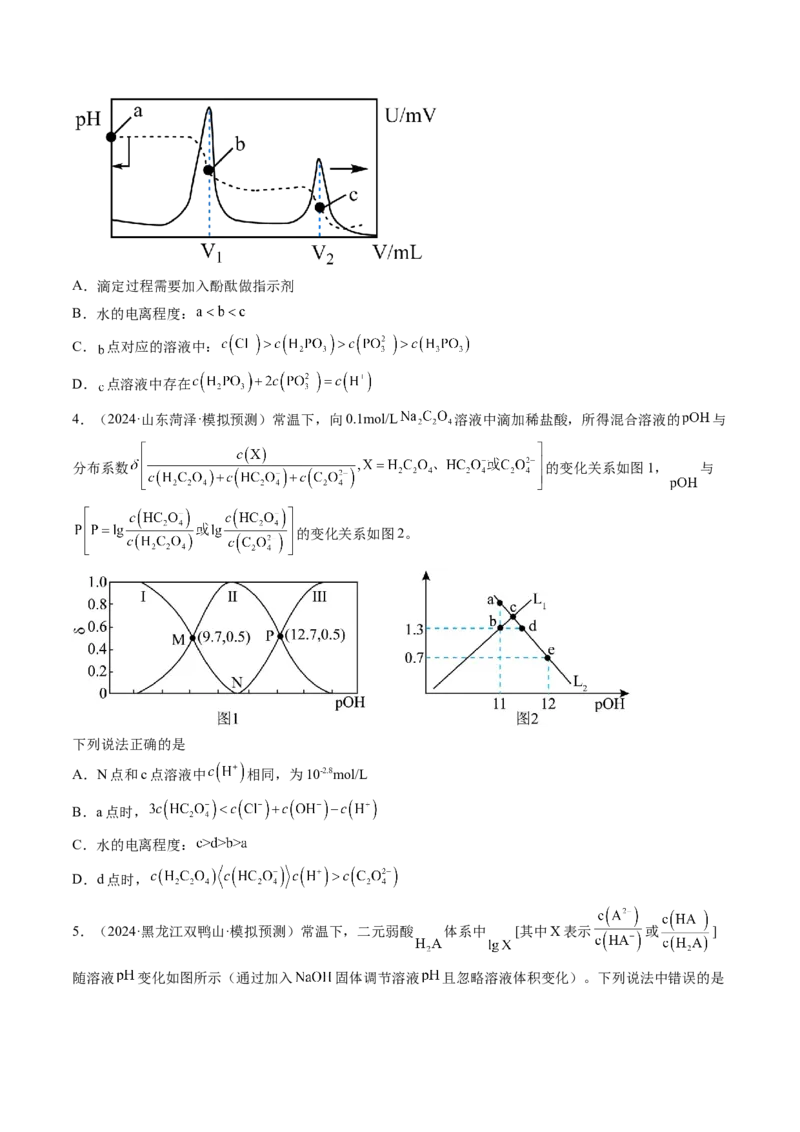
A.图中 代表: 与pH的关系, 代表 与pH的关系
B.同时产生两种沉淀时,
C.再向体系中加入硫化钠溶液, 减少, 将变小
D. 的平衡常数
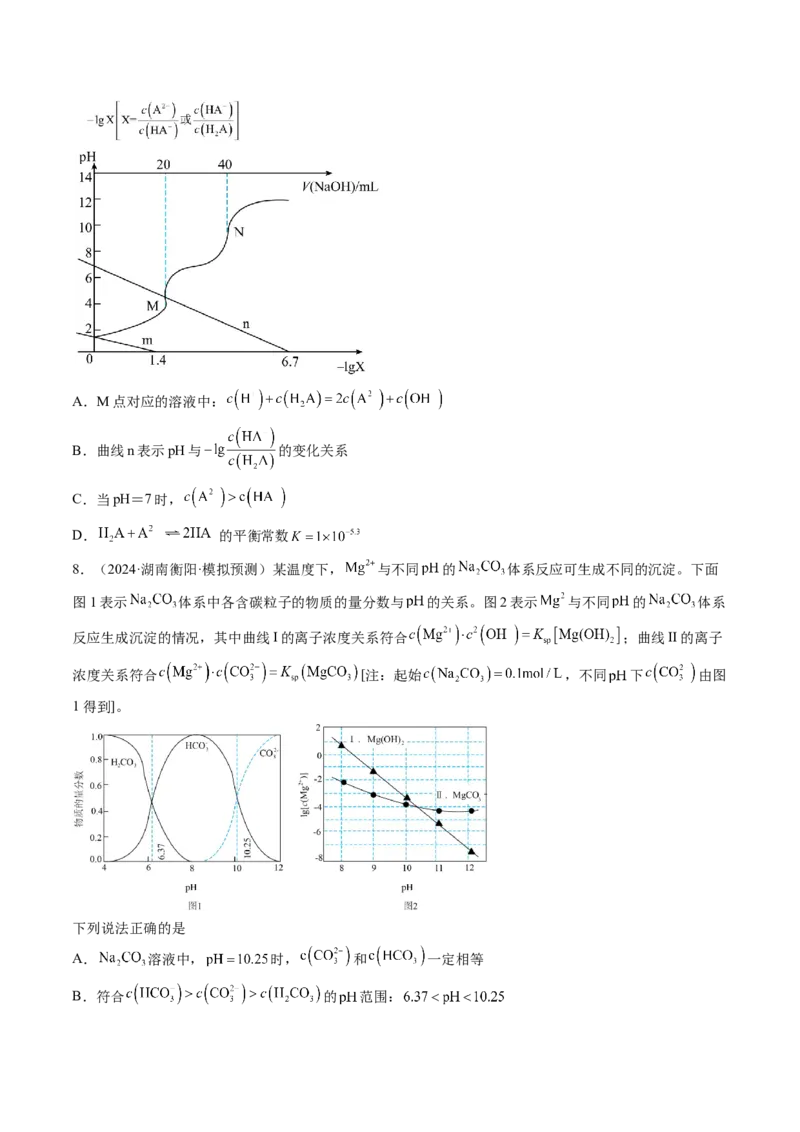
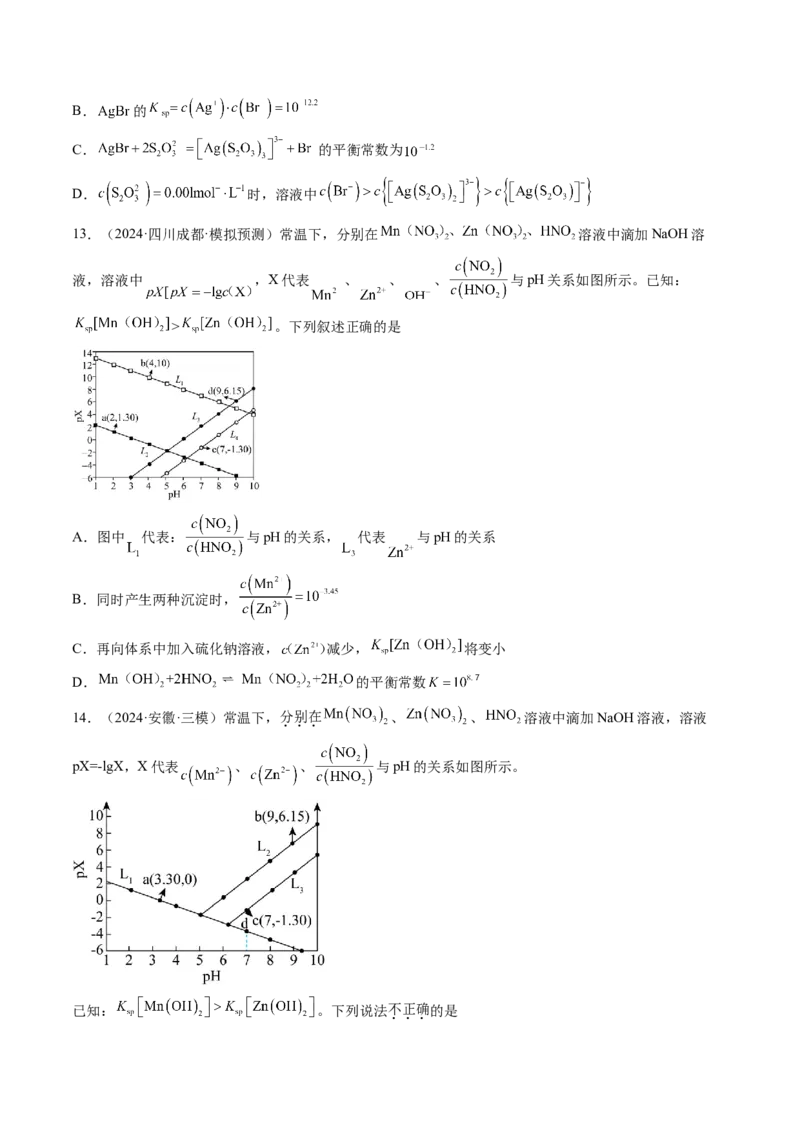
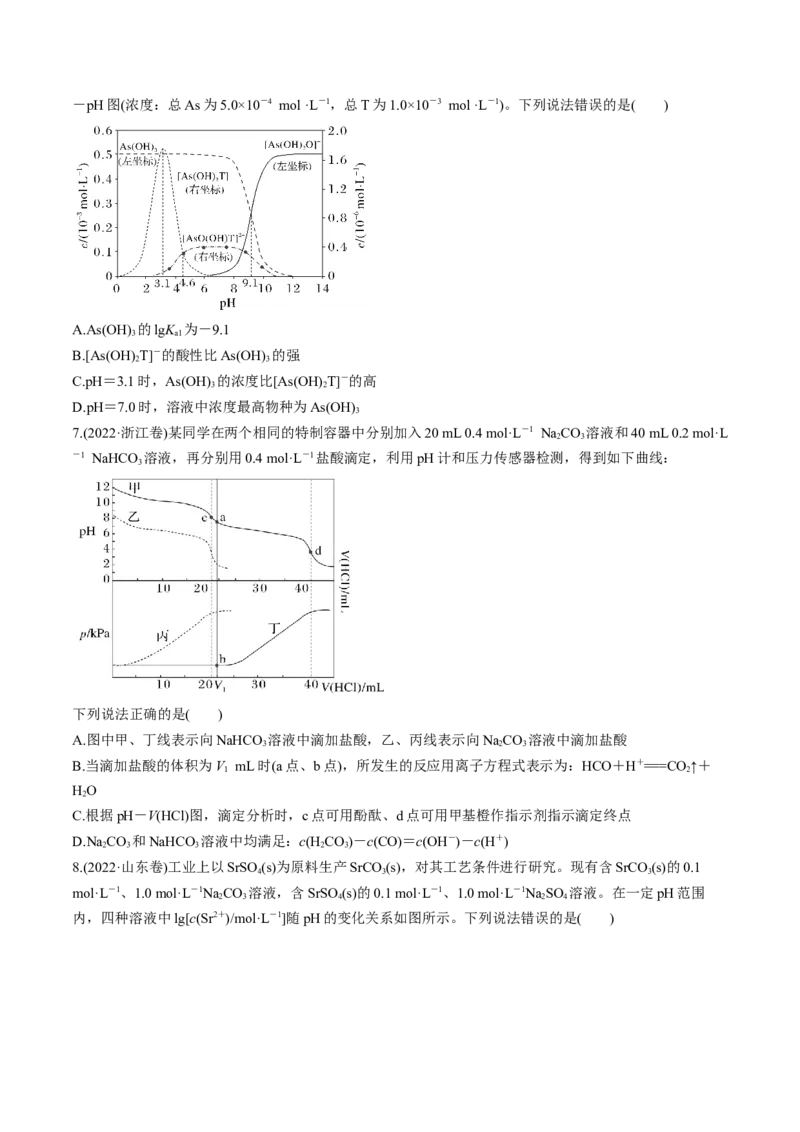
14.(2024·安徽·三模)常温下,分别在 、 、 溶液中滴加NaOH溶液,溶液
pX=-lgX,X代表 、 、 与pH的关系如图所示。
已知: 。下列说法不正确的是A.
B. 的数量级为
C.
D.d点存在
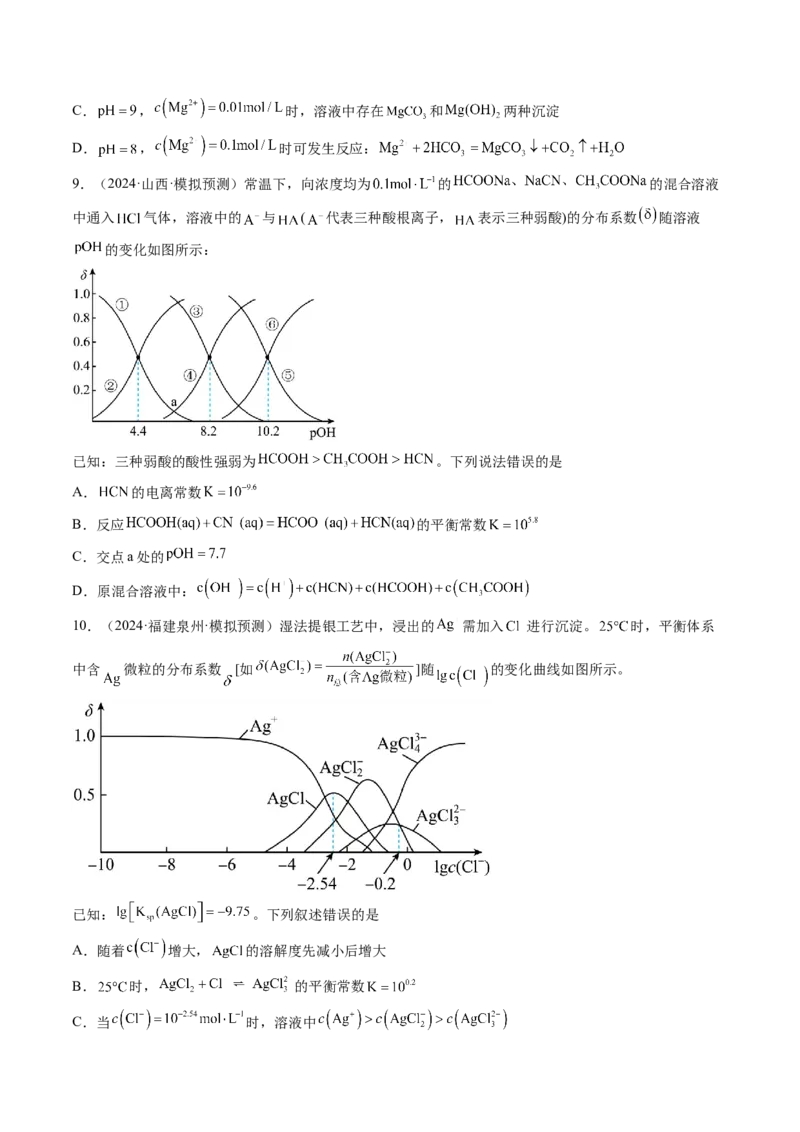
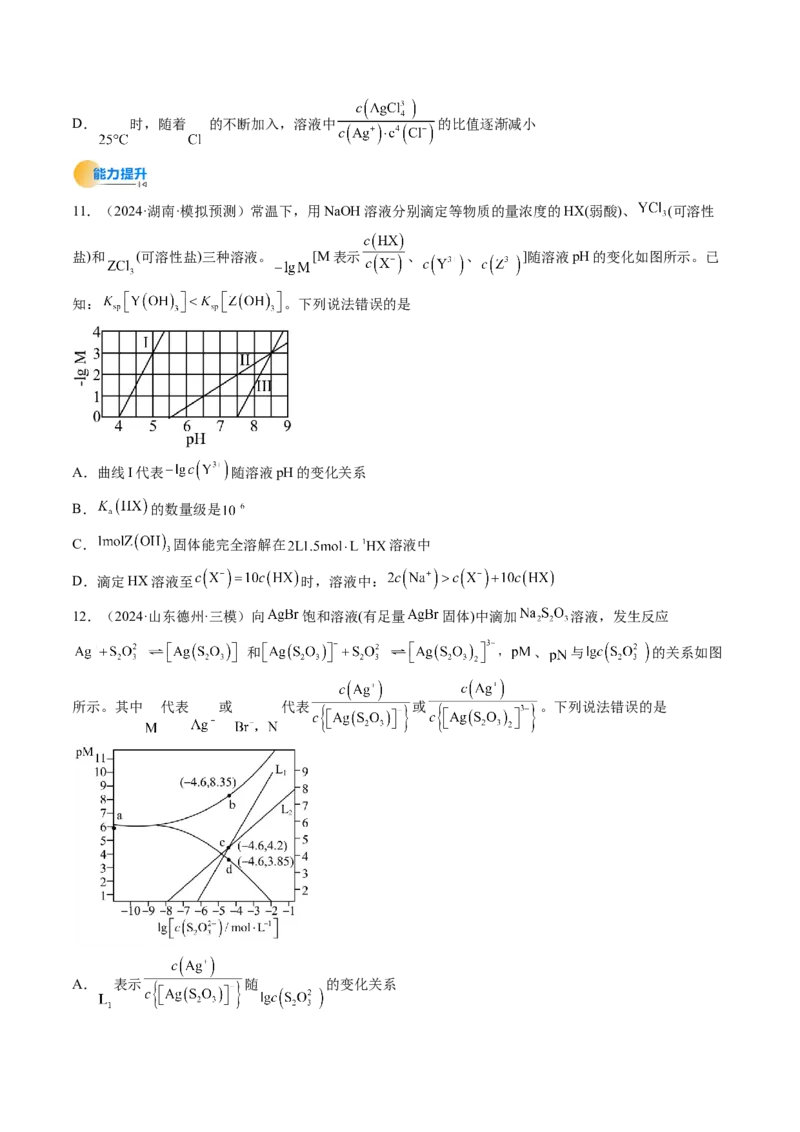
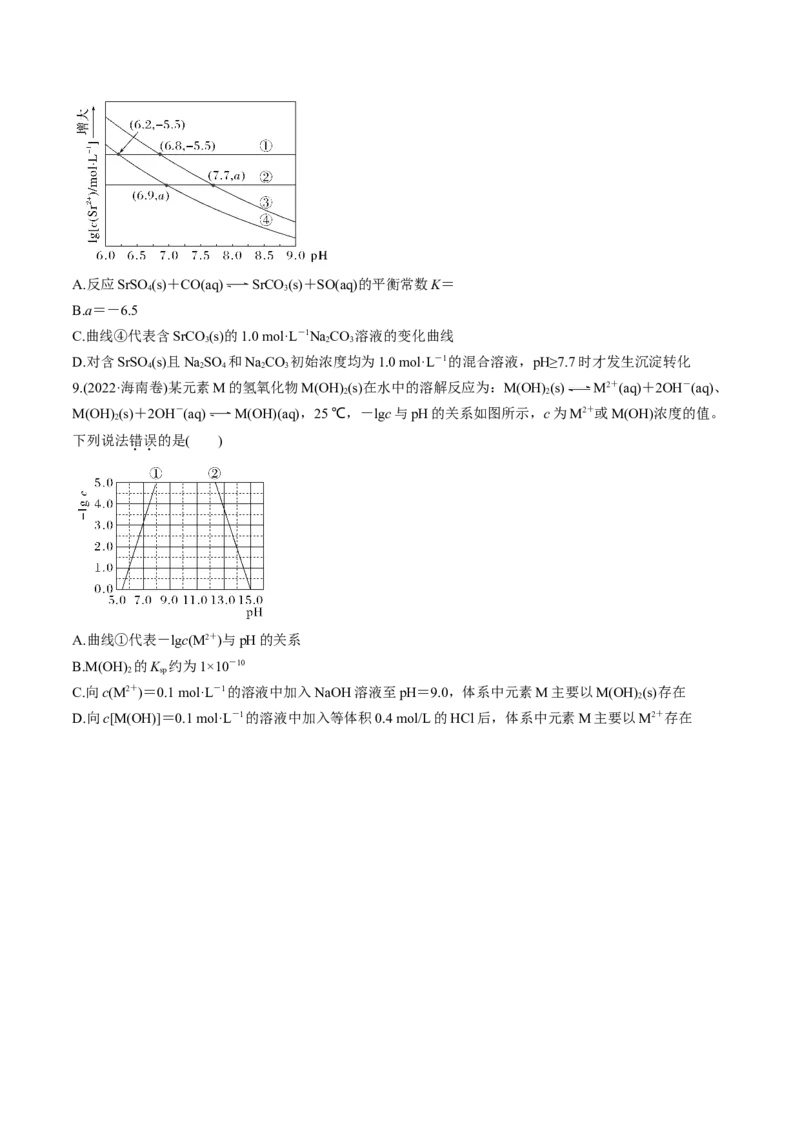
15.(2024·山西大同·模拟预测)某温度时,卤化银(AgX,X=Cl、Br、I)的3条溶解平衡曲线如图所
示,AgCl、AgBr、AgI的 依次减小。已知 , ,利用pX、pAg的坐标
系可表示出AgX的溶度积与溶液中 和 的相互关系。下列说法错误的是
A.坐标点p形成的溶液是AgCl的不饱和溶液
B.向含有 、 和 的溶液中逐滴加入 溶液, 首先沉淀
C.该温度时, 的平衡常数
D.m、n、p三点的 相同
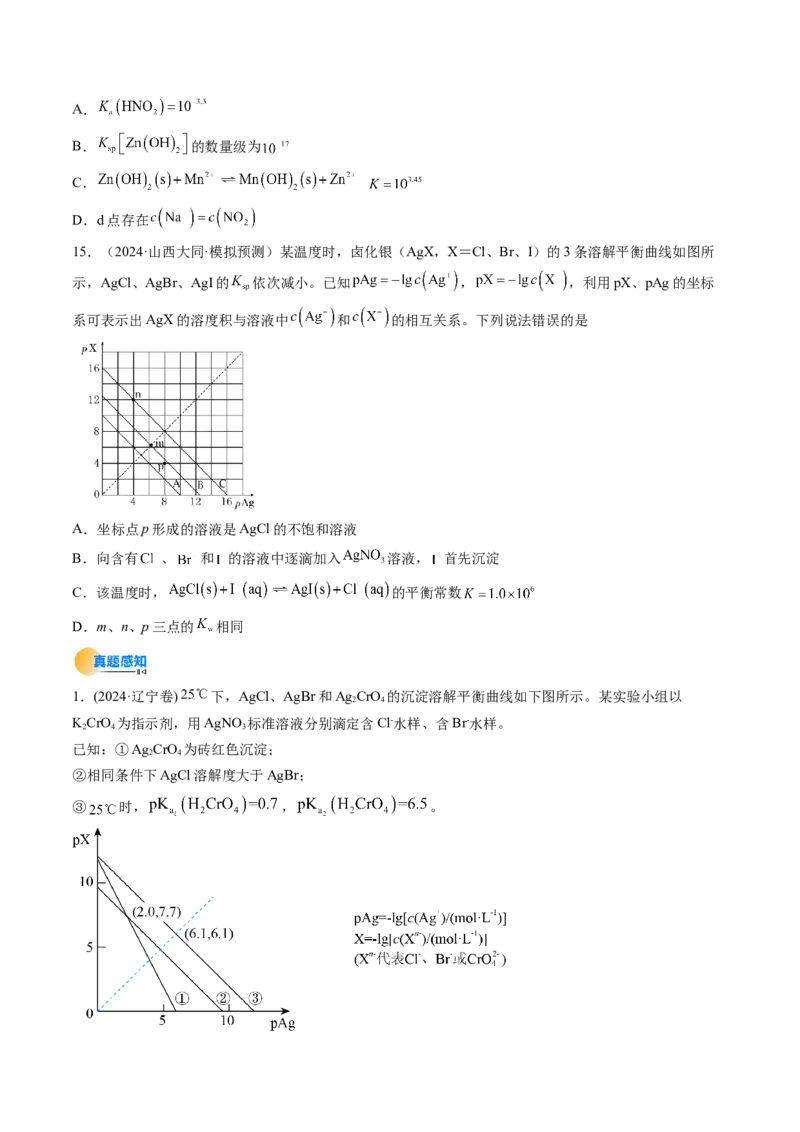
1.(2024·辽宁卷) 下,AgCl、AgBr和Ag CrO 的沉淀溶解平衡曲线如下图所示。某实验小组以
2 4
KCrO 为指示剂,用AgNO 标准溶液分别滴定含Cl-水样、含Br-水样。
2 4 3
已知:①Ag CrO 为砖红色沉淀;
2 4
②相同条件下AgCl溶解度大于AgBr;
③ 时, , 。下列说法错误的是( )
A.曲线②为AgCl沉淀溶解平衡曲线
B.反应Ag CrO+2H+ 2Ag++HCrO-的平衡常数K=10-5.2
2 4 4
C.滴定Cl-时,理论上混合液中指示剂浓度不宜超过10-2.0 mol·L-1
D.滴定Br-达终点时,溶液中
2.(2024·浙江卷)室温下,HS水溶液中各含硫微粒物质的量分数 随 变化关系如下图[例如
2
]。已知: 。
下列说法正确的是( )
A.溶解度:FeS大于Fe(OH)
2
B.以酚酞为指示剂(变色的 范围8.2~10.0),用 标准溶液可滴定HS水溶液的浓度
2
C.忽略S2-的第二步水解,0.1mol/L的NaS溶液中S2-水解率约为
2
D. 0.010mol/L的FeCl 溶液中加入等体积 的NaS溶液,反应初始生成的沉淀是FeS
2 2
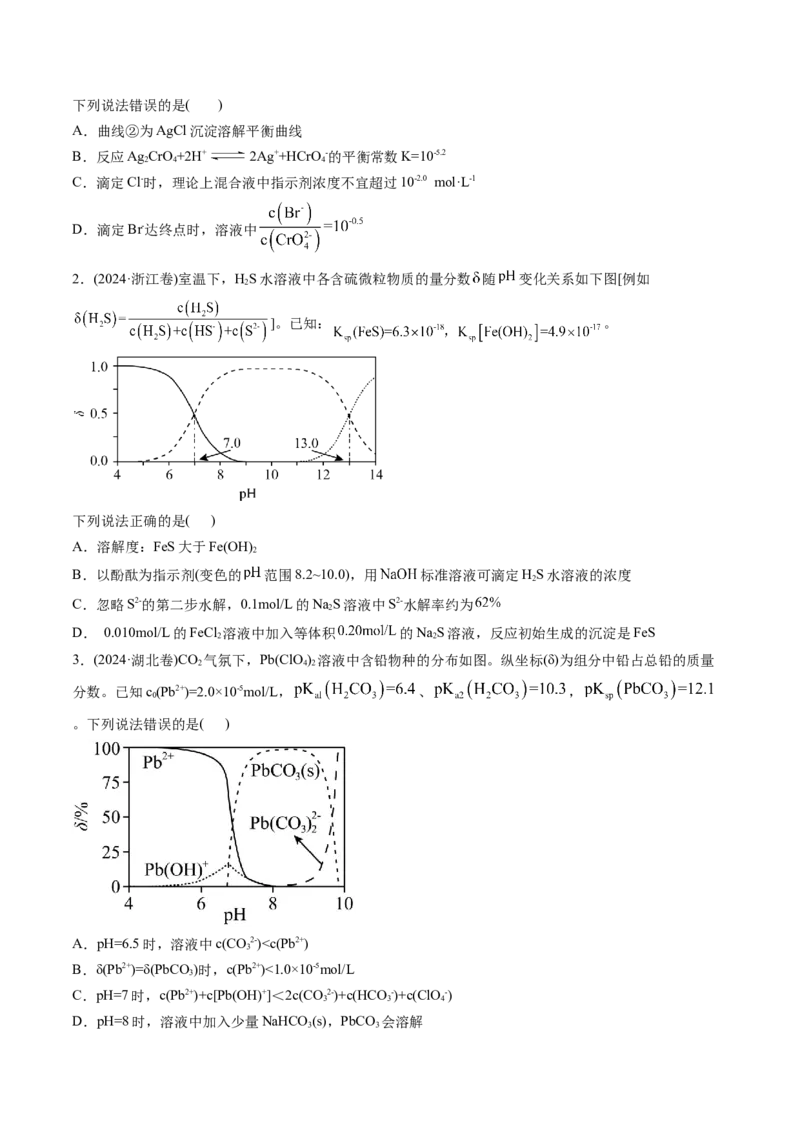
3.(2024·湖北卷)CO 气氛下,Pb(ClO) 溶液中含铅物种的分布如图。纵坐标(δ)为组分中铅占总铅的质量
2 4 2
分数。已知c(Pb2+)=2.0×10-5mol/L, 、 ,
0
。下列说法错误的是( )
A.pH=6.5时,溶液中c(CO2-)