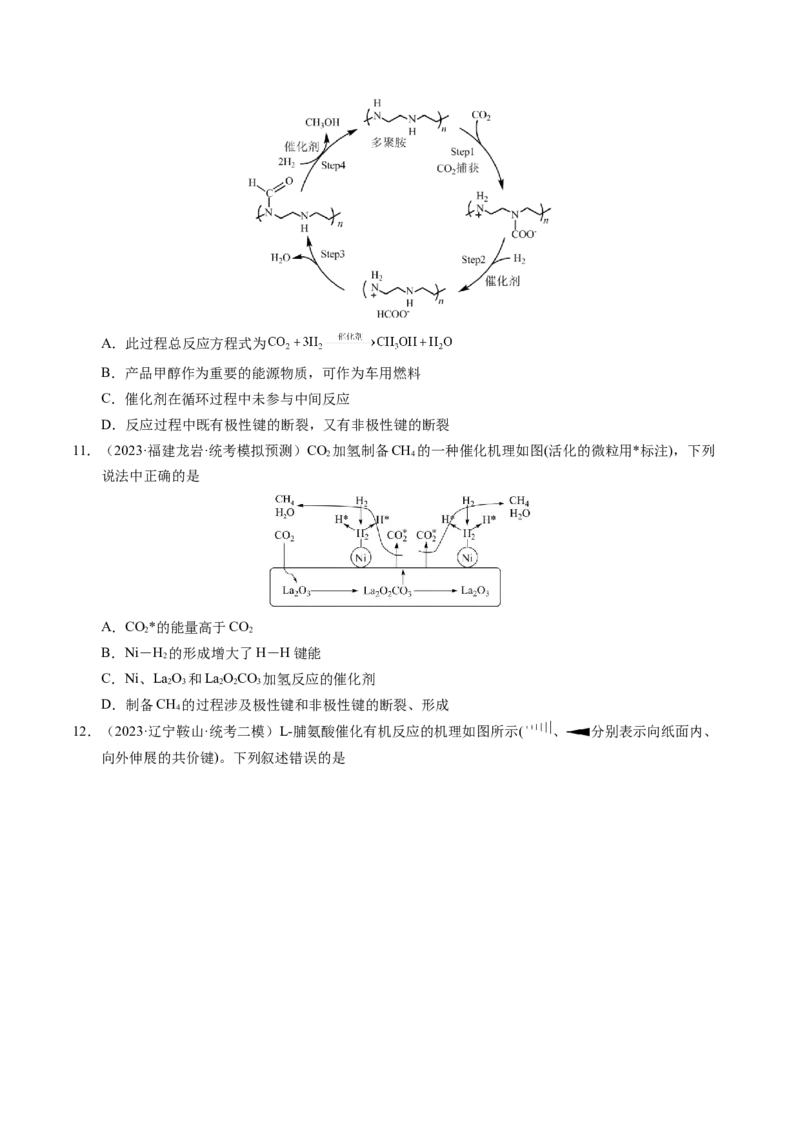
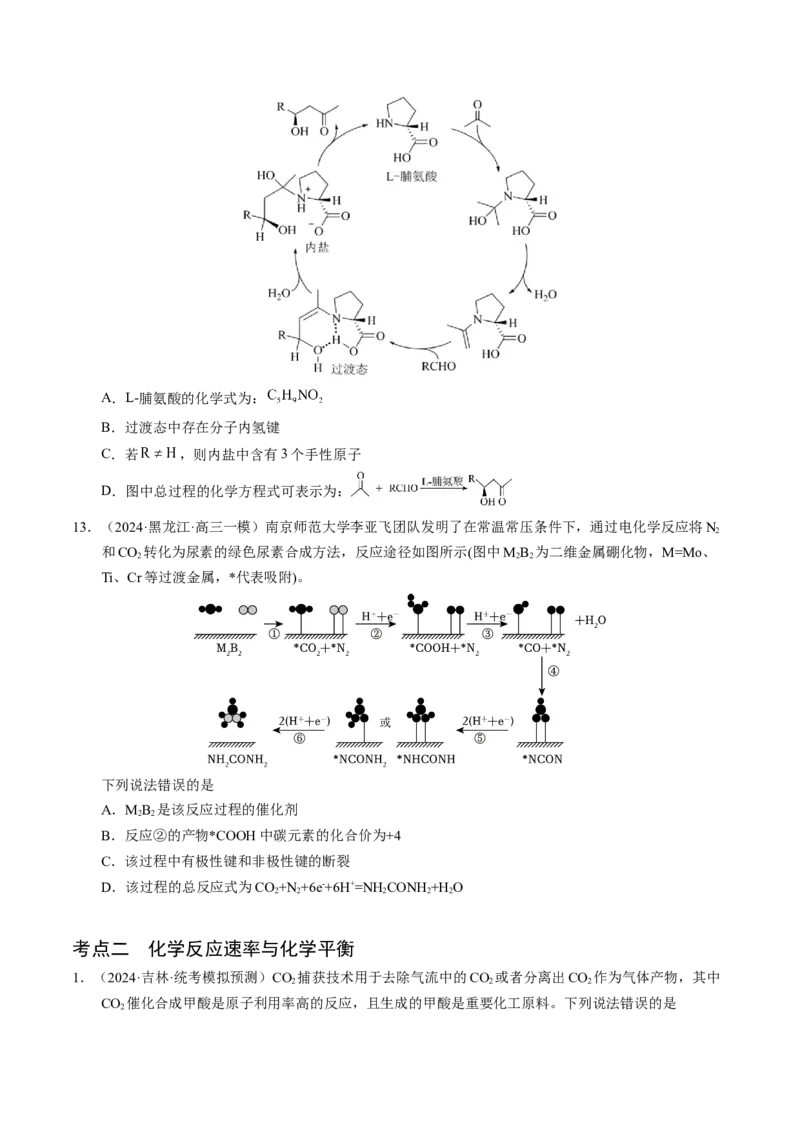
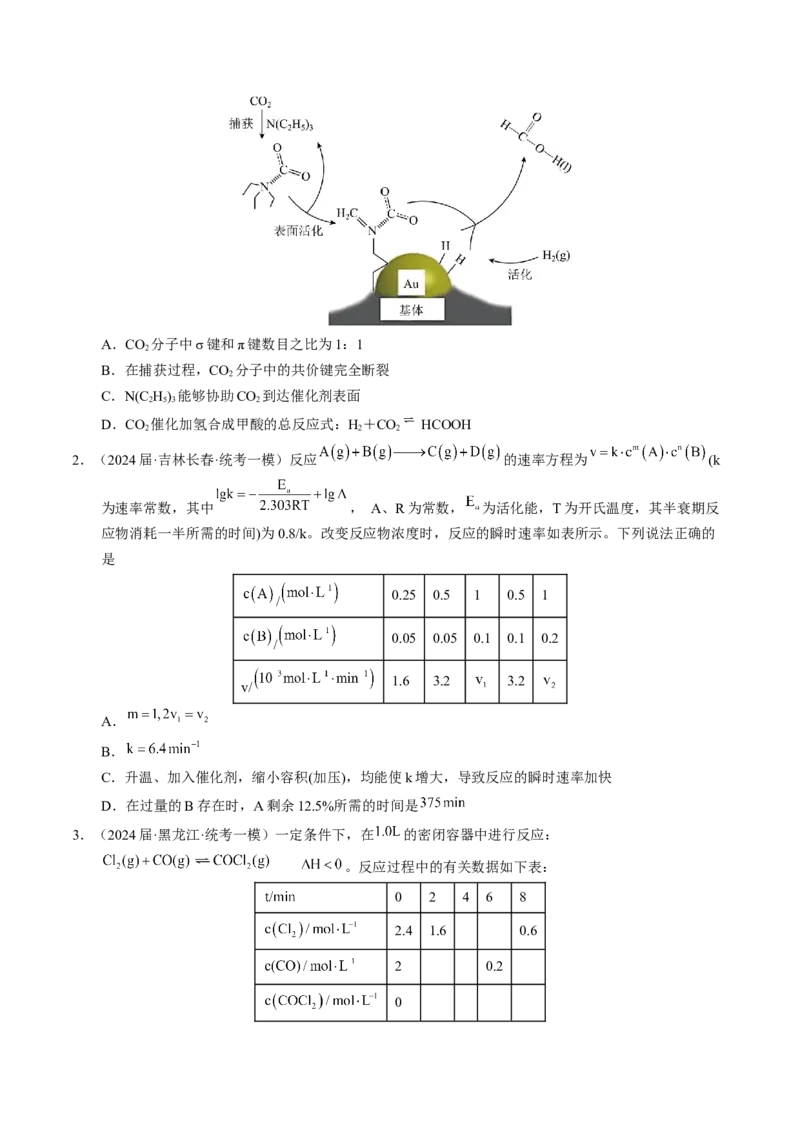
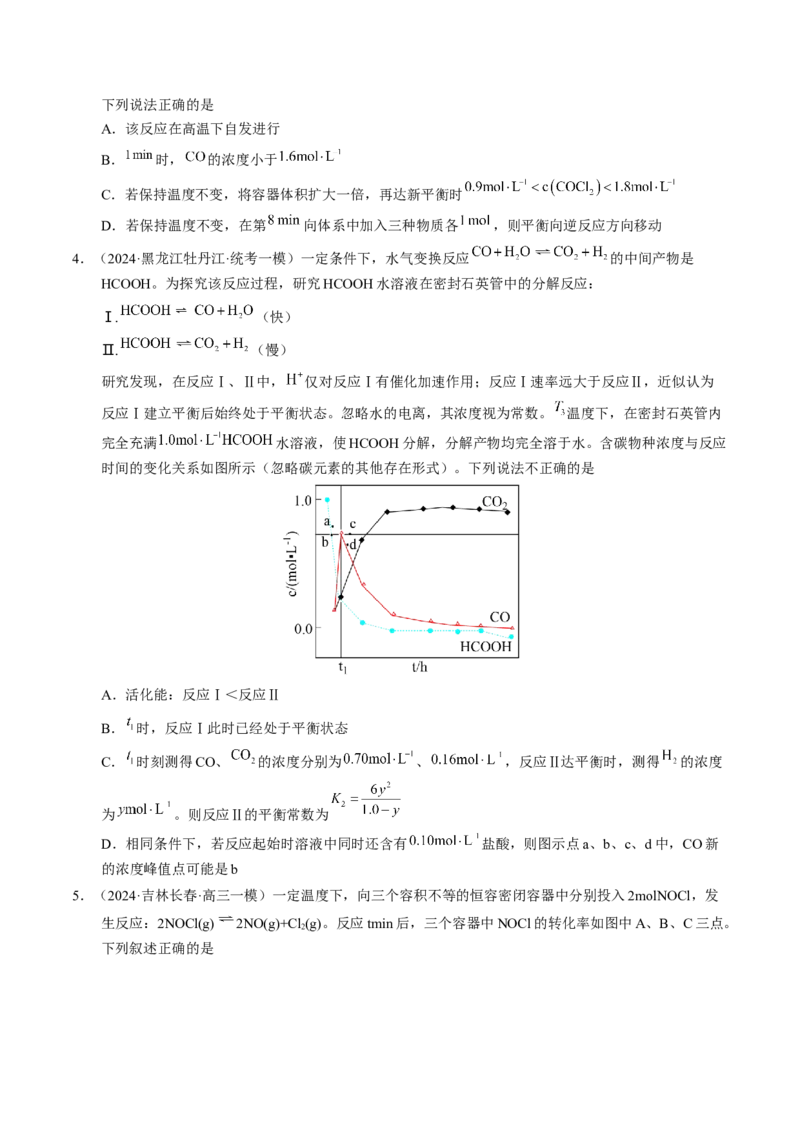
文档内容
押选择题
化学反应与能量、化学反应速率与化学平衡
核心考点 考情统计 考向预测 备考策略
化学反应与 2023·辽宁卷,12 考查热化学方程式反应热 要求考生理解盖斯定律,并能
能量 2022·辽宁卷,10、 的计算、能量变化与 运用盖斯定律进行有关反应焓
12 ΔH、活化能的图像问 变的计算。关注能源问题、科
2021·辽宁卷,11 题。 技成果,运用化学基本理论或
有机物的知识解决实际问题。
化学反应速 2022·辽宁卷,12 化学反应速率的计算和外 围绕勒夏特列原理的理解,通
率与化学平 2021·辽宁卷,12 界条件对化学反应速率的 过实验、判断、图像、计算等
衡 影响;化学平衡的特征及 形成对化学平衡移动进行综合
化学平衡常数的计算和理 考查,是化学反应速率和化学
解。 (平衡)状态的综合应用体现,
平时加强针对性强化训练,注
重规律和方法技能的总结,提
高解题能力。
1. (2023·辽宁卷)一定条件下,酸性 溶液与 发生反应, (Ⅱ)起催化作用,过程中不
同价态含 粒子的浓度随时间变化如下图所示。下列说法正确的是
A. (Ⅲ)不能氧化
B. 随着反应物浓度的减小,反应速率逐渐减小
C. 该条件下, (Ⅱ)和 (Ⅶ)不能大量共存D. 总反应为:
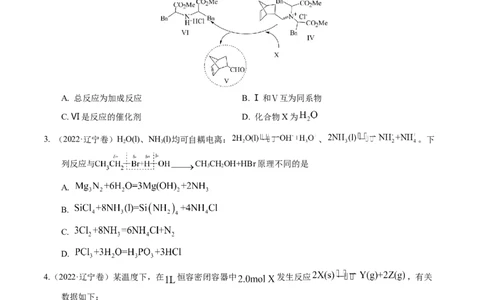
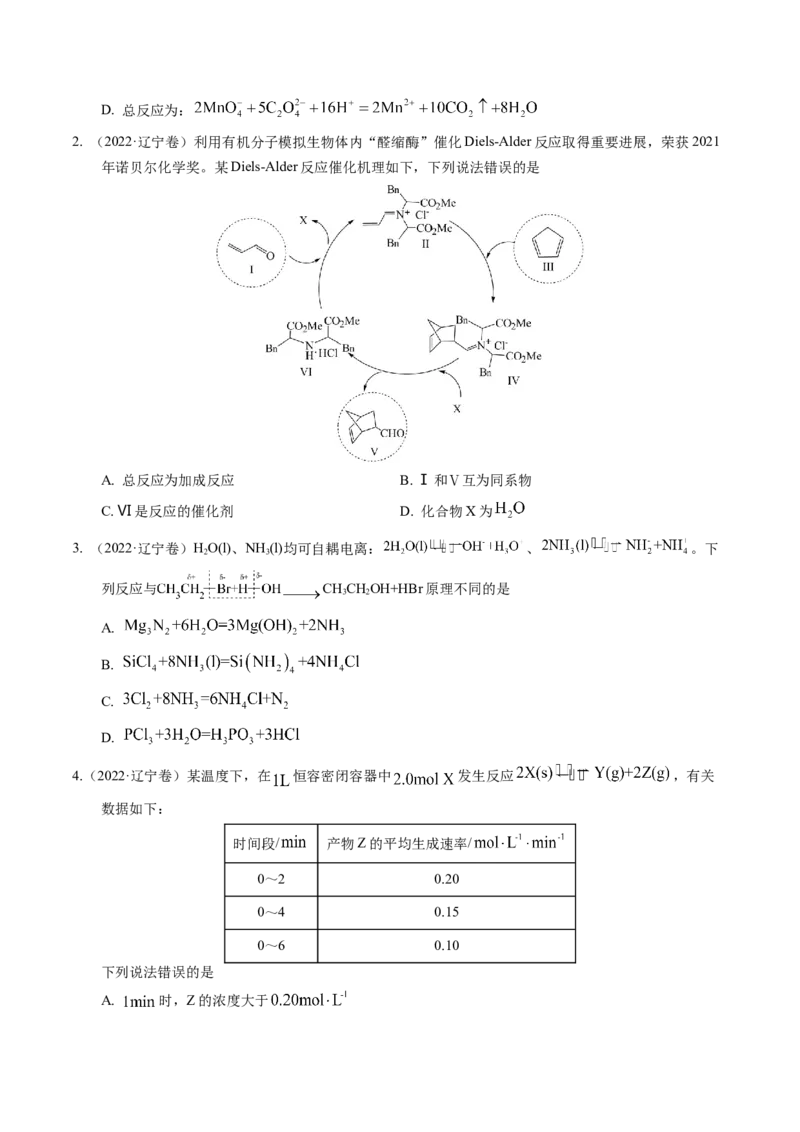
2. (2022·辽宁卷)利用有机分子模拟生物体内“醛缩酶”催化Diels-Alder反应取得重要进展,荣获2021
年诺贝尔化学奖。某Diels-Alder反应催化机理如下,下列说法错误的是
A. 总反应为加成反应 B. Ⅰ和Ⅴ互为同系物
C. Ⅵ是反应的催化剂 D. 化合物X为
3. (2022·辽宁卷)HO(l)、NH (l)均可自耦电离: 、 。下
2 3
列反应与 CHCHOH+HBr原理不同的是
3 2
A.
B.
C.
D.
4.(2022·辽宁卷)某温度下,在 恒容密闭容器中 发生反应 ,有关
数据如下:
时间段/ 产物Z的平均生成速率/
0~2 0.20
0~4 0.15
0~6 0.10
下列说法错误的是
A. 时,Z的浓度大于B. 时,加入 ,此时
C. 时,Y的体积分数约为33.3%
D. 时,X的物质的量为
5.(2021·辽宁卷)某温度下,在恒容密闭容器中加入一定量X,发生反应 ,一段时
间后达到平衡。下列说法错误的是
A. 升高温度,若 增大,则
B. 加入一定量Z,达新平衡后 减小
C. 加入等物质的量的Y和Z,达新平衡后 增大
D. 加入一定量氩气,平衡不移动
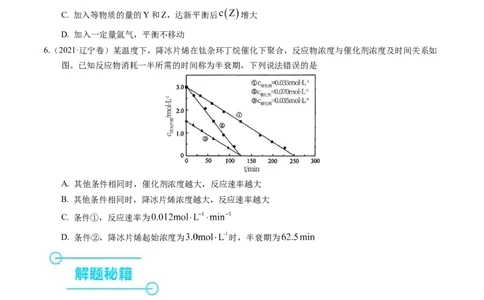
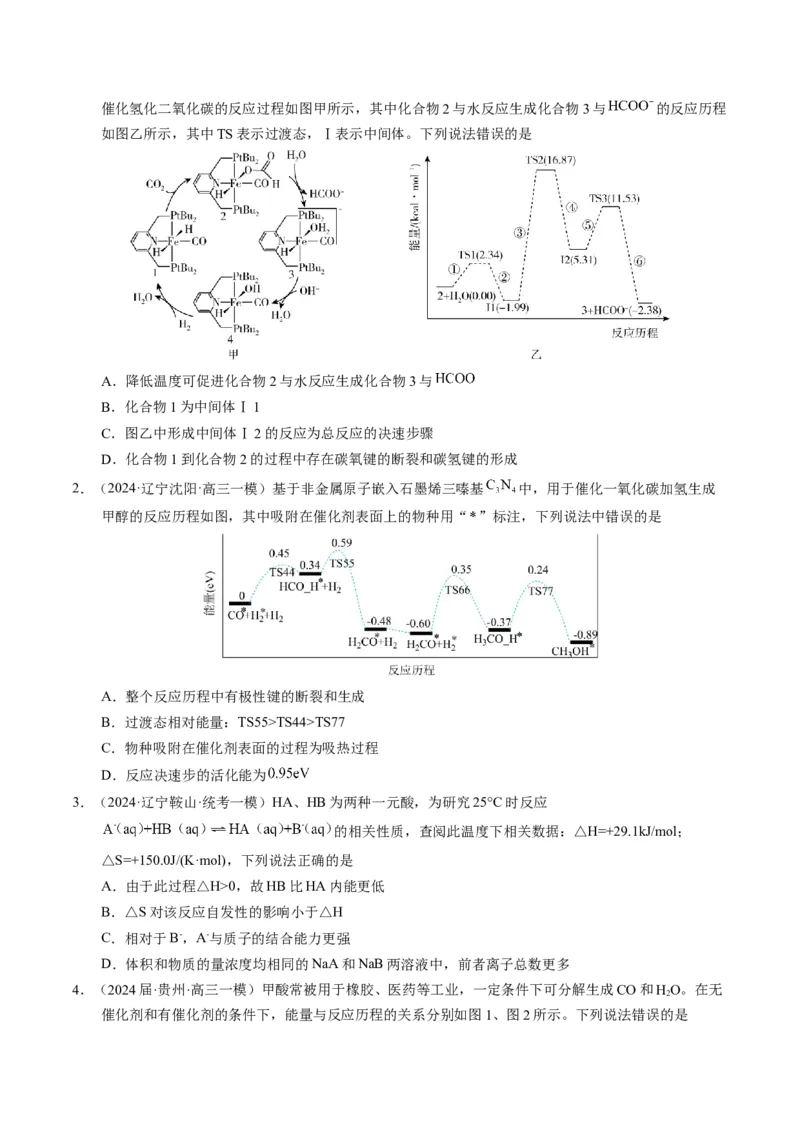
6.(2021·辽宁卷)某温度下,降冰片烯在钛杂环丁烷催化下聚合,反应物浓度与催化剂浓度及时间关系如
图。已知反应物消耗一半所需的时间称为半衰期,下列说法错误的是
A. 其他条件相同时,催化剂浓度越大,反应速率越大
B. 其他条件相同时,降冰片烯浓度越大,反应速率越大
C. 条件①,反应速率为
D. 条件②,降冰片烯起始浓度为 时,半衰期为
一、化学反应与能量
1.化学反应的能量变化——能垒图
在化学反应过程中,反应前后能量会发生变化。能垒指的是由于化学反应的成功发生对于反应物到达
能量高的过渡态的过程的依赖性而产生的一个“阻碍”,只有一部分有足够能量的分子才能跨越能垒进行
反应,每一个小的分步反应的从较低能量到过渡态所吸收的能量,可以理解成ΔH-t图中“爬坡”的阶段,
这些阶段的吸收的能量都是能垒。
活化能是对能垒的一种量化描述,它代表着反应物到过渡态的具体能量差值,在这个ΔH-t图中,最高
点(也就是能量最大的过渡态)到起始点(反应物)所吸收的能量。也就是,活化能越高,能垒越高,反应速率越慢,反之亦然。教材中的能量变化图示如下:
反应历程与活化能 催化剂对反应历程与活化能影响
人教版新教材
鲁科版新教材
苏教版
(1)反应历程中的最大能垒是指正反应过程中最大相对能量的差值,可以用估算法的方法进行确定;
(2)能垒越大,反应速率越小,即多步反应中能垒最大的反应为决速反应;
(3)相同反应物同时发生多个竞争反应,其中能垒越小的反应,反应速率越大,产物占比越高。
2.催化剂与活化能
(1)催化剂的催化机理:催化剂参与化学反应,生成能量更低的中间产物,降低了达到过渡态所需要
的活化能,使反应易于发生,速率加快。这就是我们经常说的催化剂改变反应途径,降低反应的活化能。
(2)催化剂能降低反应所需活化能,化学反应速率加快,但不影响焓变∆H的大小,不影响平衡。
(3)催化反应一般过程(简化的过程):
①反应物扩散到催化剂表面;
②反应物被吸附在催化剂表面;
③被吸附的反应物发生化学反应生成产物;
④产物的解吸。
3.常见催化剂性质及应用
(1)催化剂的特性:选择性(是指给定条件下反应物之间能够同时发生多个反应情况下,催化剂可以大幅度提高目标产物在最终产物中的比率,酶的选择性极高)。
(2)选择反应温度依据之一:在选择某反应的温度时,首先应考虑催化剂的活性温度,以便最大限
度地发挥催化剂的作用。
(3)催化剂中毒:由于某些物质(反应原料中带入的杂质、催化剂自身的某些杂质、反应产物或副
产物)的作用而使催化活性衰退或丧失的现象。
(4)催化剂影响速率不影响化学平衡:对于可逆反应,催化剂同等程度地改变正逆反应速率,因而
不能改变反应物的转化率,但可缩短反应达到化学平衡的时间。
(5)周期表中催化剂寻找区域:过渡元素区。
中学中常用的催化剂:酶是蛋白质,也是催化剂。二氧化锰、五氧化二钒、铁触媒、铂铑催化剂、
Ni、Cu、Ag,浓硫酸、稀硫酸。
(6)教材研究催化剂的三个实验:①一个反应的催化剂可能有多种。如过氧化氢溶液分解的催化剂,
除了二氧化锰之外,还可以用FeCl3、CuSO4溶液。②高锰酸钾与草酸反应,生成的Mn2+是访反应的催化
剂,褪色速率会突然加快,是易被忽视的自催化反应。③淀粉水解实验,酶的催化条件温和而高效。
4.“环式”反应历程与机理
“环式”反应过程图如下:
“入环”的物质为反应物,如图中的①④;位于“环上”的物质为催化剂或中间体,如图中的⑤⑥⑦
⑧;“出环”的物质为生成物,如图中的②③;由反应物和生成物可快速得出总反应方程式。
明确反应物:最重要的要看清图示中的箭头,明确哪些物质进行循环体系,哪些物质离子循环体系,
进行循环体系的物质为总反应的反应物,离子循环体系的物质为总反应的生成物。
明确催化剂和中间产物:从循环图示中找出分解的若干反应,通过分步反应区分哪些是催化剂,哪些
是中间产物。
写出总反应:依据质量守恒定律,确定循环 图示中没标出的物质,利用氧化还原反应的配平方法进行
配平,写出总反应,同时标出催化剂和反应条件。
二、化学反应速率与化学平衡
1.外界条件对可逆反应的正、逆反应速率的影响
方向是一致的,但影响程度不一定相同
条件改变 影响
增大反应物浓度 v 瞬间增大,v 瞬间不变,随后也增大
正 逆
v 和v 都增大,气体分子数减小方向的反应速率增大的程度大
正 逆
增大压强 对无气体参加或生成的化学反应的速率无影响
反应前后气体分子数不变的反应,正、逆反应速率同等程度地增大
升高温度 v 和v 都增大,但吸热反应方向的反应速率增大的程度大
正 逆
使用催化剂 能同等程度地改变正、逆反应速率
2.影响化学平衡的因素改变的条件(其他条件不变) 化学平衡移动的方向
增大反应物浓度或减小生成物浓度 向正反应方向移动
浓度
减小反应物浓度或增大生成物浓度 向逆反应方向移动
反应前后气体 增大压强 向气体分子总数减小的方向移动
压强(对有气体 体积改变 减小压强 向气体分子总数增大的方向移动
参加的反应) 反应前后气体
改变压强 平衡不移动
体积不变
升高温度 向吸热反应方向移动
温度
降低温度 向放热反应方向移动
催化剂 同等程度改变v 、v ,平衡不移动
正 逆
3.关于化学平衡移动方向判断的分析
化学平衡状态是一种参数恒定的状态,而化学平衡的移动是指条件改变所导致的化学反应进行的方向
的改变,化学平衡移动会带来化学平衡状态的参数的改变,但化学平衡移动不一定带来化学平衡状态的参
数的改变,且参数的变化趋势也不是恒定的。所以,化学平衡移动的方向取决于正、逆反应速率的改变。
所带来的净变化量,即决定平衡移动方向的判据为v(正)与v(逆)的关系;条件改变瞬间若带来了体系
中组分浓度的变化,且浓度商Q与平衡常数K的关系发生改变,化学平衡必然发生移动。因此,将v(正)
与v(逆)的关系及浓度商Q与平衡常数K的关系作为平衡移动及方向的判据是合理的,而百分含量、转化
率等平衡移动的判断依据没有抓住平衡移动的本质,必然带来结论的偏失。
4.牢记几种不能用勒夏特列原理解释的问题
(1)若外界条件改变后,无论平衡向正反应方向移动或向逆反应方向移动,都无法减弱外界条件的变化,
则平衡不移动。如对于H(g)+Br (g) 2HBr(g),由于反应前后气体的分子总数不变,外界压强增大或减
2 2
小时,平衡无论正向或逆向移动都不能减弱压强的改变,因此对于该反应,压强改变,平衡不发生移动。
(2)催化剂能同等程度地改变正、逆反应速率,所以催化剂不会影响化学平衡。
5.化学反应速率和化学平衡图像题解题方法
(1)分析图像纵、横坐标轴上的数据,观察图像上曲线的走向和变化趋势。
(2)若图像上的曲线有两条或者两条以上时,注意观察和理解曲线的交点和拐点所代表的意义,先出现
拐点的“温度高或压强大”。
(3)若图像中有三个量时,应“定一议二”。
(4)④加入催化剂或对等体反应改变压强,平衡不移动,但会改变到达平衡的时间。
(5)曲线斜率大表示反应速率快,可能是升温、加压或使用催化剂。
(6)综合运用勒夏特列原理解决问题。
考点一 化学反应与能量
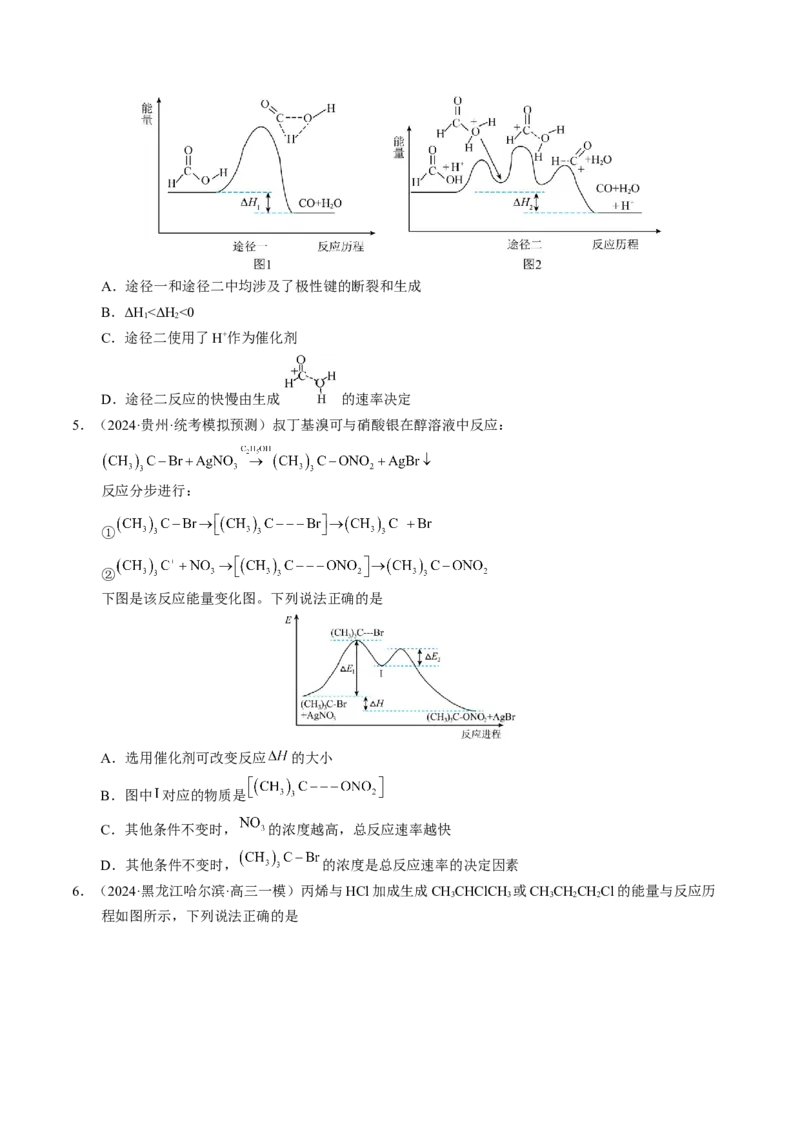
1.(2024·黑龙江大庆·高三一模)我国科学家已经成功地利用二氧化碳催化氢化获得甲酸,利用化合物1催化氢化二氧化碳的反应过程如图甲所示,其中化合物2与水反应生成化合物3与 的反应历程
如图乙所示,其中TS表示过渡态,Ⅰ表示中间体。下列说法错误的是
A.降低温度可促进化合物2与水反应生成化合物3与
B.化合物1为中间体Ⅰ1
C.图乙中形成中间体Ⅰ2的反应为总反应的决速步骤
D.化合物1到化合物2的过程中存在碳氧键的断裂和碳氢键的形成
2.(2024·辽宁沈阳·高三一模)基于非金属原子嵌入石墨烯三嗪基 中,用于催化一氧化碳加氢生成
甲醇的反应历程如图,其中吸附在催化剂表面上的物种用“ ”标注,下列说法中错误的是
A.整个反应历程中有极性键的断裂和生成
B.过渡态相对能量:TS55>TS44>TS77
C.物种吸附在催化剂表面的过程为吸热过程
D.反应决速步的活化能为
3.(2024·辽宁鞍山·统考一模)HA、HB为两种一元酸,为研究25°C时反应
的相关性质,查阅此温度下相关数据:△H=+29.1kJ/mol;
△S=+150.0J/(K·mol),下列说法正确的是
A.由于此过程△H>0,故HB比HA内能更低
B.△S对该反应自发性的影响小于△H
C.相对于B-,A-与质子的结合能力更强
D.体积和物质的量浓度均相同的NaA和NaB两溶液中,前者离子总数更多
4.(2024届·贵州·高三一模)甲酸常被用于橡胶、医药等工业,一定条件下可分解生成CO和HO。在无
2
催化剂和有催化剂的条件下,能量与反应历程的关系分别如图1、图2所示。下列说法错误的是A.途径一和途径二中均涉及了极性键的断裂和生成
B.ΔH<ΔH <0
1 2
C.途径二使用了H+作为催化剂
D.途径二反应的快慢由生成 的速率决定
5.(2024·贵州·统考模拟预测)叔丁基溴可与硝酸银在醇溶液中反应:
反应分步进行:
①
②
下图是该反应能量变化图。下列说法正确的是
A.选用催化剂可改变反应 的大小
B.图中 对应的物质是
C.其他条件不变时, 的浓度越高,总反应速率越快
D.其他条件不变时, 的浓度是总反应速率的决定因素
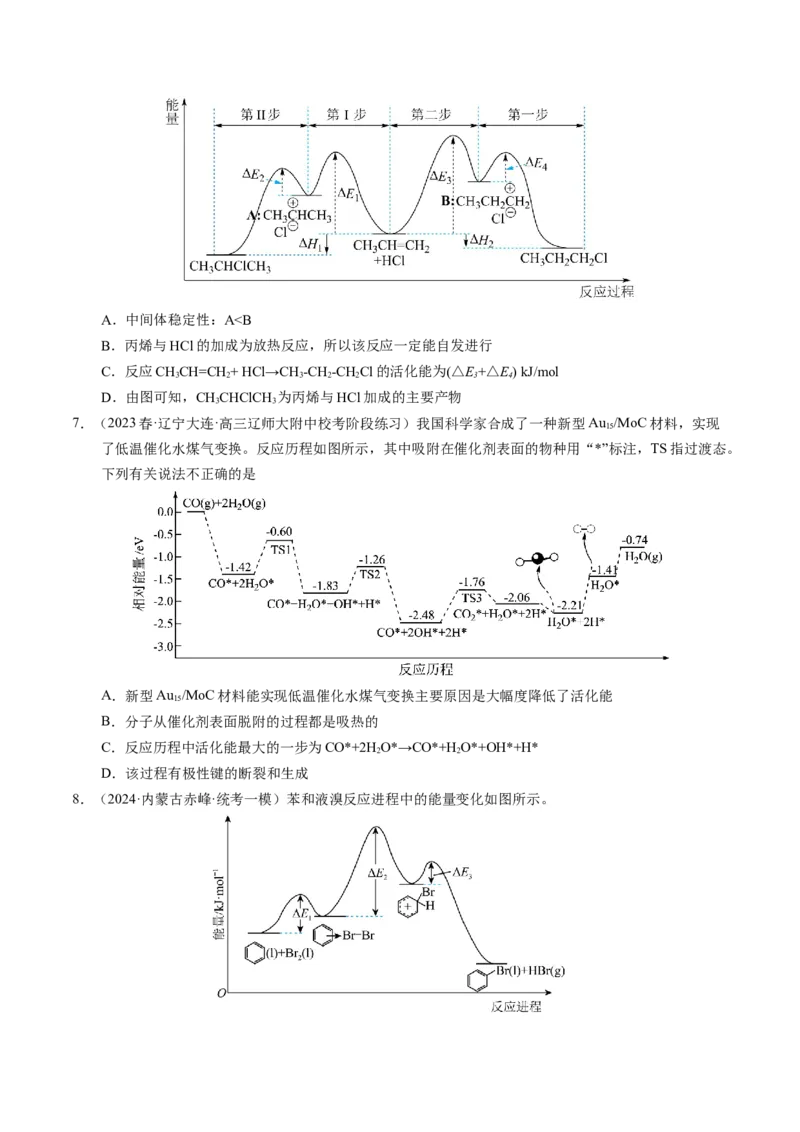
6.(2024·黑龙江哈尔滨·高三一模)丙烯与HCl加成生成CHCHClCH 或CHCHCHCl的能量与反应历
3 3 3 2 2
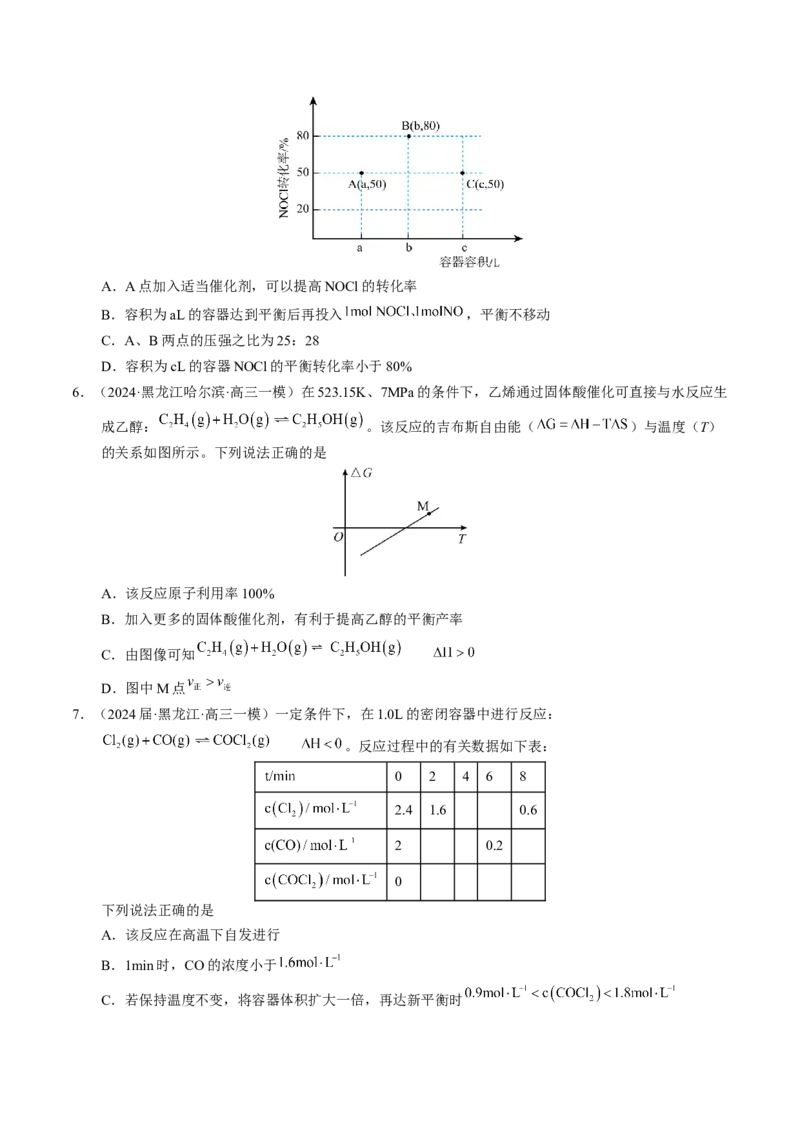
程如图所示,下列说法正确的是A.中间体稳定性:AⅠ
D.对于Ⅰ,平衡后向容器中再充入0.2mol CO和0.2mol ,平衡正向移动
9.(2023·辽宁·校联考二模)某温度下,在2L恒容密闭容器中4molNH COONH(s),发生如下反应
2 4
,在0-1min内,CO 的生成速率为0.4mol•L-1•min-1,0-2min
2
内,CO 的生成速率为0.3mol•L-1•min-1,0-3min内,CO 的生成速率为0.2mol•L-1•min-1,下列说法错误
2 2
的是
A.当混合气体的平均摩尔质量不变时,标志此反应达到了平衡状态
B.0-1min内,NH COONH(s)的反应速率为62.4g/min
2 4
C.30秒时,CO 的浓度大于0.2mol/L
2
D.2min时,再加入2molNH ,此时反应的V >V
3 逆 正
10.(2023·辽宁·校联考模拟预测)在600K下,按初始投料比 分别为1:1、1:2、1:3投
料,发生反应为 。测得不同压强下,CO平衡转化率如图所示。
下列叙述正确的是A.曲线X代表起始投料比为1:1
B. ,该反应达到平衡状态
C.若其他条件不变,升高温度会使对应的曲线上移
D.m点对应的 的平衡转化率为60%
11.(2023·辽宁·校联考三模)天然金刚石存在稌少,以石墨为原料制备人造金刚石成为当前研究热点。
下图是碳单质在不同温度、压强下存在形式的平衡图像,其中M区为金刚石的工业催化合成区,下列
有关说法错误的是
A.稳定性:金刚石<石墨
B.密度:金刚石>石墨
C.在M区实现金刚石的合成,高温环境有利于提高石墨的平衡转化率
D.上图Q区与R区中,表示气态碳单质 存在的区域应出现在R区
12.(2023·辽宁大连·大连二十四中校考模拟预测)实验室在1L的密闭容器中进行模拟合成实验,将
和 通入容器中,在催化剂的作用下发生:
反应I: (主反应);
反应II:
500℃时,将容器的体积压缩到原来的一半,在其他条件不变的情况下,平衡体系中变化正确的是
A. 减小
B.反应I正反应速率加快,逆反应速率减慢
C. 的物质的量增加D.重新平衡时 增大
13.(2023·辽宁沈阳·东北育才学校校考模拟预测)在催化剂作用下,向容积为1L的容器中加入1molX和
3molY,发生反应:X(g)+2Y(s) 2Z(s),平衡时和反应10min时X的转化率α(X)随温度的变化分
别如曲线I、Ⅱ所示。下列说法正确的是
A.使用更高效的催化剂,可以使b点移动到d点
B.保持温度和体积不变,向d点体系中再充入1molX,再次达平衡时c(X)>0.4mol/L
C.0-10min的平均反应速率:v(a)<v(c)
D.bc段变化可能是由于升高温度平衡逆向移动
14.(2023·辽宁沈阳·辽宁实验中学校考模拟预测) 可以和 发生反应:
。一定温度下,向某恒容密闭容器中加入足量铁粉并充入一定量的
气体,反应过程中 气体和 气体的浓度与时间的关系如图所示。下列说法正确的是
A. 时该化学反应达到平衡状态
B.平衡后向容器内充入 ,重新达到平衡时 增大
C.4 min时, 的转化率约为71.4%
D.4 min内, 的平均反应速率
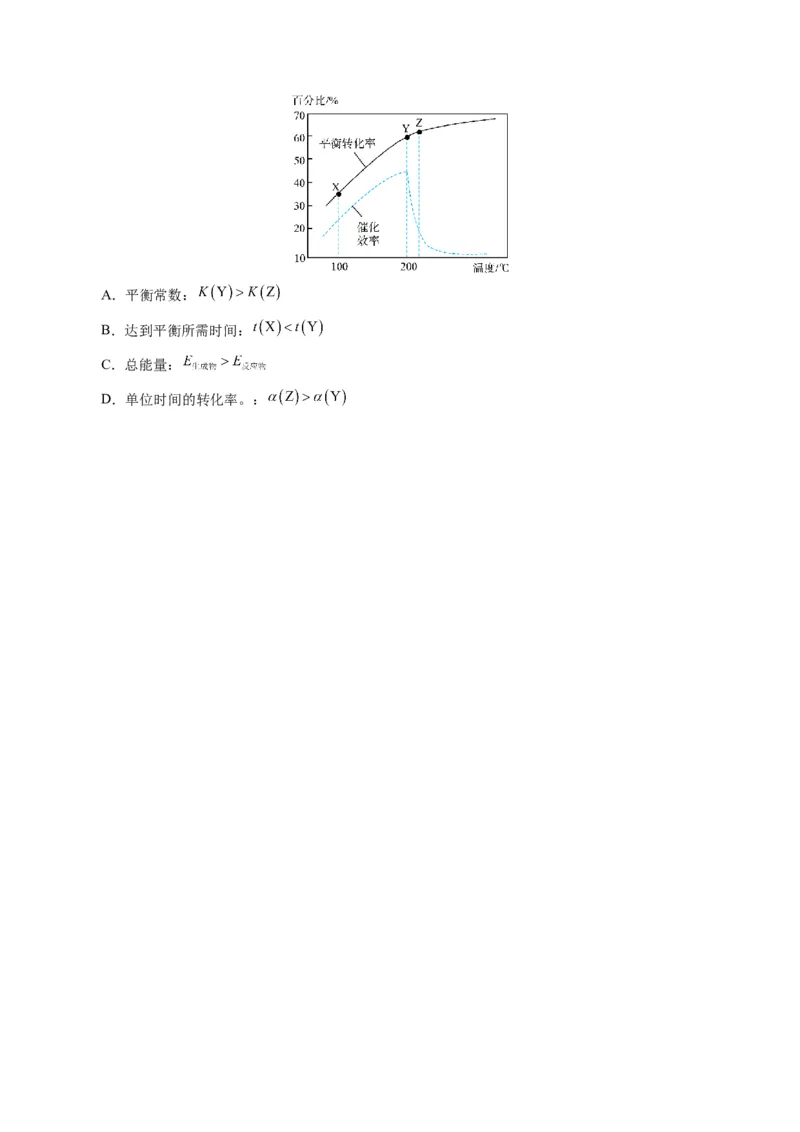
15.(2023·辽宁阜新·校联考模拟预测)一定条件下热解制取 :
。已知其他条件不变时,温度对 的平衡转化率和催化
剂催化效率的影响如图所示。下列说法一定正确的是A.平衡常数:
B.达到平衡所需时间:
C.总能量:
D.单位时间的转化率。: