文档内容
押选择题
化学反应与能量、化学反应速率与化学平衡
核心考点 考情统计 考向预测 备考策略
化学反应与 2023·辽宁卷,12 考查热化学方程式反应热 要求考生理解盖斯定律,并能
能量 2022·辽宁卷,10、 的计算、能量变化与 运用盖斯定律进行有关反应焓
12 ΔH、活化能的图像问 变的计算。关注能源问题、科
2021·辽宁卷,11 题。 技成果,运用化学基本理论或
有机物的知识解决实际问题。
化学反应速 2022·辽宁卷,12 化学反应速率的计算和外 围绕勒夏特列原理的理解,通
率与化学平 2021·辽宁卷,12 界条件对化学反应速率的 过实验、判断、图像、计算等
衡 影响;化学平衡的特征及 形成对化学平衡移动进行综合
化学平衡常数的计算和理 考查,是化学反应速率和化学
解。 (平衡)状态的综合应用体现,
平时加强针对性强化训练,注
重规律和方法技能的总结,提
高解题能力。
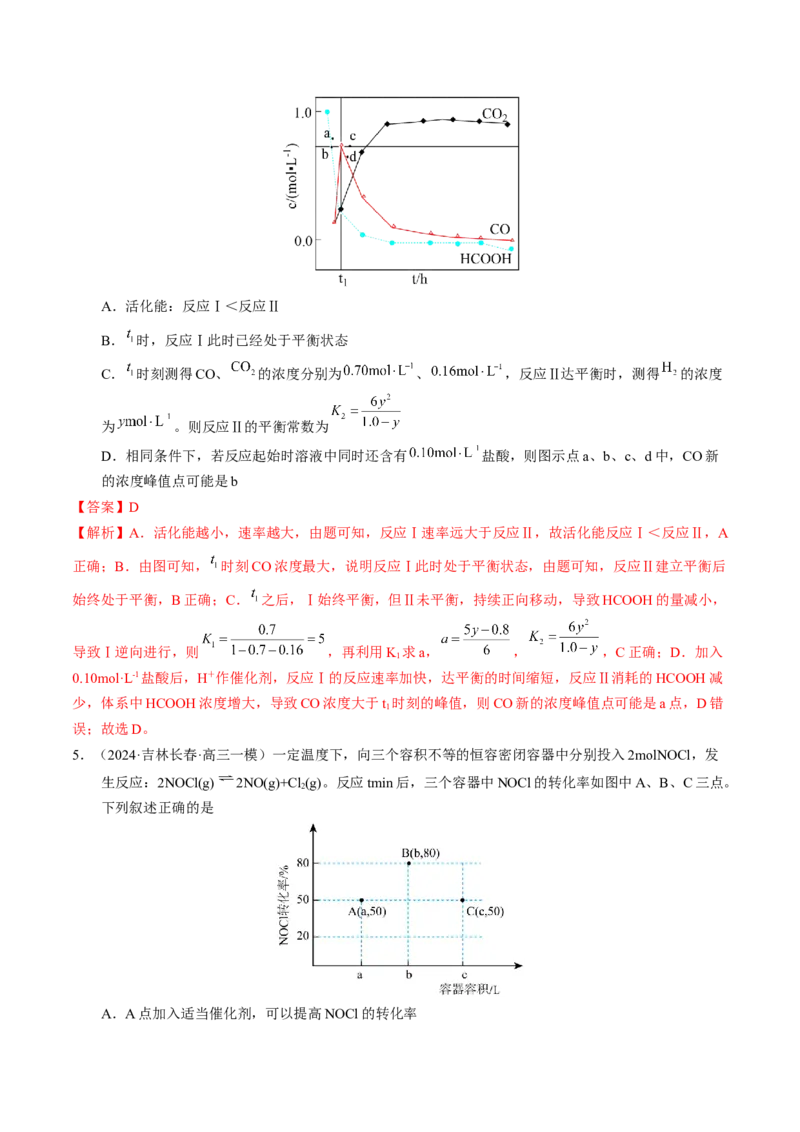
1. (2023·辽宁卷)一定条件下,酸性 溶液与 发生反应, (Ⅱ)起催化作用,过程中不
同价态含 粒子的浓度随时间变化如下图所示。下列说法正确的是
A. (Ⅲ)不能氧化
B. 随着反应物浓度的减小,反应速率逐渐减小
C. 该条件下, (Ⅱ)和 (Ⅶ)不能大量共存D. 总反应为:
【答案】C
【分析】开始一段时间(大约13min前)随着时间的推移Mn(Ⅶ)浓度减小直至为0,Mn(Ⅲ)浓度增大直至
达到最大值,结合图像,此时间段主要生成 Mn(Ⅲ),同时先生成少量Mn(Ⅳ)后Mn(Ⅳ)被消耗;后来(大
约13min后)随着时间的推移Mn(Ⅲ)浓度减少,Mn(Ⅱ)的浓度增大;据此作答。
【解析】A.由图像可知,随着时间的推移Mn(Ⅲ)的浓度先增大后减小,说明开始反应生成Mn(Ⅲ),后
Mn(Ⅲ)被消耗生成Mn(Ⅱ),Mn(Ⅲ)能氧化HC O ,A项错误;B.随着反应物浓度的减小,到大约13min
2 2 4
时开始生成Mn(Ⅱ),Mn(Ⅱ)对反应起催化作用,13min后反应速率会增大,B项错误;C.由图像可知,
Mn(Ⅶ)的浓度为0后才开始生成Mn(Ⅱ),该条件下Mn(Ⅱ)和Mn(Ⅶ)不能大量共存,C项正确;D.HC O
2 2 4
为弱酸,在离子方程式中应以化学式保留,总反应为 2 +5H C O+6H+=2Mn2++10CO ↑+8H O,D项
2 2 4 2 2
错误;答案选C 。
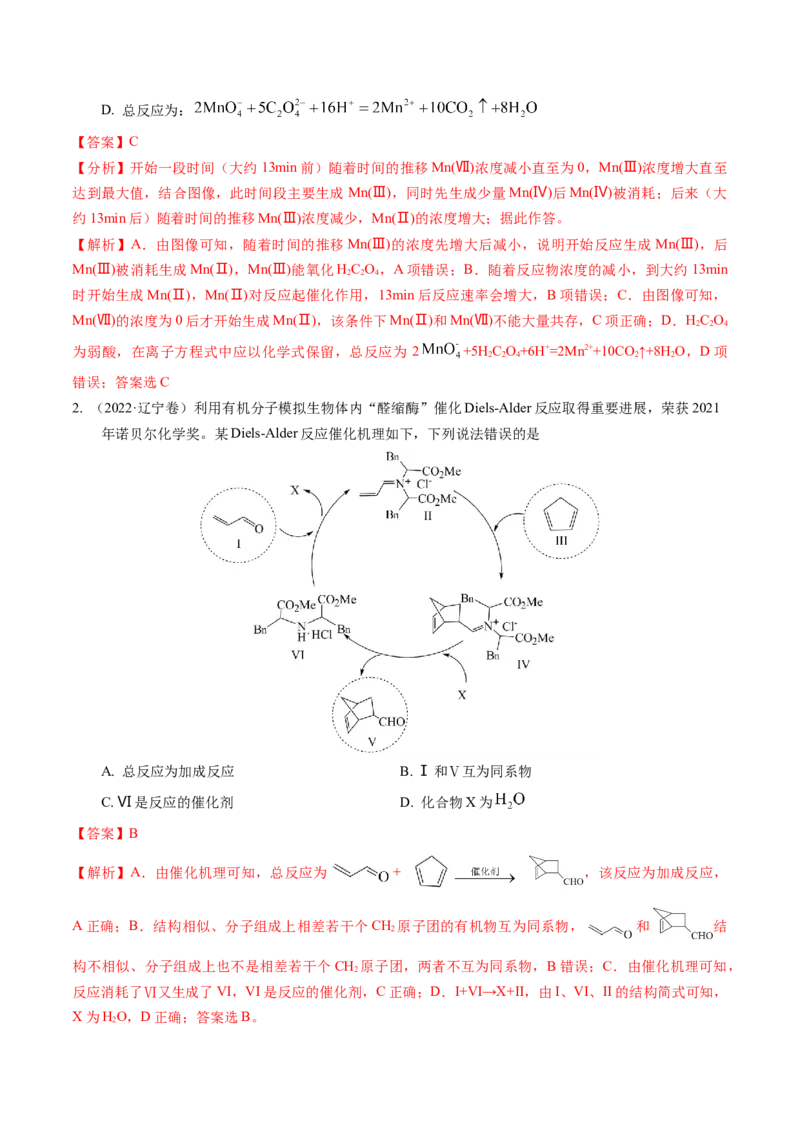
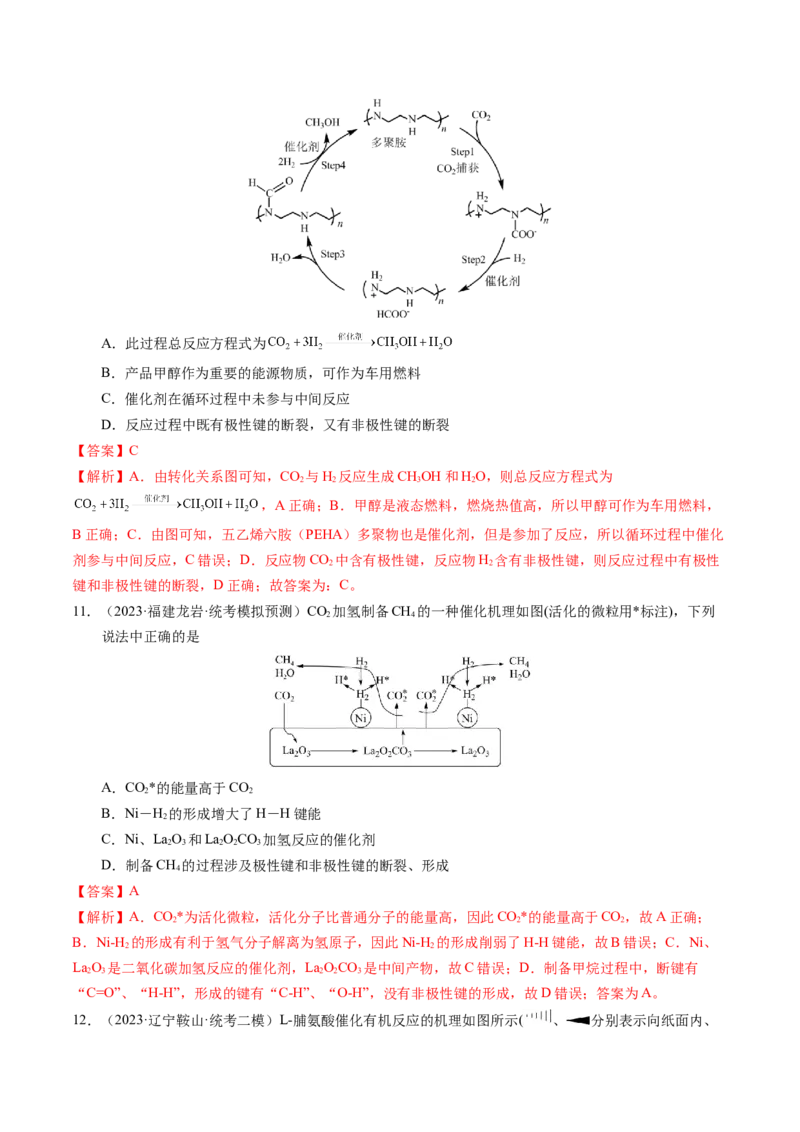
2. (2022·辽宁卷)利用有机分子模拟生物体内“醛缩酶”催化Diels-Alder反应取得重要进展,荣获2021
年诺贝尔化学奖。某Diels-Alder反应催化机理如下,下列说法错误的是
A. 总反应为加成反应 B. Ⅰ和Ⅴ互为同系物
C. Ⅵ是反应的催化剂 D. 化合物X为
【答案】B
【解析】A.由催化机理可知,总反应为 + ,该反应为加成反应,
A正确;B.结构相似、分子组成上相差若干个CH 原子团的有机物互为同系物, 和 结
2
构不相似、分子组成上也不是相差若干个CH 原子团,两者不互为同系物,B错误;C.由催化机理可知,
2
反应消耗了Ⅵ又生成了VI,VI是反应的催化剂,C正确;D.I+VI→X+II,由I、VI、II的结构简式可知,
X为HO,D正确;答案选B。
23. (2022·辽宁卷)HO(l)、NH (l)均可自耦电离: 、 。下
2 3
列反应与 CHCHOH+HBr原理不同的是
3 2
A.
B.
C.
D.
【答案】C
【解析】A.根据题目信息可知, 和 互相交换成分生成 和 。由
可得, 与 互相交换成分生成 和 ,与题述反应原理
相同,A正确;B.由于 可自电离, 可写为 , 与 交换成分生成
和 与题述反应原理相同,故B正确;C. 与 反应生成了单质 ,反应物没有
互相交换成分,与题述反应原理不同,故C错误;D. 和 互相交换成分生成了 和 ,
与题述反应原理相同,故D正确;故答案选C 。
4.(2022·辽宁卷)某温度下,在 恒容密闭容器中 发生反应 ,有关
数据如下:
时间段/ 产物Z的平均生成速率/
0~2 0.20
0~4 0.15
0~6 0.10
下列说法错误的是
A. 时,Z的浓度大于
B. 时,加入 ,此时
C. 时,Y的体积分数约为33.3%
D. 时,X的物质的量为
【答案】B
【解析】A.反应开始一段时间,随着时间的延长,反应物浓度逐渐减小,产物Z的平均生成速率逐渐减
小,则 内Z的平均生成速率大于 内的,故 时,Z的浓度大于 ,A正
确;B. 时生成的Z的物质的量为 , 时生成的Z的物质的量为 ,故反应在 时已达到平衡,设达到平衡时生
了 ,列三段式:
根据 ,得 ,则Y的平衡浓度为 ,Z的平衡浓度为 ,平衡常数
, 时Y的浓度为 ,Z的浓度为 ,加入 后
Z的浓度变为 , ,反应正向进行,故 ,B错误;
C.反应生成 的Y与Z的物质的量之比恒等于1∶2,反应体系中只有Y和Z为气体,相同条件下,体积之
比等于物质的量之比, ,故Y的体积分数始终约为33.3%,C正确;D.由B项分析可知
时反应处于平衡状态,此时生成Z为 ,则X的转化量为 ,初始X的物质的量为 ,剩
余X的物质的量为 ,D正确;故答案选B。
5.(2021·辽宁卷)某温度下,在恒容密闭容器中加入一定量X,发生反应 ,一段时
间后达到平衡。下列说法错误的是
A. 升高温度,若 增大,则
B. 加入一定量Z,达新平衡后 减小
C. 加入等物质的量的Y和Z,达新平衡后 增大
D. 加入一定量氩气,平衡不移动
【答案】C
【解析】A.根据勒夏特列原理可知,升高温度,化学平衡向着吸热反应方向移动,而 增大,说明平
衡正向移动,故则 ,A正确;B.加入一定量Z,Z的浓度增大,平衡逆向移动,故达新平衡后
减小,B正确;C.加入等物质的量的Y和Z,Z的浓度增大,平衡逆向移动,由于X、Y均为固体,
故K=c(Z),达新平衡后 不变,C错误;D.加入一定量氩气,加入瞬间,X、Z的浓度保持不变,故
正、逆反应速率不变,故平衡不移动,D正确;故答案为:C。
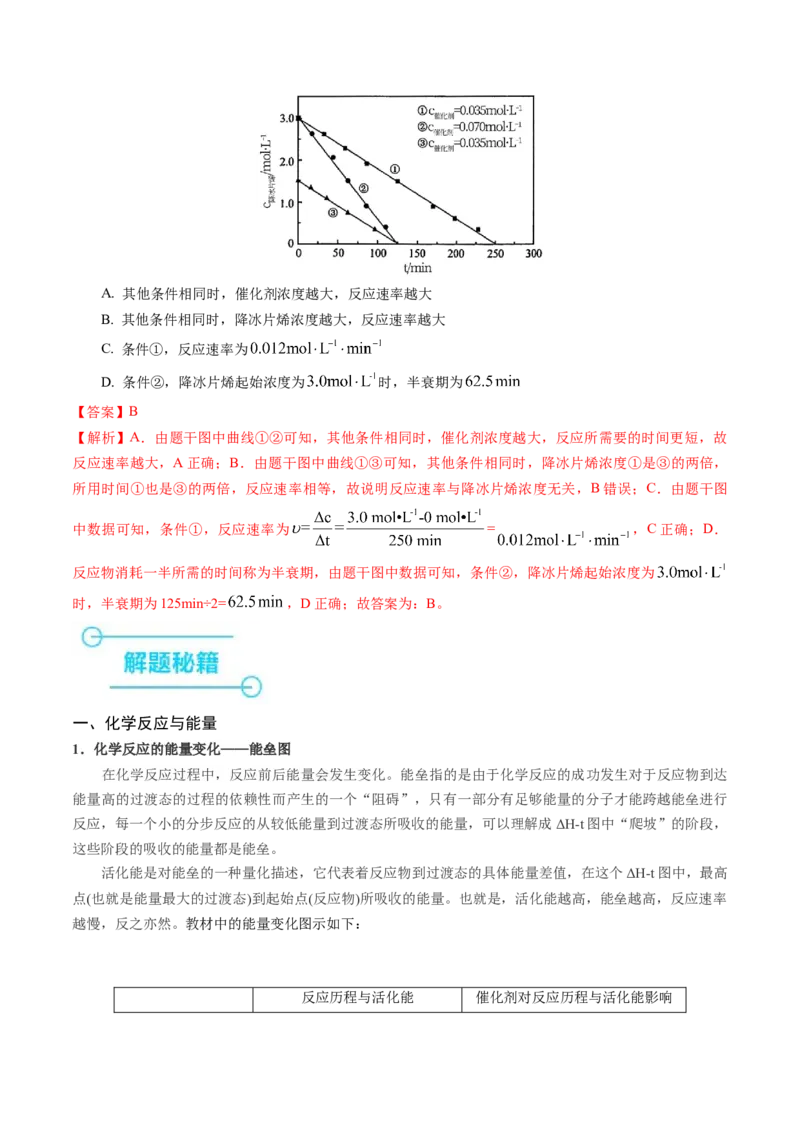
6.(2021·辽宁卷)某温度下,降冰片烯在钛杂环丁烷催化下聚合,反应物浓度与催化剂浓度及时间关系如
图。已知反应物消耗一半所需的时间称为半衰期,下列说法错误的是A. 其他条件相同时,催化剂浓度越大,反应速率越大
B. 其他条件相同时,降冰片烯浓度越大,反应速率越大
C. 条件①,反应速率为
D. 条件②,降冰片烯起始浓度为 时,半衰期为
【答案】B
【解析】A.由题干图中曲线①②可知,其他条件相同时,催化剂浓度越大,反应所需要的时间更短,故
反应速率越大,A正确;B.由题干图中曲线①③可知,其他条件相同时,降冰片烯浓度①是③的两倍,
所用时间①也是③的两倍,反应速率相等,故说明反应速率与降冰片烯浓度无关,B错误;C.由题干图
中数据可知,条件①,反应速率为 = ,C正确;D.
反应物消耗一半所需的时间称为半衰期,由题干图中数据可知,条件②,降冰片烯起始浓度为
时,半衰期为125min÷2= ,D正确;故答案为:B。
一、化学反应与能量
1.化学反应的能量变化——能垒图
在化学反应过程中,反应前后能量会发生变化。能垒指的是由于化学反应的成功发生对于反应物到达
能量高的过渡态的过程的依赖性而产生的一个“阻碍”,只有一部分有足够能量的分子才能跨越能垒进行
反应,每一个小的分步反应的从较低能量到过渡态所吸收的能量,可以理解成ΔH-t图中“爬坡”的阶段,
这些阶段的吸收的能量都是能垒。
活化能是对能垒的一种量化描述,它代表着反应物到过渡态的具体能量差值,在这个ΔH-t图中,最高
点(也就是能量最大的过渡态)到起始点(反应物)所吸收的能量。也就是,活化能越高,能垒越高,反应速率
越慢,反之亦然。教材中的能量变化图示如下:
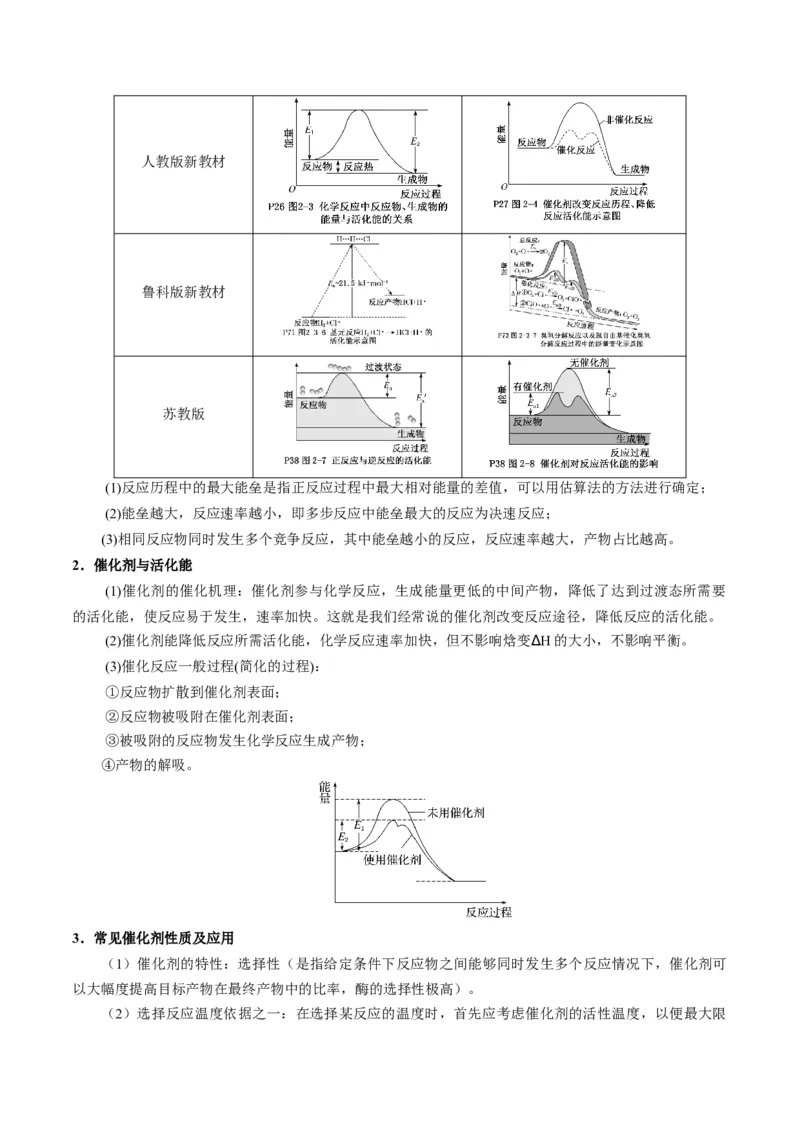
反应历程与活化能 催化剂对反应历程与活化能影响人教版新教材
鲁科版新教材
苏教版
(1)反应历程中的最大能垒是指正反应过程中最大相对能量的差值,可以用估算法的方法进行确定;
(2)能垒越大,反应速率越小,即多步反应中能垒最大的反应为决速反应;
(3)相同反应物同时发生多个竞争反应,其中能垒越小的反应,反应速率越大,产物占比越高。
2.催化剂与活化能
(1)催化剂的催化机理:催化剂参与化学反应,生成能量更低的中间产物,降低了达到过渡态所需要
的活化能,使反应易于发生,速率加快。这就是我们经常说的催化剂改变反应途径,降低反应的活化能。
(2)催化剂能降低反应所需活化能,化学反应速率加快,但不影响焓变∆H的大小,不影响平衡。
(3)催化反应一般过程(简化的过程):
①反应物扩散到催化剂表面;
②反应物被吸附在催化剂表面;
③被吸附的反应物发生化学反应生成产物;
④产物的解吸。
3.常见催化剂性质及应用
(1)催化剂的特性:选择性(是指给定条件下反应物之间能够同时发生多个反应情况下,催化剂可
以大幅度提高目标产物在最终产物中的比率,酶的选择性极高)。
(2)选择反应温度依据之一:在选择某反应的温度时,首先应考虑催化剂的活性温度,以便最大限度地发挥催化剂的作用。
(3)催化剂中毒:由于某些物质(反应原料中带入的杂质、催化剂自身的某些杂质、反应产物或副
产物)的作用而使催化活性衰退或丧失的现象。
(4)催化剂影响速率不影响化学平衡:对于可逆反应,催化剂同等程度地改变正逆反应速率,因而
不能改变反应物的转化率,但可缩短反应达到化学平衡的时间。
(5)周期表中催化剂寻找区域:过渡元素区。
中学中常用的催化剂:酶是蛋白质,也是催化剂。二氧化锰、五氧化二钒、铁触媒、铂铑催化剂、
Ni、Cu、Ag,浓硫酸、稀硫酸。
(6)教材研究催化剂的三个实验:①一个反应的催化剂可能有多种。如过氧化氢溶液分解的催化剂,
除了二氧化锰之外,还可以用FeCl3、CuSO4溶液。②高锰酸钾与草酸反应,生成的Mn2+是访反应的催化
剂,褪色速率会突然加快,是易被忽视的自催化反应。③淀粉水解实验,酶的催化条件温和而高效。
4.“环式”反应历程与机理
“环式”反应过程图如下:
“入环”的物质为反应物,如图中的①④;位于“环上”的物质为催化剂或中间体,如图中的⑤⑥⑦
⑧;“出环”的物质为生成物,如图中的②③;由反应物和生成物可快速得出总反应方程式。
明确反应物:最重要的要看清图示中的箭头,明确哪些物质进行循环体系,哪些物质离子循环体系,
进行循环体系的物质为总反应的反应物,离子循环体系的物质为总反应的生成物。
明确催化剂和中间产物:从循环图示中找出分解的若干反应,通过分步反应区分哪些是催化剂,哪些
是中间产物。
写出总反应:依据质量守恒定律,确定循环 图示中没标出的物质,利用氧化还原反应的配平方法进行
配平,写出总反应,同时标出催化剂和反应条件。
二、化学反应速率与化学平衡
1.外界条件对可逆反应的正、逆反应速率的影响
方向是一致的,但影响程度不一定相同
条件改变 影响
增大反应物浓度 v 瞬间增大,v 瞬间不变,随后也增大
正 逆
增大压强 v 和v 都增大,气体分子数减小方向的反应速率增大的程度大
正 逆对无气体参加或生成的化学反应的速率无影响
反应前后气体分子数不变的反应,正、逆反应速率同等程度地增大
升高温度 v 和v 都增大,但吸热反应方向的反应速率增大的程度大
正 逆
使用催化剂 能同等程度地改变正、逆反应速率
2.影响化学平衡的因素
改变的条件(其他条件不变) 化学平衡移动的方向
增大反应物浓度或减小生成物浓度 向正反应方向移动
浓度
减小反应物浓度或增大生成物浓度 向逆反应方向移动
反应前后气体 增大压强 向气体分子总数减小的方向移动
压强(对有气体 体积改变 减小压强 向气体分子总数增大的方向移动
参加的反应) 反应前后气体
改变压强 平衡不移动
体积不变
升高温度 向吸热反应方向移动
温度
降低温度 向放热反应方向移动
催化剂 同等程度改变v 、v ,平衡不移动
正 逆
3.关于化学平衡移动方向判断的分析
化学平衡状态是一种参数恒定的状态,而化学平衡的移动是指条件改变所导致的化学反应进行的方向
的改变,化学平衡移动会带来化学平衡状态的参数的改变,但化学平衡移动不一定带来化学平衡状态的参
数的改变,且参数的变化趋势也不是恒定的。所以,化学平衡移动的方向取决于正、逆反应速率的改变。
所带来的净变化量,即决定平衡移动方向的判据为v(正)与v(逆)的关系;条件改变瞬间若带来了体系
中组分浓度的变化,且浓度商Q与平衡常数K的关系发生改变,化学平衡必然发生移动。因此,将v(正)
与v(逆)的关系及浓度商Q与平衡常数K的关系作为平衡移动及方向的判据是合理的,而百分含量、转化
率等平衡移动的判断依据没有抓住平衡移动的本质,必然带来结论的偏失。
4.牢记几种不能用勒夏特列原理解释的问题
(1)若外界条件改变后,无论平衡向正反应方向移动或向逆反应方向移动,都无法减弱外界条件的变化,
则平衡不移动。如对于H(g)+Br (g) 2HBr(g),由于反应前后气体的分子总数不变,外界压强增大或减
2 2
小时,平衡无论正向或逆向移动都不能减弱压强的改变,因此对于该反应,压强改变,平衡不发生移动。
(2)催化剂能同等程度地改变正、逆反应速率,所以催化剂不会影响化学平衡。
5.化学反应速率和化学平衡图像题解题方法
(1)分析图像纵、横坐标轴上的数据,观察图像上曲线的走向和变化趋势。
(2)若图像上的曲线有两条或者两条以上时,注意观察和理解曲线的交点和拐点所代表的意义,先出现
拐点的“温度高或压强大”。
(3)若图像中有三个量时,应“定一议二”。
(4)④加入催化剂或对等体反应改变压强,平衡不移动,但会改变到达平衡的时间。
(5)曲线斜率大表示反应速率快,可能是升温、加压或使用催化剂。
(6)综合运用勒夏特列原理解决问题。考点一 化学反应与能量
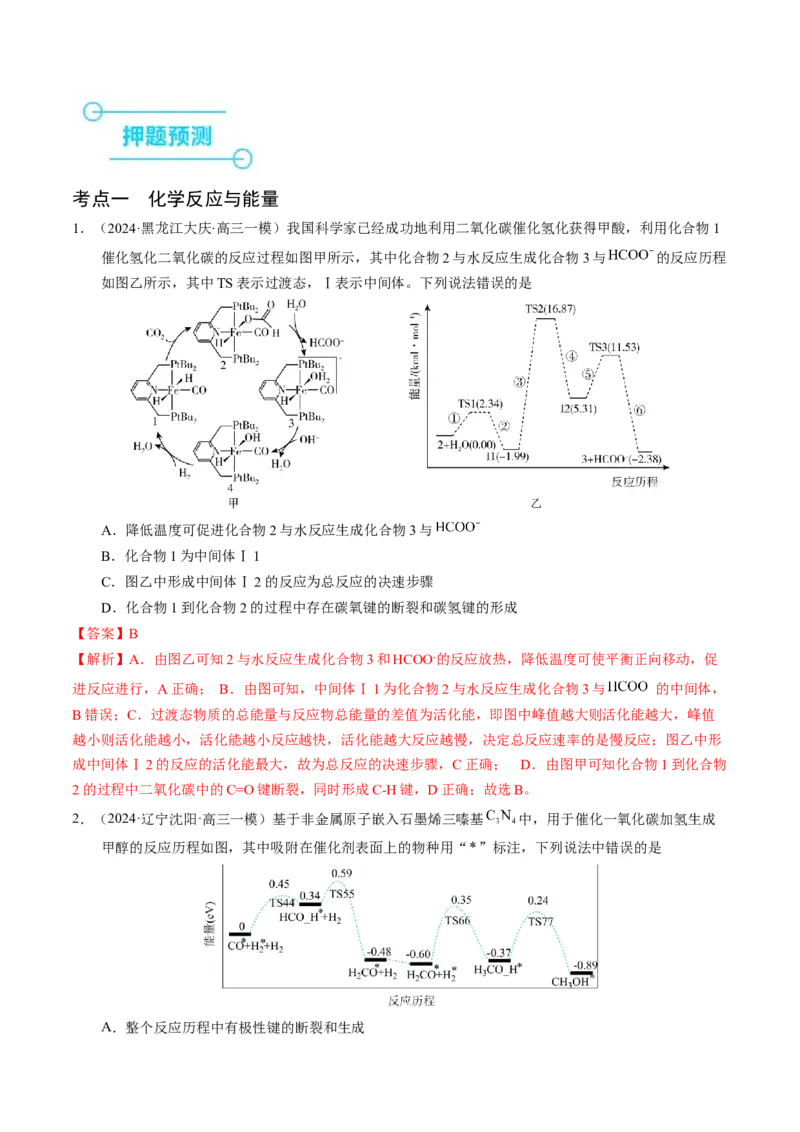
1.(2024·黑龙江大庆·高三一模)我国科学家已经成功地利用二氧化碳催化氢化获得甲酸,利用化合物1
催化氢化二氧化碳的反应过程如图甲所示,其中化合物2与水反应生成化合物3与 的反应历程
如图乙所示,其中TS表示过渡态,Ⅰ表示中间体。下列说法错误的是
A.降低温度可促进化合物2与水反应生成化合物3与
B.化合物1为中间体Ⅰ1
C.图乙中形成中间体Ⅰ2的反应为总反应的决速步骤
D.化合物1到化合物2的过程中存在碳氧键的断裂和碳氢键的形成
【答案】B
【解析】A.由图乙可知2与水反应生成化合物3和HCOO-的反应放热,降低温度可使平衡正向移动,促
进反应进行,A正确; B.由图可知,中间体Ⅰ1为化合物2与水反应生成化合物3与 的中间体,
B错误;C.过渡态物质的总能量与反应物总能量的差值为活化能,即图中峰值越大则活化能越大,峰值
越小则活化能越小,活化能越小反应越快,活化能越大反应越慢,决定总反应速率的是慢反应;图乙中形
成中间体Ⅰ2的反应的活化能最大,故为总反应的决速步骤,C正确; D.由图甲可知化合物1到化合物
2的过程中二氧化碳中的C=O键断裂,同时形成C-H键,D正确;故选B。
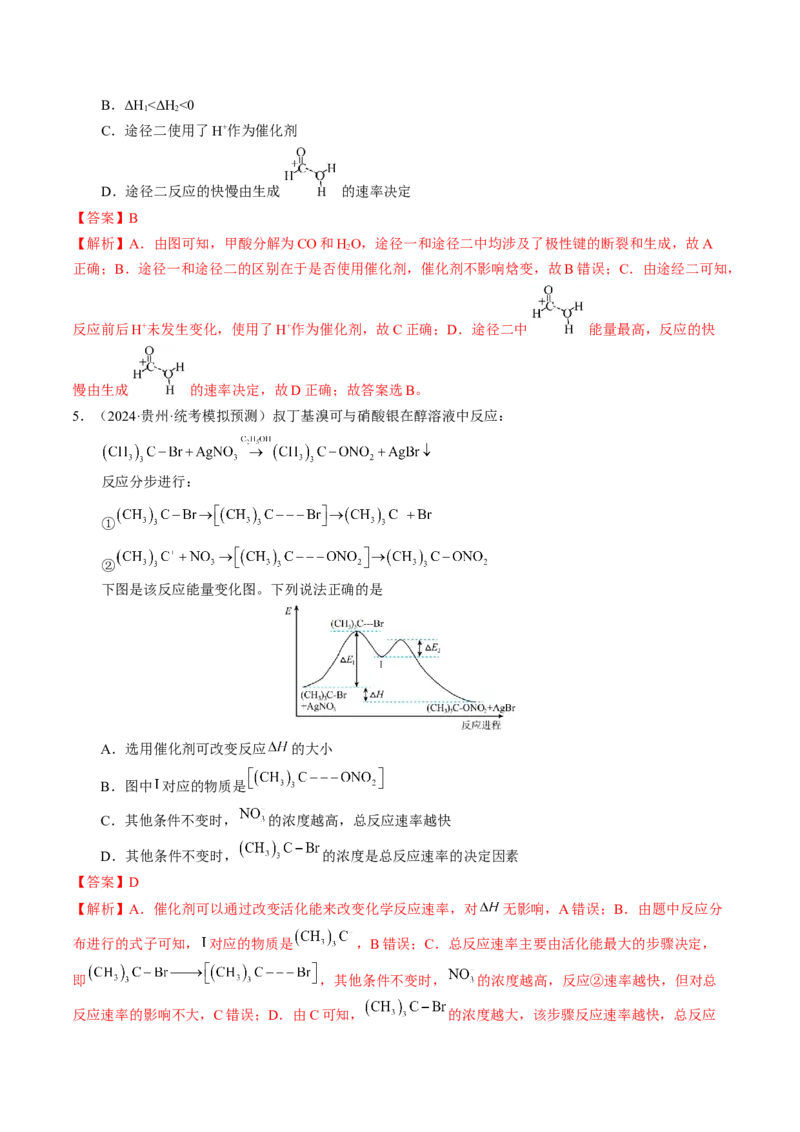
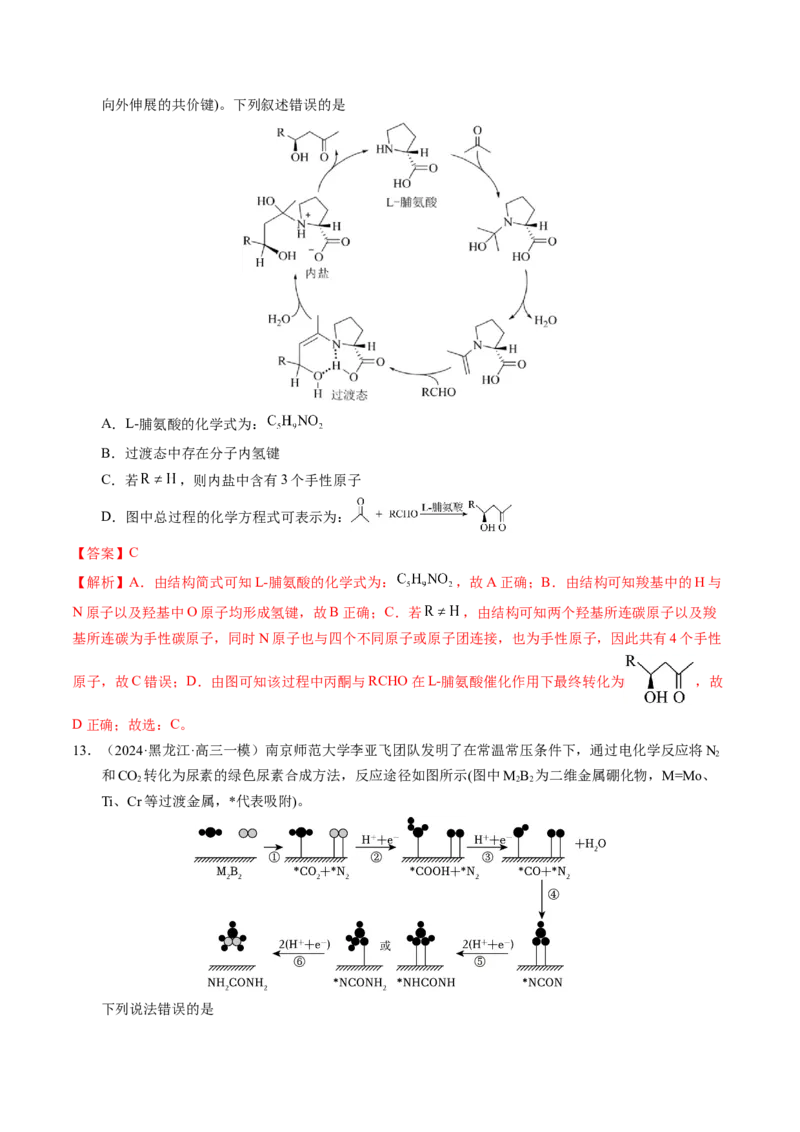
2.(2024·辽宁沈阳·高三一模)基于非金属原子嵌入石墨烯三嗪基 中,用于催化一氧化碳加氢生成
甲醇的反应历程如图,其中吸附在催化剂表面上的物种用“ ”标注,下列说法中错误的是
A.整个反应历程中有极性键的断裂和生成B.过渡态相对能量:TS55>TS44>TS77
C.物种吸附在催化剂表面的过程为吸热过程
D.反应决速步的活化能为
【答案】C
【解析】A.由图可知,一氧化碳催化加氢生成甲醇的反应中有极性键的断裂和生成,故A正确;B.由
图可知,过渡态相对能量的大小顺序为TS55>TS44>TS77,故B正确;C.由图可知,吸附在催化剂表面
的生成物总能量低于反应物的总能量,为放热过程,故C错误;D.反应的活化能越大,反应速率越慢,
反应决速步为慢反应,由图可知,反应HCO*+H =H COH 的活化能最大,反应速率最慢,则反应决速步
2 3 -
的活化能为0.35eV—(—0.60eV)=0.95eV,故D正确;故选C。
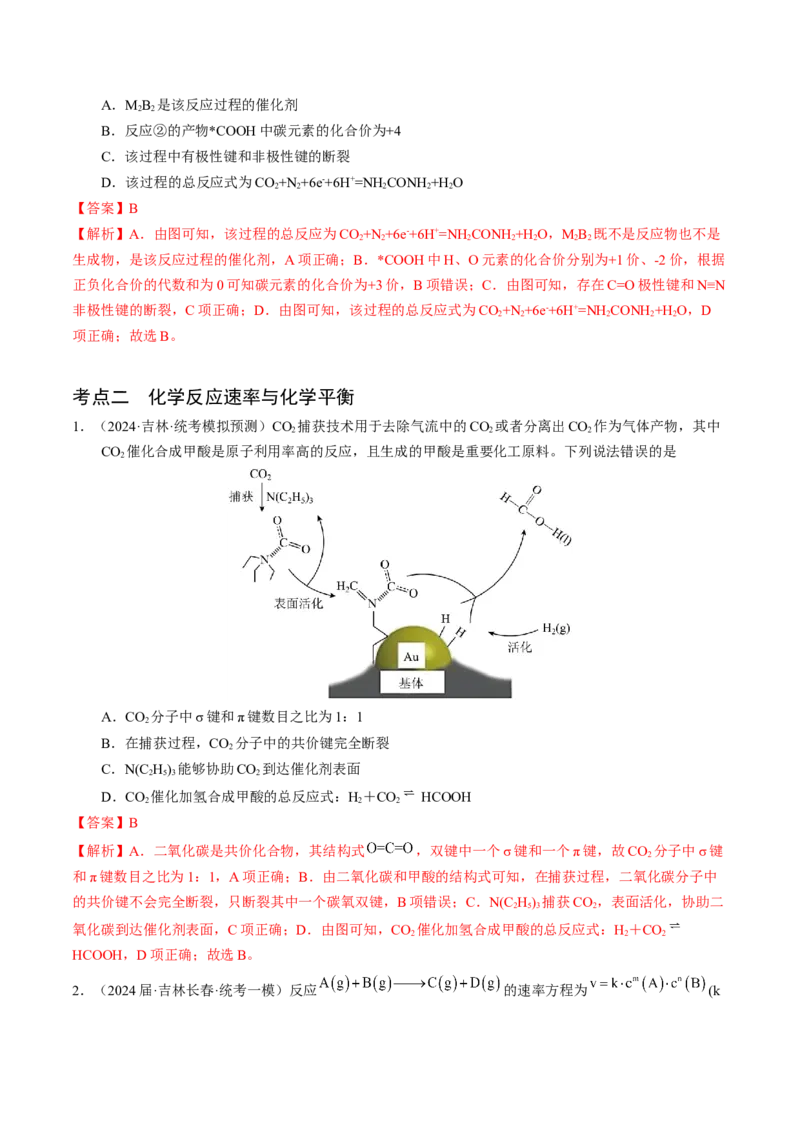
3.(2024·辽宁鞍山·统考一模)HA、HB为两种一元酸,为研究25°C时反应
的相关性质,查阅此温度下相关数据:△H=+29.1kJ/mol;
△S=+150.0J/(K·mol),下列说法正确的是
A.由于此过程△H>0,故HB比HA内能更低
B.△S对该反应自发性的影响小于△H
C.相对于B-,A-与质子的结合能力更强
D.体积和物质的量浓度均相同的NaA和NaB两溶液中,前者离子总数更多
【答案】C
【解析】A.能量越低越稳定,该反应的焓变大于0,说明反应物总能量小于生成物总能量,但无法判断
HA、HB能量的相对大小,选项A错误;B.该反应中没有气体参加,△S=0,选项B错误;C.强酸能
和弱酸盐反应生成弱酸,由A-(aq)+HB(aq) HA(aq)+B-(aq)可得,酸性HB>HA,所以结合质子能力为B-
<A-,即A-与质子的结合能力更强,选项C正确;D.由B可知,酸性HB>HA,体积和物质的量浓度均
相同的NaA和NaB两溶液中分别存在电荷守恒c(Na+)+c(H+)=c(OH﹣)+c(A﹣)、c(Na+)+c(H+)=c(OH﹣)+c(B
﹣),每一种溶液中离子浓度总和是其溶液中所有阳离子浓度的2倍,水解程度为A﹣>B﹣,则两溶液中
c(OH﹣)是NaA溶液大于NaB溶液,两溶液中c(H+)是NaA溶液小于NaB溶液,两种溶液中c(Na+)相等,两
种溶液中[c(Na+)+c(H+)]是NaA溶液小于NaB溶液,所以离子总物质的量是前者小于后者,离子总数是前
者小于后者,选项D错误;答案选C。
4.(2024届·贵州·高三一模)甲酸常被用于橡胶、医药等工业,一定条件下可分解生成CO和HO。在无
2
催化剂和有催化剂的条件下,能量与反应历程的关系分别如图1、图2所示。下列说法错误的是
A.途径一和途径二中均涉及了极性键的断裂和生成B.ΔH<ΔH <0
1 2
C.途径二使用了H+作为催化剂
D.途径二反应的快慢由生成 的速率决定
【答案】B
【解析】A.由图可知,甲酸分解为CO和HO,途径一和途径二中均涉及了极性键的断裂和生成,故A
2
正确;B.途径一和途径二的区别在于是否使用催化剂,催化剂不影响焓变,故B错误;C.由途经二可知,
反应前后H+未发生变化,使用了H+作为催化剂,故C正确;D.途径二中 能量最高,反应的快
慢由生成 的速率决定,故D正确;故答案选B。
5.(2024·贵州·统考模拟预测)叔丁基溴可与硝酸银在醇溶液中反应:
反应分步进行:
①
②
下图是该反应能量变化图。下列说法正确的是
A.选用催化剂可改变反应 的大小
B.图中 对应的物质是
C.其他条件不变时, 的浓度越高,总反应速率越快
D.其他条件不变时, 的浓度是总反应速率的决定因素
【答案】D
【解析】A.催化剂可以通过改变活化能来改变化学反应速率,对 无影响,A错误;B.由题中反应分
布进行的式子可知, 对应的物质是 ,B错误;C.总反应速率主要由活化能最大的步骤决定,
即 ,其他条件不变时, 的浓度越高,反应②速率越快,但对总
反应速率的影响不大,C错误;D.由C可知, 的浓度越大,该步骤反应速率越快,总反应速率越快,D正确;故选D。
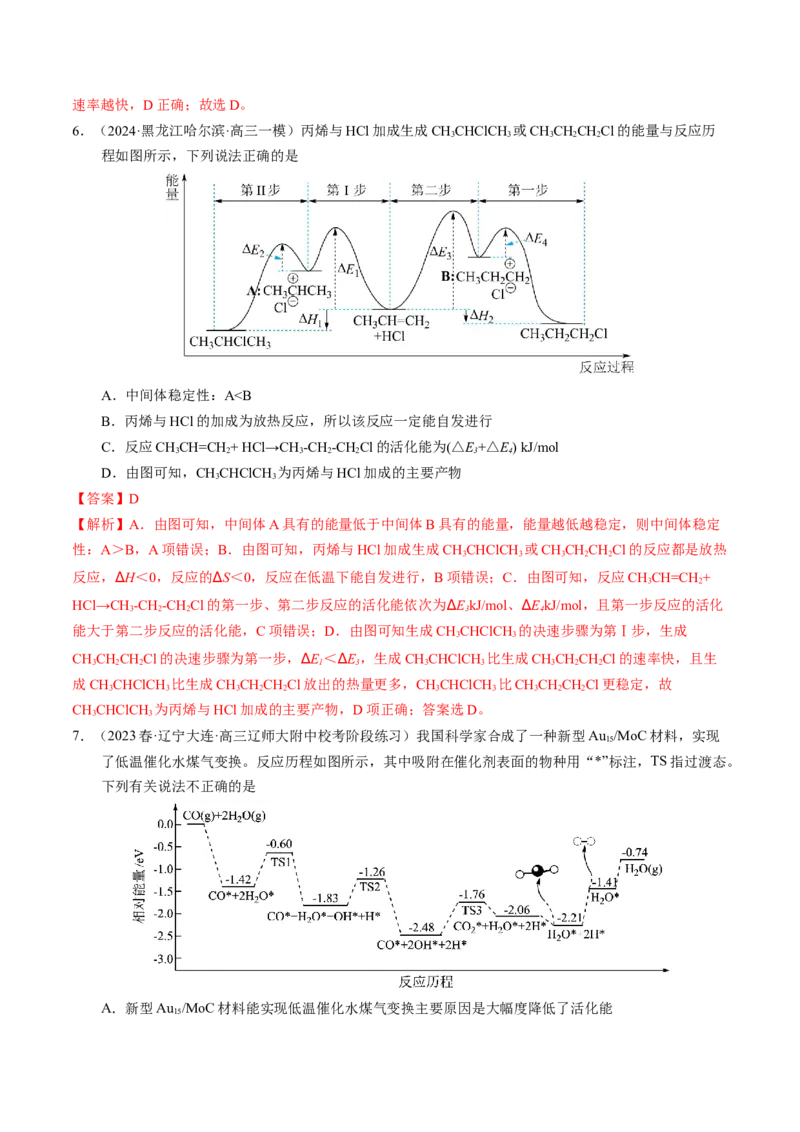
6.(2024·黑龙江哈尔滨·高三一模)丙烯与HCl加成生成CHCHClCH 或CHCHCHCl的能量与反应历
3 3 3 2 2
程如图所示,下列说法正确的是
A.中间体稳定性:AⅠ
D.对于Ⅰ,平衡后向容器中再充入0.2mol CO和0.2mol ,平衡正向移动
【答案】D
【解析】A.两次实验起始投入量相同,该反应为放热反应,温度T 达到平衡时,二氧化碳的量少,降温
2
平衡正向移动,故 ,A正确;B.Ⅰ中反应达到平衡时,CO 的物质的量为0.1mol,则参加反应的
2
CO的物质的量为0.1mol起始投入量为0.2mol,则其转化率为50%,B正确;C. ,温度越高,反应
速率越快,达到平衡所需要的的时间越短,C正确;D.恒容1L的容器中,对于反应I平衡时NO、CO、
N、CO 的物质的量分别为0.1mol、0.1mol、0.05mol、0.1mol,平衡常数K= ,平衡后向容器
2 2
中再充入0.2mol CO和0.2mol ,此时浓度商Q= ,K=Q,平衡不移动,D错误;故选
c c
D。
9.(2023·辽宁·校联考二模)某温度下,在2L恒容密闭容器中4molNH COONH(s),发生如下反应
2 4
,在0-1min内,CO 的生成速率为0.4mol•L-1•min-1,0-2min
2
内,CO 的生成速率为0.3mol•L-1•min-1,0-3min内,CO 的生成速率为0.2mol•L-1•min-1,下列说法错误
2 2
的是
A.当混合气体的平均摩尔质量不变时,标志此反应达到了平衡状态
B.0-1min内,NH COONH(s)的反应速率为62.4g/min
2 4
C.30秒时,CO 的浓度大于0.2mol/L
2
D.2min时,再加入2molNH ,此时反应的V >V
3 逆 正
【答案】A
【解析】A.此反应开始时只加入了 ,生成的 和 始终是2∶1,所以当混合气体的平均摩尔质量不变时,不可以标志此反应达到了平衡状态,A错误;通过三段式计算
,
1min内消耗 0.8mol,质量为62.4g,故反应速率为62.4g/min,B正确;C.由于反应速率
越来越慢,故30秒时, 的浓度大于0.2mol/L,C正确;D.由于反应2min已经达到平衡,当再加入
2mo 时,平衡逆移,故 ,D正确;故选A。
10.(2023·辽宁·校联考模拟预测)在600K下,按初始投料比 分别为1:1、1:2、1:3投
料,发生反应为 。测得不同压强下,CO平衡转化率如图所示。
下列叙述正确的是
A.曲线X代表起始投料比为1:1
B. ,该反应达到平衡状态
C.若其他条件不变,升高温度会使对应的曲线上移
D.m点对应的 的平衡转化率为60%
【答案】D
【解析】A.相同温度下,氢气投料越多,平衡向右移动,CO的平衡转化率越大,故曲线X代表1 : 3投
料,A项错误;B.该反应达到平衡状态时,v (H )=2v (CHOH),B项错误;C.生成甲醇是放热反应,
正 2 逆 3
其他条件不变,升高温度,CO的平衡转化率降低,平衡曲线均下移,C项错误;D.曲线Y代表1 : 2投
料,即起始按化学计量数投料,则CO、H 的平衡转化率相等,D项正确;故选D。
2
11.(2023·辽宁·校联考三模)天然金刚石存在稌少,以石墨为原料制备人造金刚石成为当前研究热点。下图是碳单质在不同温度、压强下存在形式的平衡图像,其中M区为金刚石的工业催化合成区,下列
有关说法错误的是
A.稳定性:金刚石<石墨
B.密度:金刚石>石墨
C.在M区实现金刚石的合成,高温环境有利于提高石墨的平衡转化率
D.上图Q区与R区中,表示气态碳单质 存在的区域应出现在R区
【答案】C
【解析】A.金刚石中碳碳单键的键长大于石墨中碳碳双键的键长,晶体中的共价键弱于石墨,所以稳定
性弱于石墨,故A正确;B.由图可知,在温度相同条件下,石墨变成金刚石需加压,说明石墨层与层之
间距离较大,则金刚石的密度大于石墨,故B正确;C.由图可知,在M区实现金刚石的合成时,低温环
境有利于提高石墨的平衡转化率,故C错误;D.相同温度下,压强越小,越利于气态碳存在,则图中表
示气态碳单质存在的区域应出现在R区,故D正确;故选C。
12.(2023·辽宁大连·大连二十四中校考模拟预测)实验室在1L的密闭容器中进行模拟合成实验,将
和 通入容器中,在催化剂的作用下发生:
反应I: (主反应);
反应II:
500℃时,将容器的体积压缩到原来的一半,在其他条件不变的情况下,平衡体系中变化正确的是
A. 减小
B.反应I正反应速率加快,逆反应速率减慢
C. 的物质的量增加
D.重新平衡时 增大
【答案】C
【解析】A.压缩容器体积,体积减小 增大,故A错误;B.压缩容器体积,反应物、生成物的浓度
均增大,则正逆反应速率均加快,故B错误;C.压缩体积增大压强,反应I平衡正向移动,则 的
物质的量增加,故C正确;D.将容器的体积压缩到原来的一半,体系内压强增大,反应I平衡正向移动,和 的物质的量均增加, 的物质的量增加,使得反应II平衡逆向移动,造成 的物质的
量增加程度小于 增加程度,故重新平衡时 减小,故D错误;故选:C。
13.(2023·辽宁沈阳·东北育才学校校考模拟预测)在催化剂作用下,向容积为1L的容器中加入1molX和
3molY,发生反应:X(g)+2Y(s) 2Z(s),平衡时和反应10min时X的转化率α(X)随温度的变化分
别如曲线I、Ⅱ所示。下列说法正确的是
A.使用更高效的催化剂,可以使b点移动到d点
B.保持温度和体积不变,向d点体系中再充入1molX,再次达平衡时c(X)>0.4mol/L
C.0-10min的平均反应速率:v(a)<v(c)
D.bc段变化可能是由于升高温度平衡逆向移动
【答案】A
【解析】A.由图可知,曲线I表示平衡转化率a(X)随温度变化曲线,Ⅱ表示10 min时转化率a(X)随温度
变化曲线,则b点反应未达到平衡状态,加入高效催化剂可加快反应速率,缩短平衡时间,即使用更高效
的催化剂,可以使b点移动到d点,A正确;B.由图可知,d点体系中c(X)=1mol/L×(1-60%)=0.4mol/L,
平衡常数K= , K只与温度有关,与物质的浓度变化无关,所以向d点体系中再充入
1molX,再次达平衡时K不变,c(X)=0.4mol/L,B错误;C.由图可知,10 min时a、c点X的转化率a(X)
相等,则0-10min的平均反应速率:v(a)=v(c),C错误;D.由图可知,bc段反应均未达到平衡状态,不存
在平衡移动,bc段变化是由于温度过高,催化剂活性降低,反应速率减慢,X的转化率a (X)减小,D错误;
故选A。
14.(2023·辽宁沈阳·辽宁实验中学校考模拟预测) 可以和 发生反应:
。一定温度下,向某恒容密闭容器中加入足量铁粉并充入一定量的
气体,反应过程中 气体和 气体的浓度与时间的关系如图所示。下列说法正确的是
A. 时该化学反应达到平衡状态B.平衡后向容器内充入 ,重新达到平衡时 增大
C.4 min时, 的转化率约为71.4%
D.4 min内, 的平均反应速率
【答案】C
【解析】A.由图可知,tmin时c(CO)=c(CO),相同条件下tmin后c(CO)仍在减小,c(CO)仍在增大,则
1 2 1 2
tmin时该化学反应没有达到平衡状态,故A错误;B.该反应的平衡常数K= ,只与温度有关,温
1
度不变则K不变,所以重新达到平衡时 不变,故B错误;C.由图可知,4min时,CO 的转化率
2
为 ×100%≈71.4%,故C正确;D.由图可知,4min内CO的平均反应速率v(CO)=
=0.125mol⋅L-1⋅min-1,故D错误;故选:C。
15.(2023·辽宁阜新·校联考模拟预测)一定条件下热解制取 :
。已知其他条件不变时,温度对 的平衡转化率和催化
剂催化效率的影响如图所示。下列说法一定正确的是
A.平衡常数:
B.达到平衡所需时间:
C.总能量:
D.单位时间的转化率。:
【答案】C
【解析】A.由图可知,升高温度, 的平衡转化率增大,说明反应
吸热,温度越高,平衡常数越大,温度:Z>Y,平衡常数:
,故A错误;B.温度越高,催化效率越强,反应速率越快,则Y点的反应速率大于X点的
反应速率,则达到平衡所需时间: ,故B错误;C.由图可知,升高温度, 的平衡转化率增大,说明反应 吸热,总能量: ,故C正确;
D.Z点和Y点温度差别不大,但Z点的催化效率远低于Y点,说明Y的反应速率大于Z点的反应速率,
则单位时间的转化率: ,故D错误;故选C。