文档内容
7。
c.若pH之和小于14,则混合后溶液显酸性,pH<7。
②一强一弱混合
pH之和等于14时,一元强酸溶液和一元弱碱溶液等体积混合呈碱性;一元强碱溶液和一元弱
酸溶液等体积混合呈酸性。
易错题【02】图解量器错误读数产生的误差
(1)俯视和仰视(如图b和图c)
①如图b,当用量筒测量液体的体积时,由于俯视视线向下倾斜,寻找切点的位置在凹液
面的上侧,读数高于正确的刻度线位置,即读数偏大。(量筒刻度从下到上逐渐增大)
②如图c,当用滴定管测量液体的体积时,由于仰视视线向上倾斜,寻找切点的位置在液
面的下侧,因滴定管刻度顺序与量筒不同,仰视读数偏大。(滴定管刻度从下到上逐渐减
小)(2)酸碱中和滴定实验中,两次视线呈三角形,读的体积小于实际体积(如图d);两次
视线呈梯形,读的体积小于实际体积(如图e)。
易错题【03】突破酸碱中和滴定曲线中的粒子浓度关系
(1)抓反应“一半”点,判断是什么溶质的等量混合;
(2)抓“恰好”反应点,生成的溶质是什么?判断溶液的酸碱性。
(3)抓溶液的“中性”点,生成什么溶质,哪种物质过量或不足。
(4)抓反应的“过量”点,溶液中的溶质是什么?判断哪种物质过量。
易错题【04】滴定方式及应用:
滴定方式 实例
许多还原性物质Fe2+、NO- 、HO、CO2−等。如5HO+2MnO- +6H+
直接滴定法 2 2 2 2 4 2 2 4
=5O ↑+2Mn2++8HO
2 2
氧化性物质可用返滴定法。例如,测MnO 含量时,可在HSO 溶液中加入过量
2 2 4
的NaC O 标准溶液,待与MnO 作用完毕后,用KMnO 标准液滴定过量的C
2 2 4 2 4 2
O2−。
返滴定法 4
MnO
+CO2−+4H+=Mn2++2CO↑+2HO,2MnO- +5CO2−+16H+=2Mn2
2 2 4 2 2 4 2 4
++10CO↑+8HO
2 2
某些非氧化性物质,可以用间接滴定法进行测定。例如,测Ca2+含量时,先将
Ca2+沉淀为CaC O,再用稀硫酸将所得沉淀溶解,用KMnO 标准液滴定溶液中
2 4 4
间接滴定法 的HC O,间接求得Ca2+含量。CaC O+2H+=HC O+Ca2+,2MnO- +6H++
2 2 4 2 4 2 2 4 4
5HC O=2Mn2++10CO↑+8HO
2 2 4 2 2
典例分析
例题1、已知温度T时水的离子积常数为K ,该温度下,将浓度为a mol·L-1的一元酸HA
w
与b mol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是( )
A.a=b
B.混合溶液的pH=7
C.混合溶液中,c(H+)= mol·L-1
D.混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
【解析】溶液呈中性,说明c(H+)=c(OH-),而水的离子积K =c(H+)·c(OH-)=c2(H+),所
w以c(H+)= mol·L-1,C正确。A项中a=b,不知酸和碱的强弱,故不好判断溶液酸碱性;
B项中没有指明在25 ℃时,pH=7不能作为溶液呈中性的依据;D项为电荷守恒,不能判
定该溶液呈中性。
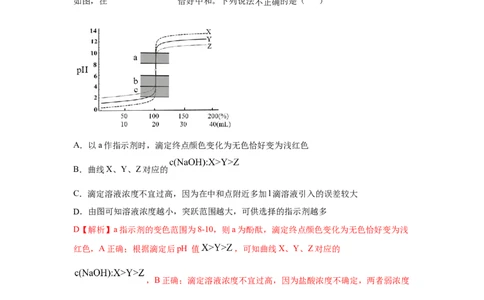
例题2、25℃时,分别用浓度为 、 和 的NaOH溶液滴定
浓度不同、体积均为20mL的3种HCl溶液,测得3个溶液的pH随 变化的曲线
如图,在 恰好中和。下列说法不正确的是( )
A.以a作指示剂时,滴定终点颜色变化为无色恰好变为浅红色
B.曲线X、Y、Z对应的
C.滴定溶液浓度不宜过高,因为在中和点附近多加l滴溶液引入的误差较大
D.由图可知溶液浓度越小,突跃范围越大,可供选择的指示剂越多
D【解析】a指示剂的变色范围为8-10,则a为酚酞,滴定终点颜色变化为无色恰好变为浅
红色,A正确;根据滴定后pH 值 ,可知曲线X、Y、Z对应的
,B正确;滴定溶液浓度不宜过高,因为盐酸浓度不确定,两者弱浓度
差较大,中和点附近多加l滴溶液引入的误差较大,C正确;由图可知溶液浓度越小,突跃
范围越大,可供选择的指示剂越少,D错误。
例题3、(1)成品中S2-的含量可以用“碘量法”测得。称取m g样品,置于碘量瓶中,移取
25.00 mL 0.100 0 mol·L-1的I-KI溶液于其中,并加入乙酸溶液,密闭,置暗处反应5 min,有单质
2
硫析出。以淀粉为指示剂,过量的I 用0.1000 mol·L-1 Na SO 溶液滴定,反应式为I+2S
2 2 2 3 2 2O2−
3=2I-+S 。测定时消耗NaSO 溶液体积V mL。终点颜色变化为________,样品中S2-的
4O2− 2 2 3
6
含量为______________________(写出表达式)。
(2)环己烯含量的测定:在一定条件下,向a g环己烯样品中加入定量制得的b mol Br ,与环己
2
烯充分反应后,剩余的Br 与足量KI作用生成I,用c mol·L-1的NaSO 标准溶液滴定,终点时
2 2 2 2 3
消耗NaSO 标准溶液V mL(以上数据均已扣除干扰因素)。测定过程中,发生的反应如下:
2 2 3
①Br +
2
②Br +2KI=I+2KBr
2 2
③I+2NaSO=2NaI+NaSO
2 2 2 3 2 4 6
滴定所用指示剂为________。样品中环己烯的质量分数为________(用字母表示)。
下列情况会导致测定结果偏低的是________(填序号)。
a.样品中含有苯酚杂质
b.在测定过程中部分环己烯挥发
c.Na SO 标准溶液部分被氧化
2 2 3
【解析】(1)滴定终点时,I 被消耗完,溶液颜色由浅蓝色变为无色。由反应式为I+2S
2 2 2O2−
3
O2−
=2I-+S 6 可知,与NaSO 溶液反应的n(I)= ×0.100 0× ,则与S2-反应的n(I)=
4 2 2 3 1 2 2 2
×0.100 0-n (I)= (mol),由电子守恒可知S2-~I,则样品中S2-的
1 2 2
含量为 ×100%。
(2)有碘单质滴定时用淀粉作指示剂。根据关系式计算与环己烯反应后剩余n(Br):
2
Br ~ I ~ 2NaSO
2 2 2 2 3
1 mol 2 mol反应消耗n(Na SO)=cV×10-3mol,则参加反应的n(Br)= cV×10-3 mol,与己烯反应消耗的
2 2 3 2
n(Br)=b- cV×10-3 mol,样品中环己烯的质量分数为:
2
样品中含有苯酚,苯酚会与溴反应,测定结果偏高;在测定过程中环己烯挥发,导致结果偏
低;Na SO 溶液被氧化时,消耗的体积增大,所测定环己烯的质量分数偏低。
2 2 3
【答案】(1)浅蓝色至无色 ×100% (2)淀粉溶液
b、c
1.(2022·湖南·高考真题)化学实验操作是进行科学实验的基础。下列操作符合规范的是
A.碱式滴定管排气泡 B.溶液加热 C.试剂存放 D.溶液滴加
2.(2022·山东·高考真题)实验室用基准 配制标准溶液并标定盐酸浓度,应选甲
基橙为指示剂,并以盐酸滴定 标准溶液。下列说法错误的是
A.可用量筒量取 标准溶液置于锥形瓶中
B.应选用配带塑料塞的容量瓶配制 标准溶液
C.应选用烧杯而非称量纸称量 固体
D.达到滴定终点时溶液显橙色
3.(2021·天津·高考真题)常温下,下列各组离子在给定溶液中能大量共存的是A.pH=1的溶液:Fe2+、Mg2+、 、
B.pH=12的溶液:K+、Na+、 、
C.pH=7的溶液:Na+、Cu2+、S2-、Cl-
D.pH=7的溶液:Al3+、K+、Cl-、
4.(2022·湖北·襄阳五中模拟预测)常温下,用0.1mol·L-1氨水滴定10mL浓度均为
0.1mol·L-1的HCl和CHCOOH的混合液,已知醋酸的电离常数为K =1.8×10-5,下列说法错
3 a
误的是
A.在氨水滴定前,混合溶液c(Cl-)>c(CHCOOH)
3
B.在氨水滴定前,混合溶液c(CHCOO-)≈Ka
3
C.当滴入氨水10mL时,c( )+c(NH ·H O)=c(CHCOOH)+c(CHCOO-)
3 2 3 3
D.当溶液呈中性时,氨水滴入量等于20mL,且c( )<c(Cl-)
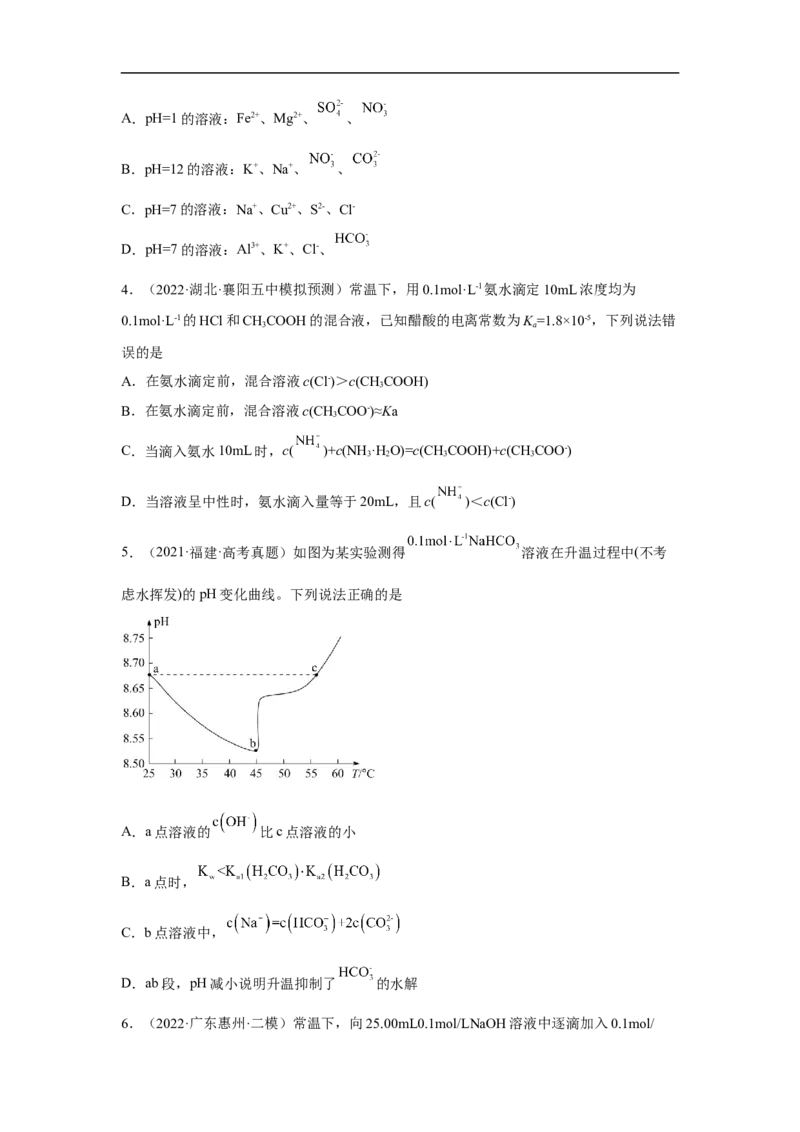
5.(2021·福建·高考真题)如图为某实验测得 溶液在升温过程中(不考
虑水挥发)的pH变化曲线。下列说法正确的是
A.a点溶液的 比c点溶液的小
B.a点时,
C.b点溶液中,
D.ab段,pH减小说明升温抑制了 的水解
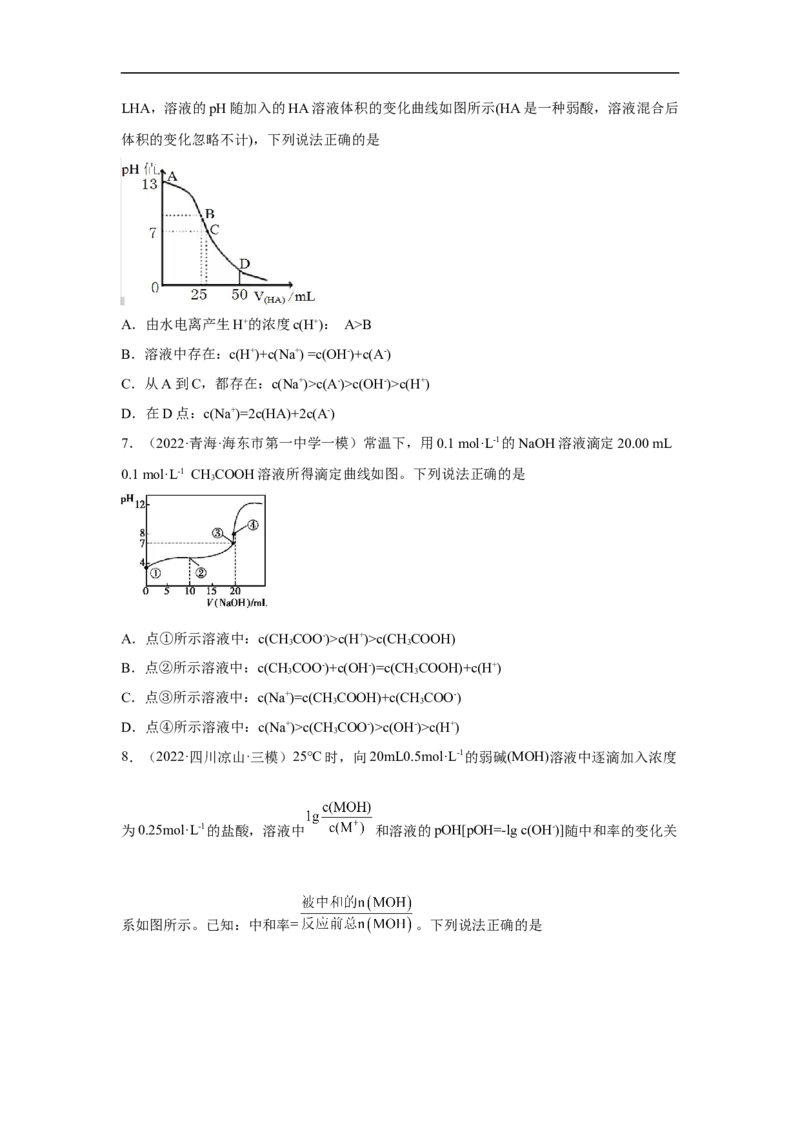
6.(2022·广东惠州·二模)常温下,向25.00mL0.1mol/LNaOH溶液中逐滴加入0.1mol/LHA,溶液的pH随加入的HA溶液体积的变化曲线如图所示(HA是一种弱酸,溶液混合后
体积的变化忽略不计),下列说法正确的是
A.由水电离产生H+的浓度c(H+): A>B
B.溶液中存在:c(H+)+c(Na+) =c(OH-)+c(A-)
C.从A到C,都存在:c(Na+)>c(A-)>c(OH-)>c(H+)
D.在D点:c(Na+)=2c(HA)+2c(A-)
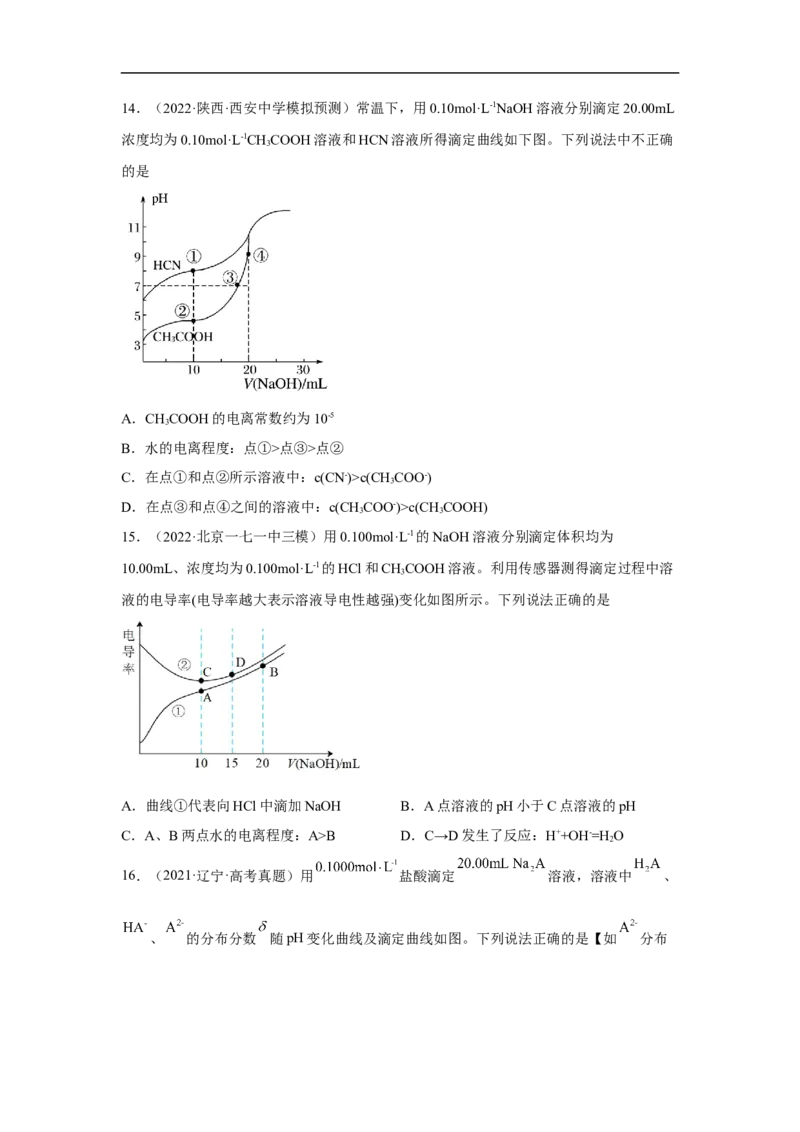
7.(2022·青海·海东市第一中学一模)常温下,用0.1 mol·L-1的NaOH溶液滴定20.00 mL
0.1 mol·L-1 CHCOOH溶液所得滴定曲线如图。下列说法正确的是
3
A.点①所示溶液中:c(CHCOO-)>c(H+)>c(CH COOH)
3 3
B.点②所示溶液中:c(CHCOO-)+c(OH-)=c(CH COOH)+c(H+)
3 3
C.点③所示溶液中:c(Na+)=c(CH COOH)+c(CH COO-)
3 3
D.点④所示溶液中:c(Na+)>c(CH COO-)>c(OH-)>c(H+)
3
8.(2022·四川凉山·三模)25°C时,向20mL0.5mol·L-1的弱碱(MOH)溶液中逐滴加入浓度
为0.25mol·L-1的盐酸,溶液中 和溶液的pOH[pOH=-lg c(OH-)]随中和率的变化关
系如图所示。已知:中和率= 。下列说法正确的是A.a点时, <1
B.b点时,c(M+)>c(Cl-)>c(H+)>c(OH-)
C.c点时,2c(M+)+c(MOH)+c(H+)<3c(Cl-)+c(OH-)
D.d点对应的溶液中升高温度pOH值一定增大
9.(2022·江西·三模)已知常温下二元弱酸HA溶液中,HA、HA-、A2-的分布分数(δ)随
2 2
pH变化如图所示[如A2-分布分数:δ(A2-)= ],下列说法错误的是
A.曲线x代表HA,曲线z代表A2-
2
B.pH从3升高至4, 的值一直减小
C.n点对应的溶液中水电离出的c(H+)=10-12.7mol·L-1
D.将浓度均为0.05mol·L-1的NaHA溶液与NaA溶液等体积混合后,所得溶液pH>4.3
2
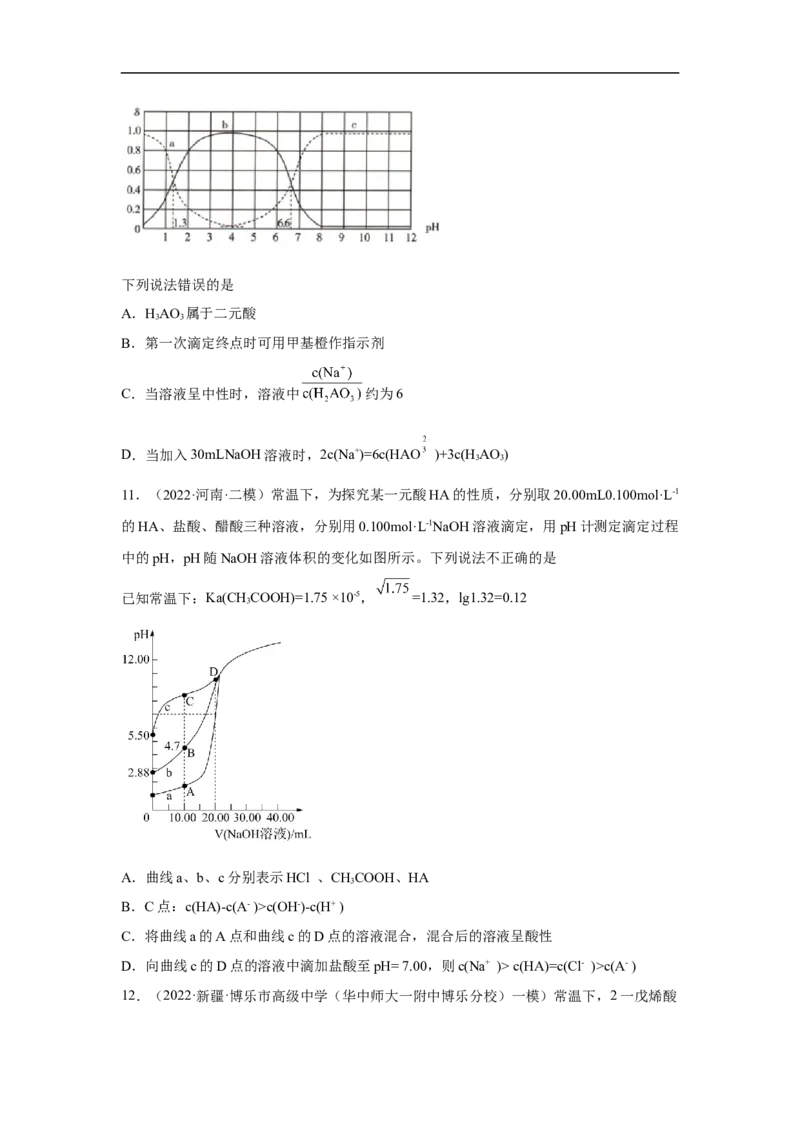
10.(2022·河南·模拟预测)25℃时,用0.1mol·L-1NaOH溶液滴定20mL0.1mol·L-1HAO 溶
3 3
液,溶液中所有含A微粒的分布分数δ(平衡时某含A微粒的浓度占各含A微粒浓度之和的
分数)与pH的关系如图所示(已知100.2=1.58):下列说法错误的是
A.HAO 属于二元酸
3 3
B.第一次滴定终点时可用甲基橙作指示剂
C.当溶液呈中性时,溶液中 约为6
D.当加入30mLNaOH溶液时,2c(Na+)=6c(HAO )+3c(H AO )
3 3
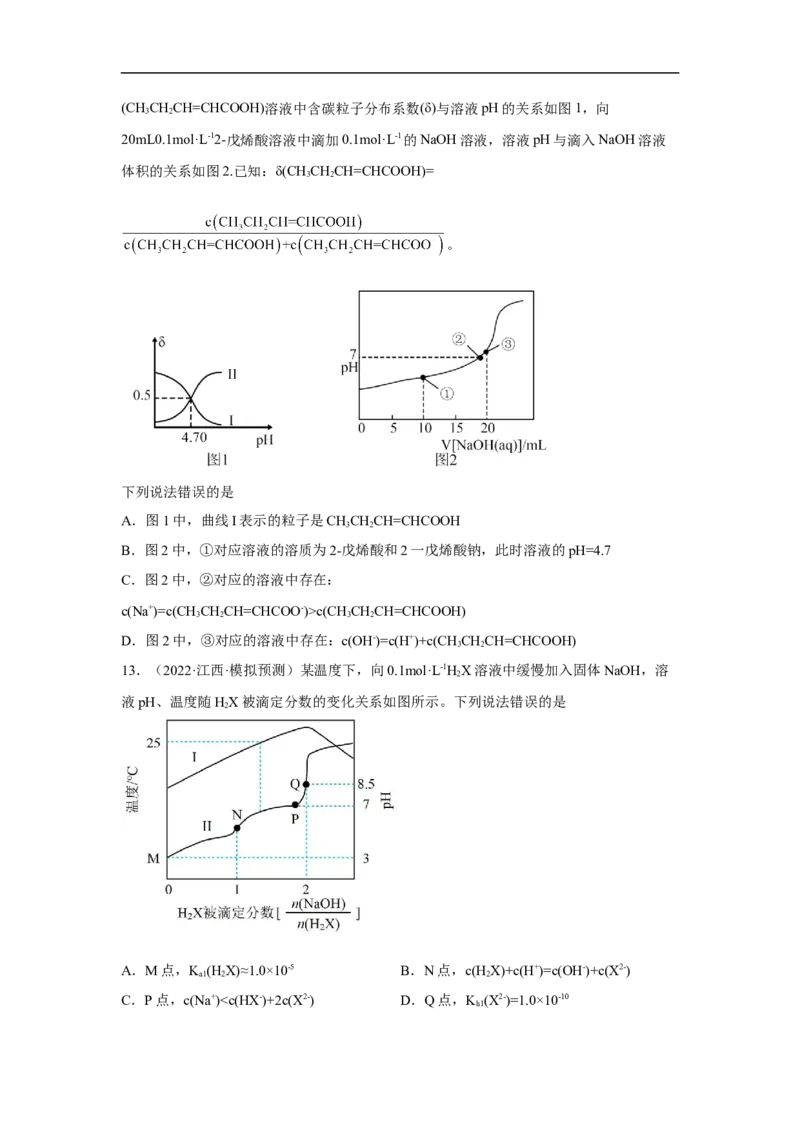
11.(2022·河南·二模)常温下,为探究某一元酸HA的性质,分别取20.00mL0.100mol·L-1
的HA、盐酸、醋酸三种溶液,分别用0.100mol·L-1NaOH溶液滴定,用pH计测定滴定过程
中的pH,pH随NaOH溶液体积的变化如图所示。下列说法不正确的是
已知常温下:Ka(CH COOH)=1.75 ×10-5, =1.32,lg1.32=0.12
3
A.曲线a、b、c分别表示HCl 、CHCOOH、HA
3
B.C点:c(HA)-c(A- )>c(OH-)-c(H+ )
C.将曲线a的A点和曲线c的D点的溶液混合,混合后的溶液呈酸性
D.向曲线c的D点的溶液中滴加盐酸至pH= 7.00,则c(Na+ )> c(HA)=c(Cl- )>c(A- )
12.(2022·新疆·博乐市高级中学(华中师大一附中博乐分校)一模)常温下,2一戊烯酸(CHCHCH=CHCOOH)溶液中含碳粒子分布系数(δ)与溶液pH的关系如图1,向
3 2
20mL0.1mol·L-12-戊烯酸溶液中滴加0.1mol·L-1的NaOH溶液,溶液pH与滴入NaOH溶液
体积的关系如图2.已知:δ(CH CHCH=CHCOOH)=
3 2
。
下列说法错误的是
A.图1中,曲线I表示的粒子是CHCHCH=CHCOOH
3 2
B.图2中,①对应溶液的溶质为2-戊烯酸和2一戊烯酸钠,此时溶液的pH=4.7
C.图2中,②对应的溶液中存在:
c(Na+)=c(CH CHCH=CHCOO-)>c(CH CHCH=CHCOOH)
3 2 3 2
D.图2中,③对应的溶液中存在:c(OH-)=c(H+)+c(CH CHCH=CHCOOH)
3 2
13.(2022·江西·模拟预测)某温度下,向0.1mol·L-1HX溶液中缓慢加入固体NaOH,溶
2
液pH、温度随HX被滴定分数的变化关系如图所示。下列说法错误的是
2
A.M点,K (H X)≈1.0×10-5 B.N点,c(HX)+c(H+)=c(OH-)+c(X2-)
a1 2 2
C.P点,c(Na+)