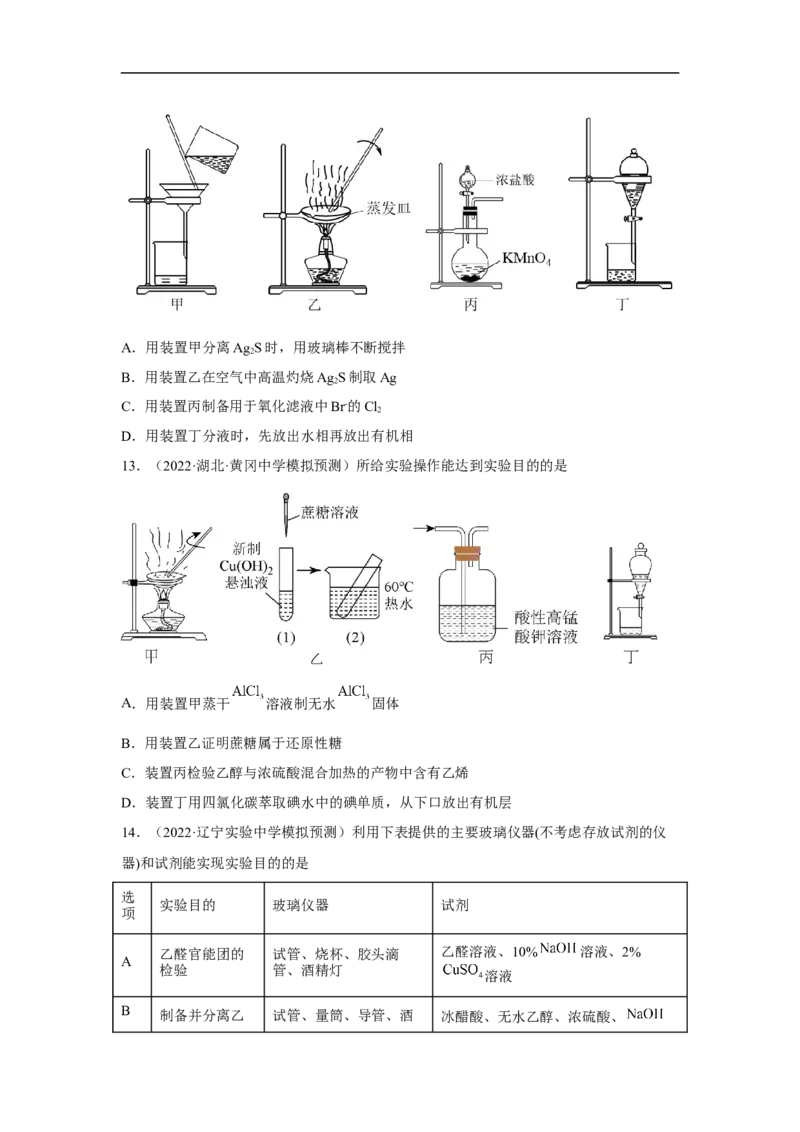
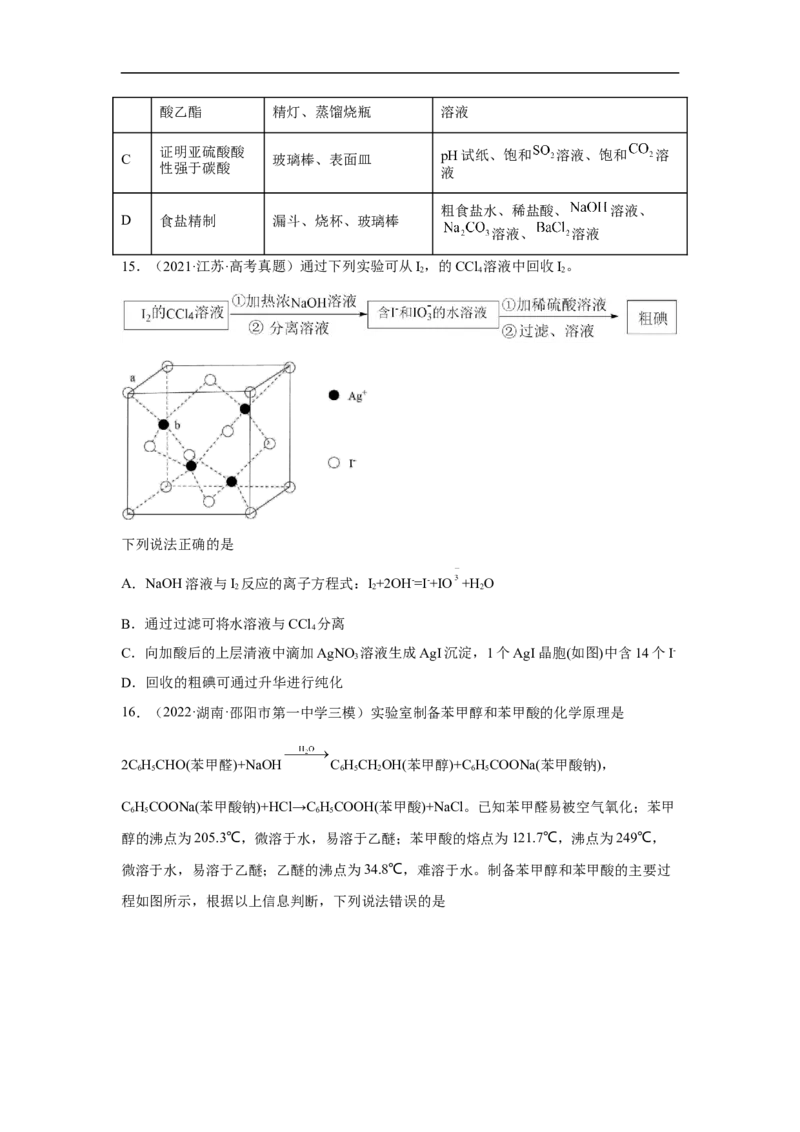
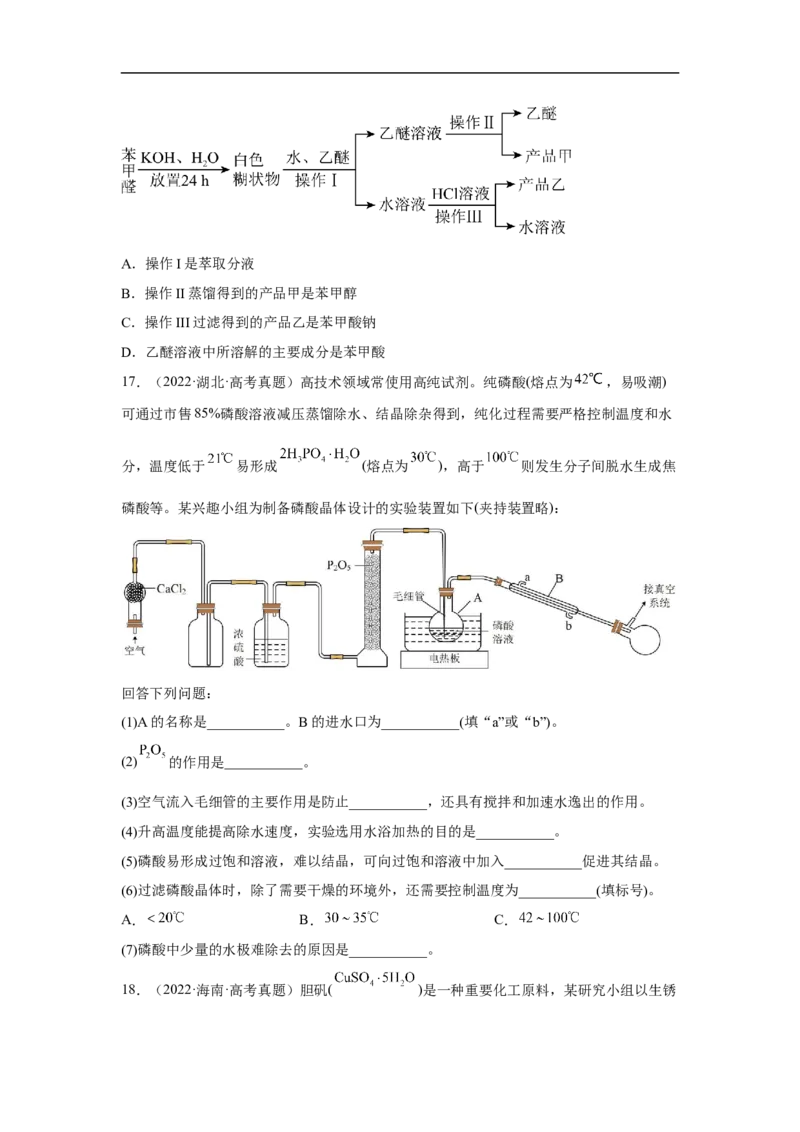
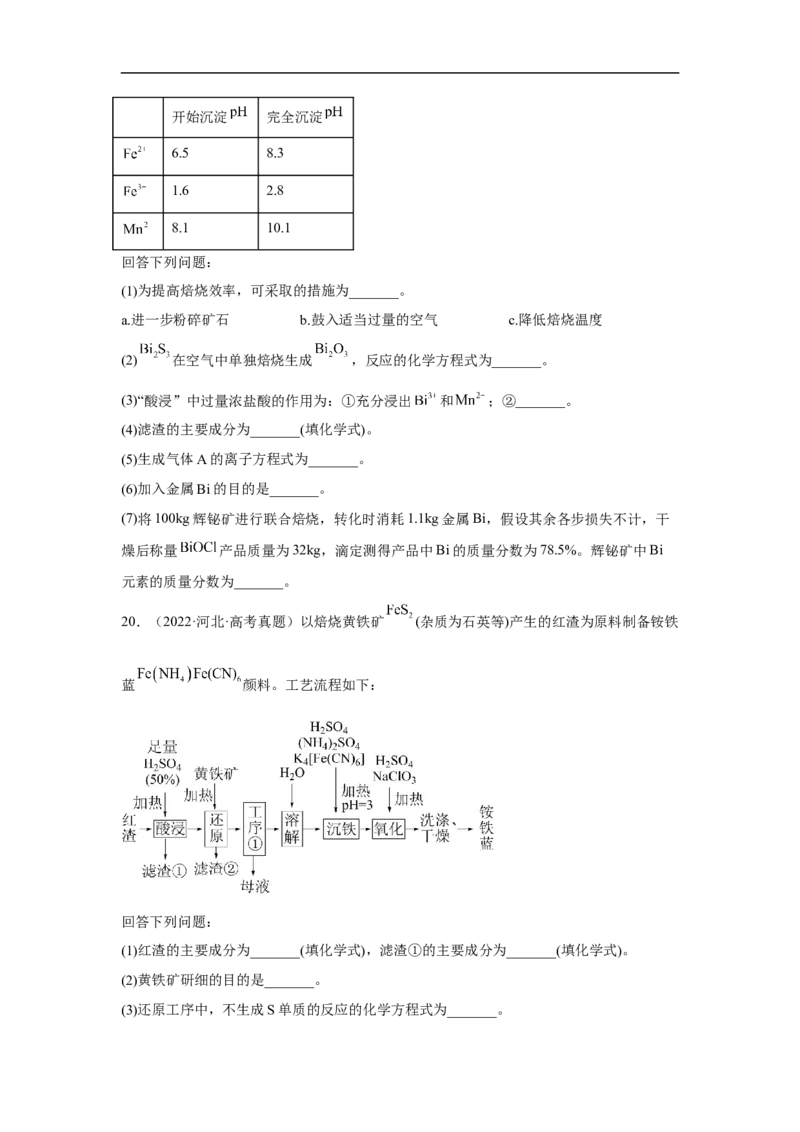
文档内容
易错点 32 物质的分离、提纯与检验
易错题【01】物质分离、提纯的区别
(1)物质的分离。
将混合物中的各组分分离开来,获得几种纯净物的过程。
(2)物质的提纯及其操作要求。
①将混合物中的杂质除去而得到纯净物的过程,又叫混合物的净化或除杂。
②提纯的“四个原则”及“四个必须”
“四个原则”:一是不增加新的杂质;二是不减少被提纯物质;三是被提纯物质与杂质易分离;
四是被提纯物质易复原。
“四个必须”:一是除杂试剂必须过量;二是过量试剂必须除尽;三是除杂途径必须最佳;四是
除去多种杂质时必须考虑加入试剂的先后顺序。
易错题【02】结晶与重结晶
(1)结晶指晶体从溶液中析出的过程。如果溶质的溶解度随温度变化较小,可采用蒸发溶剂
的方法使溶质结晶析出。如果溶质的溶解度随温度变化较大,可采用降温的方法使溶质结
晶析出。控制条件,如缓慢降温、采用低浓度溶液以减小结晶速率等,可得到较完整的大
晶体。
(2)重结晶指析出的晶体经过溶解后再次从溶液中结晶析出的过程,是一种利用物质的溶解
性不同而进行提纯、分离的方法。为了制得更纯的晶体,有时可进行多次重结晶。
易错题【03】分离提纯题的答题步骤
(1)确定被提纯物质与除杂对象:对比两者物理性质、化学性质的差异,利用差异性(溶
解度差异、密度差异、熔沸点差异、与某些物质反应的差异性等),选择合适的分离原理或
除杂试剂;除杂试剂除去杂质的同时,不消耗被提纯物质,不引入新的杂质。
(2)选择合适的分离或除杂装置:根据分离原理选择合适的分离装置(过滤、分液、蒸馏
等);根据除杂试剂的状态及反应条件,选择合适的装置,液体试剂一般选洗气瓶,固体试
剂一般用干燥管或U形管。
(3)综合分析筛选答案:综合分析物质分离是否完全,被提纯物质中的杂质是否被除去。
易错题【04】物质除杂方法的选择
原物质 所含杂质 除杂质试剂 主要操作方法
N O 灼热的铜网 吸收法
2 2
CO CO NaOH 溶液 洗气
2
CO CO 灼热 CuO 转化法
2
CO 2 H 2 S CuSO 溶液 洗气
4CO HCl 饱和 NaHCO 溶液 洗气
2 3
SO HCl 饱和 NaHSO 溶液 洗气
2 3
Cl HCl 饱和食盐水 洗气
2
炭粉 MnO 浓盐酸(加热) 过滤
2
Fe O Al O 过量NaOH 溶液 过滤
2 3 2 3
Al O SiO ①盐酸;②氨水 过滤、灼烧
2 3 2
NaHCO 溶液 NaCO CO 转化法
3 2 3 2
FeCl 溶液 FeCl Cl 转化法
3 2 2
FeCl 溶液 CuCl Fe、Cl 过滤
3 2 2
FeCl 溶液 FeCl 过滤
2 3
乙烷 乙烯 溴水 洗气
乙醇 水 新制CaO 蒸馏
乙烯 SO NaOH溶液 洗气
2
溴苯 溴 NaOH 溶液 分液
乙酸乙酯 乙酸 饱和 N aCO 溶液 分液
2 3
易错题【05】物质检验的干扰与排除
(1)离子检验中的常见干扰因素以及排除措施。
待检
干扰离子 排干扰措施
离子
SO2− 加过量的Ba(NO ) 溶液
4 3 2
Cl- CO2−
3
加稀硝酸酸化
OH-
CO2−
3
SO2− SO2− 加盐酸酸化
4 3
Ag+
SO2− CO2−
加盐酸后将产生的气体通入品红溶液中
3 3
CO2− SO2−
加硝酸后将产生的无色无味气体通入澄清石灰水中
3 3
(2)气体检验中干扰因素的排除。
气体检验中干扰因素的排除方法一般是先检验出一种可能会产生干扰的气体,并除去该气体,
而且要确认该气体已经除尽,再检验其余气体。如在SO 存在的条件下检验CO,可设计如下
2 2
检验思路:品红溶液检验SO →酸性高锰酸钾溶液除去SO →品红溶液检验SO 是否除尽→
2 2 2
澄清石灰水检验CO。与此类似的还有检验实验室制取的乙烯中含有SO 等。
2 2
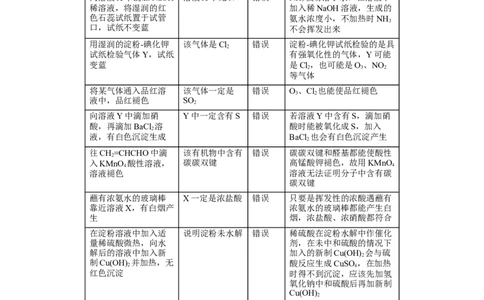
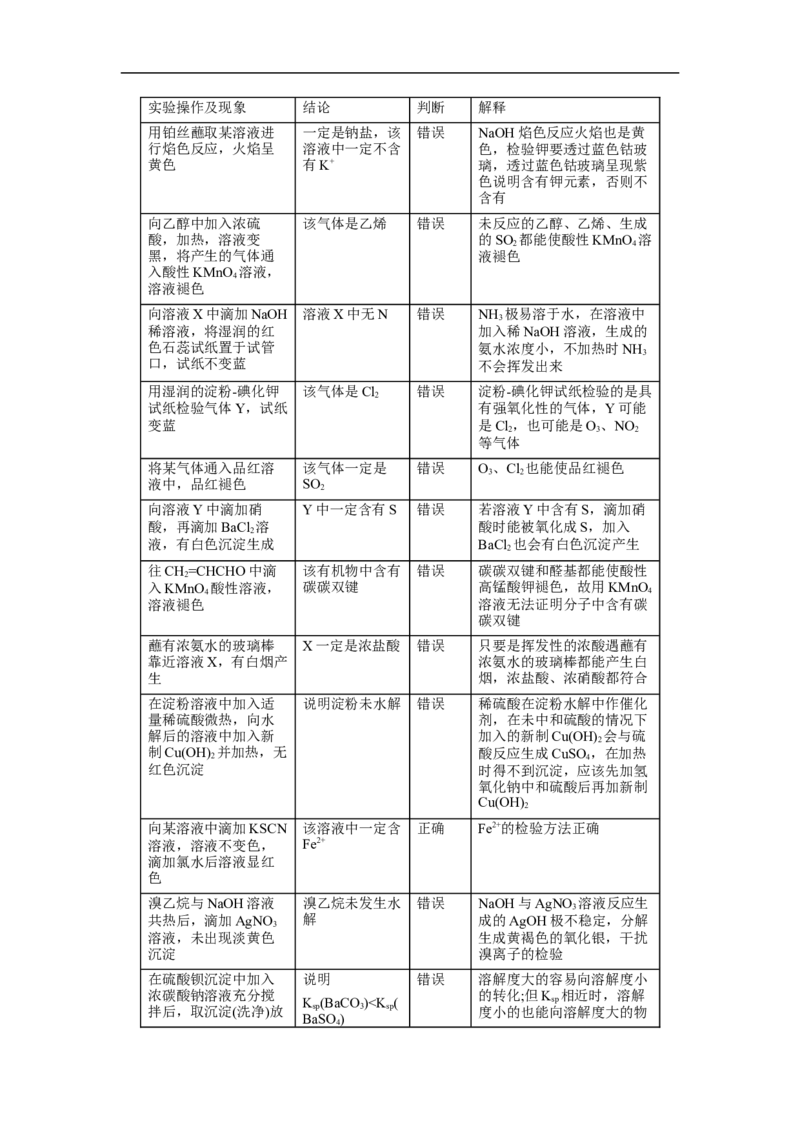
易错题【06】实验操作、现象与结论实验操作及现象 结论 判断 解释
用铂丝蘸取某溶液进 一定是钠盐,该 错误 NaOH焰色反应火焰也是黄
行焰色反应,火焰呈 溶液中一定不含 色,检验钾要透过蓝色钴玻
黄色 有K+ 璃,透过蓝色钴玻璃呈现紫
色说明含有钾元素,否则不
含有
向乙醇中加入浓硫 该气体是乙烯 错误 未反应的乙醇、乙烯、生成
酸,加热,溶液变 的SO 都能使酸性KMnO 溶
2 4
黑,将产生的气体通 液褪色
入酸性KMnO 溶液,
4
溶液褪色
向溶液X中滴加NaOH 溶液X中无N 错误 NH 极易溶于水,在溶液中
3
稀溶液,将湿润的红 加入稀NaOH溶液,生成的
色石蕊试纸置于试管 氨水浓度小,不加热时NH
3
口,试纸不变蓝 不会挥发出来
用湿润的淀粉-碘化钾 该气体是Cl 错误 淀粉-碘化钾试纸检验的是具
2
试纸检验气体Y,试纸 有强氧化性的气体,Y可能
变蓝 是Cl,也可能是O、NO
2 3 2
等气体
将某气体通入品红溶 该气体一定是 错误 O、Cl 也能使品红褪色
3 2
液中,品红褪色 SO
2
向溶液Y中滴加硝 Y中一定含有S 错误 若溶液Y中含有S,滴加硝
酸,再滴加BaCl 溶 酸时能被氧化成S,加入
2
液,有白色沉淀生成 BaCl 也会有白色沉淀产生
2
往CH=CHCHO中滴 该有机物中含有 错误 碳碳双键和醛基都能使酸性
2
入KMnO 酸性溶液, 碳碳双键 高锰酸钾褪色,故用KMnO
4 4
溶液褪色 溶液无法证明分子中含有碳
碳双键
蘸有浓氨水的玻璃棒 X一定是浓盐酸 错误 只要是挥发性的浓酸遇蘸有
靠近溶液X,有白烟产 浓氨水的玻璃棒都能产生白
生 烟,浓盐酸、浓硝酸都符合
在淀粉溶液中加入适 说明淀粉未水解 错误 稀硫酸在淀粉水解中作催化
量稀硫酸微热,向水 剂,在未中和硫酸的情况下
解后的溶液中加入新 加入的新制Cu(OH) 会与硫
2
制Cu(OH) 并加热,无 酸反应生成CuSO ,在加热
2 4
红色沉淀 时得不到沉淀,应该先加氢
氧化钠中和硫酸后再加新制
Cu(OH)
2
向某溶液中滴加KSCN 该溶液中一定含 正确 Fe2+的检验方法正确
溶液,溶液不变色, Fe2+
滴加氯水后溶液显红
色
溴乙烷与NaOH溶液 溴乙烷未发生水 错误 NaOH与AgNO 溶液反应生
3
共热后,滴加AgNO 解 成的AgOH极不稳定,分解
3
溶液,未出现淡黄色 生成黄褐色的氧化银,干扰
沉淀 溴离子的检验
在硫酸钡沉淀中加入 说明 错误 溶解度大的容易向溶解度小
浓碳酸钠溶液充分搅 的转化;但K 相近时,溶解
K (BaCO)