文档内容
易错类型 05 化学计量
【易错点01】忽视物质的状态、所处状况
【易错点02】不了解物质的组成、结构特点
【易错点03】厘不清氧化还原反应中电子转移的数目
【易错点04】忽视化学反应中微粒数目的变化
【易错点05】不清楚溶液稀释或混合的规律
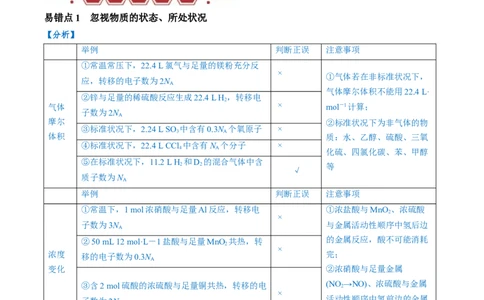
易错点1 忽视物质的状态、所处状况
【分析】
举例 判断正误 注意事项
①常温常压下,22.4 L氯气与足量的镁粉充分反
×
①气体若在非标准状况下,
应,转移的电子数为2N
A
气体摩尔体积不能用22.4 L·
②锌与足量的稀硫酸反应生成22.4 L H,转移电
2
气体 × mol-1计算;
子数为2N
A
摩尔 ②标准状况下为非气体的物
③标准状况下,2.24 L SO 中含有0.3N 个氧原子 ×
3 A
体积 质:水、乙醇、硫酸、三氧
④标准状况下,22.4 L CCl 中含有N 个分子 ×
4 A 化硫、四氯化碳、苯、甲醇
⑤在标准状况下,11.2 L H 和D 的混合气体中含
2 2 等
√
质子数为N
A
举例 判断正误 注意事项
①常温下,1 mol浓硝酸与足量Al反应,转移电 ①浓盐酸与MnO 、浓硫酸
2
×
子数为3N 与金属活动性顺序中氢后边
A
②50 mL 12 mol·L-1盐酸与足量MnO 共热,转 的金属反应,酸不可能消耗
2
×
浓度 移的电子数为0.3N 完;
A
变化 ②浓硝酸与足量金属
③含2 mol硫酸的浓硫酸与足量铜共热,转移的电 (NO 2 →NO)、浓硫酸与金属
×
子数为2N 活动性顺序中氢前边的金属
A
反应(SO →H)
2 2
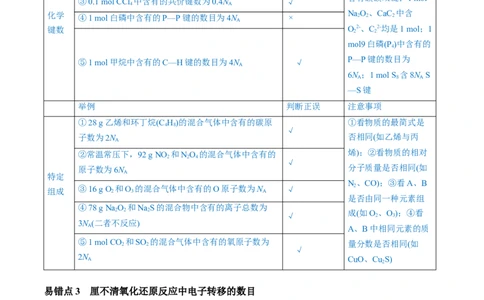
易错点2 不了解物质的组成、结构特点
【分析】
1.微粒组成结构分析中的微粒数目
举例 判断正误 注意事项
①18 g HO、DO组成的物质中含有的质子数为10NA ×
原子 2 2 应注意整体与部分的
资料整理【淘宝店铺:向阳百分百】②0.1 mol的11B中,含有0.6N 个中子 √
A
关系;是离子还是官
③1 mol OD-中含有的质子、中子数均为9N √
A
能团;是等质量还是
结构 ④1 mol的羟基与1 mol的氢氧根离子所含电子数均为
× 等物质的量;如DO
2
9N
A
与HO结构的差别
2
⑤1 mol F 和Ar所含质子数均为18N √
2 A
举例 判断正误 注意事项
①0.1 mol CaC 中含碳碳三键数为0.2N × 有机物如丙醇等应写
2 A
②1 mol苯中含有碳碳双键数为3N × 出结构式,苯环中不
A
含有碳碳双键;1 mol
③0.1 mol CCl 中含有的共价键数为0.4N √
4 A
化学 ④1 mol白磷中含有的P—P键的数目为4N × Na 2 O 2 、CaC 2 中含
A
键数 O2-、C 2-均是1 mol;1
2 2
mol9白磷(P )中含有的
4
⑤1 mol甲烷中含有的C—H键的数目为4N √
P—P键的数目为
A
6N ;1 mol S 含8N S
A 8 A
—S键
举例 判断正误 注意事项
①28 g乙烯和环丁烷(C H)的混合气体中含有的碳原 ①看物质的最简式是
4 8
√
子数为2N 否相同(如乙烯与丙
A
②常温常压下,92 g NO 和NO 的混合气体中含有的 烯);②看物质的相对
2 2 4
√
原子数为6N 分子质量是否相同(如
A
特定
N、CO);③看A、B
组成 ③16 g O 2 和O 3 的混合气体中含有的O原子数为N A √ 2
是否由同一种元素组
④78 g NaO 和NaS的混合物中含有的离子总数为
2 2 2
√
成(如O
2
、O
3
);④看
3N (二者不反应)
A A、B中相同元素的质
⑤1 mol CO 2 和SO 2 的混合气体中含有的氧原子数为 量分数是否相同(如
√
2N A CuO、Cu S)
2
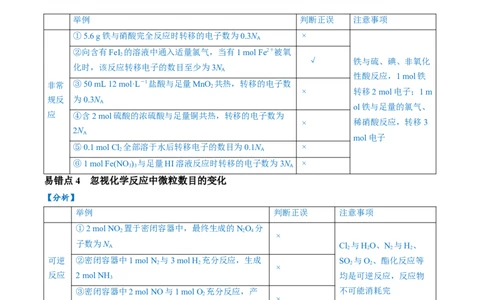
易错点3 厘不清氧化还原反应中电子转移的数目
【分析】
举例 判断正误 注意事项
常规 ①过氧化钠与水反应时,生成0.1 mol氧气转移的电子数为 要注意特殊物质,如
×
反应 0.4N 由过氧化钠、过氧化
A
②铁与硫的反应中,1 mol铁失去的电子数为3N × 氢制取1 mol氧气转
A
移2 mol电子
资料整理【淘宝店铺:向阳百分百】③3 mol铁在足量的氧气中燃烧,转移电子数为9N ×
A
④标准状况下,6.72 L NO 溶于足量的水中,转移的电子数
2
×
为0.3N
A
⑤1 mol铁在1 mol氯气中燃烧,转移的电子数为3N ×
A
⑥KIO +6HI===KI+3HO+3I 中,生成1 mol I 转移电子
3 2 2 2
×
的总数为2N
A
举例 判断正误 注意事项
①5.6 g铁与硝酸完全反应时转移的电子数为0.3N ×
A
②向含有FeI 的溶液中通入适量氯气,当有1 mol Fe2+被氧
2
√ 铁与硫、碘、非氧化
化时,该反应转移电子的数目至少为3N
A
性酸反应,1 mol铁
非常 ③50 mL 12 mol·L-1盐酸与足量MnO 共热,转移的电子数
2
× 转移2 mol电子;1 m
规反 为0.3N
A
ol铁与足量的氯气、
应 ④含2 mol硫酸的浓硫酸与足量铜共热,转移的电子数为
× 稀硝酸反应,转移3
2N
A
mol电子
⑤0.1 mol Cl 全部溶于水后转移电子的数目为0.1N ×
2 A
⑥1 mol Fe(NO ) 与足量HI溶液反应时转移的电子数为3N ×
3 3 A
易错点4 忽视化学反应中微粒数目的变化
【分析】
举例 判断正误 注意事项
①2 mol NO 置于密闭容器中,最终生成的NO 分
2 2 4
×
子数为N A Cl 2 与H 2 O、N 2 与H 2 、
可逆 ②密闭容器中1 mol N 与3 mol H 充分反应,生成 SO 与O、酯化反应等
2 2 2 2
×
反应 2 mol NH 均是可逆反应,反应物
3
③密闭容器中2 mol NO与1 mol O 充分反应,产 不可能消耗完
2
×
物的分子数为2N
A
①1 L 0.1 mol·L-1 CHCOOH溶液中所含H+的数目
3
×
电离 为0.1N 盐的水解、弱电解质的
A
水解 电离是可逆的
②2 L 1 mol·L-1 FeCl 溶液中所含Fe3+的数目为
3
×
2N
A
易错点5 不清楚溶液稀释或混合的规律
【分析】
1.溶液稀释和同种溶质的溶液混合
资料整理【淘宝店铺:向阳百分百】(1)稀释规律
溶质的质量在稀释前后保持不变,即mw =mw 。
1 1 2 2
溶质的物质的量在稀释前后保持不变,即cV=cV。
1 1 2 2
①溶质的量守恒
②溶液的量
【注意】溶液稀释时,溶液的质量守恒,即m(稀)=m(浓)+m(水),但溶液的体积一般不能相加
(2)同溶质不同物质的量浓度溶液混合的计算
①混合后溶液体积保持不变时:c V+cV=c ×(V +V )。
1 1 2 2 混 1 2
②混合后溶液体积发生改变时:c V+cV=c V ,其中V = 。
1 1 2 2 混 混 混
突破1 忽视物质的状态、所处状况
【例1】 为阿伏加德罗常数的值。下列叙述正确的是
A.(2023·辽宁卷) 含 键数目为
B.(2023·全国甲卷)标准状况下, 中电子的数目为
25 ℃ 101 kPa 28L 2.5N
C.(2022·全国甲卷) , 下, 氢气中质子的数目为 A
D.(2021·湖南卷) 和 (均为标准状况)在光照下充分反应后的分子数为
【答案】D
【解析】A. 分子含有2个 键,题中没有说是标况条件下,气体摩尔体积未知,无法计算 键个数,
A项错误;
B.在标准状况下,SO 状态为固态,不能计算出2.24L SO 物质的量,故无法求出其电子数目,B错误;
3 3
C.25℃、101kPa不是标准状况,不能用标况下的气体摩尔体积计算氢气的物质的量,故C错误;
D.甲烷和氯气在光照下发生取代,1mol氯气可取代1molH,同时产生1molHCl分子,标准状况下
的物质的量为0.5mol, 的物质的量为1mol,0.5molCH 含4molH,最多可消耗
4
4molCl ,因此CH 过量,根据1mol氯气可取代1molH,同时产生1molHCl分子可知1molCl 完全反应可
2 4 2
得1moHCl,根据C守恒,反应后含C物质的物质的量=甲烷的物质的量=0.5mol,因此 和
资料整理【淘宝店铺:向阳百分百】(均为标准状况)在光照下充分反应后的分子数为 ,D正确。
【变式1-1】设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.46g甲醚中含有C-H键的数目为3N
A
B.4.48L的14CO分子中的质子数是2.8N
A
C.2.0L1.0mol•L-1的酸性KCr O 溶液中含有的氧原子数为14N
2 2 7 A
D.1L0.1mol•L-1的NaHSO 溶液中,阴离子总数大于0.1N
3 A
【答案】D
【解析】A.46g甲醚的物质的量是1mol,其中含有C-H键的数目为6N ,A错误;
A
B.4.48L14CO的物质的量不一定是0.2mol,分子中的质子数不一定是2.8N ,B错误;
A
C.2.0L1.0mol•L-1的酸性KCr O 溶液中含有的氧原子数大于14N ,因为溶剂水分子中还含有氧原子,C
2 2 7 A
错误;
D.1L0.1mol•L-1的NaHSO 溶液中阴离子有亚硫酸氢根离子、亚硫酸根离子以及氢氧根离子,所以阴离子
3
总数大于0.1N ,D正确;
A
答案选D。
【变式1-2】设 为阿伏加德罗常数的值,下列说法正确的是
A.足量MnO 与含4molHCl的浓盐酸充分反应,转移电子数为2
2
B.标准状况下,11.2LHF含有的分子数为0.5
C.20g重水(D O)中含有的电子数为10
2
D.2molNO与1molO 在密闭容器中充分反应后的分子数为2
2
【答案】C
【解析】A. 与浓盐酸反应时,当 过量,随着反应的进行,浓盐酸浓度降低,稀盐酸不与
反应,HCl不能完全反应,所以量MnO 与含4molHCl的浓盐酸充分反应,转移电子数小于2 ;
2
B.标准状况下,HF为液态,不能根据 进行计算,故B错误;
C. 中电子数为10,相对分子质量为20,则20g重水(D O)中含有的电子数为 ,
2
故C正确;
D.根据反应 ,2mol 与1mol 在密闭容器中充分反应生成2mol , 在密闭容
器中部分转化为 ,其反应为 ,所以2molNO与1molO 在密闭容器中充分反应后的分
2
子数小于2 ,故D错误;
故选C。
突破2 不了解物质的组成、结构特点
资料整理【淘宝店铺:向阳百分百】【例2】 为阿伏加德罗常数的值。下列叙述正确的是
A.(2023·全国甲卷) 异丁烷分子中共价键的数目为
B.(2023·浙江卷)4.4gC HO中含有σ键数目最多为0.7N
2 4 A
C.(2023·辽宁卷) 晶体中含离子数目为
D.(2022·辽宁卷) 中含有的中子数为
E.(2022·浙江卷) 中含有 个阳离子
【答案】ABCD
【解析】A.异丁烷的结构式为 ,1mol异丁烷分子含有13N 共价键,所以0.50mol
A
异丁烷分子中共价键的数目为6.5N ,A正确;
A
B.1个C HO中含有6个σ键和1个π键(乙醛)或7个σ键(环氧乙烷),4.4gC HO的物质的量为0.1mol,
2 4 2 4
则含有σ键数目最多为0.7N ,B正确;
A
C.0.1mol 晶体含有离子为 、 ,含有离子数目为0.2 ,C项正确;
D.1个 原子中含有10个中子, 的物质的量为 ,故 中含有中子的物
质的量为 ,中子数为 ,故D正确;
E. 由钠离子和硫酸氢根离子构成,其中的阳离子只有钠离子, 的物质的量为
0.1mol,因此,其中只含有 个阳离子,E说法不正确。
【变式2-1】 为阿伏加德罗常数的值。下列说法错误的是
A. 分子中,S的价层电子对数是
B.常温下, 中含有氢键的数目为
C. 分子中含有的共价键数目为
D. 晶体中,阴阳离子数目之和是
【答案】B
【解析】A.一个SCl 分子中,S的孤电子对数是 ,硫氯单键是2,价层电子对数是4,所以
2
分子中,S的价层电子对数是 ,A正确;
B.常温下, 因是液态所以含有氢键的数目小于 ,B错误;
C.白磷分子是正四面体结构,一个分子有6个共价键, 分子中含有的共价键数目为 ,C正确;
资料整理【淘宝店铺:向阳百分百】D.硫酸氢钠固体中存在钠离子和硫酸氢根离子,所以 晶体中,阴阳离子数目之和是 ,D
正确;
故选B。
【变式2-2】设 为阿伏加德罗常数的数值,下列有关叙述正确的是
A.25℃时, 的 溶液中含有的 数为
B. 白磷( )分子中所含非极性共价键数为
C. 在稀硫酸溶液中水解可得到乙醇分子数为
D. 与 的混合物中所含中子数为
【答案】A
【解析】A.pH=1的硫酸溶液中氢离子浓度为0.1mol/L,体积1L,则含有的 数为 ,故A正确;
B. 分子为正四面体结构,1mol白磷( )分子中所含非极性共价键数为 ,故B错误;
C.酯的水解为可逆反应, 水解生成的乙醇分子数小于 ,故C错误;
D.1个 和1个 中均含8个中子, 和 的摩尔质量为18g/mol,则 混合物为
0.1mol,含中子数为 ,故D错误;
故选:A。
【变式2-3】(2023·湖北武汉·校联考模拟预测)甲酸甲酯常用作杀菌剂、熏蒸剂和烟草处理剂,可由甲
酸和甲醇反应制得。N 为阿伏加德罗常数的值。下列有关说法正确的是
A
A.pH=3的甲酸溶液中氢离子数目为1×10-3N
A
B.0.5 mol甲酸甲酯中含有sp3杂化的原子数目为N
A
C.50g质量分数为64%的甲醇水溶液中含有σ键数目为5N
A
D.甲醇燃料电池中,每消耗22.4L(标准状况)甲醇,转移电子数目为6N
A
【答案】B
【解析】A.该甲酸溶液体积未知,无法计算氢离子数目,A项错误;
B.甲酸甲酯中1个碳原子和1个氧原子采用sp3杂化,0.5mol甲酸甲酯中采用sp3的原子数目为N ,B项
A
正确;
C.50g质量分数为64%的甲醇水溶液中,m(CH OH)=32g,m(HO)=18g,各为1mol,1 mol CH OH中σ键
3 2 3
数目为5N ,1mol HO中σ键数目为2N ,因此50g该溶液中σ键数目为7N ,C项错误;
A 2 A A
D.标准状况下,甲醇为液体,D项错误;
故选B。
突破3 厘不清氧化还原反应中电子转移的数目
【例3】 为阿伏加德罗常数的值。下列叙述正确的是
A.(2022·海南卷)在2.8gFe中加入100mL3mol/LHCl,Fe完全溶解,则反应转移电子为0.1mol
资料整理【淘宝店铺:向阳百分百】B.(2021·全国甲卷) 的 与 完全反应时转移的电子数为
C.(2021·河北卷)电解饱和食盐水时,若阴阳两极产生气体的总质量为73g,则转移电子数为N
A
CuCl 6.4g 0.10N
D.(2022·全国甲卷)电解熔融 2,阴极增重 ,外电路中通过电子的数目为 A
【答案】A
【解析】A.2.8gFe的物质的量为0.05mol;100mL 3mol·L-1HCl中H+和Cl-的物质的量均为0.3mol,两者发
生反应后,Fe完全溶解,而盐酸过量。Fe完全溶解生成Fe2+,该反应转移电子0.1mol,A正确;
B. 与 反应的化学方程式为:3NO +H O=2HNO +NO,该反应消耗3个NO 分子转移的电子数
2 2 3 2
为2个,则有3mol的NO 参与反应时,转移的电子数为 ,B错误;
2
C.电解饱和食盐水时电极总反应为:2NaCl+2H O 2NaOH+H ↑+Cl↑,若阴阳两极产生气体分别是氢
2 2 2
气与氯气,且物质的量之比为1:1,若气体的总质量为 ,则说明反应生成的氢气与氯气的物质的量各
自为1mol,根据关系式H 2e-可知,转移的电子数为 ,C错误;
2
D.电解熔融CuCl 时,阳极反应为 ,阴极反应为 ,阴极增加的重量为Cu的质
2
量,6.4gCu的物质的量为0.1mol,根据阴极反应可知,外电路中通过电子的物质的量为0.2mol,数目为
0.2N ,故D错误。
A
【变式3-1】设N 代表阿佛加德罗常数的值,下列说法正确的是
A
A.标准状况下,2.24LCCl 含有的分子数目为0.1N
4 A
B.等物质的量的CH 和CO所含分子数均为N
4 A
C.电解精炼铜时,若阴极得到电子数为2N 个,则阳极质量减少64g
A
D.在反应KIO +6HI=KI+3I +3H O中,每生成3molI 转移的电子数为5N
3 2 2 2 A
【答案】D
【解析】A.标况下,CCl 不是气体,无法计算其物质的量,A错误;
4
B.物质的量具体数值不确定,不能由此得出CH 和CO所含分子数均为N ,B错误;
4 A
C.电解精炼铜时,阳极上杂质铁、锌等比铜活泼的金属先放电,若阴极得到2mol电子,则阳极质量减少
量不一定是64g,C错误;
D.该反应中,碘元素化合价由KIO 中+5价和HI中-1价变化为I 中的0价,电子转移5mol,生成
3 2
3molI ,所以每生成3molI 转移电子数为5N ,D正确;
2 2 A
故选D。
【变式3-2】用 表示阿伏加德罗常数的值。下列说法正确的是
A.常温下, 铁与足量浓硝酸充分反应转移的电子数为
B. 溶于足量的水充分反应转移的电子数为
C.标准状况下, 所含原子数为
资料整理【淘宝店铺:向阳百分百】D. 与 反应时,转移电子的数目为
【答案】D
【解析】A.常温下,铁遇浓硝酸钝化,A错误;
B. 与水不能完全反应,存在化学平衡,转移电子数不足1mol,B错误;
C.标准状况下, 是固体,C错误;
D.碘离子的还原性比亚铁离子强,碘离子先与氯气反应, 中含 , 与
恰好完全反应生成 和 ,转移电子 ,电子数为 ,D正确;
故选D。
突破4 忽视化学反应中微粒数目的变化
【例4】 为阿伏加德罗常数的值。下列叙述正确的是
A.(2022·全国甲卷)
2.0 L 1.0 molL1 AlCl 3溶液中,Al3
的数目为
2.0N
A
B.(2023·全国甲卷) 的 溶液中 的数目为
C.(2023·浙江卷)向1L0.1mol/LCHCOOH溶液通氨气至中性,铵根离子数为0.1N
3 A
D.(2021·河北卷)1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2N
A
E.(2021·广东卷) 与足量 反应生成的 分子数目为
【答案】D
【解析】A.Al3+在溶液中会发生水解生成Al(OH) ,因此2.0L 1.0 mol/L的AlCl 溶液中Al3+数目小于
3 3
2.0N ,故A错误;
A
B.pH=2的硫酸溶液中氢离子浓度为c(H+)=0.01mol/L,则1.0L pH=2的硫酸溶液中氢离子数目为0.01N ,
A
B错误;
C.向1L0.1mol/LCHCOOH溶液通氨气至中性,溶液中存在电荷守恒关系:c(CHCOO-)+c(OH-)=c(NH )
3 3
+c(H+),中性溶液c(OH-)=c(H+),则c(CHCOO-)=c(NH ),再根据物料守恒:n(CHCOO-)
3 3
+n(CH COOH)=0.1mol,得出铵根离子数小于0.1N ,C错误;
3 A
D.碘蒸气与氢气发生的反应为: ,反应为可逆反应,有一定的限度,所以充分
反应,生成的碘化氢分子数小于 ,D正确;
E. 为1mol,钠与足量的水反应生成氢气的关系式为: ,故1mol Na应对应生成0.5mol
H, 分子数目应为0.5 ,D错误;
2
【变式4-1】 代表阿伏加德罗常数的值。下列说法正确的是
A.1 mol 与3 mol 在一定条件下充分反应,转移的电子数为
B.11.2 L CO和 混合气体中含有的质子数为
资料整理【淘宝店铺:向阳百分百】C.1 L 1 mol·L 溴化铵水溶液中 与 的数量之和大于
D.25℃时, 的 溶液中含有 数为
【答案】C
【解析】A.1 mol 与3 mol 若完全反应生成2molNH3,转移6mol电子,转移电子数为 ,但由
于氮气和氢气的反应为可逆反应,反应不能进行完全,转移电子数少于6N ,A错误;
A
B.未指明气体所处状态,无法计算气体的物质的量,B错误;
C.1L1mol/L溴化铵水溶液中Br-数目为 ,根据电荷守恒c(Br-)+c(OH-)=c( )+c(H+),所以 与
的数量之和大于 ,C正确;
D.溶液的体积未知,无法计算 的物质的量,D错误;
故选C。
【变式4-2】设 为阿伏加德罗常数的值,下列说法正确的是
A.标准状况下, 中所含原子数目为
B.常温下, 与足量浓 反应转移电子的数目为
C.在浓硫酸作用下, 乙酸与足量乙醇发生反应生成乙酸乙酯分子的数目为
D.常温下, 的 溶液中 的数目为
【答案】D
【解析】A.标准状况下, 不是气体,无法计算物质的量,A错误;
B.常温下, 遇足量浓 钝化,B错误;
C.乙酸与乙醇的反应为可逆反应,乙酸不能完全反应,生成乙酸乙酯的分子数目无法计算,C错误;
D.常温下, 的 溶液中 ,则 ,其
,D正确;
故选D。
【变式4-3】(2023·湖南益阳·统考模拟预测)设 为阿伏加德罗常数的值,下列说法正确的是
A. 的 溶液中 的数目小于
B. 中价电子总数为
C.标准状况下, 中含有的 键数为
D.浓盐酸与 反应,产生 分子数为
【答案】C
【解析】A.溶液体积未知,不能确定离子的数目,故A错误;
B.1个 分子中价电子数为24个, 物质的量为1mol,价电子总数为 ,故B错误;
资料整理【淘宝店铺:向阳百分百】C. 结构式为: ,单键为 键,三键中有1个 键和2个 键,则标况下
中含有的 键数为 ,故C正确;
D.浓盐酸与二氧化锰反应为: ,由反应可知 完
全反应时,产生0.1mol ,分子数为 ,故D错误;
故选:C。
突破5 不清楚溶液稀释或混合的规律
【例5】将V L浓度为0.3mol/L的盐酸浓度扩大一倍,采取的措施合理的是
A.将溶液加热浓缩至原来体积的一半
B.通入标准状况下的HCl气体6.72L
C.加入3mol/L的盐酸0.2V L,再稀释至1.5V L
D.加入等体积0.9mol/L的盐酸,混合均匀
【答案】C
【解析】A.将溶液加热浓缩至原来体积的一半时,由于HCl的挥发,不能使其浓度扩大一倍,A不合理;
B.标准状况下6.72LHCl的物质的量为0.3mol,但向溶液中通入HCl气体时溶液的体积会发生变化,所以
浓度不能扩大一倍,B不合理;C.V L浓度为0.3mol/L的盐酸中有0.3VmolHCl,3mol/L的盐酸0.2V L含
HCl的物质的量为0.6Vmol,稀释至1.5V L,浓度为 =0.6mol/L,C合理;D.两种盐酸混
合后,溶液的体积不能直接加和,所以混合后溶液的物质的量浓度不是原来的2倍,D不合理;综上所述
答案为C。
【变式5-1】下列关于溶液物质的量浓度的说法正确的是
A.常温下,1 L水中溶解58.5 g NaCl,该溶液的物质的量浓度为1 mol/L
B.1 mol Na O加入适量水配成1 L溶液,该溶液的物质的量浓度为1 mol/L
2
C.200 mL0.1 mol/LNaCl溶液和100 mL0.1 mol/LMgCl 溶液,Cl-的物质的量浓度相同
2
D.10 g 98%的硫酸(密度为 )与20 mL18.4 mol/L的硫酸的浓度相同
【答案】D
【解析】A.58.5 g NaCl的物质的量是1 mol,将其溶解在1 L水中所得溶液体积不是1 L,因此所得溶液
的物质的量浓度不是1 mol/L,A错误;B.1 mol Na O加入适量水中,与水反应产生2 mol NaOH,配成的
2
1 L溶液中含有2 mol NaOH,则所得溶液的物质的量浓度为2 mol/L,B错误;C.200 mL0.1 mol/LNaCl溶
液中Cl-的浓度c(Cl-)=0.1 mol/L;100 mL0.1 mol/LMgCl 溶液中Cl-的物质的量浓度c(Cl-)=0.2 mol/L,可见两
2
种溶液中Cl-的物质的量浓度不相同,C错误;D.10 g 98%的硫酸的物质的量浓度c(H SO )=
2 4
,可见其与20 mL18.4 mol/L的硫酸的浓度相同,D正确;故合理选
项是D。
【变式5-2】a mLAl (SO ) 溶液中含有b g Al3+,取a/4 mL该溶液加水稀释到4a mL,则稀释后溶液中
2 4 3
资料整理【淘宝店铺:向阳百分百】的物质的量浓度为
A. mol·L-1 B. mol·L-1 C. mol·L-1 D. mol·L-1
【答案】A
【解析】b g Al3+的物质的量为 ,则n(Al(SO ))= ,a mL溶液中Al (SO ) 物质的量
2 4 3 2 4 3
浓度为c(Al (SO ))= ,则c( )=3 c(Al (SO ))= ,稀释前后
2 4 3 2 4 3
的物质的量不变,则n( )=cV= × = c( ) ×4a,解得稀释后溶液中 的物质的量浓度
后
为c( ) = mol·L-1,故选:A。
后
1.(2023·福建龙岩·统考模拟预测)N 为阿伏加德罗常数的值,将标况下1.12LCl 通入足量H18O中,下
A 2 2
列说法正确的是
A.该反应中转移电子数为0.1N B.0.2gH 18O中含中子数为0.1N
A 2 A
C.所得溶液中Cl-和Cl18O-总数为0.1N D.5.45gHCl18O中含H-Cl键数为0.1N
A A
【答案】B
【解析】A.氯气与水反应Cl+H 18O HCl+HCl18O,该反应中氯气既是氧化剂又是还原剂,假设氯气全
2 2
部参与反应,1mol氯气转移电子物质的量为1mol,因此标况下1.12L氯气参与反应,转移电子物质的量为
=0.05mol,故A错误;
B.1mol H18O中含有中子数为10N ,H18O的摩尔质量为20g/mol,则2g H 18O中含中子数为
2 A 2 2
=0.1N ,故B正确;
A
C.氯气与水反应Cl+H 18O HCl+HCl18O,体系中含氯微粒有Cl、Cl-、HCl18O、Cl18O-,则所得溶液中
2 2 2
Cl-和Cl18O-总数小于0.1N ,故C错误;
A
D.次氯酸的结构式为H-O-Cl,次氯酸中不含H-Cl,故D错误;
答案为B。
2.(2023·河北张家口·统考一模)设N 为阿伏加德罗常数的值.下列说法正确的是
A
A.1L0.01mol•L-1氯水中含有的Cl-、HClO和ClO-的总数为0.02N
A
B.7.8g苯中含有的σ键数目为0.6N
A
资料整理【淘宝店铺:向阳百分百】C.58g23Na35Cl中含有的中子数目为28N
A
D.由CoO制得1molCo O 时转移的电子数目为2N
3 4 A
【答案】D
【解析】A.氯水中含有氯分子,故1L 氯水中含有的 、HClO和 的总数小于 ,
A错误;
B.1个苯分子中含有12个σ键,7.8g即0.1mol苯中含有的σ键数目为 ,B错误;
C.58g 为1mol,其中含有的中子数目为 ,C错误;
D.根据化合价变化可知,由CoO制得1mol 的反应转移 电子,D正确;
故选D。
3.(2023·湖北卷)工业制备高纯硅的主要过程如下:
石英砂 粗硅 高纯硅
下列说法错误的是
A.制备粗硅的反应方程式为
B.1molSi含Si-Si键的数目约为
C.原料气HCl和 应充分去除水和氧气
D.生成 的反应为熵减过程
【答案】B
【解析】A. 和 在高温下发生反应生成 和 ,因此,制备粗硅的反应方程式为
,A说法正确;
B. 在晶体硅中,每个Si与其周围的4个Si形成共价键并形成立体空间网状结构,因此,平均每个Si形成
2个共价键, 1mol Si含Si-Si键的数目约为 ,B说法错误;
C. HCl易与水形成盐酸,在一定的条件下氧气可以将HCl氧化; 在高温下遇到氧气能发生反应生成水,
且其易燃易爆,其与 在高温下反应生成硅和HCl,因此,原料气HCl和 应充分去除水和氧气 ,
C说法正确;
D. ,该反应是气体分子数减少的反应,因此,生成 的反应为熵减过程,
D说法正确;
综上所述,本题选B。
4.(2023·安徽马鞍山·统考一模)N 为阿伏伽德罗常数的值,下列说法不正确的是
A
A.0.1 mol·L-1的NH HCO 溶液与NaOH溶液等体积混合并加热,产生的氨气标况下2.24L
4 3
B.标况下,1molN 和O 的混合气体总体积约为22.4L
2 2
资料整理【淘宝店铺:向阳百分百】C.常温常压下,2.8gCO和C H 的混合气体中含有的分子数目为0.1 N
2 4 A
D.39.0gNa O 与足量水完全反应,转移的电子数为0.5 N
2 2 A
【答案】A
【解析】A.n=cV,该条件下V未知,无法获得铵根的物质的量,更无法计算产生的NH ,A项错误;
3
B.标况下,任何气体的摩尔体积均为22.4L/mol,则该混合气体V=nVm=1mol×22.4L/mol=22.4L,B项正
确;
C.CO和C H 的摩尔质量均为28g/mol,可看作单一物质进行计算得n(气体)= ,则
2 4
混合气体中分子数目为0.1N ,C项正确;
A
D.39.0gNa O 物质的量为0.5mol,2NaO~2e-计算得电子物质的量为0.5mol,所以该反应中转移的电子数
2 2 2 2
目为0.5N ,D项正确;
A
故选A。
5.(2023·广东·校联考一模)工业烟气含有 ,可以用 溶液进行绿色化处理后再排放。设 为
阿伏加德罗常数的值,下列说法正确的是
A.6.4 g 含有的电子数目为0.3
B.1 L 1 溶液中 的数目为2
C.22.4 L (标准状况)与足量氧气反应,转移电子数目为2
D.1 溶液最多能吸收 的数目为0.1
【答案】B
【解析】A.6.4 g 的物质的量为0.1 mol,所含电子数目为3.2 ,选项A错误;
B.1 L 1 溶液中 的物质的量为2mol,其数目为2 ,选项B正确;
C. 和 的反应是可逆的,因此转移电子数小于2 ,选项C错误;
D.未给出 溶液的体积,无法计算,选项D错误;
答案选B。
6.(2022·重庆卷)工业上用N 和H 合成NH ,N 代表阿伏加德罗常数的值,下列说法正确的是
2 2 3 A
A.消耗14gN 生成NH 分子数为2 N
2 3 A
B.消耗1molH ,生成N-H键数为2 N
2 A
C.生成标准状况下22.4LNH ,电子转移数为2 N
3 A
D.氧化1molNH 生成NO,需O 分子数为2 N
3 2 A
【答案】B
【解析】A.由方程式可知,消耗14g氮气生成氨气的分子数为 ×2×N mol—1=N ,故A错误;
A A
B.由方程式可知,消耗1mol氢气生成N-H键数为1mol× ×3×N mol—1=2N ,故B正确;
A A
资料整理【淘宝店铺:向阳百分百】C.由方程式可知,生成标准状况下22.4L氨气,反应电子转移数为 ×3×N mol—1=3N ,故C错
A A
误;
D.由得失电子数目守恒可知,1mol氨气与氧气反应生成一氧化氮,需氧气分子数为1mol× ×N mol—
A
1=1.25N ,故D错误;
A
故选B。
7. N 为阿伏加德罗常数的值。下列叙述正确的是
A
A.标准状况下,11.2L氧气和臭氧混合气体中含氧原子数目为N
A
B.1 mol·L-1CHCOONa溶液中含CHCOOH、CHCOO-总数为N
3 3 3 A
C.一定条件下,1mol氢气与1mol碘单质充分反应后,分子总数为2N
A
D.含0.5mol 的酸性溶液与足量HO 反应生成 的过程中转移电子数为4N
2 2 A
【答案】C
【解析】A.O 分子中含有2个氧原子、O 分子中含有3个氧原子,标准状况下,11.2L氧气和臭氧混合气
2 3
体的物质的量为0.5mol,含氧原子数目为N ~1.5N 之间,故A错误;
A A
B.没有溶液体积,不能计算1 mol·L-1CHCOONa溶液中含CHCOOH、CHCOO-总数,故B错误;
3 3 3
C.氢气和碘反应方程式为H+I 2HI,反应前后气体分子数不变,一定条件下,1mol氢气与1mol碘单
2 2
质充分反应后,分子总数为2N ,故C正确;
A
D.含0.5mol 的酸性溶液与足量HO 反应生成 ,元素化合价均不变,不发生电子转
2 2
移,故D错误;
选C。
8.设 为阿伏加德罗常数的值,下列说法正确的是
A. 溶于水,溶液中 、 、 的粒子数之和等于
B. 晶体( )中含有 个晶胞结构单元
C.50 g质量分数为46%的乙醇( )水溶液中含有的氧原子总数为
D. ,当反应放热 时,产生 的分子数小于
【答案】C
资料整理【淘宝店铺:向阳百分百】【解析】A. 溶于水中存在平衡 和 ,根据氯原子守恒,
则 ,则 、 、HClO的粒子数之和小于 ,故A错误;
B. 晶体含有 ,根据图示可知, 晶体为面心立方结构,所以每个 晶胞中有4个
分子,则 分子可以形成0.25 mol晶胞结构单元,故B错误;
C.乙醇和水分子中均含有氧原子,50 g质量分数为46%的乙醇水溶液中含有的氧原子总数为
,故C正确;
D.根据热化学方程式可知,生成 时反应放热 ,则生成 的分子数为 ,故D错误;
选C。
9.(2023·辽宁·模拟预测)绿矾( )分解可制备铁红,同时产生 、 和 。设N 为阿
A
伏加德罗常数的值,下列说法错误的是
A. 溶液含有的阳离子数大于N
A
B.0.5mol三聚 分子( )中含有σ键数目为6 N
A
C.绿矾分解生成16g 时,转移电子数为0.2 N
A
D.22.4L 溶于水,溶液中 、 、 的数目总和为N
A
【答案】D
【解析】A.硫酸亚铁是强酸弱碱盐,亚铁离子在溶液中水解使溶液中的阳离子数目增大,则1L1mol/L硫
酸亚铁溶液含有的阳离子数大于1mol/L ×1L×N mol—1=N ,故A正确;
A A
B.由结构可知,三聚三氧化硫分子中含有的σ键为12,则0.5mol三聚三氧化硫分子中含有的σ键的数目
为0.5mol×12×N mol—1=6N ,故B正确;
A A
C.由题意可知,绿矾受热分解的方程式为2FeSO ·7H O Fe O+SO↑+SO↑+7H O,反应生成1mol三
4 2 2 3 2 3 2
氧化铁,反应转移2mol电子,则生成16g三氧化铁时,转移电子数为 ×2×N mol—1=0.2 N ,故C
A A
正确;
D.缺标准状况,无法计算22.4L二氧化硫的物质的量,且二氧化硫与水反应为可逆反应,可逆反应不可
能完全进行,所以无法计算使溶液中亚硫酸、亚硫酸氢根、亚硫酸根的数目总和,故D错误;
故选D。
10.(2022·福建卷)常温常压下,电化学还原制氨气的总反应方程式: ,
设 为阿伏加德罗常数的值,下列说法正确的是
资料整理【淘宝店铺:向阳百分百】A. 水中含有的孤电子对数为
B.每产生 失去的电子数为
C. 氨水中,含有的 分子数少于
D.消耗 (已折算为标况)时,产生的 分子数为
【答案】D
【解析】A.HO分子中孤电子对数为 =2, HO的物质的量为 =0.5mol,含有的孤电子
2 2
对数为 ,故A错误;
B.该反应中N 中N元素化合价由0价下降到-3价,34g 的物质的量为 =2mol,每产生
2
, 得到6mol电子,数目为6N ,故B错误;
A
C.氨水的体积未知,无法计算 的分子数,故C错误;
D. 的物质的量为0.5mol,由方程式可知,消耗0.5mol ,产生的0.75mol ,数目为 ,
故D正确;
故选D。
11.设 为阿伏加德罗常数的值,下列叙述正确的是
A. 中 键的数目为
B.标准状况下, 中所含质子总数为
C. 中S的价层电子对数为
D.常温下, 与足量浓硫酸反应,转移电子的数目为
【答案】C
【解析】A. 中 与 之间有四个配位键是 键, 分子内有三个 键,所以 键
的数目为 ,故A错误;
B. 在标况下不是气态,无法计算1.12L SO 的物质的量和其所含质子数,故B错误;
3
C. 中S的价层电子对数为 ,所以 中S的价层电子对数为 ,故C正确;
D.常温下, 与足量浓硫酸发生钝化,无法计算转移电子的数目,故D错误;
故选C。
12.(2021·山东卷)X、Y均为短周期金属元素,同温同压下,0.1molX的单质与足量稀盐酸反应,生成
H 体积为VL;0.1molY的单质与足量稀硫酸反应,生成H 体积为VL。下列说法错误的是
2 1 2 2
资料整理【淘宝店铺:向阳百分百】A.X、Y生成H 的物质的量之比一定为
2
B.X、Y消耗酸的物质的量之比一定为
C.产物中X、Y化合价之比一定为
D.由 一定能确定产物中X、Y的化合价
【答案】D
【分析】设与1mol X反应消耗HCl的物质的量为amol,与1mol Y反应消耗HSO 的物质的量为bmol,根
2 4
据转移电子守恒以及H原子守恒可知 、 。
【解析】A.同温同压下,气体体积之比等于其物质的量之比,因此X、Y生成H 的物质的量之比一定为
2
,故A正确;
B. X、Y反应过程中消耗酸的物质的量之比为 ,因 ,因此 ,故B正确;
C.产物中X、Y化合价之比为 ,由B项可知 ,故C正确;
D.因短周期金属单质与盐酸或稀硫酸反应时,生成的盐中金属元素化合价有+1、+2、+3三种情况,因此
存在a=1,2,3,b=0.5,1的多种情况,由 可知,当a=1,b=0.5时, =1,当a=2,b=1时,
=1,两种情况下X、Y的化合价不同,因此根据 可能无法确定X、Y的化合价,故D错误;
综上所述,错误的D项,故答案为D。
13.设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.常温常压下,1.4g乙烯与乙烷的混合气体中含有的碳原子数为0.1N
A
B.用惰性电极电解饱和食盐水,若阴极产生11.2L气体,则线路中通过N 个电子
A
C.1molAl3+完全水解生成氢氧化铝胶体粒子的数目为N
A
D.密闭容器中,2molNO与1molO 充分反应后,混合气体中含有的氧原子数为4N
2 A
【答案】D
【解析】A.1.4g乙烯中含有的碳原子数为0.1 ,1.4g乙烷中含有的碳原子数小于0.1 ,故1.4g乙烯
与乙烷的混合气体中含有的碳原子数小于0.1 ,A错误;
资料整理【淘宝店铺:向阳百分百】B.阴极产生11.2L气体,但未指明温度、压强,无法计算线路中通过的电子数,B错误;
C.多个氢氧化铝分子聚集成氢氧化铝胶体粒子,1mol 完全水解生成氢氧化铝胶体粒子的数目小于 ,
C错误;
D.2molNO与1mol 中含有的氧原子总数为4 ,根据氧原子守恒可知,反应后混合气体中含有的氧
原子数仍为4 ,D正确;
故选D。
资料整理【淘宝店铺:向阳百分百】