文档内容
素养说明:离子方程式的书写是每年高考必考内容,一般在填空题中出现较多,
常结合化工生产流程进行考查,除考查教材所涉及的常见重要的反应外,越来越
注重结合新信息书写陌生离子方程式的考查,另外还应关注与量有关的离子方程
式的书写。
[题型专练]
类型1 反应连续型离子方程式书写——“分步分析法”
(1)反应特点:反应生成的离子因又能与过量的反应物继续反应而导致其离子
方程式与用量有关。
(2)书写模型:首先分析判断出物质过量与否,再根据原理书写。
1.按用量要求书写下列离子方程式:
铝盐溶液与强碱溶液反应
铝盐过量:____________________________________________________________
强碱过量:___________________________________________________________。
答案 Al3++3OH-===Al(OH) ↓
3
Al3++4OH-===AlO+2H O
2
类型2 反应先后型离子方程式书写——“强先弱后法”
(1)反应特点:某种反应物的两种或两种以上的组成离子,都能跟另一种反应物的
组成离子反应,但因反应顺序不同而跟用量有关,又称为竞争型。
(2)书写模型:依据“竞争反应,强者优先”的规律,解决离子反应的先后顺序问
题,解答时先确定出反应先后的离子,再分步书写出离子方程式。
2.按用量要求书写下列离子方程式
NH Al(SO ) 溶液与NaOH溶液反应:
4 4 2
NaOH不足:__________________________________________________________
n[NH Al(SO ) ]∶n(NaOH)=1∶4:_______________________________________
4 4 2NaOH足量:__________________________________________________________
答案 Al3++3OH-===Al(OH) ↓ NH+Al3++4OH-===NH ·H O+Al(OH) ↓
3 3 2 3
NH+Al3++5OH-===NH ·H O+AlO+2H O
3 2 2
类型3 物质配比型离子方程式书写——“少定多变”法
【书写模型】
“定1法”书写酸式盐与碱反应的离子方程式
(1)将少量物质定为“1 mol”,若少量物质有两种或两种以上离子参加反应,则参
加反应离子的物质的量之比与物质组成之比相符。
(2)依据少量物质中离子的物质的量,确定过量物质中实际参加反应的离子的物
质的量。
3.按用量要求书写下列离子方程式
NaHCO 溶液与Ca(OH) 溶液反应
3 2
NaHCO 不足:____________________________________________________;
3
NaHCO 过量:_____________________________________________________
3
___________________________________________________________________。
答 案 HCO + OH - + Ca2 + ===CaCO ↓ + H O Ca2 + + 2OH - +
3 2
2HCO===CaCO ↓+CO+2H O
3 2
类型4 氧化还原反应型——“假设定序”法
(1)反应特点:对于氧化还原反应,按“先强后弱”的顺序书写,即氧化性(或还原
性)强的优先发生反应,氧化性(或还原性)弱的后发生反应。
(2)解题模型:第一步:确定反应的先后顺序:(氧化性:HNO >Fe3+,还原性:I-
3
>Fe2+>Br-)。如向FeI 溶液中通入Cl ,I-先与Cl 发生反应。
2 2 2
第二步:根据用量判断反应发生的程度,如少量Cl 与FeI 溶液反应时只有I-与
2 2
Cl 反应:2I-+Cl ===2Cl-+I 。
2 2 2
足量Cl 与FeI 溶液的反应时溶液中的I-和Fe2+均与Cl 发生反应:2Fe2++4I-+
2 2 2
3Cl ===2Fe3++2I +6Cl-。
2 2
第三步:用“少量定1法”书写离子方程式,即将“量”少物质的化学计量数定
为“1”进行书写。
4.按用量书写下列离子方程式
(1)FeBr 溶液中通入少量Cl :
2 2____________________________________________________________________;
(2)FeBr 溶液中通入与其等物质的量的氯气:
2
____________________________________________________________________;
(3)FeBr 溶液中通入足量Cl :
2 2
_____________________________________________________________________
。
答案 (1)①2Fe2++Cl ===2Fe3++2Cl-
2
(2)2Fe2++2Br-+2Cl ===2Fe3++Br +4Cl-
2 2
(3)2Fe2++4Br-+3Cl ===2Fe3++2Br +6Cl-
2 2
书写陌生情景中的离子方程式时,要有效的接受、吸收、整合题目信息,推断并写
出反应物和生成物,然后再运用质量守恒定律、得失电子守恒规律(氧化还原反
应)、电荷守恒规律,遵循“先电子、再电荷、后原子”的顺序配平。
【书写模型】
步骤一 根据信息分离出反应物和产物
步骤二 根据得失电子配平涉及氧化还原反应的物质或离子
步骤三 根据电荷守恒配平其它离子(H+、OH-)
步骤四 根据原子守恒配平其它物质(H O)
2
说明:非氧化还原反应型离子方程式的书写,通过步骤一、三、四完成
5.根据题设要求完成离子方程式书写。
(1)[2018·课标全国Ⅰ,27(1)(4)]焦亚硫酸钠(Na S O )在医药、橡胶、印染、食品等
2 2 5
方面应用广泛。回答下列问题:
①生产Na S O ,通常是由NaHSO 过饱和溶液经结晶脱水制得。写出该过程的化
2 2 5 3
学方程式________________________________________________________。
②Na S O 可用作食品的抗氧化剂。在测定某葡萄酒中Na S O 残留量时,取
2 2 5 2 2 5
50.00 mL葡萄酒样品,用0.010 00 mol·L-1的碘标准液滴定至终点,消耗 10.00
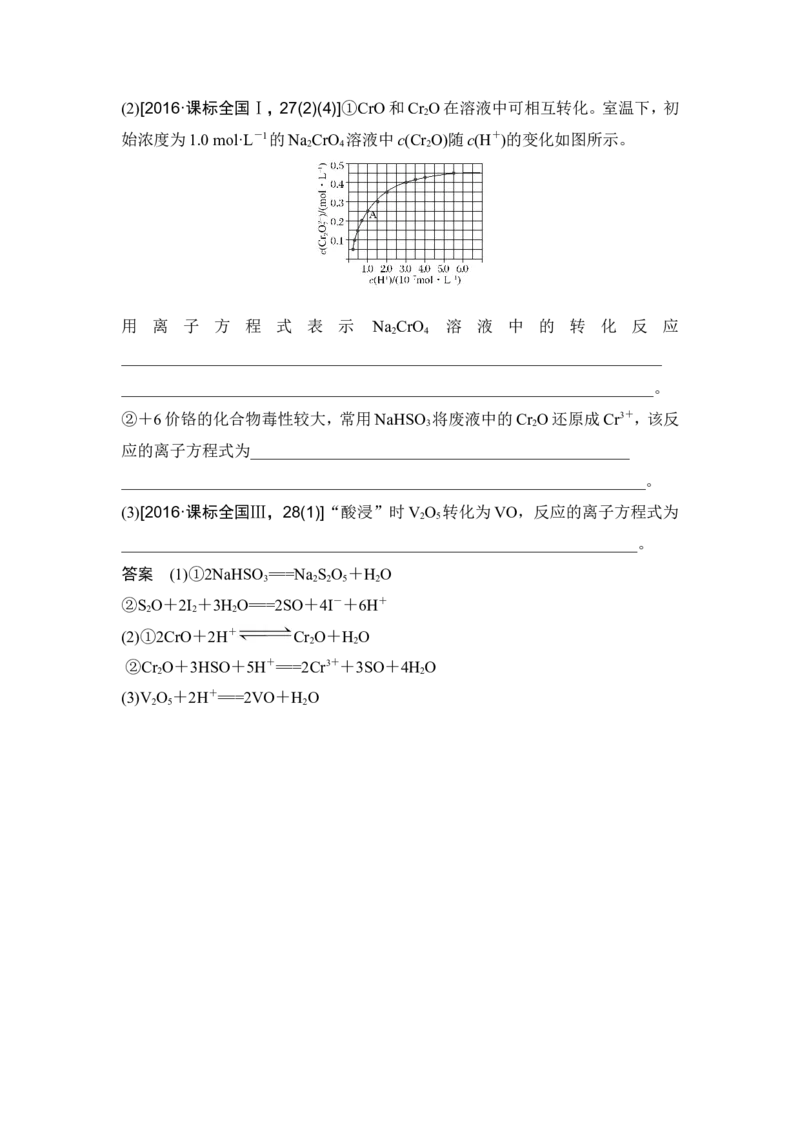
mL。滴定反应的离子方程式为______________________________________。(2)[2016·课标全国Ⅰ,27(2)(4)]①CrO和Cr O在溶液中可相互转化。室温下,初
2
始浓度为1.0 mol·L-1的Na CrO 溶液中c(Cr O)随c(H+)的变化如图所示。
2 4 2
用 离 子 方 程 式 表 示 Na CrO 溶 液 中 的 转 化 反 应
2 4
___________________________________________________________________
__________________________________________________________________。
②+6价铬的化合物毒性较大,常用NaHSO 将废液中的Cr O还原成Cr3+,该反
3 2
应的离子方程式为_______________________________________________
_________________________________________________________________。
(3)[2016·课标全国Ⅲ,28(1)]“酸浸”时V O 转化为VO,反应的离子方程式为
2 5
________________________________________________________________。
答案 (1)①2NaHSO ===Na S O +H O
3 2 2 5 2
②S O+2I +3H O===2SO+4I-+6H+
2 2 2
(2)①2CrO+2H+ Cr O+H O
2 2
②Cr O+3HSO+5H+===2Cr3++3SO+4H O
2 2
(3)V O +2H+===2VO+H O
2 5 2