文档内容
素养说明:近年来,在高考化学试题尤其是新课程高考试题中凸现出了一种新的
题型—动态多变量图像题。此类试题的图像中隐含信息量大,对学生读图获取信
息能力的要求较高;由于多变量的存在,要求学生会多角度、多层面去思考和探
究问题,有效的考查了学生综合分析、推理判断能力。
用数形结合思想理解Na CO 、NaHCO 与盐酸的反应:
2 3 3
实验操作和反应 n(CO )-n(HCl)图像
2
向Na CO 溶液中逐滴加入盐酸,离子方程式:Oa段:
2 3
CO+H+===HCO
ab段:HCO+H+===H O+CO ↑
2 2
图像特点Oa=ab
向NaHCO 溶液中逐滴加入盐酸,离子方程式:HCO+
3
H+===H O+CO ↑
2 2
向等物质的量的NaOH、Na CO 的混合溶液中逐滴加
2 3
入盐酸,离子方程式:
Oa段:H++OH-===H O、CO+H+===HCO
2
ab段:HCO+H+===H O+CO ↑
2 2
图像特点:Oa>ab
向等物质的量的Na CO 、NaHCO 的混合溶液中逐滴
2 3 3
加入盐酸,离子方程式:Oa段:CO+H+===HCO
ab段:HCO+H+===H O+CO ↑
2 2
图像特点:Oa<ab
[题型专练]
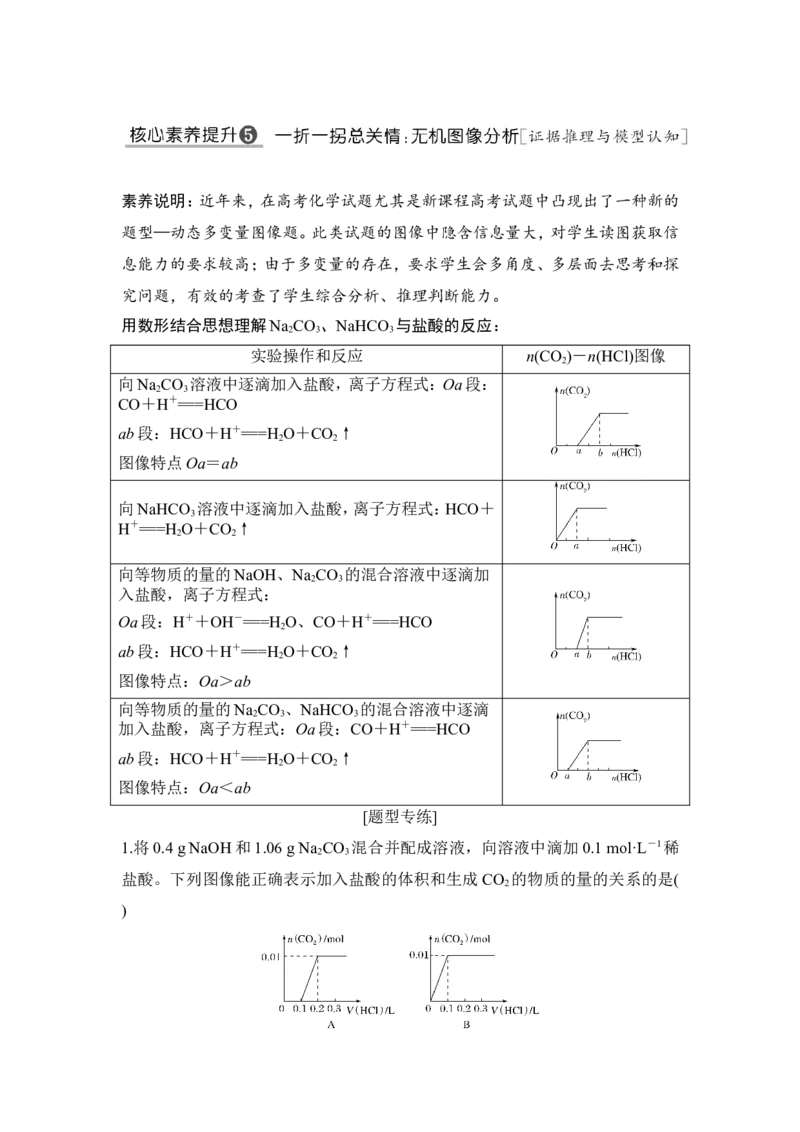
1.将0.4 g NaOH和1.06 g Na CO 混合并配成溶液,向溶液中滴加0.1 mol·L-1稀
2 3
盐酸。下列图像能正确表示加入盐酸的体积和生成CO 的物质的量的关系的是(
2
)解析 0.01 mol NaOH先与0.01 mol H+中和,CO再与H+生成HCO,又消耗0.01
mol H+,最后0.01 mol HCO与H+反应生成0.01 mol CO 。
2
答案 C
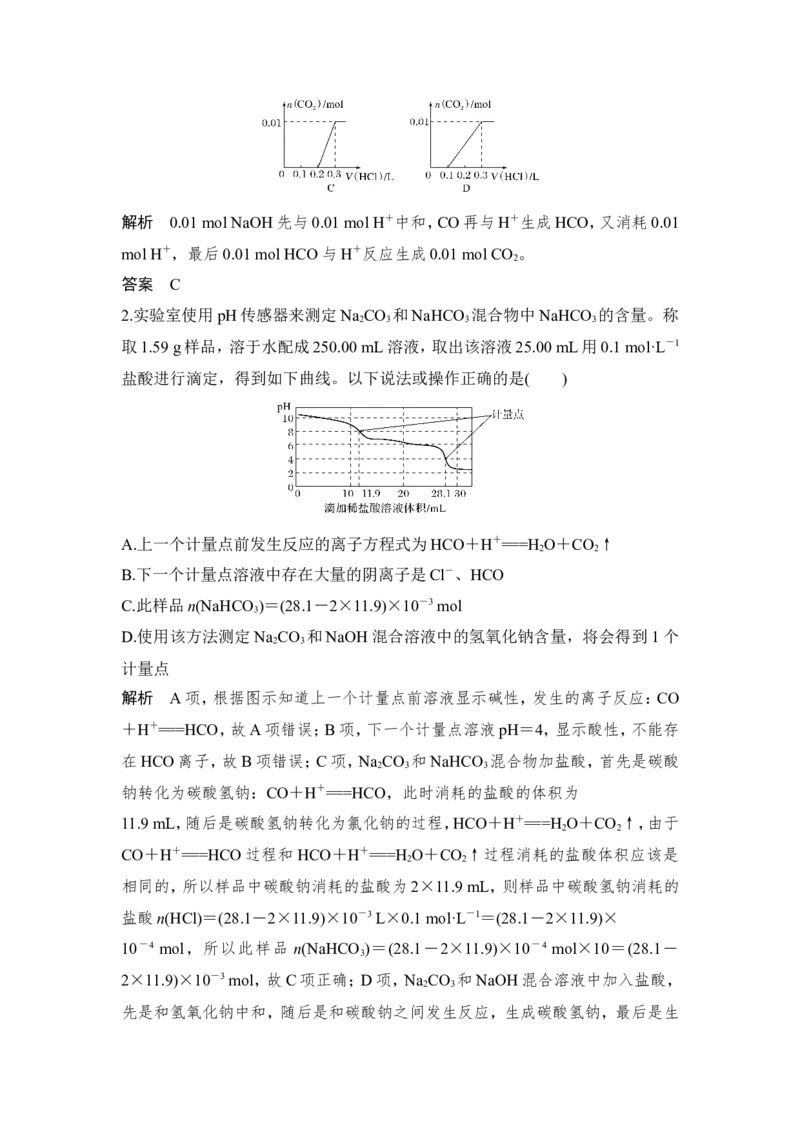
2.实验室使用pH传感器来测定Na CO 和NaHCO 混合物中NaHCO 的含量。称
2 3 3 3
取1.59 g样品,溶于水配成250.00 mL溶液,取出该溶液25.00 mL用0.1 mol·L-1
盐酸进行滴定,得到如下曲线。以下说法或操作正确的是( )
A.上一个计量点前发生反应的离子方程式为HCO+H+===H O+CO ↑
2 2
B.下一个计量点溶液中存在大量的阴离子是Cl-、HCO
C.此样品n(NaHCO )=(28.1-2×11.9)×10-3 mol
3
D.使用该方法测定Na CO 和NaOH混合溶液中的氢氧化钠含量,将会得到 1个
2 3
计量点
解析 A项,根据图示知道上一个计量点前溶液显示碱性,发生的离子反应:CO
+H+===HCO,故A项错误;B项,下一个计量点溶液pH=4,显示酸性,不能存
在HCO离子,故B项错误;C项,Na CO 和NaHCO 混合物加盐酸,首先是碳酸
2 3 3
钠转化为碳酸氢钠:CO+H+===HCO,此时消耗的盐酸的体积为
11.9 mL,随后是碳酸氢钠转化为氯化钠的过程,HCO+H+===H O+CO ↑,由于
2 2
CO+H+===HCO过程和HCO+H+===H O+CO ↑过程消耗的盐酸体积应该是
2 2
相同的,所以样品中碳酸钠消耗的盐酸为2×11.9 mL,则样品中碳酸氢钠消耗的
盐酸n(HCl)=(28.1-2×11.9)×10-3 L×0.1 mol·L-1=(28.1-2×11.9)×
10-4 mol,所以此样品 n(NaHCO )=(28.1-2×11.9)×10-4 mol×10=(28.1-
3
2×11.9)×10-3 mol,故C项正确;D项,Na CO 和NaOH混合溶液中加入盐酸,
2 3
先是和氢氧化钠中和,随后是和碳酸钠之间发生反应,生成碳酸氢钠,最后是生成氯化钠,不止得到1个计量点,是3个计量点,故D项错误。
答案 C
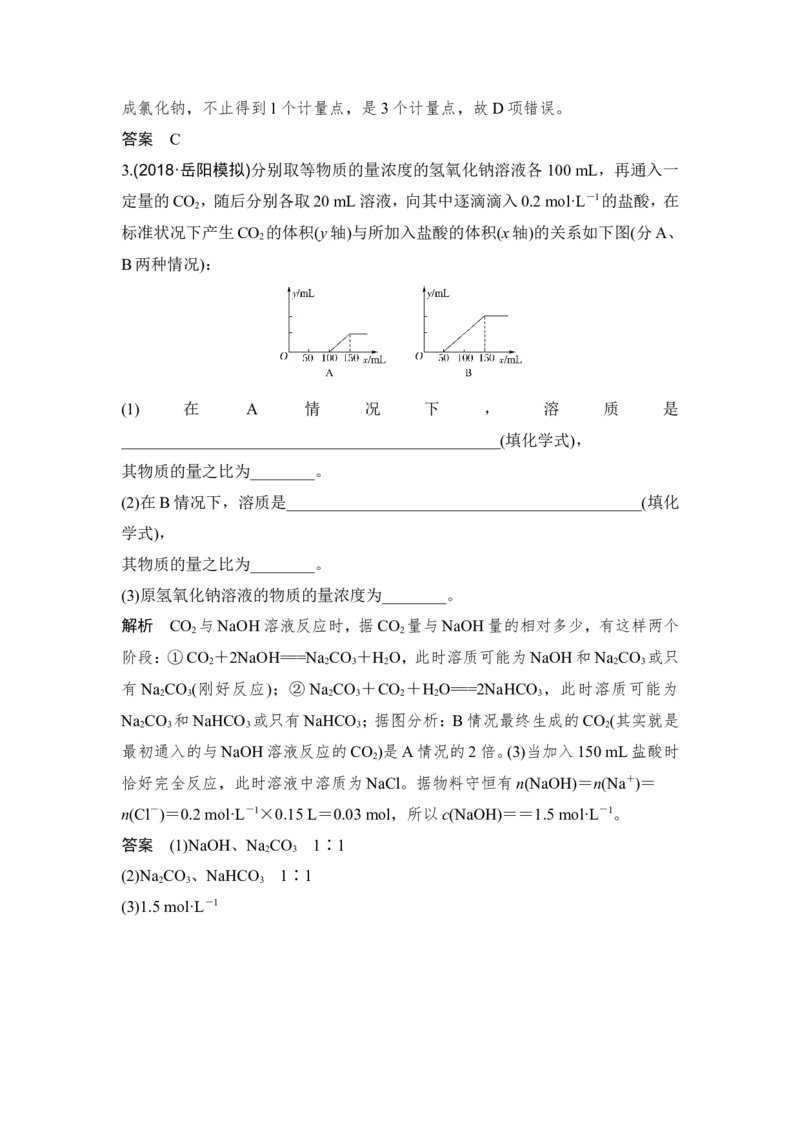
3.(2018·岳阳模拟)分别取等物质的量浓度的氢氧化钠溶液各 100 mL,再通入一
定量的CO ,随后分别各取20 mL溶液,向其中逐滴滴入0.2 mol·L-1的盐酸,在
2
标准状况下产生CO 的体积(y轴)与所加入盐酸的体积(x轴)的关系如下图(分A、
2
B两种情况):
(1) 在 A 情 况 下 , 溶 质 是
_______________________________________________(填化学式),
其物质的量之比为________。
(2)在B情况下,溶质是____________________________________________(填化
学式),
其物质的量之比为________。
(3)原氢氧化钠溶液的物质的量浓度为________。
解析 CO 与NaOH溶液反应时,据CO 量与NaOH量的相对多少,有这样两个
2 2
阶段:①CO +2NaOH===Na CO +H O,此时溶质可能为NaOH和Na CO 或只
2 2 3 2 2 3
有 Na CO (刚好反应);② Na CO +CO +H O===2NaHCO ,此时溶质可能为
2 3 2 3 2 2 3
Na CO 和NaHCO 或只有NaHCO ;据图分析:B情况最终生成的CO (其实就是
2 3 3 3 2
最初通入的与NaOH溶液反应的CO )是A情况的2倍。(3)当加入150 mL盐酸时
2
恰好完全反应,此时溶液中溶质为NaCl。据物料守恒有n(NaOH)=n(Na+)=
n(Cl-)=0.2 mol·L-1×0.15 L=0.03 mol,所以c(NaOH)==1.5 mol·L-1。
答案 (1)NaOH、Na CO 1∶1
2 3
(2)Na CO 、NaHCO 1∶1
2 3 3
(3)1.5 mol·L-1