文档内容
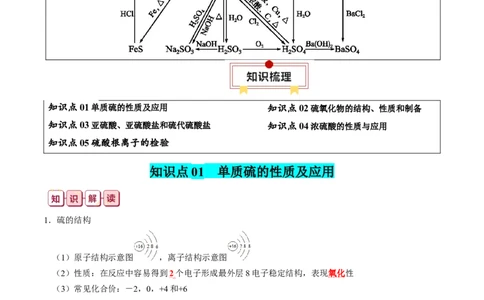
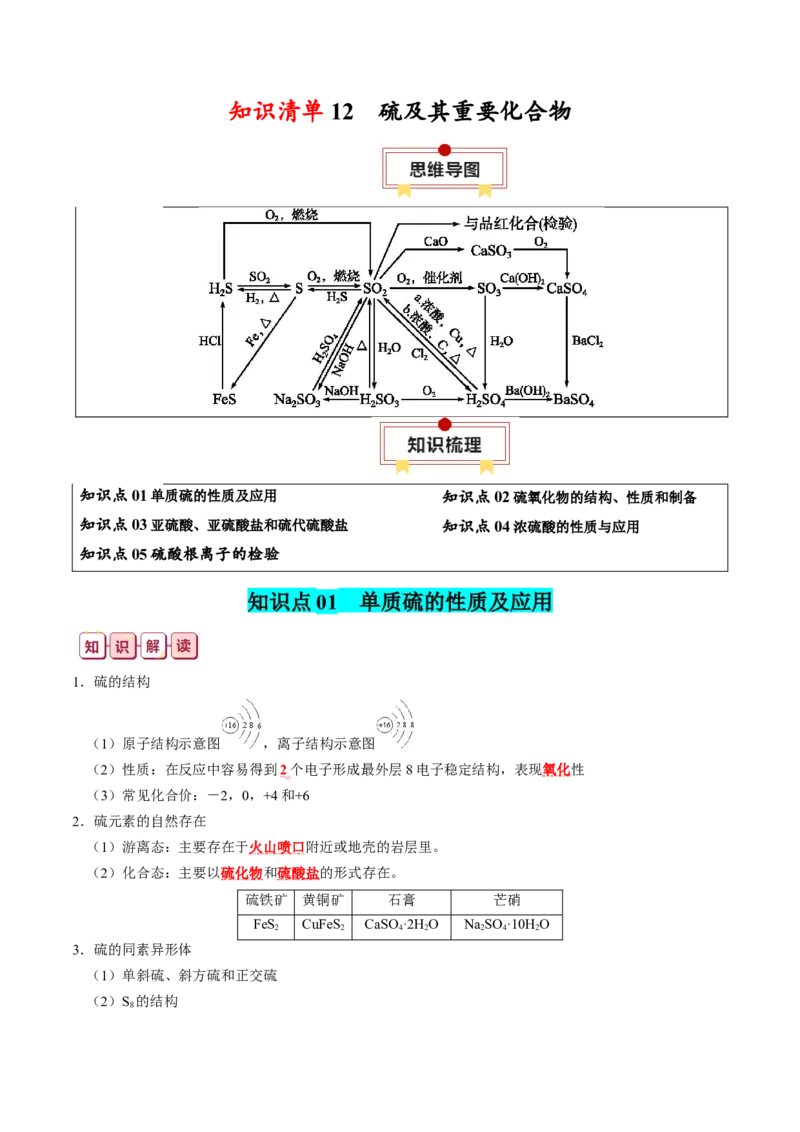
知识清单 12 硫及其重要化合物
知识点01单质硫的性质及应用 知识点02硫氧化物的结构、性质和制备
知识点03亚硫酸、亚硫酸盐和硫代硫酸盐 知识点04浓硫酸的性质与应用
知识点05硫酸根离子的检验
知识点 01 单质硫的性质及应用
1.硫的结构
(1)原子结构示意图 ,离子结构示意图
(2)性质:在反应中容易得到2 个电子形成最外层8电子稳定结构,表现氧化性
(3)常见化合价:-2,0,+4和+6
2.硫元素的自然存在
(1)游离态:主要存在于火山喷口附近或地壳的岩层里。
(2)化合态:主要以硫化物和硫酸盐的形式存在。
硫铁矿 黄铜矿 石膏 芒硝
FeS CuFeS CaSO·2HO NaSO ·10HO
2 2 4 2 2 4 2
3.硫的同素异形体
(1)单斜硫、斜方硫和正交硫
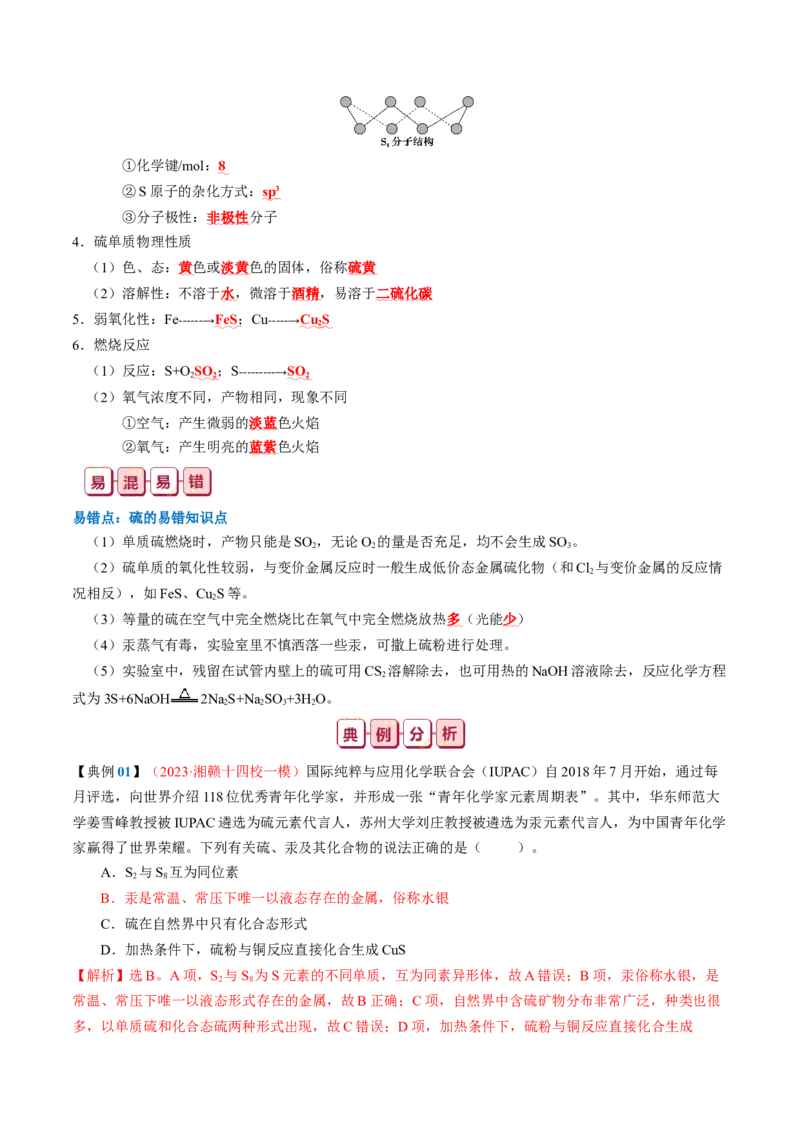
(2)S 的结构
8①化学键/mol:8
②S原子的杂化方式: sp 3
③分子极性:非极性分子
4.硫单质物理性质
(1)色、态:黄色或淡黄色的固体,俗称硫黄
(2)溶解性:不溶于水,微溶于酒精,易溶于二硫化碳
5.弱氧化性:Fe------→FeS;Cu-----→Cu S
2
6.燃烧反应
(1)反应:S+OSO ;S---------→SO
2 2 2
(2)氧气浓度不同,产物相同,现象不同
①空气:产生微弱的淡蓝色火焰
②氧气:产生明亮的蓝紫色火焰
易错点:硫的易错知识点
(1)单质硫燃烧时,产物只能是SO ,无论O 的量是否充足,均不会生成SO 。
2 2 3
(2)硫单质的氧化性较弱,与变价金属反应时一般生成低价态金属硫化物(和Cl 与变价金属的反应情
2
况相反),如FeS、Cu S等。
2
(3)等量的硫在空气中完全燃烧比在氧气中完全燃烧放热多(光能少)
(4)汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理。
(5)实验室中,残留在试管内壁上的硫可用CS 溶解除去,也可用热的NaOH溶液除去,反应化学方程
2
式为3S+6NaOH 2NaS+Na SO +3H O。
2 2 3 2
【典例01】(2023·湘赣十四校一模)国际纯粹与应用化学联合会(IUPAC)自2018年7月开始,通过每
月评选,向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。其中,华东师范大
学姜雪峰教授被IUPAC遴选为硫元素代言人,苏州大学刘庄教授被遴选为汞元素代言人,为中国青年化学
家赢得了世界荣耀。下列有关硫、汞及其化合物的说法正确的是( )。
A.S 与S 互为同位素
2 8
B.汞是常温、常压下唯一以液态存在的金属,俗称水银
C.硫在自然界中只有化合态形式
D.加热条件下,硫粉与铜反应直接化合生成CuS
【解析】选B。A项,S 与S 为S元素的不同单质,互为同素异形体,故A错误;B项,汞俗称水银,是
2 8
常温、常压下唯一以液态形式存在的金属,故B正确;C项,自然界中含硫矿物分布非常广泛,种类也很
多,以单质硫和化合态硫两种形式出现,故C错误;D项,加热条件下,硫粉与铜反应直接化合生成Cu S,故D错误。
2
【典例02】S单质的常见形式是S,其环状分子结构模型示意图如下:
8
下列说法正确的是( )。
A.32gS 中含有0.125molσ键
8
B.CHCOOH适合作溶解硫粉(S)的溶剂
3 8
C.固态硫S 属于共价晶体
8
D.S原子采用的轨道杂化方式是sp3
【解析】选D。1个S 分子中含有8个σ键,则32g即0.125molS 分子中含有1molσ键,A选项错误;S 的
8 8 8
环状结构为对称结构,则S 是非极性分子,CHCOOH是极性分子,根据相似相溶原理:极性分子易溶于
8 3
极性溶剂,非极性分子易溶于非极性溶剂,所以S 不易溶于CHCOOH,B选项错误;S 是分子晶体(1个
8 3 8
分子中含有8个原子),C选项错误;S 是一个环形分子,每个S与两个其它S原子相连,S原子外层6个
8
电子,两对孤对电子,两上σ键,所以S是sp3杂化,D选项正确。
知识点 02 硫氧化物的结构、性质和制备
一、二氧化硫的结构和性质
1.结构
4
(1)大 键:Π3
(2)S原子杂化方式: sp 2
(3)空间构型: V 形
(4)分子极性:极性分子
(5)等电子体:SO 、 O 、 NO -
2 3 2
2.物理性质
(1)色味态:无色有刺激性气味的气体
(2)密度:比空气的大
(3)溶解性:易溶于水(1∶40),不溶于 饱和 NaHSO 溶液
3
(4)熔沸点:比较低,沸点-10℃,易液化
3.酸性氧化物的通性
(1)与水化合成亚硫酸:SO +H O HSO
2 2 2 3
(2)与碱性氧化物化合成亚硫酸盐
①CaO: CaO +SO CaSO
2 3②NaO:Na O +SO Na SO
2 2 2 2 3
(3)与碱性溶液反应:少量SO 生成亚硫酸盐,过量SO 生成亚硫酸氢盐
2 2
①少量SO : 2NaOH + SO Na SO + H O
2 2 2 3 2
②过量SO : NaOH + SO NaHSO
2 2 3
(4)与弱酸盐反应:强酸制弱酸
①SO +2NaHCO NaSO +CO↑+HO
2 3 2 3 2 2
②NaSiO+SO+H O=HSiO↓+Na SO
2 3 2 2 2 3 2 3
(5)与亚硫酸盐反应生成亚硫酸氢盐
①NaSO :SO + Na SO + H O 2NaH S O
2 3 2 2 3 2 3
②CaSO:SO +C aSO + H O C a ( H S O )
3 2 3 2 3 2
4.弱氧化性:与HS气体混合
2
(1)反应:2HS+SO = 2H O+3S ↓
2 2 2
(2)现象:容器壁上有水珠出现,析出黄色固体
5.强还原性
SO -------------------------------------------→SO 或SO 2-
2 3 4
(1)催化氧化
①反应:2SO +O 2 SO
2 2 3
②应用:工业上制硫酸的第二步反应
(2)能够使卤水褪色
①氯水:SO +Cl+2H O 2HCl+H SO
2 2 2 2 4
②溴水:SO +Br +2H O 2HBr+H SO (检验或除去SO )
2 2 2 2 4 2
③碘水:SO + I +2H O 2H I +H SO
2 2 2 2 4
(3)能够使酸性高锰酸钾溶液褪色
①反应:2MnO - + 5 SO + 2 H O 2Mn 2+ + 5 SO 2 - + 4 H +
4 2 2 4
②应用:检验或除去SO
2
(4)能够使铁盐变色
①反应: 2Fe 3+ + SO + 2 H O 2Fe 2+ +4 H + + SO 2-
2 2 4
②现象:溶液由棕黄色变成浅绿色
(5)能够被过氧化物氧化成硫酸或硫酸盐
①NaO:SO +Na O Na SO
2 2 2 2 2 2 4
②HO:SO +HO HSO
2 2 2 2 2 2 4
(6)能够将硝酸根离子还原
①浓硝酸:2NO -+3SO+2HO 3SO 2-+2NO↑+4H+
3 2 2 4
②稀硝酸:2NO -+SO SO 2-+2NO↑
3 2 4 2
(7)SO 和氧化性盐溶液的反应
2①BaCl 溶液 没有现象;Ba(NO ) 产生BaSO 沉淀。
2 3 2 4
②Ca(ClO) 产生CaCO 沉淀;Ca(ClO) 产生 Ca SO 沉淀。
2 3 2 4
6.漂白性:检验SO 气体的最佳方法
2
(1)现象:能使品红溶液褪色,加热变红
(2)原理即特点
①化合性:亚硫酸和品红发生化合反应(加成反应)
②选择性:只能漂白品红,不能漂白其他指示剂
③暂时性:生成物不稳定,加热或长时间放置会恢复原色
二、三氧化硫的结构和性质
1.物理性质
(1)熔沸点:熔点为16.8℃,沸点为44.8℃
(2)颜色状态
①常温常压下为无色、易挥发的液体
②标准状况下,冷凝成为无色晶体
(3)溶解性:易溶于水,能够被98 .3 %的浓硫酸 完全吸收
2.化学性质:酸性氧化物的通性
(1)与水反应
①反应:SO +H O HSO (工业生产硫酸)
3 2 2 4
②特点:反应放出大量的热
(2)与碱(如NaOH)反应
①少量SO :SO +2NaOH Na SO +H O
3 3 2 4 2
②过量SO :SO +NaOH NaHSO
3 3 4
(3)与碱性氧化物反应
①CaO: CaO + SO CaSO
3 4
②NaO:SO +Na O NaSO
2 3 2 2 4
(4)与某些弱酸盐反应
①NaCO 溶液:Na CO + SO + H O Na SO + CO ↑ + H O
2 3 2 3 3 2 2 4 2 2
②NaSO 溶液:Na S O + SO + H O Na SO +S O ↑ + H O
2 3 2 3 3 2 2 4 2 2
三、实验室制二氧化硫
1.反应原理及装置
(1)装置类型:“固体+固体 气体”型
①方法:Cu与浓HSO 混合加热
2 4
②反应:Cu+2H SO ( 浓 ) CuSO +SO ↑ +2H O
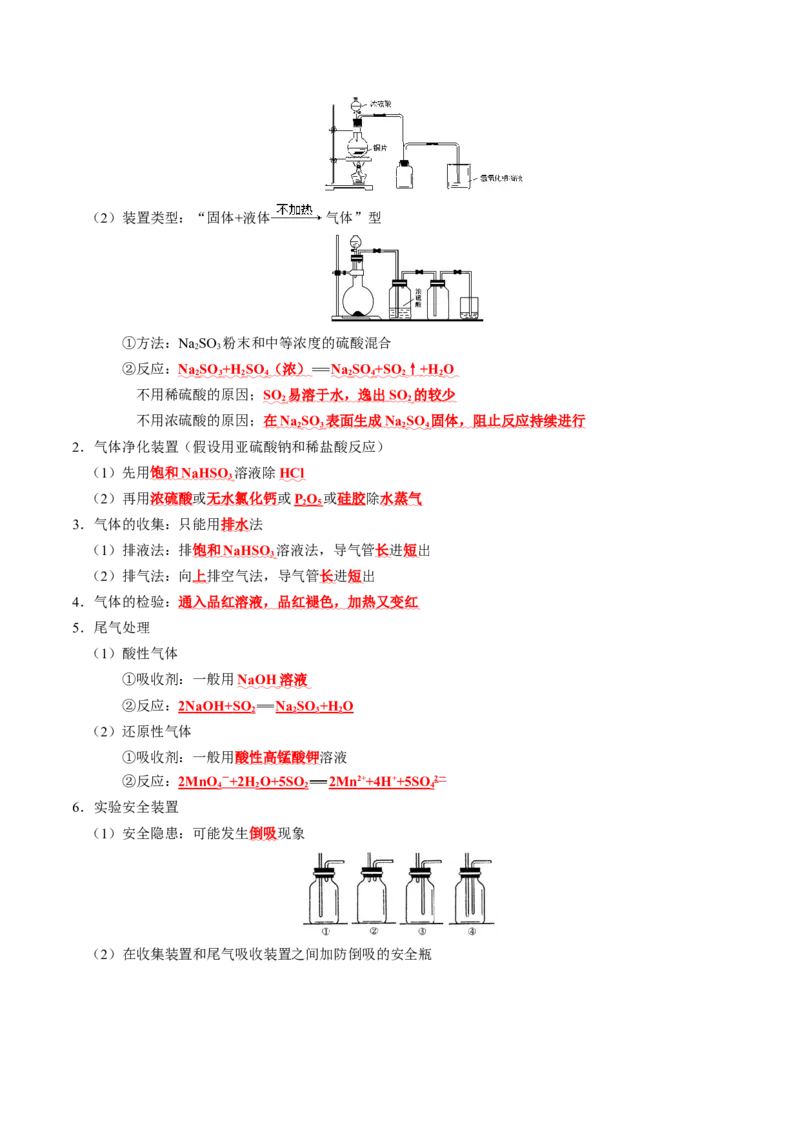
2 4 4 2 2(2)装置类型:“固体+液体 气体”型
①方法:NaSO 粉末和中等浓度的硫酸混合
2 3
②反应:Na SO +H SO ( 浓 ) Na SO +SO ↑ +H O
2 3 2 4 2 4 2 2
不用稀硫酸的原因;SO 易溶于水 , 逸出 SO 的较少
2 2
不用浓硫酸的原因; 在 N a SO 表面生成 N a SO 固体 , 阻止反应持续进行
2 3 2 4
2.气体净化装置(假设用亚硫酸钠和稀盐酸反应)
(1)先用 饱和 NaHSO 溶液除HCl
3
(2)再用浓硫酸或无水氯化钙或PO 或硅胶除水蒸气
2 5
3.气体的收集:只能用排水法
(1)排液法:排 饱和 NaHSO 溶液法,导气管长进短出
3
(2)排气法:向上排空气法,导气管长进短出
4.气体的检验:通入品红溶液,品红褪色,加热又变红
5.尾气处理
(1)酸性气体
①吸收剂:一般用 NaOH 溶液
②反应: 2NaOH + SO Na SO + H O
2 2 3 2
(2)还原性气体
①吸收剂:一般用酸性高锰酸钾溶液
②反应:2MnO - + 2 H O+ 5SO 2Mn 2+ +4H + + 5 SO 2-
4 2 2 4
6.实验安全装置
(1)安全隐患:可能发生倒吸现象
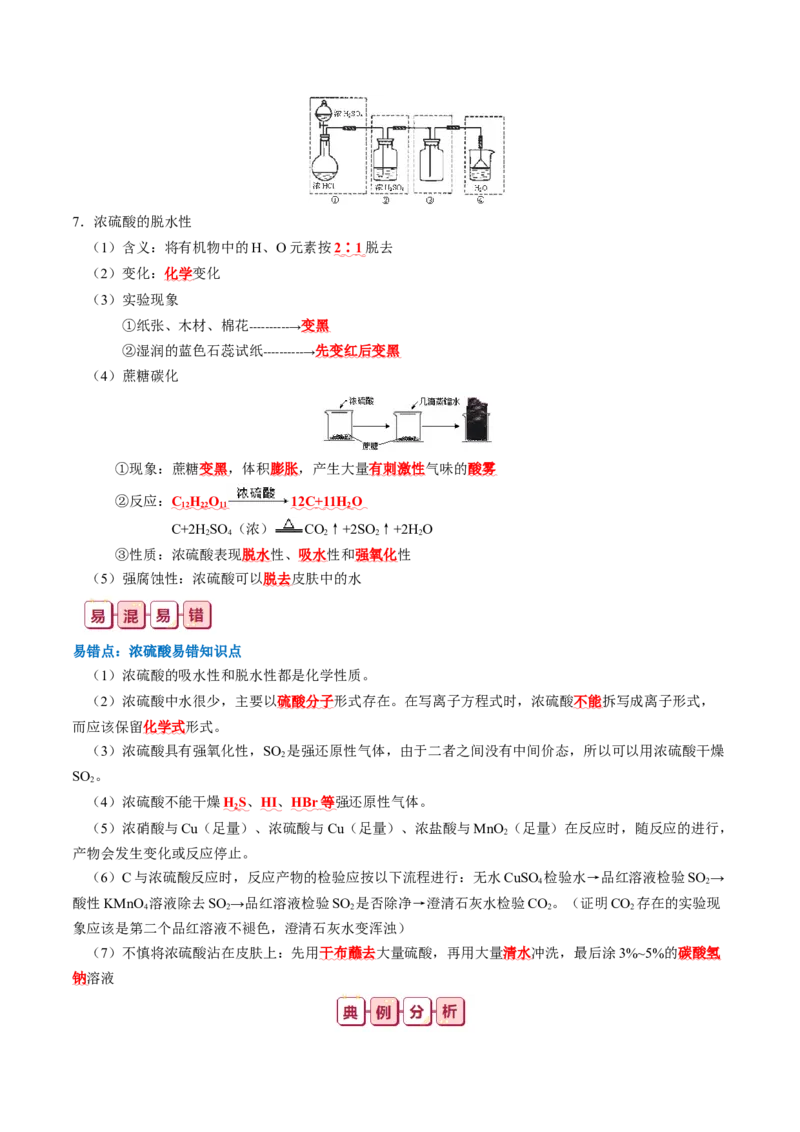
(2)在收集装置和尾气吸收装置之间加防倒吸的安全瓶7.检验碳与浓硫酸反应所有气体产物
(1)各仪器中的试剂及其作用
①A:CuSO 粉末,检验产生的水蒸气
4
②B:品红溶液, 检验产生的 SO 气体
2
③C: 酸性 KMnO 溶液或溴水, 除去 SO 气体
4 2
④D:品红溶液, 检验 SO 能否完全除去
2
⑤E:澄清石灰水, 检验产生的 C O 气体
2
(2)证明有CO 气体的现象
2
①当 D 中品红溶液不褪色 , E 中澄清石灰水变浑浊时 ,说明产物中CO 气体
2
②若把装置D去掉,当 C 中溶液颜色未完全褪去 , E 中澄清石灰水变浑浊时 ,说明产物中有CO
2
气体
易错点1:二氧化硫漂白性的易错知识点
(1)SO 不能漂白酸碱指示剂,向石蕊试液中通入SO 的现象是溶液变红,但不褪色
2 2
(2)SO 使溴水、酸性高锰酸钾溶液褪色,体现的是SO 的还原性,而不是漂白性
2 2
(3)SO 显红色的酚酞试液褪色,体现的是SO 是一种酸性气体,与碱反应,而不是漂白性
2 2
(4)SO 与氧化性漂白剂混合,会发生氧化还原反应,漂白性减弱
2
易错点2:三类漂白剂的区别
类型 原理 举例 特点 备注
HClO、NaClO、Ca
将有机色质内部“生色团”破 不可逆、持 无选
氧化型 (ClO) 、NaO 、
2 2 2
坏掉 久 择性
HO、O 等
2 2 3
与有机色质内部“生色团” 可逆、不持 有选
加合型 SO
2
“化合”成无色物质 久 择性
吸附
吸附型 将有色物质吸附而退色 活性炭 物理变化
色素
易错点3:二氧化硫和某些盐溶液反应的原理
(1)把SO 气体通入BaCl 溶液中,没有BaSO 沉淀生成
2 2 3
(2)把SO 气体通入BaCl 溶液中,再通入NH 或加入NaOH溶液,有BaSO 沉淀生成
2 2 3 3(3)Ba(NO ) 产生BaSO 沉淀。
3 2 4
(4)Ca(ClO) 产生CaCO 沉淀;Ca(ClO) 产生 Ca SO 沉淀。
2 3 2 4
【典例03】(2021·北京等级考)室温下,1体积的水能溶解约40体积的SO 。用试管收集SO 后进行如下
2 2
实验。对实验现象的分析正确的是( )。
A.试管内液面上升,证明SO 与水发生了反应
2
B.试管中剩余少量气体,是因为SO 的溶解已达饱和
2
C.取出试管中的溶液,立即滴入紫色石蕊试液,溶液显红色,原因是:SO +H O HSO 、HSO
2 2 2 3 2 3
H++HSO -、HSO - H++SO 2-
3 3 3
D.取出试管中溶液,在空气中放置一段时间后pH下降,是由于SO 挥发
2
【解析】选C。由信息可知,SO 易溶于水,也能使液面上升,故A错误;二氧化硫与水的反应为可逆反
2
应,当反应达到限度后,二氧化硫的量不再减少,液面高度也无明显变化,故 B错误;滴入石蕊试液,溶
液变为红色,说明溶液显酸性,SO 与水反应生成亚硫酸,亚硫酸为弱酸,分步电离出氢离子,故C正确;
2
亚硫酸具有较强的还原性,易被氧化为硫酸,弱酸变强酸,也能使pH下降,故D错误。
【典例04】(2023•上海松江区模拟)某学生对SO 与漂粉精的反应进行实验探究,下列叙述错误的是(
2
)。
操作 现象
①取4g漂粉精固体,加入100mL 部分固体溶解,溶液略有颜色
水
②过滤,测漂粉精溶液的pH pH试纸先变蓝,最后褪色
液面上方出现白雾;稍后,出
现浑浊,溶液变为黄绿色;最
③ 终,产生大量白色沉淀,黄绿
色褪去
A.Cl 和Ca(OH) 制取漂粉精的化学方程式是:2Cl+2Ca(OH)=CaCl +Ca(ClO)+2H O
2 2 2 2 2 2 2
B.pH试纸颜色的变化说明漂粉精溶液具有碱性、漂白性
C.液面上方出现白雾,白雾中一定只含HCl
D.最后,产生大量白色沉淀,黄绿色褪去,推测白色沉淀主要是CaSO
4
【解析】选C。Cl 和Ca(OH) 反应生成氯化钙、次氯酸钙和水,化学方程式为:2Cl+2Ca(OH)=
2 2 2 2
CaCl +Ca(ClO)+2H O,故A正确;次氯酸钙为强碱弱酸盐,水解显碱性,水解生成的次氯酸具有漂白
2 2 2
性,所以pH试纸先变蓝,最后褪色,故B正确;液面上方出现白雾,白雾中除了含有HCl外还含有通入
的为反应的二氧化硫,故C错误;亚硫酸钙被氯气氧化成硫酸钙,故D正确。
【典例05】(2023·山西省重点高中联考)利用如图装置可制取二水亚硫酸铜(I,II)(Cu SO ·CuSO ·2HO)。下列说法错误的是( )。
2 3 3 2
A.滴加浓硫酸前需先打开止水夹K
B.装置①中NaSO 可换成铜屑
2 3
C.装置②加热时宜采用热水浴
D.装置③中的NaOH溶液可防止尾气污染
【解析】选B。滴加浓硫酸前若不打开止水夹K,则滴加过程中烧瓶内气体的压强增大,浓硫酸难以顺利
流下,A正确;装置①中NaSO 不可换成铜屑,因为铜与浓硫酸在常温下不反应,不能生成SO ,B错误;
2 3 2
装置②的加热温度为60~80℃,可以采用热水浴,C正确;SO 为酸性气体,能被NaOH溶液吸收,装置③
2
中的NaOH溶液可防止尾气污染,D正确。
知识点 03 亚硫酸、亚硫酸盐和硫代硫酸盐
1.亚硫酸的性质
(1)弱酸性:H S O H + + H S O -
2 3 3
①相对强弱:酸性比碳酸的强
②实验验证:饱和NaHCO 溶液中通入足量SO,将产生的气体先通过足量的酸性高锰酸钾溶液,
3 2
溶液未完全褪色,再将剩余气体通入澄清石灰水中,溶液变浑浊,则可说明亚硫酸的酸性比碳酸的强
(2)不稳定性:HSO SO ↑ +H O
2 3 2 2
(3)强还原性
①O:2HSO +O 2HSO (HSO 密封保存)
2 2 3 2 2 4 2 3
②Cl:Cl +H SO +H O HSO +2HCl
2 2 2 3 2 2 4
(4)弱氧化性:2H S+ H SO 3S ↓ +3H O
2 2 3 2
2.亚硫酸钠的性质
(1)弱碱性: S O 2 - +H O H S O - +OH -
3 2 3
(2)强还原性:Cl+Na SO +H O NaSO +2HCl
2 2 3 2 2 4
(3)弱氧化性:2NaS+Na SO +3H SO 3NaSO +3S↓+3H O
2 2 3 2 4 2 4 2
3.亚硫酸钠在空气中变质
(1)变质反应:2Na SO +O 2Na SO
2 3 2 2 4
(2)保存方法:密封保存
(3)实验验证:取样→加水溶解→加入足量BaCl 溶液→加入足量盐酸溶液
2
①完全变质:产生的白色沉淀不溶解②没有变质:产生的白色沉淀全部溶解
③部分变质:产生的白色沉淀部分溶解
4.硫代硫酸钠与稀硫酸反应
(1)化学:NaSO+H SO NaSO +S ↓ +SO ↑ +H O
2 2 3 2 4 2 4 2 2
(2)离子:SO 2 - + 2 H + S ↓ +SO ↑ +H O
2 3 2 2
(3)应用:通过测定单位时间内产生沉淀的质量探究外界条件对化学反应速率从影响
易错点:亚硫酸盐的易错点
(1)NaSO 具有强还原性,在空气中加热蒸干NaSO 溶液,最终得到Na SO 固体。
2 3 2 3 2 4
(2)SO 2-和S2-能够大量共存,但是在酸性条件下不能大量共存:2S2-+SO2-+6H+ 3S↓+3H O。
3 3 2
【典例06】(2023·聊城二模)为探究NaSO 溶液的性质,在白色点滴板的a、b、c、d四个凹槽中滴入
2 3
NaSO 溶液,再分别滴加下图所示的试剂:
2 3
对实验现象的“解释或结论”错误的是( )。
选项 实验现象 解释或结论
A a中溴水褪色 还原性:SO 2->Br-
3
b中加硫酸后产生淡黄 SO 2-和S2-在酸性条件下发生
3
B
色沉淀 反应
c中滴入酚酞溶液变 SO 2-+H O HSO -+OH
3 2 3
红,再加BaCl 溶液后 -,所以滴入酚酞变红;Ba2+
2
C
产生白色沉淀且红色 +SO2-=BaSO↓(白),使
3 3
褪去 水解平衡左移,红色褪去
D d中产生白色沉淀 NaSO 溶液已被氧化变质
2 3
【解析】选D。a中滴入溴水后褪色,说明亚硫酸钠具有还原性,被溴单质氧化为硫酸钠,A选项正确;b
中是滴入硫化钠溶液和稀硫酸,硫离子和亚硫酸根离子发生氧化还原反应生成淡黄色沉淀单质硫,发生反
应的离子方程式是:SO 2-+2S2-+6H+=3S↓+3H O,B选项正确;c中滴入酚酞溶液变红,再加入BaCl 溶
3 2 2
液后产生沉淀且红色褪去,在NaSO 溶液中,SO 2-水解显碱性:SO 2-+H O HSO -+OH-,所以滴
2 3 3 3 2 3
入酚酞后溶液变红;在该溶液中加入BaCl 后,Ba2++SO2-=BaSO↓(白色),水解平衡左移,氢氧根离
2 3 3
子浓度减小,红色褪去,C选项正确;d中无论是亚硫酸钠是被氧化还是未被氧化都会产生白色沉淀,D
选项错误。
【典例07】(2021·辽宁省选择考)含S元素的某钠盐a能发生如图转化。下列说法错误的是( )。A.a可能为正盐,也可能为酸式盐
B.c为不溶于盐酸的白色沉淀
C.d为含极性键的非极性分子
D.反应②中还可能生成淡黄色沉淀
【解析】选C。由题干信息可知,盐a与足量的稀盐酸产生刺激性气味气体d,d能使KMnO 溶液褪色,
4
故d为SO ,则盐a为NaSO 或者NaHSO,也可能是NaSO,盐a与足量Cl 反应后将生成SO 2-,与
2 2 3 3 2 2 3 2 4
BaCl 溶液反应得到沉淀c,故c为BaSO。由分析可知,盐a为NaSO 或者NaHSO,也可能是NaSO,
2 4 2 3 3 2 2 3
故a可能为正盐,也可能为酸式盐,A正确;由分析可知,c为BaSO,故c为不溶于盐酸的白色沉淀,B
4
正确;由分析可知,d为SO ,由SO 易溶于水并根据“相似相溶”原理可知,d是含有极性键的极性分子,
2 2
C错误;由分析可知,盐a为NaSO 或者NaHSO,也可能是NaSO,当NaSO+2HCl
2 3 3 2 2 3 2 2 3
2NaCl+S↓+SO↑+H O,反应②中还可能生成淡黄色沉淀,D正确。
2 2
知识点 04 浓硫酸的性质与应用
1.硫酸的结构
(1)S原子杂化方式: sp 3 杂化
(2)化学键:含2 个配位键,提供孤对电子的是硫原子
(3)SO 2-的空间构型:正四面体形
4
(4)SO 2-的等电子体
4
①分子:SiF、CCl 、CF、SiCl
4 4 4 4
②阴离子:ClO-、SO 2-、PO 3-、SiO4-、BF-
4 4 4 4 4
2.物理性质
(1)色、态:无色黏稠状液体
(2)溶解性:以 任意 比 和水互溶,同硝酸、乙醇
①原因:浓硫酸与水分子之间可以形成氢键
②热效应:溶解时放出大量的热
③稀释:将浓硫酸沿玻璃棒缓慢倒入水中,边加边搅拌
(3)沸点:338℃,具有难挥发性,原因是:浓硫酸中存在分子间氢键
(4)浓度和密度
①常用浓硫酸浓度为98.3%,密度1.84g/cm3,物质的量浓度为18.4mol/L
②浓硫酸中水很少,主要以硫酸分子形式存在③在写离子方程式时,浓硫酸不能拆写成离子形式,而应该保留化学式形式
④氨气通入浓硫酸的现象是:产生白色沉淀,不能用浓硫酸作为氨气的吸收剂,否则易堵塞导气
管
3.浓硫酸与金属单质反应
(1)铝和铁与浓硫酸反应,条件不同,反应不同
①Al、Fe----------→钝化(表现强氧化性)
②Al、Fe----------→剧烈反应,生成硫酸盐和SO 气体(表现酸性和强氧化性)
2
(2)Au、Pt----------→不反应
(3)氢前的活泼金属(如Zn)与浓硫酸常温反应,先放出SO 气体,后放出H
2 2
① Zn+2 H SO ( 浓 ) Zn SO + SO ↑ + 2H O(表现酸性和强氧化性)
2 4 4 2 2
②Zn+H SO (稀) ZnSO +H ↑(表现酸性和氧化性)
2 4 4 2
(4)氢后的不活泼金属(如Cu)与浓硫酸加热反应,先放出SO 气体,后反应停止
2
①化学方程式:Cu+2H SO (浓) CuSO +SO ↑ +2H O(表现酸性和强氧化性)
2 4 4 2 2
②离子方程式:Cu+2H SO (浓) CuSO +SO↑+2H O(不能拆)
2 4 4 2 2
4.浓硫酸与碳等非金属单质加热反应
(1)过程:C----------→先放CO 和 SO 气体,后反应停止
2 2
(2)反应:C+2H SO (浓) CO ↑ +2SO ↑ +2H O(表现强氧化性)
2 4 2 2 2
5.浓硫酸与还原性化合物反应:浓HSO ---------------------→SO
2 4 2
(1)HS+HSO (浓) S+SO ↑+2HO(表现强氧化性)
2 2 4 2 2
(2)2HI+HSO (浓) I+SO ↑+2HO(表现强氧化性)
2 4 2 2 2
(3)2NaBr+2HSO (浓) NaSO +Br ↑+SO ↑+2HO(表现酸性、强氧化性)
2 4 2 4 2 2 2
(4)2FeO+4HSO (浓) Fe (SO )+SO ↑+4HO(表现酸性、强氧化性)
2 4 2 4 3 2 2
6.浓硫酸的吸水性
(1)含义:吸收自由水或结晶水
(2)变化:化学变化(形成HSO ·xHO)
2 4 2
(3)作干燥剂,不能干燥四种气体
①强还原性气体:HS、HI、HBr
2
②碱性气体:NH
3
(4)浓盐酸和浓硫酸混合制备HCl
①少量:将浓盐酸滴加入浓硫酸中
②大量:将浓硫酸加入浓盐酸中7.浓硫酸的脱水性
(1)含义:将有机物中的H、O元素按 2 ∶ 1 脱去
(2)变化:化学变化
(3)实验现象
①纸张、木材、棉花----------→变黑
②湿润的蓝色石蕊试纸----------→先变红后变黑
(4)蔗糖碳化
①现象:蔗糖 变 黑 ,体积膨胀,产生大量有刺激性气味的酸雾
②反应:C H O 12C + 11H O
12 22 11 2
C+2H SO (浓) CO↑+2SO↑+2H O
2 4 2 2 2
③性质:浓硫酸表现脱水性、吸水性和强氧化性
(5)强腐蚀性:浓硫酸可以脱去皮肤中的水
易错点:浓硫酸易错知识点
(1)浓硫酸的吸水性和脱水性都是化学性质。
(2)浓硫酸中水很少,主要以硫酸分子形式存在。在写离子方程式时,浓硫酸不能拆写成离子形式,
而应该保留化学式形式。
(3)浓硫酸具有强氧化性,SO 是强还原性气体,由于二者之间没有中间价态,所以可以用浓硫酸干燥
2
SO 。
2
(4)浓硫酸不能干燥HS、HI、 HBr 等 强还原性气体。
2
(5)浓硝酸与Cu(足量)、浓硫酸与Cu(足量)、浓盐酸与MnO (足量)在反应时,随反应的进行,
2
产物会发生变化或反应停止。
(6)C与浓硫酸反应时,反应产物的检验应按以下流程进行:无水CuSO 检验水→品红溶液检验SO →
4 2
酸性KMnO 溶液除去SO →品红溶液检验SO 是否除净→澄清石灰水检验CO。(证明CO 存在的实验现
4 2 2 2 2
象应该是第二个品红溶液不褪色,澄清石灰水变浑浊)
(7)不慎将浓硫酸沾在皮肤上:先用干布蘸去大量硫酸,再用大量清水冲洗,最后涂3%~5%的碳酸氢
钠溶液【典例08】(2023·山西阳泉二模)向浓硫酸中分别加入下列三种固体,对实验现象的分析正确的是(
)。
A.对比实验①和②可知还原性:Br->Cl-
B.对比实验①和③可知氧化性:Br >SO
2 2
C.对比实验②和③可知酸性:HSO >HCl>HSO
2 4 2 3
D.由实验可知浓硫酸具有强酸性、难挥发性、氧化性、脱水性
【解析】选A。实验①生成棕色气体是溴蒸气,实验②白雾是氯化氢,说明浓硫酸能将溴离子氧化成溴单
质,而不能将氯离子氧化成氯气,与同一种氧化剂在相同条件下反应,溴离子被氧化成溴单质,而氯离子
不能被氧化,说明还原性:Br->Cl-,A正确;实验③生成是二氧化硫气体,非氧化还原反应,而且亚硫
酸钠与溴化钠不是同一类型,所以不能比较Br 、SO 的氧化性,B错误;实验②白雾说明氯化氢易挥发,
2 2
不能说明酸性HSO >HCl,而实验③生成是二氧化硫气体,非氧化还原反应,而是强酸制弱酸,能说明
2 4
HSO >HSO ,C错误;实验中不能得知浓硫酸具有脱水性,D错误。
2 4 2 3
【典例09】某小组同学用如图装置进行铜与浓硫酸反应时,发现试管中有黑色物质产生。同学猜测,黑色
物质中可能含有CuO、Cu S和CuS,针对产生的黑色物质,该小组同学继续进行实验探究,获得数据如表。
2
下列说法不正确的是( )。
黑色物质出现的温度 黑色物质消失的温度
硫酸浓度/mol·L﹣1
∕℃ ∕℃
15 约150 约236
16 约140 约250
18 约120 不消失
A.硫酸浓度越大,黑色物质越易出现、越难消失
B.黑色物质消失过程中有SO 、HS生成
2 2
C.硫酸浓度为16mol·L﹣1时,先升温至250℃以上,再将铜丝与浓硫酸接触,可以避免产生黑色物质
D.取黑色物质洗涤、干燥后,加稀硫酸充分混合,固体质量不变,说明黑色物质中不含CuO
【解析】选B。从表中数据可以看出,硫酸浓度越大,黑色物质出现的温度越低,黑色物质不消失,说明
硫酸浓度越大,黑色物质越易出现、越难消失,故A正确;由于浓硫酸有氧化性,会将硫化氢氧化,根据
分析可知,黑色物质消失过程中有SO 生成,HS不存在,故B错误;由表格中数据可知,硫酸浓度为
2 2
16mol·L﹣1时,黑色固体消失的温度在250℃,先升温至250℃以上,再将铜丝与浓硫酸接触,可以避免产生黑色物质,故C正确;黑色物质中若含CuO,加入加稀硫酸充分混合,氧化铜会与稀硫酸反应生成硫
酸铜和水,硫酸铜溶于水,固体质量会减小,现固体质量不变,说明黑色物质中不含CuO,故D正确。
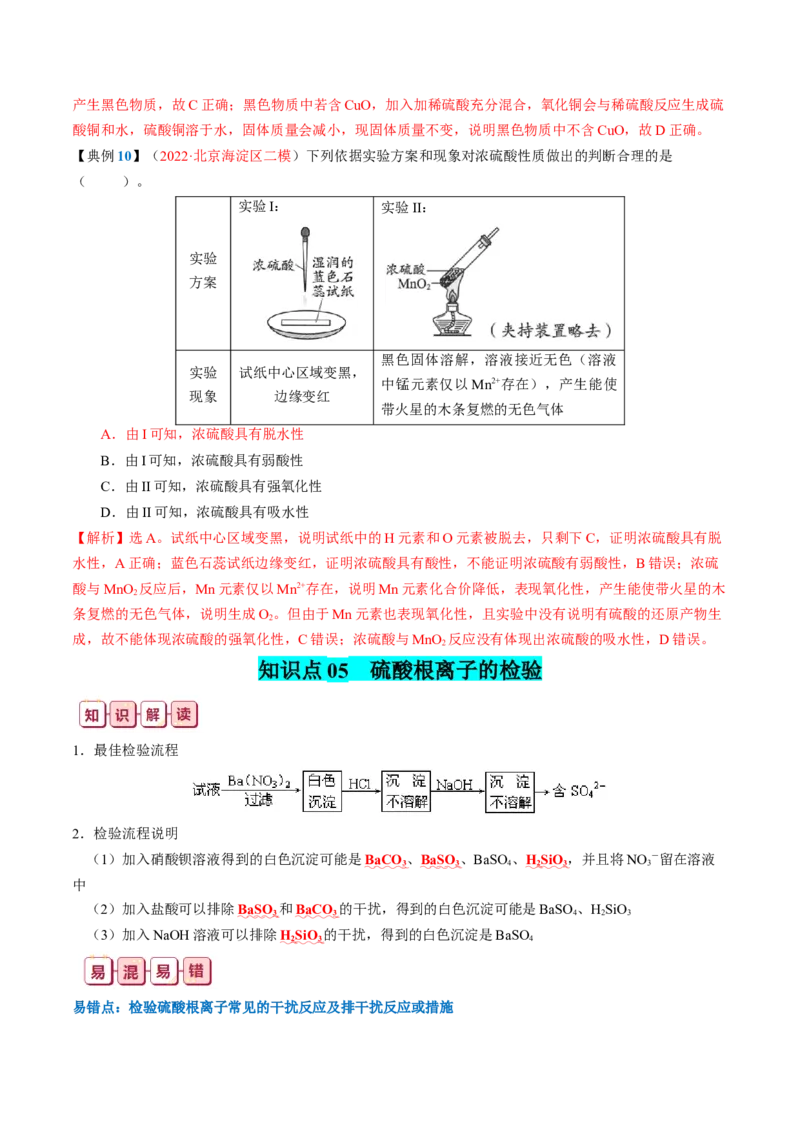
【典例10】(2022·北京海淀区二模)下列依据实验方案和现象对浓硫酸性质做出的判断合理的是
( )。
实验I: 实验II:
实验
方案
黑色固体溶解,溶液接近无色(溶液
实验 试纸中心区域变黑,
中锰元素仅以Mn2+存在),产生能使
现象 边缘变红
带火星的木条复燃的无色气体
A.由I可知,浓硫酸具有脱水性
B.由I可知,浓硫酸具有弱酸性
C.由II可知,浓硫酸具有强氧化性
D.由II可知,浓硫酸具有吸水性
【解析】选A。试纸中心区域变黑,说明试纸中的H元素和O元素被脱去,只剩下C,证明浓硫酸具有脱
水性,A正确;蓝色石蕊试纸边缘变红,证明浓硫酸具有酸性,不能证明浓硫酸有弱酸性,B错误;浓硫
酸与MnO 反应后,Mn元素仅以Mn2+存在,说明Mn元素化合价降低,表现氧化性,产生能使带火星的木
2
条复燃的无色气体,说明生成O。但由于Mn元素也表现氧化性,且实验中没有说明有硫酸的还原产物生
2
成,故不能体现浓硫酸的强氧化性,C错误;浓硫酸与MnO 反应没有体现出浓硫酸的吸水性,D错误。
2
知识点 05 硫酸根离子的检验
1.最佳检验流程
2.检验流程说明
(1)加入硝酸钡溶液得到的白色沉淀可能是 B aCO 、 B a S O 、BaSO、HSiO ,并且将NO -留在溶液
3 3 4 2 3 3
中
(2)加入盐酸可以排除 B a S O 和 B aCO 的干扰,得到的白色沉淀可能是BaSO、HSiO
3 3 4 2 3
(3)加入NaOH溶液可以排除HSiO 的干扰,得到的白色沉淀是BaSO
2 3 4
易错点:检验硫酸根离子常见的干扰反应及排干扰反应或措施(1)Ag+:Ag++Cl-=AgCl↓,不加氯化物
(2)CO2-:Ba2++CO 2- BaCO↓,CO2-+2H+ HO+CO↑,加盐酸排除
3 3 3 3 2 2
(3)SO2-:Ba2++SO2- BaSO↓,SO2-+2H+ HO+SO↑,加盐酸排除
3 3 3 3 2 2
(4)SiO2-:SiO2-+2H+ HSiO↓,HSiO+2OH- SiO2-+2HO,加NaOH溶液排除
3 3 2 3 2 3 3 2
(5)SO2-和NO -:3SO 2-+2H++2NO - 3SO2-+2NO↑+HO,溶液中不能同时含H+和NO -
3 3 3 3 4 2 3
【典例11】(2023·沧州模拟)下列过程中,最终的白色沉淀不一定是BaSO 的是( )。
4
A.Fe(NO ) 白色沉淀
3 2
B.Ba(NO ) 白色沉淀
3 2
C.无色溶液 白色沉淀
D.无色溶液 无沉淀 白色沉淀
【解析】选C。A选项中,Fe(NO ) 中加入盐酸后,相当于产生了硝酸(硝酸亚铁电离出NO -,HCl电
3 2 3
离出H+,NO -和H+组成硝酸)。硝酸将二氧化硫氧化为硫酸:3SO +2HNO +2H O=3HSO +2NO,硫酸
3 2 3 2 2 4
和氯化钡溶液生成硫酸钡沉淀:BaCl +H SO =BaSO↓+2HCl,此沉淀一定是硫酸钡。B选项中,Ba
2 2 4 4
(NO ) 中加入盐酸后,相当于产生了硝酸(硝酸钡电离出NO -,HCl电离出H+,NO -和H+组成硝酸)。
3 2 3 3
硝酸可以将NaSO 氧化为硫酸钠:2HNO+3Na SO =3NaSO ↓+2NO↑+H O,硫酸钠溶液和硝酸钡溶液生
2 3 3 2 3 2 4 2
成硫酸钡沉淀:NaSO +Ba(NO )=BaSO↓+2NaNO ,此沉淀一定是硫酸钡。C选项中,无色溶液中可
2 4 3 2 4 3
能含有Cl-,最后得到的沉淀可能是氯化银沉淀,Cl-+Ag+=AgCl↓。D选项中,加入盐酸无沉淀,说明不
存在Ag+,加入氯化钡溶液后出现沉淀,则此沉淀一定是硫酸钡沉淀。