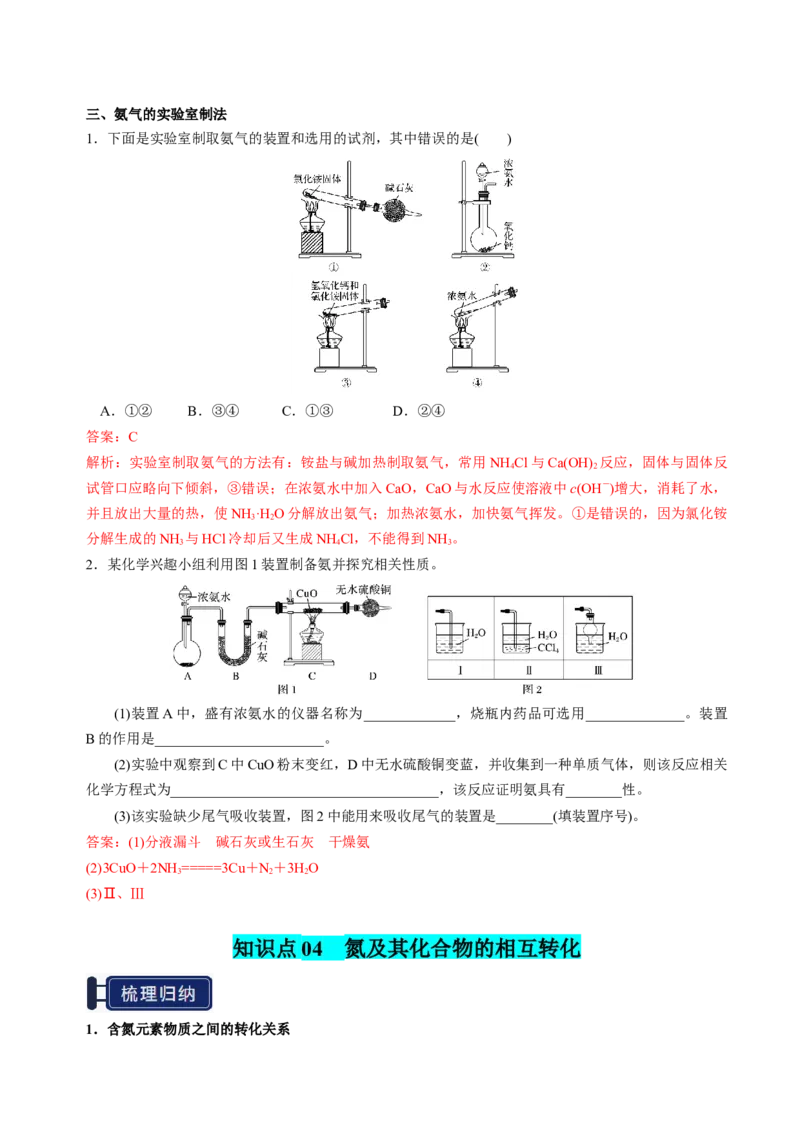
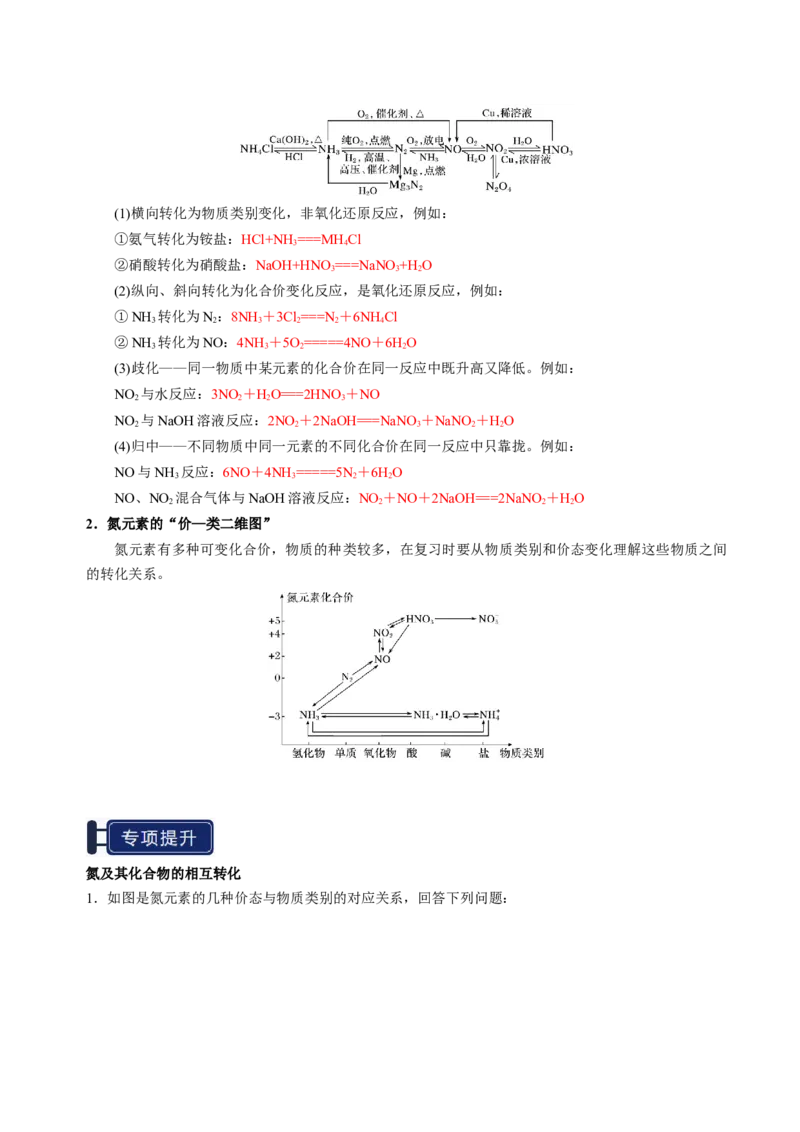
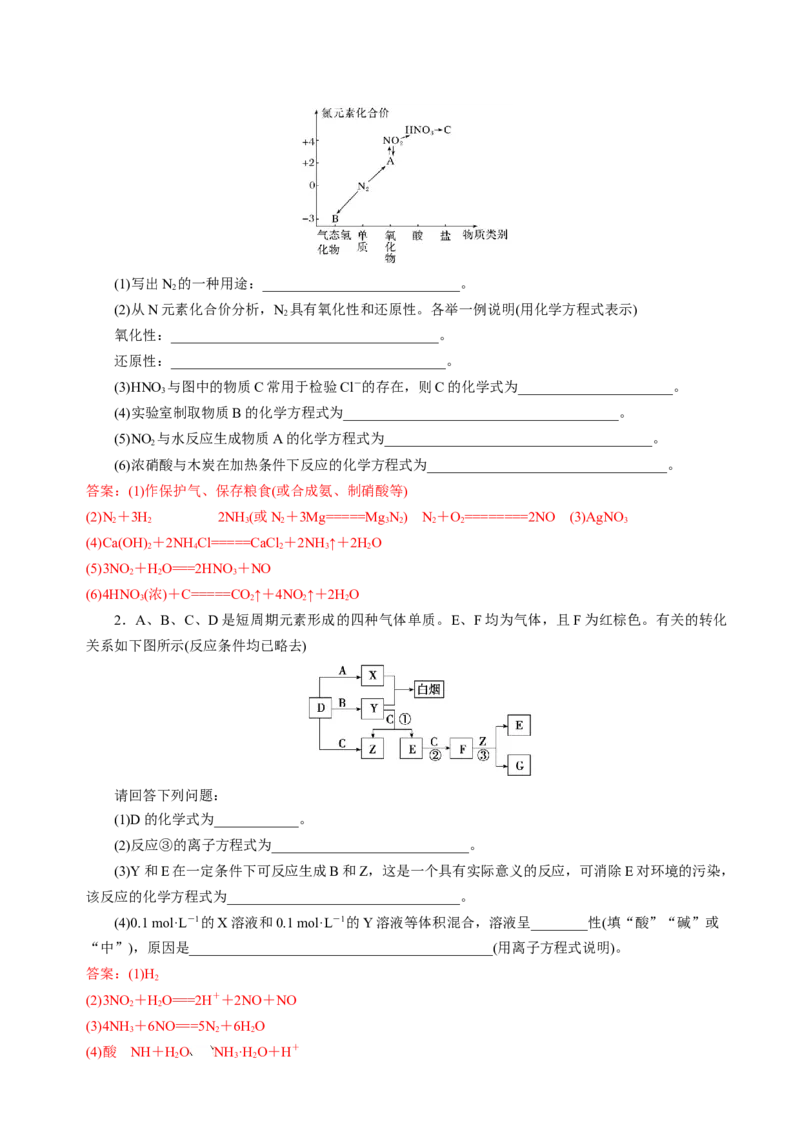
文档内容
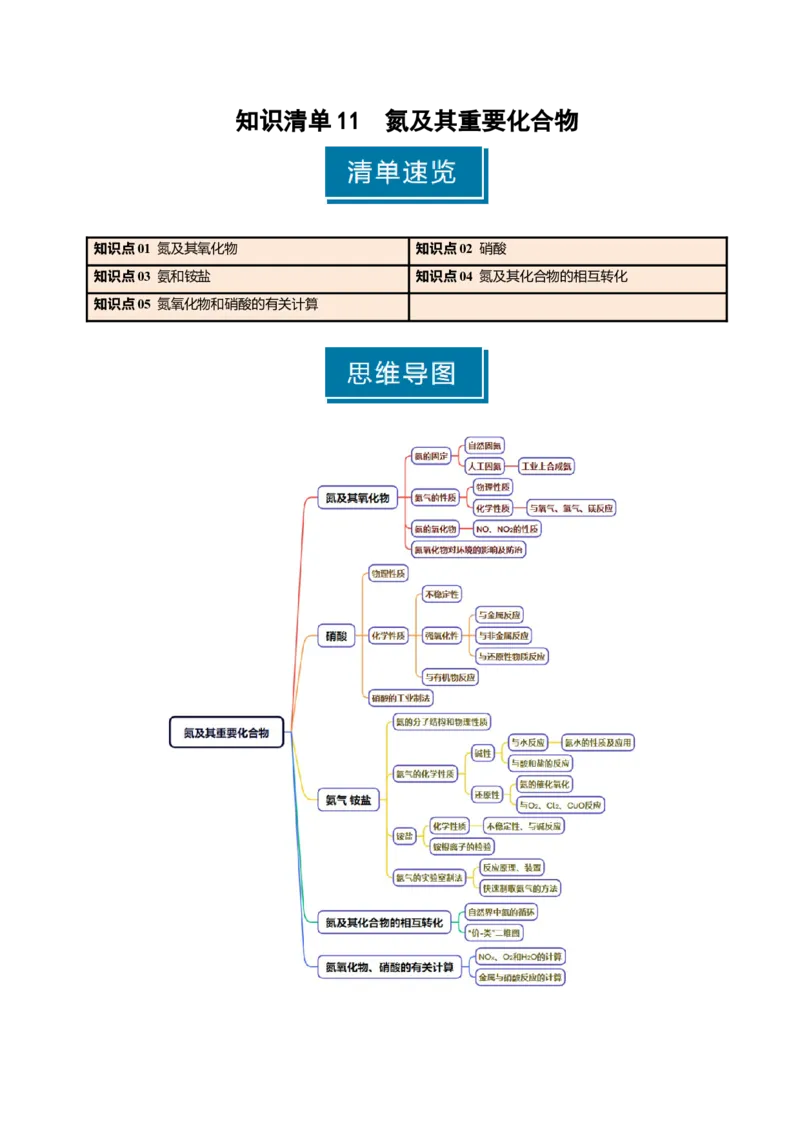
知识清单 11 氮及其重要化合物
知识点01 氮及其氧化物 知识点02 硝酸
知识点03 氨和铵盐 知识点04 氮及其化合物的相互转化
知识点05 氮氧化物和硝酸的有关计算知识点 01 氮及其氧化物
1.氮元素的存在和氮的固定
(1)氮元素的存在
游离态:N(空气中体积分数约为78%)
2
化合态:动植物体内的蛋白质中,还有部分存在于土壤、海洋里的硝酸盐和铵盐中。
(2)氮的固定
①含义:将大气中游离态的氮转化为氮的化合物的过程。
②分类:
氮的固定
2.氮气分子结构和性质
(1)氮分子的结构
氮气分子的电子式为 ,结构式为N≡N。
(2)氮气的化学性质
①与O 化合:N+O=========2NO。
2 2 2
②镁在氮气中燃烧:3Mg+N=====MgN。
2 3 2
③与氢气化合:N+3H2NH ;应用:工业上合成氨。
2 2 3
(3)用途
①氮气常用作保护气,如焊接金属、填充灯泡、保存食品等。
②氮气是合成氨、制硝酸的重要原料。
③液氮可用作制冷剂,应用于医学、科技等领域。
3.氮的氧化物
(1)氮的氧化物
N的化合价 +1 +2 +3 +4 +5
对应氧化物 NO(笑气) NO NO NO 、NO NO
2 2 3 2 2 4 2 5
其中属于酸性氧化物的是NO 和NO,对应的酸分别是HNO(亚硝酸)和HNO。
2 3 2 5 2 3
(2)NO和NO 的比较
2
性质 NO NO
2
色、态、味 无色、无味的气体 红棕色、有刺激性气味的气体
溶解性 难溶于水 与水反应
毒性 有毒,大气污染物之一 有毒,大气污染物之一
与水反应 不反应 3NO +HO===2HNO+NO
2 2 3
与氧气反应 2NO+O===2NO 不反应
2 2(3)NO 的收集和检验
x
①NO采用排水法收集,不用排空气法收集;NO 采用排空气法收集,不用排水法收集。
2
②NO的检验:通入O(或空气),无色气体变为红棕色。
2
4.氮氧化物对环境的污染及防治
(1)氮氧化物的来源
氮氧化物(NO )主要包括NO和NO 。化石燃料的燃烧、硝酸生产和机动车辆尾气的排放是氮氧化
x 2
物的主要来源。
(2)氮氧化物的危害
①形成酸雨:
NO 形成酸雨的过程为3NO +HO=2HNO +NO(用化学方程式表示)。
2 2 2 3
②光化学烟雾
在日光照射下,NO 使氧气经过复杂的反应生成臭氧(O ),臭氧与空气中的一些碳氢化合物在紫外线
2 3
照射下发生作用后,产生了一种有毒的烟雾,人们称之为光化学烟雾。
③破坏臭氧层:NO 可使平流层中的臭氧减少,导致地面紫外线辐射量增加。
2
④NO与血红蛋白结合使人中毒。
(3)氮氧化物污染治理方法
①汽车尾气“催化转化法”:2CO+2NO=====2CO+N
2 2
②氨还原法:
6NO+4NH =====5N+6HO;6NO +8NH =====7N+12HO
3 2 2 2 3 2 2
③碱液吸收法:
2NO +2NaOH=NaNO+NaNO +HO;NO+NO +2NaOH=NaNO+HO
2 3 2 2 2 2 2
(1)固氮反应一定属于氧化还原反应(√)
提示:固氮是将大气中游离态的氮转化为氮的化合物的过程。
(2)N 与O 在放电条件下直接化合成NO (×)
2 2 2
错因:N 与O 在放电条件下生成NO。
2 2
(3)用向上排空气法收集铜粉与稀硝酸反应产生的气体(×)
错因:Cu与稀硝酸生成NO,NO与空气中的O 反应,不能用排空气法收集。
2
(4)NO 溶于水时,NO 是氧化剂,水是还原剂(×)
2 2
错因:NO 与HO反应,NO 既是氧化剂又是还原剂。
2 2 2
(5)可用NO 与水反应制取硝酸,故NO 是酸性氧化物(×)
2 2
错因:NO 与HO反应生成HNO 和NO,所以NO 不是酸性氧化物。
2 2 3 2
(6)CO、NO、NO 都是大气污染气体,在空气中都稳定存在(×)
2
错因:NO与氧气反应生成NO2。
(7)利用AgNO 溶液、CCl 和HO均可鉴别NO 和溴蒸气(√)
3 4 2 2
提示:NO 与水反应生成HNO 和NO,溶液呈无色,Br 溶于水得到呈黄色的溴水溶液,Br 与HO反应
2 3 2 2 2生成HBr和HBrO,HBr与反应生成淡黄色AgBr沉淀,NO 不溶于CCl ,Br 易溶于CCl 呈橙红色。
2 4 2 4
(8)NO 通入FeSO 溶液中,无明显现象(×)
2 4
错因:NO 与水反应生成HNO,HNO 具有强氧化性,能氧化Fe2+。
2 3 3
(8)可用湿润的淀粉碘化钾试纸鉴别NO 与溴蒸气(×)
2
错因:NO 与水反应生成HNO,HNO 具有强氧化性,能将KI氧化为I,Br2也能将KI氧化为I。
2 3 3 2 2
(9)一定条件下,1 mol N 可与3 mol H 充分反应反应生成NH ,转移的电子数为6N (×)
2 2 3 A
错因:氮气与氢气反应生成氨气是可逆反应。
(10)SO 、CO、NO 都是可形成酸雨的气体(×)
2 2 2
错因:SO 和NO 都是可形成酸雨的气体,CO 不能形成酸雨。
2 2 2
一、氮气的性质及应用
1.Mg能与空气中的O、N 和CO 反应。
2 2 2
(1)Mg与CO 反应的方程式为:2Mg+CO=====2MgO+C,该反应属于四种基本反应类型中的置换
2 2
反应。
(2)Mg与N 反应生成MgN。
2 3 2
①MgN 的电子式: ,Mg2+与N3-的半径大小为:Mg2+ ,剩余气体为NO。
(2)NO 和O 的混合气体通入水中
2 2
由3NO +HO===2HNO +NO和2NO+O===2NO,得总反应为4NO +O+2HO=== 4HNO。
2 2 3 2 2 2 2 2 3
① = ,恰好完全反应;
② < ,剩余气体为O;
2
③ > ,剩余气体为NO。
(3)NO、NO 和O 三种混合气体通入水中
2 2
先按3NO +HO===2HNO +NO计算出生成NO的体积,再加上原来混合气体中NO体积,再按(1)
2 2 3
计算。
2.电子守恒法
NO 转化为硝酸时失去电子,如果是NO 与O 的混合气体,则反应中O 得到的电子数与NO 失去的
x x 2 2 x
电子数相等。
4NO +O 和4NO+3O 从组成上均相当于2NO ,都与NO +HO===2HNO 等效;当NO、NO 、
2 2 2 2 5 2 5 2 3 2
O 的混合气体溶于水时利用混合气体中N、O原子个数比进行分析判断。
2
① < ,剩余气体为O;
2
② = ,恰好完全反应;
③ > ,剩余气体为NO。
二、金属与硝酸反应的计算
1.金属与硝酸反应的思维模型2.计算方法(以Cu与硝酸反应为例)
(1)原子守恒:
反应前所有的N元素只存在于HNO 中,反应后含N元素的物质有HNO 的还原产物(假设有NO 、
3 3 2
NO)和Cu(NO ),则有n(HNO) =n(NO )+n(NO)+n[Cu(NO )]。
3 2 3 消耗 2 3 2
(2)电子守恒:反应中失去电子的是参加反应的 Cu,Cu-2e-―→Cu2+;得到电子的是被还原的
HNO(假设还原产物为NO 、NO),NO+e-―→NO 、NO+3e-―→NO。根据得失电子守恒,则有
3 2 2
2n(Cu)=n(NO )+3n(NO)。
2
若将生成的氮的氧化物气体与一定量的氧气共同通入水中,氮的氧化物完全生成硝酸,由于开始反
应物为硝酸,中间生成了氮的氧化物,但最终又变回了硝酸,所以相当于铜失的电子最终由氧气得到,
则有2n(Cu)=n(O )。
2
(3)电荷守恒:
在Cu与HNO 反应后的溶液中,若HNO 不过量,阳离子只有Cu2+,阴离子只有NO(此类计算不考
3 3
虑HO电离出的极少量的H+、OH-);若HNO 过量,溶液中的阳离子有Cu2+和H+,阴离子只有NO。
2 3
则有①若HNO 不过量:n(NO)=2n(Cu2+);②若HNO 过量:n(NO)=2n(Cu2+)+n(H+)。
3 3
(4)离子方程式计算:
金属与硫酸、硝酸的混合酸反应时,由于硝酸盐中NO在硫酸提供H+的条件下能继续与金属反应,
故此类题目应用离子方程式来计算3Cu+8H++2NO===3Cu2++2NO↑+4HO。先作过量判断,然后根据
2
完全反应的金属或H+或NO进行相关计算,且要符合电荷守恒。
一、NO 与HO、O 反应的计算
x 2 2
1.有一充有20 mL NO和NO 混合气体的试管,倒置于盛有水的水槽中,充分反应后,仍有12 mL 无色
2
气体,则原混合气体中NO和NO 的体积之比为(气体体积均在相同状况下测得)2:3。
2
解析:二氧化氮和水反应生成硝酸和一氧化氮,一氧化氮和水不反应,所以,剩余的气体为一氧化氮,
设混合气体中二氧化氮的体积为V,则:
3NO +HO===2HNO +NO 气体体积减少
2 2 3
3 1 2
V 20 mL-12 mL=8 mL
所以V==12 mL,即二氧化氮的体积为12 mL,则原混合气体中一氧化氮的体积为20 mL-12 mL=8
mL,则原混合气体中NO和NO 的体积之比为8 mL∶12 mL=2∶3。
2
2.将盛有12 mL NO 和O 的混合气体的量筒倒立于水槽中,充分反应后,还剩余2 mL无色气体。
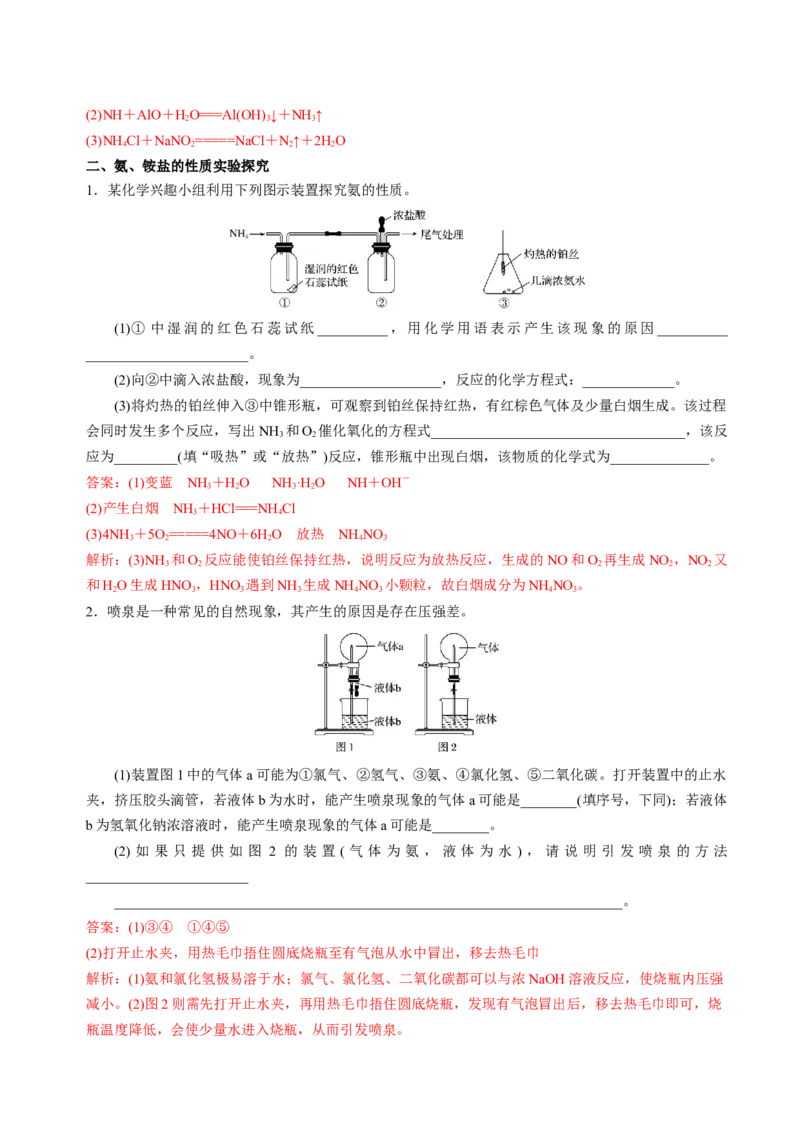
2 2(1)若剩余的气体是________,则NO 、O 的体积分别是________。
2 2
(2)若剩余的气体是________,则NO 、O 的体积分别是________。
2 2
答案:(1)O 8 mL、4 mL (2)NO 10.8 mL、1.2 mL
2
解析:解题依据的化学方程式:
4NO +O+2HO===4HNO ;
2 2 2 3
3NO +HO===2HNO +NO。
2 2 3
设O 的体积为x,剩余的气体有两种可能:
2
(1)若剩余O,则V =x-×(12 mL-x)=2 mL,
2 剩
解得x=4 mL,则NO 体积是8 mL;
2
(2)若剩余NO,则V =×[(12 mL-x)-4x]=2 mL,
剩
解得x=1.2 mL,则NO 体积是10.8 mL。
2
二、金属与硝酸反应的计算
1.将14 g铜银合金与足量的硝酸反应,放出的气体与标准状况下体积为1.12 L的O 混合后再通入水中,
2
恰好全部吸收,则合金中铜的质量为3.2 g。
解析:分析整个过程,金属失去的电子等于氧气获得的电子,标准状况下,n(O )==0.05 mol,设Cu、
2
Ag的物质的量分别为x、y,则根据质量列方程:x×64 g·mol-1+y×108 g·mol-1=14 g,根据得失电子守恒列
方程:2x+y=0.05 mol×4=0.2 mol,解得x=0.05 mol,y=0.1 mol,m(Cu)=0.05 mol×64 g·mol-1=3.2 g。
2.将3.84 g Cu和一定量的浓HNO 反应,当Cu反应完全时,共收集到气体2.24 L NO 和NO(标准状况,
3 2
不考虑NO 转化为NO),则反应中消耗HNO 的物质的量为0.22 mol。
2 2 4 3
解析:铜与硝酸反应转化为Cu(NO ) 、NO和NO ,根据铜原子守恒n[Cu(NO )]=n(Cu)==0.06 mol,
3 2 2 3 2
NO和NO 的物质的量共为n===0.1 mol,根据氮原子守恒:n(HNO)=2n[Cu(NO )]+n(NO)+n(NO )
2 3 3 2 2
=2×0.06 mol+0.1 mol=0.22 mol。