文档内容
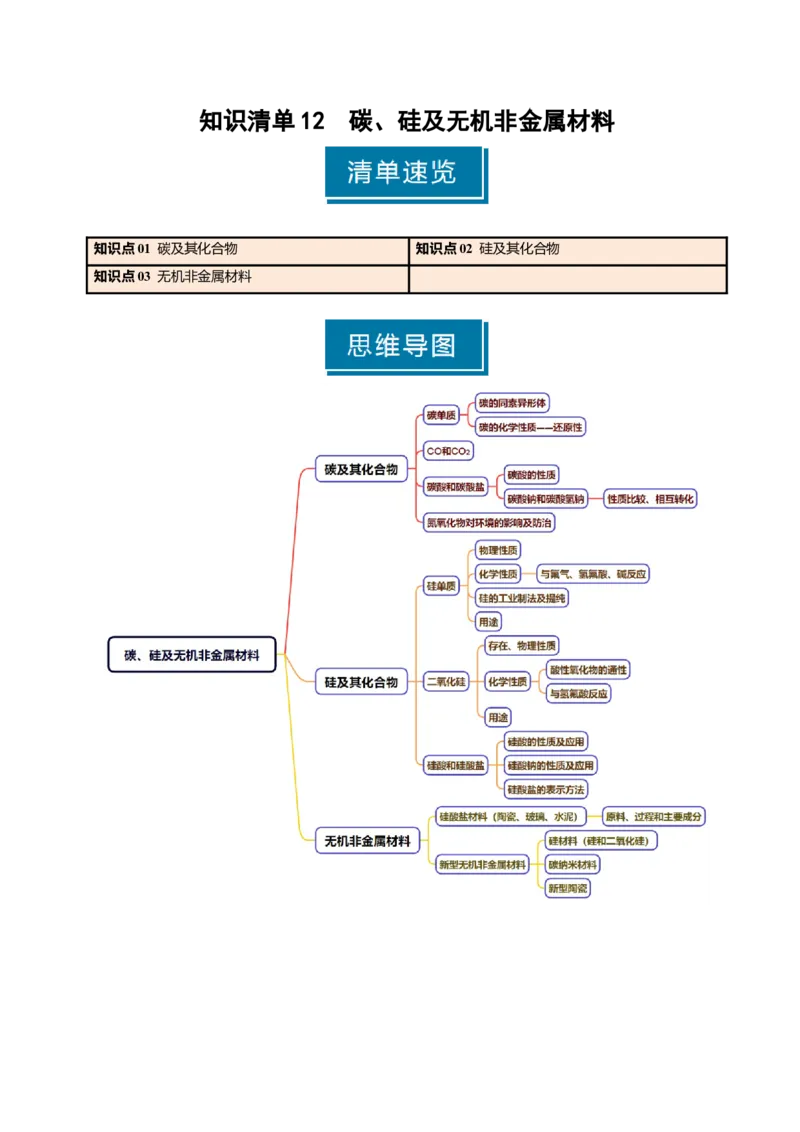
知识清单 12 碳、硅及无机非金属材料
知识点01 碳及其化合物 知识点02 硅及其化合物
知识点03 无机非金属材料知识点 01 碳及其化合物
1.碳单质
(1)存在形式:有金刚石、石墨、无定形碳、足球烯,它们互为_________________。
金刚石 石墨 足球烯
①金刚石:__________空间网状结构。
物理性质:熔点____,硬度_____,_____导电。
②石墨:层状结构,每层为___________的平面网状结构。
物理性质:熔点_____,硬度______,_____导电,具有润滑性。
③足球烯(C ):笼状分子,由正五边形和正六边形排列而成。_____导电。
60
(2)主要化学性质——还原性
O 不足:________________________
2
可燃性
O 充足:________________________
2
CuO:________________________________ (冶炼金属);
与氧化物反应 SiO:________________________________ (制取粗硅);
2
HO:________________________________ (制取水煤气)
2
浓HSO :________________________________;
2 4
与强氧化性酸反应
浓HNO:________________________________。
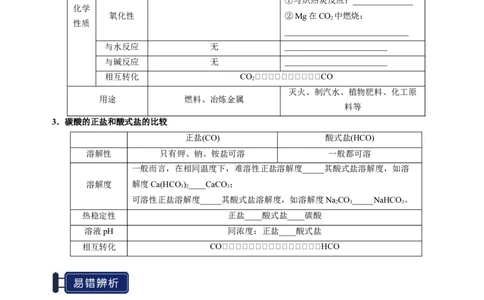
32.CO、CO 的性质对比
2
CO CO
2
____色____味气体,密度比空气 ____色_____味气体,密度比空气
物理性质
_____,_____溶于水 _____,____溶于水
毒性 有毒(易结合________) 无毒(________效应)
可燃性:________________
还原性 还原氧化铁: 无(灭火)
________________________
①与炽热炭反应:______________
化学
氧化性 ②Mg在CO 中燃烧:
2
性质
_____________________________
与水反应 无 ________________________
与碱反应 无 ________________________
相互转化 COCO
2
灭火、制汽水、植物肥料、化工原
用途 燃料、冶炼金属
料等
3.碳酸的正盐和酸式盐的比较
正盐(CO) 酸式盐(HCO)
溶解性 只有钾、钠、铵盐可溶 一般都可溶
一般而言,在相同温度下,难溶性正盐溶解度_____其酸式盐溶解度,如溶
溶解度 解度Ca(HCO )____CaCO ;
3 2 3
可溶性正盐溶解度_____其酸式盐溶解度,如溶解度NaCO_____NaHCO 。
2 3 3
热稳定性 正盐____酸式盐____碳酸
溶液pH 同浓度:正盐____酸式盐
相互转化 COHCO
(1)金刚石和石墨由相同的元素组成,因此它们具有相同的性质( )
(2)石墨转变为金刚石的反应属于氧化还原反应( )
(3)向空气中排放二氧化碳会形成酸雨( )
(4)向CaCl 溶液中通入CO 气体,溶液变浑浊,继续通入CO 至过量,浑浊消失( )
2 2 2
(5)氨化的饱和食盐水中通入足量的CO 气体,会析出晶体( )
2
(6) 激光法蒸发石墨得到C 发生的物理变化( )
60
一、碳及其重要化合物的转化碳的重要化合物转化关系如下:
用化学方程式表示标有序号的各步变化。
①___________________________________;
②___________________________________;
③___________________________________;
④___________________________________;
⑤____________________________________;
⑥____________________________________。
二、碳氧化物的除杂问题
写出除去下列气体中混有的杂质(括号内为杂质)可采取的方法。
(1)CO(CO ):_________________________________;
2
(2)CO (CO):_________________________________;
2
(3)CO (O ):__________________________________;
2 2
(4)CO (SO ):_________________________________;
2 2
(5)CO (HCl):_________________________________。
2
知识点 02 硅及其化合物
1.硅单质
(1)硅元素在自然界中主要以_________和_________等化合态的形式存在于地壳中。
(2)物理性质
晶体硅是灰黑色、有金属光泽、硬而脆的固体,其结构类似于金刚石,熔沸点____、硬度_____,
导电能力介于导体和绝缘体之间,是良好的_________材料。
(3)化学性质
①与氟气反应:___________________________;
②与氢氟酸反应:___________________________;
③与NaOH溶液反应:____________________________________。
(4)用途:良好的半导体材料、太阳能电池、计算机芯片等。
(5)硅的工业制法及提纯
――――→――→――→
涉及的化学方程式:
①____________________________________;
②____________________________________;③____________________________________。
2.二氧化硅
(1)SiO 的存在:石英砂、水晶、玛瑙的主要成分。
2
(2)物理性质:_____溶于水,硬度_____,熔点_____。
(3)化学性质:
①酸性氧化物,与NaOH溶液反应的方程式为:____________________________。
②高温条件下与碱性氧化物反应,与氧化钙反应的方程式为:____________________________。
③高温下,NaCO、CaCO 与SiO 反应制玻璃:
2 3 3 2
___________________________________、___________________________________。
④与氢氟酸反应(特殊):___________________________________。
(4)用途:光导纤维、光学仪器、电子器件等。
3.硅酸
(1)硅酸是_______于水的弱酸。酸性比碳酸______:___________________________________。
(2)硅酸不稳定,受热易分解:____________________________。
(3)用途:硅胶可用于催化剂载体和袋装食品、瓶装药品等的干燥剂。
4.硅酸盐
(1)硅酸盐是由硅、氧与其他化学元素结合而成的化合物的总称,是构成地壳岩石的主要成分。
(2)硅酸钠
①白色、可溶于水的粉末状固体,其水溶液俗称_______。有黏性,水溶液显碱性。
②与酸性比硅酸强的酸反应
a.与盐酸反应:___________________________________。
b.与CO 水溶液反应:___________________________________。
2
③用途:黏合剂(矿物胶),耐火阻燃材料。
(3)硅酸盐组成的表示方法:通常用二氧化硅和金属氧化物的组合形式表示硅酸盐的组成。
①氧化物的书写顺序:_______金属氧化物→_______金属氧化物→二氧化硅→水,不同氧化物间以
“·”隔开。
②各元素的化合价保持不变,且满足化合价代数和为零,各元素原子个数比符合原来的组成。
如硅酸钠(Na SiO)可表示为______________,长石(KAlSi O)可表示为______________。
2 3 3 8
(1)硅在自然界中只以化合态的形式存在( )
(2)晶体硅熔点高、硬度大,故可用于制作半导体材料( )
(3)工业上用焦炭和二氧化硅制取粗硅时生成粗硅和CO 气体( )
2
(4)Si是半导体材料,可用作太阳能电池( )
(5)SiO 与NaOH溶液反应生成盐和水,也可以和氢氟酸反应,所以SiO 是两性氧化物( )
2 2
(6)NaOH溶液不能用玻璃瓶盛放( )
(7)高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱会“断路”( )(8)SiO 是HSiO 的酸酐,所以SiO 和水反应生成HSiO( )
2 2 3 2 2 3
(9)Si和SiO 都可用于制造光导纤维( )
2
(10)SiO 是酸性氧化物,可溶于强碱(NaOH),不溶于任何酸( )
2
(11)水玻璃是一种特殊的玻璃,泡花碱属于碱( )
(12)由SiO+2C=====Si+2CO↑可推知硅的非金属性比碳强( )
2
(13)由NaSiO+CO+HO===Na CO+HSiO↓可推知碳的非金属性比硅强( )
2 3 2 2 2 3 2 3
(14)由CaCO +SiO=====CaSiO +CO↑可推知HSiO 的酸性比HCO 强( )
3 2 3 2 2 3 2 3
一、高纯硅的制备
制备硅半导体材料必须先得到高纯硅。三氯甲硅烷(SiHCl )还原法是当前制备高纯硅的主要方法,生产过
3
程示意图如下:
――→――→――→――→
(1)写出由纯SiHCl 制备高纯硅的化学反应方程式:______________________________。
3
(2)整个制备过程必须严格控制无水无氧。SiHCl 遇水剧烈反应生成HSiO、HCl和另一种物质,写
3 2 3
出化学反应方程式: _____________________________;H 还原SiHCl 过程中若混有O,可能引起的后
2 3 2
果是___________________。
二、硅及其化合物的性质
化学研究性学习小组在探究硅的制取方法时,从资料查阅到下列信息:
Ⅰ.Mg在高温条件下可与SiO 反应;
2
Ⅱ.金属硅化物与稀HSO 反应生成硫酸盐和SiH;
2 4 4
Ⅲ.SiH 在空气中自燃。
4
他们根据信息进行实验,当用足量稀HSO 溶解第Ⅰ步实验获得的固体产物时,发现有爆鸣声和火
2 4
花;然后过滤、洗涤、干燥;最后称量、计算,测得其产率只有预期值的63%左右。
(1)第Ⅰ步实验发生反应的化学方程式是________________________________。
(2) 用 稀 HSO 溶 解 第 Ⅰ 步 实 验 获 得 的 固 体 产 物 时 , 产 生 爆 鸣 声 和 火 花 的 原 因 是
2 4
___________________
________________________________________。
知识点 03 无机非金属材料
1.硅酸盐材料
(1)陶瓷
陶瓷以_______ (主要成分为含水的__________)为主要原料,经_______烧结而成的。
(2)玻璃
①主要原料:_______、_______和_______。②生产过程:将原料经混合、粉碎,在________中熔融,发生复杂的_____________________而制
得。
③普通玻璃的主要成分为____________________________。
④用途:生产建筑材料、光学仪器和各种器皿,还可制造__________,用于高强度_________等。
(3)水泥
①主要原料:______________。
②生产过程:将原料与其他辅料经混合、研磨后在______________中煅烧,发生复杂的物理变化和
化学变化,加入适量_______调节水泥硬化速率,再研成细粉得到普通水泥。
③应用:混凝土是水泥、_______和_______等与水混合得到的。
3.新型无机非金属材料
材料类型 主要特性 示例 用途
能承受高温,强度 汽轮机叶片、轴承、永久性模具
高温结构陶瓷 氮化硅陶瓷
高 等
半导体陶瓷 具有电学特性 二氧化锡陶瓷 集成电路中的半导体
光学材料 具有光学特性 光导纤维 光缆通讯、医疗、照明等
生物陶瓷 具有生物功能 氧化铝陶瓷 人造骨骼、人造关节、接骨螺钉
3.碳纳米材料
碳纳米材料是一类新型的无机非金属材料
(1)类型:富勒烯、碳纳米管、石墨烯等。
(2)用途:在能源、信息、医药等领域有广阔的应用前景。
材料类型 性能 用途
碳纳米管 比表面积大,高强度,优良的电学性能 生产复合材料、电池和传感器等
用于光电器件、超级电容器、电池
石墨烯 电阻率低,热导率高,具有很高的强度
和复合材料等
(1)晶体硅的导电性介于导体和绝缘体之间,常用于制造光导纤维( )
(2)飞船返回舱表层材料中的玻璃纤维属于天然有机高分子( )
(3)制造5G芯片的氮化铝晶圆属于无机非金属材料( )
(4)石灰石是制造玻璃和水泥的主要原料之一( )
(5)火炬“飞扬”使用的碳纤维属于有机高分子材料( )