文档内容
专项训练 离子交换膜种类的判断(解析版)
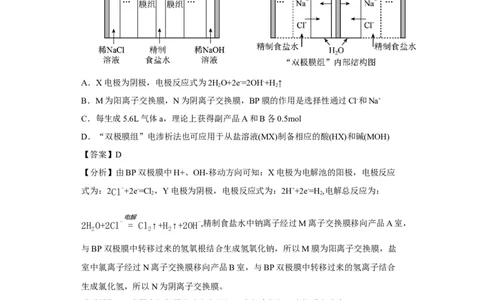
1.(2023·全国·高三专题练习)目前可采用“双极膜组”电渗析法淡化海水,同时获
得副产品A和B,模拟工作原理如图所示。M和N为离子交换膜,在直流电作用下,
双极阴阳膜(BP)复合层间的H O解离成H+和OH-,作为H+和OH-的离子源。下列说法正
2
确的是
A.X电极为阴极,电极反应式为2HO+2e-=2OH-+H ↑
2 2
B.M为阳离子交换膜,N为阴离子交换膜,BP膜的作用是选择性通过Cl-和Na+
C.每生成5.6L气体a,理论上获得副产品A和B各0.5mol
D.“双极膜组”电渗析法也可应用于从盐溶液(MX)制备相应的酸(HX)和碱(MOH)
【答案】D
【分析】由BP双极膜中H+、OH-移动方向可知:X电极为电解池的阳极,电极反应
式为:2Cl-+2e-=Cl,Y电极为阴极,电极反应式为:2H++2e-=H ,电解总反应为:
2 2
电解
2H O+2Cl- = Cl ↑+H ↑+2OH-,精制食盐水中钠离子经过M离子交换膜移向产品A室,
2 2 2
与BP双极膜中转移过来的氢氧根结合生成氢氧化钠,所以M膜为阳离子交换膜,盐
室中氯离子经过N离子交换膜移向产品B室,与BP双极膜中转移过来的氢离子结合
生成氯化氢,所以N为阴离子交换膜。
【详解】A.由图中氢氧根移动方向可知X电极为阳极,电极反应式为:2Cl-+2e-
=Cl,A错误;
2
B.由题意可知,精制食盐水中钠离子经过M离子交换膜移向产品A室,与BP双极
膜中转移过来的氢氧根结合生成氢氧化钠,所以M膜为阳离子交换膜,盐室中氯离子
经过N离子交换膜移向产品B室,与BP双极膜中转移过来的氢离子结合生成氯化氢,
所以N为阴离子交换膜,BP双极膜的作用是选择性通过氢离子和氢氧根离子,B错误;
C.阳极反应式为:2Cl-+2e-=Cl,电路中每生成标况下5.6L气体氯气,其物质的量为
2
0.25mol,转移电子0.5mol,理论上获得副产品A(氢氧化钠溶液)和B(氯化氢溶
1 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司液)各0.5mol,需标明标准状况,C错误;
D.“双极膜组”电渗析法从氯化钠溶液中获得酸(HCl)和碱(NaOH),由此可知:
也可从M溶液制备相应的酸(HX)和碱(MOH),D正确;
故选D。
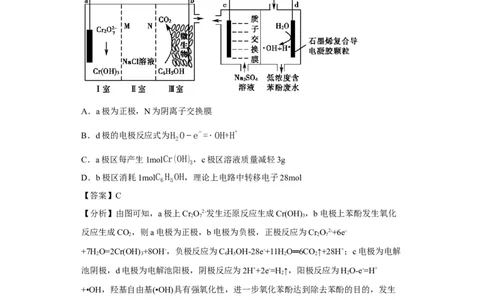
2.(2023·全国·高三统考专题练习)科学家设计了一种能产生羟基自由基(·OH)的原电
池—电解池组合装置,·OH能将苯酚氧化为CO 和H O,实现发电、环保二位一体,如
2 2
图所示。下列说法错误的是
A.a极为正极,N为阴离子交换膜
B.d极的电极反应式为H O−e−=· OH+H+
2
C.a极区每产生1molCr(OH) ,c极区溶液质量减轻3g
3
D.b极区消耗1molC H OH,理论上电路中转移电子28mol
6 5
【答案】C
【分析】由图可知,a极上Cr O2-发生还原反应生成Cr(OH) ,b电极上苯酚发生氧化
2 7 3
反应生成CO,则a电极为正极,b电极为负极,正极反应为Cr O2-+6e-
2 2 7
+7H O=2Cr(OH) +8OH-,负极反应为C HOH-28e-+11H O═6CO ↑+28H+;c电极为电解
2 3 6 5 2 2
池阴极,d电极为电解池阳极,阴极反应为2H++2e-=H ↑,阳极反应为HO-e-=H+
2 2
+•OH,羟基自由基(•OH)具有强氧化性,进一步氧化苯酚达到除去苯酚的目的,发生
的反应为C HOH+28•OH═6CO ↑+17H O,据此分析解答。
6 5 2 2
【详解】A.由上述分析可知,左侧装置为原电池,右侧装置为电解池,a电极为正极,
b电极为负极,负极方程式为:C HOH-28e-+11H O═6CO ↑+28H+,阳离子浓度增大,
6 5 2 2
则Cl-通过N膜计入b极区,N为阴离子交换膜,故A正确;
B.d电极为电解池阳极,阳极上HO失电子生成H+、•OH,阳极反应为HO-e-=H+
2 2
+•OH,故B正确;
C.正极反应为Cr O❑ 2− +6e-+7H O=2Cr(OH) +8OH-,a极区每产生1mol Cr(OH) 时转
2 7 2 3 3
试卷第2页,共27页移3mol电子,通过质子交换膜移向阴极的n(H+)=3mol,阴极反应为2H++2e-=H ↑,
2
1
n(H )=
n(H+)=1.5mol,m(H)=1.5mol×2g/mol=3g,即c极区溶液质量不变,故C错
2 2 2
误;
D.由分析可知,b极区电极方程式为:C HOH-28e-+11H O═6CO ↑+28H+,消耗1mol
6 5 2 2
C H OH,理论上电路中转移电子28mol,故D正确;
6 5
故选C。
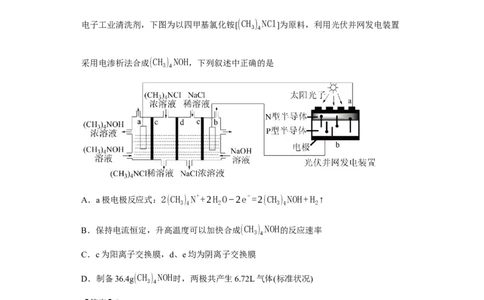
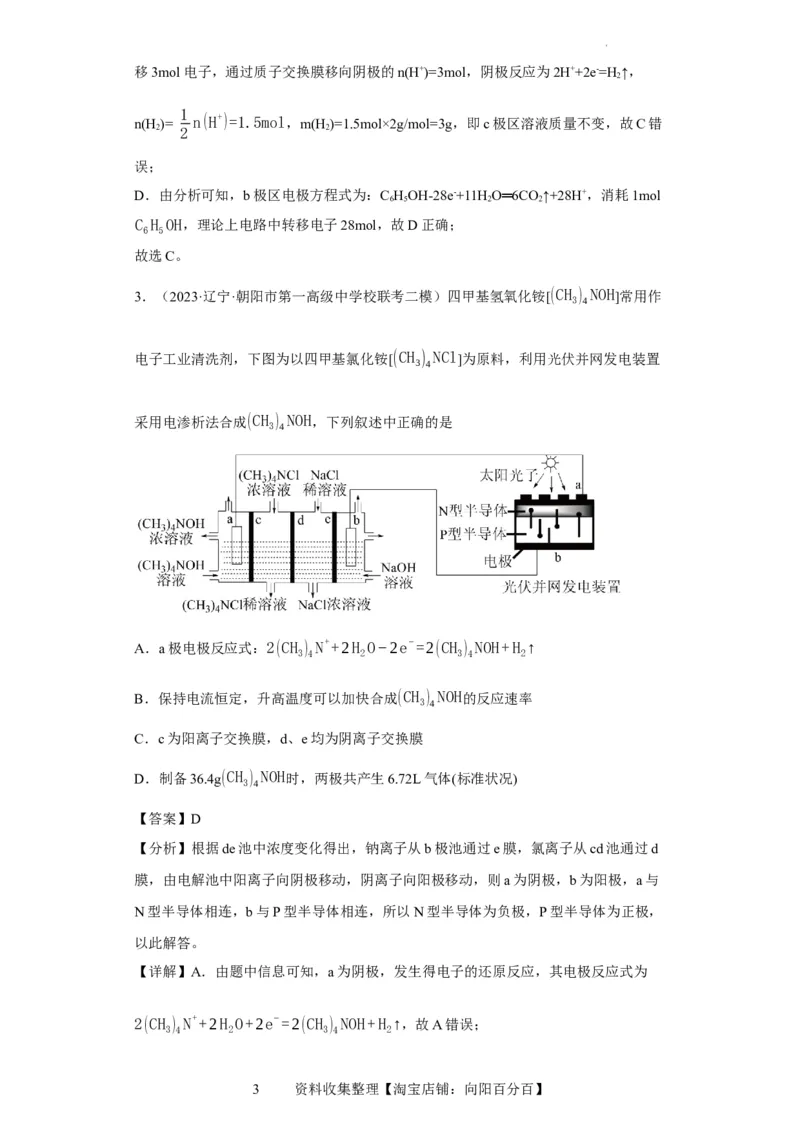
3.(2023·辽宁·朝阳市第一高级中学校联考二模)四甲基氢氧化铵[(CH ) NOH]常用作
3 4
电子工业清洗剂,下图为以四甲基氯化铵[(CH ) NCl ]为原料,利用光伏并网发电装置
3 4
采用电渗析法合成(CH ) NOH,下列叙述中正确的是
3 4
A.a极电极反应式:2(CH ) N++2H O−2e−=2(CH ) NOH+H ↑
3 4 2 3 4 2
B.保持电流恒定,升高温度可以加快合成(CH ) NOH的反应速率
3 4
C.c为阳离子交换膜,d、e均为阴离子交换膜
D.制备36.4g(CH ) NOH时,两极共产生6.72L气体(标准状况)
3 4
【答案】D
【分析】根据de池中浓度变化得出,钠离子从b极池通过e膜,氯离子从cd池通过d
膜,由电解池中阳离子向阴极移动,阴离子向阳极移动,则a为阴极,b为阳极,a与
N型半导体相连,b与P型半导体相连,所以N型半导体为负极,P型半导体为正极,
以此解答。
【详解】A.由题中信息可知,a为阴极,发生得电子的还原反应,其电极反应式为
2(CH ) N++2H O+2e−=2(CH ) NOH+H ↑,故A错误;
3 4 2 3 4 2
3 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司B.保持电流恒定,则单位时间a极得到的电子数目是恒定的,升高温度,电极反应
2(CH ) N++2H O+2e−=2(CH ) NOH+H ↑的速率不变,故B错误;
3 4 2 3 4 2
C.由题中图示信息可知,Na+离子通过e膜,Cl-通过d膜,(CH)N+通过c膜,所以
3 4
c、e膜为阳离子交换膜,d为阴离子交换膜,故C错误;
36.4g
D.36.4g(CH ) NOH的物质的量为 = 0.4mol,a极电极反应式为2(CH ) N+
3 4 91g/mol 3 4
+2H O+2e-=2(CH ) NOH+H ↑,收集氢气0.2mol,转移电子为0.4mol,b极电极反应式
2 3 4 2
为4OH--4e-=O ↑+2H O,收集氧气为0.1mol,标况下两极可得气体体积为0.3mol×
2 2
22.4L/ mol =6.72L L,故D正确;
故选D。
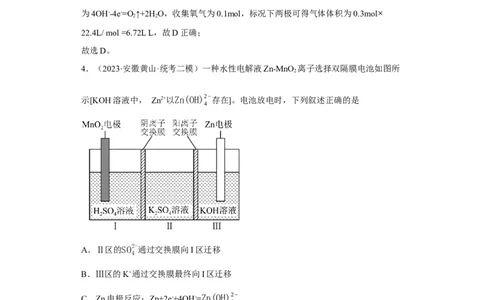
4.(2023·安徽黄山·统考二模)一种水性电解液Zn-MnO 离子选择双隔膜电池如图所
2
示[KOH溶液中, Zn2+以Zn(OH)2−存在]。电池放电时,下列叙述正确的是
4
A.Ⅱ区的SO2-通过交换膜向I区迁移
4
B.Ⅲ区的K+通过交换膜最终向I区迁移
C.Zn电极反应:Zn+2e-+4OH-=Zn(OH)2−
4
D.电池总反应:Zn+4OH-+MnO+4H+=Zn(OH)2− +Mn2++2H O
2 4 2
【答案】D
【分析】根据图示的电池结构和题目所给信息可知,Ⅲ区Zn为电池的负极,电极反应
为Zn-2e-+4OH-=Zn(OH)❑ 2−,Ⅰ区MnO 为电池的正极,电极反应为MnO +2e-
4 2 2
+4H+=Mn2++2H O;电池在工作过程中,阳离子向正极迁移、阴离子向负极迁移,因此
2
试卷第4页,共27页Ⅰ区的SO❑ 2−向Ⅱ区移动,Ⅲ区的K+向Ⅱ区移动;
4
【详解】A.根据分析,Ⅱ区的SO2−向Ⅲ区移动,但是不能通过阳离子交换膜,A错
4
误;
B.根据分析,Ⅲ区的K+通过交换膜Ⅱ区移动,不能通过阴离子交换膜向I区迁移,B
错误;
C.根据分析,Zn电极反应:Zn-2e-+4OH-=Zn(OH)2−,C错误;
4
D.根据正、负极电极分析,电池总反应:Zn+4OH-+MnO+4H+=Zn(OH)2− +Mn2+
2 4
+2H O,D正确;
2
故选D。
5.(2023·湖北·高三统考专题练习)双极膜(BP)可以在电场作用下,使水分子快速解
离为OH−和H+,并透过阴、阳离子膜进入溶液。用此工艺捕获烟道气中的CO 过程如图
2
所示,已知盐室中生成CaCO 实现捕获,下列说法正确的是
3
A.捕获装置中,阴极反应为2H++2e−=H ↑
2
B.溶液中的X为H+
C.交换膜A为阳离子交换膜
D.捕获1.12L CO 转化为沉淀,则转移电子2mol
2
【答案】A
【详解】A.阴极发生还原反应,溶液中H+放电,为2H++2e−=H ↑,A正确;
2
B.碱室是CO 转化为CO2−,应由双极膜产生OH−不断补充,保持碱的浓度,X应为OH−,
2 3
B错误;
C.盐室生成CaCO ,就需要CO2−穿过交换膜A,所以交换膜A为阴离子交换膜,C错
3 3
5 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司误;
D.捕获1.12L CO ,未指明标准状况,无法计算转移电子数,D错误;
2
故选A。
6.(2023春·江西·高二铅山县第一中学校联考阶段练习)电解法转化CO 可实现CO 资
2 2
源化利用。电解CO 制甲酸盐(HCOO−)的原理如图所示。下列说法不正确的是
2
A.电解一段时间后,阳极区的KHCO 溶液浓度降低
3
B.Sn片上发生的电极反应为CO +HCO−+2e−=HCOO−+CO2−
2 3 3
C.若将阳离子交换膜换成阴离子交换膜,会使HCOO−的产率降低
D.Sn极上每消耗0.1mol CO ,同时有0.2mol K+从Sn极区向Pt极区迁移
2
【答案】D
【分析】CO、HCOO-中碳元素的化合价分别为+4、+2,阴极发生还原反应,电极
2
(Sn电极)反应为CO+2e-+H+= HCOO-(或2CO+2e-+H O=HCO❑ - +HCOO-),阳极
2 2 2 3
(Pt电极)生成O:4HCO--4e-=O ↑+4CO ↑+2H O,由电极反应可得出电解总反应
2 3 2 2 2
电解
为2CO+2H O= = 2HCOOH+ O ↑,据此分析解答。
2 2 2
❑
【详解】A.电解过程中,Pt电极发生反应:4HCO--4e-=O ↑+4CO ↑+2H O,Pt电极
3 2 2 2
为阳极,同时K+向Sn电极移动,所以左侧中KHCO 溶液浓度降低;右侧Sn电极发生
3
反应:CO +HCO-+2e-=HCOO-+CO2- ,Sn电极为阴极,右侧中KHCO 溶液浓度降低,
2 3 3 3
A正确;
B.右侧Sn电极发生反应:CO +HCO-+2e-=HCOO-+CO2-,B正确;
2 3 3
C.若将阳离子交换膜换成阴离子交换膜,左侧钾离子不能移向Sn电极,不能得到甲
酸盐,会使HCOO−的产率降低,C正确;
D.电解过程中,阳离子向阴极移动,Sn极上每消耗0.1mol CO ,转移0.1mol电子,
2
试卷第6页,共27页则同时有0.2mol K+从Pt极区向Sn极区迁移,D错误;
故选D。
7.(2023·全国·统考模拟预测)利用双极膜电渗析法处理废水,可实现废水的高效净
化,其原理如图所示。双极膜是特种离子交换膜,它是由一张阳膜和一张阴膜制成的
阴、阳复合膜。在直流电场的作用下,阴、阳膜复合层间的HO分子解离成H+和OH-
2
并分别通过阳膜和阴膜。下列说法正确的是
A.电极X连接电源的正极,其电极反应式为4OH--4e-=O ↑+2H O
2 2
B.Z为淡水,M为HSO 溶液,b膜为阳离子交换膜
2 4
C.理论上,每转移2mol电子,两极共产生1.5mol气体
D.该装置中,电子的转移方向为电极X→电解质溶液→电极Y
【答案】C
【分析】在直流电场的作用下,阴、阳膜复合层间的HO分子解离成H+和OH-并分别
2
通过阳膜和阴膜,电解过程中,阳离子H+向阴极移动,则电极X为阴极,连接电源的
负极,Y为阳极,连接电源的正极。
【详解】A.电解过程中,阳离子H+向阴极移动,则电极X为阴极,连接电源的负极,
A项错误;
B.Na+、Ni2+向阴极移动,a膜为阳离子交换膜,SO2−向阳极移动,b膜为阴离子交换
4
膜,Z为淡水,N为H SO 溶液,B项错误;
2 4
C.阴极上H+放电,产生H ,阳极上OH−放电,产生O ,根据得失电子守恒,理论上每
2 2
转移2mol电子,产生1molH 和0.5molO ,C项正确;
2 2
D.电子通过外电路移动,不会经过电解质溶液,D项错误。
故选C。
8.(2023·湖北·高三统考专题练习)双极膜是阴、阳复合膜,在直流电的作用下,阴、
阳膜复合层间的H O解离成H+和OH−,作为H+和OH−离子源。利用双极膜制取NaOH和
2
7 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司H PO ,产品室1的产品是NaOH,其装置如图所示。
3 4
已知:产品室1的产品是NaOH,则下列说法正确的是
A.a为铅蓄电池的正极,电子由b极流出经装置流入a极
B.膜1为阴离子交换膜,膜2为阳离子交换膜
C.电极Ⅱ的电极反应式为2H O+4e−=O ↑+4H+
2 2
D.若要制60g NaOH,理论上铅蓄电池的负极增重72g
【答案】D
【分析】已知产品室1的产品是NaOH,说明原料室中Na+往左移动,电极Ⅰ是阴极,
a为铅蓄电池的负极,b为铅蓄电池的正极,膜1为阳离子交换膜,HPO❑ −向右移动
2 4
到产品室2中,膜2为阴离子交换膜,双极膜向左解离生成氢离子,从而得到磷酸,
解离生成的氢氧根离子向右移动到电极Ⅱ(阳极)区,阳极发生失电子的氧化反应,
据此分析解答。
【详解】A.根据上述分析可知,a为铅蓄电池的负极,电子由a极流出经装置流入b
极,A错误;
B.结合上述分析可知,膜1为阴离子交换膜,膜2为阳离子交换膜,B错误;
C.电极Ⅱ为阳极,水发生失电子的氧化反应,其电极反应式为:
2H O−4e−=O ↑+4H+ ,C错误;
2 2
D.铅蓄电池的负极反应为:Pb−2e−+SO2−=PbSO ,当转移2mol电子时,负极增加
4 4
1mol SO2−的质量,即96g,生成的60g NaOH,即为1.5mol,转移的Na+也是1.5mol,
4
电路中转移1.5mol电子,负极增重的质量为72g,故D正确;
故选D。
9.(2023·湖北·高三统考专题练习)羟基自由基(⋅OH)具有极强的氧化能力,它能有
效地氧化降解废水中的有机污染物。在直流电源作用下,利用双极膜电解池产生羟基
自由基(⋅OH)处理含苯酚废水和含甲醛废水,原理如图所示。已知:双极膜中间层中
试卷第8页,共27页的H O解离为H+和OH−。下列说法错误的是
2
A.M极为阴极,电极反应式:O +2e−+2H+=2⋅OH
2
B.双极膜中H O解离出的OH−透过膜a向N极移动
2
C.每处理6.0g甲醛,理论上有0.4molH+透过膜b
D.通电一段时间后,理论上苯酚和甲醛转化生成CO 物质的量之比为6∶7
2
【答案】C
【详解】A.M电极通入O ,发生反应生成自由基⋅OH,反应式为:
2
O +2e−+2H+=2⋅OH,M作阴极,A正确;
2
B.N为阳极,电解时阴离子向阳极移动,所以OH−透过膜a向N极移动,B正确;
C.甲醛与⋅OH反应生成CO 的反应:HCHO-4e-+4OH−+⋅OH→CO +4H O,6.0g甲醛
2 2 2
为0.2mol,有0.8molH+,透过膜b,C错误;
D.1mol甲醛生成CO 转移4mole−,苯酚与⋅OH反应生成CO 的反应为:1molC H O转
2 2 6 6
移28mole−,理论上苯酚和甲醛转化生成CO 物质的量之比为6∶7,D正确;
2
故选C。
10.(2023·全国·高三专题练习)某有色金属工业的高盐废水中主要含有H+、Cu2+、
Zn2+、SO2− 、F−和Cl−,利用如图电解装置可回收ZnSO 、CuSO 并尽可能除去F−和
4 4 4
Cl−,其中双极膜(BP)中间层的H O解离为H+和OH−,并在直流电场作用下分别向两极
2
迁移,M膜、N膜需在一价阴离子交换膜和阳离子交换膜中选择。下列说法错误的是
9 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司A.BP膜中H+均向右侧溶液迁移,M膜为一价阴离子交换膜
B.溶液a的溶质主要为HF和HCl,溶液b的溶质主要为ZnSO 和CuSO
4 4
C.当阳极产生22.4L气体(标准状况)时,有4mol离子通过N膜
D.电解过程中,应控制高盐废水的pH不能过高
【答案】B
【分析】由图可知,最左侧为阳极室,水放电生成氧气和氢离子;最右侧为阴极室,
水放电生成氢气和氢氧根离子;
【详解】A.电解池中阳离子向阴极移动,BP膜中H+均向右侧溶液迁移;氟离子、氯
离子通过M膜向左侧迁移,故M膜为一价阴离子交换膜,A正确;
B.溶液a中氟离子、氯离子通过M膜向左侧迁移,氢离子与右侧双极膜迁移出来的
OH-中和,故反应后溶液a的溶质主要为ZnSO 和CuSO ;溶液b的溶质主要为右侧迁
4 4
移过来的氟离子、氯离子与左侧前过来的氢离子生成的为HF和HCl,B错误;
C.阳极反应为2H O- 4e-=4H++O ↑,当阳极产生22.4L气体(标准状况下为1mol)时,
2 2
根据电子守恒可知,有4mol离子通过N膜,C正确;
D.电解过程中,若pH过高则会导致锌离子、铜离子转化为沉淀,故应控制高盐废水
的pH不能过高,D正确;
故选B。
11.(2023·全国·模拟预测)甲酸钠燃料电池是一种膜基碱性电池,提供电能的同时可
以获得烧碱,其工作原理如图所示,下列有关说法正确的是
试卷第10页,共27页A.CEM隔膜为质子交换膜
B.甲为电池负极,电极反应为:HCOO--e-+H O=H CO +H+
2 2 3
C.电池在工作时,乙极附近溶液pH增大
D.单位时间内甲极产生的H CO 与乙极消耗的O 物质的量之比为4:1
2 3 2
【答案】C
【详解】A.该装置同时可以获得烧碱,则钠离子应与氢氧根离子结合,若为质子交
换膜(只允许氢离子自由通过),则钠离子与正极生成的氢氧根离子不能接触,无法得到
NaOH,故A错误;
B.由装置信息可知乙电极上氧气得电子,则甲电极上HCOONa失电子生成碳酸,电
极反应为:HCOO--2e-+H O=H CO +H+ ,故B错误;
2 2 3
C.电池在工作时,乙极发生反应:O +2H O+4e-=4OH-,电极附近溶液氢氧根离子浓
2 2
度增大,pH增大,故C正确;
D.由电极反应可知转移4mol电子正极消耗1mol氧气,负极生成2mol碳酸,则单位
时间内甲极产生的H CO 与乙极消耗的O 物质的量之比为2:1,故D错误;
2 3 2
故选:C。
12.(2023·山东济南·山东省实验中学校考一模)在直流电源作用下,双极膜中间层中
的H O解离为H+和OH−。某技术人员利用双极膜(膜c、膜d)和离子交换膜高效制备
2
H SO 和NaOH,工作原理如图所示:
2 4
11 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司下列说法错误的是
A.电势:N电极>M电极
B.双极膜膜c输出H+,膜a、膜e为阳离子交换膜
C.M极电极反应式为2H O+2e−=H +2OH−
2 2
D.当电路中转移2mole−时,整套装置将制得1molH SO
2 4
【答案】D
【分析】由题意可知该电解池可以高效制备H SO 和NaOH,说HO在M极得到电子生
2 4 2
成H 和OH-,电极方程式为:2H O+2e−=H +2OH−,膜a是阳离子交换膜,Na+通过
2 2 2
膜a进入M极,双极膜膜c输出H+,膜b是阴离子交换膜,SO❑ 2−通过膜b进入膜b
4
和膜c之间的区域生成H SO ;HO在N极失去电子生成O 和H+,电极方程式为:
2 4 2 2
2H O−4e−=O +4H+ ,膜f是阴离子交换膜,SO❑ 2−通过膜f进入N极,双极膜膜d
2 2 4
输出OH-,膜e是阳离子交换膜,Na+通过膜e进入膜e和膜d之间的区域生成NaOH;
以此解答。
【详解】A.由分析可知,HO在M极得到电子生成H 和OH-,M为阴极,HO在N
2 2 2
极失去电子生成O 和H+,N极为阳极,则电势:N电极>M电极,故A正确;
2
B.由分析可知,双极膜膜c输出H+,膜a、膜e为阳离子交换膜,故B正确;
C.由分析可知,M极电极反应式为2H O+2e−=H +2OH−,故C正确;
2 2
D.由分析可知,N极电极方程式为2H O−4e−=O +4H+ ,当电路中转移2mole−时,
2 2
N极生成1molH SO ,同时在膜b和膜c之间的区域生成1mol H SO ,故D错误;
2 4 2 4
故选D。
试卷第12页,共27页13.(2023·浙江·高三专题练习)NO-空气质子交换膜燃料电池实现了制硝酸、发电、
环保一体化,某兴趣小组用该电池模拟工业处理废气和废水的过程,装置如图。下列
说法不正确的是
A.b膜为阴离子交换膜
通电
B.乙池中总反应的离子方程式为5SO
2
+2NO+8H
2
O ¿2NH++5SO2-+8H+
4 4
¿
C.当浓缩室得到4L浓度为0.6mol⋅L−1的盐酸时,M室溶液的质量变化为36g(溶液
体积变化忽䅂不计)
D.在标准状况下,若甲池有5.6LO 参加反应,则乙池中处理废气(SO 和NO)的总体积
2 2
为15.68L
【答案】C
【分析】由图可知,甲为原电池,乙和丙为电解池;甲中通入NO的一极作负极,通
入氧气的一极作正极;乙池中通入 SO 的电极连接电源的正极,为阳极,阳极上二氧
2
化硫发生氧化反应生成硫酸根离子,阴极上一氧化氮发生还原反应生成铵根离子;丙
池中阳极上水放电,发生氧化反应生成氧气和氢离子,氢离子从M室通过a膜进入浓
缩室,N室中氯离子向阳极移动,通过b膜进入浓缩室,最终得到较浓的盐酸;据此
分析解答。
【详解】A.丙中阳极上水放电,发生氧化反应生成氧气和氢离子,氢离子从M室通
过a膜进入浓缩室,N室中氯离子向阳极移动,通过b膜进入浓缩室,最终得到较浓的
盐酸,故b膜为阴离子交换膜,A正确;
B.乙池中通入SO 的电极连接电源的正极,为阳极,阳极上二氧化硫发生氧化反应生
2
成硫酸根离子,阴极上一氧化氮发生还原反应生成铵根离子,电池总反应的离子方程
通电
式为5SO
2
+2NO+8H
2
O ¿2NH++5SO2−+8H+,B正确;
4 4
¿
C.当浓缩室得到4L浓度为0.6mol⋅L−1的盐酸时,迁移过来的氢离子的物质的量为
13 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司4L×(0.6mol⋅L−1−0.1mol⋅L−1)=2mol
,
2H O−4e−=4H++O ↑
,则反应掉1mol
2 2
水,M室溶液的质量减小1mol×18g⋅mol−1=18g,C错误;
D.乙池中SO 转化为硫酸根离子,NO转化为铵根离子,在标准状况下,若甲池有
2
5.6LO (0.25mol)参加反应,根据电子守恒可知,O ∼4e− ∼2SO 、
2 2 2
4
O ∼4e− ∼ NO,则乙池中处理废气( SO 和NO)共0.7mol,总体积为15.68L,D正确;
2 5 2
故选C。
14.(2023·重庆·高三重庆巴蜀中学校考阶段练习)微信山城学术圈刊登了一种Zn﹣
PbO 电池,电解质为KSO 、HSO 和KOH,通过a和b两种离子交换膜将电解质溶
2 2 4 2 4
液隔开(减少参加电极反应的离子的迁移更有利于放电),形成M、R、N三个电解质溶
液区域,结构示意图如图所示。下列说法正确的是
A.a为阴离子交换膜,b为阳离子交换膜
B.电池放电后R区域的电解质溶液浓度增大
C.充电时,Zn电极反应为Zn﹣2e﹣+4OH﹣=Zn(OH)❑ 2−
4
D.放电时,消耗13gZn,N区域电解质溶液减少39.2g
【答案】B
【分析】由图可知,原电池工作时,Zn为负极,被氧化生成Zn(OH)2-,PbO 为正极,
4 2
发生还原反应,电解质溶液M为KOH,R为KSO ,N为HSO ,原电池工作时,负
2 4 2 4
极反应为Zn﹣2e﹣+4OH﹣=Zn(OH)2-,则消耗OH﹣,钾离子向正极移动,正极电极反
4
试卷第14页,共27页应式为PbO +SO2- +2e﹣+4H+=PbSO+2H O,正极消耗氢离子,阴离子向负极移动,则a
2 4 4 2
是阳离子交换膜,b是阴离子交换膜,在同一闭合回路中电子转移数目相等,结合溶
液酸碱性及电极材料书写电极反应式和总反应的方程式,以此解答该题。
【详解】A.Zn为负极,负极反应为Zn﹣2e﹣+4OH﹣=Zn(OH)2-,则消耗OH﹣,钾离
4
子向正极移动,则a是阳离子交换膜,PbO 为正极,正极电极反应式为PbO +SO2- +2e
2 2 4
﹣+4H+=PbSO+2H O,消耗H+的物质的量为SO2-的4倍,则SO2-离子向负极移动,b是
4 2 4 4
阴离子交换膜,A错误;
B.原电池工作时,负极反应为Zn﹣2e﹣+4OH﹣=Zn(OH)2-,则消耗OH﹣,钾离子向正
4
极移动,正极电极反应式为PbO +SO2- +2e﹣+4H+=PbSO+2H O,正极消耗氢离子,阴
2 4 4 2
离子向负极移动,电池放电后R区域的电解质溶液浓度增大,B正确;
C.充电时,Zn为阴极,Zn电极反应为Zn(OH)2- +2e﹣=Zn+4OH﹣,C错误;
4
D.13gZn的物质的量为0.2mol,负极反应为Zn﹣2e﹣+4OH﹣=Zn(OH)2-,电路中转移
4
电子0.4mol,N区域转移0.2molSO2-,正极反应为PbO +SO2- +2e﹣
4 2 4
+4H+=PbSO+2H O,电路中转移电子0.4mol,消耗0.2molSO2-,溶液中增加0.4molO
4 2 4
原子,所以N区域电解质溶液减少的质量为0.4mol×96g/mol﹣0.4mol×16g/mol=32.0g,
D错误;
故选B。
【点睛】根据电极材料金属的活泼性判断出正负极,书写出电极反应,从而可以确定
各区域的电解质溶液种类,根据阴阳离子的移动方向可以确定离子交换膜种类,进行
电解质溶液质量计算时要综合考虑离开体系和进入体系的粒子。
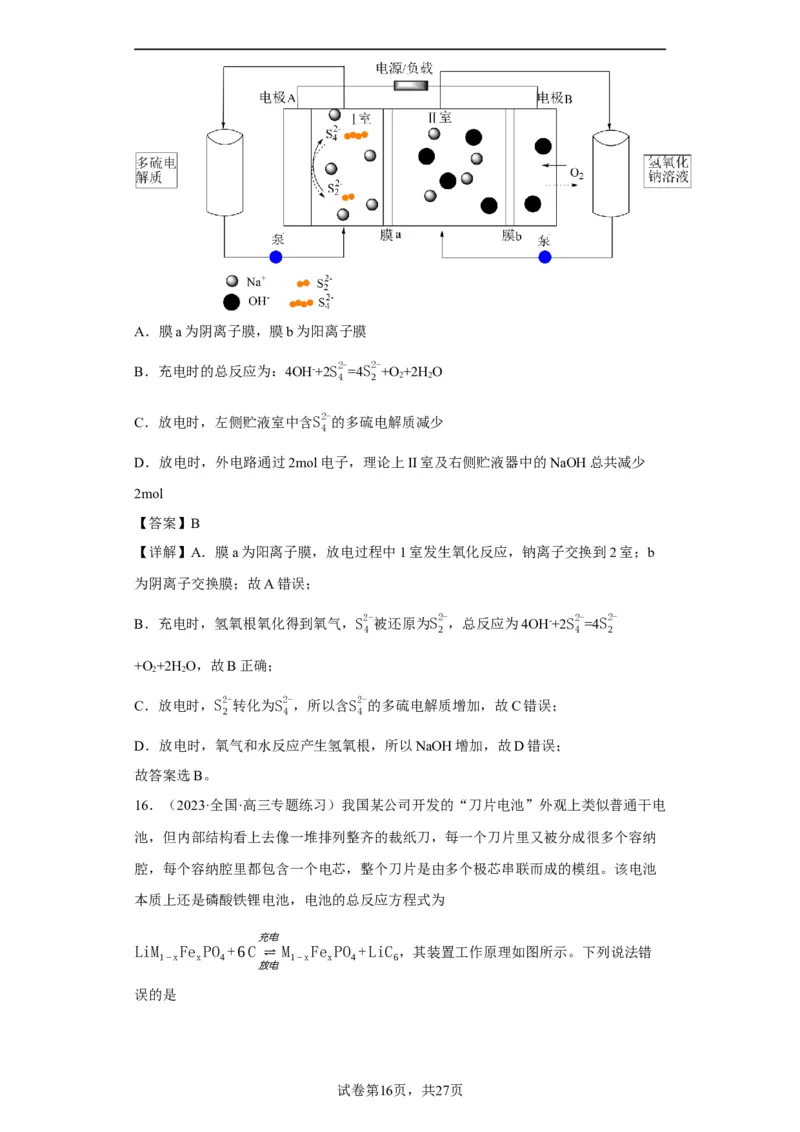
15.(2023春·河南·高三专题练习)一种稳定且具有低成本效益的碱性混合多硫化物-
空气氧化还原液流电池结构如图所示。下列说法正确的是
15 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司A.膜a为阴离子膜,膜b为阳离子膜
B.充电时的总反应为:4OH-+2S2- =4S2-
+O +2H O
4 2 2 2
C.放电时,左侧贮液室中含S2-的多硫电解质减少
4
D.放电时,外电路通过2mol电子,理论上II室及右侧贮液器中的NaOH总共减少
2mol
【答案】B
【详解】A.膜a为阳离子膜,放电过程中1室发生氧化反应,钠离子交换到2室;b
为阴离子交换膜;故A错误;
B.充电时,氢氧根氧化得到氧气,S2-被还原为S2- ,总反应为4OH-+2S2- =4S2-
4 2 4 2
+O +2H O,故B正确;
2 2
C.放电时,S2- 转化为S2-,所以含S2-的多硫电解质增加,故C错误;
2 4 4
D.放电时,氧气和水反应产生氢氧根,所以NaOH增加,故D错误;
故答案选B。
16.(2023·全国·高三专题练习)我国某公司开发的“刀片电池”外观上类似普通干电
池,但内部结构看上去像一堆排列整齐的裁纸刀,每一个刀片里又被分成很多个容纳
腔,每个容纳腔里都包含一个电芯,整个刀片是由多个极芯串联而成的模组。该电池
本质上还是磷酸铁锂电池,电池的总反应方程式为
充电
LiM Fe PO +6C ⇌ M Fe PO +LiC ,其装置工作原理如图所示。下列说法错
1−x x 4 1−x x 4 6
放电
误的是
试卷第16页,共27页A.该电池工作时,负极的电极反应式为LiM Fe PO −e−=M Fe PO +Li+
1−x x 4 1−x x 4
B.该电池中的聚合物隔膜是阳离子交换膜,在充电时,阳离子由左向右移动
C.该电池充电时阴极的电极反应式为Li++6C+e−=LiC
6
D.刀片电池可以搭载在新能源汽车上,作为动力来源
【答案】A
【分析】根据电池的总反应方程式可知,放电时,磷酸铁锂做正极,石墨做负极,该
电池工作时,负极的电极反应式为LiC −e−=Li++6C,正极的电极反应式为
6
M Fe PO +Li++e−=LiM Fe PO 。
1−x x 4 1−x x 4
【详解】A.由分析可知:负极的电极反应式为LiC −e−=Li++6C,A项错误;
6
B.根据电极反应式可知,充电时阴极消耗Li+,阳极生成Li+,所以该电池中的聚合
物隔膜是阳离子交换膜,在充电时,Li+由左向右移动,B项正确;
C.根据电池的总反应方程式可知,充电时阴极的电极反应式为Li++6C+e−=LiC
,
6
C项正确;
D.该刀片电池具有多个容纳腔,比能量高,绿色环保,可以搭载在新能源汽车上,
作为动力来源,D项正确;
答案选A。
17.(2023秋·辽宁丹东·高三统考期末)隔膜电解法处理酸性的硝基苯废水,采用惰
性电极,装置示意图如下,下列说法错误的是
17 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司A.M为电源的正极
B.离子膜应为质子交换膜
C.b电极反应式为: +6e-+4H O= +6OH-
2
D.电解一段时间后,理论上左侧电极室溶液pH不变
【答案】C
【分析】根据b电极是 变为 ,化合价降低,得到电子,则b极为阴极,
a极为阳极,N为负极,M为正极。
【详解】A.由分析可知,M为电源的正极,故A正确;
B.a为阳极,M为正极,阳极上,水中OH-失去电子变为氧气,剩余H+,H+穿过离子
膜进入到右边,因此离子膜应为质子交换膜,故B正确;
C.根据电解法处理酸性的硝基苯废水,则b电极反应式为: +6e-+6H+=
+2H O,故C错误;
2
D.电解一段时间后,左侧电极室中生成氧气和H+,H+通过离子膜进入到右侧,左侧
硫酸钠浓度增大,但由于硫酸钠溶液呈中性,因此理论上左侧电极室溶液pH不变,故
D正确;
综上所述,答案为C。
18.(2022秋·贵州铜仁·高三铜仁市第二中学校考阶段练习)利用钠碱循环法可脱除
试卷第18页,共27页烟气中的SO 。在钠碱循环法中Na SO 溶液作为吸收液,当吸收液完全转化为NaHSO
2 2 3 3
溶液时,送至电解槽再生,再生装置如图所示。下列说法正确的是
A.X、Y分别接直流电源正、负极
B.a、b分别为阴、阳离子交换膜
C.阳极主要电极反应式为2H O−4e−=O ↑+4H+
2 2
D.外电路通过1mole−时,X电极区约增加1molNa+
【答案】D
【详解】A.根据再生示意图可知X,Y电极均为HSO−分别发生还原反应、氧化反应,
3
X、Y分别为电解池阴极、阳极,A错误;
B.Na+通过a膜进入X电极区,HSO−通过b膜进入Y电极区,则a、b分别为阳、阴
3
离子交换膜,B错误;
C.阳极区阴离子的放电顺序为HSO−>OH−,故电极主要反应式为
3
HSO−+H O−2e−=3H++SO2−
,C错误;
3 2 4
D.X电极区电极反应为2HSO−+2e−=2SO2−+H ↑,反应前后离子数目几乎不变,当
3 3 2
外电路通过1mol电子时,由于通过a的阳离子有Na+和极少量的H+,故约有1molNa+
通过a膜进入X电极区,D正确;
故选D。
19.(2023·上海·高三专题练习)电解K MnO 水溶液制备KMnO 的装置如图所示。电
2 4 4
解后测得b极区溶液中溶质的总物质的量增大。下列说法错误的是
19 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司A.K MnO 水溶液盛放在a极区
2 4
B.离子交换膜为阳离子交换膜
C.当外电路转移2 mol电子时,两极室溶液质量变化相差76 g
D.“电解法”所得副产品可用作“酸性歧化法”制备KMnO 的原料
4
【答案】C
【分析】电解K MnO 水溶液制备KMnO ,阳极反应为:MnO2−−e−=MnO− ,阴极反应
2 4 4 4 4
为:2H O+2e-=H ↑+2OH- ,K+向阴极移动,使KOH物质的量增大,所以b极为阴极,a
2 2
极为阳极;
【详解】A.a极为阳极,K MnO 水溶液盛放在a极区,A正确;
2 4
B.K+通过离子交换膜向阴极移动,所以离子交换膜为阳离子交换膜,B正确;
C.当外电路转移2 mol电子时,阴极反应2H O+2e-=H ↑+2OH-,有2 molK+移向阴极,
2 2
生成1molH ,阴极质量增大39×2−2=76g,阳极质量减少2×39=78g,两极室溶
2
液质量变化相差154 g,C错误;
D.“电解法”所得副产品KOH,可用作“酸性歧化法”制备KMnO 的原料,D正确;
4
故选C。
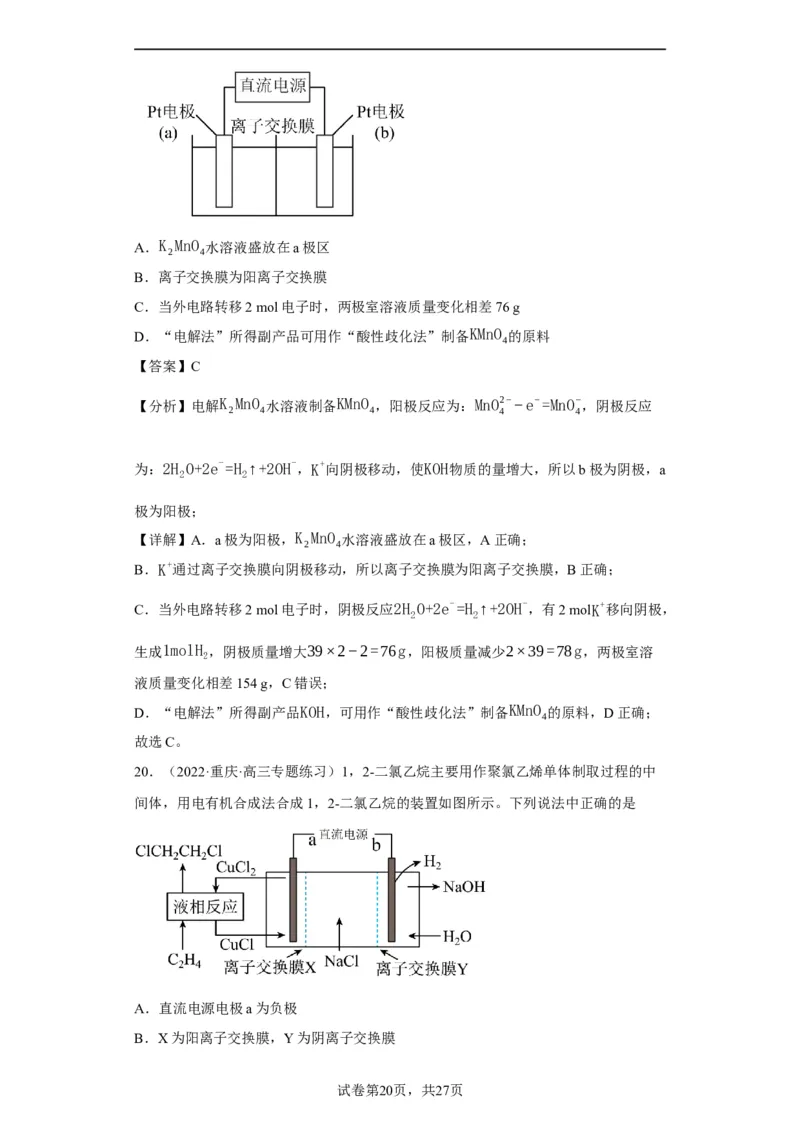
20.(2022·重庆·高三专题练习)1,2-二氯乙烷主要用作聚氯乙烯单体制取过程的中
间体,用电有机合成法合成1,2-二氯乙烷的装置如图所示。下列说法中正确的是
A.直流电源电极a为负极
B.X为阳离子交换膜,Y为阴离子交换膜
试卷第20页,共27页C.液相反应中,C H 被氧化为1,2-二氯乙烷
2 4
电解
D.该装置总反应为2Cl−+2H
2
O ¿2OH−+H ↑+Cl ↑
2 2
¿
【答案】C
【分析】由电解池装置图可知,左侧亚铜离子失去电子生成二价铜离子,为电解池的
阳极,则a为电源正极,溶液中的氯离子经过阴离子交换膜X移向阳极,右侧氢离子
得到电子生成氢气,为阴极,则b为电源的负极,溶液中的钠离子经过阳离子交换膜
Y移向阴极,同时生成氢氧化钠。液相反应中氯化铜与乙烯反应生成1,2—二氯乙烷
和氯化亚铜,据此解答。
【详解】A.根据分析,直流电源电极a为正极,A错误;
B.由分析可知,X为阴离子交换膜,Y为阳离子交换膜,B错误;
C.液相反应中,C H 与CuCl 反应生成1,2-二氯乙烷时碳元素化合价升高,发生氧
2 4 2
化反应,应为C H 被CuCl 氧化为1,2-二氯乙烷,C正确;
2 4 2
D.以NaCl溶液和乙烯为原料合成1,2-二氯乙烷中, CuCl循环使用,其实质是
电解
NaCl、H 2 O与 CH 2 =CH 2 反应,所以总反应为CH 2 =CH 2 +2H 2 O+2NaCl ¿
¿
H↑+2NaOH+ClCH CHCl,D错误;
2 2 2
故答案选C。
21.(2022秋·安徽·高三校联考阶段练习)微生物脱盐电池既可以处理废水中
CH COOH和NH+ ,又可以实现海水淡化,原理如下图所示。下列说法不正确的是
3 4
A.生物电极b为电池的正极
B.电极a的电极反应式为CH COOH−8e−+2H O=2CO ↑+8H+
3 2 2
C.离子交换膜a为阳离子交换膜,离子交换膜b为阴离子交换膜
D.每生成标准状况下2.24LN 时,电路中转移0.6mol电子
2
21 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司【答案】C
【分析】由图可知,a电极上发生氧化反应生成二氧化碳,为负极;b电极上发生还原
反应生成氮气,为正极;
【详解】A.由分析可知,生物电极b为电池的正极,A正确;
B.电极a上CH COOH发生氧化反应生成二氧化碳,电极反应式为
3
CH COOH-8e-+2H O=2CO ↑+8H+ ,B正确;
3 2 2
C.原电池中阳离子向正极、阴离子向负极运动,则氯离子向左侧移动、钠离子向右侧
移动,中间室得到淡水,故离子交换膜b为阳离子交换膜,离子交换膜a为阴离子交
换膜,C错误;
D.NO❑ - 得到电子发生还原反应生成氮气,电子转移为N ∼6e- ,每生成标准状况下
2 2
2.24LN (为0.1mol)时,电路中转移0.6mol电子,D正确;
2
故选C。
22.(2022·重庆·西南大学附中校联考模拟预测)下列如图为光伏并网发电装置,左图
甲基氢氧化铵[(CH ) NOH]常用作电子工业清洗剂,以四甲基氯化铵[(CH ) NCl]为原料,
3 4 3 4
采用电渗析法合成[(CH ) NOH](M=91g/mol)其工作原理如图所示,下列叙述中不正
3 4
确的是
A.图中N型半导体为负极,P型半导体为正极
B.制备18.2g(CH ) NOH,两极共产生4.48L气体(标准状况)
3 4
C.a极电极反应式:2(CH ) N++2H O+2e−=2(CH ) NOH+H ↑
3 4 2 3 4 2
D.c、e均为阳离子交换膜,d为阴离子交换膜
【答案】B
【详解】A.根据第三个池中离子浓度的变化,稀的NaCl溶液变成浓的NaCl溶液,
试卷第22页,共27页Cl-从第二个池,通过d膜移到第三个池中,电解池中,阴离子向阳极移动,所以a为
电解池的阴极,b为阳极,N型半导体为负极,P型半导体为正极,A正确;
18.2g
B.18.2g(CH ) NOH物质的量为: =0.2mol,a电极发生反应为:
3 4 91g/mol
2(CH ) N++2H O+2e-=2(CH ) NOH+H ↑,0.2mol(CH ) NOH,生成0.1molH ,转
3 4 2 3 4 2 3 4 2
移0.2mol电子,b电极发生反应:4OH--4e-=O ↑+2H O,根据得失电子,转移
2 2
0.2mol电子,产生0.5molO ,所以生成的气体总体积为:0.15×22.4=3.36L,B
2
错误;
C.a为阴极,得电子发生还原反应,生成(CH ) NOH,电极反应为:
3 4
2(CH ) N++2H O+2e−=2(CH ) NOH+H ↑,C正确;
3 4 2 3 4 2
D.由图中信息可知,Na+通过e膜,Cl-通过,d膜,(CH ) N+ 通过c膜,则c、e为阳
3 4
离子交换膜,d为阴离子交换膜,D正确;
故选B。
23.(2023·山东·统考高考真题)利用热再生氨电池可实现CuSO 电镀废液的浓缩再生。
4
电池装置如图所示,甲、乙两室均预加相同的CuSO 电镀废液,向甲室加入足量氨水
4
后电池开始工作。下列说法正确的是
A.甲室Cu电极为正极
B.隔膜为阳离子膜
C.电池总反应为:Cu2++4NH =[Cu(NH ) ] 2+
3 3 4
D.NH 扩散到乙室将对电池电动势产生影响
3
【答案】CD
【详解】A. 向甲室加入足量氨水后电池开始工作,则甲室Cu电极溶解,变为铜离子与
23 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司氨气形成[Cu(NH ) ]
2+
,因此甲室Cu电极为负极,故A错误;
3 4
B. 再原电池内电路中阳离子向正极移动,若隔膜为阳离子膜,电极溶解生成的铜离子
要向右侧移动,通入氨气要消耗铜离子,显然左侧阳离子不断减小,明显不利于电池
反应正常进行,故B错误;
C. 左侧负极是Cu−2e−+4NH =[Cu(NH ) ] 2+ ,正极是Cu2++2e−=Cu,则电池总反应
3 3 4
为:Cu2++4NH =[Cu(NH ) ] 2+ ,故C正确;
3 3 4
D. NH 扩散到乙室会与铜离子反应生成[Cu(NH ) ] 2+ ,铜离子浓度降低,铜离子得电子
3 3 4
能力减弱,因此将对电池电动势产生影响,故D正确。
综上所述,答案为CD。
24.(2023·全国·高三专题练习)羟基自由基(⋅OH)具有极强的氧化性,一种能将苯酚
氧化为CO 和H O的组合装置如图所示。下列说法错误的是
2 2
A.离子交换膜n为阴离子交换膜
B.a极的电极反应式为Cr O -+6e-+7H O=2Cr(OH) ↓+8OH-
2 7 2 3
C.b、c两极产生气体的体积比为3:7(标准状况)
D.电池工作时,d极室溶液pH逐渐增大
【答案】AD
【分析】由图可知,左侧为原电池,a极六价铬转化为三价铬发生还原反应,为正极,
则b为负极;右侧为电解池,c为阴极、d为阳极。
【详解】A.b为负极,电极反应式为:C HOH−28e−+11HO=6CO↑+28H+,a为正
6 5 2 2
极,原电池中阳离子向正极移动,生成的氢离子会通过离子交换膜n迁移到左侧,故n
为阳离子交换膜,故A错误;
B.a电极为正极,发生还原反应,电极反应式:Cr O−+6e-+7H O=2Cr(OH) ↓+8OH- ;
2 7 2 3
试卷第24页,共27页故B正确;
C.c极电极反应为:2H++2e−=H ↑;b为负极,电极反应式为:C HOH−28e−+
2 6 5
11HO=6CO↑+28H+,当转移电子数为28时,c极生成14mol气体,b电极生成6mol
2 2
气体,所以b、c两极产生气体的体积比为3:7(标准状况);故C正确;
D.d极为电解池阳极,电极反应为HO−e−=H++•OH,生成氢离子,d极室溶液pH
2
逐渐减小,故D错误;
故答案选AD。
25.(2023·山东烟台·校联考模拟预测)二甲基砜是重要的有机合成中间体,可采用
“成对间接电氧化”法合成。电解槽中某电极区反应过程如图所示,其电解液显碱性。
下列说法正确的是
A.电极反应式为O +2e−+2H+=H O
2 2 2
B.离子交换膜为阴离子交换膜
C.反应前后n(WO2−):n(WO2−)不变
4 5
D.消耗1 mol氧气,理论上可得到1 mol二甲基砜
【答案】CD
【详解】A.其电解液显碱性,则电极反应式为O +2e−+2H O=H O +2OH−,故A
2 2 2 2
错误;
B.惰性电极为阴极,左边产生了氢氧根,阴离子浓度增大,为了使电荷守恒,则阳离
子会向穿过离子交换膜进入,因此离子交换膜为阳离子交换膜,故B错误;
C.左边H O 与WO2−反应生成WO2−和水,WO2−与二甲基亚砜反应生成二甲基砜和WO2−,
2 2 4 5 5 4
因此反应前后n(WO2−):n(WO2−)不变,故C正确;
4 5
D.根据O +2e−+2H O=H O +2OH−,消耗1 mol氧气,得到1mol H O ,又根据左
2 2 2 2 2 2
25 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司边H O 与WO2−反应生成WO2−和水,WO2−与二甲基亚砜反应生成二甲基砜和WO2−,则理
2 2 4 5 5 4
论上可得到1 mol二甲基砜,故D正确。
综上所述,答案为CD。
26.(2023·全国·高三专题练习)目前,应用电渗析法进行海水淡化是解决淡水资源匮
乏的有效途径之一,该方法是利用电解原理通过多组电渗析膜实现,工作原理如图所
示(以NaCl溶液代替海水),同时获得产品Cl、H、NaOH。下列说法错误的是
2 2
A.a是直流电源的正极
B.电极M处产生的气体X为氯气
C.膜pq、st分别为阳离子交换膜、阴离子交换膜
D.出口I、Ⅱ分别接收NaCl浓溶液、淡水
【答案】CD
【详解】A.据图N极生成氢气,可判断b为电源负极,a极与电极M相连,是直流电
源的正极,A正确;
B. a为直流电源的正极,电极M为阳极,溶液中氯离子失去电子,可知X为Cl,B
2
正确;
C.电极N区制备NaOH,Na+通过膜st移入阴极区,溶液中的Cl-通过膜pq移入阳极
区,同时Cl-在阳极区放电生成Cl,阳极区NaCl浓度保持不变,C错误;
2
D.出口I、Ⅱ分别接收淡水、浓NaCl溶液,D错误;
故选CD。
27.(2023·全国·高三专题练习)微生物脱盐电池是一种高效、经济的能源装置,利用
微生物处理有机废水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用
惰性电极,用下图装置处理有机废水(以含CH COO−的溶液为例)。下列说法错误的是
3
试卷第26页,共27页A.负极反应为CH COO−+2H O−8e−=2CO +7H+
3 2 2
B.隔膜1为阳离子交换膜,隔膜2为阴离子交换膜
C.当电路中转移1mol电子时,模拟海水理论上除盐58.5g
D.加热a极区,升高温度,以加快反应速率,提升电池的效率
【答案】BD
【分析】由图可知,碳元素价态升高失电子,a极为负极,电极反应式为CHCOO−+
3
2HO−8e−=2CO ↑+7H+,b极为正极,电极反应式为2H++2e−=H↑,据此作答。
2 2 2
【详解】A.a极为负极,电极反应式为CHCOO−+2HO−8e−=2CO ↑+7H+,故A正
3 2 2
确;
B.左侧正电荷增加,氯离子透过隔膜1进入左侧,隔膜1为阴离子交换膜,右侧正电
荷减少,钠离子透过隔膜2进入右侧,隔膜2为阳离子交换膜,故B错误;
C.当电路中通过8mol电子时,正极产生4mol氢气,负极产生2mol二氧化碳,正、
负极产生气体的物质的量之比为4mol:2mol=2:1,故C正确;
D.该装置为微生物脱盐电池,温度过高会导致微生物死亡,海水淡化效果变差,故D
错误;
故答案选BD。
【点睛】本题考查原电池原理,题目难度中等,能依据图像和题目信息准确判断正负
极是解题的关键,难点是电极反应式的书写。
28.(2023·山东·高三专题练习)钾离子电池因其低成本和较高的能量/功率密度,引
放电
起了广泛关注。一种钾离子电池的总反应为xKC +K MnO ⇌8xC+K MnO ,其
8 0.5−x 2 0.5 2
充电
工作原理如图所示。下列说法正确的是
27 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司A.该电池的交换膜为阳离子交换膜
B.充电时,a极接电源的负极发生氧化反应
C.放电时,b极发生的反应为K MnO +xK++xe−=K MnO
0.5−x 2 0.5 2
D.放电时,理论上电路通过4mole−,a极质量减小39g
【答案】AC
放电
【分析】总反应:xKC +K MnO ⇌8xC+K MnO ,放电时,a极:
8 0.5−x 2 0.5 2
充电
KC −e−=K++8C;b极:K MnO +xK++xe−=K MnO ,因此该电池交换膜为阳
8 0.5−x 2 0.5 2
离子交换膜,以保证充放电时K+能够顺利通过。
【详解】A.由分析可知,该电池的交换膜为阳离子交换膜,A正确;
B.根据总反应可知,充电时,a极电极反应式为:8C+e−+K+=KC
,因此a极接电源
8
的负极,发生还原反应,B错误;
C.由总反应式可知,放电时,b极发生的反应为K MnO +xK++xe−=K MnO ,C
0.5−x 2 0.5 2
正确;
D.放电时,a极电极反应式为:KC −e−=K++8C,当转移1个电子时,a极减少一个
8
K+的质量;当电路通过4mole−,a极减少4molK+的质量,即146g,D错误。
本题选AC。
29.(2022秋·湖南长沙·高三雅礼中学校考阶段练习)钠碱脱硫液(NaOH+Na SO )吸
2 3
收一定量SO 气体后,可通过以下装置实现再生。下列说法正确的是
2
试卷第28页,共27页A.电极a为负极 B.m应为阳离子交换膜
C.出液2仍为HSO ,与进液的浓度相同 D.出液1可使溴水褪色
2 4
【答案】BD
【分析】此装置的作用是在左侧生成钠碱脱硫液(NaOH+Na SO ),因此脱硫完后的溶
2 3
液在阴极区发生析氢反应,生成OH-使阴极区pH上升,过量的OH-与HSO−反应生成
3
SO2− 或与Na+结合生成NaOH。所以左侧再生液为NaOH和Na SO 溶液,由电荷守恒,
3 2 3
中间区的Na+进入左侧,而在右侧,发生氧化反应2H O−4e−=O +4H+ ,H+透过阳膜
2 2
进入中间区,因此,出液1为H SO 溶液。此反应本质是双阳膜电解法。
2 3
【详解】A.电极a,发生还原反应4H O+4e−=4OH−+2H ↑,为阴极,故A错误;
2 2
B.由以上分析知,左侧发生析氢反应,有电荷守恒,中间区的H+和Na+进入左侧,所
以m为阳离子交换膜,在左侧出现再生液,故B正确;
C.由于右侧水放电,放氧生酸,水的量减少,故H SO 的浓度变大,故C错误;
2 4
D.由以上分析知出液1为H SO 溶液,H SO 可与溴水发生氧化还原反应而使溴水褪
2 3 2 3
色,故D正确;
故答案选BD。
30.(2022·河北邯郸·邯郸一中校考模拟预测)据2022年1月统计,我国光伏发电并
网装机容量突破3亿千瓦,连续七年稳居全球首位。已知四甲基氢氧化铵[(CH )NOH]
3 4
常用作电子工业清洗剂,以四甲基氯化铵[(CH )NCl]为原料,采用电渗析法合成
3 4
[(CH )NOH],工作原理如图。下列说法正确的是
3 4
29 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司A.光伏并网发电装置中N型半导体为正极
B.c、e为阳离子交换膜,d为阴离子交换膜
C.保持电流恒定,温度越高合成四甲基氢氧化铵的速率越快
D.制备182g四甲基氢氧化铵,两极共产生33.6L气体(标准状况)
【答案】BD
【分析】根据第三个池中浓度变化得出,钠离子从第四池通过e膜,氯离子从第二池
通过d膜,由电解池中阳离子向阴极移动,阴离子向阳极移动,则a为阴极,电极反
应式为2(CH ) N++2H O+2e-=2(CH ) NOH+H ↑,b为阳极,电极反应式为
3 4 2 3 4 2
4OH--4e-=O +2H O,a与N型半导体相连,b与P型半导体相连,所以N型半导体为
2 2
负极,P型半导体为正极,据此分析解答。
【详解】A.由分析可知,N型半导体为负极,A错误;
B.Na+离子通过e膜,Cl-通过d膜,(CH)N+通过c膜,所以c、e膜为阳离子交换膜,
3 4
d为阴离子交换膜,B正确;
C.温度过高,四甲基氯化铵[(CH )NCl]会分解,四甲基氯化铵浓度降低,不能加快合
3 4
成四甲基氢氧化铵的速率,C错误;
182g
D.182g(CH ) NOH的物质的量为 =2mol,a极电极反应式为
3 4 91g/mol
2(CH ) N++2H O+2e-=2(CH ) NOH+H ↑,则收集氢气1mol,转移电子为2mol,b极
3 4 2 3 4 2
电极反应式为4OH--4e-=O +2H O,则收集氧气为0.5mol,标况下两极可得气体体积
2 2
为1.5mol×22.4L/mol=33.6L,D正确;
答案选BD。
试卷第30页,共27页