文档内容
第 02 讲 原子结构与性质
目 录
01 考情透视·目标导航.........................................................................................................................2
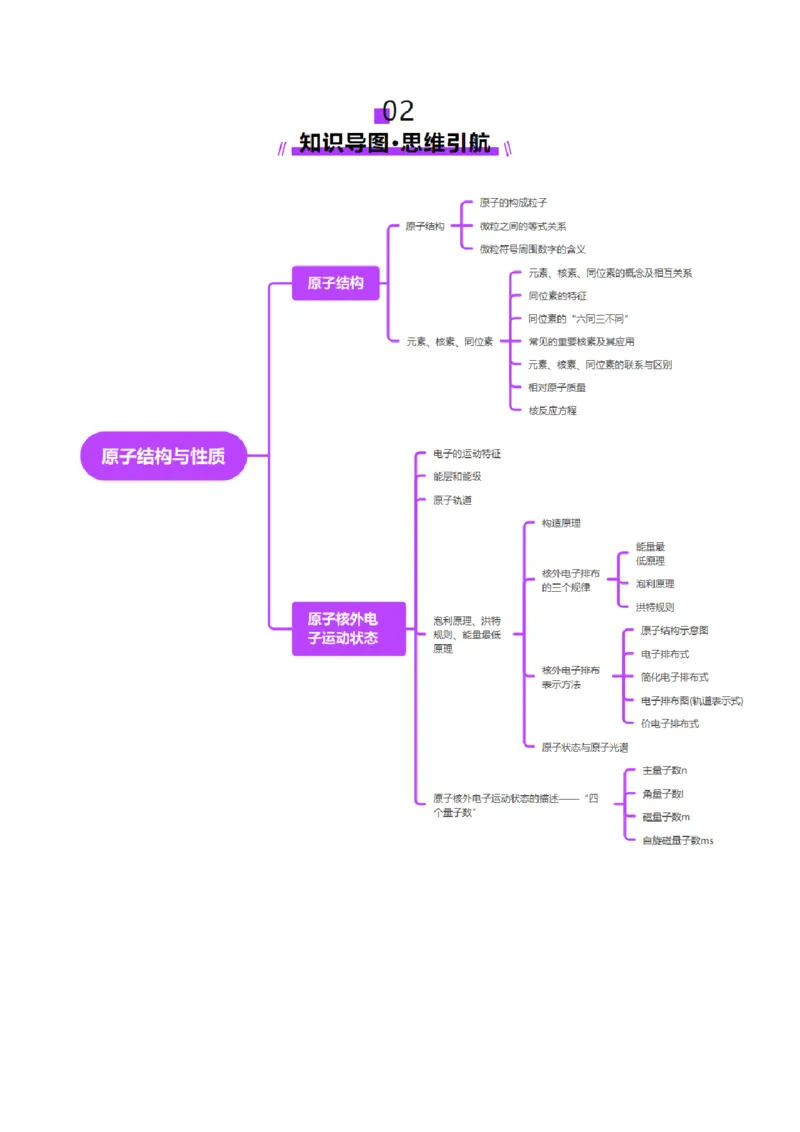
02 知识导图·思维引航.........................................................................................................................3
03 考点突破·考法探究.........................................................................................................................4
考点一 原子结构.........................................................................................................................4
知识点1 原子结构...................................................................................................................4
知识点2 元素、核素、同位素...............................................................................................5
考向1 考查核反应方程的简单分析.......................................................................................6
考向2 考查“五同”概念辨析...............................................................................................7
考点二 原子核外电子运动状态.................................................................................................8
知识点1 电子的运动特征.......................................................................................................8
知识点2 能层和能级...............................................................................................................8
知识点3 原子轨道——电子在原子核外的一个空间运动状态..........................................9
知识点4 泡利原理、洪特规则、能量最低原理...................................................................9
知识点5 原子核外电子运动状态的描述——“四个量子数”........................................11
考向1 电子排布式表达式的规范书写.................................................................................11
考向2 电子跃迁与原子光谱.................................................................................................13
04 ........................................................................................................................................................14考点要求 考题统计 考情分析
2024·广东卷第3题,2分 分析近三年的高考试题,高考命题在本讲有以下规律:
2024·湖北卷第12题,3分 1.从考查题型和内容上看,高考命题以选择题、非选择题
2024·北京卷第1题,3分 呈现,考查内容主要有以下3个方面:
2024·上海卷第2题,3分 (1)元素、核素、同位素、同素异形体概念的辨析。
2024·河北卷第8题,3分 (2)原子中质量数、质子数、中子数、核外电子数之间的
原子结构 2023湖南卷第2题,3分 相互关系及计算。
(3)根据原子核外电子排布判断元素种类、书写电子排布
2023·江苏卷第5题,3分
式和电子排布图。
2022·北京卷第3题,3分
2.从命题思路上看,主要以选择题的形式为主。
2022·天津卷第10题,3分
(1)选择题
2022浙江1月卷第7题,2分
以最新的科技成果、新闻事件为背景,考查原子结构、同
2021卷广东卷第3题,2分
位素、核素知识,核外电子排布表达式的正误判断。
(2)非选择题
2024·江苏卷第4题,3分
直接考查电子排布式和电子排布图的书写,利用核外电子
2024·甘肃卷第2题,3分
排布推断元素等。
2024·山东卷第3题,3分
3.根据高考命题的特点和规律,复习时要注意以下几个方
2023·北京卷第2题,3分
面:
原子核外电
2023浙江1月卷第3题,2分
(1)同位素和同素异形体的概念分析、原子构成微粒之间
子运动状态
2022·海南卷第5题,2分
的关系。
2022浙江六卷第7题,2分
(2)原子结构及核外电子排布特性(全空、半充满、全充
2022·北京卷第2题,3分
满的稳定性)。
2021天津卷第20题(1),2分
(3)规范化学术语的书写,重点掌握第四周期过渡元素的
电子排布式和电子排布图。
复习目标:
1.能说明微观粒子的运动状态与宏观物体运动特点的差异。
2.能结合能量最低原理、泡利原理、洪特规则书写1~36号元素基态原子的核外电子排布式和电子排布图,
并说明含义。考点一 原子结构
知识点1 原子结构
1.原子的构成粒子
2.微粒之间的等式关系
1)质量关系:质量数(A)=质子数(Z)+中子数(N);
2)电性关系:
①原子中:质子数(Z)=核电荷数=核外电子数;
②阳离子的核外电子数=质子数-阳离子所带的电荷数,如Mg2+的核外电子数是10。
③阴离子的核外电子数=质子数+阴离子所带的电荷数,如Cl-的核外电子数是18。
3.微粒符号周围数字的含义
【特别提醒】①原子中不一定都含有中子,如H中没有中子。
②电子排布完全相同的原子不一定是同一种原子,如互为同位素的各原子。
③易失去1个电子形成+1价阳离子的不一定是金属原子,如氢原子失去1个电子形成H+。
④形成稳定结构的离子最外层不一定是8个电子,如Li+为2个电子稳定结构。
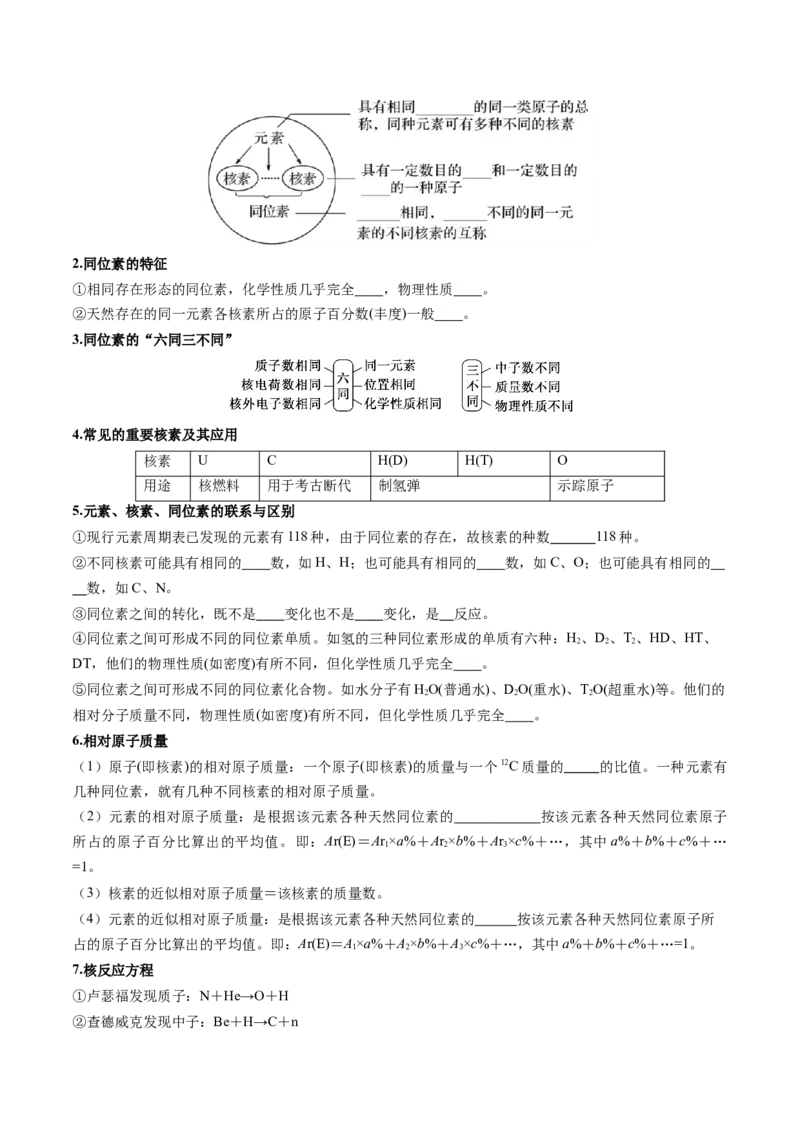
知识点2 元素、核素、同位素
1.元素、核素、同位素的概念及相互关系2.同位素的特征
①相同存在形态的同位素,化学性质几乎完全相同,物理性质不同。
②天然存在的同一元素各核素所占的原子百分数(丰度)一般不变。
3.同位素的“六同三不同”
4.常见的重要核素及其应用
核素 U C H(D) H(T) O
用途 核燃料 用于考古断代 制氢弹 示踪原子
5.元素、核素、同位素的联系与区别
①现行元素周期表已发现的元素有118种,由于同位素的存在,故核素的种数远大于 118种。
②不同核素可能具有相同的质子数,如H、H;也可能具有相同的中子数,如C、O;也可能具有相同的质
量数,如C、N。
③同位素之间的转化,既不是物理变化也不是化学变化,是核反应。
④同位素之间可形成不同的同位素单质。如氢的三种同位素形成的单质有六种:H、D、T、HD、HT、
2 2 2
DT,他们的物理性质(如密度)有所不同,但化学性质几乎完全相同。
⑤同位素之间可形成不同的同位素化合物。如水分子有HO(普通水)、DO(重水)、TO(超重水)等。他们的
2 2 2
相对分子质量不同,物理性质(如密度)有所不同,但化学性质几乎完全相同。
6.相对原子质量
(1)原子(即核素)的相对原子质量:一个原子(即核素)的质量与一个12C质量的_____的比值。一种元素有
几种同位素,就有几种不同核素的相对原子质量。
(2)元素的相对原子质量:是根据该元素各种天然同位素的相对原子质量按该元素各种天然同位素原子
所占的原子百分比算出的平均值。即:Ar(E)=Ar×a%+Ar×b%+Ar×c%+…,其中a%+b%+c%+…
1 2 3
=1。
(3)核素的近似相对原子质量=该核素的质量数。
(4)元素的近似相对原子质量:是根据该元素各种天然同位素的质量数按该元素各种天然同位素原子所
占的原子百分比算出的平均值。即:Ar(E)=A×a%+A×b%+A×c%+…,其中a%+b%+c%+…=1。
1 2 3
7.核反应方程
①卢瑟福发现质子:N+He→O+H
②查德威克发现中子:Be+H→C+n③铀核裂变反应:U+n→Kr+Ba+3n
④氘核与氚核聚变反应:H+H→He+n
考向1 考查核反应方程的简单分析
例1科学家利用 粒子(即氦核 )进行多种核反应: 、 。已知
和 都具有放射性,下列说法错误的是
A.X元素位于元素周期表的第二周期第ⅥA族
B. 和 互为同位素,化学性质相同
C. 、 都可作为示踪原子
D.核反应产生的能量可用于发电,属于化学能转化为电能
【思维建模】核反应方程分析思路
(1)质量数守恒:各微粒左上角数字之和在核反应前后相等;
(2)电荷数守恒:各微粒左下角数字之和(正电荷数)在核反应前后相等
例:碳14的β衰变:C→N+e
质量数守恒表达式:14=14+0;电荷数守恒表达式:6=7-1。
【变式训练1】(2024·山东泰安·三模)核反应 和 为研究原子结构和发现
新原子做出了重要贡献。下列说法错误的是
A.c=13b
B.X、Y、Z形成的单质分子均为非极性分子
C.Q、R 为质量数相同的不同核素
D.基态 W 与Z原子核外电子的空间运动状态种类相等
【变式训练2】(23-24高三下·河北石家庄·阶段考试)卢瑟福发现质子的核反应为 ;卢瑟
福的学生查德威克发现中子的核反应为 。下列说法错误的是
A.Y元素的第一电离能高于同周期相邻元素的
B.元素的电负性:
C. 和 的简单氢化物中中心原子的价层电子对数目相同
D. 的空间结构为直线形
考向2 考查“五同”概念辨析
例2(2024·浙江杭州·模拟预测)下列说法不正确的是
A. 和 互为同位素 B.石墨烯和丙烯互为同系物
C.氧气和臭氧互为同素异形体 D.乙酸甲酯和甲酸乙酯互为同分异构体
【思维建模】同系物、同分异构体、同位素、同素异形体、同种物质的比较\s\up11(
定义 比较对象 分子式 结构 性质
比较)
质子数相同、
符号表示不 电子排布相 物理性质不相
中子数不同的
同位素 核素(原子) 同,如:H、 同,原子核结 同,化学性质
核素(原子)互
H、H 构不同 相同
称为同位素
元素符号表示
相同,分子式 物理性质不
同一元素组成 单质的组成或
同素异形体 单质 可不同,如: 同,化学性质
的不同单质 结构不同
金刚石和石 相似
墨、O 和O
2 3
分子式相同,
物理性质不
结构不同的化
同分异构体 化合物 相同 不同 同,化学性质
合物互称为同
不一定相同
分异构体
分子式和结构
同种物质 式都相同的物 - 相同 相同 相同
质
结构相似,分
物理性质不
子组成上相差
同系物 化合物 不相同 相似 同,化学性质
若干个CH 原
2
相似
子团的有机物
【变式训练1】(2024·江西宜春·模拟预测)科技发展与化学密切相关。下列说法错误的是
A.TiO 光催化乙苯脱氢转化为苯乙烯,两种有机物互为同分异构体
2
B.科研团队合成环状的C 和C ,C 和C 互为同素异形体
10 14 10 14
C.铌酸锂(LiNbO)纳米超材料具有独特光学特性, 的中子数为52
3
D.通过原电池原理将氮气和氢气转化为NH 同时放出电能,该过程属于人工固氮的过程
3
【变式训练2】(2024·广东东莞·模拟预测)科学技术是第一生产力,下列说法正确的是
A.“海基一号”成功从深海开采石油和天然气水合物,天然气属于新能源
B.我国首次获得公斤级丰度99%100Mo产品,100Mo与98Mo互为同位素
C.“煤制烯现代化成套技术开发及应用”中煤的气化属于物理变化
D.“歼-35”战斗机机翼所使用的“碳纤维布”(聚丙烯腈经碳化而成)与金刚石互为同素异形体
考点二 原子核外电子运动状态
知识点1 电子的运动特征电子是质量轻、带负电的微观粒子,并具有波粒二象性。电子可以在原子内部进行圆周运动,运动速度很
快,接近光速,与宏观物体的运动有极大不同:不能同时确定速度和位置,不能描绘运动轨迹。
知识点2 能层和能级
1.能层:根据多电子原子的核外电子的能量差异,将核外电子分成不同的能层,能层用n 表示。n值越大,
能量越高。
2.能级
(1)根据多电子原子中同一能层电子能量的不同,将它们分成不同能级。
(2)能级用相应能层的序数和字母s、p、d、f组合在一起来表示,如n能层的能级按能量由低到高的顺
序排列为 n s 、 n p 、 n d 、 n f 等。
(3)能层序数等于该能层所包含的能级数,如第三能层有 3s 、 3p 、 3d 能级。
(4)s、p、d、f能级可容纳的电子数为1、3、5、7的二倍。
3.能层、能级与其容纳的最多电子数之间的关系
能层(n) 一 二 三 四 五 六 七 …
符号 K L M N O P Q …
能级 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s … … … …
容 纳 最 2 2 6 2 6 10 2 6 10 14 2 … … … …
多 电 子
2 8 18 32 …… … … 2n2
数
知识点3 原子轨道——电子在原子核外的一个空间运动状态
1.电子云:电子云是处于一定空间运动状态的电子在原子核外空间的 概率密 度 分布的形象化描述。小黑点
越密,表示概率密度越大。由于核外电子的概率密度分布看起来像一片云雾,因而被形象地称作电子云。
2.电子轮廓图:
概率密度 为 90% 的 电子云图,s电子云轮廓图是球形;p电子云轮廓图是哑铃形,p电子云有三种伸展方向
(p,p,p,它们相互垂直),即p能级电子有3 个伸展方向;d能级电子有5 个伸展方向;f能级电子有
x y z
7 个伸展方向。
3.原子轨道:量子力学把电子在原子核外的一个空间运动状态称为一个原子轨道,即电子云的伸展方向。
能级符号 电子云形状 空间延伸方向
s 球形 一种
三种(相互垂直,分别相对
p 哑铃形
于x、y、z轴对称)
d / /
f / /
4.轨道能量
①同能层的不同能级能量s