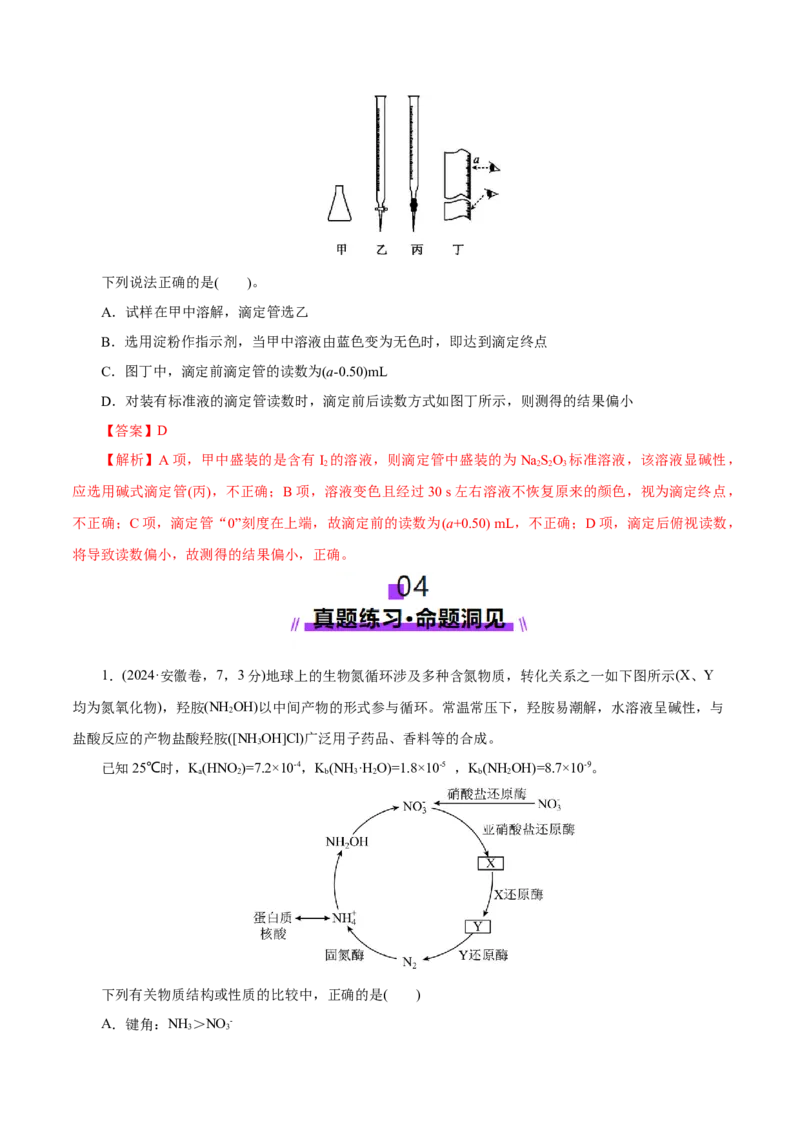
文档内容
第 02 讲 水的电离和溶液的酸碱性
目录
01
考情透视·目标导航
02 知识导图·思维引航...................................................................................................................
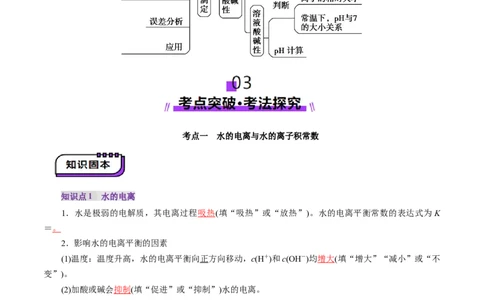
03考点突破·考法探究....................................................................................................................
考点一 物水的电离与水的离子积常数.......................................................................................
知识点1 水的电离.....................................................................................................................
知识点2 水的离子积..................................................................................................................
考向1 水的电离及影响因素........................................................................................................
考向2 水的电离平衡曲线...........................................................................................................
考向3 水电离的c(H+)或c(OH-)的计算.........................................................................................
考点二 溶液的酸碱性与pH.........................................................................................................
知识点1 溶液的酸碱性............................................................................................................
知识点2 溶液的pH..................................................................................................................
知识点3 溶液pH的计算..........................................................................................................
考向1 溶液的酸碱性与pH........................................................................................................
考向2 溶液pH的计算..............................................................................................................
考向3 酸碱溶液稀释后酸碱性的判断........................................................................................
考点二 酸碱中和滴定...................................................................................................................
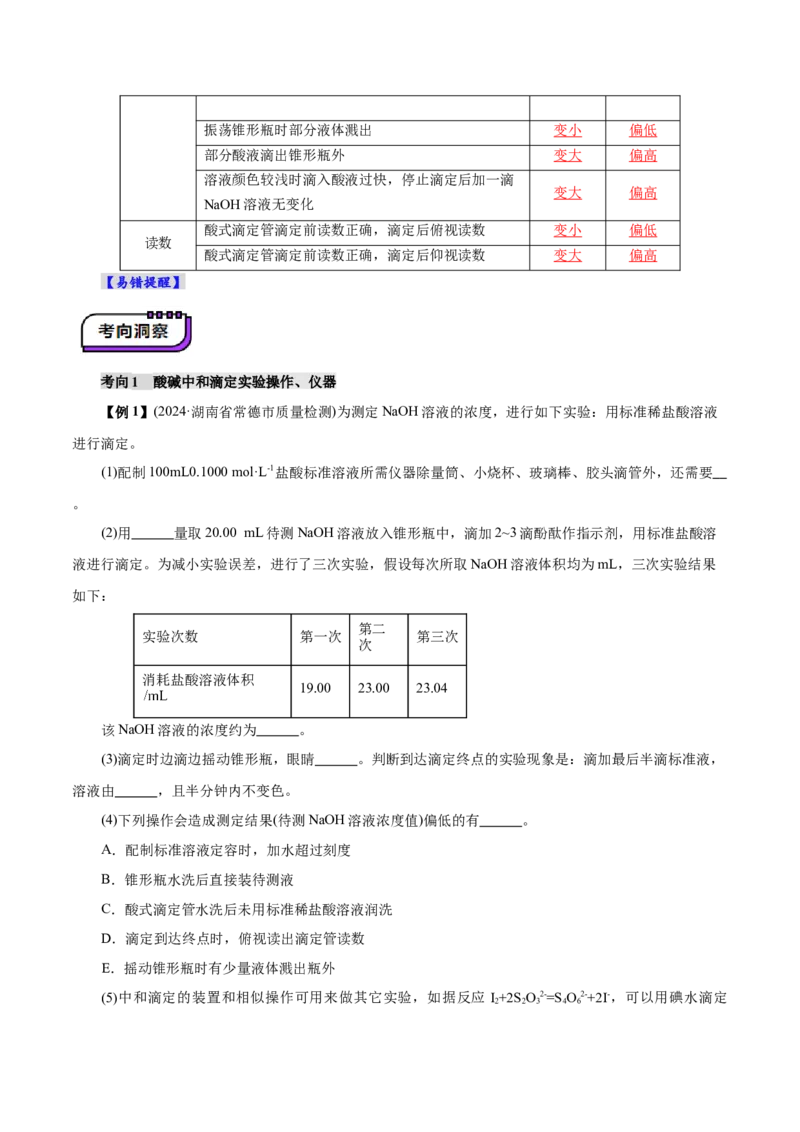
知识点1 酸碱中和滴定的原理与操作.......................................................................................
知识点2 误差分析...................................................................................................................
考向1 酸碱中和滴定实验操作、仪器........................................................................................
考向2 酸碱中和滴定图像.........................................................................................................
考向3 酸碱中和滴定误差分析..................................................................................................
04真题练习·命题洞见....................................................................................................................考点要
考题统计 考情分析
求
2024·安徽卷7题,3分;2024· 本讲常见的命题形式:(1)结合图像考查溶液的酸
水的电离和 安徽卷7题,3分;2024·山东
碱性判断、pH的计算,以及离子浓度的大小比较等;
溶液的酸碱 卷10题,2分;2022·浙江省1
性 月选考1题,2分;2022·浙江 (2)以酸碱中和滴定为载体,考查“强”滴“弱”过程
省1月选考17题,2分
中微粒浓度的变化以及其他相关知识;(3)以滴定为基
础,考查相关操作和计算等。预测本考点依然会结合
2023湖南卷12题,4分;2021
图像,考查水的电离平衡与溶液酸碱性的关系,以及
酸碱中和滴 辽宁卷15题,3分;2021湖北
pH的相关计算等;还会基于中和滴定,考查氧化还原
定 卷14题,3分;2021海南卷14
题,4分; 滴定、沉淀滴定等有关计算,注意滴定现象、操作、
滴定终点判断的规范表达,能进行误差分析。
复习目标:
1.了解水的电离、离子积常数(K )。
w
2.了解溶液pH的含义及其测定方法,能进行pH的简单计算。
3.能选择实例说明溶液pH的调控在工农业生产和科学研究中的重要作用。
4.理解酸碱中和滴定,能根据实验试题要求分析或处理实验数据,得出合理结论;能够分析以图
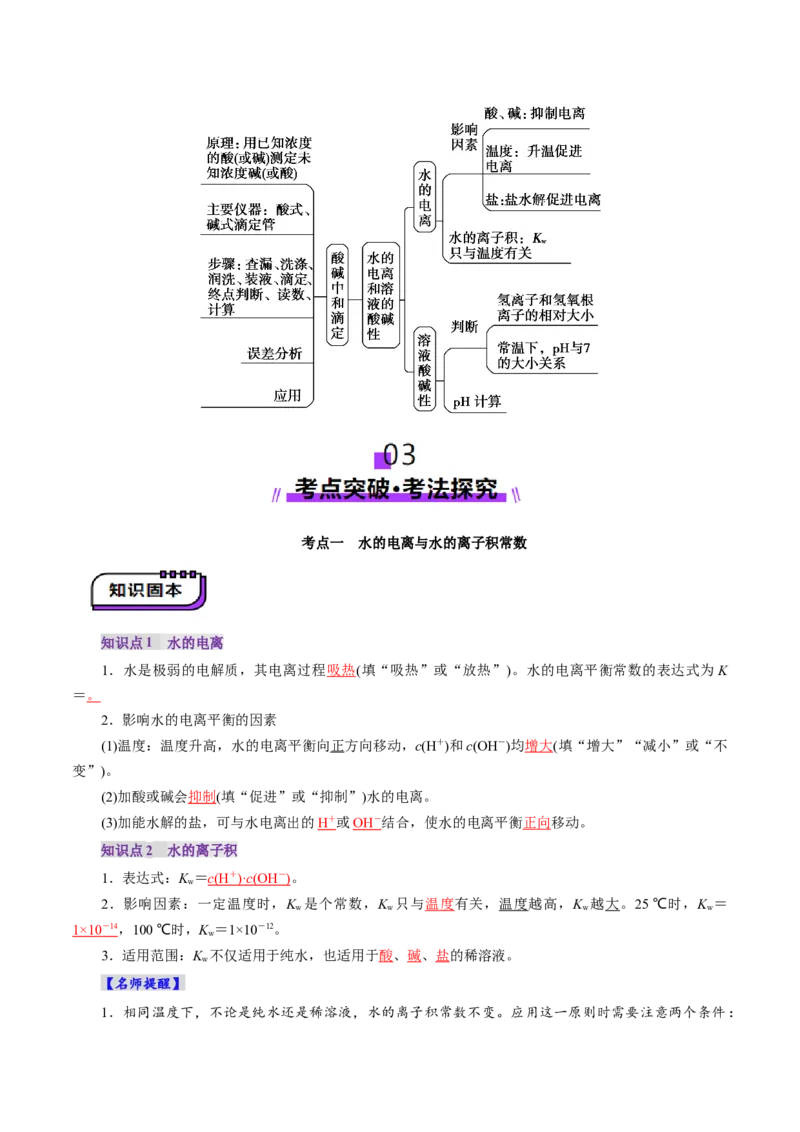
像形式考查滴定曲线。考点一 水的电离与水的离子积常数
知识点1 水的电离
1.水是极弱的电解质,其电离过程吸热(填“吸热”或“放热”)。水的电离平衡常数的表达式为K
=。
2.影响水的电离平衡的因素
(1)温度:温度升高,水的电离平衡向正方向移动,c(H+)和c(OH-)均增大(填“增大”“减小”或“不
变”)。
(2)加酸或碱会抑制(填“促进”或“抑制”)水的电离。
(3)加能水解的盐,可与水电离出的 H + 或 OH - 结合,使水的电离平衡正向移动。
知识点2 水的离子积
1.表达式:K = c (H + )· c (OH - ) 。
w
2.影响因素:一定温度时,K 是个常数,K 只与温度有关,温度越高,K 越大。25 ℃时,K =
w w w w
1×10 - 14 ,100 ℃时,K =1×10-12。
w
3.适用范围:K 不仅适用于纯水,也适用于酸、碱、盐的稀溶液。
w
【名师提醒】
1.相同温度下,不论是纯水还是稀溶液,水的离子积常数不变。应用这一原则时需要注意两个条件:水溶液必须是稀溶液;温度必须相同。
2.关注酸式盐的特殊性,如硫酸氢钠完全电离,会抑制水的电离,碳酸氢钠以水解为主,呈碱性,
促进水的电离。
考向1 水的电离及影响因素
【例1】25 ℃时,水存在平衡状态:HO H++OH- ΔH>0。下列叙述正确的是( )。
2
A.加热,K 增大,c(OH-)增大
w
B.滴入稀氨水,水的电离平衡向左移动,c(OH-)减小,K 减小
w
C.加入少量NaHSO 固体,水的电离平衡向左移动,c(H+)减小,K 不变
4 w
D.加入少量金属Na,水的电离平衡向右移动,c(H+)增大
【答案】A
【解析】水的电离是吸热过程,升高温度,平衡右移,c(H+)、c(OH-)同等程度地增大,K 增大;K 只
w w
受温度影响,向水中加稀氨水,水的电离平衡左移,c(OH-)增大,K 不变;加入少量NaHSO 固体,因
w 4
NaHSO=Na++H++SO2-,c(H+)增大,水的电离平衡左移,K 不变;加入少量Na,Na与水电离出的H+反应,
4 4 w
水的电离平衡右移,c(H+)减小,c(OH-)增大。
【思维建模】
1.抑制水电离的方法。
(1)外加酸或碱;
(2)加入强酸的酸式盐固体(如NaHSO);(3)通入酸性气体(如CO、SO )或碱性气体(如NH );
4 2 2 3
(4)降温。
2.促进水电离的方法。
(1)升温;(2)加入强酸弱碱盐或强碱弱酸盐或弱酸弱碱盐。
【变式训练】已知液氨的性质与水相似。T ℃时,NH +NH
NH+ +NH- ,NH+
的平衡浓度为
3 3 4 2 4
1×10-15 mol·L-1。下列说法错误的是( )。
A.在此温度下液氨的离子积为1×10-30
B.在液氨中加入金属钠,可生成NaNH
2
C.恒温下,在液氨中加入NH Cl,可使液氨的电离平衡逆向移动
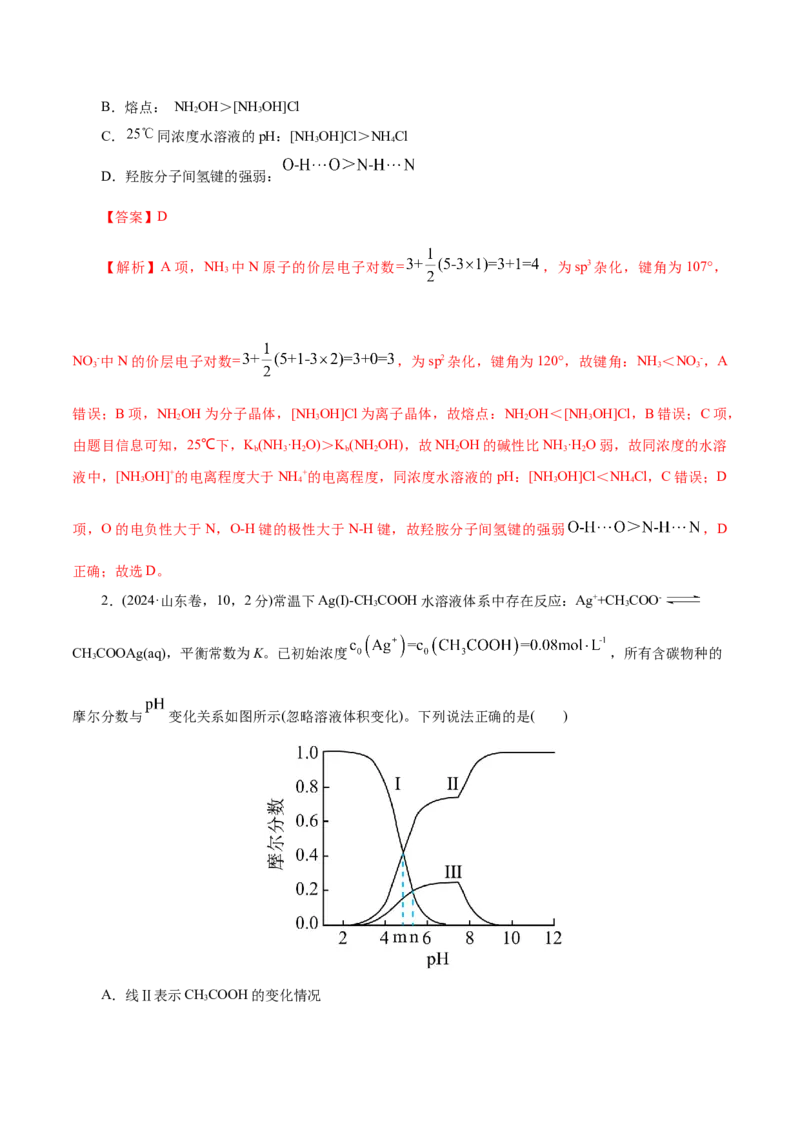
4D.降低温度,可使液氨的电离平衡逆向移动,且c(NH+ )25)( )
A.图中A、B、D三点处K 的大小关系:B>A>D
w
c(N H+)
B.25 ℃时,向pH=1的稀硫酸中逐滴加入pH=8的稀氨水,溶液中 4 逐渐减小
c(N H ·H O)
3 2
C.25 ℃时,保持温度不变,在水中加入适量NH Cl固体,体系可以从A点变化到C点
4
D.A点所对应的溶液中,可同时大量存在Na+、Fe3+、Cl-、SO2-
4
【答案】B
【解析】A、D两点都处于25 ℃的条件下,K 相等,B点温度大于25 ℃,水的电离是吸热过程,温
w
度越高,K 越大,故题图中 A、B、D 三点处 K 的大小关系为 B>A=D,A 错误;K (NH ·H O)=
w w b 3 2
c(N H+
4
)·c(OH-) ,则 c(N H+
4
) = K
b
(N H
3
·H
2
O) ,25 ℃时,K
b
(NH
3
·H
2
O)为定值,
c(N H ·H O) c(N H ·H O) c(OH-)
3 2 3 2
向 pH=1 的稀硫酸中逐滴加入 pH=8 的稀氨水的过程中,pH 逐渐增大,即 c(OH-)逐渐增大,则K
b
(N H
3
·H
2
O)
逐渐减小,即
c(N H+
4
)
逐渐减小,B正确;温度不变,K
w
不变,向水中加
c(OH-) c(N H ·H O)
3 2
入适量氯化铵固体,溶液中c(H+)增大,c(OH-)减小,而A点到C点过程中c(H+)、c(OH-)都增大,C错误;
A点所对应的溶液中,pH=7,Fe3+不能大量存在,D错误。
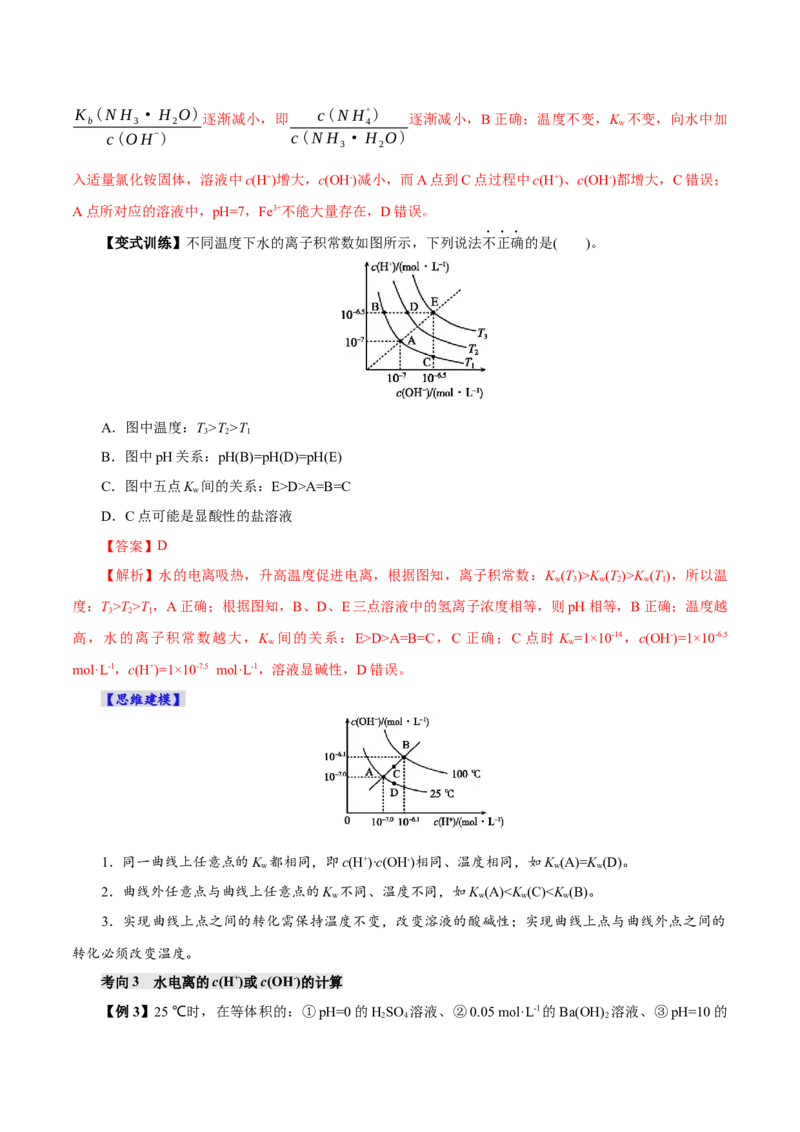
【变式训练】不同温度下水的离子积常数如图所示,下列说法不正确的是( )。
A.图中温度:T>T >T
3 2 1
B.图中pH关系:pH(B)=pH(D)=pH(E)
C.图中五点K 间的关系:E>D>A=B=C
w
D.C点可能是显酸性的盐溶液
【答案】D
【解析】水的电离吸热,升高温度促进电离,根据图知,离子积常数:K (T)>K (T)>K (T),所以温
w 3 w 2 w 1
度:T>T>T ,A正确;根据图知,B、D、E三点溶液中的氢离子浓度相等,则pH相等,B正确;温度越
3 2 1
高,水的离子积常数越大,K 间的关系:E>D>A=B=C,C 正确;C 点时 K =1×10-14,c(OH-)=1×10-6.5
w w
mol·L-1,c(H+)=1×10-7.5 mol·L-1,溶液显碱性,D错误。
【思维建模】
1.同一曲线上任意点的K 都相同,即c(H+)·c(OH-)相同、温度相同,如K (A)=K (D)。
w w w
2.曲线外任意点与曲线上任意点的K 不同、温度不同,如K (A)”、“<”或“=”)1×10-14,理由是 。
1 2 w
(2)在t ℃时,测得纯水中的c(H+)=2.4×10-7 mol·L-1,则c(OH-)= mol·L-1。该温度下,测得某
1
HSO
溶液中c(SO2-
)=5×10-6 mol·L-1,该溶液中c(OH-)= mol·L-1。
2 4 4
(3)25 ℃时,pH=10的NaOH溶液和NaCO 溶液中,水电离出的c (OH-)分别为 mol·L-1和
2 3 水
mol·L-1。
【答案】(1)> 水的电离是吸热过程,升高温度,平衡向电离方向移动,c(H+)增大,c(OH-)增大,
K =c(H+)·c(OH-),K 增大
w w(2)2.4×10-7 5.76×10-9 (3)1×10-10 1×10-4
【解析】(1)水是弱电解质,存在电离平衡,电离吸热,所以温度升高,水的离子积增大。(2)水电离出
的 c(H+)和 c(OH-)相等,K =2.4×10-7×2.4×10-7=5.76×10-14。该温度下,某 HSO 溶液中 c(H+)=1×10-5
w 2 4
5.76×10-14
mol·L-1,c(OH-)= mol·L-1=5.76×10-9 mol·L-1。(3)pH=10说明c(H+)=1×10-10 mol·L-1,水电离产
1×10-5
生的 c(H+)与 c(OH-)相等,所以 pH=10 的 NaOH 溶液中水电离出的 c(OH-)=1×10-10 mol·L-1;pH=10 的
NaCO 溶液中c(OH-)=10-4 mol·L-1,全部来自水的电离。
2 3
考点二 溶液的酸碱性与pH
知识点1 溶液的酸碱性
溶液的酸碱性取决于c(H+)和c(OH-)的相对大小
常温下
溶液的酸碱性 c(H+)与c(OH-) 比较
c(H+)大小 pH
酸性溶液 c(H+)>c(OH-) c(H+)>1.0×10-7mol·L-1 <7
中性溶液 c(H+)=c(OH-) c(H+)=1.0×10-7mol·L-1 =7
碱性溶液 c(H+)7
知识点2 溶液的pH
1.计算公式:pH= - lg c (H + )。
2.溶液的酸碱性与pH的关系(25 ℃):
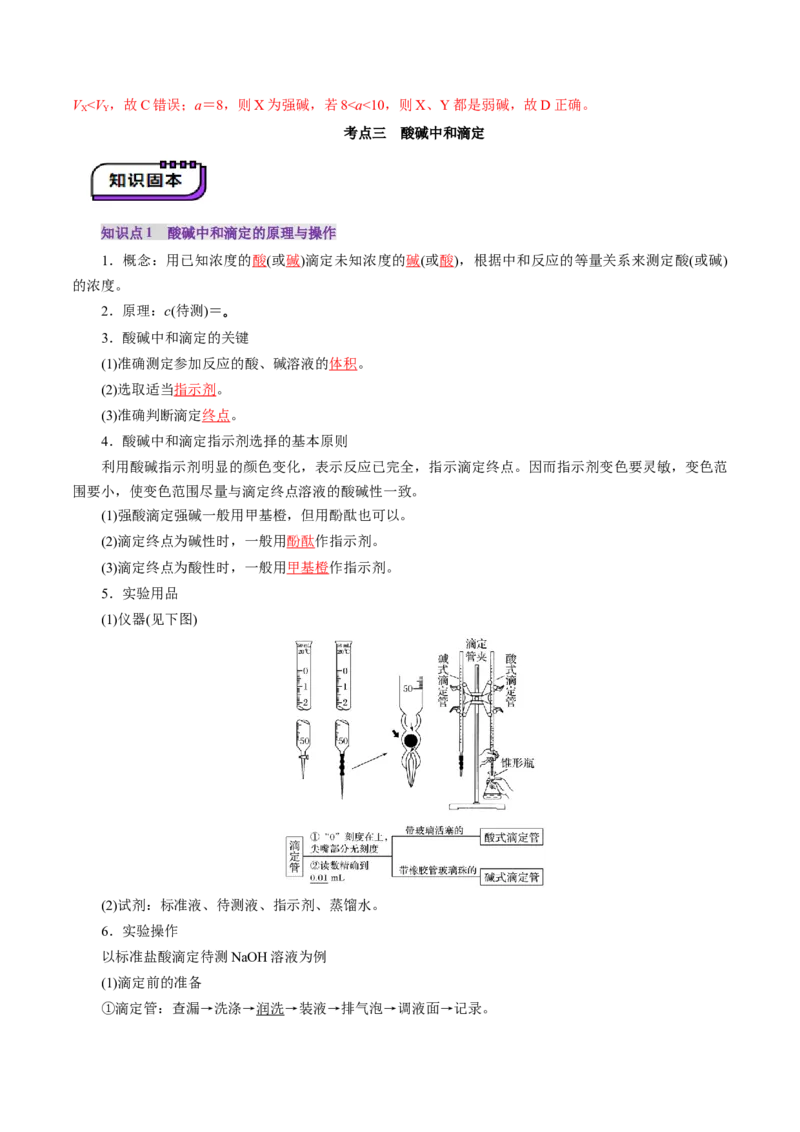
3.pH的测定方法
(1)pH试纸法
①适用范围:0~14。
②测定操作:用镊子夹取一小块试纸放在洁净的玻璃片或表面皿上,用玻璃棒蘸取待测液点在试纸的
中央,变色后与标准比色卡对照。
③常用的广范pH试纸只能读取1~14的整数。
(2)pH计测定:可精确测定溶液的pH,可读取一位或两位小数。
4.常用酸碱指示剂及变色范围
指示剂 变色范围的pH石蕊 <5.0红色 5.0~8.0紫色 >8.0蓝色
甲基橙 <3.1红色 3.1~4.4橙色 >4.4黄色
酚酞 <8.2无色 8.2~10.0浅红色 >10.0红色
【易错提醒】
1.pH=7的溶液不一定呈中性。只有在常温下pH=7的溶液才呈中性,当在100 ℃时,水的离子积
常数为1×10-12,此时pH=6的溶液为中性溶液,pH>6时为碱性溶液,pH<6时为酸性溶液。
2.使用pH试纸测溶液pH时,若先用蒸馏水润湿,测量结果不一定偏小。若先用蒸馏水润湿,相当
于将待测液稀释了,若待测液为碱性溶液,则所测结果偏小;若待测液为酸性溶液,则所测结果偏大;若
待测液为中性溶液,则所测结果没有误差。
知识点3 溶液pH的计算
1.单一溶液pH的计算
强酸溶液:如HA,设浓度为c mol·L-1,c(H+)=nc mol·L-1,pH=-lg c(H+)= - lg ( n c )。
n
强碱溶液(25 ℃):如B(OH) ,设浓度为c mol·L-1,c(H+)= mol·L-1,pH=-lg c(H+)= 14 + lg
n
( nc ) 。
2.混合溶液pH的计算类型
(1)两种强酸混合:直接求出c(H+) ,再据此求pH。c(H+) =。
混 混
(2)两种强碱混合:先求出c(OH-) ,再根据K 求出c(H+) ,最后求pH。c(OH-) =。
混 w 混 混
(3)强酸、强碱混合:先判断哪种物质过量,再由下式求出溶液中H+或OH-的浓度,最后求pH。c(H
+) 或c(OH-) =。
混 混
【易错提醒】
误区一:不能正确理解酸、碱的无限稀释规律
常温下任何酸或碱溶液无限稀释时,溶液的pH都不可能大于7或小于7,只能接近7。
误区二:不能正确理解弱酸、弱碱的稀释规律
溶液 稀释前溶液pH 稀释后溶液pH
强酸 加水稀释到 pH=a+n
酸 pH=a
弱酸 体积为原来 a<pH<a+n
强碱 的10n倍 pH=b-n
碱 pH=b
弱碱 b-n<pH<b
误区三:不能正确掌握混合溶液的定性规律
pH=n(n<7)的强酸和pH=14-n的强碱溶液等体积混合,pH=7;pH=n(n<7)的醋酸 和 pH=14-n
的氢氧化钠溶液等体积混合,混合溶液pH<7;pH=n(n<7)的盐酸和pH=14-n的氨水溶液等体积混合,
混合溶液pH>7。考向1 溶液的酸碱性与pH
【例1】下列有关溶液的酸碱性与pH的说法错误的是( )
A.溶液pH越小,酸性越强,反之,碱性越强
B.pH<7的溶液,可能呈酸性
C.当溶液中的c(H+)或c(OH-)较小时,用pH表示其酸碱性更为方便
D.把pH试纸直接插入待测溶液中,测其pH
【答案】D
【解析】A项因pH=-lgc(H+),所以pH越小,c(H+)越大,酸性越强,pH越大,c(H+)越小,则
c(OH-)越大,碱性越强,A项正确;B项在室温下,pH<7的溶液呈酸性,B项正确;C项当c(H+)或c(OH
-)小于1 mol·L-1时,使用pH表示其酸碱性更为方便,故C项正确;D项用pH试纸测溶液pH时,不能把
pH试纸直接插入待测溶液中测pH,正确的做法为取一小片pH试纸,放在洁净的表面皿上或玻璃片上,
用玻璃棒蘸取待测液点于试纸中央,然后与标准比色卡对照读取数据,所以D项错误。
【易错警示】
1.溶液显酸碱性的实质是溶液中c(H+)与c(OH-)的相对大小。
2.用pH判断溶液酸碱性时,要注意条件,即温度。不能简单地认为pH等于7的溶液一定为中性,如
100℃时,pH=6为中性,pH<6才显酸性,pH>6显碱性,所以使用pH时需注明温度,若未注明温度,一
般认为是常温,就以pH=7为中性。
【变式训练】工农业生产和科学实验中常常涉及溶液的酸碱性,生活和健康也与溶液的酸碱性有密切
关系。pH是表示溶液酸碱度的一种方法。下列说法不正确的是( )
A.可以用pH试纸测量溶液的pH,也可以用酸度计来测量
B.测量和调控溶液的pH,对工农业生产,科学研究都具有重要意义
C.pH试纸可测量任何溶液的pH值
D.酸碱指示剂是一些有机弱酸或弱碱,在溶液中存在电离平衡,指示剂的颜色变化在一定pH范围内
发生
【答案】C
【解析】A项,可以用pH试纸测量溶液的pH,也可以用酸度计来测量,选项A正确;B项,测试和
调控溶液的pH对工农业生产、科学研究及日常生活和医疗保健都有重要意义,选项B正确;C项,不是
任何溶液的pH都能用pH试纸测,因为试纸有范围要求,也不能测量氯水等溶液的pH,选项C不正确;
D项,酸碱指示剂是一些有机弱酸或弱碱,在溶液中存在电离平衡,指示剂的颜色变化在一定pH范围内
发生,选项D正确;故选C。
考向2 溶液pH的计算
【例2】(2023·浙江省艾青中学质检)T℃时,水的离子积常数K =10-13,该温度下,V mLpH=12的
w 1
Ba(OH) 稀溶液与V mLpH=2的稀硫酸充分反应(混合后的体积变化忽略不计),恢复到T℃,测得混合溶
2 2液的pH=3,则V:V 的值为( )
1 2
A.9∶101 B.99∶101 C.1∶100 D.1∶10
【答案】A
【解析】T℃时,水的离子积常数K =10-13,该温度下,V mLpH=12的Ba(OH) 稀溶液,c(H+)=10-12
w 1 2
mol/L,则c(OH-)=10-1 mol/L mol/L;V mLpH=2的稀硫酸c(H+)=10-2 mol/L,二者反应后恢复到T℃,测得
2
混合溶液的pH=3,c(H+)=10-3 mol/L,说明酸过量,则c(H+)= ,解得V:
1
V=9∶101,故选A。
2
【思维建模】
溶液pH计算的一般思维模型
【变式训练】某温度时水的离子积常数K =10-13,在此温度下将同浓度的NaOH溶液与稀硫酸按体积
w
之比 3∶1混合,若所得混合液pH=12,则原溶液的浓度为( )
A.0.40 mol·L-1 B.0.20 mol·L-1 C.0.04 mol·L-1 D.0.50 mol·L-1
【答案】A
【解析】某温度时水的离子积常数K =10-13,设NaOH溶液与稀硫酸的浓度为c,体积分别为3V和
w
V,则 NaOH 溶液中 c(OH-)=c,硫酸中 c(H+)=2c,所得混合液 pH=12,即 c(H+)=10-12 mol·L-1,c(OH-)=
K 10-13 3cV -2cV
w = mol·L-1=0.1 mol·L-1,则碱过量,混合后 c(OH-)= =0.1 mol·L-1,则 c=0.40
c(H+) 10-12 3V +V
mol·L-1。
考向3 酸碱溶液稀释后酸碱性的判断2.常温下,关于溶液稀释的下列说法正确的是( )
A.pH=3的醋酸溶液稀释100倍,pH=5
B.pH=4的HSO 溶液加水稀释100倍,溶液中由水电离产生的c(H+)=1×10-6 mol·L-1
2 4
C.将1 L 0.1 mol·L-1的Ba(OH) 溶液稀释为2 L,pH=13
2
D.pH=8的NaOH溶液稀释100倍,其pH=6
【答案】C
【解析】A项,pH=3的醋酸溶液在稀释过程中电离平衡正向移动,稀释100倍时,3V
X Y
D.若8d,故D错误;故选D。
4.(2022•山东卷)实验室用基准NaCO 配制标准溶液并标定盐酸浓度,应选甲基橙为指示剂,并以盐
2 3
酸滴定NaCO 标准溶液。下列说法错误的是( )
2 3
A.可用量筒量取25.00 mL Na CO 标准溶液置于锥形瓶中
2 3B.应选用配带塑料塞的容量瓶配制NaCO 标准溶液
2 3
C.应选用烧杯而非称量纸称量NaCO 固体
2 3
D.达到滴定终点时溶液显橙色
【答案】A
【解析】根据中和滴定过程批示剂选择原则,以盐酸滴定NaCO 标准溶液,选甲基橙为指示剂,则
2 3
应利用盐酸滴定碳酸钠,即将NaCO 标准溶液置于锥形瓶中,将待测盐酸置于酸式滴定管中,滴定终点时
2 3
溶液由黄色变为橙色。A项,量筒的精确度为0.1 mL,不可用量简量取NaCO 标准溶液,应该用碱式滴定
2 3
管或移液管量取25.00 mL Na CO 标准溶液置于锥形瓶中,A错误;B项,NaCO 溶液显碱性,盛放
2 3 2 3
NaCO 溶液的容器不能用玻璃塞,以防碱性溶液腐蚀玻璃产生有粘性的硅酸钠溶液而将瓶塞粘住,故应选
2 3
用配带塑料塞的容量瓶配制NaCO 标准溶液,B正确;C项,NaCO 有吸水性且有一定的腐蚀性,故应选
2 3 2 3
用烧杯而非称量纸称量NaCO 固体,C正确;D项,NaCO 溶液显碱性,甲基橙滴入NaCO 溶液中显黄
2 3 2 3 2 3
色,当滴入最后一滴盐酸时,溶液由黄色突变为橙色且半分钟之内不变色即为滴定终点,故达到滴定终点
时溶液显橙色,D正确;故选A。
5.(2022·浙江1月选考,23)某同学在两个相同的特制容器中分别加入20 mL 0.4 mol·L-1 Na CO 溶液
2 3
和40 mL 0.2 mol·L-1 NaHCO 溶液,再分别用0.4 mol·L-1盐酸滴定,利用pH计和压力传感器检测,得到如
3
下曲线:
下列说法正确的是( )。
A.图中甲、丁线表示向NaHCO 溶液中滴加盐酸,乙、丙线表示向NaCO 溶液中滴加盐酸
3 2 3
B.当滴加盐酸的体积为 V mL 时(a 点、b 点),所发生的反应用离子方程式表示为
HCO-
1 3
+H+=CO ↑+H O
2 2
C.根据pH-V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点
D.NaCO 和NaHCO 溶液中均满足:c(H
CO)-c(CO2-
)=c(OH-)-c(H+)
2 3 3 2 3 3
【答案】C【解析】碳酸钠的水解程度大于碳酸氢钠,故碳酸钠溶液的碱性强于碳酸氢钠溶液,碳酸钠与盐酸反
应先生成碳酸氢钠,再产生二氧化碳气体,故图中甲、丁线表示向NaCO 溶液中滴加盐酸,乙、丙线表示
2 3
向NaHCO 溶液中滴加盐酸,A项错误;当滴加盐酸的体积为V mL时(a点、b点),所发生反应的离子方
3 1
程式为HCO-
+H+=H CO,B项错误;根据pH-V(HCl)图,滴定分析时,c点的pH在9左右,符合酚酞的指
3 2 3
示范围,故可用酚酞作指示剂,d点的pH在4左右,符合甲基橙的指示范围,故可用甲基橙作指示剂,C
项正确;根据电荷守恒和元素质量守恒,NaCO 溶液中存在c(OH-)-c(H+)=2c(H
CO)+c(HCO-
),NaHCO
2 3 2 3 3 3
溶液中存在c(H
CO)-c(CO2-
)=c(OH-)-c(H+),D项错误。
2 3 3
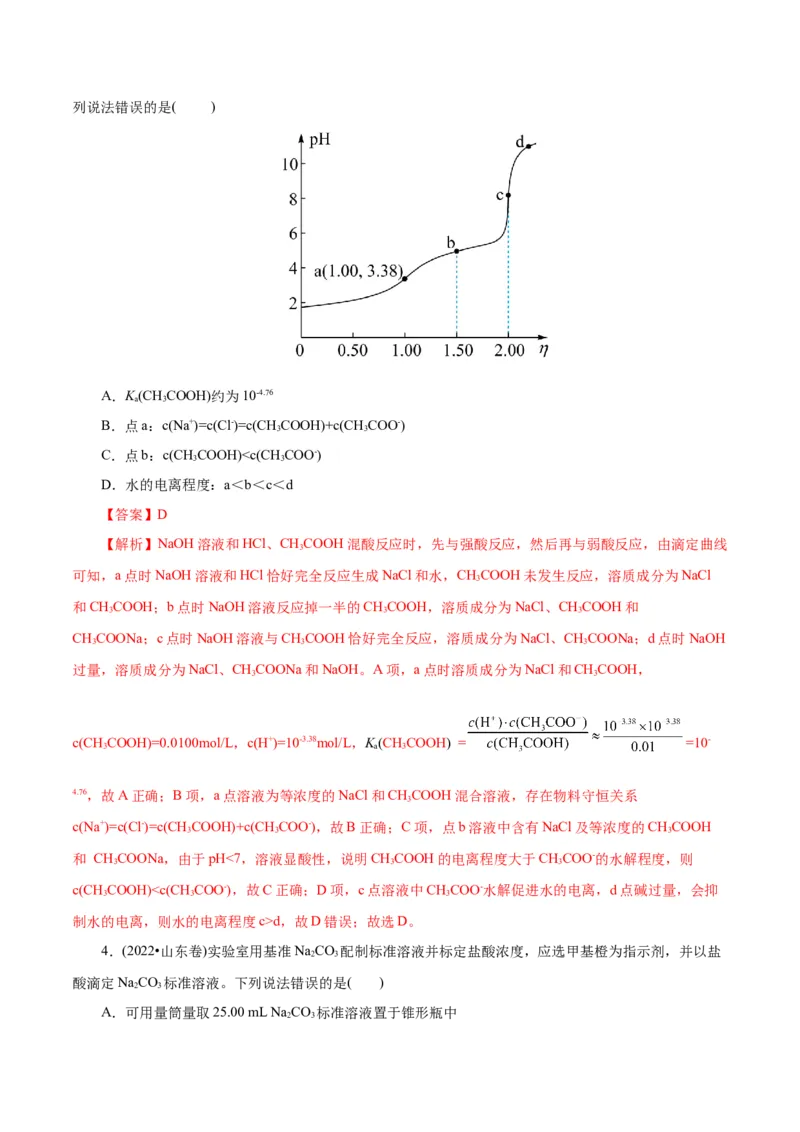
6.(2021•辽宁选择性考试,15)用0.1000mol·L-1盐酸滴定20.00 mLNa A溶液,溶液中HA、HA-、A2-
2 2
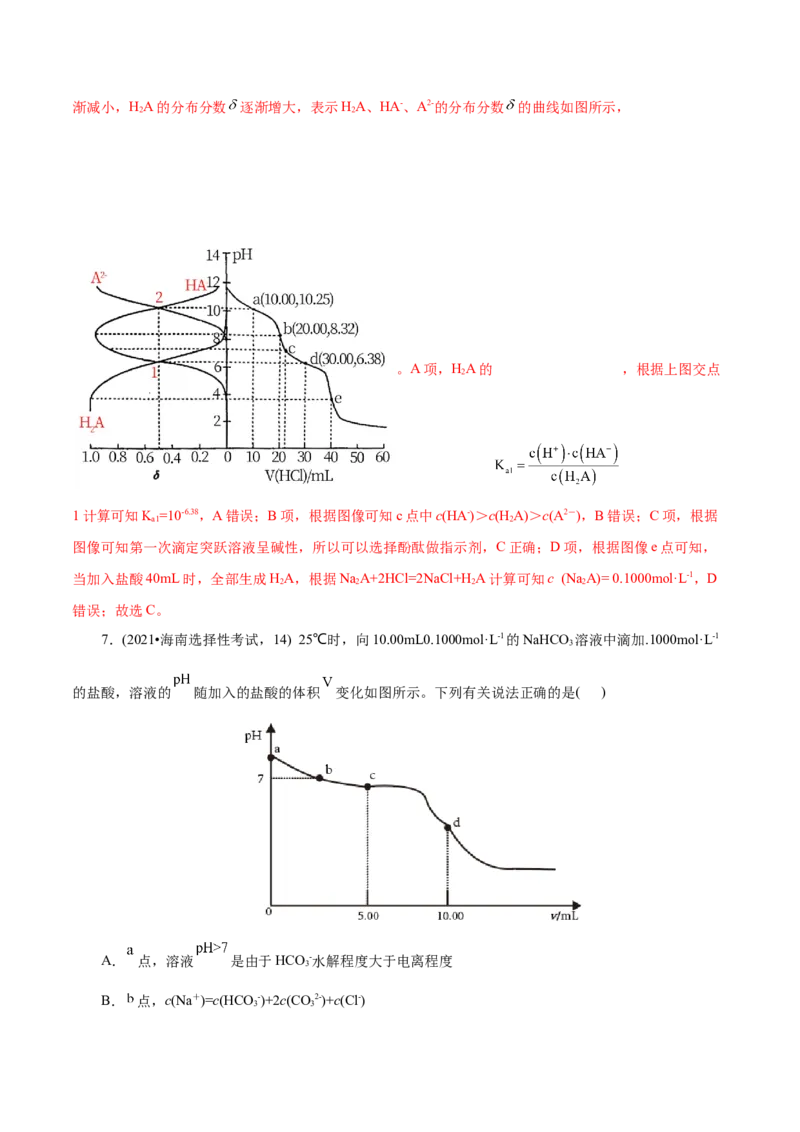
的分布分数 随pH变化曲线及滴定曲线如图。下列说法正确的是(如A2-分布分数:
)
A.HA的K 为10-10.25 B.c点:c(HA-)>c(A2-)>c(H A)
2 a1 2
C.第一次突变,可选酚酞作指示剂 D.c (NaA)= 0.2000mol·L-1
2
【答案】C
【解析】用0.1000mol·L-1盐酸滴定20.00 mLNa A溶液,pH较大时A2-的分布分数 最大,随着pH的
2
减小,A2-的分布分数 逐渐减小,HA-的分布分数 逐渐增大,恰好生成NaHA之后,HA-的分布分数 逐渐减小,HA的分布分数 逐渐增大,表示HA、HA-、A2-的分布分数 的曲线如图所示,
2 2
。A项,HA的 ,根据上图交点
2
1计算可知K =10-6.38,A错误;B项,根据图像可知c点中c(HA-)>c(H A)>c(A2-),B错误;C项,根据
a1 2
图像可知第一次滴定突跃溶液呈碱性,所以可以选择酚酞做指示剂,C正确;D项,根据图像e点可知,
当加入盐酸40mL时,全部生成HA,根据NaA+2HCl=2NaCl+H A计算可知c (Na A)= 0.1000mol·L-1,D
2 2 2 2
错误;故选C。
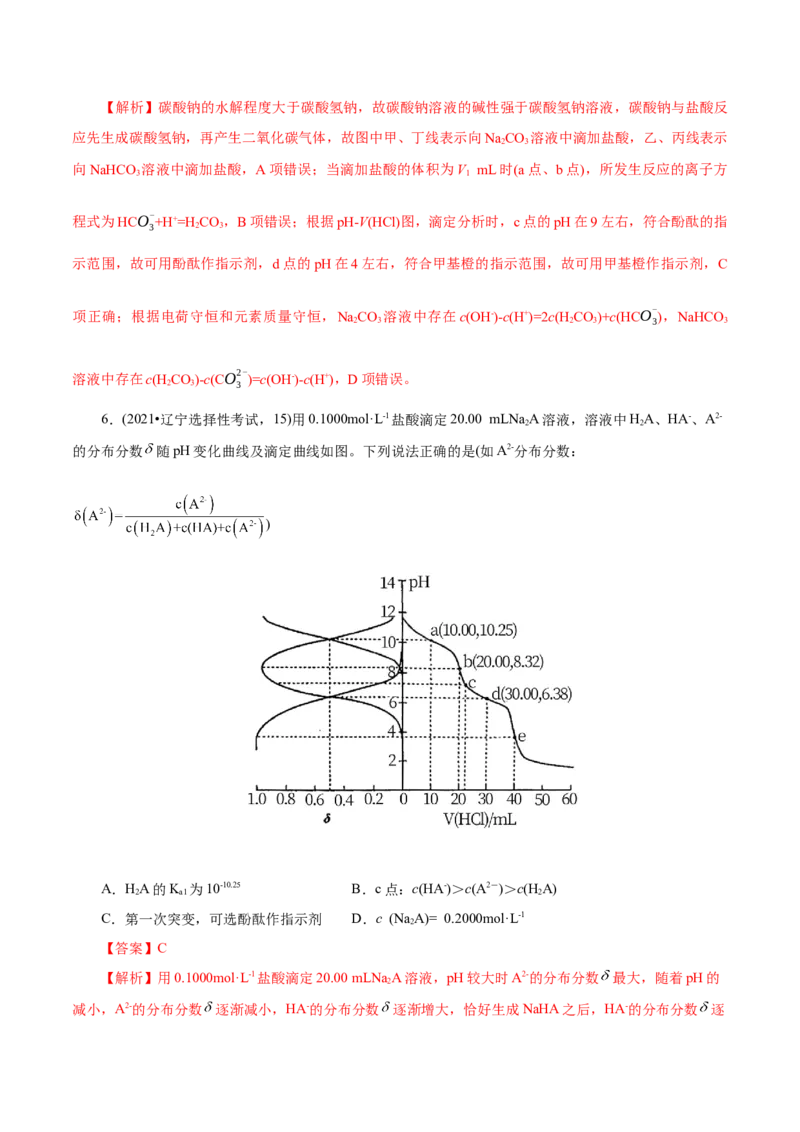
7.(2021•海南选择性考试,14) 25℃时,向10.00mL0.1000mol·L-1的NaHCO 溶液中滴加.1000mol·L-1
3
的盐酸,溶液的 随加入的盐酸的体积 变化如图所示。下列有关说法正确的是( )
A. 点,溶液 是由于HCO -水解程度大于电离程度
3
B. 点,c(Na+)=c(HCO -)+2c(CO2-)+c(Cl-)
3 3C.c 点,溶液中的 主要来自HCO -的电离
3
D.d点,c(Na+)= c(Cl-)= 0.1000mol·L-1
【答案】AB
【解析】A项,HCO -存在水解平衡和电离平衡,a点溶液pH>7是由于HCO -水解程度大于电离程度,
3 3
故A正确;B项,根据电荷守恒c(Na+)+c(H+)=c(HCO -)+2c(CO2-)+c(Cl-)+c(OH―),b点pH=7即c(H+)=
3 3
c(OH-),所以c(Na+)=c(HCO -)+2c(CO2-)+c(Cl-),故B正确;C项,c点,溶质为碳酸氢钠、氯化钠、碳酸,
3 3
溶液中的H+主要来自HCO 的电离,故C错误;D项,d点,碳酸氢钠和盐酸恰好反应,c(Na+)= c(Cl-)=
2 3
0.0500mol·L-1,故D错误;选AB。