文档内容
第 02 讲 物质的量浓度
目录
01考情透视·目标导航..........................................................................................................2
02知识导图·思维引航..........................................................................................................3
03考点突破·考法探究..........................................................................................................3
考点一 物质的量浓度及相关计算....................................................................................................................3
知识点1 物质的量浓度..............................................................3
知识点2 物质的量浓度和溶质质量分数的比较..........................................4
考向1 理解物质的量浓度概念........................................................4
考向2 物质的量浓度及相关计算......................................................5
考点二 溶液浓度的计算与换算........................................................................................................................6
知识点1 理解公式..................................................................6
知识点2 掌握规律..................................................................7
考向1 有关气体溶于水的浓度计算....................................................8
考向2 混合规律的应用..............................................................9
考点三 一定物质的量浓度溶液的配制..........................................................................................................10
知识点1 容量瓶的构造及使用.......................................................10
知识点2 配制一定物质的量浓度溶液操作.............................................10
考向1 配制一定物质的量浓度的溶液.................................................11
考向2 配制一定物质的量浓度的溶液的误差分析.......................................14
04真题练习·命题洞见........................................................................................................16考点要
考题统计 考情分析
求
物质的量浓
度的计算
从近三年高考试题来看,有关物质的量浓度的概念主
2022•海南卷7题,2分
要体现在N 、水溶液中的离子平衡及化学计算中;
A
一定物质的量浓度溶液的配制是重要的化学定量实验
之一,融合于选择题的化学实验基本操作,填空题主
要以穿插在生活、生产中的化学分析计算(如食品污
染物空气污染物的测定、食品中的营养物质的测定、
2023•全国甲卷9题,6分; 化工生产中的产品是否合格等等)为主,中需关注滴
定实验中有关物质的量浓度的计算。
一定物质的 2022山东卷6题,2分;
量浓度溶液
2022•全国乙卷27(1)题,2分;
的配制及误
差分析 2022•广东卷7题(1)(2),4分;
2021广东卷7题,2分
复习目标:
1.掌握物质的量浓度的含义和应用,能运用物质的量浓度进行简单计算。
2.建立n、M、V 、c之间相互转化关系及进行简单计算的思维模型。
m
3.掌握一定物质的量浓度的溶液的配制方法。
4.学会一定物质的量浓度的溶液的配制的过程中的误差分析。考点一 物质的量浓度及相关计算
知识点1 物质的量浓度
1.概念
物质的量浓度表示单位体积的溶液里所含溶质B的物质的量,也称为 B 的物质的量浓度 ,符号为c 。
B2.常用单位:mol/L 或 mol·L - 1 。
3.公式:n=c V⇒
B
【名师提醒】
1.V是溶液的体积,不是溶剂的体积,也不是溶质与溶剂的体积之和。
2.n必须是溶质B的物质的量。
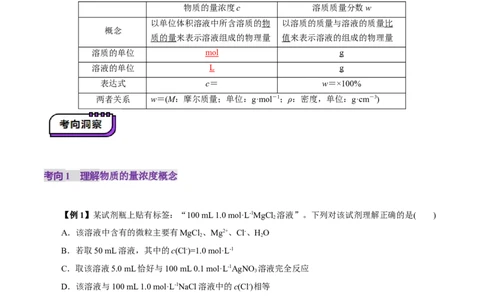
知识点2 物质的量浓度和溶质质量分数的比较
物质的量浓度c 溶质质量分数w
以单位体积溶液中所含溶质的物 以溶质的质量与溶液的质量比
概念
质的量来表示溶液组成的物理量 值来表示溶液的组成的物理量
溶质的单位 mol g
溶液的单位 L g
表达式 c= w=×100%
两者关系 w=(M:摩尔质量;单位:g·mol-1;ρ:密度,单位:g·cm-3)
考向1 理解物质的量浓度概念
【例1】某试剂瓶上贴有标签:“100 mL 1.0 mol·L-1MgCl 溶液”。下列对该试剂理解正确的是( )
2
A.该溶液中含有的微粒主要有MgCl 、Mg2+、Cl-、HO
2 2
B.若取50 mL溶液,其中的c(Cl-)=1.0 mol·L-1
C.取该溶液5.0 mL恰好与100 mL 0.1 mol·L-1AgNO 溶液完全反应
3
D.该溶液与100 mL 1.0 mol·L-1NaCl溶液中的c(Cl-)相等
【答案】C
【解析】MgCl 是强电解质,在水溶液中完全电离,水是弱电解质,在水溶液中部分电离,所以溶液
2
中存在的微粒有Mg2+、Cl-、HO、H+、OH-,A项错误;该溶液的浓度为1.0 mol·L-1,根据Cl原子守恒可
2
得c(Cl-)=2c(MgCl )=2×1.0 mol·L-1=2.0 mol·L-1,浓度与溶液的体积无关,B项错误;n(Cl-)=2.0 mol·L-1×0.005
2
L=0.01 mol,n(Ag+)=0.1 mol·L-1×0.1 L=0.01 mol,二者以1∶1的比例进行反应,所以n(Cl-)=n(Ag+)时,二者
恰好完全反应,C项正确;1.0 mol·L-1 NaCl溶液中的c(Cl-)=c(NaCl)=1.0 mol·L-1,D项错误。
【易错警示】1 . 注 意 物 质 溶 于 水 后 溶 质 是 否 改 变 , 如 : NaO 、 NaO―→NaOH , SO ―→HSO ,
2 2 2 3 2 4
CuSO ·5H O―→CuSO 。
4 2 4
2.不能用水的体积代替溶液的体积,尤其是固体、气体溶于水,一般根据溶液的密度进行计算。
【变式训练】设N 为阿伏加德罗常数的值,下列对0.3 mol·L-1KSO 溶液的叙述正确的是( )。
A 2 4
A.1 L该溶液中含有0.3N 个K+
A
B.1 L该溶液中含有K+和SO 2-的总数为0.9N
4 A
C.2 L该溶液中K+的浓度为1.2 mol·L-1
D.将0.3 mol硫酸钾溶于1 L水中,所得硫酸钾溶液的浓度为0.3 mol·L-1
【答案】B
【解析】在0.3 mol·L-1KSO 溶液中,c(K+)=0.6 mol·L-1,c(SO 2-)=0.3 mol·L-1,则1 L该溶液中所含
2 4 4
K+的数目为0.6N ,K+和SO 2-的总数为0.9N ,A项错误,B项正确;物质的量浓度表示的是1 L溶液中所
A 4 A
含溶质的物质的量,其不受溶液体积大小的影响,故2 L 0.3 mol·L-1KSO 溶液中K+的浓度为0.6 mol·L-1,
2 4
C项错误;体积应为溶液的体积而不是溶剂的体积,D项错误。
考向2 物质的量浓度及相关计算
【例2】(2024•安徽省芜湖市期中)下列溶液的物质的量浓度的相关计算正确的是( )
A.同浓度的三种物质的溶液:NaSO 、MgSO 、Al (SO ) 溶液体积之比为3∶2∶1,则SO 2-浓度之
2 4 4 2 4 3 4
比为3∶2∶3
B.将100mL 5 的盐酸加水稀释至1L,再取出5mL,这5mL溶液的物质的量浓度为0.5mol/L
C.将1mol•L-1的NaCl溶液和0.5mol•L-1的BaCl 溶液等体积混合后,忽略溶液体积变化,
2
c(Cl-)=0.75mol•L-1
D.标准状况下,22.4L HCl溶于1L水,盐酸的物质的量浓度为1mol•L-1
【答案】B
【解析】A项,假设三种溶液的浓度均为1mol/L,则NaSO 、MgSO 、Al (SO ) 溶液中SO 2-浓度分别
2 4 4 2 4 3 4
=1mol/L×1=1mol/L、1mol/L×1=1mol/L和1mol/L×3=3mol/L,即浓度之比为1∶1∶3,A错误;B项,溶液
稀释前后溶质的物质的量不变,则稀释后盐酸物质的量浓度= =0.5mol/L,溶液具有均一性、
稳定性,所以稀释后溶液中盐酸浓度都是相同的,与溶液体积大小无关,5mL溶液物质的量浓度为
0.5mol/L,B正确;C项,1mol·L-1的NaCl溶液中c(Cl-)=1mol/L×1=1mol/L,0.5mol•L-1的BaCl 溶液中
2c(Cl-)=0.5mol/L×2=1mol/L,故两者混合后,不考虑体积的变化,c(Cl-)=1mol•L-1,C错误;D项,1L为水
的体积,不是溶液的体积,则溶液体积未知不能计算盐酸的物质的量浓度,D错误;故选B。
【变式训练】某同学购买了一瓶“84”消毒液,包装说明如图:
净含量:1000 mL
主要成分: 25%NaClO
密度:1.19 g·cm-3
使用方法:稀释100倍(体积比)后使用
注意事项:密封保存,易吸收空气中的CO 而变质
2
根据以上信息和相关知识判断,下列分析不正确的是( )。
A.该“84”消毒液的物质的量浓度约为4.0 mol·L-1
B.一瓶该“84”消毒液最多能吸收空气中CO 约为89.6 L(标准状况)
2
C.取100 mL该“84”消毒液稀释100倍后用于消毒,稀释后的溶液中c(Na+)约为0.04 mol·L-1
D.参阅该“84”消毒液的配方,欲用 NaClO固体配制480 mL含25%NaClO的消毒液,需要称量
NaClO固体的质量约为143 g
【答案】D
1000ρw 1000×1.19×25%
【解析】根据c= 得,c(NaClO)= mol·L-1≈4.0 mol·L-1,A项正确;一瓶该
M 74.5
“84”消毒液含有的n(NaClO)约为1 L×4.0 mol·L-1=4.0 mol,根据反应CO+NaClO+H O NaHCO +HClO
2 2 3
可知,吸收CO 的物质的量最多为4.0 mol,即标准状况下V(CO)约为4.0 mol×22.4 L· mol-1=89.6 L,则最
2 2
多能吸收约89.6 L的CO ,B项正确;根据稀释前后溶质的物质的量不变,有 100 mL×4.0 mol·L-1=100
2
mL×100×c(NaClO),解得稀释后c(NaClO)=0.04 mol·L-1,c(Na+)=c(NaClO)=0.04 mol·L-1,C项正确;应选取
500 mL 的容量瓶进行配制,然后取出 480 mL,所以需要 NaClO的质量约为 0.5 L×4.0 mol·L-1×74.5 g·
mol-1=149 g,D项错误。
考点二 溶液浓度的计算与换算知识点1 理解公式
1.物质的量浓度与溶质质量分数之间的换算
c====,w= 。(ρ:g·cm-3)
2.物质的量浓度与溶解度(S)的换算(饱和溶液)
c===,S=。(ρ:g·cm-3)
3.气体溶质溶于水中制得溶液,其物质的量浓度和质量分数的计算
在标准状况下,1 L水中溶解某气体V L,所得溶液密度为ρ,则:c===(ρ:g·cm-3),w=×100%=
=×100%。
【易错提醒】
1.溶液的体积不能用溶剂水的体积和溶质的体积之和来代替,应该用溶液的质量除以溶液的密度;
2.两溶液混合,由于其密度可不相等,所以体积不等于两混合溶液体积之和。
3.物质溶于水后注意看溶质是否发生了变化。如 Na、NaO 、NO 、SO 等溶于水,由于它们与水反
2 2 2 3
应,所以溶质发生了变化。
知识点2 掌握规律
1.稀释定律
(1)如用V、V、c、c 分别表示稀释前后溶液的体积和溶质的物质的量浓度,有cV = cV。
1 2 1 2 1 1 2 2
(2)如用m、m、w 、w 分别表示稀释前后溶液的质量和质量分数,有mw = m w 。
1 2 1 2 1 1 2 2
2.混合规律
同一溶质不同浓度的溶液混合后溶质质量分数的判断方法:设溶质质量分数分别为 w 和w 的两溶液
1 2
混合后所得溶液溶质的质量分数为w。
(1)两溶液等质量混合:w=(w +w )。
1 2
(2)两溶液等体积混合:
a.若溶液中溶质的密度大于溶剂的密度,则w≥(w +w ),如HSO 溶液。
1 2 2 4
b.若溶液中溶质的密度小于溶剂的密度,则w≤(w +w ),如氨水、酒精溶液。
1 2
考向1 有关气体溶于水的浓度计算
【例1】标准状况下V L氨气溶解在1 L水中(水的密度近似为1 g·mL-1),所得溶液的密度为ρ g·mL-1,质量分数为w,物质的量浓度为c mol·L-1,则下列关系中不正确的是( )
A.ρ=(17V+22 400)/(22.4+22.4V)
B.w=17c/(1 000ρ)
C.w=17V/(17V+22 400)
D.c=1 000Vρ/(17V+22 400)
【答案】A
【解析】由c=== mol·L-1;由上可推知:ρ=,设溶液的体积为1 L,由c=可得,w==,w==
=,因此只有A项不正确。
【思维建模】
计算气体溶于水后物质的量浓度的一般思路
【变式训练】在T ℃时,将a g NH 完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g·cm-3,
3
溶质的质量分数为w,其中含NH的物质的量为b mol。下列叙述中正确的是 ( )
A.溶质的质量分数为w=×100%
B.溶质的物质的量浓度c= mol·L-1
C.溶液中c(OH-)= mol·L-1
D.上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w
【答案】B
【解析】根据题中给出的已知量及各选项的要求,利用待求量的最基本计算关系代入求解即可。A不
正确,w应为×100%;根据公式c=进行计算知B正确;由溶液中的电荷守恒可知c(OH-)= mol·L-1+c(H
+),C错误;因为氨水的密度小于水的密度,故上述溶液再加 V mL水后,所得溶液溶质的质量分数小于
0.5w,故D不正确。
考向2 混合规律的应用
【例2】若以w 和w 分别表示浓度为a mol·L-1和 b mol·L-1的氨水的质量分数,且知2a=b,则下
1 2
列判断正确的是 ( )
A.2w =w B.2w =w C.w >2w D.w <w <2w
1 2 2 1 2 1 1 2 1【答案】C
【解析】根据溶质的质量分数和物质的量浓度之间的换算关系,有:a=
①;b= ②;将上述两式相比得:==2,即=,因为氨水的密度比纯水的小,氨水浓度越大,密度
越小,所以ρ>ρ,即w >2w 。
1 2 2 1
【思维建模】
1.溶液稀释
(1)溶质的质量在稀释前后保持不变,即mw =mw 。
1 1 2 2
(2)溶质的物质的量在稀释前后保持不变,即cV=c V。
1 1 2 2
(3)溶液质量守恒,m(稀)=m(浓)+m(水)(体积一般不守恒)。
2.溶液混合,混合前后:cV+c V=c V ,其中V =m /ρ ,据此可进行相关计算。
1 1 2 2 混 混 混 混 混
【变式训练】浓度不等的两种硫酸溶液等质量混合后,溶液中溶质的质量分数为 a%,而等体积混合
后,溶质的质量分数为b%;浓度不等的两种氨水等质量混合时,其溶质的质量分数为 a%,而等体积混合
后,溶质的质量分数为c%,那么a、b、c数值的关系是 ( )
A.a>b>c B.b>a>c C.c>b>a D.c>a>b
【答案】B
【解析】由混合后溶质质量分数的判定规律知,硫酸溶液密度大于1 g·cm-3,故b>a;氨水密度小于1
g·cm-3,且浓度越大,密度越小,则c