文档内容
第 04 讲 沉淀溶解平衡
目录
01 模拟基础练
【题型四】沉淀溶解平衡及影响因素
【题型四】沉淀溶解平衡的应用
【题型四】和K 有关的计算与判断
sp
【题型四】沉淀溶解平衡图像
02 重难创新练
03 真题实战练
题型一 沉淀溶解平衡及影响因素
1.把Ca(OH) 放入蒸馏水中,一段时间后达到平衡:Ca(OH) (s) Ca2+(aq)+2OH-(aq)。下列说法
2 2
正确的是( )
A.恒温下向溶液中加入CaO,溶液的pH增大
B.给溶液加热,溶液的pH增大
C.向溶液中加入NaCO 溶液,其中固体质量增加
2 3
D.向溶液中加入少量NaOH固体,Ca(OH) 固体质量不变
2
2.工业上向锅炉里注入NaCO 溶液,在浸泡过程中将水垢中的CaSO 转化为CaCO ,再用盐酸除去。
2 3 4 3
下列叙述不正确的是( )
A.升高温度,NaCO 溶液的K 和c(OH-)均会增大
2 3 w
B.沉淀转化的离子方程式为CO2-(aq)+CaSO (s) CaCO (s)+ SO2-(aq)
3 4 3 4
C.在盐酸中,CaCO 的溶解度大于CaSO
3 4
D.NaCO 溶液中通入CO 后,阴离子浓度均减小
2 3 2
3.向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成。经查资料得知:
Ag++2NH·H O [Ag(NH)]++2H O。下列分析不正确的是( )
3 2 3 2 2
A.浊液中存在沉淀溶解平衡:AgCl (s) Ag+(aq)+Cl-(aq)
B.实验可以证明NH 结合Ag+的能力比Cl-的强
3C.实验表明实验室可用氨水洗涤银镜反应后的试管
D.由资料信息可推知,加浓硝酸后生成的沉淀为AgCl
4.牙齿表面覆盖的牙釉质是人体中最坚硬的部分,起着保护牙齿的作用,其主要成分为羟基磷酸钙
[Ca (PO )OH]。在牙齿表面存在着如下平衡:Ca (PO )OH(s) 5Ca2+(aq)+3PO(aq)+OH-(aq) K =
5 4 3 5 4 3 sp
6.8×10-37。已知Ca (PO )F(s)的K =2.8×10-51。下列说法错误的是( )
5 4 3 sp
A.残留在牙齿上的糖发酵会产生H+,经常吃糖易造成龋齿
B.由题述平衡可知,小孩长牙时要少吃糖多补钙
C.若减少OH-的浓度,题述平衡将向右移动,K 的值相应增大
sp
D.使用含氟的牙膏能防止龋齿,是因为Ca (PO )OH(s)转化为更难溶的Ca (PO )F(s)
5 4 3 5 4 3
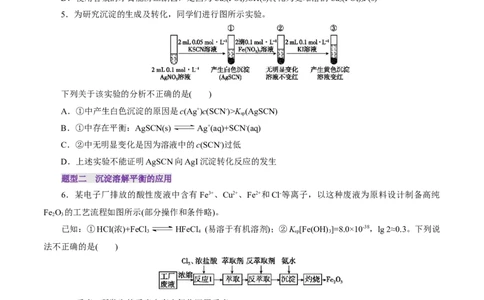
5.为研究沉淀的生成及转化,同学们进行图所示实验。
下列关于该实验的分析不正确的是( )
A.①中产生白色沉淀的原因是c(Ag+)c(SCN-)>K (AgSCN)
sp
B.①中存在平衡:AgSCN(s) Ag+(aq)+SCN-(aq)
C.②中无明显变化是因为溶液中的c(SCN-)过低
D.上述实验不能证明AgSCN向AgI沉淀转化反应的发生
题型二 沉淀溶解平衡的应用
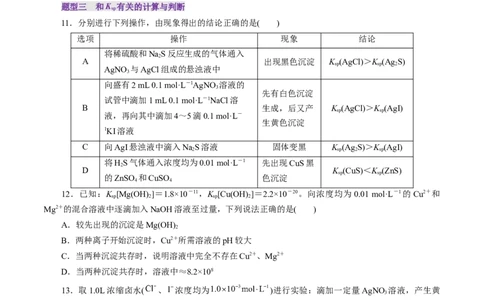
6.某电子厂排放的酸性废液中含有Fe3+、Cu2+、Fe2+和Cl-等离子,以这种废液为原料设计制备高纯
Fe O 的工艺流程如图所示(部分操作和条件略)。
2 3
已知:①HCl(浓)+FeCl HFeCl (易溶于有机溶剂);②K [Fe(OH) ]=8.0×10-38,lg 2≈0.3。下列说
3 4 sp 3
法不正确的是( )
A.反应1所发生的反应中存在氧化还原反应
B.在反萃取过程中利用了平衡移动原理,可用水作为反萃取剂
C.氨水的作用是调节pH使Fe3+沉淀,相关反应离子方程式为Fe3++3OH-=Fe(OH) ↓
3
D.为使Fe3+沉淀完全(浓度小于1×10-5mol·L-1),需调节溶液pH>3.3
7.高纯碳酸锰在电子工业中有着重要的应用,湿法浸出软锰矿(主要成分为MnO ,含有少量Fe、
2
Al、Mg等杂质元素)制备高纯碳酸锰的流程如图所示:其中除杂过程包括:①向浸出液中加入一定量的试剂X,调节浸出液的pH为3.5~5.5;②再加入一定
量的软锰矿和双氧水,过滤;③……
已知室温下:K [Mg(OH) ]=1.8×10-11,K [Al(OH) ]=3.0×10-34,K [Fe(OH) ]=4.0×10-38。
sp 2 sp 3 sp 3
下列说法正确的是( )
A.浸出时加入植物粉的作用是作还原剂
B.除杂过程中调节浸出液的pH为3.5~5.5可完全除去Fe、Al、Mg等杂质
C.试剂X可以是MnO、MnO 、MnCO 等物质
2 3
D.为增大沉淀MnCO 步骤的速率可以持续升高温度
3
8.钛酸钡(BaTiO )在工业上有重要用途,主要用于制作电子陶瓷、PTC热敏电阻、电容器等多种电子
3
元件。以下是生产钛酸钡的一种工艺流程图:
BaCO 浸出液 浸出液和TiCl 的混合液 草酸氧钛钡晶体 BaTiO
3 4 3
已知:①草酸氧钛钡晶体的化学式为BaTiO(C O)·4H O;②25 ℃时,BaCO 的溶度积K =2.58×10-
2 4 2 2 3 sp
9。
下列说法错误的是( )
A.BaTiO 中Ti元素的化合价为+4
3
B.在“酸浸”过程中为加快反应速率可用浓硫酸代替浓盐酸
C.流程中可以通过过滤得到草酸氧钛钡晶体
D.若浸出液中c(Ba2+)=0.1 mol·L-1,则c(CO2-)在浸出液中的最大浓度为2.58×10-8mol·L-1
3
9.(2024·浙江省衢州、丽水、湖州三地市教学质量检测)苯酚是重要的化工原料,将废水中的苯酚富
集并加入NaCO;转化为苯酚钠,再通入CO,可进一步分离回收。已知:K(C HOH)=1.0×10-10,
2 3 2 a 6 5
K (H CO)=4.5×10-7,K (H CO)=4.7×10-11。下列说法正确的是( )
a1 2 3 a2 2 3
A.NaCO;也可用NaOH或NaHCO 替代
2 3 3
B.2HCO - HCO+CO 2-的平衡常数K约为9.57×103
3 2 3 3
C.转化反应中若c(Na+)=2c(C HO-)+ 2c(C HOH),此时溶液中c(HCO -)>c(C HO-)
6 5 6 5 3 6 5
D.当通入CO 至溶液pH=10时,溶液中的C HONa完全转化为C HOH
2 6 5 6 5
10.(2024·浙江金华一中高三期中)室温下,通过下列实验探究NaCO 的性质。已知:25℃时,HSO
2 3 2 3
的K =1.42×10-2、K =1.0×10-7,HCO 的K =4.3×10-7、K =5.6×10-11。
a1 a2 2 3 a1 a2
实验1:配制50mL0.1mol·L-1 Na CO 溶液,测得溶液 约为12;
2 3实验2:取10mL0.1mol·L-1 Na CO 溶液,向其中加入少量CaSO 固体充分搅拌,一段时间后过滤。向
2 3 4
滤渣中加入足量稀盐酸,固体完全溶解;
实验3:取10mL0.1mol·L-1 Na CO 溶液,向其中缓慢滴入等体积0.1mol·L-1稀盐酸。
2 3
下列说法正确的是( )
A.实验1所得溶液中,c(Na+)<c(HCO -)+c(CO 2-)
3 3
B.根据实验2,可推测K (CaCO) >K (CaSO)
sp 3 sp 4
C.实验3反应后溶液中存在:c(Na+)=c(H CO)+c(HCO-)+c(CO 2-)
2 3 3 3
D.25℃时,反应CO2-+H SO HCO -+ HSO -的平衡常数K=2.5×10-8
3 2 3 3 3
题型三 和K
sp
有关的计算与判⇌断
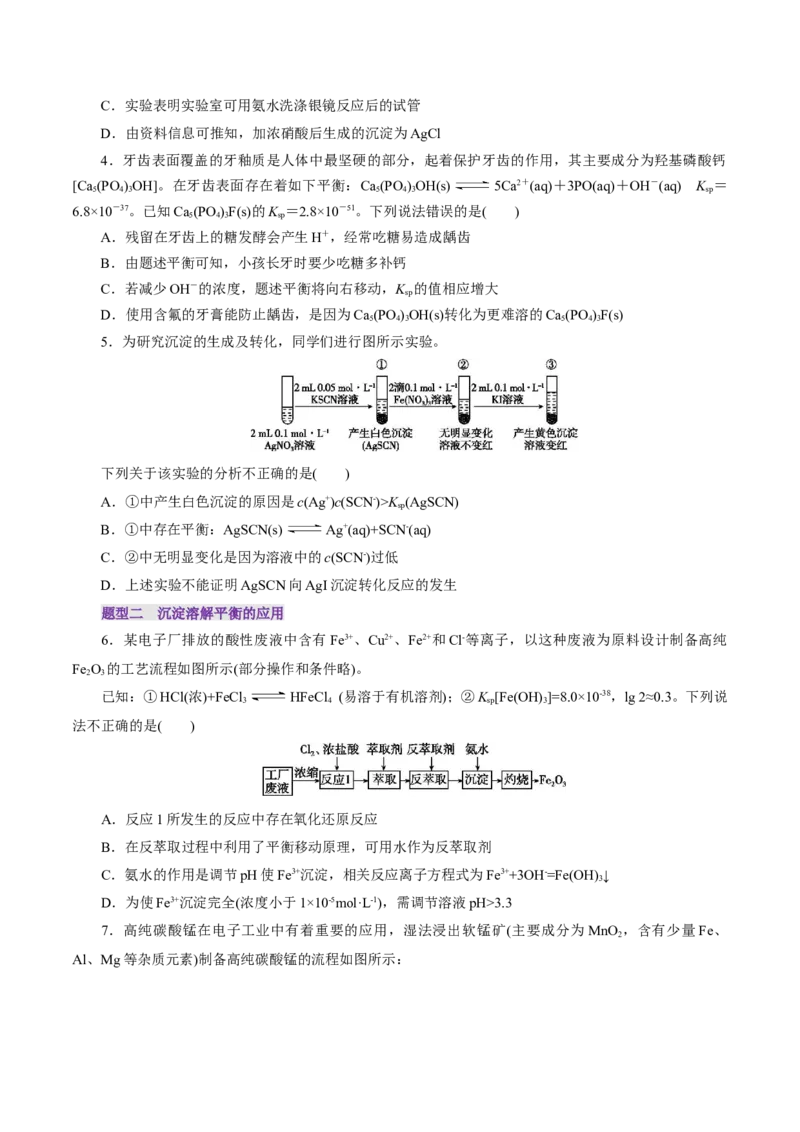
11.分别进行下列操作,由现象得出的结论正确的是( )
选项 操作 现象 结论
将稀硫酸和NaS反应生成的气体通入
2
A 出现黑色沉淀 K (AgCl)>K (Ag S)
sp sp 2
AgNO 与AgCl组成的悬浊液中
3
向盛有2 mL 0.1 mol·L-1AgNO 溶液的
3
先有白色沉淀
试管中滴加1 mL 0.1 mol·L-1NaCl溶
B 生成,后又产 K (AgCl)>K (AgI)
sp sp
液,再向其中滴加4~5滴0.1 mol·L-
生黄色沉淀
1KI溶液
C 向AgI悬浊液中滴入NaS溶液 固体变黑 K (Ag S)>K (AgI)
2 sp 2 sp
将HS气体通入浓度均为0.01 mol·L-1 先出现CuS黑
2
D K (CuS)<K (ZnS)
sp sp
的ZnSO 和CuSO 色沉淀
4 4
12.已知:K [Mg(OH) ]=1.8×10-11,K [Cu(OH) ]=2.2×10-20。向浓度均为0.01 mol·L-1的Cu2+和
sp 2 sp 2
Mg2+的混合溶液中逐滴加入NaOH溶液至过量,下列说法正确的是( )
A.较先出现的沉淀是Mg(OH)
2
B.两种离子开始沉淀时,Cu2+所需溶液的pH较大
C.当两种沉淀共存时,说明溶液中完全不存在Cu2+、Mg2+
D.当两种沉淀共存时,溶液中≈8.2×108
13.取1.0L浓缩卤水( 、 浓度均为 )进行实验:滴加一定量AgNO 溶液,产生黄
3
色沉淀;继续滴加,产生白色沉淀。已知: 、 。下列分析不正确的
是( )
A.黄色沉淀是AgI,白色沉淀是Ag Cl
B.产生白色沉淀时,溶液中存在AgI(s) Ag+(sq)+ I-(aq)
C.若起始时向卤水中滴加2滴(0.1 ) AgNO,能产生沉淀
3D.白色沉淀开始析出时,
14.相关物质的溶度积常数见下表(25 ℃):
物质 Mg(OH) CHCOOAg AgCl Ag CrO
2 3 2 4
K 1.1×10-11 2.3×10-3 1.8×10-10 1.9×10-12
sp
下列有关说法不正确的是( )
A.浓度均为0.2 mol·L-1的AgNO 溶液和CHCOONa溶液等体积混合一定产生CHCOOAg沉淀
3 3 3
B.将0.001 mol·L-1的AgNO 溶液滴入0.001 mol·L-1的KCl和0.001 mol·L-1的KCrO 混合溶液中,
3 2 4
先产生AgCl沉淀
C.0.11 mol·L-1的MgCl 溶液中加入氨水产生Mg(OH) 沉淀时溶液的pH为9
2 2
D.在其他条件不变的情况下,向饱和AgCl溶液中加入NaCl溶液,K (AgCl)增大
sp
15.钡(Ba)和锶(Sr)及其化合物在工业上有着广泛的应用,它们在地壳中常以硫酸盐的形式存在,
BaSO 和SrSO 都是难溶性盐。工业上提取钡和锶时首先是将BaSO 和SrSO 转化成难溶弱酸盐。
4 4 4 4
已知:SrSO (s) Sr2+(aq)+ SO 2-(aq) K =2.5×10-7;
4 4 sp
SrCO (s) Sr2+(aq)+ CO2- (aq) K =2.5×10-9。
3 3 sp
(1)将SrSO 转化成SrCO 的离子方程式为 ,反应的平衡常数K的表达式为
4 3
;该反应能发生的原因是 (用沉淀溶解平衡的有关理论解释)。
(2)对于上述反应,实验证明增大CO2-的浓度或降低温度都有利于提高SrSO 的转化率。判断在下列两
3 4
种情况下,平衡常数K的变化情况(填“增大”、“减小”或“不变”):
①升高温度,平衡常数K将 。
②增大CO2-的浓度,平衡常数K将 。
3
(3)已知SrSO 和SrCO 在酸中的溶解性与BaSO 和BaCO 类似,设计实验证明上述过程中 SrSO 是否
4 3 4 3 4
完 全 转 化 成 SrCO 。 实 验 所 用 的 试 剂 为 ; 实 验 现 象 及 其 相 应 结 论 为
3
。
题型四 沉淀溶解平衡图像
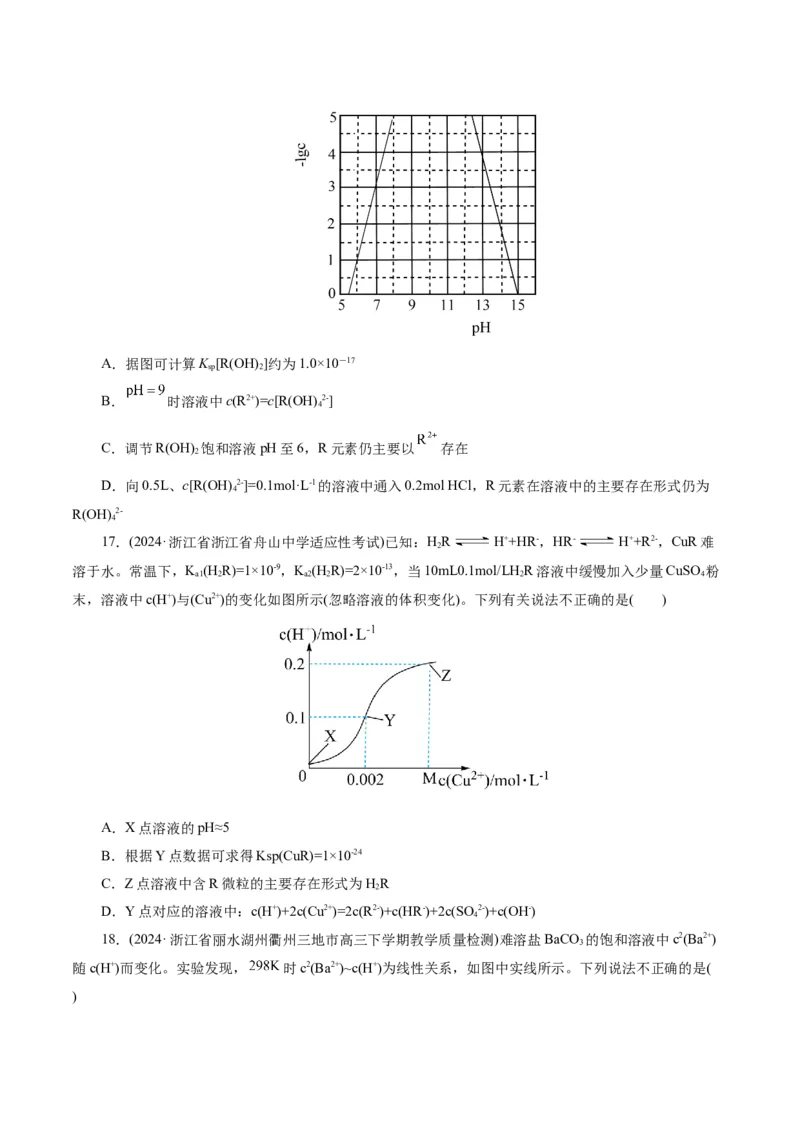
16.(2024·浙江省精诚联盟高三三模)溶液中存在:R(OH) (s) R2+(aq)+2OH−(aq)、R(OH) (s)
2 2
+2OH−(aq) R(OH) 2-(aq)。已知25℃时R2+或R(OH) 2-浓度的负对数(-lgc)与pH的关系如图,下列说法
4 4
不正确的是( )A.据图可计算K [R(OH) ]约为1.0×10-17
sp 2
B. 时溶液中c(R2+)=c[R(OH) 2-]
4
C.调节R(OH) 饱和溶液pH至6,R元素仍主要以 存在
2
D.向0.5L、c[R(OH) 2-]=0.1mol·L-1的溶液中通入0.2mol HCl,R元素在溶液中的主要存在形式仍为
4
R(OH) 2-
4
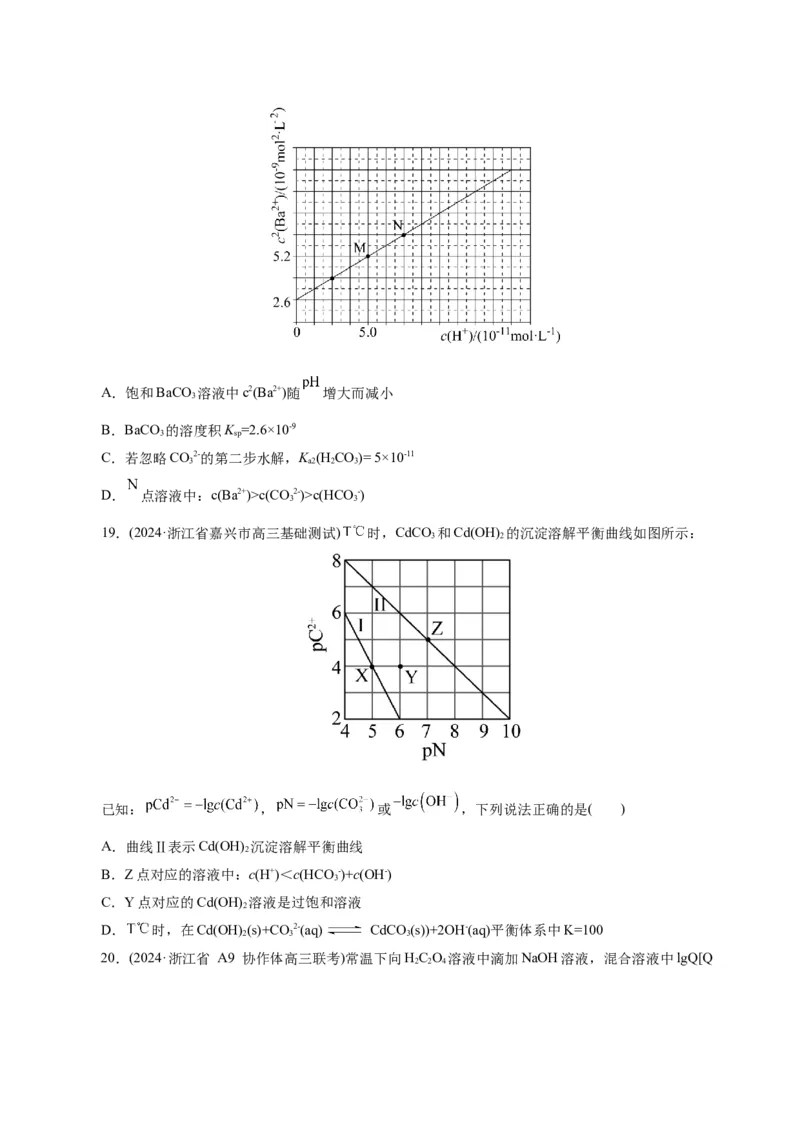
17.(2024·浙江省浙江省舟山中学适应性考试)已知:HR H++HR-,HR- H++R2-,CuR难
2
溶于水。常温下,K (H R)=1×10-9,K (H R)=2×10-13,当10mL0.1mol/LH R溶液中缓慢加入少量CuSO 粉
a1 2 a2 2 2 4
末,溶液中c(H+)与(Cu2+)的变化如图所示(忽略溶液的体积变化)。下列有关说法不正确的是( )
A.X点溶液的pH≈5
B.根据Y点数据可求得Ksp(CuR)=1×10-24
C.Z点溶液中含R微粒的主要存在形式为HR
2
D.Y点对应的溶液中:c(H+)+2c(Cu2+)=2c(R2-)+c(HR-)+2c(SO2-)+c(OH-)
4
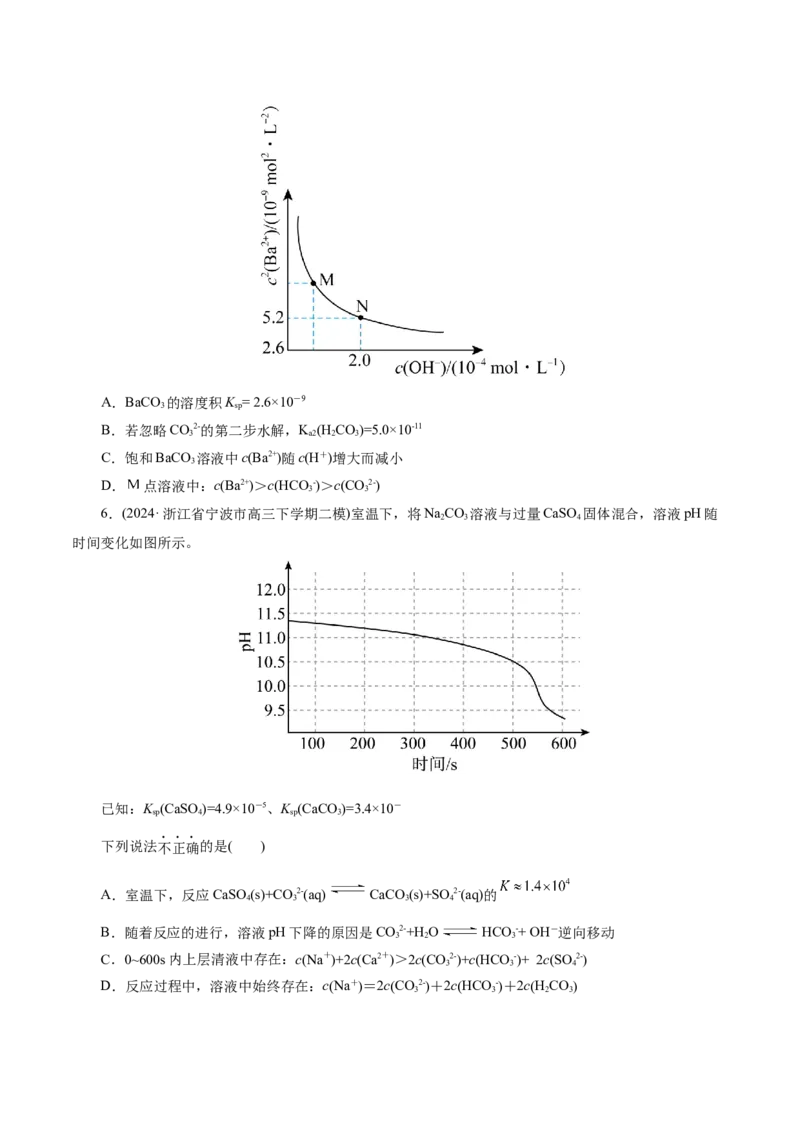
18.(2024·浙江省丽水湖州衢州三地市高三下学期教学质量检测)难溶盐BaCO 的饱和溶液中c2(Ba2+)
3
随c(H+)而变化。实验发现, 时c2(Ba2+)~c(H+)为线性关系,如图中实线所示。下列说法不正确的是(
)A.饱和BaCO 溶液中c2(Ba2+)随 增大而减小
3
B.BaCO 的溶度积K =2.6×10-9
3 sp
C.若忽略CO2-的第二步水解,K (H CO)= 5×10-11
3 a2 2 3
D. 点溶液中:c(Ba2+)>c(CO 2-)>c(HCO-)
3 3
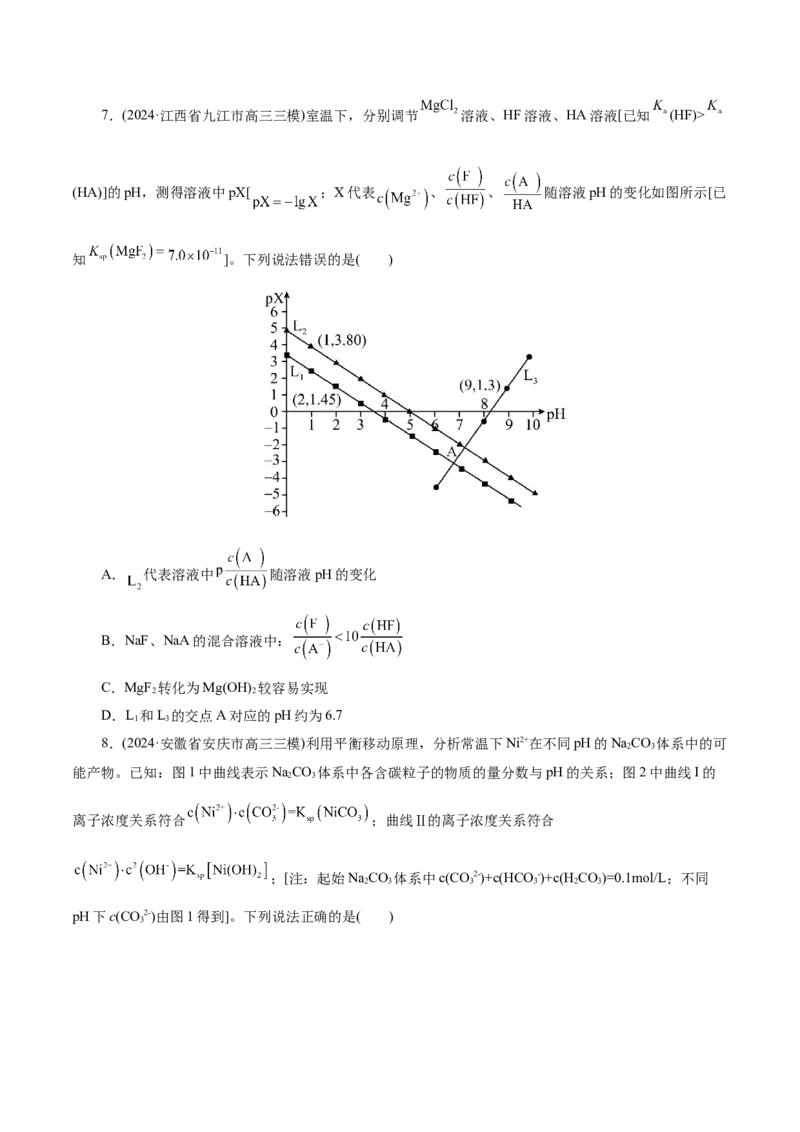
19.(2024·浙江省嘉兴市高三基础测试) 时,CdCO 和Cd(OH) 的沉淀溶解平衡曲线如图所示:
3 2
已知: , 或 ,下列说法正确的是( )
A.曲线Ⅱ表示Cd(OH) 沉淀溶解平衡曲线
2
B.Z点对应的溶液中:c(H+)<c(HCO -)+c(OH-)
3
C.Y点对应的Cd(OH) 溶液是过饱和溶液
2
D. 时,在Cd(OH) (s)+CO2-(aq) CdCO(s))+2OH-(aq)平衡体系中K=100
2 3 3
20.(2024·浙江省 A9 协作体高三联考)常温下向HC O 溶液中滴加NaOH溶液,混合溶液中lgQ[Q
2 2 4表示 或 随pH的变化关系如图所示。已知常温下,Ksp(CaC O)=10-8.63,下列说法不正
2 4
确的是( )
A.NaHC O 溶液中:c(HC O)c(C O2-)>c(H C O)
2 2 4 2 2 4
1.(2024·天津市第七中学高三检测)已知:室温下氢硫酸(H S)的K =1×10-7,K =1.3×10-13;CuS、FeS
2 a1 a2
的K 分别为6.3×10-36,6.5×10-18。下列说法不正确的是( )
sp
A.反应H++FeS Fe2++HS-的平衡常数K=5×10-5
B.可以用FeS除去污水中的CuS
C.从上述数据可推出CuS难溶于稀硫酸
D.0.1mol/L的HS溶液中加入等体积0.1mol/L的NaOH溶液,则有:
2
c(Na+)>c(HS-)>c(H S)>c(S2-)>c(OH-)>c(H+)
2
2.(2024·北京市西城区高三一模)实验小组设计实验除去粗盐溶液中的Ca2+、Mg2+、SO 2-并进行定性
4
检验。
已知:K [Mg(OH) ]=5.6×10-12,K (BaSO)=1.1×10-10,K (BaCO)=2.6×10-9。
sp 2 sp 4 sp 3下列说法不正确的是( )
A.调节溶液的pH>12,可使滤液中c(Mg2+)<1×10-5mol/L
B.加入NaCO 溶液发生的反应是Ba2++CO 2-=BaCO ↓、Ca2++CO 2-=CaCO ↓
2 3 3 3 3 3
C.加入盐酸发生的反应是2H++CO 2-=CO ↑+H O、H++OH-=H O
3 2 2 2
D.若步骤①加入BaCl 溶液后进行过滤,可以避免白色沉淀M的生成
2
3.(2024·浙江省金丽衢十二校高三联考模拟预测)钡餐造影检查是以医用硫酸钡作为造影剂,口服后
随着人体消化管道的蠕动,涂抹在胃肠道内管壁及充填在管腔内,在X线照射下与周围器官形成明显对比,
可以观察胃、食管等器官的外形、大小、位置、扩张性及蠕动波情况,进而显示消化道有无病变。
已知:常温下,K (BaCO)=5.0×10-9,K (BaSO)=1.0×10-10;HCO 的电离平衡常数K =4.5×10-7,
sp 3 sp 2 3 a1
K =5.6×10-11;饱和BaCO 溶液pH约为9.6,人体胃液pH约为2;HSO 的一级电离是完全电离,二级电
a2 3 2 4
离电离常数K =1.0×10-2。结合信息,以下推断不正确的是( )
a2
A.BaSO 在胃液中的溶解度大于1.0×10-5mol·L-1
4
B.若每次加入1L1mol·L-1的NaCO 溶液,至少需要4次加入才能将0.1mol BaSO 全部转化为BaCO
2 3 4 3
C.饱和BaCO 溶液通入少量CO 后溶液中:c(CO2-)<c(HCO -)
3 2 3 3
D.若误服BaCO ,医学上可采用适当浓度的NaSO 溶液洗胃或静脉缓注NaSO 溶液实现解毒
3 2 4 2 4
4.(2024·浙江省强基联盟高三联考)HCO 是二元弱酸。某小组做如下两组实验:
2 3
实验Ⅰ:向 浓度均为0.1mol·L-1的NaCO 和NaHCO 的混合溶液中滴加0.1mol·L-1HCl 溶液。
2 3 3
实验Ⅱ:向20mL0.1mol·L-1NaHCO 溶液中滴加0.1mol·L-1CaCl 溶液,产生白色沉淀。[已知:HCO
3 2 2 3
的电离常数K =4.5×10-7,K =4.7×10-11;K (CaCO)= 3.3×10-9;不考虑碳酸的分解]
a1 a2 sp 3
下列说法不正确的是( )
A.实验Ⅰ可选用双指示剂指示终点,依次为酚酞、甲基红(变色范围4.4~6.2)
B.实验Ⅰ中 时,存在2c(Na+)=3[c(CO2-)+c(HCO -)+c(H CO)]
3 3 2 3
C.实验Ⅱ中发生反应:Ca2++2HCO-=CaCO ↓ +H CO
3 3 2 3
D.实验Ⅱ中, 时,溶液中c(CO2-)= 1.0×10-11mol·L-1
3
5.(2024·河北省部分示范高中高三三模)饱和BaCO 溶液中,c2(Ba2+)随c(OH-)而变化,在 温度下,
3
c2(Ba2+)与c(OH-)关系如右图所示。下列说法错误的是( )A.BaCO 的溶度积K = 2.6×10-9
3 sp
B.若忽略CO2-的第二步水解,K (H CO)=5.0×10-11
3 a2 2 3
C.饱和BaCO 溶液中c(Ba2+)随c(H+)增大而减小
3
D. 点溶液中:c(Ba2+)>c(HCO -)>c(CO2-)
3 3
6.(2024·浙江省宁波市高三下学期二模)室温下,将NaCO 溶液与过量CaSO 固体混合,溶液pH随
2 3 4
时间变化如图所示。
已知:K (CaSO)=4.9×10-5、K (CaCO)=3.4×10-
sp 4 sp 3
下列说法不正确的是( )
A.室温下,反应CaSO(s)+CO2-(aq) CaCO (s)+SO 2-(aq)的
4 3 3 4
B.随着反应的进行,溶液pH下降的原因是CO2-+H O HCO -+ OH-逆向移动
3 2 3
C.0~600s内上层清液中存在:c(Na+)+2c(Ca2+)>2cCO2-+cHCO -+ 2cSO 2-
3 3 4
D.反应过程中,溶液中始终存在:cNa+=2cCO2-+2cHCO -+2cHCO
3 3 2 37.(2024·江西省九江市高三三模)室温下,分别调节 溶液、HF溶液、HA溶液[已知 (HF)>
(HA)]的pH,测得溶液中pX[ ;X代表 、 、 随溶液pH的变化如图所示[已
知 ]。下列说法错误的是( )
A. 代表溶液中 随溶液pH的变化
B.NaF、NaA的混合溶液中:
C.MgF 转化为Mg(OH) 较容易实现
2 2
D.L 和L 的交点A对应的pH约为6.7
1 3
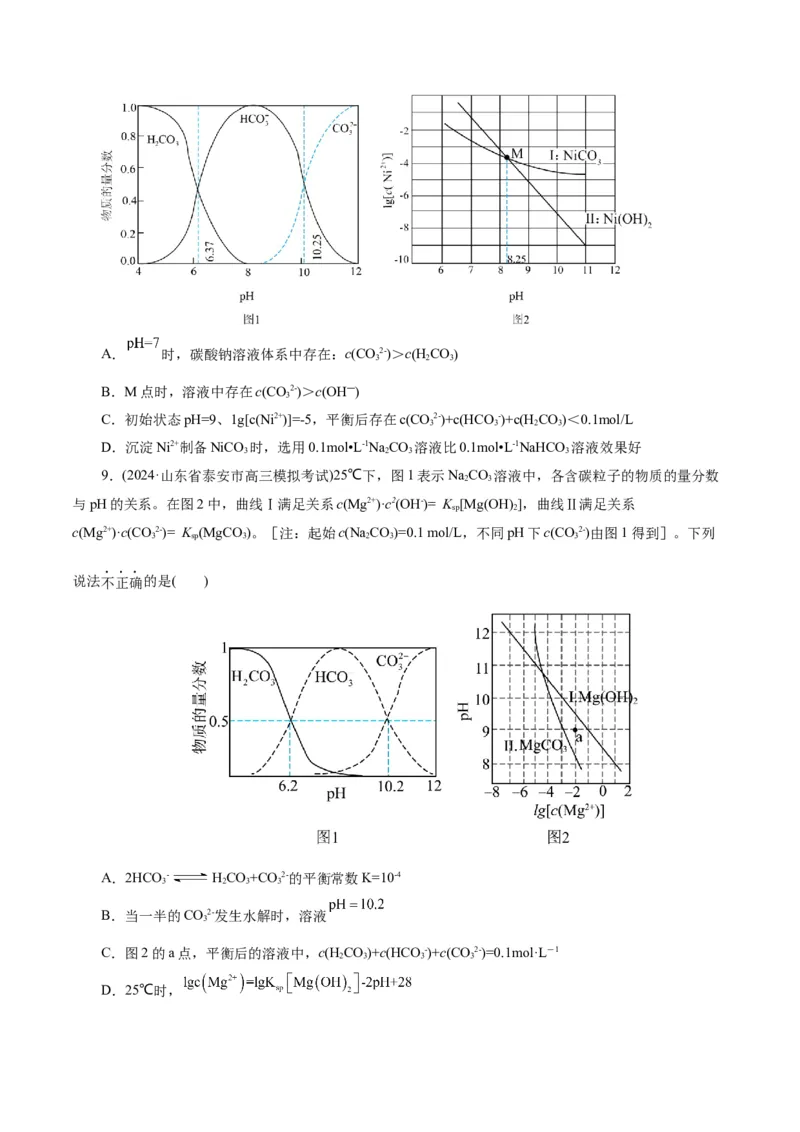
8.(2024·安徽省安庆市高三三模)利用平衡移动原理,分析常温下Ni2+在不同pH的NaCO 体系中的可
2 3
能产物。已知:图1中曲线表示NaCO 体系中各含碳粒子的物质的量分数与pH的关系;图2中曲线I的
2 3
离子浓度关系符合 ;曲线Ⅱ的离子浓度关系符合
;[注:起始NaCO 体系中c(CO2-)+c(HCO-)+c(H CO)=0.1mol/L;不同
2 3 3 3 2 3
pH下c(CO2-)由图1得到]。下列说法正确的是( )
3A. 时,碳酸钠溶液体系中存在:c(CO2-)>cHCO
3 2 3
B.M点时,溶液中存在c(CO2-)>c(OH―)
3
C.初始状态pH=9、1g[c(Ni2+)]=-5,平衡后存在c(CO2-)+c(HCO-)+c(H CO)<0.1mol/L
3 3 2 3
D.沉淀Ni2+制备NiCO 时,选用0.1mol•L-1NaCO 溶液比0.1mol•L-1NaHCO 溶液效果好
3 2 3 3
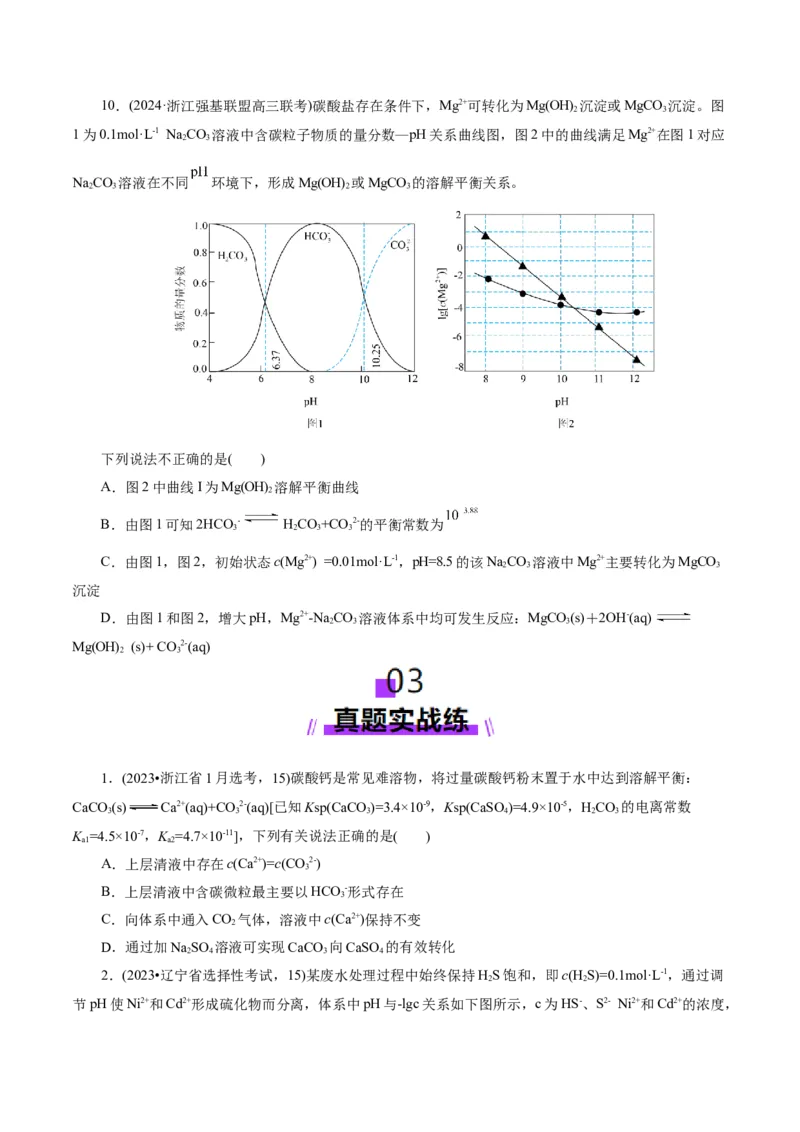
9.(2024·山东省泰安市高三模拟考试)25℃下,图1表示NaCO 溶液中,各含碳粒子的物质的量分数
2 3
与pH的关系。在图2中,曲线Ⅰ满足关系c(Mg2+)·c2(OH-)= K [Mg(OH) ],曲线Ⅱ满足关系
sp 2
c(Mg2+)·c(CO2-)= K (MgCO )。[注:起始c(Na CO)=0.1 mol/L,不同pH下c(CO2-)由图1得到]。下列
3 sp 3 2 3 3
说法不正确的是( )
A.2HCO - HCO+CO 2-的平衡常数K=10-4
3 2 3 3
B.当一半的CO2-发生水解时,溶液
3
C.图2的a点,平衡后的溶液中,c(H CO)+c(HCO -)+c(CO2-)=0.1mol·L-1
2 3 3 3
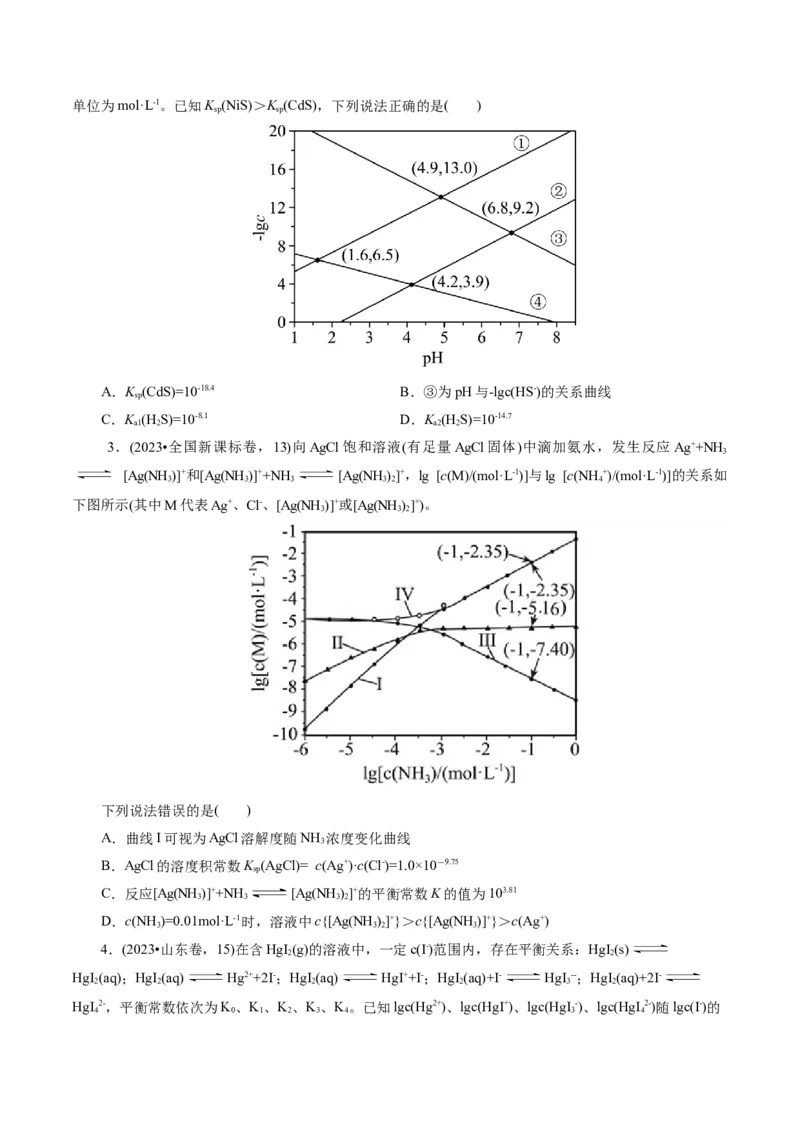
D.25℃时,10.(2024·浙江强基联盟高三联考)碳酸盐存在条件下,Mg2+可转化为Mg(OH) 沉淀或MgCO 沉淀。图
2 3
1为0.1mol·L-1 Na CO 溶液中含碳粒子物质的量分数—pH关系曲线图,图2中的曲线满足Mg2+在图1对应
2 3
NaCO 溶液在不同 环境下,形成Mg(OH) 或MgCO 的溶解平衡关系。
2 3 2 3
下列说法不正确的是( )
A.图2中曲线I为Mg(OH) 溶解平衡曲线
2
B.由图1可知2HCO - HCO+CO 2-的平衡常数为
3 2 3 3
C.由图1,图2,初始状态c(Mg2+) =0.01mol·L-1,pH=8.5的该NaCO 溶液中Mg2+主要转化为MgCO
2 3 3
沉淀
D.由图1和图2,增大pH,Mg2+-Na CO 溶液体系中均可发生反应:MgCO(s)+2OH-(aq)
2 3 3
Mg(OH) (s)+ CO 2-(aq)
2 3
1.(2023•浙江省1月选考,15)碳酸钙是常见难溶物,将过量碳酸钙粉末置于水中达到溶解平衡:
CaCO (s) Ca2+(aq)+CO 2-(aq)[已知Ksp(CaCO)=3.4×10-9,Ksp(CaSO )=4.9×10-5,HCO 的电离常数
3 3 3 4 2 3
K =4.5×10-7,K =4.7×10-11],下列有关说法正确的是( )
a1 a2
A.上层清液中存在c(Ca2+)=c(CO2-)
3
B.上层清液中含碳微粒最主要以HCO -形式存在
3
C.向体系中通入CO 气体,溶液中c(Ca2+)保持不变
2
D.通过加NaSO 溶液可实现CaCO 向CaSO 的有效转化
2 4 3 4
2.(2023•辽宁省选择性考试,15)某废水处理过程中始终保持HS饱和,即c(H S)=0.1mol·L-1,通过调
2 2
节pH使Ni2+和Cd2+形成硫化物而分离,体系中pH与-lgc关系如下图所示,c为HS-、S2- Ni2+和Cd2+的浓度,单位为mol·L-1。已知K (NiS)>K (CdS),下列说法正确的是( )
sp sp
A.K (CdS)=10-18.4 B.③为pH与-lgc(HS-)的关系曲线
sp
C.K (H S)=10-8.1 D.K (H S)=10-14.7
a1 2 a2 2
3.(2023•全国新课标卷,13)向AgCl饱和溶液(有足量AgCl固体)中滴加氨水,发生反应 Ag++NH
3
[Ag(NH)]+和[Ag(NH)]++NH [Ag(NH)]+,lg [c(M)/(mol·L-1)]与lg [c(NH +)/(mol·L-1)]的关系如
3 3 3 3 2 4
下图所示(其中M代表Ag+、Cl-、[Ag(NH)]+或[Ag(NH)]+)。
3 3 2
下列说法错误的是( )
A.曲线I可视为AgCl溶解度随NH 浓度变化曲线
3
B.AgCl的溶度积常数K (AgCl)= c(Ag+)·c(Cl-)=1.0×10-9.75
sp
C.反应[Ag(NH)]++NH [Ag(NH)]+的平衡常数K的值为103.81
3 3 3 2
D.c(NH )=0.01mol·L-1时,溶液中c{[Ag(NH)]+}>c{[Ag(NH)]+}>c(Ag+)
3 3 2 3
4.(2023•山东卷,15)在含HgI (g)的溶液中,一定c(I-)范围内,存在平衡关系:HgI (s)
2 2
HgI (aq);HgI (aq) Hg2++2I-;HgI (aq) HgI++I-;HgI (aq)+I- HgI --;HgI (aq)+2I-
2 2 2 2 3 2
HgI 2-,平衡常数依次为K、K、K、K、K。已知lgc(Hg2+)、lgc(HgI+)、lgc(HgI -)、lgc(HgI 2-)随lgc(I-)的
4 0 1 2 3 4 3 4变化关系如图所示,下列说法错误的是( )
A.线 表示lgc(HgI 2-)的变化情况
4
B.随c(I-)增大,c[HgI (aq)]先增大后减小
2
C.
D.溶液中I元素与 元素的物质的量之比始终为2:1
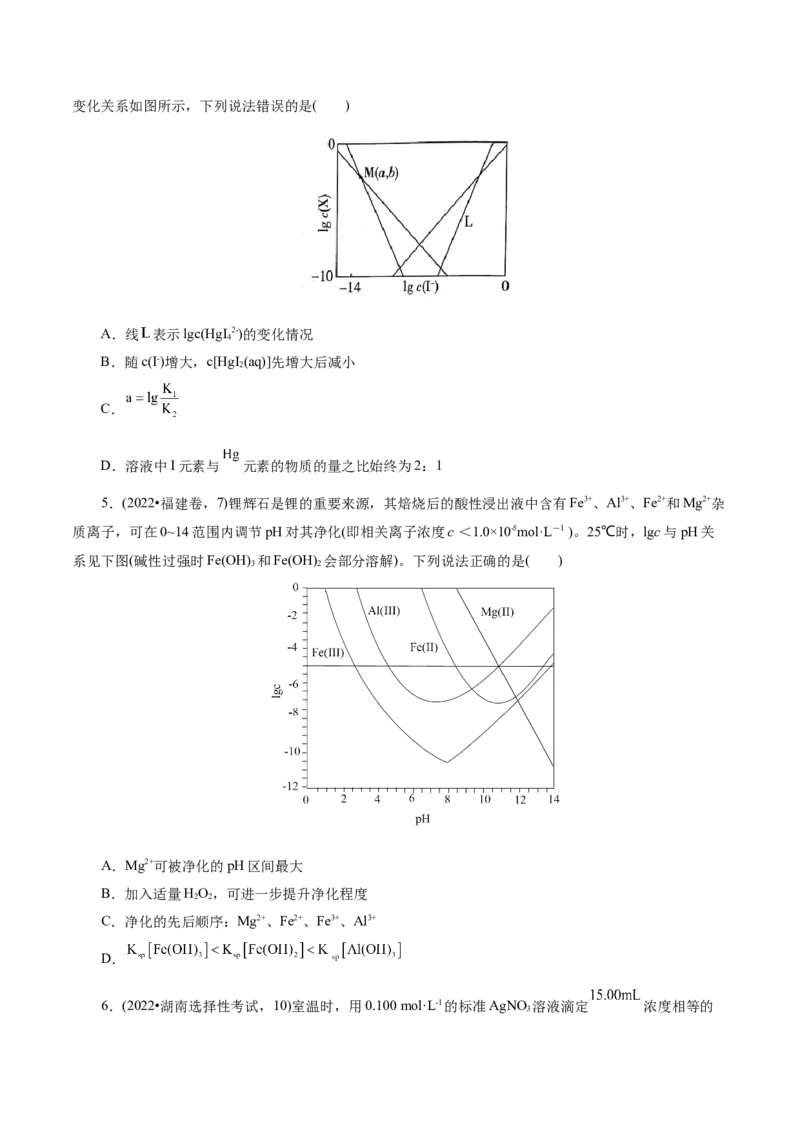
5.(2022•福建卷,7)锂辉石是锂的重要来源,其焙烧后的酸性浸出液中含有Fe3+、Al3+、Fe2+和Mg2+杂
质离子,可在0~14范围内调节pH对其净化(即相关离子浓度c <1.0×10-5mol·L-1 )。25℃时,lgc与pH关
系见下图(碱性过强时Fe(OH) 和Fe(OH) 会部分溶解)。下列说法正确的是( )
3 2
A.Mg2+可被净化的pH区间最大
B.加入适量HO,可进一步提升净化程度
2 2
C.净化的先后顺序:Mg2+、Fe2+、Fe3+、Al3+
D.
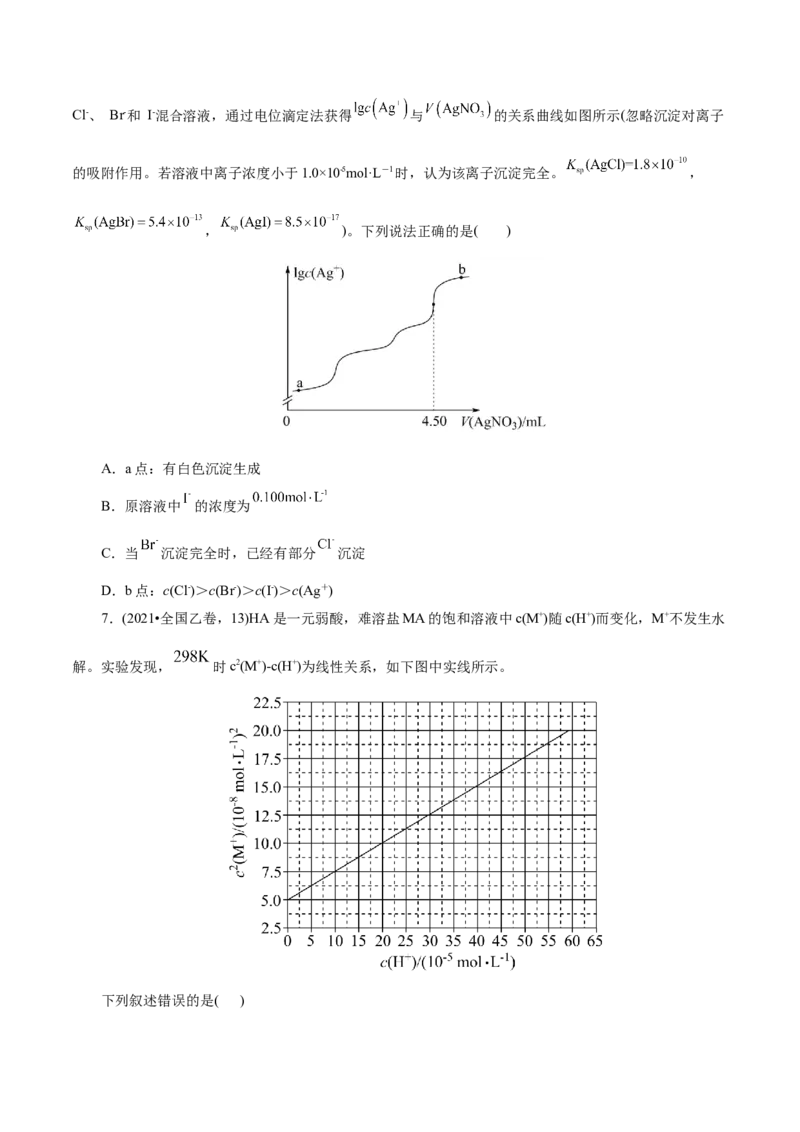
6.(2022•湖南选择性考试,10)室温时,用0.100 mol·L-1的标准AgNO 溶液滴定 浓度相等的
3Cl-、 Br-和 I-混合溶液,通过电位滴定法获得 与 的关系曲线如图所示(忽略沉淀对离子
的吸附作用。若溶液中离子浓度小于1.0×10-5mol·L-1时,认为该离子沉淀完全。 ,
, )。下列说法正确的是( )
A.a点:有白色沉淀生成
B.原溶液中 的浓度为
C.当 沉淀完全时,已经有部分 沉淀
D.b点:c(Cl-)>c(Br-)>c(I-)>c(Ag+)
7.(2021•全国乙卷,13)HA是一元弱酸,难溶盐MA的饱和溶液中c(M+)随c(H+)而变化,M+不发生水
解。实验发现, 时c2(M+)-c(H+)为线性关系,如下图中实线所示。
下列叙述错误的是( )A.溶液pH=4时,c(M+)<3.0×10-4mol·L-1
B.MA的溶度积度积K (MA)=5.0×10-8
sp
C.溶液pH=7时,c(M+)+c(H+) =c(A-)+c(OH―)
D.HA的电离常数K (HA)≈2.0×10-4
a1