文档内容
课题3 溶质的质量分数(三课时)
第三课时
[提问]1.20℃时,食盐的溶解度是36g,这句话的含义是什么?
2.什么叫溶质的质量分数?写出溶质质量分数的计算公式。
[回答]
[设问]溶解度与溶质的质量分数概念间有什么区别和联系?
[板书]三、溶解度与溶质的质量分数间的区别和联系
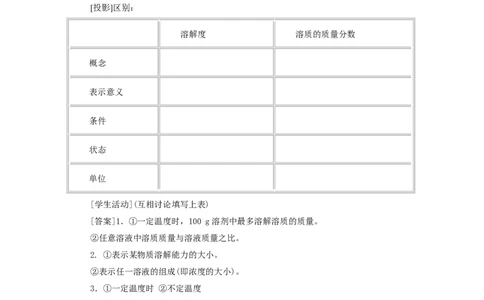
[投影]区别:
溶解度 溶质的质量分数
概念
表示意义
条件
状态
单位
[学生活动](互相讨论填写上表)
[答案]1.①一定温度时,100 g溶剂中最多溶解溶质的质量。
②任意溶液中溶质质量与溶液质量之比。
2. ①表示某物质溶解能力的大小。
②表示任一溶液的组成(即浓度的大小)。
3.①一定温度时 ②不定温度
4.①饱和状态 ②可饱和可不饱和
5.①g ②无单位
[设问]两个概念间有何联系?
[讨论]1.溶液是均一的,一种溶液各部分的溶质的质量分数是否相同?
2.对饱和溶液来说,若溶剂的质量是100 g,溶质的质量是多少?
3.试分析溶解度与饱和溶液中溶质的质量分数的关系。
[小结]1. 一种溶液各部分的溶质的质量分数是相同的。
12.对饱和溶液(某温度)来说,若溶剂的质量是100 g,溶质的质量是该温度下此溶质的溶解
度。
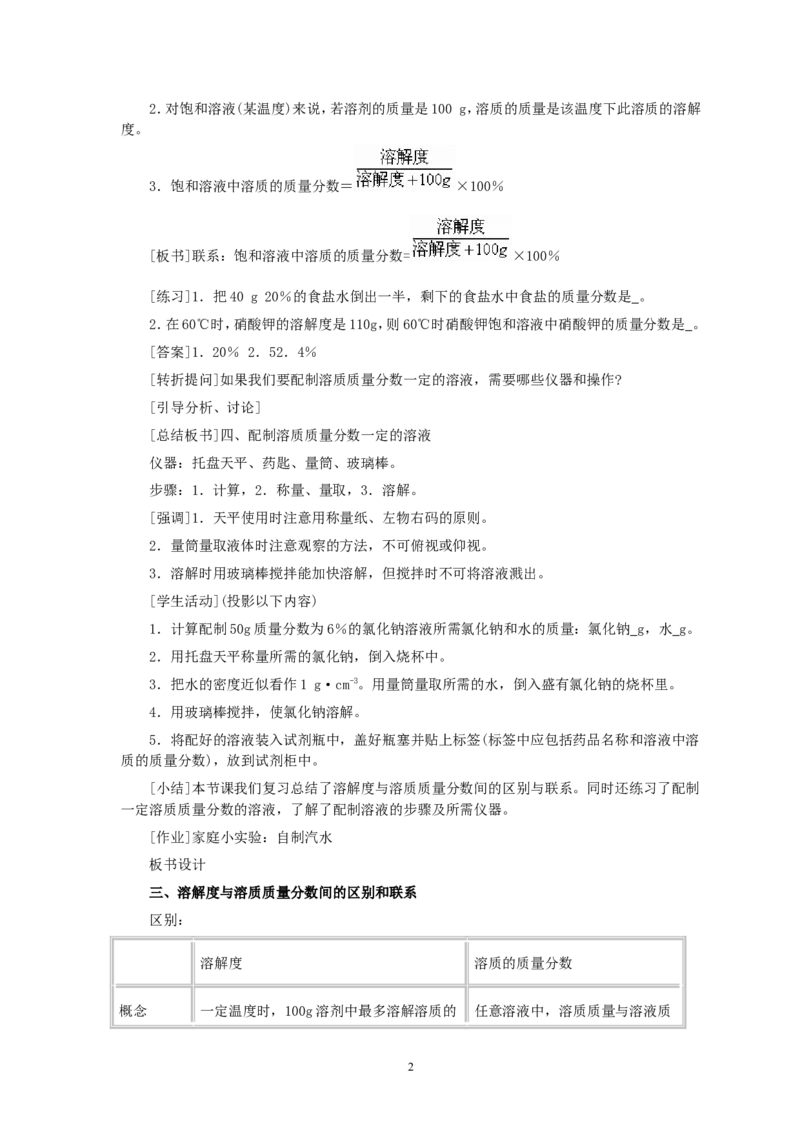
3.饱和溶液中溶质的质量分数= ×100%
[板书]联系:饱和溶液中溶质的质量分数= ×100%
[练习]1.把40 g 20%的食盐水倒出一半,剩下的食盐水中食盐的质量分数是 。
2.在60℃时,硝酸钾的溶解度是110g,则60℃时硝酸钾饱和溶液中硝酸钾的质量分数是 。
[答案]1.20% 2.52.4%
[转折提问]如果我们要配制溶质质量分数一定的溶液,需要哪些仪器和操作?
[引导分析、讨论]
[总结板书]四、配制溶质质量分数一定的溶液
仪器:托盘天平、药匙、量筒、玻璃棒。
步骤:1.计算,2.称量、量取,3.溶解。
[强调]1.天平使用时注意用称量纸、左物右码的原则。
2.量筒量取液体时注意观察的方法,不可俯视或仰视。
3.溶解时用玻璃棒搅拌能加快溶解,但搅拌时不可将溶液溅出。
[学生活动](投影以下内容)
1.计算配制50g质量分数为6%的氯化钠溶液所需氯化钠和水的质量:氯化钠 g,水 g。
2.用托盘天平称量所需的氯化钠,倒入烧杯中。
3.把水的密度近似看作1 g·cm-3。用量筒量取所需的水,倒入盛有氯化钠的烧杯里。
4.用玻璃棒搅拌,使氯化钠溶解 。
5.将配好的溶液装入试剂瓶中,盖好瓶塞并贴上标签(标签中应包括药品名称和溶液中溶
质的质量分数),放到试剂柜中。
[小结]本节课我们复习总结了溶解度与溶质质量分数间的区别与联系。同时还练习了配制
一定溶质质量分数的溶液,了解了配制溶液的步骤及所需仪器。
[作业]家庭小实验:自制汽水
板书设计
三、溶解度与溶质质量分数间的区别和联系
区别:
溶解度 溶质的质量分数
概念 一定温度时,100g溶剂中最多溶解溶质的 任意溶液中,溶质质量与溶液质
2质量 量之比
表示意义 某物质溶解能力的大小 任一溶液的浓度大小
条件 一定温度 不定温度
状态 饱和状态 可饱和可不饱和
单位 g 无单位
联系:
饱和溶液中溶质的质量分数= ×100%
四、配制溶质质量分数一定的溶液
仪器:托盘天平、药匙、量简、玻璃棒。
步骤:1. 计算.2.称量、量取,3.溶解。
考题回顾
1.有关溶液(溶质为固体)的说法中,正确的是 ……………( )
A.对于同一溶质的溶液而言,饱和溶液一定比不饱和溶液浓
B. 只要温度不变,某物质饱和溶液中溶质的质量分数也不变
C. 饱和溶液中析出晶体后,溶质的质量分数一定减小
D. 不饱和溶液转化为饱和溶液,其溶质的质量分数一定增加
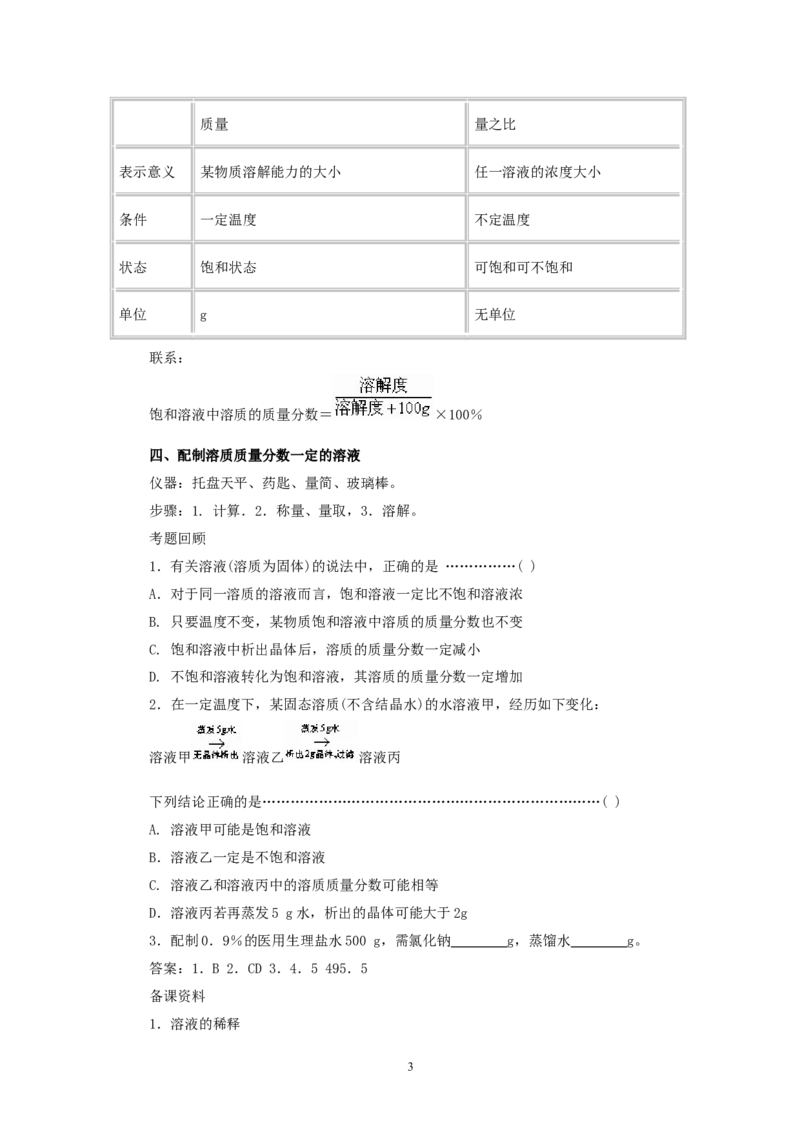
2.在一定温度下,某固态溶质(不含结晶水)的水溶液甲,经历如下变化:
溶液甲 溶液乙 溶液丙
下列结论正确的是………………………………………………………………( )
A. 溶液甲可能是饱和溶液
B.溶液乙一定是不饱和溶液
C. 溶液乙和溶液丙中的溶质质量分数可能相等
D.溶液丙若再蒸发5 g水,析出的晶体可能大于2g
3.配制0.9%的医用生理盐水500 g,需氯化钠________g,蒸馏水________g。
答案:1.B 2.CD 3.4.5 495.5
备课资料
1.溶液的稀释
3根据稀释前后溶质的总量不变进行运算,无论是用水,或是用稀溶液来稀释浓溶液,都可计
算。
(1)用水稀释浓溶液
设稀释前的浓溶液的质量为m,其溶质的质量分数为a%,稀释时加入水的质量为n,稀释后
溶质的质量分数为b%。
则可得 m×a%=(m+n)×b%
(2)用稀溶液稀释浓溶液
设浓溶液的质量为A,其溶质的质量分数为a%,稀溶液的质量为B,其溶质的质量分数为
b%,两液混合后的溶质的质量分数为c%。
则可得 A×a%+B×b%=(A+B)×c% (1)
或 (2)
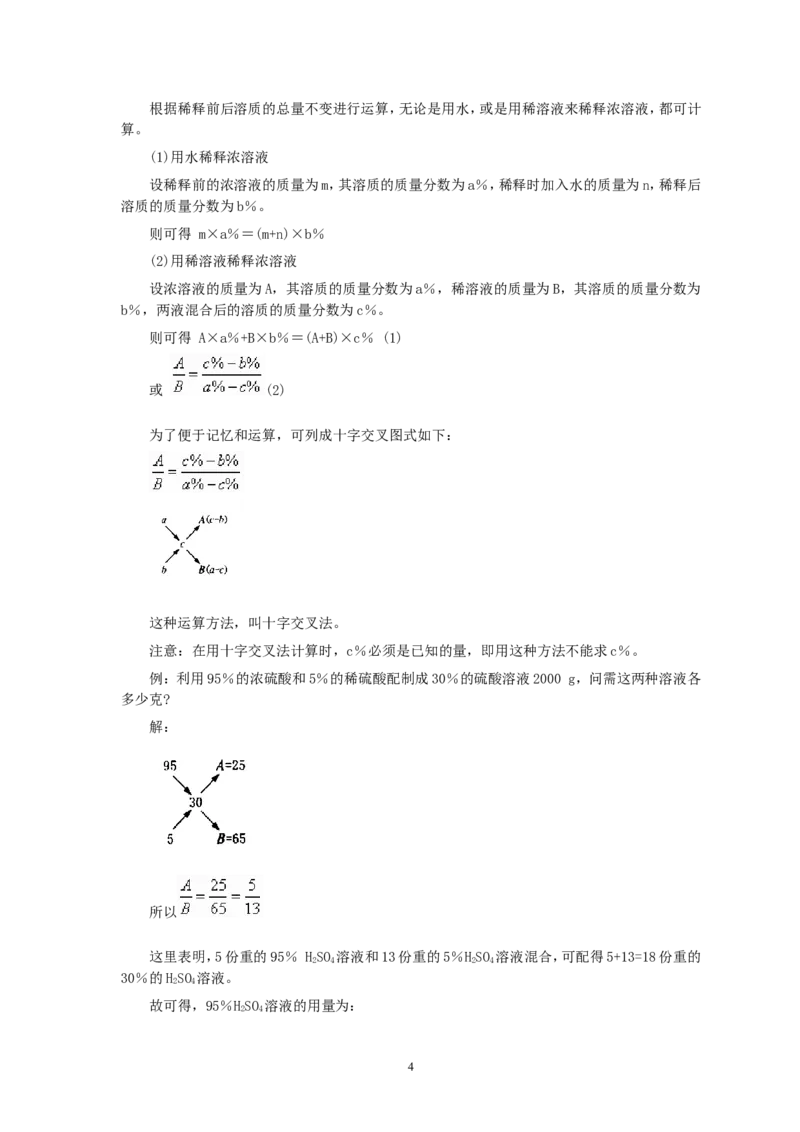
为了便于记忆和运算,可列成十字交叉图式如下:
这种运算方法,叫十字交叉法。
注意:在用十字交叉法计算时,c%必须是已知的量,即用这种方法不能求c%。
例:利用95%的浓硫酸和5%的稀硫酸配制成30%的硫酸溶液2000 g,问需这两种溶液各
多少克?
解:
所以
这里表明,5份重的95% HSO 溶液和13份重的5%HSO 溶液混合,可配得5+13=18份重的
2 4 2 4
30%的HSO 溶液。
2 4
故可得,95%HSO 溶液的用量为:
2 4
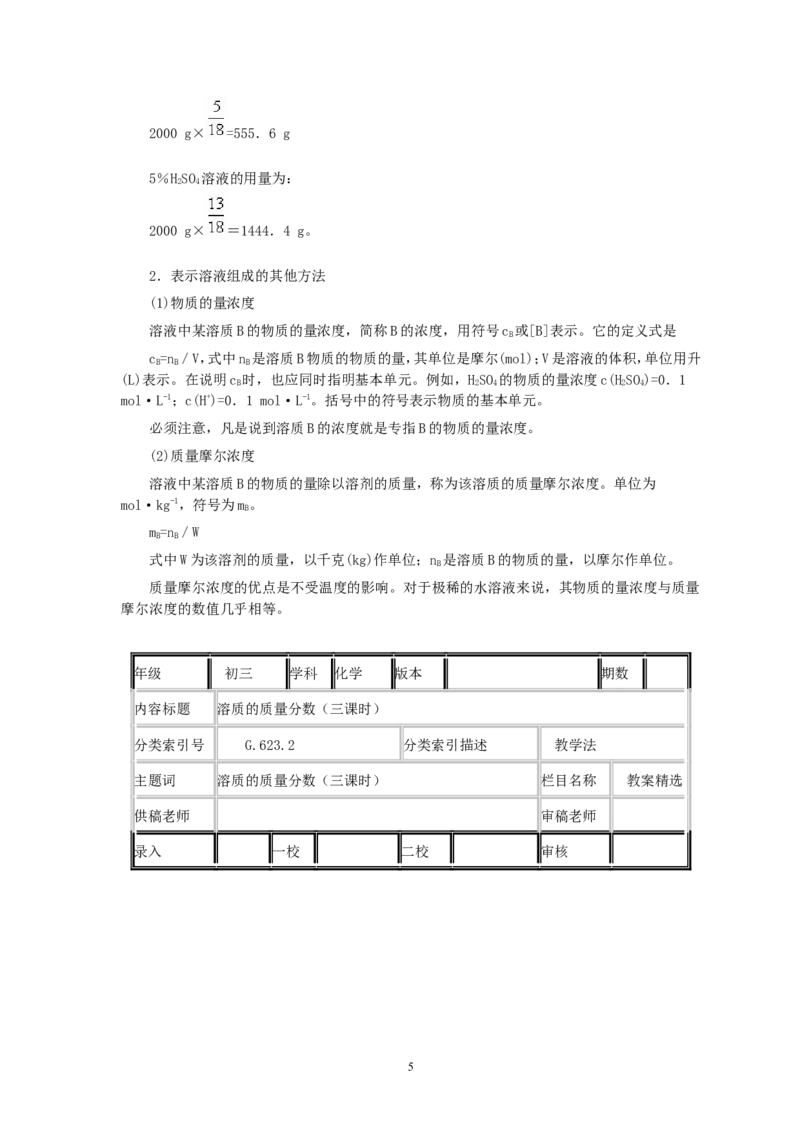
42000 g× =555.6 g
5%HSO 溶液的用量为:
2 4
2000 g× =1444.4 g。
2.表示溶液组成的其他方法
(1)物质的量浓度
溶液中某溶质B的物质的量浓度,简称B的浓度,用符号c 或[B]表示。它的定义式是
B
c=n/V,式中n 是溶质B物质的物质的量,其单位是摩尔(mol);V是溶液的体积,单位用升
B B B
(L)表示。在说明c 时,也应同时指明基本单元。例如,HSO 的物质的量浓度c(HSO)=0.1
B 2 4 2 4
mol·L-1;c(H+)=0.1 mol·L-1。括号中的符号表示物质的基本单元。
必须注意,凡是说到溶质B的浓度就是专指B的物质的量浓度。
(2)质量摩尔浓度
溶液中某溶质B的物质的量除以溶剂的质量,称为该溶质的质量摩尔浓度。单位为
mol·kg-1,符号为m。
B
m=n/W
B B
式中W为该溶剂的质量,以千克(kg)作单位;n 是溶质B的物质的量,以摩尔作单位。
B
质量摩尔浓度的优点是不受温度的影响。对于极稀的水溶液来说,其物质的量浓度与质量
摩尔浓度的数值几乎相等。
年级 初三 学科 化学 版本 期数
内容标题 溶质的质量分数(三课时)
分类索引号 G.623.2 分类索引描述 教学法
主题词 溶质的质量分数(三课时) 栏目名称 教案精选
供稿老师 审稿老师
录入 一校 二校 审核
5