文档内容
第 05 讲 氧化还原反应方程式的配平、书写及计算
01 模拟基础练
【题型一】氧化还原反应方程式的书写与配平
【题型二】氧化还原反应的计算方法——电子守恒法
02 重难创新练
03 真题实战练
题型一 氧化还原反应方程式的书写与配平
1.水热法制备 纳米颗粒的反应如下(反应条件忽略):
。下列说法错误的是
A.该反应中 作氧化剂 B.该反应中 和 都是还原剂
C.3个 参加反应时有1个 被氧化 D.离子方程式中
【答案】C
【解析】A.该反应 中氧元素化合价降低,所以O 作氧化剂,故A正确;
2
B.该反应中 的铁元素化合价升高, 中硫元素平均化合价为+2价, 中硫元素的平均化合价
为+2.5价,即S元素化合价升高,所以 和 都是还原剂,故B正确;
C.该反应中每有3个Fe2+参加反应,消耗一个O,但反应时 中氧元素化合价降低,O 作氧化剂被还
2 2
原,故C错误;
D.由电荷守恒可知,3×(+2)+2×(-2)+x×(-1)=1×(-2),解得x=4,故D正确 ;
故答案为:C。
2.工业制硫酸的原理示意图如图:
下列说法不正确的是A.燃烧的化学方程式为4FeS+11O 2Fe O+8SO
2 2 2 3 2
B.1mol SO 和足量O 充分反应转移2mol电子
2 2
C.用98.3%的浓硫酸吸收三氧化硫可避免形成酸雾
D.可用浓氨水吸收生产过程中的尾气并转化为铵盐
【答案】B
【解析】A.FeS 燃烧生成氧化铁和二氧化硫,反应的化学方程式为4FeS+11O 2Fe O+8SO,故A
2 2 2 2 3 2
正确;
B. 反应可逆,1mol SO 和足量O 充分反应转移电子的物质的量小于2mol,故B错
2 2
误;
C.用98.3%的浓硫酸吸收三氧化硫可避免形成酸雾,故C正确;
D.用浓氨水吸收生产过程中的尾气二氧化硫生成亚硫酸铵,故D正确;
选B。
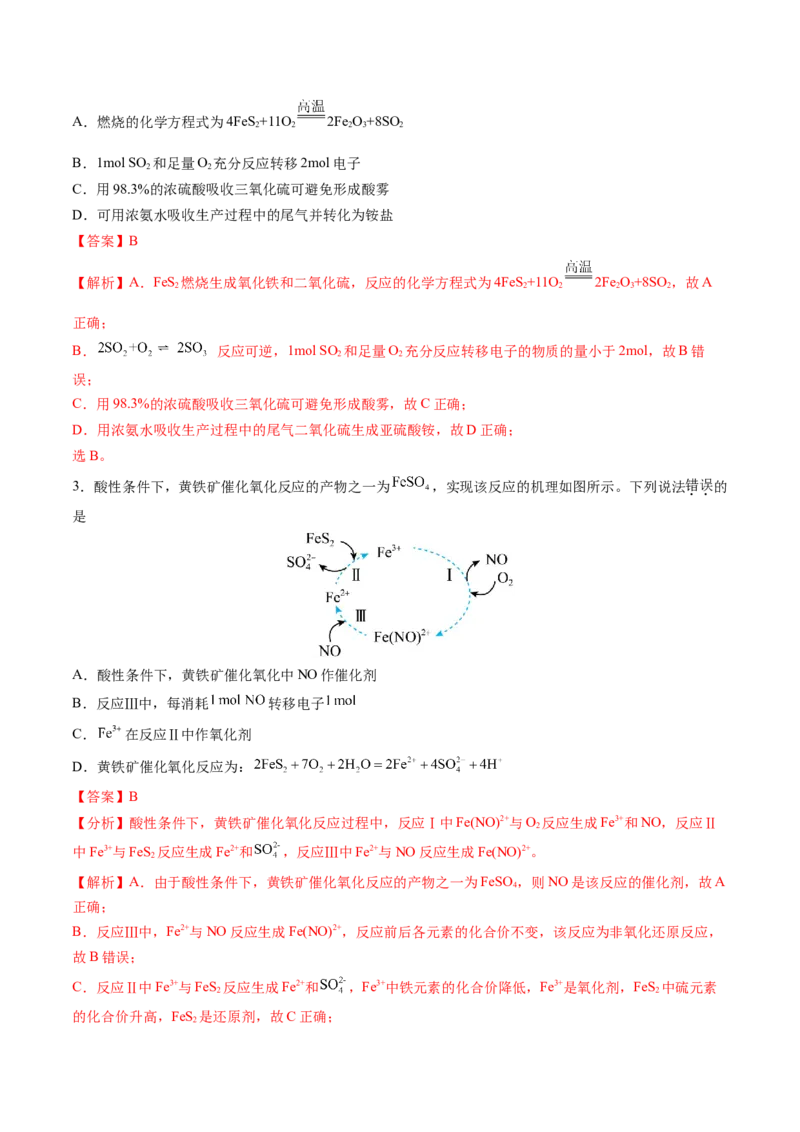
3.酸性条件下,黄铁矿催化氧化反应的产物之一为 ,实现该反应的机理如图所示。下列说法错误的
是
A.酸性条件下,黄铁矿催化氧化中NO作催化剂
B.反应Ⅲ中,每消耗 转移电子
C. 在反应Ⅱ中作氧化剂
D.黄铁矿催化氧化反应为:
【答案】B
【分析】酸性条件下,黄铁矿催化氧化反应过程中,反应Ⅰ中Fe(NO)2+与O 反应生成Fe3+和NO,反应Ⅱ
2
中Fe3+与FeS 反应生成Fe2+和 ,反应Ⅲ中Fe2+与NO反应生成Fe(NO)2+。
2
【解析】A.由于酸性条件下,黄铁矿催化氧化反应的产物之一为FeSO ,则NO是该反应的催化剂,故A
4
正确;
B.反应Ⅲ中,Fe2+与NO反应生成Fe(NO)2+,反应前后各元素的化合价不变,该反应为非氧化还原反应,
故B错误;
C.反应Ⅱ中Fe3+与FeS 反应生成Fe2+和 ,Fe3+中铁元素的化合价降低,Fe3+是氧化剂,FeS 中硫元素
2 2
的化合价升高,FeS 是还原剂,故C正确;
2D.由图可知,黄铁矿催化氧化过程中FeS 和O 是反应物,Fe2+和 是生成物,其反应的离子方程式
2 2
为:2FeS+7O +2H O=2Fe2++4 +4H+,故D正确;
2 2 2
故选:B。
4.(2024·江苏扬州·模拟预测)CuCl为难溶于水的白色固体。室温下,以CuO为原料制备CuCl的过程如
图所示。下列说法正确的是
A.0.1 溶液中:
B.“还原”发生反应的离子方程式为:
C.“还原”后的溶液中:
D.“过滤”后得到的滤液中:
【答案】B
【分析】CuO为碱性氧化物,与稀硫酸发生CuO+2H+=Cu2++H O,“还原”步骤中发生2Cu2++SO +2Cl-
2
+H O=2CuCl↓+SO +2H+,据此分析;
2
【解析】A.利用质子守恒,0.1molNa SO 溶液中存在c(OH-)=c(HSO )+2c(H SO )+c(H+),故A错误;
2 3 2 3
B.“酸溶”步骤中发生CuO+2H+=Cu2++H O,“还原”步骤通入亚硫酸钠和NaCl,得到CuCl,该步骤中
2
Cu2+作氧化剂,亚硫酸钠作还原剂,发生的反应为2Cu2++SO +2Cl-+H O=2CuCl↓+SO +2H+,故B正确;
2
C.还原后溶液还存在Na+,因此根据电荷守恒,推出c(Na+)+2c(Cu2+)+c(H+)=c(OH-)+2c(SO )+c(Cl-),故C
错误;D.过滤后,CuCl为饱和溶液,因此有c(Cu+)·c(Cl-)=K (CuCl),推出c(Cu2+)= ,故D错
sp
误;答案为B。
5.(2024·河北保定·二模) 是一种重要的还原剂,常用于造纸等行业。下列离子方程式错误的是
A.在溴水中滴加 溶液,溶液褪色:
B.在 和 的混合液中滴加稀硫酸:
C.在 溶液中滴加少量 溶液:
D.在石灰乳中滴加少量的饱和 溶液:
【答案】A
【解析】A.在溴水中滴加 溶液,溶液褪色: ,A错误;B.在 和 的混合液中滴加稀硫酸: ,B正确;C.在 溶液
中滴加少量 溶液: ,C正确;D.在石灰乳中滴加少量的饱和 溶
液: ,D正确;故选A。
6.(2024·四川绵阳·模拟预测)下列离子方程式书写正确的是
A.KClO碱性溶液与 反应制备高铁酸钾:
B.用白醋浸泡过的淀粉—KI试纸检验加碘盐中的 :
C.向NaClO溶液中通入少量 气体:
D. 溶液与足量的NaOH溶液反应:
【答案】B
【解析】A.KClO碱性溶液与 反应制备高铁酸钾:
,A错误;B.用白醋浸泡过的淀粉—KI试纸检验加碘盐中的 :
,B正确;C.向NaClO溶液中通入少量 气体:
,C错误;D. 溶液与足量的NaOH溶液反应生成
Mg(OH) 、NaCO 和HO,其反应的离子方程式为:
2 2 3 2
,D错误;故选B。
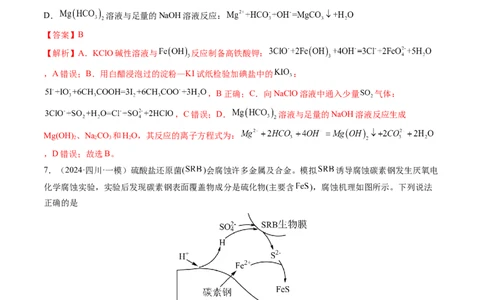
7.(2024·四川·一模)硫酸盐还原菌( )会腐蚀许多金属及合金。模拟 诱导腐蚀碳素钢发生厌氧电
化学腐蚀实验,实验后发现碳素钢表面覆盖物成分是硫化物(主要含 ),腐蚀机理如图所示。下列说法
正确的是
A.碳素钢厌氧腐蚀过程中 做还原剂
B.温度越高, 诱导碳素钢厌氧腐蚀速率越快
C.碳作负极,电极反应为:
D.该实验生成 的总反应:
【答案】D
【解析】A.氢原子将+6价的硫酸根离子还原为-2价的硫离子,SRB不做还原剂,A错误;B.温度超过
一定范围,硫酸盐还原菌(SRB)活性下降,速率减慢,B错误;C.碳作正极,电极反应为:H+ +e−=H,C错误;D.根据示意图可知,总反应的化学方程式为 ,D正确;故选
D。
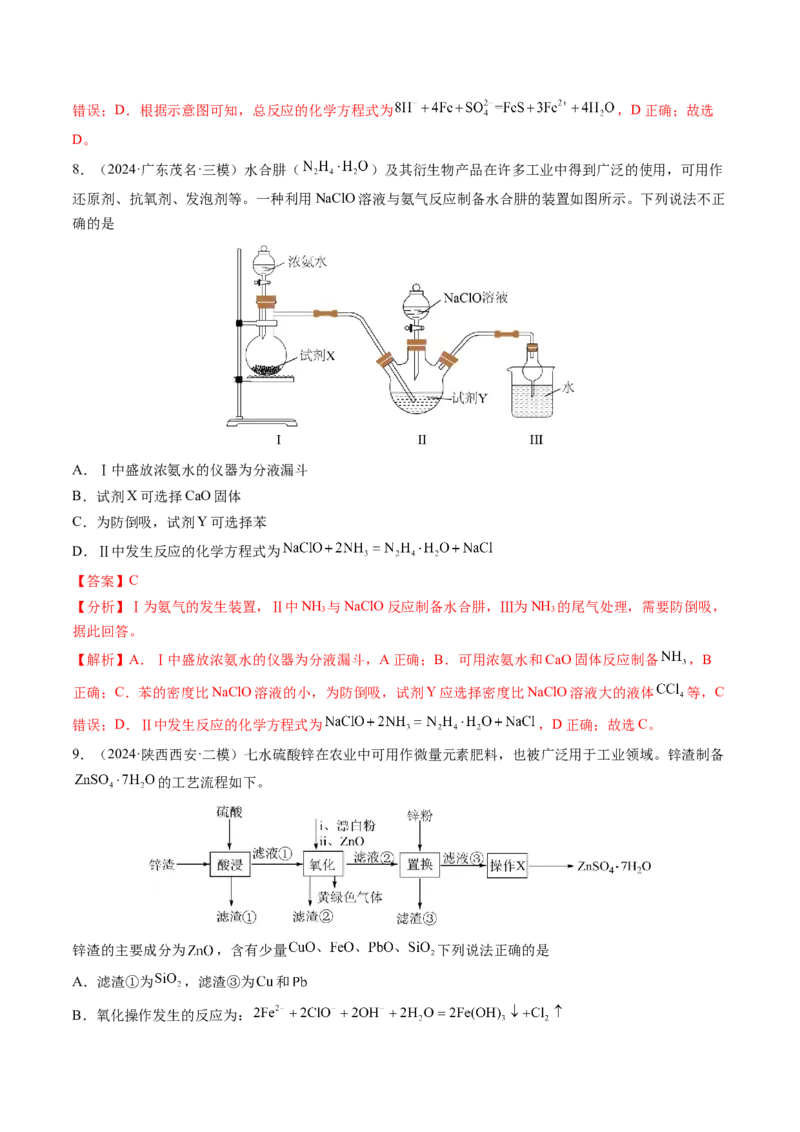
8.(2024·广东茂名·三模)水合肼( )及其衍生物产品在许多工业中得到广泛的使用,可用作
还原剂、抗氧剂、发泡剂等。一种利用NaClO溶液与氨气反应制备水合肼的装置如图所示。下列说法不正
确的是
A.Ⅰ中盛放浓氨水的仪器为分液漏斗
B.试剂X可选择CaO固体
C.为防倒吸,试剂Y可选择苯
D.Ⅱ中发生反应的化学方程式为
【答案】C
【分析】Ⅰ为氨气的发生装置,Ⅱ中NH 与NaClO反应制备水合肼,Ⅲ为NH 的尾气处理,需要防倒吸,
3 3
据此回答。
【解析】A.Ⅰ中盛放浓氨水的仪器为分液漏斗,A正确;B.可用浓氨水和CaO固体反应制备 ,B
正确;C.苯的密度比NaClO溶液的小,为防倒吸,试剂Y应选择密度比NaClO溶液大的液体 等,C
错误;D.Ⅱ中发生反应的化学方程式为 ,D正确;故选C。
9.(2024·陕西西安·二模)七水硫酸锌在农业中可用作微量元素肥料,也被广泛用于工业领域。锌渣制备
的工艺流程如下。
锌渣的主要成分为 ,含有少量 下列说法正确的是
A.滤渣①为 ,滤渣③为 和
B.氧化操作发生的反应为:C.加入 的主要作用是调节溶液的
D.操作X用到的玻璃仪器有蒸发皿、玻璃棒、漏斗
【答案】C
【分析】锌渣的主要成分为ZnO,含有少量CuO、FeO、PbO、SiO,加入硫酸酸浸,二氧化硅不反应,
2
PbO与硫酸反应生成硫酸铅沉淀,所以滤渣1中为SiO 和PbSO ,滤液①溶质主要为硫酸锌、硫酸铜、硫
2 4
酸亚铁,加入漂白粉将Fe2+氧化为Fe3+,次氯酸根离子转化为氯气,再加ZnO调节溶液pH值,使Fe3+沉
淀,滤渣②为Fe(OH) ,滤液②主要溶质为硫酸锌和硫酸铜,加入Zn置换硫酸铜生成Cu,滤渣③中为Cu
3
和过量的锌,滤液③主要为硫酸锌,通过蒸发浓缩、冷却结晶、过滤、洗涤、干燥得到ZnSO⋅7HO,据
4 2
此回答。
【解析】A.根据分析可知,滤渣①中为SiO 和PbSO ,滤渣③中为Cu和过量的锌,A错误;B.氧化操
2 4
作发生的反应为: ,B错误;C.根据分析可知,ZnO调节溶液pH
值,使Fe3+沉淀,C正确;D.操作X用到的玻璃仪器有玻璃棒、漏斗、烧杯,D错误;故选C。
题型二 氧化还原反应的计算方法——电子守恒法
10.(2024·吉林·模拟预测)元宵佳节松花江畔焰火璀璨,燃放烟花时发生:
,同时在火药中会加入 等物质。下列说法正确
的是
A.加入 能得到绿色的烟花
B.该反应中,氧化产物与还原产物的物质的量之比为3∶2
C.每生成 ,转移电子的物质的量为
D.燃放烟花对环境没有污染
【答案】B
【分析】 该反应中N元素化合价由+5价降为0价,S元素化合价由0
价降为-2价,C元素化合价由0价升为+4价,故S和为氧化剂,C为还原剂,CO 氧化产物,KS、N 为还
2 2 2
原产物,据此分析解题。
【解析】A.钙离子的焰色反应为蓝色,不能得到绿色的烟花,A错误;B.C为还原剂,CO 氧化产物,
2
KS、N 为还原产物,氧化产物与还原产物的物质的量之比为3∶2 ,B正确;C.反应中N元素化合价由+5
2 2
价降为0价,S元素化合价由0价降为-2价,每生成1molN ,转移电子的物质的量为12mol,C错误;D.
2
燃放烟花产生大量有毒烟尘颗粒物污染环境,D错误;故选B。
11.(2024·山东菏泽·二模)工业上以钛铁矿( ,其中Ti为+4价)为主要原料制备金属钛的工艺流
程如图所示。下列说法错误的是A.Ti位于元素周期表中第4周期ⅣB族
B.氯化时,被氧化的元素有碳和铁
C.制备Ti时,Ar气做保护气,可用氮气代替
D.氯化时,每生成0.1 mol ,转移电子0.7 mol
【答案】C
【解析】A.Ti位于元素周期表中第4周期ⅣB族,A正确;B.氯化发生的反应为:
,根据产物判断被氧化的元素有碳和铁,B正确;C.高温下
Ti与N 反应,由TiCl 制备Ti的过程中,Ar气不可换成氮气,C错误;D.根据反应方程式,每生成0.1
2 4
mol FeCl ,转移0.7 mol电子,D正确;故本题答案选C。
3
12.(2024·湖南长沙·二模)乙二醇的生产工艺中,需使用热的 溶液(脱碳液)脱除 ,脱碳液中含
有的 能减少溶液对管道的腐蚀。可使用“碘量法”测定脱碳液中 的含量,操作中涉及两个反应
如下:
① ;② 。
下列说法错误的是
A.反应①中氧化剂与还原剂物质的量之比为3∶2
B.反应①生成1mol 时,反应转移1mol电子
C.V的最高价为+5价,推测 有氧化性和还原性
D.溶液酸性过强时,反应②易发生其他反应
【答案】A
【解析】A.KI中I元素的化合价由-1价升高到0价,则KI作还原剂, 中V元素的化合价由+5价降
低到+4价,则 作氧化剂,故氧化剂与还原剂的物质的量之比为1∶2,A错误;B.生成2mol ,
转移2mol电子,则生成1mol 时转移1mol 电子,B正确;C. 中V显+5价,处于最高价,O
显-2价,处于最低价,即 既具有氧化性又具有还原性,C正确;D.在酸性过强时, 与 反应
生成S、 和 ,D正确;故选A。
13.(2024·福建漳州·三模)连二亚硫酸钠 俗称保险粉,是印染工业中常用的漂白剂。实验室制
备流程如下:
下列说法错误的是
A.将锌粉溶于水形成悬浊液可以提高反应速率B.生成 的反应中氧化剂和还原剂物质的量之比为
C.温度超过 会导致 溶解度降低
D.加入 有利于 析出,提高产率
【答案】B
【分析】锌粉水悬浊液与SO 在35-45°C环境下反应生成ZnS O 溶液,加入NaOH溶液除去Zn(OH) 后得
2 2 4 2
到NaSO 溶液,用NaCl固体析出NaSO·2H O,系列操作后得到无水NaSO
2 2 4 2 2 4 2 2 2 4。
【解析】A. 锌粉溶于水形成悬浊液可增大反应接触面积从而提高反应速率,A正确;B. 生成
的反应为 ,氧化剂和还原剂物质的量之比为 ,B错误;C. 温度过高会降低气体溶
解度,C正确;D. 根据同离子效应加入 可降低 溶解度,提高产率,D正确;故选
B。
14.(2024·广东·二模)高铁酸钾是一种新型的消毒剂,可以做到消毒、净水两用。高铁酸钾常用反应
3ClO-+2Fe3++10OH-=2 +3Cl-+5H O制备,下列说法不正确的是
2
A.生成1mol ,转移3mol电子
B.高铁酸钾可以消毒净水两用是因其有强氧化性且生成胶体
C.高铁酸钾消毒剂不能和洁厕灵混合
D.氧化产物与还原产物物质的量之比为2:5
【答案】D
【解析】A.上述反应铁化合价由+3变为+6,则生成1mol 离子,转移3 mol电子,A正确;B.高铁
酸根离子中铁元素处于高价态,具有强氧化性,可以消毒,溶于水能生成氢氧化铁胶体可以净水,B正
确;C.洁厕灵的主要成分是盐酸,高铁酸钾可以和其反应生成有毒的氯气,两者不能混用,C正确;D.
该反应中氧化产物是 ,还原产物是Cl-,根据方程式可知,两者物质的量之比为2∶3,D错误;故选
D。
15.(2024·四川德阳·二模) 是有毒的污染性气体,可将其与氧气的混合气体通入
的混合溶液中进行处理,其物质转化如图所示。下列说法正确的是
A.过程①中发生的反应是复分解反应B.过程②中每生成 转移 个电子
C.过程③中每转化 ,需
D.总反应为
【答案】A
【分析】过程①发生复分解反应由硫化氢生成氯化氢,由弱酸生成强酸;过程②中,Fe3+转化为Fe2+,发生
的离子方程式为:CuS+2Fe3+=Cu2++2Fe2++S;过程③中,Fe2+被氧化为Fe3+。
【解析】A.过程①中,生成CuS的反应为HS+Cu2+=CuS↓+2H+,发生复分解反应,A正确;B.过程②
2
中,三价铁离子具有氧化性,将-2价硫氧化为硫单质,发生的反应为CuS+2Fe3+=Cu2++2Fe2++S,每生成
32gS转移电子数为2N ,B错误;C.过程③中反应为4Fe2++O +4H+=4Fe3++ 2H O,每转化1molFe2+,需
A 2 2
0.25molO,没有指明标准状况,无法计算氧气的体积,C错误;D.从总反应看,Fe2+、Fe3+、Cu2+循环使
2
用,则回收S的总反应为2HS+O=2S↓+2H O, D错误;故答案为:A。
2 2 2
16.(2024·重庆·模拟预测)科学研究发现某些酶可以促进H+和e-的转移(如下图a、b和c过程),可将海
洋中的NO 转化为N,反应过如图所示。下列说法正确的是
2 2
A.过程I的离子方程式为: +2H+ NO+H O
2
B.消耗1molNO,b过程转移2mole-
C.高温有利于促进该过程中H+和e-的转移
D.过程I→III的总反应中氧化剂和还原剂的物质的量之比为1∶1
【答案】D
【解析】A.该离子方程式电荷不守恒,A错误;B.b过程反应为 , 消耗
1molNO, 转移3mole⁻,B错误,
C.高温下酶会失去活性,不利于H⁺和e⁻的转移,C错误;D.总反应式为: ,氧化
剂为 ,还原剂为 ,过程I→III的总反应中氧化剂和还原剂的物质的量之比为1∶1,D正确;故选
D。
17.(2024·新疆乌鲁木齐·二模)光催化CO 还原是一种有望在固碳和绿色能源领域应用的技术。水溶液
2中复合材料BM﹣MS(Bi MoO ﹣MoS )光催化CO 还原为醇类的机理图如图,h+是电子跃迁后留下的空
2 6 2 2
穴,具有强氧化性。下列说法不正确的是
A.HO在富集空穴的MoS 材料上发生氧化反应
2 2
B.光催化CO 还原在一定条件下也可以生成甲烷等有机物
2
C.在BiMoO 材料上,消耗标准状况下2.24 LCO 时,转移0.4 mol电子
2 6 2
D.光催化过程的总反应是2CO+3H O=C HOH+3O 和2CO+4H O=2CHOH+3O
2 2 2 5 2 2 2 3 2
【答案】C
【分析】在上述原电池反应中,H+、CO 得到电子被还原为C HOH、CHOH,HO失去电子被氧化变为
2 2 5 3 2
O、H+,因此通入CO 的电极为正极,加入HO的电极为负极,根据气体的物质的量,结合元素化合价变
2 2 2
化判断和计算反应过程中电子转移总数。
【解析】A.根据图示可知HO在富集空穴的MoS 材料上失去电子,发生氧化反应变为H+、O,A正
2 2 2
确;B.根据图示可知在BiMoO 电极上CO 得到电子,发生还原反应与H+反应产生CHOH、C HOH、
2 6 2 3 2 5
CH、HO等物质,B正确;C.标准状况下2.24 LCO 的物质的量是0.1 mol,CO 得到电子被还原为
4 2 2 2
CHOH、C HOH时,C元素化合价由反应前CO 中的+4价变为反应后CHOH、C HOH中的-2价,化合
3 2 5 2 3 2 5
价降低6价,每1molCO 反应转移6mol电子,因此0.1molCO 反应,转移0.6mol电子,C错误;D.根据
2 2
图示可知反应物为HO、CO,生成物为CHOH、C HOH及HO,则根据反应过程中电子转移数目相等,
2 2 3 2 5 2
可知光催化过程的总反应是2CO+3H O=C HOH+3O 和2CO+4H O=2CHOH+3O ,D正确;故选C。
2 2 2 5 2 2 2 3 2
18.(2024·湖南·模拟预测)钛(Ti)和钛合金被广泛应用于火箭、导弹、航天飞机等领域。工业上以钛铁矿
(FeTiO,其中Ti为+4价)为主要原料制备金属钛的工艺流程如下图所示:
3
已知:TiCl 的熔点―25℃,沸点136.4℃
4
下列说法错误的是
A.步骤①的反应过程元素的化合价没有发生变化
B.步骤③的操作名称是加热或高温煅烧
C.步骤④的反应方程式TiO+2C+2Cl TiCl +2CO
2 2 4
D.由TiCl 制备Ti的过程中,可以加入氮气做保护气体
4【答案】D
【分析】由题干流程图可知,以钛铁矿(FeTiO,其中Ti为+4价)为主要原料加入硫酸,生成硫酸氧钛
3
TiOSO ,反应方程式为:FeTiO+2H SO =FeSO+TiOSO+2H O,然后TiOSO 发生水解生成钛酸HTiO,
4 3 2 4 4 4 2 4 2 3
HTiO 加热或灼烧进行TiO,TiO 和C、Cl 混合加热发生反应TiO+2C+2Cl TiCl +2CO,最后用Mg
2 3 2 2 2 2 2 4
还原TiCl 得到Ti,据此分析解题。
4
【解析】A.由分析可知,步骤①的反应FeTiO+2H SO =FeSO+TiOSO+2H O,该过程种元素的化合价没
3 2 4 4 4 2
有发生变化,A正确;B.由分析可知,步骤③的操作名称是加热或高温煅烧,B正确;C.由分析可知,
步骤④的反应方程式为TiO+2C+2Cl TiCl +2CO,C正确;D.由于N 能与Mg发生反应生成
2 2 4 2
MgN,故由TiCl 制备Ti的过程中,可以加入氩气做保护气体,不能用N 作保护气,D错误;故答案
3 2 4 2
为:D。
19.(2024·北京海淀·三模)用高分子吸附树脂提取卤水中的碘(主要以 形式存在)的工艺流程如下:
下列说法正确的是
A.经①和④所得溶液中, 后者小于前者
B.④的作用是将吸附的碘还原而脱离高分子树脂
C.若②和⑤中分别得到等量 ,则消耗的
D.由⑥能得到碘产品是因为碘分子为极性分子,与溶液中的其他微粒间的作用力较弱
【答案】B
【分析】卤水中含碘离子,酸化后,通入氯气可氧化碘离子生成碘单质,高分子吸附树脂吸附碘单质,然
后碘与亚硫酸钠发生氧化还原反应生成NaI和硫酸钠,离子反应为I+SO +H O═2I-+SO +2H+,氧化时
2 2
氯酸钾可氧化NaI生成碘,升华可得到粗产品,以此来解答。
【解析】A.经①和④所得溶液中,碘离子的物质的量相同,为碘富集过程,浓度增大,c(I-)后者大于前
者,故A错误;B.④的作用是将吸附的碘还原而脱离高分子树脂,故B正确;C.若②和⑤中分别得到
等量I,由电子守恒可知n(Cl )×2×(1-0)=n(KClO )×[5-(-1)],则消耗的 ,故C错误;
2 2 3
D.由⑥能得到碘产品是因为碘分子为非极性分子,与溶液中的其他微粒间的作用力较弱,故D错误。答
案选B。
20.(2024·湖南长沙·三模)一种利用含钴废料(主要成分为 ,还含有少量 等杂
质)制备 的工艺流程如下。已知:①常温下,部分金属离子沉淀的 如下表:
金属离子
开始沉淀的 8.5 2.2 3.4 7.8
完全沉淀 (金属离子) 的的 10.0 3.0 4.5 9.4
② 的 的 。
下列说法不正确的是
A.由流程可知氧化性:
B.常温下加入的 溶液显碱性
C.气体 通入氨水至过量后所得溶液可循环利用
D.“高温焙烧”时的化学方程式:
【答案】A
【分析】钴废料(主要成分为 ,还含有少量 等杂质)中加硫酸、HO 酸浸,
2 2
还原为Co2+, 转化为对应硫酸盐,二氧化硅不溶解,滤渣为二氧化硅,滤液中加氨水调溶液的
pH,沉淀Al3+、Fe3+,过滤,滤液中加碳酸氢铵沉钴,得CoCO 沉淀,然后碳酸钴和碳酸锂高温焙烧生成
3
。
【解析】A.由流程可知,钴废料(主要成分为 ,还含有少量 等杂质)中加硫酸、
HO 酸浸, 被HO 还原为Co2+,所以氧化性: ,故A错误;B.电离常数:碳酸
2 2 2 2
的 ,所以水解常数 ,所以
溶液显碱性,故B正确;C.气体 为CO,通入氨水至过量后所得溶液为 溶液,
2
溶液可循环利用,故C正确;D.“高温焙烧”时,碳酸钴和碳酸锂反应生成 ,钴元素
化合价升高,则有氧气参与,反应的化学方程式: ,故D正
确;故答案为:A。
21.(2024·山东日照·三模)二氧化氯(ClO )是一种高效、安全的杀菌消毒剂。一种制备ClO 的工艺流
2 2
程及ClO 的分子结构(O-Cl-O的键角为117.6°)如图所示。
2下列说法错误的是
A.等物质的量ClO 的消毒效率为Cl 的2.5倍
2 2
B. ClO 分子中含有大π键( ),Cl原子杂化方式为sp2杂化
2
C.“ClO 发生器”中发生的反应为
2
D.“电解”时,阳极与阴极产物的物质的量之比为3∶1
【答案】D
【解析】A.已知ClO 作氧化剂时每摩ClO 需得到5mol电子,而Cl 作氧化剂时每摩Cl 只能得到2mol电
2 2 2 2
子,故等物质的量ClO 的消毒效率为Cl 的2.5倍,A正确;B.由题干ClO 的结构示意图可知,ClO 分子
2 2 2 2
中含有大π键( ),则Cl周围2个σ键和一对孤电子对即价层电子对数为3,Cl原子杂化方式为sp2杂
化,B正确;C.由题干流程图可知,“ClO 发生器”中即NaClO 和HCl反应生成ClO 、Cl 和NaCl,根
2 3 2 2
据氧化还原反应配平可得,发生的反应为 ,C正确;
D.由题干流程图可知,“电解”时,阳极发生氧化反应,电极反应为:Cl-+3H O-6e-= +6H+,阴极发
2
生还原反应,电极反应为:2HO+2e-=H ↑+2OH-,根据电子守恒可知,阳极与阴极产物的物质的量之比为
2 2
1∶3,D错误;故答案为:D。
22.(2024·辽宁·一模)以辉锑矿(主要成分为 ,含少量 、CuO、 等)为原料制备金属锑的
工艺流程如图所示。
已知:浸出液中除含过量盐酸和 之外,还含有 、 、 等。
下列说法错误的是
A.“还原”过程加适量Sb目的是更好地循环利用Sb元素
B.“除铜”时,不宜加过多的 ,是为了防止生成 或产生有毒物质
C.“除砷”时有 生成,该反应每生产2molAs,消耗
D.“电解”时,被氧化的Sb元素与被还原的Sb元素的质量之比为3:2
【答案】C【分析】辉锑矿加入盐酸和 ,得到浸出液中除含过量盐酸和 之外,还含有 、 、
;加入适量Sb,将五价Sb转化为三价Sb,加入NaS生成CuS沉淀除去铜,加入 ,
2
和加入的 反应生成As、 ,之后得到 溶液,电解生成Sb和 。
【解析】A.浸出液中含过量 ,加适量Sb两者反应生成 且不引入新杂质,目的是更好地循环利
用Sb元素,A正确;B.过多的 会和 反应生成 ,导致Sb元素流失; 具有还原性也
可能会和 反应生成有毒的As单质,故“除铜”时,不宜加过多的 ,B正确;C.由流程可知,
“除砷”时 和加入的 反应生成As,As元素化合价降低同时P元素化合价升高会生成
,该反应的化学方程式为: ,反应每生
产2molAs,消耗 ,C错误;D.“电解”时, 生成Sb和 ,根据电子守恒可知,
3Sb3+~6e-~3Sb5+、2Sb3+~6e-~2Sb,则被氧化的Sb元素与被还原的Sb元素的质量之比为3∶2,D正确;
故选C。
23.(2022·北京卷)某 的多孔材料刚好可将NO“固定”,实现了NO 与NO 分离并制备HNO,
2 4 2 2 4 3
如图所示:
已知:2NO (g) NO(g) ΔH<0
2 2 4
下列说法不正确的是
A.气体温度升高后,不利于NO 的固定
2 4
B.NO 被固定后,平衡正移,有利于NO 的去除
2 4 2
C.制备HNO 的原理为:2NO+O +2H O=4HNO
3 2 4 2 2 3
D.每制备0.4molHNO ,转移电子数约为
3
【答案】D
【解析】A.已知:2NO (g) NO(g) ΔH<0,升高温度,平衡逆向移动,NO 的浓度减小,不利于NO
2 2 4 2 4 2 4
的固定,故A正确;B.NO 被固定后,NO 浓度减小,平衡正移,有利于NO 的去除,故B正确;C.
2 4 2 4 2
被固定的四氧化二氮和氧气、水反应生成硝酸,制备HNO 的原理为:2NO+O +2H O=4HNO ,故C正
3 2 4 2 2 3
确;D.由C化学方程式可知,4HNO~4e-,每制备0.4molHNO ,转移电子数约为0.4× ,故D错
3 3
误。故选D。24.(2021·北京卷)用电石(主要成分为CaC ,含CaS和Ca P 等)制取乙炔时,常用CuSO 溶液除去乙
2 3 2 4
炔中的杂质。反应为:
①CuSO+H S=CuS↓+H SO
4 2 2 4
②11PH +24CuSO+12H O=3HPO +24H SO +8Cu P↓
3 4 2 3 4 2 4 3
下列分析不正确的是
A.CaS、Ca P 发生水解反应的化学方程式:CaS+2H O=Ca(OH) +H S↑、Ca P+6H O=3Ca(OH) +2PH↑
3 2 2 2 2 3 2 2 2 3
B.不能依据反应①比较硫酸与氢硫酸的酸性强弱
C.反应②中每24 mol CuSO 氧化11 mol PH
4 3
D.用酸性KMnO 溶液验证乙炔还原性时,HS、PH 有干扰
4 2 3
【答案】C
【解析】A.水解过程中元素的化合价不变,根据水解原理结合乙炔中常混有HS、PH 可知CaS的水解方
2 3
程式为CaS+2H O=Ca(OH) +H S↑;Ca P 水解方程式为Ca P+6H O=3Ca(OH) +2PH↑,A项正确;B.该反
2 2 2 3 2 3 2 2 2 3
应能发生是因为有不溶于水也不溶于酸的CuS生成,因此反应①不能说明HS的酸性强于HSO ,事实上
2 2 4
硫酸的酸性强于氢硫酸,B项正确;C.反应②中Cu元素化合价从+2价降低到+1价,得到1个电子,P元
素化合价从-3价升高到+5价,失去8个电子,则24molCuSO 完全反应时,可氧化PH 的物质的量是
4 3
24mol÷8=3mol,C项错误;D.HS、PH 均被KMnO 酸性溶液氧化,所以会干扰KMnO 酸性溶液对乙炔
2 3 4 4
性质的检验,D项正确;答案选C。
25.(2021·浙江卷)关于反应KHIO +9HI=2KI+4I +6H O,下列说法正确的是
2 3 6 2 2
A. KHIO 发生氧化反应 B.KI是还原产物
2 3 6
C.生成12.7g I 时,转移0.1mol电子 D.还原剂与氧化剂的物质的量之比为7:1
2
【答案】D
【解析】A.反应中I元素的化合价降低,发生得电子的反应,发生还原反应,A错误;B.KI中的I-由HI
变化而来,化合价没有发生变化,KI既不是氧化产物也不是还原产物,B错误;C.12.7g I 的物质的量为
2
0.05mol,根据反应方程式,每生成4mol I 转移7mol电子,则生成0.05mol I 时转移电子的物质的量为
2 2
0.0875mol,C错误;D.反应中HI为还原剂,KHIO 为氧化剂,在反应中每消耗1mol KHIO 就有7mol
2 3 6 2 3 6
HI失电子,则还原剂与氧化剂的物质的量的比为7:1,D正确;故答案选D。
26.(2021·浙江卷)关于反应8NH +6NO=7N +12H O,下列说法正确的是
3 2 2 2
A.NH 中H元素被氧化
3
B.NO 在反应过程中失去电子
2
C.还原剂与氧化剂的物质的量之比为3:4
D.氧化产物与还原产物的质量之比为4:3
【答案】D
【分析】由反应8NH +6NO==7N +12H O可知,其中NH 的N元素的化合价由-3升高到0、NO 中的N元
3 2 2 2 3 2
素的化合价由-+4降低到0,因此,NH 是还原剂, NO 是氧化剂。
3 2
【解析】A.NH 中H元素的化合价没有发生变化,故其未被氧化,被氧化的是N元素,A不正确;B.
3
NO 在反应过程中得到电子,B不正确;C.该反应中,NH 是还原剂,NO 是氧化剂。由化学方程式可
2 3 2
知,还原剂与氧化剂的物质的量之比为4:3,C说法不正确;D.该反应中氧化产物和还原产物均为N。
2还原剂被氧化后得到氧化产物,氧化剂被还原后得到还原产物,还原剂与氧化剂的物质的量之比为4:3,
因此,氧化产物与还原产物的质量之比为4:3 ,D说法正确。综上所述,本题选D。
27.(2020·浙江卷) 是硅酸盐水泥的重要成分之一,其相关性质的说法不正确的是
A.可发生反应:
B.具有吸水性,需要密封保存
C.能与 ,反应生成新盐
D.与足量盐酸作用,所得固体产物主要为
【答案】D
【分析】将Ca SiO 改写为氧化物形式后的化学式为:3CaO·SiO ,性质也可与NaSiO 相比较,据此解
3 5 2 2 3
答。
【解析】A.Ca SiO 与NH Cl反应的方程式为:Ca SiO+4NHCl CaSiO +2CaCl +4NH↑+2H O,A正
3 5 4 3 5 4 3 2 3 2
确;B.CaO能与水反应,所以需要密封保存,B正确;C.亚硫酸的酸性比硅酸强,当二氧化硫通入到
Ca SiO 溶液时,发生反应:3SO +H O+ Ca SiO=3 CaSO+H SiO,C正确;D.盐酸的酸性比硅酸强,当盐
3 5 2 2 3 5 3 2 3
酸与Ca SiO 反应时,发生反应:6HCl+ Ca SiO=3CaCl +H SiO+2H O,D不正确;故选D。
3 5 3 5 2 2 3 2
28.(2022·江苏卷)用尿素水解生成的 催化还原 ,是柴油机车辆尾气净化的主要方法。反应为
,下列说法正确的是
A.上述反应
B.上述反应平衡常数
C.上述反应中消耗 ,转移电子的数目为
D.实际应用中,加入尿素的量越多,柴油机车辆排放的尾气对空气污染程度越小
【答案】B
【解析】A.由方程式可知,该反应是一个气体分子数增大的反应,即熵增的反应,反应△S>0,故A错
误;B.由方程式可知,反应平衡常数 ,故B正确;C.由方程式可知,反应每
消耗4mol氨气,反应转移12mol电子,则反应中消耗1mol氨气转移电子的数目为3mol×4×
×6.02×1023=3×6.02×1023,故C错误;D.实际应用中,加入尿素的量越多,尿素水解生成的氨气过量,柴
油机车辆排放的氨气对空气污染程度增大,故D错误;故选B。
29.(2022·浙江卷)关于反应 ,下列说法正确的是
A. 发生还原反应
B. 既是氧化剂又是还原剂C.氧化产物与还原产物的物质的量之比为2∶1
D. 发生反应,转移 电子
【答案】B
【分析】NaSO+H SO =Na SO +S ↓+SO ↑ +H O,该反应的本质是硫代硫酸根离子在酸性条件下发生歧化
2 2 3 2 4 2 4 2 2
反应生成硫和二氧化硫,化合价发生变化的只有S元素一种,硫酸的作用是提供酸性环境。
【解析】A.HSO 转化为硫酸钠和水,其中所含元素的化合价均未发生变化,故其没有发生还原反应,A
2 4
说法不正确;B.NaSO 中的S的化合价为+2,其发生歧化反应生成S(0价)和SO (+4价),故其既是氧化
2 2 3 2
剂又是还原剂,B说法正确;C.该反应的氧化产物是SO ,还原产物为S,氧化产物与还原产物的物质的
2
量之比为1:1,C说法不正确;D.根据其中S元素的化合价变化情况可知,1mol Na SO 发生反应,要转
2 2 3
移2 mol电子,D说法不正确。
综上所述,本题选B。
30.(2020·浙江卷)反应 中,氧化产物与还原产物的物质的量
之比是
A.1:2 B.1:1 C.2:1 D.4:1
【答案】B
【解析】由反应方程式可知,反应物MnO 中的Mn元素的化合价为+4价,生成物MnCl 中Mn元素的化
2 2
合价为+2价,反应物HCl中Cl元素的化合价为-1价,生成物Cl 中Cl元素的化合价为0价,故MnCl 是还
2 2
原产物,Cl 是氧化产物,由氧化还原反应中得失电子守恒可知,n(Cl ):n(MnCl )=1:1,B符合题意;答
2 2 2
案选B。