文档内容
第 05 讲 氧化还原反应方程式的配平、书写及计算
目 录
01
考情透视·目标导航 2
02 知识导图·思维引航.........................................................................................................................2
03 考点突破·考法探究.........................................................................................................................3
考点一 氧化还原反应方程式的书写与配平.............................................................................3
知识点1 氧化还原反应方程式配平.......................................................................................3
知识点2 “信息型”氧化还原反应(离子)方程式的书写..................................................6
考向1 考查氧化还原方程式的配平.......................................................................................7
考向2 考查“信息型”氧化还原反应方程式的书写................................................................9
考点二 氧化还原反应的计算方法——电子守恒法..............................................................12
知识点1 计算原理.................................................................................................................12
知识点2 守恒法解题的思维流程.........................................................................................12
知识点3 电子守恒在氧化还原反应计算中的应用.............................................................12
考向1 考查多元素之间得失电子守恒问题.........................................................................13
考向2 考查多步反应得失电子守恒问题.............................................................................14
04 ........................................................................................................................................................15考点要求 考题统计 考情分析
氧化还原反应方程式的配平、书写及计算属于高频考
氧化还原反
点,从近几年高考试题来看,化工流程题或实验综合题
应方程式的
中有关氧化还原反应的化学(或离子)方程式的书写仍是
配平
2024浙江卷第4题,2分
高考命题的热点。
2023北京卷第12题,3分 预测新的一年高考可能会在化工流程或综合实验题中考
2023浙江1月卷第10题,2分 查氧化还原反应方程式的书写和氧化还原滴定计算,题
2022浙江6月卷第10题,2分 目的难度较大,如:
氧化还原反
2021浙江6月卷第8题,2分 (1)氧化还原反应与离子方程式、电极反应式相结
应的计算方
2021湖南卷第8题,3分 合,考查在新情境下陌生氧化还原方程式的书写与配平
法——电子
2020浙江6月卷第10题,2分 等;
守恒法
2020全国Ⅰ卷第26题,6分 (2)氧化还原反应的计算等;
(3)最近几年出现氧化还原反应的循环图中陌生氧化
还原方程式的书写与配平。
复习目标:
1.掌握常见氧化还原反应的书写、配平和相关计算。
2.能利用得失电子守恒原理进行相关计算。考点一 氧化还原反应方程式的书写与配平
知识点1 氧化还原反应方程式配平
1.氧化还原方程式配平的基本原则——配平三大原则
(1)电子守恒:氧化剂和还原剂得失电子总数相等,化合价升高总数=化合价降低总数;
(2)质量守恒:反应前后原子的种类和个数不变;
(3)电荷守恒:离子反应前后,阴、阳离子所带电荷总数相等。
2.“五步骤”配平氧化还原反应方程式
(1)标变价:标明反应前后变价元素的化合价;
(2)列得失:根据化合价的变化值,列出变价元素得失电子数;
(3)求总数:通过求最小公倍数使得失电子总数相等;
(4)配系数:确定氧化剂、还原剂、氧化产物、还原产物的化学计量数,观察法配平其他物质的化学计
量数;
(5)查守恒:检查质量、电荷、电子是否守恒。
3.记住元素的价态
(1)记住元素的常见价态
氢H
物质
金属氢化物、NaBH 、LiAlH H HO
4 4 2 2
价态
-1 0 +1
氧O
HO HO、NaO 等 O OF
2 2 2 2 2 2 2
-2 -1 0 +2
碳C
物质 CH C H C CO、HCN HC O CO、CO2-
4 2 2 2 2 4 2 3
价态 -4 -1 0 +2 +3 +4
硫S
物质 HS FeS S SO2- SO 、SO 2- SO 、SO 2-、SO
2 2 2 3 2 3 3 4 2
价态 -2 -1 0 +2 +4 +6
氮N物质 NH、LiNH、HCN、 NH N HNO NO HNO NO HNO
3 2 2 4 2 2 2 3
CO(NH )
2 2
价态 -3 -2 0 +1 +2 +3 +4 +5
氯Cl
物质 Cl- Cl HClO ClO HClO ClO HClO HClO
2 2 2 3 4
价态 -1 0 +1 +2 +3 +4 +5 +7
碘I
物质 I- I HIO HIO IO HIO HIO 、HIO
2 2 4 9 3 4 5 6
价态 -1 0 +1 +3 +3(1/4) 、 +5 +7
+5(3/4)
铜Cu
物质 Cu Cu O、Cu S Cu O、Cu2+
2 2 2
价态 0 +1 +2
铁Fe
物质 Fe FeO、Fe2+ Fe O Fe O、Fe3+、CuFeS KFeO
3 4 2 3 2 2 4
价态 0 +2 +2 ( 1/3 )、 +3 +3 +6
( 2/ 3 )
铬Cr
物质 Cr Cr3+ KCrO、KCr O
2 4 2 2 7
价态 0 +3 +6
锰Mn
物质 Mn Mn2+、 MnO(OH) MnO KMnO KMnO
2 2 4 4
MnO
价态 0 +2 +3 +4 +6 +7
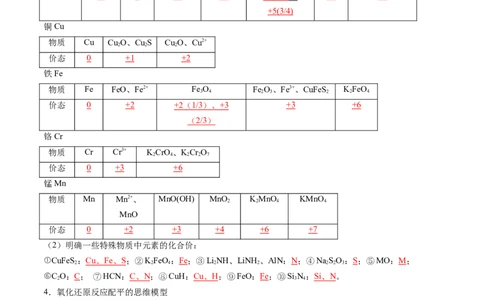
(2)明确一些特殊物质中元素的化合价:
①CuFeS: Cu 、 Fe 、 S ;②KFeO:Fe;③LiNH、LiNH、AlN:N;④NaSO:S;⑤MO:M;
2 2 4 2 2 2 2 3
⑥C O:C; ⑦HCN: C 、 N ;⑧CuH: Cu 、 H ;⑨FeO:Fe;⑩Si N: Si 、 N 。
2 3 4
4.氧化还原反应配平的思维模型
第一步:根据元素化合价的升降,判断氧化剂、还原剂、氧化产物、还原产物;
第二步:按“氧化剂+还原剂→还原产物+氧化产物”写出方程式,根据得失电子守恒配平上述物质;
第三步:根据电荷守恒和反应物的酸碱性,在方程式左边或右边补充 H + 、 OH -或HO 等;
2
第四步:根据质量守恒配平反应方程式;
第五步:检查原子、电荷、电子是否守恒。
5.配平方法
(1)正向配平法(2)逆向配平法
适用于一种元素的化合价既升高又降低的反应和分解反应中的氧化还原反应。
先确定生成物的化学计量数,然后再确定反应物的化学计量数。
由于S的化合价既升又降,而且升降总数要相等,所以KS的化学计量数为2,KSO 的化学计量数为1,
2 2 3
然后确定S的化学计量数为3。
(3)缺项型氧化还原反应方程式的配平
缺项方程式是指某些反应物或生成物的分子式没有写出来,一般为水、酸或碱。
1)配平方法
先用“化合价升降法”配平含有变价元素的物质的化学计量数,然后由原子守恒确定未知物,再根据原子
守恒进行配平。
2)补项原则
条件 补项原则
酸性条件下 缺 H( 氢 ) 或多 O( 氧 ) 补H+,少 O( 氧 ) 补HO(水)
2
缺H(氢)或多O(氧)补H O( 水 ) ,少O(氧)补OH
2
碱性条件下
-
知识点2 “信息型”氧化还原反应(离子)方程式的书写
1.“信息型”氧化还原反应化学(离子)方程式的书写程序
根据溶液的酸
根据电子转移数或常见化 根据 根据 根据原子
碱性确定参与
合价确定未知产物中元素 电子 电荷 守恒确定
→ → → →
的化合价;根据溶液的酸 守恒 反应的H或 守恒 并配平其
碱性确定未知物的类别 配平 OH 配平 他物质
2.熟记常见的氧化剂及对应的还原产物、还原剂及对应的氧化产物
KMnO (H+)、 KClO 、ClO
4 3
氧化剂 Cl O 浓HSO HNO Fe3+ HO
2 2 2 4 3 2 2
MnO -
2
还原产物 Cl- O2- SO 2 NO 、 Mn2+ Fe2+ Cl- H 2 ONO
2
SO 、
2
还原剂 I- S2-(H S) CO、C Fe2+ NH HO
2 3 2 2
SO
氧化产物 I S CO Fe3+ NO 、N SO 2- O
2 2 2 4 2
3.掌握书写信息型氧化还原反应化学(离子)方程式的步骤(4步法)
第1步:根据题干信息或流程图,判断氧化剂、还原剂、氧化产物、还原产物
第2步:按“氧化剂+还原剂-还原产物+氧化产物”写出方程式,根据氧化还原反应的守恒规律配平氧化
剂、还原剂、还原产物、氧化产物的相应化学计量数。
第3步:根据电荷守恒和溶液的酸碱性,通过在反应方程式的两端添加 H+或OH-的形式使方程式的两端
的电荷守恒。
第4步:根据原子守恒,通过在反应方程式两端添加HO(或其他小分子)使方程式两端的原子守恒。
2
4.氧化还原反应化学(离子)方程式的配平步骤:
① 标出化合价变化了的元素的化合价。
② 列变化:分别标出化合价升高数和化合价降低数
③ 根据化合价升降总数相等确定发生氧化还原反应的物质的化学计量数。
④ 利用元素守恒,观察配平其他物质
5. “补缺”的技巧
缺项化学(离子)方程式的配平:
配平化学(离子)方程式时,有时要用H+、OH-、HO来使化学方程式两边电荷及原子守恒,总的原则是
2
酸性溶液中不能出现OH-,碱性溶液中不能出现H+,具体方法如下:
酸性环境 碱性环境
反应物中少氧 左边加HO,右边加H+ 左边加OH-,右边加HO
2 2
反应物中多氧 左边加H+,右边加HO 左边加HO,右边加OH-
2 2
注:绝不可能出现的情况:H+→OH- 或者OH-→H+。
考向1 考查氧化还原方程式的配平
例1(1)重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeO·Cr2O3,还含有硅、
铝等杂质:
铬铁矿
熔块
该步骤的主要反应为 FeO·Cr O+Na CO+NaNO NaCrO+Fe O+CO ↑+NaNO 。上述反应配平后
2 3 2 3 3 2 4 2 3 2 2
FeO·Cr O 与NaNO 的化学计量数比为 。
2 3 3
(2)酸性条件下,MnO(OH)2将I-氧化为I2:MnO(OH) +I-+H+→Mn2++I +H O(未配平)。配平该反应的方程式,
2 2 2
其化学计量数依次为 。【答案】(1)2∶7 (2)1、2、4、1、1、3
【解析】(1)根据得失电子守恒和质量守恒,配平化学方程式可得:2FeO·CrO+4Na CO+7NaNO
2 3 2 3 3
4NaCrO+Fe O+4CO ↑+7NaNO ,故FeO·Cr O 与NaNO 的化学计量数比为2∶7。
2 4 2 3 2 2 2 3 3
(2)I元素化合价由-1价升高到0价,Mn元素化合价由+4价降低到+2价,根据元素化合价升降总数相等可
得MnO(OH) 和I-的化学计量数分别为1、2,再结合原子守恒和电荷守恒配平:MnO(OH) +2I-+4H+===Mn2+
2 2
+I +3H O。
2 2
【思维建模】(1)两种常用方法
①全变从左侧配:氧化剂、还原剂中某元素化合价全变化的,一般从左侧反应物开始配平;
②自变从右侧配:自身氧化还原反应(包括分解、歧化)一般从右侧配平。
(2)“三步法”配平缺项氧化还原反应方程式 ,缺项方程式是指某些反应物或生成物在方程式中没有写出
来,它们一般为水、酸(H+)或碱(OH-),其配平流程为:
【变式训练1】配平下列方程式
(1) ;
(2) ;
【解析】(1)反应中 ,Cl元素化合价由+5价降低到+4价,共降低1价, ,
C元素化合价由+3价升高到+4价,每消耗1个 ,共升高2价,化合价升降最小公倍数为 2,故
、 前系数为2, 前系数为1, 前系数为2,再根据原子守恒配平其它物质的系数,
配平后的方程式为 ;(2)反应中
,Mn元素化合价由+7价降低到+2价,共降低5价, ,C元素化合价由-2价升高
到+4价,每消耗1个 ,共升高12价,化合价升降最小公倍数为60,故 、 前系数为
12, 前系数为5, 前系数为10,再根据原子守恒配平其它物质的系数,配平后的方程式为
。
【答案】(1)
(2)
【变式训练2】配平下列方程式(1) ;
(2) ;
(3) ;
(4) ;
【解析】(1)反应中 ,Mn元素化合价由+4价降低到+2价,共降低2价, ,Cl
元素化合价由-1价升高到0价,每生成1个 ,共升高2价,化合价升降最小公倍数为2,故 、
前系数为1, 前系数为1,再根据原子守恒配平其它物质的系数,配平后的方程式为
;(2)反应中 ,N元素化合价由+5价降低
到+2价,共降低3价, ,Cu元素化合价由0价升高到+2价,共升高2价,化合价升降最
小公倍数为6,故 前系数为2, 、 前系数为3,再根据原子守恒配平其它物质的系数,配
平后的方程式为 ;(3)反应中 ,I元素化合价由
+5价降低到0价,共降低5价, ,I元素化合价由-1价升高到0价,共升高1价,化合价升降最小
公倍数为5,故 前系数为1, 前系数为5,根据I原子守恒, 前系数为3,再根据原子守恒配平其
它物质的系数,配平后的方程式为 ;(4)反应中
,Mn元素化合价由+7价降低到+2价,共降低5价, ,Cl元素化合价由-1价升高到0价,
每生成1个Cl,共升高2价,化合价升降最小公倍数为10,故 、 前系数为2, 前系数为
2
5, 前系数为10,根据电荷守恒,H+前系数为16,再根据原子守恒配平其它物质的系数,配平后的方
程式为 。
【答案】(1)
(2)
(3)
(4)
考向2 考查“信息型”氧化还原反应方程式的书写
例2根据图示信息书写方程式。
(1)NaN 是一种易溶于水(NaN =Na++ )的白色固体,可用于有机合成和汽车安全气囊的产气等。钠法
3 3
(液氨法)制备NaN 的工艺流程如下:
3①反应I的化学方程式为_______。
②销毁NaN 可用NaClO溶液,该销毁反应的离子方程式为_______( 被氧化为N)。
3 2
(2)利用钴渣[含Co(OH) 、Fe(OH) 等]制备钴氧化物的工艺流程如下:
3 3
Co(OH) 溶解还原反应的离子方程式为_______。
3
【分析】钠法(液氨法)制备NaN 的工艺流程为:金属Na与液氨反应生成NaNH 和H,加热硝酸铵发生反
3 2 2
应NH NO NO↑+2HO↑获得NO,NaNH 和NO加热到210 ~ 220℃发生反应
4 3 2 2 2 2 2
,生成NaN ,分离出NaOH得到NaN 。
3 3
【解析】(1)①反应I是NaNH 、NO在210-220℃发生氧化还原反应产生NaN 、NH 、NaOH,该反应
2 2 3 3
的化学方程式为 ;
②NaClO具有强氧化性,NaN 具有还原性,二者会发生氧化还原反应产生NaCl、NaOH、N,根据电子守
3 2
恒、电荷守恒、原子守恒,结合物质的拆分原则,可得该反应的离子方程式为:
;
(2)Co(OH) 具有氧化性, 具有还原性,二者在溶液中会发生氧化还原反应产生Co2+、 ,同时反
3
应产生HO,该反应的离子方程式为: 。
2
【答案】(1)
(2)
【思维建模】“信息型”氧化还原方程式的分析方法和思维模型【变式训练1】(2024秋·江苏·高三开学考试)根据信息书写方程式或描述反应过程。
(1)BMO(Bi MoO )是一种高效光催化剂,可用于光催化降解苯酚,弱酸性条件下降解苯酚的反应原理如
2 6
下图所示。
①虚线框内BMO降解苯酚的过程可描述为:_______。
②写出 与苯酚反应的离子方程式:_______。
(2)氯化银可以溶于氨水中,写出该反应的离子方程式:_______。
【答案】(1)①C HOH+7O 6CO+3H O ②3C HOH+28O-+28H+=18 CO↑+23H O
6 5 2 2 2 6 5 2 2 2
(2)AgCl+2NH= +Cl-
3
【解析】(1)①根据图知,虚线框内BMO降解苯酚的过程中:反应物是苯酚和氧气,生成物是二氧化碳
和水。所以该过程的总反应为:C HOH+7O 6CO+3H O;故答案为:C HOH+7O
6 5 2 2 2 6 5 2
6CO+3H O;
2 2
②由图可知,C HOH可被 氧化生成水和二氧化碳,反应的离子方程式是:3C HOH+28 +28H+=18
6 5 6 5
CO↑+23H O;故答案为:3C HOH+28 +28H+=18 CO↑+23H O;
2 2 6 5 2 2
(2)氯化银可以溶于氨水中生成银氨络离子,该反应的离子方程式为 :AgCl+2NH=
3
+Cl-;故答案为:AgCl+2NH= +Cl-。
3
【变式训练2】SCR(选择性催化还原)技术可有效降低柴油发动机在空气过量条件下的NO 排放,其工作原
x
理如图:
(1)尿素[CO(NH)]水溶液热分解为NH 和CO,该反应的化学方程式:________________________
2 2 3 2
________________________________________________。
(2)反应器中NH 还原NO 的化学方程式:____________________________________。
3 2(3)当燃油中含硫量较高时,尾气中SO 在O 作用下会形成(NH )SO ,使催化剂中毒。用化学方程式表
2 2 4 2 4
示(NH )SO 的形成:_______________________________________。
4 2 4
【答案】 (1)CO(NH)+HO====CO↑+2NH ↑
2 2 2 2 3
(2)8NH +6NO =====7N+12HO
3 2 2 2
(3)2SO +O+4NH +2HO===2(NH)SO
2 2 3 2 4 2 4
【解析】(1)反应物为HO和CO(NH) ,生成物为NH 和CO ,反应条件为加热,结合元素守恒可写出
2 2 2 3 2
该反应的化学方程式。(2)反应物为NH 和NO ,生成物为N 和HO,反应需在催化剂作用下进行。
3 2 2 2
(3)NH 、SO 、O 和HO反应生成(NH )SO 。
3 2 2 2 4 2 4
考点二 氧化还原反应的计算方法——电子守恒法
知识点1 计算原理
对于氧化还原反应的计算,要根据氧化还原反应的实质——反应中氧化剂得到的电子总数与还原剂失去的
电子总数相等,即得失电子守恒。利用守恒思想,可以抛开繁琐的反应过程,可不写化学方程式,不追究
中间反应过程,只要把物质分为始态和终态,从得电子与失电子两个方面进行整体思维,便可迅速获得正
确结果。
知识点2 守恒法解题的思维流程
1.“一找各物质”:找出氧化剂、还原剂及相应的还原产物和氧化产物。
2.“二定得失数”:确定一个原子或离子得失电子数(注意化学式中粒子的个数)。
3.“三列恒等式”:根据题中物质的物质的量和得失电子守恒列出等式。
n(氧化剂)×变价原子个数×化合价变化值(高价-低价)=n(还原剂)×变价原子个数×化合价变化值(高价-低
价)。
知识点3 电子守恒在氧化还原反应计算中的应用
得失电子守恒是指在发生氧化还原反应时,氧化剂得到的电子总数一定等于还原剂失去的电子总数。得失
电子守恒法常用于氧化还原反应中氧化剂、还原剂、氧化产物、还原产物的有关计算及电解过程中电极产
物的有关计算等。
(1)直接计算反应物与产物或反应物与反应物之间的数量关系。
(2)对于多步连续的氧化还原反应则可根据“电子传递”,找出起始反应物与最终生成物之间的关系进
行计算,忽略反应过程。
(3)以电子守恒为核心,建立起“等价代换”,找出有关物质之间的关系进行计算等。
(4)多池串联时,流经各个电极上的电子数相等。
考向1 考查多元素之间得失电子守恒问题例1(23-24高三上·海南海口·期末)某铁的“氧化物”样品,用5mol/L的盐酸140mL恰好完全溶解,所
得溶液还能吸收标准状况下0.56L氯气,使其中Fe2+全部转化为Fe3+。该样品可能的化学式是
A.Fe O B.Fe O C.Fe O D.Fe O
2 3 3 4 4 5 5 7
【答案】D
【解析】铁的“氧化物”样品,用5mol/L的盐酸140mL恰好完全溶解,HCl的物质的量为0.7mol,则生
成HO的物质的量为0.35mol,从而得出铁的“氧化物”中O原子的物质的量为0.35mol;标准状况下
2
0.56L氯气的物质的量为0.025mol,此时溶质全部为FeCl ,Cl-的物质的量为0.7mol+0.025mol×2=0.75mol,
3
由此得出铁的“氧化物”中Fe原子的物质的量为0.25mol,该样品中Fe、O的原子个数比为
0.25mol:0.35mol=5:7,则该样品可能的化学式是Fe O,故选D。
5 7
【思维建模】在利用得失电子守恒法解题时,一般分为三步:
①“一找各物质”:找出氧化剂、还原剂及相应的还原产物和氧化产物。
②“二定得失数”:确定一个原子或离子得失电子数(注意化学式中原子的个数)。
③“三列关系式”:根据题中物质的物质的量和电子守恒列出等式。
n(氧化剂)×变价原子个数×化合价变化值=n(还原剂)×变价原子个数×化合价变化值。
【变式训练1】(2024·广西南宁·二模)一种利用金属磷化物作为催化剂,将CHOH转化成甲酸钠的电化
3
学示意图如下,阴极生成 和一种气体。下列说法错误的是
A.b为电源正极
B.Na+由右侧室向左侧室移动
C.阴极的电极反应式为2CO+2H O+2e-=2HCO +H ↑
2 2 2
D.理论上,当电路中转移 时,阴极室质量增加134g
【答案】D
【分析】由CHOH制取HCOONa,C元素由-2价升高到+2价,则右侧电极为阳极,b电极为正极;左侧
3
电极为阴极,a为负极。
【解析】A.由分析可知,右侧为阳极,电极发生氧化反应,与电源正极相连,则b为电源正极,A正
确;B.阴极的电极反应式为2CO+2H O+2e-=2HCO +H ↑,阳极的电极反应式为
2 2 2
,根据电极反应式的离子消耗与生成情况可知, 由阳极向阴极移动,即由右侧室向左侧室移动,B正确;C.由B选项可知,阴极的电极反应式为2CO+2H O+2e-=2HCO
2 2
+H ↑,C正确;D.当电路中转移2mole-时,根据 ,吸收
2
n(CO)=n(e-)=2mol,生成n(H )=1mol,定向移动到阴极的n(Na+)=n(e-)=2mol,则阴极室增加的质量
2 2
m=m(CO)+m(Na+)-m(H )=2mol×44g/mol+2mol×23g/mol-1mol×2g/mol=132g,D错误;故选D。
2 2
【变式训练2】某试样含有 、 及㤢性物质。称取试样 ,溶解后配制到 容量瓶中。
吸取 ,在 介质中用 将 还原为 ,除去过量的 后调至中性测定 ,消
耗 溶液 。另吸取 试液用 酸化后加热除去 ,再调至中性,滴
定过剩 时消耗了上述 溶液 。计算试样中 、 的质量分数 、 。
【答案】16.7% 71.4%
【解析】设去除的25.00mL试液中的KBrO 、KBr的物质的量分别为nmol、nmol,
3 1 2
由 可知, ,故n+n=
1 2
=0.00175, ,n 5n = =0.00025,解得
2- 1
n=0.00025,n=0.0015,原样品中n(KBrO )=4n =0.001mol,n(KBr)=4n =0.006mol,故KBrO 的质量分数
1 2 3 1 2 3
为: ,KBr的质量分数为: 。
考向2 考查多步反应得失电子守恒问题
例1金属锡的纯度可以通过下述方法分析:将试样溶于盐酸,反应的化学方程式为Sn+2HCl===SnCl +
2
H↑,再加入过量的 FeCl 溶液,发生如下反应:SnCl +2FeCl ===SnCl +2FeCl ,最后用已知浓度的
2 3 2 3 4 2
KCr O 溶液滴定生成的Fe2+,反应的化学方程式为6FeCl +KCr O +14HCl===6FeCl +2KCl+2CrCl +
2 2 7 2 2 2 7 3 3
7HO。现有金属锡试样0.613 g,经上述反应后,共用去0.100 mol·L-1 KCr O 溶液16.0 mL。求试样中锡
2 2 2 7
的百分含量(假定杂质不参加反应,锡的相对原子质量为119)。
【答案】93.2%。
【解析】Sn与KCr O 物质的量的关系:
2 2 7
3Sn~3SnCl ~6FeCl ~KCr O
2 2 2 2 7
3×119 g 1 mol
x 0.100×0.016 mol
x==0.571 2 g
w(Sn)=×100%≈93.2%。
【方法指导】有些试题涉及的氧化还原反应较多,数量关系较为复杂,若用常规方法求解比较困难,若抓
住失电子总数等于得电子总数这一关系,则解题就变得很简单。解这类试题时,注意不要遗漏某个氧化还
原反应,要理清具体的反应过程,分析在整个反应过程中化合价发生变化的元素得电子数目和失电子数
目,即可迅速求解。
【变式训练1】将1.08 g FeO完全溶解在100 mL 1.00 mol·L-1硫酸中,然后加入25.00 mL K Cr O 溶 液,
2 2 7恰好使Fe2+全部转化为Fe3+,且Cr O中的铬全部转化为Cr3+。则KCr O 的物质的量浓度是________。
2 2 2 7
【答案】0.100 mol·L-1
【解析】由电子守恒知,FeO中+2价铁所失电子的物质的量与Cr O中+6价铬所得电子的物质的量相
2
等,×(3-2)=0.025 00 L×c(Cr O)×(6-3)×2,得c(Cr O)=0.100 mol·L-1。
2 2
【变式训练2】在氧气中燃烧0.22 g硫和铁组成的混合物,使其中的硫全部转化为二氧化硫,把这些二氧
化硫全部氧化成三氧化硫并转变为硫酸,这些硫酸可用10 mL 0.5 mol·L-1氢氧化钠溶液完全中和,则原混
合物中硫的百分含量为( )
A.72% B.40% C.36% D.18%
【答案】C
【解析】由S原子守恒和有关反应可得出:
S~HSO ~2NaOH
2 4
32 g 2 mol
m(S) 0.5×10×10-3 mol
得m(S)=0.08 g
原混合物中w(S)=×100%=36%。
1.(2024·浙江卷)汽车尾气中的 和 在催化剂作用下发生反应: ,下列
说法不正确的是( 为阿伏加德罗常数的值)
A.生成 转移电子的数目为 B.催化剂降低 与 反应的活化能
C. 是氧化剂, 是还原剂 D. 既是氧化产物又是还原产物
【答案】D
【分析】NO中N的化合价为+2价,降低为0价的N,1个NO得2个电子,作氧化剂,发生还原反应,
2
CO中C为+2价,化合价升高为+4价的CO,失去2个电子,作还原剂发生氧化反应;
2
【解析】A.根据分析,1molCO 转移2N 的电子,A正确;B.催化剂通过降低活化能,提高反应速率,
2 A
B正确;C.根据分析,NO是氧化剂,CO是还原剂,C正确;D.根据分析,N 为还原产物,CO 为氧化
2 2
产物,D错误;故答案为:D。
2.(2023·浙江卷)关于反应 ,下列说法正确的是
A.生成 ,转移 电子 B. 是还原产物
C. 既是氧化剂又是还原剂 D.若设计成原电池, 为负极产物
【答案】A
【解析】A.由方程式可知,反应生成1mol一氧化二氮,转移4mol电子,故A正确;B.由方程式可知,反应中氮元素的化合价升高被氧化,NH OH是反应的还原剂,故B错误;C.由方程式可知,反应中氮元
2
素的化合价升高被氧化,NH OH是反应的还原剂,铁元素的化合价降低被还原,铁离子是反应的氧化剂,
2
故C错误;D.由方程式可知,反应中铁元素的化合价降低被还原,铁离子是反应的氧化剂,若设计成原
电池,铁离子在正极得到电子发生还原反应生成亚铁离子,亚铁离子为正极产物,故D错误;故选A。
3.(2023·北京卷)离子化合物 和 与水的反应分别为① ;②
。下列说法正确的是
A. 中均有非极性共价键
B.①中水发生氧化反应,②中水发生还原反应
C. 中阴、阳离子个数比为 , 中阴、阳离子个数比为
D.当反应①和②中转移的电子数相同时,产生的 和 的物质的量相同
【答案】C
【解析】A.NaO 中有离子键和非极性键,CaH 中只有离子键而不含非极性键,A错误;B.①中水的化
2 2 2
合价不发生变化,不涉及氧化还原反应,②中水发生还原反应,B错误;C.NaO 由Na+和 组成.
2 2
阴、阳离子个数之比为1∶2,CaH 由Ca2+和H-组成,阴、阳离子个数之比为2∶1,C正确;D.①中每生成1
2
个氧气分子转移2个电子,②中每生成1个氢气分子转移1个电子,转移电子数相同时,生成氧气和氢气
的物质的量之比为1∶2,D错误;故选C。
4.(2022·海南卷)在2.8gFe中加入100mL3mol/LHCl,Fe完全溶解。N 代表阿伏加德罗常数的值,下列
A
说法正确的是
A.反应转移电子为0.1mol B.HCl溶液中 数为3N
A
C. 含有的中子数为1.3N D.反应生成标准状况下气体3.36L
A
【答案】A
【分析】2.8gFe的物质的量为0.05mol;100mL 3mol·L-1HCl中H+和Cl-的物质的量均为0.3mol,两者发生
反应后,Fe完全溶解,而盐酸过量。
【解析】A.Fe完全溶解生成Fe2+,该反应转移电子0.1mol,A正确;B.HCl溶液中Cl-的物质的量为
0.3mol,因此,Cl-数为0.3N ,B不正确;C.56Fe 的质子数为26、中子数为30,2.8g56Fe的物质的量为
A
0.05mol,因此,2.8g56Fe含有的中子数为1.5N ,C不正确;D.反应生成H 的物质的量为0.05mol,在标
A 2
准状况下的体积为1.12L ,D不正确;综上所述,本题A。
5.(2021·山东卷)X、Y均为短周期金属元素,同温同压下,0.1molX的单质与足量稀盐酸反应,生成H
2
体积为VL;0.1molY的单质与足量稀硫酸反应,生成H 体积为VL。下列说法错误的是
1 2 2
A.X、Y生成H 的物质的量之比一定为
2
B.X、Y消耗酸的物质的量之比一定为C.产物中X、Y化合价之比一定为
D.由 一定能确定产物中X、Y的化合价
【答案】D
【分析】设与1mol X反应消耗HCl的物质的量为amol,与1mol Y反应消耗HSO 的物质的量为bmol,根
2 4
据转移电子守恒以及H原子守恒可知 、 。
【解析】A.同温同压下,气体体积之比等于其物质的量之比,因此X、Y生成H 的物质的量之比一定为
2
,故A正确;B. X、Y反应过程中消耗酸的物质的量之比为 ,因 ,因此 ,故B
正确;C.产物中X、Y化合价之比为 ,由B项可知 ,故C正确;D.因短周期金属单质与盐酸
或稀硫酸反应时,生成的盐中金属元素化合价有+1、+2、+3三种情况,因此存在a=1,2,3,b=0.5,1的
多种情况,由 可知,当a=1,b=0.5时, =1,当a=2,b=1时, =1,两种情况下X、Y的化合
价不同,因此根据 可能无法确定X、Y的化合价,故D错误;综上所述,错误的D项,故答案为D。
6.(2021·湖南卷) 常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第一步反应为
。下列说法错误的是
A.产生22.4L(标准状况) 时,反应中转移
B.反应中氧化剂和还原剂的物质的量之比为11:6
C.可用石灰乳吸收反应产生的 制备漂白粉
D.可用酸化的淀粉碘化钾溶液检验食盐中 的存在
【答案】A
【解析】A.该反应中只有碘元素价态升高,由0价升高至KH(IO) 中+5价,每个碘原子升高5价,即6I
3 2 2
60e-,又因方程式中6I 3Cl,故3Cl 60e-,即Cl 20e-,所以产生22.4L (标准状况) Cl 即1mol Cl
2 2 2 2 2 2
时,反应中应转移20 mol e-,A错误;B.该反应中KClO 中氯元素价态降低,KClO 作氧化剂,I 中碘元
3 3 2
素价态升高,I 作还原剂,由该方程式的计量系数可知,11KClO 6I,故该反应的氧化剂和还原剂的物质
2 3 2
的量之比为11:6,B正确;C.漂白粉的有效成分是次氯酸钙,工业制漂白粉可用石灰乳与氯气反应,C正
确;D.食盐中 可先与酸化的淀粉碘化钾溶液中的H+、I-发生归中反应 生成
I,I 再与淀粉发生特征反应变为蓝色,故可用酸化的淀粉碘化钾溶液检验食盐中 的存在,D正确。故
2 2
选A。7.(2022·山东卷)实验室制备 过程为:①高温下在熔融强碱性介质中用 氧化 制备
;②水溶后冷却,调溶液 至弱碱性, 歧化生成 和 ;③减压过滤,将滤
液蒸发浓缩、冷却结晶,再减压过滤得 。下列说法正确的是
A.①中用瓷坩埚作反应器
B.①中用 作强碱性介质
C.②中 只体现氧化性
D. 转化为 的理论转化率约为66.7%
【答案】D
【分析】由题中信息可知,高温下在熔融强碱性介质中用KClO 氧化 MnO 制备KMnO ,然后水溶后冷
3 2 2 4
却调溶液pH至弱碱性使KMnO 歧化生成KMnO 和MnO ,Mn元素的化合价由+6变为+7和+4。
2 4 4 2
【解析】A.①中高温下在熔融强碱性介质中用KClO 氧化 MnO 制备KMnO ,由于瓷坩埚易被强碱腐
3 2 2 4
蚀,故不能用瓷坩埚作反应器,A说法不正确;B.制备KMnO 时为防止引入杂质离子,①中用KOH作
4
强碱性介质,不能用 ,B说法不正确;C.②中KMnO 歧化生成KMnO 和MnO ,故其既体现氧化
2 4 4 2
性又体现还原性,C说法不正确;D.根据化合价的变化分析,KMnO 歧化生成KMnO 和MnO 的物质的
2 4 4 2
量之比为2:1,根据Mn元素守恒可知,MnO 中的Mn元素只有 转化为KMnO ,因此,MnO 转化为
2 4 2
KMnO 的理论转化率约为66.7%,D说法正确;综上所述,本题选D。
4