文档内容
第 09 讲 无机非金属材料
【化学学科素养】
1.变化观念与平衡思想:根据碳、硅的结构,预测在一定条件下碳、硅及其化合物可能发生的化学变
化。
2.科学态度与社会责任:关注与碳、硅有关的热点问题(如光导纤维、硅电池、半导体材料),形成
可持续发展的意识;知道碳、硅及其化合物对社会发展的重大贡献。
【必备知识解读】
一、硅单质
1.存在
硅单质主要有晶体和无定形两大类。
2.物理性质
带有金属光泽的灰黑色固体,熔点高,硬度大,有脆性。
3.化学性质
常温下与F、HF、NaOH反应;加热时能与H 化合生成不稳定的氢化物SiH,加热时还能与Cl、O
2 2 4 2 2
化合分别生成SiCl 、SiO。涉及的化学方程式如下:
4 2
①与非金属单质反应
②与氢氟酸反应:Si+4HF===SiF ↑+2H↑。
4 2
③与NaOH溶液反应:
Si+2NaOH+HO===Na SiO+2H↑。
2 2 3 2
(4)制备方法
①制取粗硅:工业上,用焦炭在电炉中还原SiO 得到含有少量杂质的粗硅:SiO+2C=====Si+
2 2
2CO↑。
②粗硅提纯:Si+2Cl=====SiCl ,SiCl +2H=====Si+4HCl。
2 4 4 2
【特别提醒】①用焦炭还原SiO,产物是CO而不是CO。
2 2
②粗硅中含碳等杂质,与Cl 反应生成的SiCl 中含有CCl 等杂质,经过分馏提纯SiCl 后,再用H 还
2 4 4 4 2
原,得到高纯度硅。
(5)主要用途
①良好的半导体材料;②太阳能电池;③计算机芯片。
二、二氧化硅
1.存在自然界中,碳元素既有游离态,又有化合态,而硅元素仅有化合态,主要以氧化物和硅酸盐的形式存
在。天然SiO 有晶体和无定形两种,统称硅石。
2
2.结构
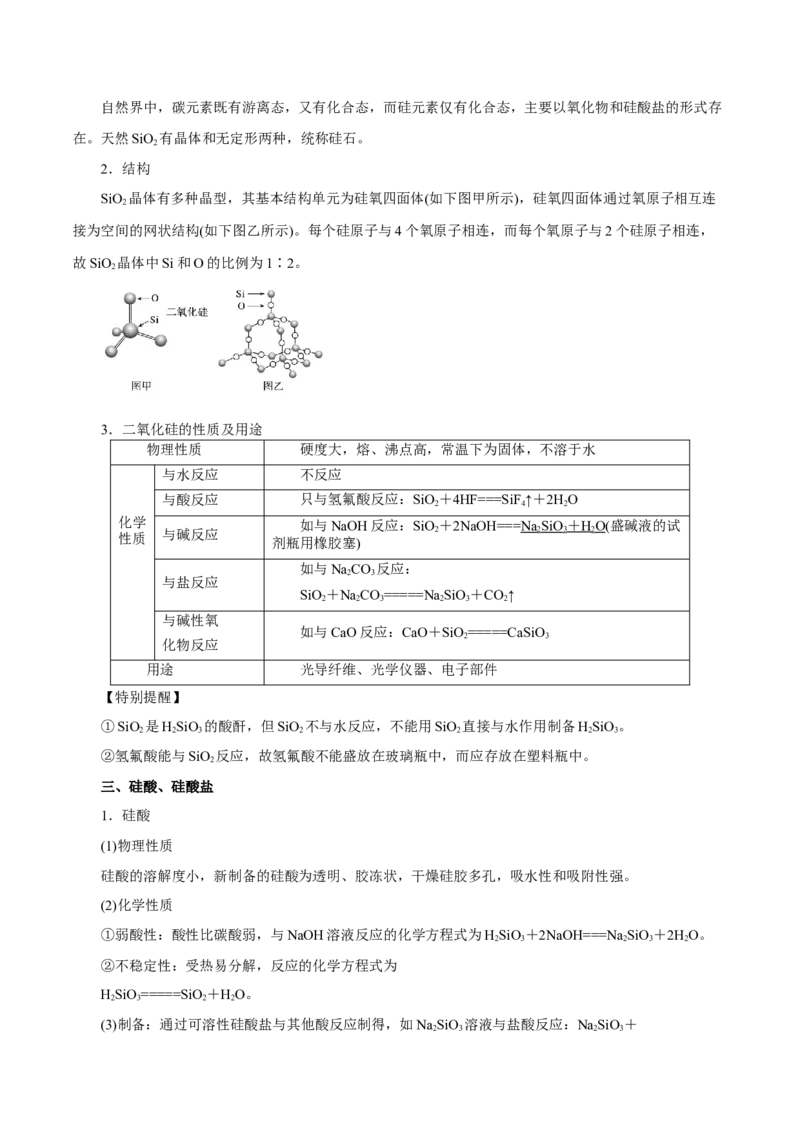
SiO 晶体有多种晶型,其基本结构单元为硅氧四面体(如下图甲所示),硅氧四面体通过氧原子相互连
2
接为空间的网状结构(如下图乙所示)。每个硅原子与4个氧原子相连,而每个氧原子与2个硅原子相连,
故SiO 晶体中Si和O的比例为1∶2。
2
3.二氧化硅的性质及用途
物理性质 硬度大,熔、沸点高,常温下为固体,不溶于水
与水反应 不反应
与酸反应 只与氢氟酸反应:SiO+4HF===SiF ↑+2HO
2 4 2
化学 如与NaOH反应:SiO+2NaOH===NaSiO + H O(盛碱液的试
性质 与碱反应 2 2 3 2
剂瓶用橡胶塞)
如与NaCO 反应:
2 3
与盐反应
SiO+NaCO=====NaSiO+CO↑
2 2 3 2 3 2
与碱性氧
如与CaO反应:CaO+SiO=====CaSiO
2 3
化物反应
用途 光导纤维、光学仪器、电子部件
【特别提醒】
①SiO 是HSiO 的酸酐,但SiO 不与水反应,不能用SiO 直接与水作用制备HSiO。
2 2 3 2 2 2 3
②氢氟酸能与SiO 反应,故氢氟酸不能盛放在玻璃瓶中,而应存放在塑料瓶中。
2
三、硅酸、硅酸盐
1.硅酸
(1)物理性质
硅酸的溶解度小,新制备的硅酸为透明、胶冻状,干燥硅胶多孔,吸水性和吸附性强。
(2)化学性质
①弱酸性:酸性比碳酸弱,与NaOH溶液反应的化学方程式为HSiO+2NaOH===NaSiO+2HO。
2 3 2 3 2
②不稳定性:受热易分解,反应的化学方程式为
HSiO=====SiO+HO。
2 3 2 2
(3)制备:通过可溶性硅酸盐与其他酸反应制得,如NaSiO 溶液与盐酸反应:NaSiO+
2 3 2 32HCl===2NaCl+HSiO(胶体)。
2 3
(4)用途:硅胶可用作干燥剂、催化剂的载体等。
2.硅酸盐
①白色、可溶于水的粉末状固体,其水溶液俗称水玻璃,有黏性,水溶液显碱性。
②与酸性较硅酸强的酸反应:
a.与盐酸反应的化学方程式:
NaSiO+2HCl===2NaCl+HSiO↓。
2 3 2 3
b.与CO 水溶液反应的化学方程式:
2
NaSiO+HO+CO===Na CO+HSiO↓。
2 3 2 2 2 3 2 3
③用途:黏合剂(矿物胶),耐火阻燃材料。
(3)硅酸盐组成的表示
通常用二氧化硅和金属氧化物的组合形式表示硅酸盐的组成。如硅酸钠(Na SiO)可表示为
2 3
NaO·SiO ,石棉(CaMg Si O )可表示为CaO·3MgO·4SiO 。
2 2 3 4 12 2
推背图①NaSiO 的水溶液是一种黏合剂,是制备硅胶和木材防火剂等的原料;NaSiO 易与空气中的
2 3 2 3
CO、HO反应,要密封保存。
2 2
②可溶性碳酸盐、硅酸盐的水溶液呈碱性,保存该溶液的试剂瓶不能用玻璃塞,应用橡胶塞。
四、无机非金属材料
1.传统无机非金属材料,如水泥、玻璃、陶瓷等硅酸盐材料。
(1)常见硅酸盐材料比较
水泥 玻璃 陶瓷
生产原料 石灰石、黏土 纯碱、石灰石、石英 黏土
主要设备 水泥回转窑 玻璃窑 陶瓷窑
(2)玻璃生产中的两个重要反应:NaCO+SiO=====NaSiO+CO↑;CaCO +SiO=====CaSiO +
2 3 2 2 3 2 3 2 3
CO↑。
2
2.新型陶瓷
高温结构陶瓷(碳化硅、氮化硅);压电陶瓷(钛酸盐和锆酸盐);透明陶瓷(氧化铝、氧化钇、氮化铝、
氟化钙);超导陶瓷等。材料类型 主要特性 示例 用途
火箭发动机的尾管及燃
高温结构陶 碳化硅、氮化硅与某些金
耐高温、抗氧化、耐磨蚀 烧室、汽车发动机、高
瓷 属氧化物等烧结而成
温电极材料等
实现机械能与电能的相互 滤波器、扬声器、声纳
压电陶瓷 钛酸盐、锆酸盐
转化 探伤器、点火器等
优异的光学性能,耐高 氧化铝、氧化钇、氮化 高压钠灯、激光器、高
透明陶瓷
温,绝缘性好 铝、氟化钙 温探测窗等
在某一临界温度下电阻为 可用于电力、交通、医
超导陶瓷
零 疗等领域
(1)新型陶瓷在组成上不再限于传统的硅酸盐体系,在光学、热学、电学、磁学等方面具有很多新的
特性和功能。
(2)碳化硅(SiC)俗称金刚砂,碳原子和硅原子通过共价键连接,具有类似金刚石的结构,硬度很大,
可用作砂纸和砂轮的磨料。碳化硅还耐高温,可用作耐高温结构材料、耐高温半导体材料等。
3.碳纳米材料
碳纳米材料是一类新型的无机非金属材料
(1)类型:富勒烯、碳纳米管、石墨烯等。
(2)用途:在能源、信息、医药等领域有广阔的应用前景。
结构特点 应用
由碳原子构成的一系列笼形分子的总 代表物C 开启碳纳米材料研究和应
60
富勒烯
称 用的新时代
由石墨片层卷成的管状物,具有纳米
碳纳米管 用于生产复合材料、电池和传感器等
尺度的直径
应用于光电器件、超级电容器、电池
石墨烯 只有一个碳原子直径厚度的单层石墨
和复合材料等
【关键能力拓展】
一、碳、硅及其化合物“反常”性质
(1)一般情况下,非金属元素单质熔、沸点低,硬度小,但晶体硅、金刚石熔、沸点高,硬度大,其中
金刚石为自然界中硬度最大的物质。
(2)一般情况下,非金属单质为绝缘体,但硅为半导体,石墨为电的良导体。
(3)Si的还原性强于C,但C在高温下能还原出Si:SiO+2C=====Si+2CO↑。
2
(4)非金属单质与碱反应一般既作氧化剂又作还原剂,且无氢气放出,但硅与强碱溶液反应只作还原
剂,且放出氢气:Si+2NaOH+HO===Na SiO+2H↑。
2 2 3 2(5)非金属单质一般不与非氧化性酸反应,但硅能跟氢氟酸反应:Si+4HF===SiF ↑+2H↑。
4 2
(6)一般情况下,碱性氧化物+酸―→盐+水,二氧化硅是酸性氧化物,却能与氢氟酸反应:SiO+
2
4HF===SiF ↑+2HO(SiF 不属于盐,故SiO 不是两性氧化物)。
4 2 4 2
(7)一般情况下,无机酸能溶于水,但硅酸却难溶于水。
(8)一般情况下,较强酸+较弱酸的盐―→较弱酸+较强酸的盐(溶液中的反应)。
因碳酸的酸性强于硅酸,所以水玻璃在空气中易变质:NaSiO+HO+CO===Na CO+HSiO(胶
2 3 2 2 2 3 2 3
体)。
但在高温下,可发生反应NaCO+SiO=====NaSiO+CO↑(CO 离开反应体系促进反应的正向进
2 3 2 2 3 2 2
行)。
(9)一般情况下,金属(Na、K)能置换出水中的氢,但C在高温下也能置换出HO中的氢:C+
2
HO(g)=====H+CO。
2 2
(10)一般情况下,酸性氧化物与水反应生成相应的含氧酸,但二氧化硅不溶于水,也不与水反应。
【核心题型例解】
高频考点一 硅和二氧化硅
例1.(2023·辽宁卷第3题)下列有关物质的工业制备反应错误的是( )
A. 合成氨:N+3H 2NH B. 制HCl:H+Cl=======2HCl
2 2 3 2 2
C. 制粗硅:SiO+2C=======Si+2CO D. 冶炼镁:2MgO(熔融)=======2Mg+O↑
2 2
【变式探究】(2023·湖北卷第3题)工业制备高纯硅的主要过程如下:
石英砂 粗硅 高纯硅
下列说法错误的是( )
A. 制备粗硅的反应方程式为
B. 1molSi含Si-Si键的数目约为
C. 原料气HCl和 应充分去除水和氧气
D. 生成 的反应为熵减过程
【变式探究】(2022·浙江卷)下列说法不正确的是( )
A.晶体硅的导电性介于导体和绝缘体之间,常用于制造光导纤维
B.高压钠灯发出的黄光透雾能力强、射程远,可用于道路照明C.氧化铝熔点高,常用于制造耐高温材料
D.用石灰右-石膏法对燃煤烟气进行脱硫,同时可得到石膏
高频考点二 二氧化硅
例2.(2023·广东卷第3题)建设美丽乡村,守护中华家园,衣食住行皆化学。下列说法正确的是(
)
A. 千家万户通光纤,光纤的主要材质为
B. 乡村公路铺沥青,沥青属于天然无机材料
C. 美容扮靓迎佳节,化妆品中的甘油难溶于水
D. 均衡膳食助健康,主食中的淀粉可水解为葡萄糖
【变式探究】(2022·广东卷)陈述Ⅰ和Ⅱ均正确但不具有因果关系的是
选项 陈述Ⅰ 陈述Ⅱ
A 用焦炭和石英砂制取粗硅 SiO 可制作光导纤维
2
B 利用海水制取溴和镁单质 可被氧化,Mg2+可被还原
C 石油裂解气能使溴CCl 的溶液褪色 石油裂解可得到乙烯等不饱和烃
4
D FeCl 水解可生成Fe(OH) 胶体 FeCl 可用作净水剂
3 3 3
高频考点二 硅酸盐及其应用
例3.(2023·广东卷第1题)“高山流水觅知音”。下列中国古乐器中,主要由硅酸盐材料制成的是(
)
B.裴李岗文化骨
A.九霄环佩木古琴 C.商朝后期陶埙 D.曾侯乙青铜编钟
笛
【变式探究】(2023·山东卷第1题)下列之物具有典型的齐鲁文化特色,据其主要化学成分不能与其
他三种归为一类的是( )A. 泰山墨玉 B. 龙山黑陶 C. 齐国刀币 D. 淄博琉璃
【变式探究】中国历史的发展和化学的发展紧密结合,中国的传世国宝,无不体现了劳动人民对化学
的认识和应用。下列四种国宝级文物的主要成分(载体)是硅酸盐的是( )
A.被称为“臻于极致 C.成为中国文化遗
B.被誉为“白瓷之王”的 D.被尊为“墨皇”的牙
的青铜典范”的四羊方 产标志的太阳神鸟金
定窑孩儿枕 色麻纸本墨迹《平复帖》
尊 饰
高频考点三 无机非金属材料
例3.随着科学技术的发展,无机非金属材料突破了传统的硅酸盐体系。下列物质中属于新型无机非金
属材料的是( )
A.水泥 B.普通玻璃 C.石墨烯 D.陶瓷
【变式探究】下列我国科研成果所涉及材料中,主要成分为同主族元素形成的无机非金属材料的是(
)
A.4.03米大口径碳 B.2022年冬 C.能屏蔽电磁波的 D.“玉兔二
化硅反射镜 奥会聚氨酯速滑服 碳包覆银纳米线 号”钛合金筛网轮
【变式探究】 北京故宫藏有大量珍贵文物,据统计总共达1862690件之多,统称文物100万件,占全
国文物总数的六分之一。下列故宫文物的主要部件属于陶瓷的是( )
A.带牙座的水晶球 B.御窑盘碟 C.金大吉葫芦 D.青玉交龙钮玉玺
高频考点四 与Si有关的无机化工流程题例4.(2023·湖北卷第16题) 是生产多晶硅的副产物。利用 对废弃的锂电池正极材料
进行氯化处理以回收Li、Co等金属,工艺路线如下:
回答下列问题:
(1)Co位于元素周期表第_______周期,第_______族。
(2)烧渣是LiCl、 和 的混合物,“500℃焙烧”后剩余的 应先除去,否则水浸时会
产生大量烟雾,用化学方程式表示其原因_______。
(3)鉴别洗净的“滤饼3”和固体 常用方法的名称是_______。
(4)已知 ,若“沉钴过滤”的pH控制为10.0,则溶液中 浓度为
_______ 。“850℃煅烧”时的化学方程式为_______。
(5)导致 比 易水解的因素有_______(填标号)。
a.Si-Cl键极性更大 b.Si的原子半径更大
c.Si-Cl键键能更大 d.Si有更多的价层轨道
【变式探究】 法生产多晶硅的流程如下。下列说法错误的是( )
A.合成1反应中 作氧化剂B.合成2的反应为:
C.上述流程说明 可溶于
D.净化、热解中生成的多晶硅为还原产物
【变式探究】以含镍废料(主要成分为NiO,含少量FeO、Fe O、CoO、BaO和SiO)为原料制备碳酸
2 3 2
钴(CoCO)和Ni O 的工艺流程如图。下列说法正确的是 ( )
3 x y
A.“滤渣I”成分是SiO
2
B.“氧化”时为证明添加NaClO 已足量,可用KSCN溶液进行检验
3
C.“沉钴”反应的离子方程式为2 +Co2+=CoCO ↓+CO ↑+H O
3 2 2
D.NiSO 溶液通过蒸发结晶获得NiSO ·6H O晶体
4 4 2
高频考点五、与Si有关的化学实验题
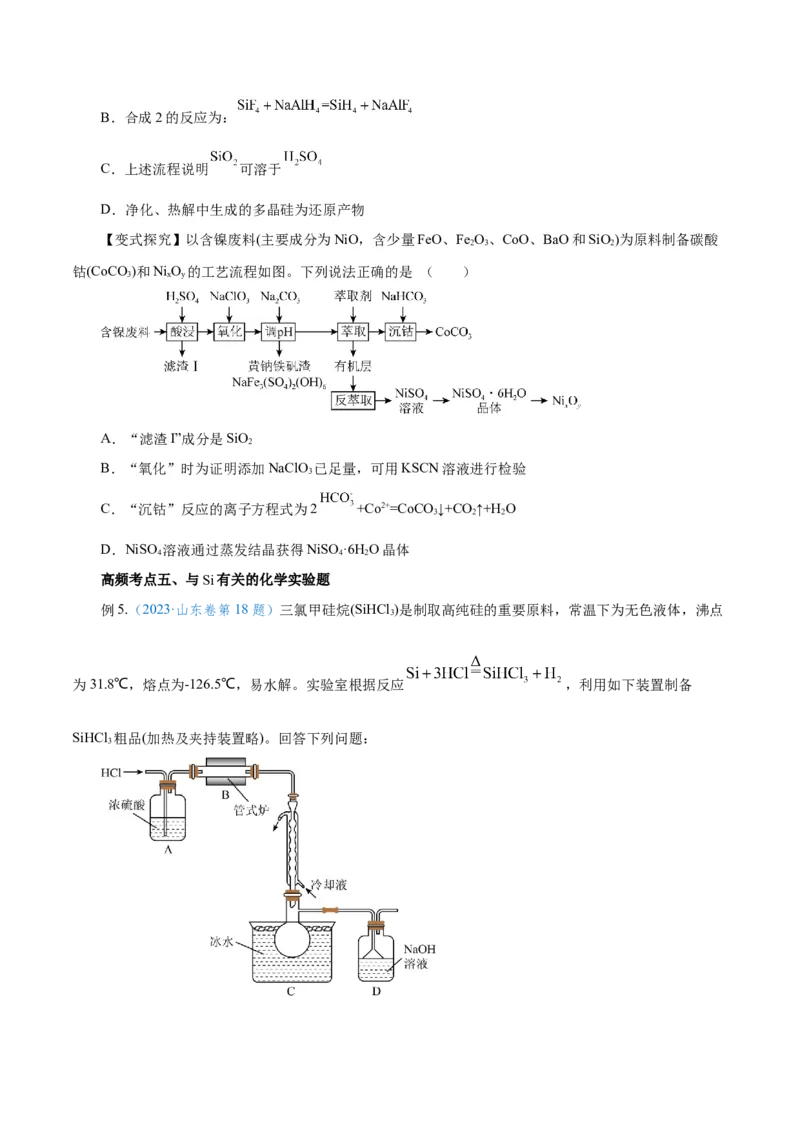
例5.(2023·山东卷第18题)三氯甲硅烷(SiHCl )是制取高纯硅的重要原料,常温下为无色液体,沸点
3
为31.8℃,熔点为-126.5℃,易水解。实验室根据反应 ,利用如下装置制备
SiHCl 粗品(加热及夹持装置略)。回答下列问题:
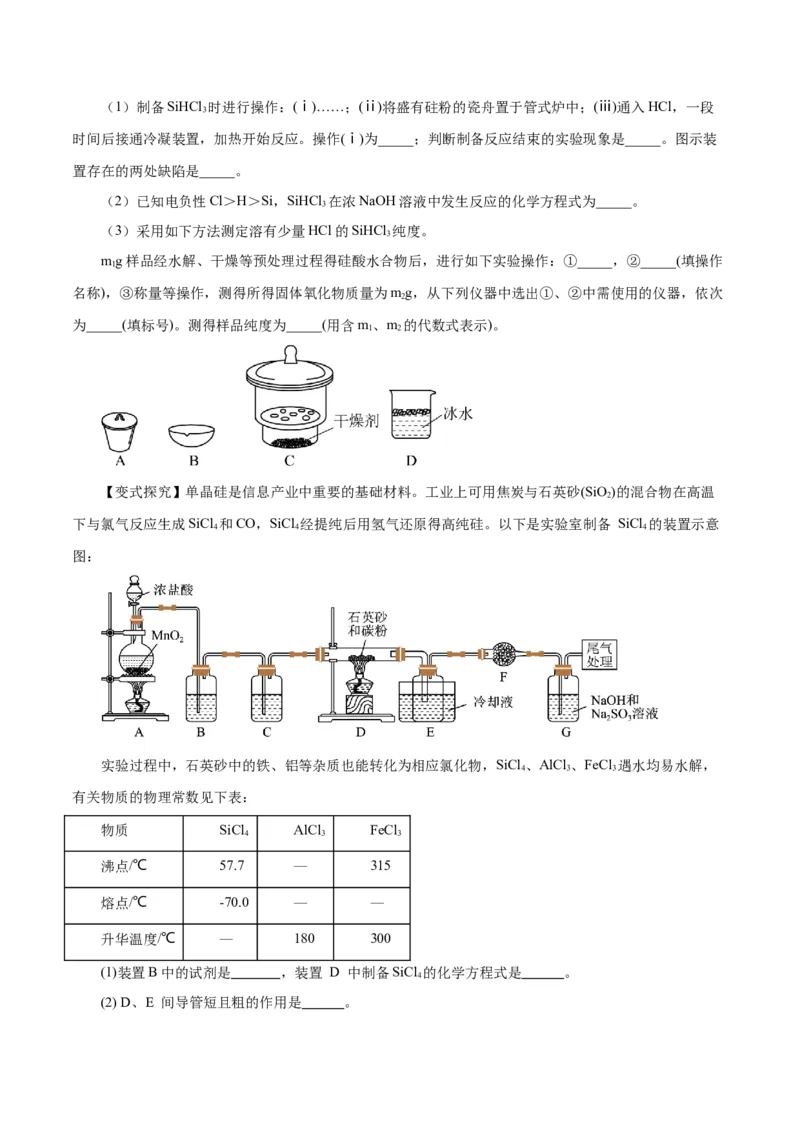
3(1)制备SiHCl 时进行操作:(ⅰ)……;(ⅱ)将盛有砫粉的瓷舟置于管式炉中;(ⅲ)通入HCl,一段
3
时间后接通冷凝装置,加热开始反应。操作(ⅰ)为_____;判断制备反应结束的实验现象是_____。图示装
置存在的两处缺陷是_____。
(2)已知电负性Cl>H>Si,SiHCl 在浓NaOH溶液中发生反应的化学方程式为_____。
3
(3)采用如下方法测定溶有少量HCl的SiHCl 纯度。
3
mg样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①_____,②_____(填操作
1
名称),③称量等操作,测得所得固体氧化物质量为mg,从下列仪器中选出①、②中需使用的仪器,依次
2
为_____(填标号)。测得样品纯度为_____(用含m、m 的代数式表示)。
1 2
【变式探究】单晶硅是信息产业中重要的基础材料。工业上可用焦炭与石英砂(SiO)的混合物在高温
2
下与氯气反应生成SiCl 和CO,SiCl 经提纯后用氢气还原得高纯硅。以下是实验室制备 SiCl 的装置示意
4 4 4
图:
实验过程中,石英砂中的铁、铝等杂质也能转化为相应氯化物,SiCl 、AlCl 、FeCl 遇水均易水解,
4 3 3
有关物质的物理常数见下表:
物质 SiCl AlCl FeCl
4 3 3
沸点/℃ 57.7 — 315
熔点/℃ -70.0 — —
升华温度/℃ — 180 300
(1)装置B中的试剂是 ,装置 D 中制备SiCl 的化学方程式是 。
4
(2) D、E 间导管短且粗的作用是 。(3)G中吸收尾气一段时间后,吸收液中肯定存在OH-、Cl-和SO 2-,请设计实验,探究该吸收液中可能
4
存在的其他酸根离子(忽略空气中CO 的影响)。
2
【提出假设】假设1:只有SO 2-;假设2:既无SO 2-也无ClO-;假设3: 。
3 3
【设计方案进行实验】可供选择的实验试剂有:3 mol/L H SO 、1 mol/L NaOH、0.01 mol/LKMnO 、
2 4 4
溴水、淀粉-KI、品红等溶液。
取少量吸收液于试管中,滴加 3 mol/L H SO 至溶液呈酸性,然后将所得溶液分置于a、b、c三支试
2 4
管中,分别进行下列实验。请完成下表:
序
操作 可能出现的现象 结论
号
若溶液褪色 则假设1成立
① 向a试管中滴加几滴 溶液
若溶液不褪色 则假设2或3成立
若溶液褪色 则假设1或3成立
② 向b试管中滴加几滴 溶液
若溶液不褪色 假设2成立
③ 向c试管中滴加几滴 溶液 假设3成立