文档内容
第 63 讲 卤代烃 醇 酚
[复习目标] 1.了解卤代烃的组成、结构特点,掌握卤代烃的性质,能利用卤代烃的形成和
转化进行有机合成。2.能从结构的角度辨识醇和酚,了解重要醇、酚的性质和用途。3.能从
官能团、化学键的特点及基团之间的相互影响分析醇和酚的反应规律,并能正确书写有关反
应的化学方程式。
考点一 卤代烃
1.卤代烃的概念
(1)卤代烃是烃分子里的氢原子被__________取代后生成的化合物。通式可表示为R—X(其
中R—表示烃基)。
(2)官能团是________。
2.卤代烃的物理性质
(1)沸点:比同碳原子数的烃沸点要____。
(2)溶解性:______于水,______于有机溶剂。
(3)密度:一般一氟代烃、一氯代烃比水小,其余比水大。
3.卤代烃的水解反应和消去反应
反应类型 水解反应(取代反应) 消去反应
反应条件 强碱的水溶液加热 强碱的醇溶液加热
断键方式
化学方 RCHCHX+NaOH――→RCH==CH+
2 2 2
RCHX+NaOH――→RCHOH+NaX
2 2
程式 NaX+HO
2
消去H、X,生成物中含有碳碳双键
产物特征 引入—OH
或碳碳三键
特别提醒 卤代烃能发生消去反应的结构条件
①卤代烃中碳原子数≥2;②存在β-H;③苯环上的卤素原子不能消去。
4.卤代烃中卤素原子的检验(1)检验流程
(2)加入稀硝酸酸化是为了中和过量的 NaOH,防止NaOH与AgNO 反应,产生棕褐色的
3
Ag O沉淀。
2
5.卤代烃的获取
(1)不饱和烃与卤素单质、卤化氢等的加成反应
CH—CH==CH+Br ―→____________;
3 2 2
CH—CH==CH+HBr――→____________________________________________________;
3 2
CH≡CH+HCl――→____________。
(2)取代反应
CHCH+Cl――→____________;
3 3 2
+Br ――→________________;
2
C HOH+HBr――→____________。
2 5
1.CHCHCl的沸点比CHCH 的沸点高( )
3 2 3 3
2.溴乙烷与NaOH的乙醇溶液共热生成乙烯( )
3.在溴乙烷中加入AgNO 溶液,立即产生浅黄色沉淀( )
3
4.所有卤代烃都能够发生消去反应( )
一、卤代烃的性质
1.在卤代烃RCHCHX中化学键如图所示,下列说法正确的是( )
2 2
A.发生水解反应时,被破坏的键是①和③
B.发生消去反应时,被破坏的键是①和④
C.发生水解反应时,被破坏的键是①
D.发生消去反应时,被破坏的键是②和③
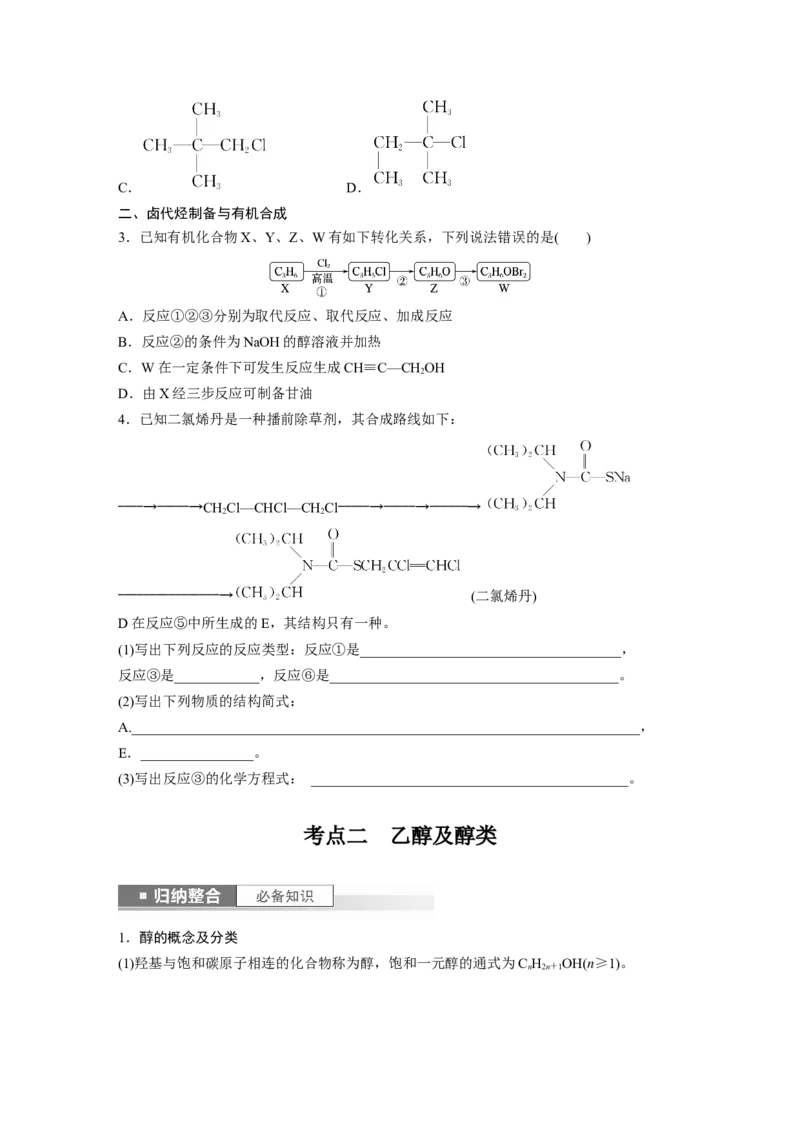
2.下列化合物中,既能发生水解反应,又能发生消去反应,且消去后只生成一种不饱和化
合物的是( )
A.CHCl B.
3C. D.
二、卤代烃制备与有机合成
3.已知有机化合物X、Y、Z、W有如下转化关系,下列说法错误的是( )
A.反应①②③分别为取代反应、取代反应、加成反应
B.反应②的条件为NaOH的醇溶液并加热
C.W在一定条件下可发生反应生成CH≡C—CHOH
2
D.由X经三步反应可制备甘油
4.已知二氯烯丹是一种播前除草剂,其合成路线如下:
――――→―――――→CHCl—CHCl—CH Cl―――――→―――――→――――――→
2 2
――――――――――――――――→ (二氯烯丹)
D在反应⑤中所生成的E,其结构只有一种。
(1)写出下列反应的反应类型:反应①是_____________________________________,
反应③是____________,反应⑥是_________________________________________。
(2)写出下列物质的结构简式:
A.________________________________________________________________________,
E.________________。
(3)写出反应③的化学方程式: _____________________________________________。
考点二 乙醇及醇类
1.醇的概念及分类
(1)羟基与饱和碳原子相连的化合物称为醇,饱和一元醇的通式为C H OH(n≥1)。
n 2n+1(2)
2.醇类的物理性质
熔、沸点 溶解性 密度
①高于相对分子质量接近的
①饱和一元醇随碳原子数的增
____________;
加而________;
醇 ②随碳原子数的增加而________; 比水小
②羟基个数越多,溶解度
③碳原子数相同时,羟基个数越
__________
多,熔、沸点________
思考 (1)醇比同碳原子烃的沸点高的原因为________________________________
________________________________________________________________________。
(2)甲醇、乙醇、丙醇可与水以任意比例互溶的原因为____________________________。
3.几种重要醇的物理性质和用途
物理性质 用途
无色、有特殊香味的液体,易挥
燃料;化工原料;常用的溶剂;体
乙醇 发,密度比水______,能与水
积分数为____时可作医用消毒剂
________________
无色液体,沸点低、易挥发、易溶
甲醇(木醇) 化工生产、车用燃料
于水
乙二醇 无色、黏稠液体,与水以任意比例 重要化工原料,制造化妆品、发动
丙三醇(甘油) 互溶 机、防冻液等
4.从官能团、化学键的视角理解醇的化学性质
(1)根据结构预测醇类的化学性质
醇的官能团羟基(—OH),决定了醇的主要化学性质,受羟基的影响,C—H的极性增强,一
定条件下也可能断键发生化学反应。
(2)醇分子的断键部位及反应类型
按要求完成下列方程式,并指明反应类型及断键部位。
(ⅰ)乙醇与Na反应: _____________________________________________________________________________________________________________________________。
(ⅱ)乙醇与HBr反应: ___________________________________________________
________________________________________________________________________。
(ⅲ)醇分子内脱水(以2-丙醇为例): ________________________________________
________________________________________________________________________。
(ⅳ)醇分子间脱水
a.乙醇在浓HSO 、140 ℃条件下: _______________________________________
2 4
________________________________________________________________________。
b.乙二醇在浓HSO 、加热条件下生成六元环醚: ___________________________
2 4
________________________________________________________________________。
(ⅴ)醇的催化氧化
a.乙醇:______________________________________________________________
________________________________________________________________________。
b.2-丙醇: _____________________________________________________________
________________________________________________________________________。
5.加成反应、取代反应、消去反应的特点
反应类型 概念 特点
A1 ===B1+A2—B2
有机化合物分子中的________
――→__________________________________
两端的原子与______________
加成反应 ______________________________________
结合,生成饱和的或比较饱和
。“只上不下”, 反应物中一般含碳碳双
的有机化合物的反应
键、碳碳三键、苯环等
A1—B1+A2—B2 ―→________+
有机化合物分子中的某些
________。
取代反应 ____________被其他
“有上有下”,反应中一般有副产物生成;
____________代替的反应
卤代、水解、硝化、酯化均属于取代反应
有机物在一定条件下从一个分
消去反应 子中脱去小分子(如H
2
O、HX ________________。
等)生成____________的反应 “只下不上”,反应物一般是醇或卤代烃
一、醇的性质及应用
1.下列关于醇的化学性质的说法正确的是( )
A.乙醇分子中的氢原子均可被金属钠取代
B.乙醇在浓硫酸作催化剂时加热至140 ℃可以制备乙烯C.所有的醇都可以被氧化为醛或酮
D.交警检查司机酒后驾车是利用了乙醇能被重铬酸钾氧化的性质
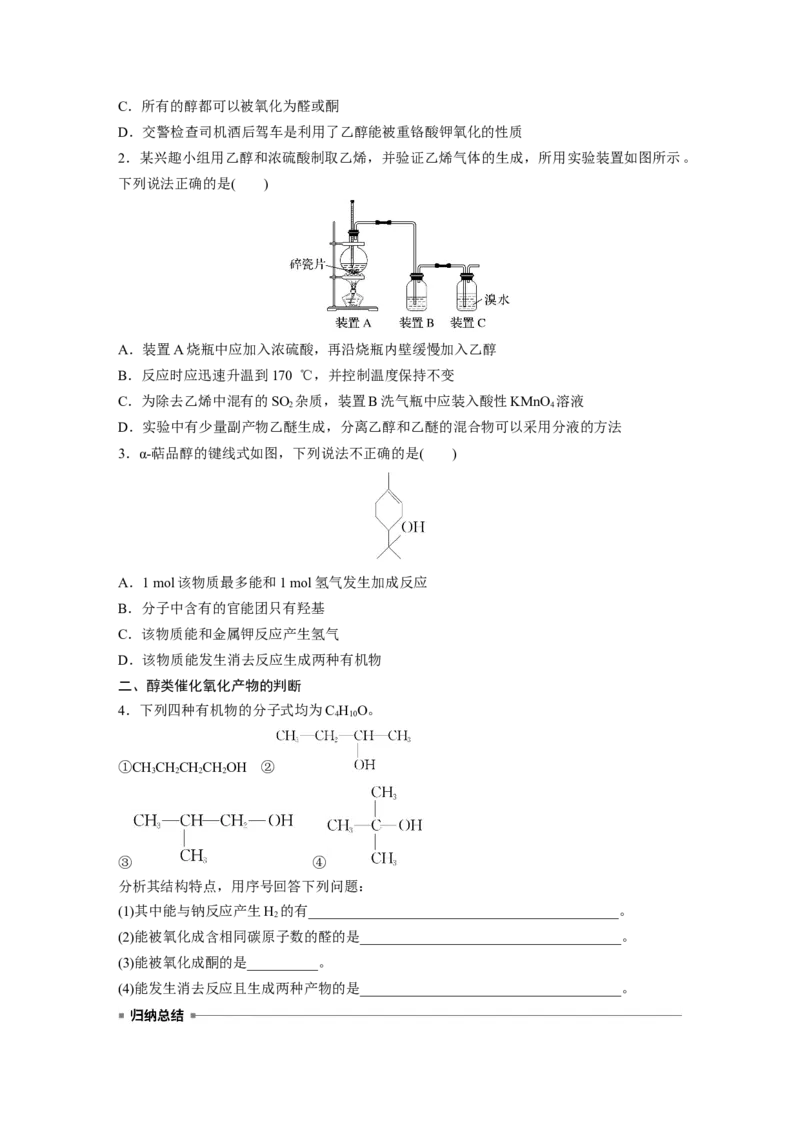
2.某兴趣小组用乙醇和浓硫酸制取乙烯,并验证乙烯气体的生成,所用实验装置如图所示。
下列说法正确的是( )
A.装置A烧瓶中应加入浓硫酸,再沿烧瓶内壁缓慢加入乙醇
B.反应时应迅速升温到170 ℃,并控制温度保持不变
C.为除去乙烯中混有的SO 杂质,装置B洗气瓶中应装入酸性KMnO 溶液
2 4
D.实验中有少量副产物乙醚生成,分离乙醇和乙醚的混合物可以采用分液的方法
3.α-萜品醇的键线式如图,下列说法不正确的是( )
A.1 mol该物质最多能和1 mol氢气发生加成反应
B.分子中含有的官能团只有羟基
C.该物质能和金属钾反应产生氢气
D.该物质能发生消去反应生成两种有机物
二、醇类催化氧化产物的判断
4.下列四种有机物的分子式均为C H O。
4 10
①CHCHCHCHOH ②
3 2 2 2
③ ④
分析其结构特点,用序号回答下列问题:
(1)其中能与钠反应产生H 的有____________________________________________。
2
(2)能被氧化成含相同碳原子数的醛的是_____________________________________。
(3)能被氧化成酮的是__________。
(4)能发生消去反应且生成两种产物的是_____________________________________。醇类催化氧化产物的判断
三、常见有机反应类型的判断
5.请观察下图中化合物A~H的转化反应的关系(图中副产物均未写出),并填写空白:
已知:① ――→
R—CH==CH+CHCOOH;
2 3
② ――――――→ 。
(1)写出图中化合物C、G、H的结构简式:
C______________________,G___________________________________________,
H______________________。
(2)属于取代反应的有________(序号,下同)。
(3)属于消去反应的是____________。
(4)写出反应⑨的化学方程式并指明其反应类型:________________________________,
________________________________________________________________________。
考点三 苯酚及酚类
1.概念
酚是____________直接相连而形成的化合物。
应用举例下列化合物中,属于酚类的是________(填字母)。
A.
B.
C.
D.
2.苯酚的化学性质
(1)弱酸性
+HO +HO+,苯酚具有________,俗称石炭酸。酸性:
2 3
HCO> >HCO,苯酚不能使酸碱指示剂变色,其酸性仅表现在与金属、强碱
2 3
的反应中。
与NaOH反应: _________________________________________________________
________________________________________________________________________;
与NaCO 反应: ________________________________________________________
2 3
________________________________________________________________________。
(2)与溴水的取代反应
苯酚滴入过量浓溴水中产生的现象为_______________________________________
________________________________________________________________________。
化学方程式: ___________________________________________________________。
(3)显色反应:与FeCl 溶液作用显____色。
3
(4)苯酚与甲醛在催化剂作用下,可发生缩聚反应,化学方程式: ________________
________________________________________________________________________。
(5)氧化反应:易被空气氧化为________色。
注意 苯酚有毒,浓溶液对皮肤有强腐蚀性,如皮肤不慎沾上苯酚溶液,应立即用乙醇冲洗,
再用水冲洗。
3.基团之间的相互影响
(1)苯酚与溴的取代反应比苯、甲苯易进行,原因是_________________________________。
(2)醇、酚、羧酸分子中羟基上氢原子的活泼性比较
名称 乙醇 苯酚 乙酸
酸性 中性 比碳酸弱 比碳酸强
氢原子
逐渐增强
活泼性―→
1.下列说法正确的是( )
A.苯甲醇和苯酚都能与浓溴水反应产生白色沉淀
B.苯甲醇、苯酚在分子组成上相差一个CH 原子团,故两者互为同系物
2
C. 、 、 互为同分异构体
D.乙醇、苯甲醇、苯酚都既能与钠反应,又能与NaOH反应
2.某化妆品的组成Z具有美白功效,可用如图反应制备。下列叙述不正确的是( )
+ ―→
A.可以通过红外光谱来鉴别X和Y
B.可用酸性高锰酸钾溶液鉴定Z中是否含有Y
C.Y、Z均可与溴水反应,但反应类型不同
D.X可作缩聚反应单体,Y可作加聚反应单体
3.苯酚的性质实验如下:
步骤1:常温下,取1 g苯酚晶体于试管中,向其中加入5 mL蒸馏水,充分振荡后液体变浑
浊,将该液体平均分成三份。
步骤2:向第一份液体中滴加几滴FeCl 溶液,观察到溶液显紫色(查阅资料可知配离子
3
[Fe(C HO) ]3-显紫色)。
6 5 6
步骤3:向第二份液体中滴加少量浓溴水,振荡,无白色沉淀。
步骤4:向第三份液体中加入5% NaOH溶液并振荡,得到澄清溶液,再向其中通入少量
CO,溶液又变浑浊,静置后分层。下列说法错误的是( )
2
A.步骤1说明常温下苯酚的溶解度小于20 g
B.步骤2中紫色的[Fe(C HO) ]3-由Fe3+提供空轨道
6 5 6
C.步骤3中生成的2,4,6-三溴苯酚溶解在过量的苯酚中,观察不到沉淀
D.步骤4中CO 与苯酚钠反应生成苯酚和NaCO
2 2 3
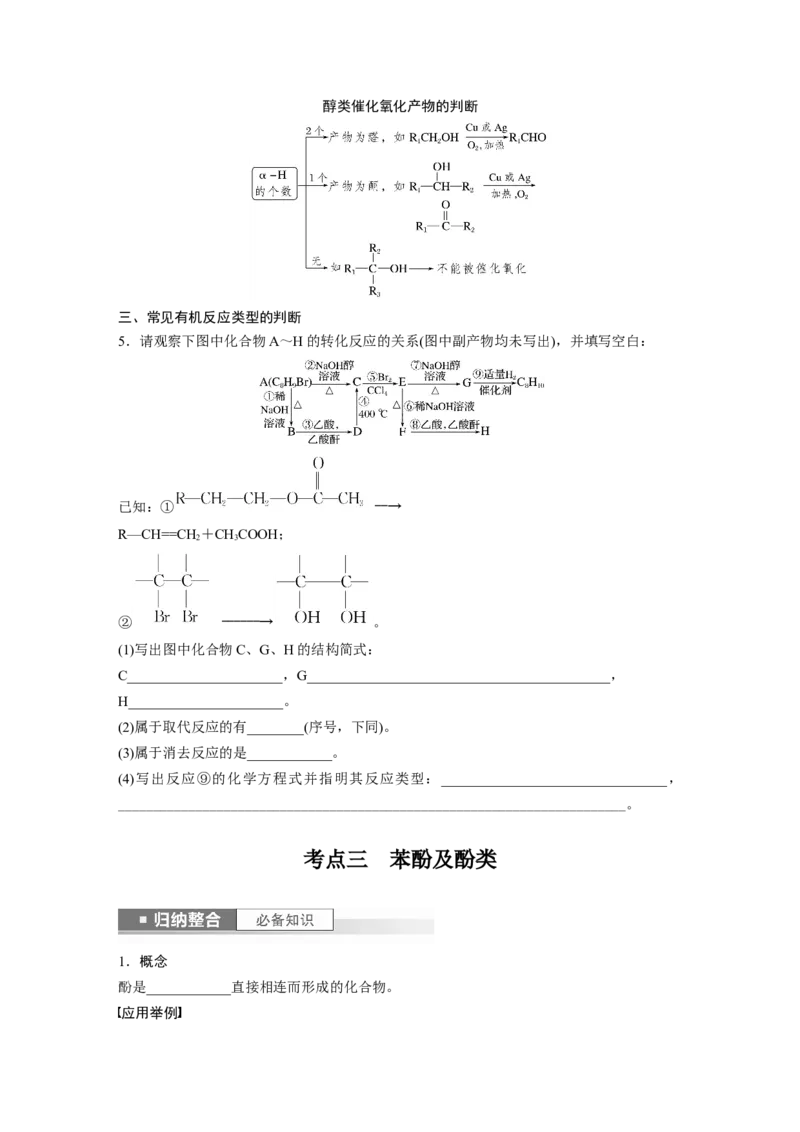
4.某超市违规出售的一种鸡蛋为“橡皮蛋”,煮熟后蛋黄韧性胜过乒乓球,但经检测为真
鸡蛋。专家介绍,这是由于鸡饲料里添加了棉籽饼,从而使鸡蛋里含有过多棉酚。棉酚的结
构简式如图所示。下列说法不正确的是( )
A.该化合物的分子式为C H O
30 30 8
B.1 mol棉酚最多可与14 mol H 加成
2
C.1 mol棉酚最多可与6 mol NaOH反应
D.该物质可以使酸性高锰酸钾溶液褪色
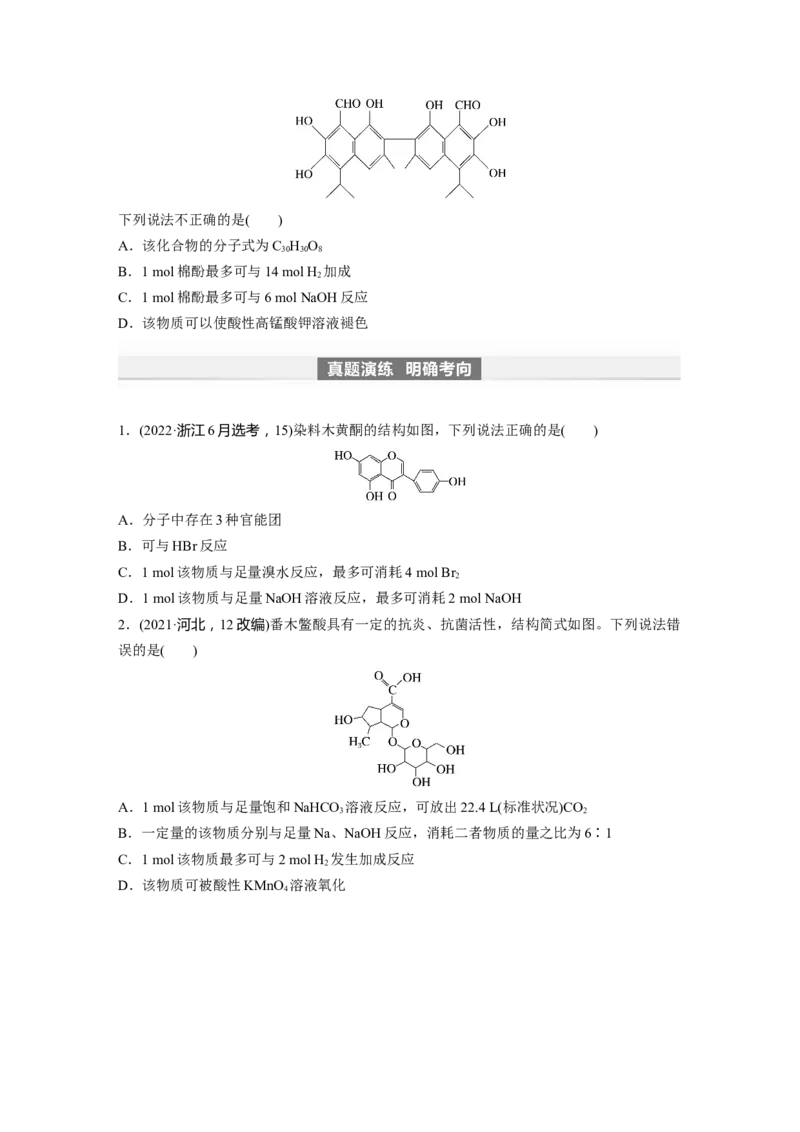
1.(2022·浙江6月选考,15)染料木黄酮的结构如图,下列说法正确的是( )
A.分子中存在3种官能团
B.可与HBr反应
C.1 mol该物质与足量溴水反应,最多可消耗4 mol Br
2
D.1 mol该物质与足量NaOH溶液反应,最多可消耗2 mol NaOH
2.(2021·河北,12改编)番木鳖酸具有一定的抗炎、抗菌活性,结构简式如图。下列说法错
误的是( )
A.1 mol该物质与足量饱和NaHCO 溶液反应,可放出22.4 L(标准状况)CO
3 2
B.一定量的该物质分别与足量Na、NaOH反应,消耗二者物质的量之比为6∶1
C.1 mol该物质最多可与2 mol H 发生加成反应
2
D.该物质可被酸性KMnO 溶液氧化
4