文档内容
第 10 讲 氯及其化合物
【练基础】
1.化学来源于生活,也服务于生活。下列有关生活中的化学知识叙述正确的是( )
A.氯气和活性炭均可作为漂白剂,若同时使用,漂白效果会明显加强
B.氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂
C.测定溶液pH的实验中,用干燥pH试纸测定新制氯水的pH,测定结果无影响
D.洁厕灵不能与84消毒液混用,原因是两种溶液混合产生的HClO易分解
2.下列有关含氯化合物的说法正确的是( )
A.HClO是弱酸,所以NaClO是弱电解质
B.氯水中具有漂白性的物质是HClO
C.检验Cl 中是否混有HCl,可以用湿润的淀粉KI试纸
2
D.NaClO和Ca(ClO) 的溶液能杀菌消毒的原理是二者水解均呈碱性
2
3.Cl 是一种重要的工业原料,液氯储存区贴有的说明卡如下:
2
包装 钢瓶
储运要求 远离金属粉末、氨、烃类、醇类物质;设置氯气检测仪
泄漏处理 NaOH、NaHSO 溶液吸收
3
下列解释事实的方程式不正确的是( )
A.电解饱和食盐水制取Cl:2Cl-+2HO=====2OH-+H↑+Cl↑
2 2 2 2
B.氯气用于自来水消毒:Cl+HO2H++Cl-+ClO-
2 2
C.浓氨水检验泄漏的氯气,产生白烟:8NH +3Cl===6NHCl+N
3 2 4 2
D.氯气“泄漏处理”中NaHSO 溶液的作用:HSO+Cl+HO===SO+3H++2Cl-
3 2 2
4.为探究新制氯水的性质,某学生做了如下实验:
实验 装置 试剂a 现象
① 紫色的石蕊试液 溶液先变红后褪色
② NaHCO 溶液 产生气泡
3
HNO 酸化的AgNO 溶
③ 3 3 产生白色沉淀
液
④ FeCl 溶液、KSCN溶液 溶液变红
2
由上述实验可得新制氯水的性质与对应的解释或离子方程式不相符的是( )
A.实验①说明新制氯水中含有H+、HClO
B.实验②发生的反应为HCO+HClO===ClO-+CO↑+HO
2 2
C.实验③说明新制氯水中有Cl-,Cl-+Ag+===AgCl↓D.实验④说明氯气具有强氧化性,Cl+2Fe2+===2Cl-+2Fe3+
2
5.溴化碘(IBr)的化学性质与卤素单质相似,能与大多数金属反应生成金属卤化物,和某些非金属单
质反应生成相应的卤化物,跟水反应的化学方程式为IBr+HO===HBr+HIO。下列有关IBr的叙述中,不
2
正确的是( )
A.IBr是双原子分子
B.在很多反应中,IBr是强氧化剂
C.与NaOH溶液反应生成NaBr和NaIO
D.与水反应时,IBr既是氧化剂又是还原剂
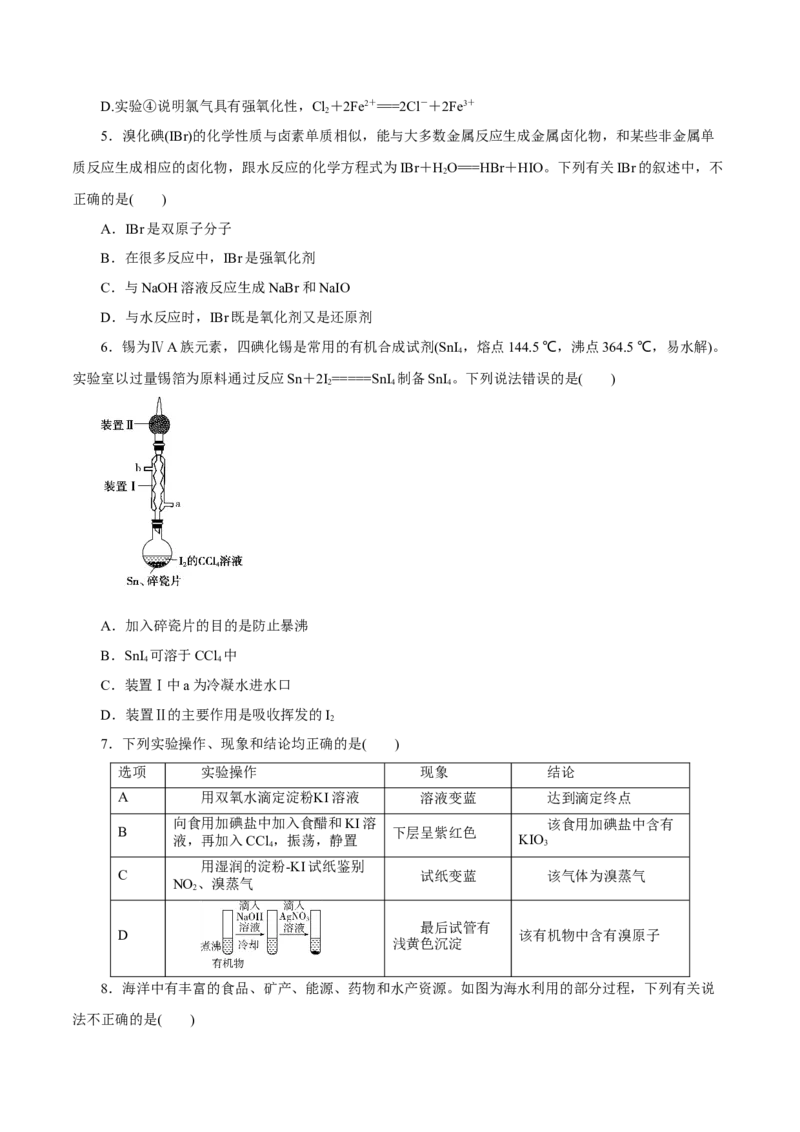
6.锡为ⅣA族元素,四碘化锡是常用的有机合成试剂(SnI ,熔点144.5 ℃,沸点364.5 ℃,易水解)。
4
实验室以过量锡箔为原料通过反应Sn+2I=====SnI 制备SnI 。下列说法错误的是( )
2 4 4
A.加入碎瓷片的目的是防止暴沸
B.SnI 可溶于CCl 中
4 4
C.装置Ⅰ中a为冷凝水进水口
D.装置Ⅱ的主要作用是吸收挥发的I
2
7.下列实验操作、现象和结论均正确的是( )
选项 实验操作 现象 结论
A 用双氧水滴定淀粉KI溶液 溶液变蓝 达到滴定终点
向食用加碘盐中加入食醋和KI溶 该食用加碘盐中含有
B 下层呈紫红色
液,再加入CCl ,振荡,静置 KIO
4 3
用湿润的淀粉-KI试纸鉴别
C 试纸变蓝 该气体为溴蒸气
NO 、溴蒸气
2
最后试管有
D 该有机物中含有溴原子
浅黄色沉淀
8.海洋中有丰富的食品、矿产、能源、药物和水产资源。如图为海水利用的部分过程,下列有关说
法不正确的是( )A.制取NaHCO 的反应利用了NaHCO 的溶解度小于NaCl
3 3
B.侯氏制碱法应先通NH 再通CO
3 2
C.在第②、③、④步骤中,溴元素均被氧化
D.③④的目的是进行溴的富集
9.二氧化氯(ClO )是国际上公认的安全、无毒的绿色消毒剂,对酸性污水中的Mn2+也有明显的去除
2
效果,其反应原理为ClO +Mn2+―→MnO ↓+Cl-(部分反应物和产物省略、未配平),下列有关该反应的
2 2
说法正确的是( )
A.工业上可用更为廉价的Cl 来代替ClO
2 2
B.利用该原理处理含Mn2+的污水后溶液的pH增大
C.该反应中氧化产物和还原产物的物质的量之比为5∶2
D.理论上处理含1 mol Mn2+的污水,需要标准状况下的ClO 8.96 L
2
10.I-具有还原性,含碘食盐中的碘元素主要以KIO 的形式存在,I-、I、IO在一定条件下可发生如
3 2
图转化关系。下列说法不正确的是( )
A.用淀粉KI试纸和食醋可检验食盐是否加碘
B.由图可知氧化性的强弱顺序为Cl>IO>I
2 2
C.生产等量的碘,途径Ⅰ和途径Ⅱ转移电子数目之比为2∶5
D.途径Ⅲ反应的离子方程式:3Cl+I-+3HO===6Cl-+IO+6H+
2 2
【练提升】
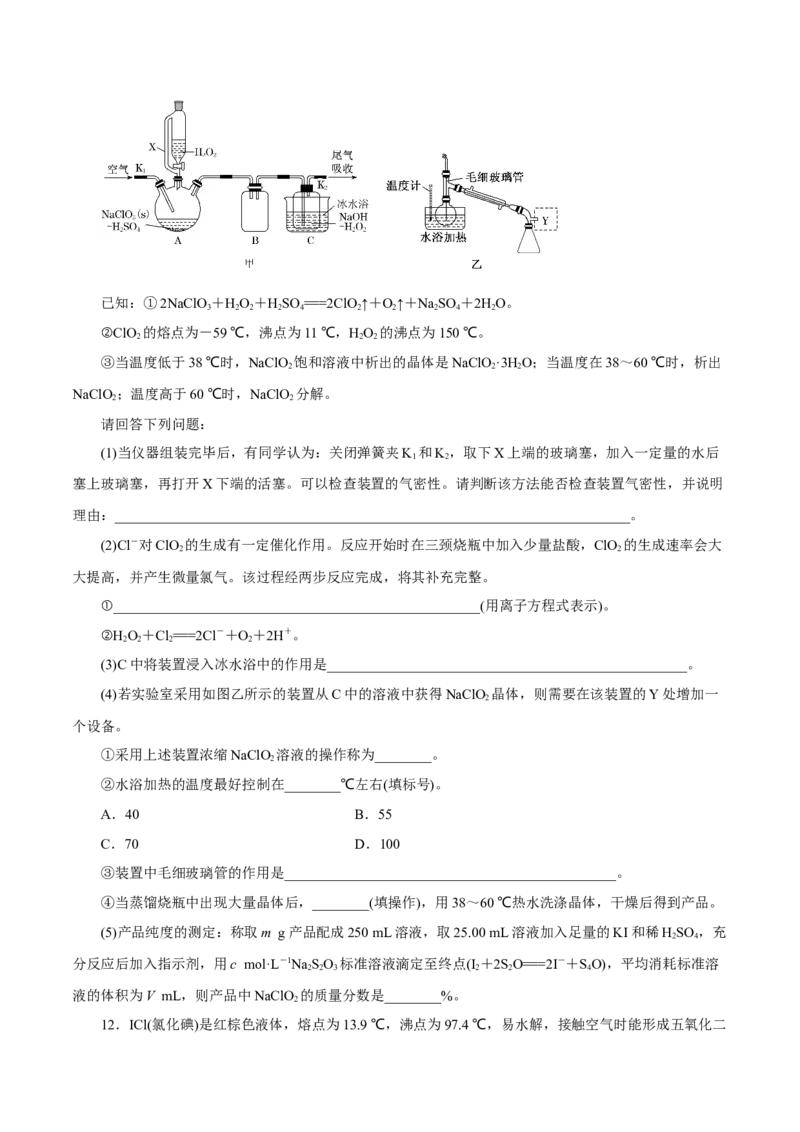
11.ClO 是一种优良的消毒剂,浓度过高时易发生分解,常将其制备成NaClO 固体以便运输和贮
2 2
存。过氧化氢法制备NaClO 的实验装置如图甲所示:
2已知:①2NaClO+HO+HSO ===2ClO ↑+O↑+NaSO +2HO。
3 2 2 2 4 2 2 2 4 2
②ClO 的熔点为-59 ℃,沸点为11 ℃,HO 的沸点为150 ℃。
2 2 2
③当温度低于38 ℃时,NaClO 饱和溶液中析出的晶体是NaClO·3H O;当温度在38~60 ℃时,析出
2 2 2
NaClO;温度高于60 ℃时,NaClO 分解。
2 2
请回答下列问题:
(1)当仪器组装完毕后,有同学认为:关闭弹簧夹K 和K,取下X上端的玻璃塞,加入一定量的水后
1 2
塞上玻璃塞,再打开X下端的活塞。可以检查装置的气密性。请判断该方法能否检查装置气密性,并说明
理由:_________________________________________________________________________。
(2)Cl-对ClO 的生成有一定催化作用。反应开始时在三颈烧瓶中加入少量盐酸,ClO 的生成速率会大
2 2
大提高,并产生微量氯气。该过程经两步反应完成,将其补充完整。
①____________________________________________________(用离子方程式表示)。
②H O+Cl===2Cl-+O+2H+。
2 2 2 2
(3)C中将装置浸入冰水浴中的作用是___________________________________________________。
(4)若实验室采用如图乙所示的装置从C中的溶液中获得NaClO 晶体,则需要在该装置的Y处增加一
2
个设备。
①采用上述装置浓缩NaClO 溶液的操作称为________。
2
②水浴加热的温度最好控制在________℃左右(填标号)。
A.40 B.55
C.70 D.100
③装置中毛细玻璃管的作用是_______________________________________________。
④当蒸馏烧瓶中出现大量晶体后,________(填操作),用38~60 ℃热水洗涤晶体,干燥后得到产品。
(5)产品纯度的测定:称取m g产品配成250 mL溶液,取25.00 mL溶液加入足量的KI和稀HSO ,充
2 4
分反应后加入指示剂,用c mol·L-1NaSO 标准溶液滴定至终点(I+2SO===2I-+SO),平均消耗标准溶
2 2 3 2 2 4
液的体积为V mL,则产品中NaClO 的质量分数是________%。
2
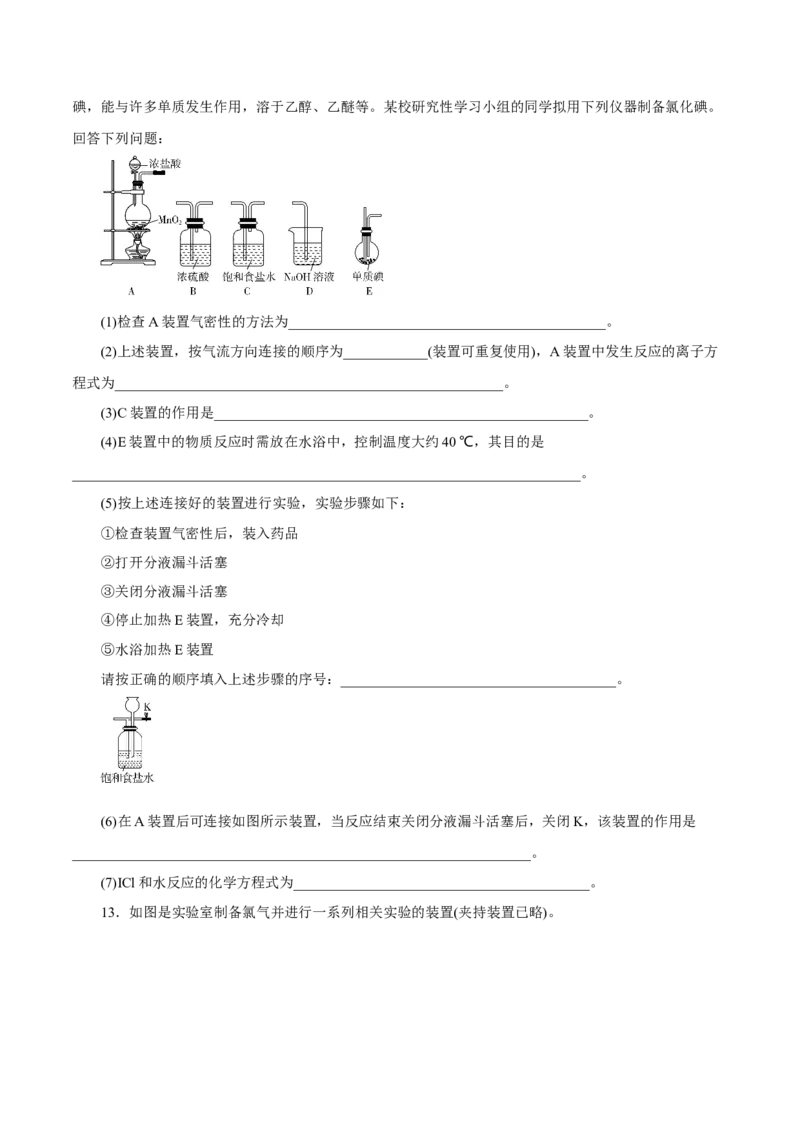
12.ICl(氯化碘)是红棕色液体,熔点为13.9 ℃,沸点为97.4 ℃,易水解,接触空气时能形成五氧化二碘,能与许多单质发生作用,溶于乙醇、乙醚等。某校研究性学习小组的同学拟用下列仪器制备氯化碘。
回答下列问题:
(1)检查A装置气密性的方法为_____________________________________________。
(2)上述装置,按气流方向连接的顺序为____________(装置可重复使用),A装置中发生反应的离子方
程式为_______________________________________________________。
(3)C装置的作用是_____________________________________________________。
(4)E装置中的物质反应时需放在水浴中,控制温度大约40 ℃,其目的是
________________________________________________________________________。
(5)按上述连接好的装置进行实验,实验步骤如下:
①检查装置气密性后,装入药品
②打开分液漏斗活塞
③关闭分液漏斗活塞
④停止加热E装置,充分冷却
⑤水浴加热E装置
请按正确的顺序填入上述步骤的序号:_______________________________________。
(6)在A装置后可连接如图所示装置,当反应结束关闭分液漏斗活塞后,关闭K,该装置的作用是
_________________________________________________________________。
(7)ICl和水反应的化学方程式为__________________________________________。
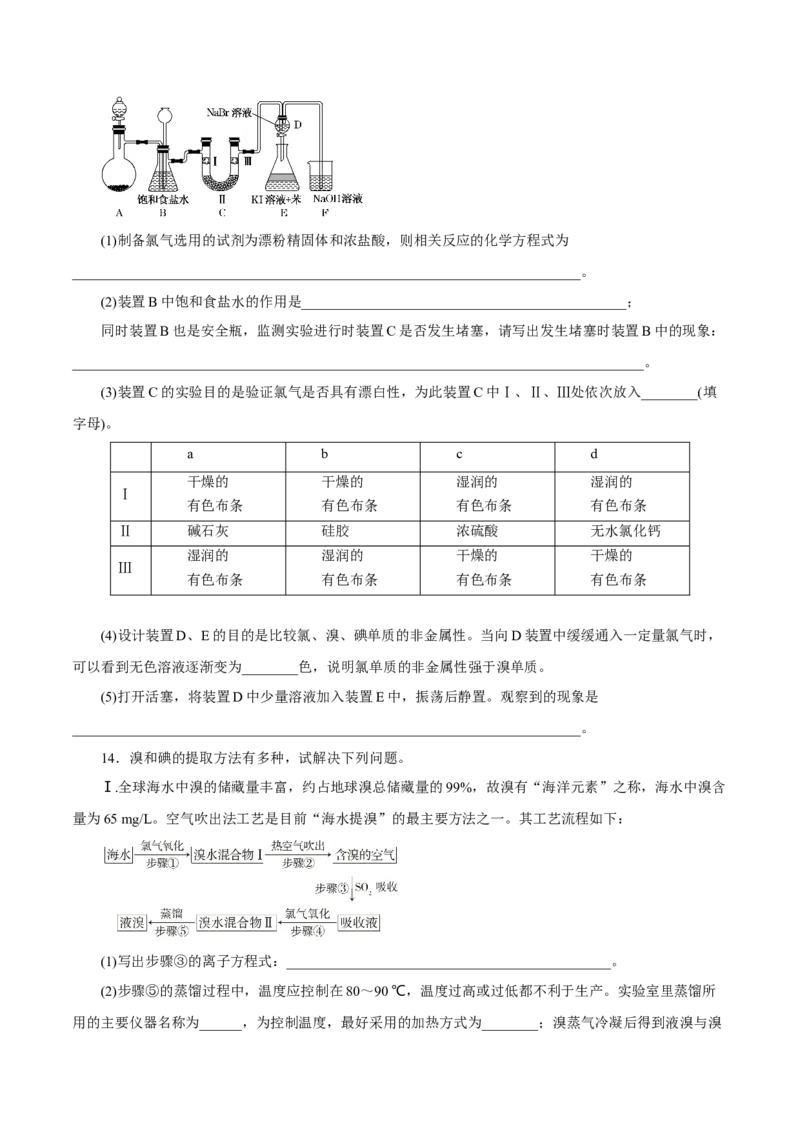
13.如图是实验室制备氯气并进行一系列相关实验的装置(夹持装置已略)。(1)制备氯气选用的试剂为漂粉精固体和浓盐酸,则相关反应的化学方程式为
________________________________________________________________________。
(2)装置B中饱和食盐水的作用是______________________________________________;
同时装置B也是安全瓶,监测实验进行时装置C是否发生堵塞,请写出发生堵塞时装置B中的现象:
_________________________________________________________________________________。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此装置C中Ⅰ、Ⅱ、Ⅲ处依次放入________(填
字母)。
a b c d
干燥的 干燥的 湿润的 湿润的
Ⅰ
有色布条 有色布条 有色布条 有色布条
Ⅱ 碱石灰 硅胶 浓硫酸 无水氯化钙
湿润的 湿润的 干燥的 干燥的
Ⅲ
有色布条 有色布条 有色布条 有色布条
(4)设计装置D、E的目的是比较氯、溴、碘单质的非金属性。当向D装置中缓缓通入一定量氯气时,
可以看到无色溶液逐渐变为________色,说明氯单质的非金属性强于溴单质。
(5)打开活塞,将装置D中少量溶液加入装置E中,振荡后静置。观察到的现象是
________________________________________________________________________。
14.溴和碘的提取方法有多种,试解决下列问题。
Ⅰ.全球海水中溴的储藏量丰富,约占地球溴总储藏量的99%,故溴有“海洋元素”之称,海水中溴含
量为65 mg/L。空气吹出法工艺是目前“海水提溴”的最主要方法之一。其工艺流程如下:
(1)写出步骤③的离子方程式:______________________________________________。
(2)步骤⑤的蒸馏过程中,温度应控制在80~90 ℃,温度过高或过低都不利于生产。实验室里蒸馏所
用的主要仪器名称为______,为控制温度,最好采用的加热方式为________;溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离,分离仪器的名称是________________。
(3)溴水混合物Ⅱ中溶有一定量的氯气,因此在步骤⑤中可将蒸馏产生的气体通过________(填试剂名
称)溶液,以除去氯气。
(4)步骤①中用硫酸酸化可提高Cl 的利用率,理由是____________________________。
2
(5)提取溴单质,采用蒸馏“溴水混合物Ⅱ”而不是蒸馏“溴水混合物Ⅰ”,请说明原因:
________________________________________________________________________。
Ⅱ.实验室从含碘废液(除HO外,含有CCl 、I、I-等)中回收碘,其实验过程如下:
2 4 2
向含碘废液中加入稍过量的NaSO 溶液,将废液中的I 还原为I-,其离子方程式为
2 3 2
__________________;该操作将I 还原为I-的目的是________________________。操作X的名称为
2
________。
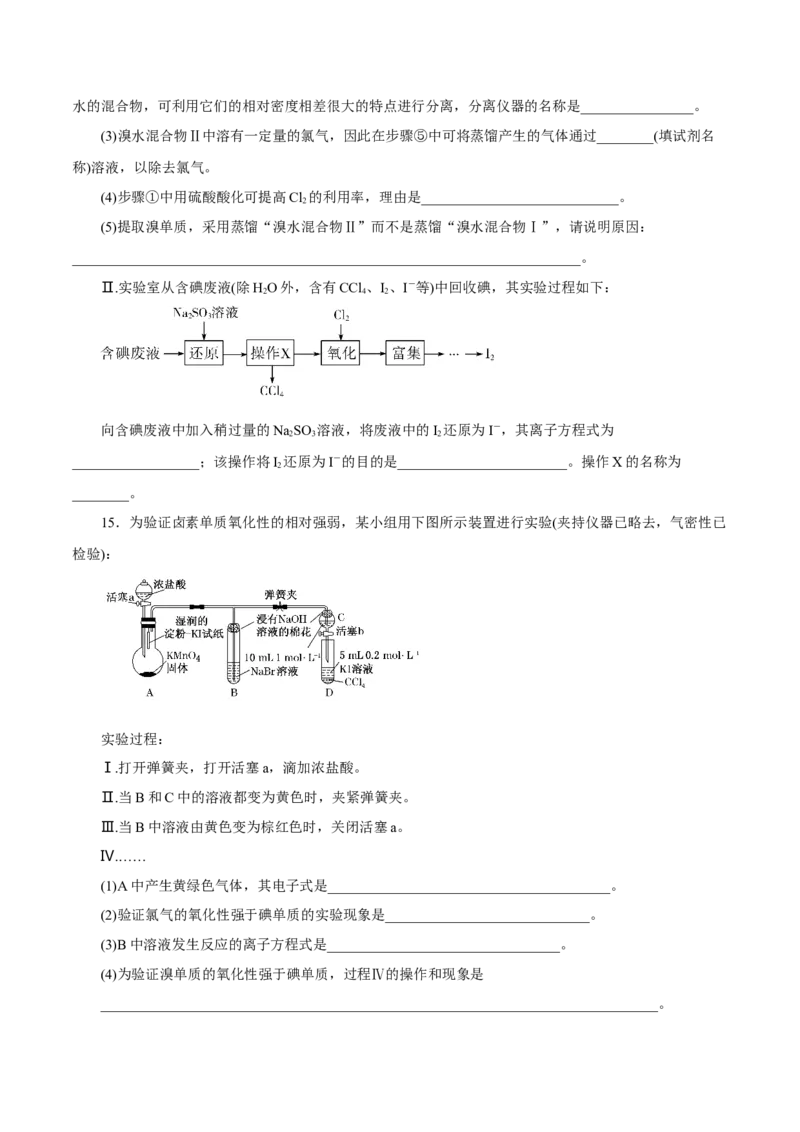
15.为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已
检验):
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,其电子式是________________________________________。
(2)验证氯气的氧化性强于碘单质的实验现象是_____________________________。
(3)B中溶液发生反应的离子方程式是_________________________________。
(4)为验证溴单质的氧化性强于碘单质,过程Ⅳ的操作和现象是
_______________________________________________________________________________。(5)过程Ⅲ实验的目的是________________________________________________________________。
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下________,得电子能力逐渐减弱。