文档内容
第十二讲 铜及其重要化合物 无机化工流程
【基础巩固】
1.某研究小组通过实验探究Cu及其重要化合物的性质,下列操作正确且能达到目的的是( )
A.将铜丝插入浓硫酸中加热,反应完后把水加入反应器中,观察硫酸铜溶液的颜色
B.常温下将铜丝伸入盛满氯气的集气瓶中,观察CuCl 的生成
2
C.将CuCl 溶液在蒸发皿中加热蒸干,得到无水CuCl 固体
2 2
D.将表面有铜绿的铜器放入稀盐酸中浸泡,除去铜绿
【答案】 D
【解析】 A项,应将反应后的液体倒入盛水的烧杯中,并不断搅拌;B项,应将铜丝在空气中加热到红
热后伸入盛满氯气的集气瓶中;C项,CuCl 水解生成的盐酸易挥发,加热蒸干 CuCl 溶液得不到无水
2 2
CuCl 固体。
2
2.(2020·全国卷Ⅲ,7)宋代《千里江山图》描绘了山清水秀的美丽景色,历经千年色彩依然,其中绿色来自
孔雀石颜料[主要成分为Cu(OH) ·CuCO],青色来自蓝铜矿颜料[主要成分为Cu(OH) ·2CuCO]。下列说法
2 3 2 3
错误的是( )
A.保存《千里江山图》需控制温度和湿度 B.孔雀石、蓝铜矿颜料不易被空气氧化
C.孔雀石、蓝铜矿颜料耐酸耐碱 D.Cu(OH) ·CuCO 中铜的质量分数高于Cu(OH) ·2CuCO
2 3 2 3
【答案】 C
3.我国古代“药金”的冶炼方法是将炉甘石(ZnCO)和赤铜矿(Cu O)与木炭按一定的比例混合后加热至
3 2
800 ℃,即可炼出闪烁似金子般光泽的“药金”。下列叙述正确的是( )
A.“药金”实质上是铜锌合金 B.冶炼炉中炉甘石直接被木炭还原为锌
C.用王水可区别黄金和“药金” D.用火焰灼烧不能区别黄金和“药金”
【答案】 A
【解析】 冶炼“药金”的相关反应的化学方程式为 ZnCO =====ZnO+CO↑、2ZnO+C=====2Zn+
3 2
CO↑、2Cu O+C=====4Cu+CO↑,A项正确、B项错误;王水可以溶解黄金和“药金”,C项错误;用
2 2 2
火焰灼烧可以区别黄金和“药金”,因为高温下黄金跟空气不反应,而“药金”可以与空气反应,生成的
CuO是黑色的,ZnO是白色的,D项错误。
4.人类最早冶金的历史年代曲线图如图所示(-1000表示公元前1000年)。下列说法正确的是( )
A.金属越活泼,冶炼的年代一定越晚
B.冶炼金属的历史:电解氯化物比电解氧化物早
资料整理【淘宝店铺:向阳百分百】C.自然界中铜元素以游离态形式存在,故铜的冶炼年代最早
D.金属氧化物(如Al O、Cu O)也属于金属材料
2 3 2
【答案】 B
【解析】 图中铜冶炼的年代比银和金早,而铜比银和金活泼,故A错误;金属氯化物的沸点一般比金属
氧化物的低,在冶炼初期会选择电解金属氯化物,故B正确;自然界中铜以化合态存在,故C错误。
5.(2022·湖南,7)铝电解厂烟气净化的一种简单流程如下:
下列说法错误的是( )
A.不宜用陶瓷作吸收塔内衬材料 B.采用溶液喷淋法可提高吸收塔内烟气吸收效率
C.合成槽中产物主要有NaAlF 和CO D.滤液可回收进入吸收塔循环利用
3 6 2
【答案】 C
【解析】 烟气(含HF)通入吸收塔,加入过量的碳酸钠,发生反应:NaCO+HF===NaF+NaHCO ,向合
2 3 3
成槽中通入 NaAlO ,发生反应:6NaF+NaAlO +4NaHCO ===Na AlF↓+4NaCO +2HO,过滤得到
2 2 3 3 6 2 3 2
NaAlF 和含有NaCO 的滤液。陶瓷的成分中含有SiO ,SiO 能与HF发生反应,因此不宜用陶瓷作吸收
3 6 2 3 2 2
塔内衬材料,故A正确;采用溶液喷淋法可增大反应物的接触面积,提高吸收塔内烟气吸收效率,故B正
确;由上述分析知,合成槽内产物主要有 NaAlF 、NaCO 、HO,故 C 错误;滤液的主要成分为
3 6 2 3 2
NaCO,可进入吸收塔循环利用,故D正确。
2 3
6.(2022·陕西榆林模拟)水合肼(N H·H O)的性质类似氨水。利用水合肼处理铜氨{[Cu(NH )]2+}
2 4 2 3 4
废液回收铜粉的实验流程如图:
下列说法错误的是( )
A.上述三步反应过程均为氧化还原反应
B.反应1的目的是制备NaClO
C.合成水合肼的反应中每消耗1 mol CO(NH ) 转移电子数为N
2 2 A
D.反应3完成后要用到过滤操作
【答案】 C
【解析】 反应1是氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,氯元素化合价发生变化;反应2是
次氯酸钠将尿素氧化为水合肼,氯元素、氮元素化合价发生变化;反应3是[Cu(NH )]2+被水合肼还原为
3 4
Cu,铜元素、氮元素化合价发生变化,则上述三步反应过程均为氧化还原反应,故 A正确;经分析知反应
1的目的是制备NaClO,用NaClO将尿素氧化为水合肼,故B正确;次氯酸钠将尿素氧化为水合肼,氮元
素化合价由-3价升高至-2价,每消耗1 mol CO(NH ) 转移电子数为2N ,故C错误;反应3完成后要把
2 2 A
铜粉分离出来,用到过滤操作,故D正确。
资料整理【淘宝店铺:向阳百分百】7.(2023·北京·高三专题练习)氯化亚铜(CuCl)是白色粉末,微溶于水,广泛应用于化工和印染等行业。
某研究性学习小组模拟热分解CuCl •2H O制备CuCl的过程,并进行相关物质转化的探究。
2 2
已知:酸性条件下Cu+不稳定
下列说法不正确的是
A.X气体是HCl,可抑制CuCl •2H O加热时水解
2 2
B.途径1中产生的Cl 可以回收利用,也可以通入饱和NaOH溶液中除去
2
C.途径2中200℃时反应的化学方程式为Cu (OH) Cl 2CuO+2HCl↑
2 2 2
D.CuCl与稀硫酸反应的离子方程式为2Cu++4H++SO =2Cu2++SO↑+2H O
2 2
【答案】D
【解析】 热分解CuCl2•2H2O 制备CuCl,为抑制CuCl2水解,要在HCl气流下加热,加热温度大于
300C,发生 ,直接加热CuCl2•2H2O会生成Cu2 (OH ) 2Cl2,Cu2 (OH ) 2Cl2加热
到 200C 生成 CuO。据此解答。A.氯化铜水解生成氢氧化铜和氯化氢,X 气体是 HCl,可抑制
CuCl2•2H2O加热时水解,A正确;B.氯气能被饱和氢氧化钠溶液吸收,防止污染,也可以将其转化为氯
化氢,回收循环利用,B正确;C.途径2中200℃时反应生成氧化铜,由原子守恒可知,还生成氯化氢,
该反应的化学方程式为Cu2(OH)2Cl2 2CuO+2HCl↑,C正确;D.氯化亚铜不溶于水,书写离子方程
式时不能拆开,D错误;故选D。
8.(2023.全国甲卷) 是一种压电材料。以 为原料,采用下列路线可制备粉状 。
回答下列问题:
(1)“焙烧”步骤中碳粉的主要作用是_______。
资料整理【淘宝店铺:向阳百分百】(2)“焙烧”后固体产物有 、易溶于水的 和微溶于水的 。“浸取”时主要反应的离子方
程式为_______。
(3)“酸化”步骤应选用的酸是_______(填标号)。
a.稀硫酸 b.浓硫酸 c.盐酸 d.磷酸
(4)如果焙烧后的产物直接用酸浸取,是否可行?_______,其原因是_______。
(5)“沉淀”步骤中生成 的化学方程式为_______。
(6)“热分解”生成粉状钛酸钡,产生的 _______。
【答案】(1)做还原剂,将BaSO 还原 (2)S2-+Ca2+ =CaS↓
4
(3)c (4)①. 不可行 ②. 产物中的硫化物与酸反应生成的有毒气体 HS会污染空气,而且CaS
2
与盐酸反应生成可溶于水的CaCl ,导致BaCl 溶液中混有CaCl 杂质无法除去、最终所得产品的纯度降低
2 2 2
(5)BaCl + TiCl + HO +2(NH)C O=BaTi(C O) ↓ +4NHCl + 2HCl (6)1:1
2 4 2 4 2 2 4 2 4 2 4
【解析】
【分析】由流程和题中信息可知,BaSO 与过量的碳粉及过量的氯化钙在高温下焙烧得到 CO、BaCl 、易
4 2
溶于水的BaS和微溶于水的CaS;烧渣经水浸取后过滤,滤渣中碳粉和CaS,滤液中有BaCl 和BaS;滤液
2
经酸化后浓缩结晶得到BaCl 晶体;BaCl 晶体溶于水后,加入TiCl 和(NH )C O 将钡离子充分沉淀得到
2 2 4 4 2 2 4
BaTi(C O) ;BaTi(C O) 经热分解得到BaTiO 。(1)“焙烧”步骤中,BaSO 与过量的碳粉及过量的氯
2 4 2 2 4 2 3 4
化钙在高温下焙烧得到CO、BaCl 、BaS和CaS,BaSO 被还原为BaS,因此,碳粉的主要作用是做还原剂,
2 4
将BaSO 还原。(2)“焙烧”后固体产物有BaCl 、易溶于水的BaS和微溶于水的CaS。易溶于水的BaS
4 2
与过量的CaCl 可以发生复分解反应生成硫化钙沉淀,因此,“浸取”时主要反应的离子方程式为S2-+Ca2+
2
=CaS↓。
(3)“酸化”步骤是为了将BaS转化为易溶液于的钡盐,由于硫酸钡和磷酸钡均不溶于水,而BaCl 可溶
2
于水,因此,应选用的酸是盐酸,选c。(4)如果焙烧后的产物直接用酸浸取是不可行的,其原因是:产
物中的硫化物与酸反应生成的有毒气体HS会污染空气,而且CaS与盐酸反应生成可溶于水的CaCl ,导
2 2
致BaCl 溶液中混有CaCl 杂质无法除去、最终所得产品的纯度降低。(5)“沉淀”步骤中生成
2 2
BaTi(C O) 的化学方程式为:BaCl + TiCl + HO +2(NH)C O=BaTi(C O) ↓ +4NHCl + 2HCl 。
2 4 2 2 4 2 4 2 2 4 2 4 2 4
(6)“热分解”生成粉状钛酸钡,该反应的化学方程式为:
BaTi(C O) BaTiO +2CO ↑+2CO↑,因此,产生的n(CO): n(CO)=1:1。
2 4 2 3 2 2
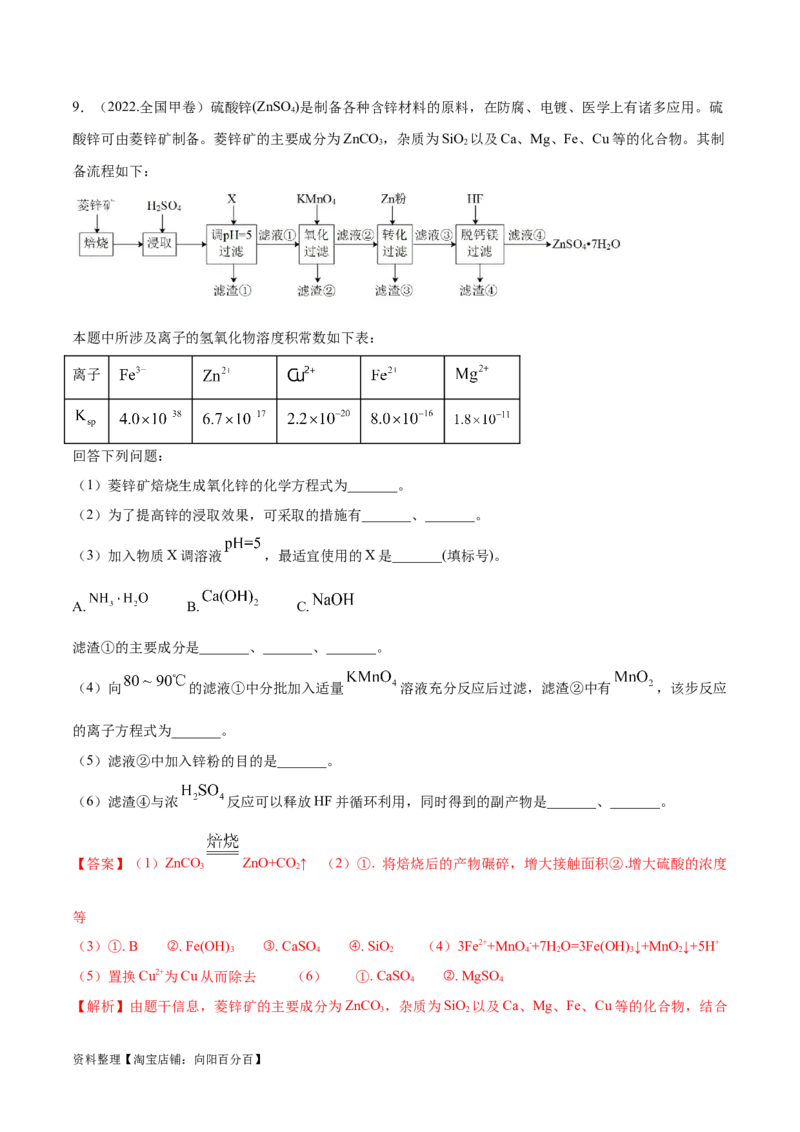
资料整理【淘宝店铺:向阳百分百】9.(2022.全国甲卷)硫酸锌(ZnSO)是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多应用。硫
4
酸锌可由菱锌矿制备。菱锌矿的主要成分为ZnCO ,杂质为SiO 以及Ca、Mg、Fe、Cu等的化合物。其制
3 2
备流程如下:
本题中所涉及离子的氢氧化物溶度积常数如下表:
离子
回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为_______。
(2)为了提高锌的浸取效果,可采取的措施有_______、_______。
(3)加入物质X调溶液 ,最适宜使用的X是_______(填标号)。
A. B. C.
滤渣①的主要成分是_______、_______、_______。
(4)向 的滤液①中分批加入适量 溶液充分反应后过滤,滤渣②中有 ,该步反应
的离子方程式为_______。
(5)滤液②中加入锌粉的目的是_______。
(6)滤渣④与浓 反应可以释放HF并循环利用,同时得到的副产物是_______、_______。
【答案】(1)ZnCO ZnO+CO ↑ (2)①. 将焙烧后的产物碾碎,增大接触面积②.增大硫酸的浓度
3 2
等
(3)①. B ②. Fe(OH) ③. CaSO ④. SiO (4)3Fe2++MnO -+7H O=3Fe(OH) ↓+MnO↓+5H+
3 4 2 4 2 3 2
(5)置换Cu2+为Cu从而除去 (6) ①. CaSO ②. MgSO
4 4
【解析】由题干信息,菱锌矿的主要成分为ZnCO ,杂质为SiO 以及Ca、Mg、Fe、Cu等的化合物,结合
3 2
资料整理【淘宝店铺:向阳百分百】流程图分析,菱锌矿焙烧,主要发生反应 ZnCO ZnO+CO ↑,再加入HSO 酸浸,得到含Zn2+、
3 2 2 4
Ca2+、Mg2+、Fe2+、Fe3+、Cu2+的溶液,加入物质 X 调节 pH=5,结合表格数据,过滤得到 Fe(OH) 、
3
CaSO 、SiO 的滤渣①,滤液①中主要含有Zn2+、Cu2+、Mg2+、Ca2+、Fe2+,再向滤液①中加入KMnO 溶液
4 2 4
氧化Fe2+,过滤得到Fe(OH) 和MnO 的滤渣②,滤液②中加入锌粉,发生反应Zn+Cu2+=Zn2+=Cu,过滤后
3 2
得到滤渣③为Cu,再向滤液③中加入HF脱钙镁,过滤得到滤渣④为CaF 、MgF ,滤液④为ZnSO 溶液,
2 2 4
经一系列处理得到 ZnSO·7H O,据此分析解答。(1)由分析,焙烧时,生成 ZnO的反应为:ZnCO
4 2 3
ZnO+CO ↑;(2)可采用将焙烧后的产物碾碎,增大接触面积、增大硫酸的浓度等方式提高锌的浸
2
取率;(3)A.NH ·H O易分解产生NH 污染空气,且经济成本较高,故A不适宜;B.Ca(OH) 不会引
3 2 3 2
入新的杂质,且成本较低,故B适宜;C.NaOH会引入杂质Na+,且成本较高,C不适宜;故答案选B;
当沉淀完全时(离子浓度小于10-5mol/L),结合表格Ksp计算各离子完全沉淀时pH<5的只有Fe3+,故滤渣
①中有Fe(OH) ,又CaSO 是微溶物,SiO 不溶于酸,故滤渣①的主要成分是Fe(OH) 、CaSO、SiO;
3 4 2 3 4 2
(4)向80~90℃滤液①中加入KMnO 溶液,可氧化Fe2+,得到Fe(OH) 和MnO 的滤渣②,反应的离子方
4 3 2
程式为3Fe2++MnO -+7H O=3Fe(OH) ↓+MnO↓+5H+;(5)滤液②中加入锌粉,发生反应
4 2 3 2
Zn+Cu2+=Zn2+=Cu,故加入锌粉的目的为置换Cu2+为Cu从而除去;(6)由分析,滤渣④为CaF 、MgF ,
2 2
与浓硫酸反应可得到HF,同时得到的副产物为CaSO、MgSO 。
4 4
【拔高练习】
1.氯化亚铜(CuCl)是一种微溶于水、难溶于乙醇、易被氧化的白色粉末,以黄铜矿(主要成分为CuFeS)为
2
原料制取CuCl的流程如图所示:
已知:在水溶液中存在平衡:CuCl(s)+2Cl-(aq)[CuCl ]2-(aq)。下列说法错误的是( )
3
A.“浸取”后所得浸取液可用来腐蚀铜制电路板
B.加入浓盐酸的目的是为了实现CuCl的净化
C.[CuCl ]2-中加水可使平衡CuCl(s)+2Cl-(aq)[CuCl ]2-(aq)逆向移动
3 3
D.采用乙醇洗涤和真空干燥有利于提高CuCl的产率和纯度
【答案】 A
【解析】 “浸取”后所得浸取液含有FeCl ,FeCl 与Cu单质不能发生反应,因此不可用来腐蚀铜制电路
2 2
资料整理【淘宝店铺:向阳百分百】板,A错误;加入浓盐酸后溶液中的c(Cl-)增大,CuCl(s)+2Cl-(aq)[CuCl ]2-(aq)正向移动,过滤除杂
3
后加水稀释,平衡逆向移动,从而可得纯净的CuCl,故该操作的目的是为了实现CuCl的净化,B、C正确;
乙醇沸点低易挥发,真空中无O 可防止CuCl被氧化,故采用乙醇洗涤和真空干燥有利于提高CuCl的产率
2
和纯度,D正确。
2.(2022·四川广元高三模拟)含铬废水会严重污染环境,一种烟气协同处理含铬废水(含CrO、Cr O、泥沙
2
等)的流程如图:
下列说法不正确的是( )
A.“沉降”的主要目的是除去泥沙等不溶物
B.溶液A通常选用硫酸“调pH”,目的是将CrO转化为Cr O
2
C.“还原”过程涉及的氧化还原反应,氧化剂与还原剂的物质的量之比为2∶3
D.母液经处理可获得 SO
2 4
【答案】 C
【解析】 “沉降”可以除去不溶性物质,主要目的是除去泥沙等不溶物,A正确;Cr O+HO2CrO+
2 2
2H+,加入稀硫酸,氢离子浓度变大,平衡逆向移动,CrO转化为Cr O,B正确;“还原”过程涉及的氧
2
化还原反应,二氧化硫生成硫酸根离子,正六价铬转化为正三价铬,根据得失电子守恒可知,3SO ~
2
Cr O,氧化剂与还原剂的物质的量之比为1∶3,C错误;加入氨水得到Cr(OH) 沉淀和硫酸铵,过滤,母液
2 3
经处理可获得 SO ,D正确。
2 4
3.(2023·银川高三模拟)工业上以碳酸锰矿(主要成分为MnCO ,另含FeO、Fe O 、CaO等杂质)为主要原
3 2 3
料生产锰酸锂(LiMn O),工艺流程如下:
2 4
下列说法错误的是( )
A.可采用搅拌的方法提高“酸浸”时碳酸锰矿的浸出速率
B.加入CaO的目的是调节pH,使Fe3+转化为Fe(OH) 除去
3
C.“合成MnO ”的化学方程式为MnSO +KSO+2HO===MnO↓+KSO +2HSO
2 4 2 2 8 2 2 2 4 2 4
D.“气体1”中含两种气体,一种是CO,另一种可能是CO
2
【答案】 D
【解析】 搅拌可使反应物之间更充分的接触,从而提高“酸浸”时碳酸锰矿的浸出速率,故 A正确;加
入CaO生成氢氧化钙,能使铁离子转化成氢氧化铁沉淀除去,故B正确;“合成MnO ”是硫酸锰作还原剂,
2
KSO 作氧化剂,根据得失电子守恒可得反应:MnSO +KSO +2HO===MnO↓+KSO +2HSO ,故C
2 2 8 4 2 2 8 2 2 2 4 2 4
正确;二氧化锰与碳酸锂混合反应生成LiMn O ,LiMn O 中Mn的化合价有+3价、+4价两种,可知发
2 4 2 4
资料整理【淘宝店铺:向阳百分百】生了氧化还原反应,二氧化锰作氧化剂,则化合价升高的只能是-2价氧元素,故产物中还有氧气,“气
体1”中所含两种气体应为二氧化碳和氧气,故D错误。
4.(2022·陕西延安高三模拟)黏土钒矿(主要成分为钒的+3、+4、+5价的化合物以及SiO、Al O 等)中钒
2 2 3
的化合物溶于酸后多以VO+、VO2+、VO形式存在,采用如图所示工艺流程可由黏土钒矿制备VO。已知:
2 5
VO 在碱性条件下以VO形式存在。下列说法不正确的是( )
2 5
A.“酸浸氧化”中欲使3 mol VO+被氧化成VO,至少需要1 mol KClO
3
B.滤液1中主要的阴离子有AlO、VO、Cl-、OH-、SO
C.“煅烧”时需要的仪器主要有蒸发皿、玻璃棒、三脚架、酒精灯
D.“煅烧”时,NH VO 受热分解:2NH VO =====VO+2NH ↑+HO
4 3 4 3 2 5 3 2
【答案】 C
【解析】 黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括SiO 、Al O 等,加入稀硫酸,使
2 2 3
Al O 生成Al3+;加入KClO 将VO+和VO2+氧化成VO,滤渣1为SiO ,滤液含有VO、K+、Cl-、Al3+、
2 3 3 2
SO;加入KOH溶液至pH>13,滤液1含有K+、AlO、VO、Cl-、OH-、SO,通入CO 生成氢氧化铝沉淀,
2
滤液中加入NH HCO 沉钒得到NH VO ,最后煅烧得到VO。VO+中V元素为+3价,VO中V元素为+5
4 3 4 3 2 5
价,3 mol VO+被氧化成VO,失去6 mol电子,1 mol KClO 变为KCl得到6 mol电子,得失电子守恒,故
3
A正确;由上述分析可知,滤液1中主要的阴离子有AlO、VO、Cl-、OH-、SO,故B正确;“煅烧”时
需要的仪器主要有坩埚、玻璃棒、三脚架、酒精灯、泥三角等,故C错误;NH VO 煅烧生成VO ,化学
4 3 2 5
方程式为2NH VO =====VO+2NH ↑+HO,故D正确。
4 3 2 5 3 2
5.钼酸钠是一种白色结晶性粉末,广泛应用于颜料和化工等领域。工业上用钼精矿(主要成分是 ,含
少量的 )制备钼酸钠晶体( )的简化流程如图所示。下列说法错误的是
已知:浸取液溶质主要为 和 。
A.焙烧时发生反应 B.气体X为 ,废渣的主要成分为
C.从滤液中获得 的操作为蒸发结晶 D.利用纯碱吸收 ,可获得副产品亚硫酸
资料整理【淘宝店铺:向阳百分百】钠
【答案】C
【解析】钼精矿,主要成分是 MoS ,含少量的PbS,在空气中焙烧,MoS 被氧化成MoO ,PbS生成
2 2 3
PbO,S元素变成SO (g),再加入纯碱溶液浸取,得到NaMoO 和NaPbO ,加入NaS,得到PbS而除
2 2 4 2 2 2
去Pb元素,最后将NaMoO 溶液蒸发浓缩,冷却结晶,得到产品NaMoO ·2H O。A.焙烧时,MoS 被氧
2 4 2 4 2 2
化成MoO ,反应的方程式为: ,A正确;B.向溶液中加入纯碱溶液浸取,得
3
到NaMoO 和NaPbO 和CO 气体,再加入NaS,得到PbS而除去Pb元素,B正确;C.NaMoO ·2H O
2 4 2 2 2 2 2 4 2
为含有水分子的结晶水合物,所以将NaMoO 溶液蒸发浓缩,冷却结晶,得到产品NaMoO ·2H O,不能
2 4 2 4 2
直接蒸发结晶,C错误;D.因为HSO >H CO ,可以发生反应:NaCO + SO = NaSO +CO ,所以利
2 3 2 3 2 3 2 2 3 2
用纯碱吸收SO (g),可获得副产品亚硫酸钠,D正确; 故选C。
2
6.(2023春·湖南岳阳·高三岳阳一中校考阶段练习)氨广泛应用于化工、化肥、制药等领域,一种新型合
成方法如图所示。下列说法正确的是
A.反应①属于自然固氮
B.反应③可利用电解 溶液的方法实现
C.该转化过程的总反应为
D.反应①、②、③、④均属于氧化还原反应
【答案】C
【解析】A.反应①属于人工固氮,A错误; B.反应③可利用电解熔融的MgCl 方法实现,B错误;C.
2
该转化过程的总反应为 ,C正确;D.反应②属于非氧化还原反应,D错误;故选
C。
7.(2023秋·黑龙江齐齐哈尔·高三校联考期末)氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业;
CuCl难溶于水和乙醇,潮湿时易水解氧化。工业以硫化铜精矿为原料,设计符合绿色化学理念的制备
CuCl的流程如图:
下列说法错误的是
A.步骤①焙烧产生的有毒气体用NaOH溶液吸收后可用于③的循环利用
资料整理【淘宝店铺:向阳百分百】B.步骤②中可以用硝酸代替硫酸,不影响后续处理
C.步骤③离子方程式:
D.步骤④用乙醇洗涤的目的是使CuCl加速干燥,防止发生水解氧化
【答案】B
【解析】步骤①焙烧产生的气体是 SO ,用NaOH溶液吸收,并产生 NaSO ,该物质可用于③的循环利
2 2 3
用,A正确;若步骤②用硝酸代替硫酸,会有硝酸铜生成,所得溶液中含有的 HNO 有氧化性,不利于
3
CuCl的生成,B错误;步骤③中,Cu2+、Cl-和SO 2-反应产生CuCl沉淀和SO 2-,该反应的离子方程式为
3 4
,C正确;CuCl难溶于水和乙醇,潮湿时易水解氧化,步
骤④用乙醇洗涤的目的是使CuCl加速干燥,防止发生水解氧化,D正确。
8.(2023秋·江西吉安·高三江西省宜丰中学统考期末)化工专家侯德榜发明的侯氏制碱法为我国纯碱工业
和国民经济发展做出了重要贡献。某化学兴趣小组在实验室中模拟侯氏制碱法制备 ,进一步处理
得到产品 和 。实验流程如图:
下列说法正确的是
A.气体N、M分别为 和
B.该流程中只有“食盐水”可以循环使用
C.操作1为过滤,为了加快过滤速率常用玻璃棒搅拌
D.向“母液”中加入NaCl粉末并通入 可得到副产品 ,通入 的目的是增大 的浓度,
有利于析出 并提高纯度
【答案】 D
【解析】 侯氏制碱法的原理为:NaCl + H2O+CO2+NH =NaHCO↓ + NH Cl,NH 极易溶于水,所以
3 3 4 3
资料整理【淘宝店铺:向阳百分百】先通入NH ,有利于CO 的溶解吸收,充分反应后过滤得到固体NaHCO ,NaHCO 受热分解得到碳酸钠、
3 2 3 3
二氧化碳和水,母液的主要溶质为NH Cl,向母液中加入NaCl粉末并通入NH 有利于氯化铵的析出,得到
4 3
纯度更高的NH Cl。A.NH 极易溶于水,所以先通入NH ,有利于CO 的溶解吸收,即气体N、M分别为
4 3 3 2
NH 和CO ,A项错误;B.根据流程可知,NaHCO 受热分解得到的二氧化碳也可以循环使用,B项错误
3 2 3
C.根据分析可知操作1为过滤,过滤时,为了避免滤纸被损坏,不能用玻璃棒搅拌,C项错误;D.向
“ 母 液 ” 中 加 入 NaCl 粉 末 并 通 入 NH 可 得 到 副 产 品 NH Cl , 通 入 NH , 会 发 生 反 应 :
3 4 3
,平衡正向移动,增大了NH +的浓度,有利于析出NH Cl并提高
4 4
纯度,D项正确;答案选D。
9.(2023·天津·校联考一模)合成氨及其衍生工业是化工生产的重要门类,请结合图示判断下列说法不正
确的是
A.合成氨采用400~500℃是为了提高原料转化率和反应速率
B.湿润的淀粉KI试纸不可以鉴别气体2和溴蒸气
C.生成固体1的化学方程式为NaCl+NH +CO +H O=NaHCO ↓+NHCl
3 2 2 3 4
D.1L气体1、2的混合气与1 L NH 在一定条件下转化为对环境无害的物质,混合气中二者的体积比为
3
1∶1
【答案】A
【解析】由图可知:NH3在催化剂条件下与氧气反应生成气体1为NO气体,NO被氧化生成气体2为
NO2气体,NO2气体与水反应生成硝酸,NH3与CO2、H2O、NaCl反应生成固体1为NaHCO3,NaHCO3
受热分解生成固体2为Na2CO3,据此答题。A.合成氨反应为放热反应,温度越低,反应越向着正向移动,
原料的转化率越高,所以400~500℃不利于提高原料的转化率,故A错误;B.由分析可知:气体2为
NO2气体,NO2气体和溴蒸气都有较强的氧化性,都能使淀粉碘化钾试纸变蓝,故B正确;C.固体1为
碳 酸 氢 钠 , 氯 化 钠 、 二 氧 化 碳 、 水 和 氨 气 可 以 生 成 碳 酸 氢 钠 固 体 , 故 方 程 式 为 :
NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl,故C正确;D.由分析可知:气体1为NO,气体2为NO2,
1LNO、NO2 的混合气与 1LNH3 在一定条件下转化为对环境无害的物质,反应方程式为:
资料整理【淘宝店铺:向阳百分百】,NO、NO2的体积比等于化学计量数之比,为1:1,故D正确;故选A。
10.(2023.全国乙卷) LiMn O 作为一种新型锂电池正极材料受到广泛关注。由菱锰矿(MnCO ,含有
2 4 3
少量Si、Fe、Ni、Al等元素)制备LiMn O 的流程如下:
2 4
已知:K [Fe(OH) ]=2.8×10-39,K [Al(OH) ]=1.3×10-33,K [Ni(OH) ]=5.5×10-16。
sp 3 sp 3 sp 2
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为_______。为提高溶矿速率,可采取的措施_______(举1例)。
(2)加入少量MnO 的作用是_______。不宜使用HO 替代MnO ,原因是_______。
2 2 2 2
(3)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)=_______mol·L-1;用石灰乳调节至pH≈7,除去的
金属离子是_______。
(4)加入少量BaS溶液除去Ni2+,生成的沉淀有_______。
(5)在电解槽中,发生电解反应的离子方程式为_______。随着电解反应进行,为保持电解液成分稳定,
应不断_______。电解废液可在反应器中循环利用。
(6)缎烧窑中,生成LiMn O 反应的化学方程式是_______。
2 4
【答案】(1)①. MnCO +H SO =MnSO +H O+CO↑ ②. 粉碎菱锰矿
3 2 4 4 2 2
(2) ①. 将Fe2+氧化为Fe3+ ②. Fe3+可以催化HO 分解
2 2
(3)①. 2.8×10-9 ②. Al3+ (4)BaSO、NiS
4
(5)①. Mn2++2H O H↑+MnO↓+2H+ ②. 加入Mn(OH)
2 2 2 2
(6)2LiCO+8MnO 4LiMn O+2CO ↑+O ↑
2 3 2 2 4 2 2
【解析】根据题给的流程,将菱锰矿置于反应器中,加入硫酸和MnO ,可将固体溶解为离子,将杂质中
2
的Fe、Ni、Al等元素物质也转化为其离子形式,同时,加入的MnO 可以将溶液中的Fe2+氧化为Fe3+;随
2
后将溶液pH调至制约等于7,此时,根据已知条件给出的三种氢氧化物的溶度积可以将溶液中的Al3+沉淀
出来;随后加入BaS,可以将溶液中的Ni2+沉淀,得到相应的滤渣;后溶液中含有大量的 Mn2+,将此溶液
置于电解槽中电解,得到MnO ,将MnO 与碳酸锂共同煅烧得到最终产物LiMn O。
2 2 2 4
资料整理【淘宝店铺:向阳百分百】(1)菱锰矿中主要含有 MnCO ,加入硫酸后可以与其反应,硫酸溶矿主要反应的化学方程式为:
3
MnCO +H SO =MnSO +H O+CO↑ ; 为 提 高 溶 矿 速 率 , 可 以 将 菱 锰 矿 粉 碎 ; 故 答 案 为 :
3 2 4 4 2 2
的
MnCO +H SO =MnSO +H O+CO↑、粉碎菱锰矿。(2)根据分析,加入MnO 作用是将酸溶后溶液中含
3 2 4 4 2 2 2
有的Fe2+氧化为Fe3+,但不宜使用HO 氧化Fe2+,因为氧化后生成的Fe3+可以催化HO 分解,不能使溶液
2 2 2 2
中的Fe2+全部氧化为Fe3+;故答案为:将Fe2+氧化为Fe3+、Fe3+可以催化HO 分解。(3)溶矿完成以后,
2 2
反应器中溶液 pH=4,此时溶液中 c(OH-)=1.0×10-10mol·L-1,此时体系中含有的 c(Fe3+)=
=2.8×10-9mol·L-1,这时,溶液中的c(Fe3+)小于1.0×10-5,认为Fe3+已经沉淀完全;用石灰乳调节至pH≈7,
这时溶液中 c(OH-)=1.0×10-7mol·L-1,溶液中 c(Al3+)=1.3×10-12mol·L-1,c(Ni2+)=5.5×10-4mol·L-1,c(Al3+)小于
1.0×10-5,Al3+沉淀完全,这一阶段除去的金属离子是Al3+;故答案为:2.8×10-9、Al3+。(4)加入少量BaS
溶液除去Ni2+,此时溶液中发生的离子方程式为 BaS+Ni2++SO2-=BaSO ↓+NiS↓,生成的沉淀有BaSO 、
4 4 4
NiS。(5)在电解槽中,Mn2+发生反应生成 MnO ,反应的离子方程式为 Mn2++2H O
2 2
H↑+MnO↓+2H+;电解时电解液中Mn2+大量减少,H+大量增加,需要加入Mn(OH) 以保持电解液成分的稳
2 2 2
定;故答案为:Mn2++2H O H↑+MnO↓+2H+、加入Mn(OH) 。
2 2 2 2
(6)煅烧窑中 MnO 与 LiCO 发生反应生成 LiMn O ,反应的化学方程式为 2LiCO+8MnO
2 2 3 2 4 2 3 2
4LiMn O+2CO ↑+O ↑;故答案为:2LiCO+8MnO 4LiMn O+2CO ↑+O ↑。
2 4 2 2 2 3 2 2 4 2 2
11.(2023.课标I卷)铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、
铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:
已知:最高价铬酸根在酸性介质中以Cr O 存在,在碱性介质中以CrO 存在。
2
回答下列问题:
资料整理【淘宝店铺:向阳百分百】(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为___________(填化学
式)。
(2)水浸渣中主要有SiO 和___________。
2
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是___________。
(4)“除硅磷”步骤中,使硅、磷分别以MgSiO 和MgNH PO 的形式沉淀,该步需要控制溶液的pH≈9
3 4 4
以达到最好的除杂效果,若pH<9时,会导致___________;pH>9时,会导致___________。
(5)“分离钒”步骤中,将溶液pH调到1.8左右得到VO 沉淀,VO 在pH<1时,溶解为VO 或
2 5 2 5
VO3+在碱性条件下,溶解为VO 或VO ,上述性质说明VO 具有___________(填标号)。
2 5
A.酸性 B.碱性 C.两性
(6)“还原”步骤中加入焦亚硫酸钠(Na SO)溶液,反应的离子方程式为___________。
2 2 5
【答案】(1)NaCrO (2)Fe O (3)Al(OH)
2 4 2 3 3
(4)①. 磷酸根会与H+反应使其浓度降低导致MgNH PO 无法完全沉淀,同时可能产生硅酸胶状沉淀不
4 4
宜处理 ②. 会导镁离子生成氢氧化镁沉淀,不能形成MgSiO 沉淀,导致产品中混有杂质,同时溶液中
3
铵根离子浓度降低导致MgNH PO 无法完全沉淀 (5)C (6)2Cr O2-+3S O2-+10H+=4Cr3++6SO2-
4 4 2 7 2 5 4
+5H O
2
【解析】由题给流程可知,铬钒渣在氢氧化钠和空气中煅烧,将钒、铬、铝、硅、磷等元素转化为相应的
最高价含氧酸盐,煅烧渣加入水浸取、过滤得到含有二氧化硅、氧化铁的滤渣和滤液;向滤液中加入稀硫
酸调节溶液pH将Al元素转化为氢氧化铝沉淀,过滤得到强氧化铝滤渣和滤液;向滤液中加入硫酸镁溶液、
硫酸铵溶液将硅元素、磷元素转化为MgSiO 和MgNH PO 沉淀,过滤得到含有MgSiO 、MgNH PO 的滤
3 4 4 3 4 4
渣和滤液;向滤液中加入稀硫酸调节溶液 pH将钒元素转化为五氧化二钒,过滤得到五氧化二钒和滤液;
向滤液中焦亚硫酸钠溶液将铬元素转化为三价铬离子,调节溶液 pH将铬元素转化为氢氧化铬沉淀,过滤
得到氢氧化铬。(1)由分析可知,煅烧过程中,铬元素转化为铬酸钠,故答案为:NaCrO ;(2)由分
2 4
析可知,水浸渣中主要有二氧化硅、氧化铁,故答案为:Fe O;(3)由分析可知,沉淀步骤调pH到弱碱
2 3
性的目的是将Al元素转化为氢氧化铝沉淀,故答案为:Al(OH) ;(4)由分析可知,加入硫酸镁溶液、硫
3
酸铵溶液的目的是将硅元素、磷元素转化为 MgSiO 和MgNH PO 沉淀,若溶液pH<9时,磷酸根会与
3 4 4
H+反应使其浓度降低导致MgNH PO 无法完全沉淀,同时可能产生硅酸胶状沉淀不宜处理;若溶液 pH>9
4 4
时,会导镁离子生成氢氧化镁沉淀,不能形成MgSiO 沉淀,导致产品中混有杂质,同时溶液中铵根离子
3
浓度降低导致MgNH PO 无法完全沉淀,故答案为:磷酸根会与H+反应使其浓度降低导致MgNH PO ,同
4 4 4 4
资料整理【淘宝店铺:向阳百分百】时可能产生硅酸胶状沉淀不宜处理;会导镁离子生成氢氧化镁沉淀,不能形成 MgSiO 沉淀,导致产品中
3
混有杂质,同时溶液中铵根离子浓度降低导致 MgNH PO 无法完全沉淀;(5)由题给信息可知,五氧化
4 4
二钒水能与酸溶液反应生成盐和水,也能与碱溶液发生生成盐和水的两性氧化物,故选C;(6)由题意可
知,还原步骤中加入焦亚硫酸钠溶液的目的是将铬元素转化为铬离子,反应的离子方程式为 2Cr O2-
2 7
+3S O2-+10H+=4Cr3++6SO2-+5H O,故答案为:2Cr O2-+3S O2-+10H+=4Cr3++6SO2-+5H O。
2 5 4 2 2 7 2 5 4 2
资料整理【淘宝店铺:向阳百分百】