文档内容
第 15 讲 碳、硅及无机非金属材料
目录
考情分析 知识点3 硅酸
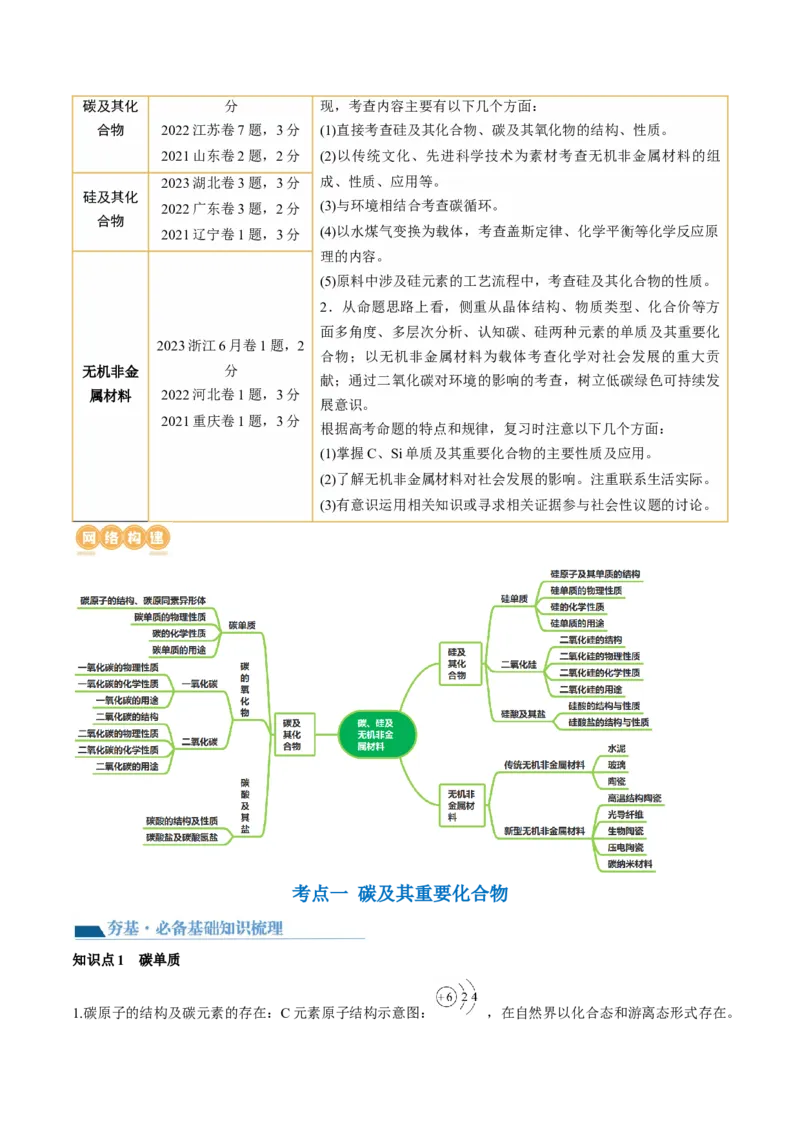
网络构建 知识点4 硅酸盐
知识点5 碳、硅及其化合物性质“反常”小
考点一 碳及其化合物
结
【夯基·必备基础知识梳理】
【提升·必考题型归纳】
知识点1 碳单质
考向1 考查硅、二氧化硅的性质及其应用
知识点2 碳的氧化物
考向2 考查硅的制备
知识点3 碳酸、碳酸盐
考向3 考查硅酸、硅酸盐的性质及其应用
知识点4 碳元素在自然界中的循环
考点三 无机非金属材料
知识点5 CO 与碱、盐溶液的反应规律
2
【提升·必考题型归纳】 【夯基·必备基础知识梳理】
考向1 考查碳及及其化合物性质和应用 知识点1 传统无机非金属材料
考向2 考查CO 与碱反应图像分析 知识点2 新型无机非金属材料
2
考向3 考查碳元素在自然界中的循环 【提升·必考题型归纳】
考向1 考查传统无机非金属材料的分类和
考点二 硅及基化合物
应用
【夯基·必备基础知识梳理】
考向2 考查传统无机非金属材料的分类和
知识点1 单质硅
应用
知识点2 二氧化硅
真题感悟
考点要求 考题统计 考情分析
分析近三年高考试题,高考命题在本讲有以下规律:
2023浙江1月卷7题,2
1.从考查题型和内容上看,高考命题以选择题和非选择题呈碳及其化 分 现,考查内容主要有以下几个方面:
合物 2022江苏卷7题,3分 (1)直接考查硅及其化合物、碳及其氧化物的结构、性质。
2021山东卷2题,2分 (2)以传统文化、先进科学技术为素材考查无机非金属材料的组
2023湖北卷3题,3分 成、性质、应用等。
硅及其化
2022广东卷3题,2分 (3)与环境相结合考查碳循环。
合物
2021辽宁卷1题,3分 (4)以水煤气变换为载体,考查盖斯定律、化学平衡等化学反应原
理的内容。
(5)原料中涉及硅元素的工艺流程中,考查硅及其化合物的性质。
2.从命题思路上看,侧重从晶体结构、物质类型、化合价等方
面多角度、多层次分析、认知碳、硅两种元素的单质及其重要化
2023浙江6月卷1题,2
合物;以无机非金属材料为载体考查化学对社会发展的重大贡
无机非金 分
献;通过二氧化碳对环境的影响的考查,树立低碳绿色可持续发
属材料 2022河北卷1题,3分
展意识。
2021重庆卷1题,3分
根据高考命题的特点和规律,复习时注意以下几个方面:
(1)掌握C、Si单质及其重要化合物的主要性质及应用。
(2)了解无机非金属材料对社会发展的影响。注重联系生活实际。
(3)有意识运用相关知识或寻求相关证据参与社会性议题的讨论。
考点一 碳及其重要化合物
知识点1 碳单质
1.碳原子的结构及碳元素的存在:C元素原子结构示意图: ,在自然界以化合态和游离态形式存在。2.常见碳单质的结构和物理性质
常见的碳单质有金刚石、石墨、无定形碳、足球烯、碳纳米管等,它们互为_________。
3.碳单质化学性质
a.与O 的反应(用化学方程式表示):
2
①O 不足:2C+O=====2CO;
2 2
②O 充足:C+O=====CO。
2 2 2
b.与氧化物反应(用化学方程式表示):
①与CuO反应:__________________;
②与Fe O 反应:__________________;
2 3
③与CO 反应:__________________;
2
④与水蒸气反应:_________ _________ (制水煤气);
⑤与SiO 反应:_________ _________ (制粗硅);_________ _________ (制金刚砂)
2
c.与强氧化性酸反应
①与浓硫酸反应:__________________。
②与浓硝酸反应:__________________。
4.碳单质的用途:
①金刚石结构坚硬,作玻璃刻刀、机器钻头、装饰品等;
②石墨的细鳞片状结构质软、导电性、滑腻性、耐高温 铅笔芯、电极、润滑剂、坩埚;
③木炭和活性炭的疏松多孔的结构吸附性吸附食品色素、除臭、防毒面具、冰箱除味剂等;
④作燃料,用于家庭取暖、做饭等;
⑤作还原剂:冶炼金属,如冶炼金属铜、铁等。
知识点2 碳的氧化物CO和CO
2
1.碳的氧化物的物理性质
色态味 密度(比空气) 水溶性 毒性 相互转化
CO 无色、无 小 难溶 有(易结合血红蛋白)
CO 味、气体 大 能溶 无(温室效应)
22.碳的氧化物的化学性质
①CO具有较强的还原性,可以与O、金属氧化物等发生反应。
2
如与Fe O 反应:Fe O+3CO=====2Fe+3CO。
2 3 2 3 2
②CO 是典型的酸性氧化物,也具有氧化性。
2
a.酸性氧化物
①与水反应:CO+HO HCO
2 2 2 3
②与碱反应:CO 少量:CO+2NaOH===Na CO+HO;CO 足量:CO+NaOH===NaHCO
2 2 2 3 2 2 2 3
③与碱性氧化物反应:CO+CaO=CaCO
2 3
④与Ca(ClO) 盐溶液反应:___________________________(CO 少量);
2 2
___________________________(CO 过量);
2
b.氧化性
①与C反应:CO+C 2CO;
2
②与Mg反应:2Mg+CO 2MgO+C
2
【特别提醒】溶液中通入CO 气体产生沉淀的问题:向BaCl 或CaCl 溶液中通入CO 气体,由于盐酸的酸
2 2 2 2
性比碳酸的强,不会产生BaCO 或CaCO 沉淀。
3 3
3.CO、CO 气体的除杂方法
2
CO中混有CO 通过盛有_________溶液的洗气瓶,然后干燥气体
2
CO 中混有CO 通过盛有灼热_________的硬质玻璃管
2
CO 中混有O 通过盛放灼热_________网的硬质玻璃管
2 2
通过盛有饱和_________溶液或酸性_________溶液的洗气瓶,然后干燥
CO 中混有少量SO
2 2
气体
CO 中混有少量HCl 通过盛有_________溶液的洗气瓶,然后干燥气体
2
【易错提醒】①澄清石灰水只用于检验CO,不能用于除去混合气体中的CO,应用NaOH溶液除去;
2 2
②CO、SO 通入CaCl 或BaCl 溶液均无沉淀产生。
2 2 2 2
知识点3 碳酸和碳酸盐
1.碳酸
二元弱酸、不稳定,常用CO+HO代替HCO,但酸性比苯酚、次氯酸_________。
2 2 2 3
2.碳酸的正盐和酸式盐的比较
正盐(CO) 酸式盐(HCO)
溶解性 只有钾、钠、铵盐可溶 一般都可溶
热稳定性 正盐>酸式盐溶液pH 同浓度:正盐>酸式盐
相互转化
CO HCO
知识点4 碳元素在自然界中的循环
1.CO 的主要来源:大量含碳燃料的燃烧。
2
2.自然界消耗CO 的主要反应:
2
a.溶于江水、海水中:CO+HO HCO;
2 2 2 3
b.光合作用将CO 转化为O;
2 2
c.岩石的风化:CaCO +HO+CO===Ca(HCO)。
3 2 2 3 2
知识点5 CO 与碱、盐溶液的反应规律
2
1、与碱溶液的反应
(1)反应原理
NaOH――→NaCO――→NaHCO
2 3 3
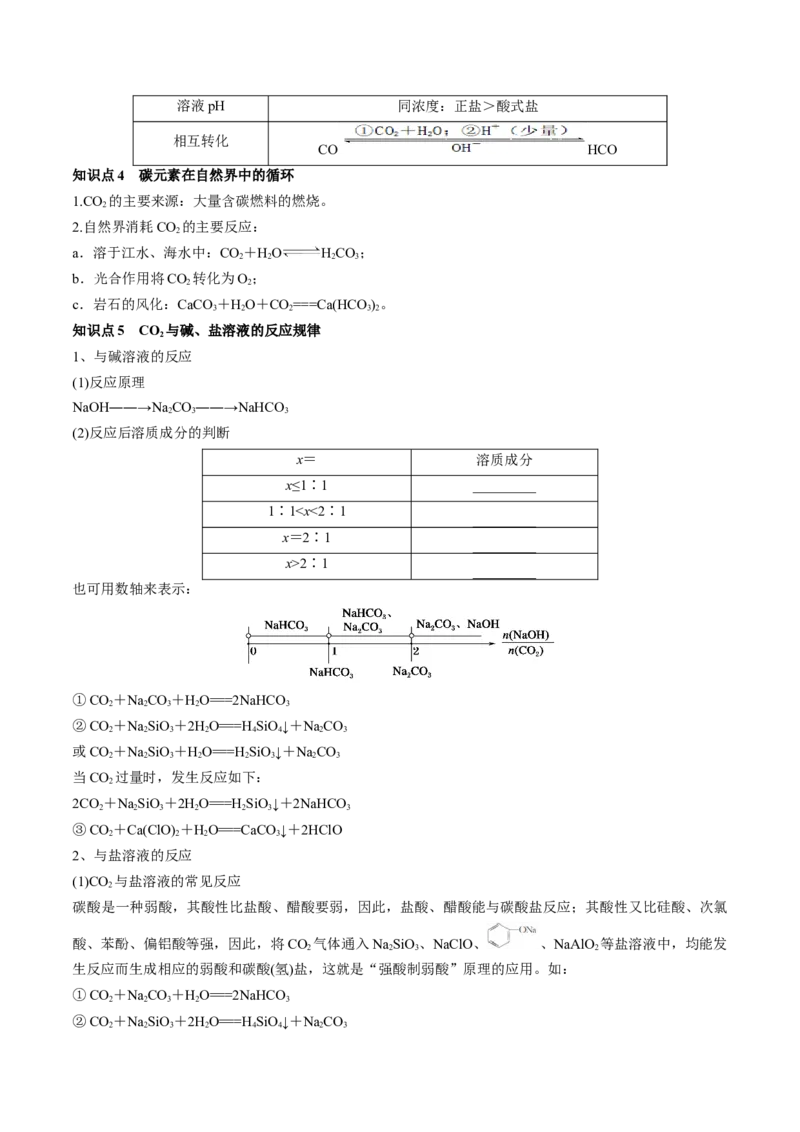
(2)反应后溶质成分的判断
x= 溶质成分
x≤1∶1 _________
1∶12∶1
_________
也可用数轴来表示:
①CO+NaCO+HO===2NaHCO
2 2 3 2 3
②CO+NaSiO+2HO===H SiO↓+NaCO
2 2 3 2 4 4 2 3
或CO+NaSiO+HO===H SiO↓+NaCO
2 2 3 2 2 3 2 3
当CO 过量时,发生反应如下:
2
2CO+NaSiO+2HO===H SiO↓+2NaHCO
2 2 3 2 2 3 3
③CO+Ca(ClO) +HO===CaCO ↓+2HClO
2 2 2 3
2、与盐溶液的反应
(1)CO 与盐溶液的常见反应
2
碳酸是一种弱酸,其酸性比盐酸、醋酸要弱,因此,盐酸、醋酸能与碳酸盐反应;其酸性又比硅酸、次氯
酸、苯酚、偏铝酸等强,因此,将CO 气体通入NaSiO、NaClO、 、NaAlO 等盐溶液中,均能发
2 2 3 2
生反应而生成相应的弱酸和碳酸(氢)盐,这就是“强酸制弱酸”原理的应用。如:
①CO+NaCO+HO===2NaHCO
2 2 3 2 3
②CO+NaSiO+2HO===H SiO↓+NaCO
2 2 3 2 4 4 2 3或CO+NaSiO+HO===H SiO↓+NaCO
2 2 3 2 2 3 2 3
当CO 过量时,发生反应如下:
2
2CO+NaSiO+2HO===H SiO↓+2NaHCO
2 2 3 2 2 3 3
③CO+Ca(ClO) +HO===CaCO ↓+2HClO
2 2 2 3
当CO 过量时,发生反应如下:
2
2CO+Ca(ClO) +2HO===Ca(HCO )+2HClO
2 2 2 3 2
④CO+ +HO―→ +NaHCO
2 2 3
⑤CO+NaAlO +2HO===Al(OH) ↓+NaHCO (CO 过量时)
2 2 2 3 3 2
CO+2NaAlO +3HO===2Al(OH) ↓+NaCO(CO 少量时)
2 2 2 3 2 3 2
(2)注意事项
①“强酸制弱酸”是一个重要的化学反应规律,但不可认为弱酸就不能“制取”强酸。在某些条件下,当
弱酸的酸根阴离子被沉淀或被氧化后,H+就被“释放”出来,从而生成了强酸。如将HS通入CuSO 溶液
2 4
中或向氢硫酸中滴加氯水,均由氢硫酸这种弱酸生成了强酸:HS+CuSO ===CuS↓+HSO (S2-与Cu2+结
2 4 2 4
合成难溶的CuS),HS+Cl===S↓+2HCl(S2-被氧化)。
2 2
② CO 与 溶液反应的产物与 CO 的用量无关,都生成 NaHCO ,因为酸性 HCO>
2 2 3 2 3
>HCO。
③CO 与NaClO溶液反应的产物与CO 的量无关,也只能生成NaHCO ,不能生成NaCO ,因为酸性
2 2 3 2 3
HCO>HClO>HCO。
2 3
④CO、SO 通入CaCl 或BaCl 溶液均不反应,无沉淀产生。
2 2 2 2
考向1 考查碳及及其化合物性质和应用
例1.(2023·广东梅州·统考二模)为了获得良好的草酸酯加氢的催化效果,通常需要保持铜催化剂中Cu0
和Cu+的组成相对稳定,将C 作为电子缓冲剂,通过中性碳团簇(C )与负离子(C )的切换可有效地稳定铜
60 60
催化剂中Cu0和Cu+的比例。下列说法正确的是
A.C 是新型化合物
60
B.当1molC 转变为C 时,失去60mol电子
60
C.当C 转变为C 时,铜催化剂中Cu0和Cu+的个数比减小
60
D.草酸酯催化加氢过程中,需要不断补充C
60
【变式训练1】(2023·全国·高三专题练习)科学家发现了纯碳新材料“碳纳米泡沫”,每个泡沫含有约
4000个碳原子,直径约6~9nm,在低于-183℃时,泡沫具有永久磁性。下列叙述错误的是
A.“碳纳米泡沫”与石墨互为同素异形体
B.把“碳纳米泡沫”分散到适当的溶剂中能产生丁达尔现象
C.“碳纳米泡沫”是一种新型的碳单质
D.“碳纳米泡沫”和金刚石的性质相同【变式训练2】(2023·山东济南·统考三模)下列关于“碳”的说法错误的是
A.自然界中的14C来自宇宙射线(中子)撞击14N,其过程可表示为
B.高压下制得的CO 共价晶体结构与SiO 晶体相似,其硬度和熔沸点均高于SiO 晶体
2 2 2
C.石墨烯、石墨炔都是全碳二维平面结构材料,二者碳原子杂化方式完全相同
D.用风能、光能等清洁能源代替煤和石油,有利于实现“双碳”目标
考向2 CO 与碱反应图像分析
2
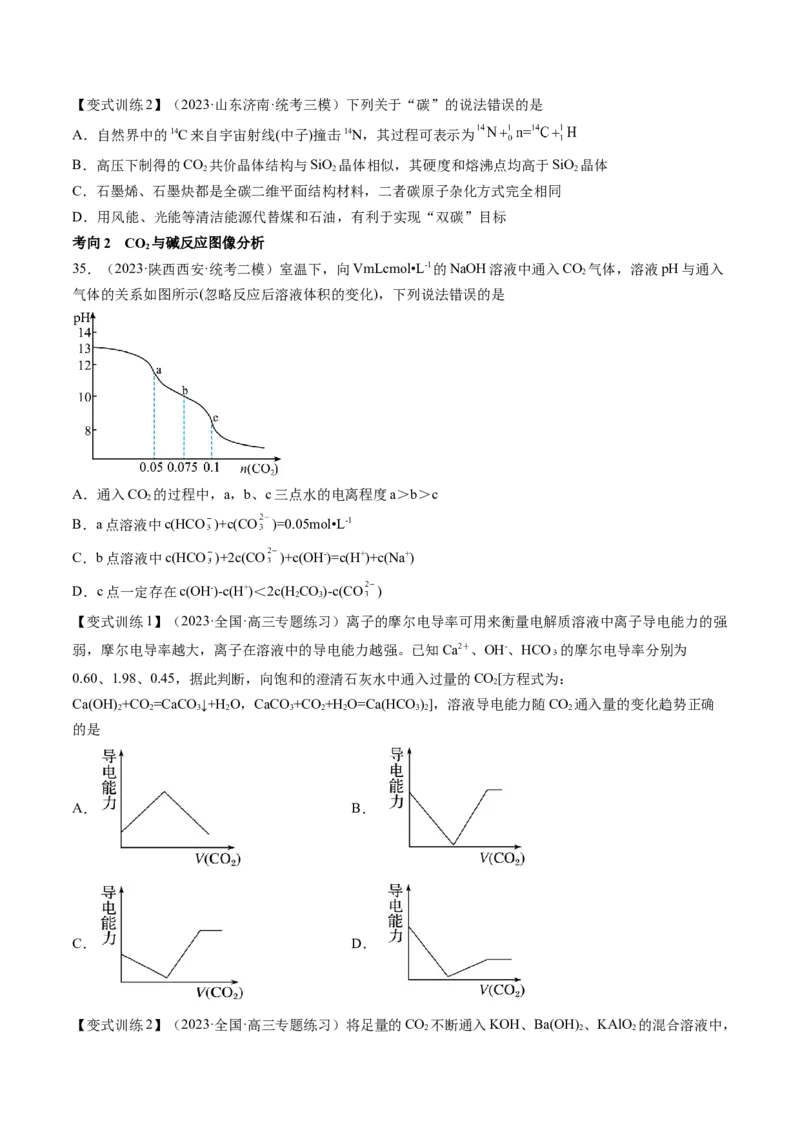
35.(2023·陕西西安·统考二模)室温下,向VmLcmol•L-1的NaOH溶液中通入CO 气体,溶液pH与通入
2
气体的关系如图所示(忽略反应后溶液体积的变化),下列说法错误的是
A.通入CO 的过程中,a,b、c三点水的电离程度a>b>c
2
B.a点溶液中c(HCO )+c(CO )=0.05mol•L-1
C.b点溶液中c(HCO )+2c(CO )+c(OH-)=c(H+)+c(Na+)
D.c点一定存在c(OH-)-c(H+)<2c(HCO)-c(CO )
2 3
【变式训练1】(2023·全国·高三专题练习)离子的摩尔电导率可用来衡量电解质溶液中离子导电能力的强
弱,摩尔电导率越大,离子在溶液中的导电能力越强。已知Ca2+、OH-、HCO 的摩尔电导率分别为
0.60、1.98、0.45,据此判断,向饱和的澄清石灰水中通入过量的CO[方程式为:
2
Ca(OH) +CO =CaCO ↓+H O,CaCO +CO +H O=Ca(HCO )],溶液导电能力随CO 通入量的变化趋势正确
2 2 3 2 3 2 2 3 2 2
的是
A. B.
C. D.
【变式训练2】(2023·全国·高三专题练习)将足量的CO 不断通入KOH、Ba(OH) 、KAlO 的混合溶液中,
2 2 2生成沉淀的物质的量与所通入CO 的体积关系如图所示.下列关于整个反应过程中的叙述不正确的是
2
A.Oa段反应的化学方程式是Ba(OH) +CO ═BaCO↓+H O
2 2 3 2
B.ab段与cd段所发生的反应相同
C.de段沉淀减少是由于BaCO 固体消失
3
D.bc段反应的离子方程式是2AlO﹣+3H O+CO═2Al(OH)↓+CO 2﹣
2 2 2 3 3
考向3 考查碳元素在自然界中的循环的应用
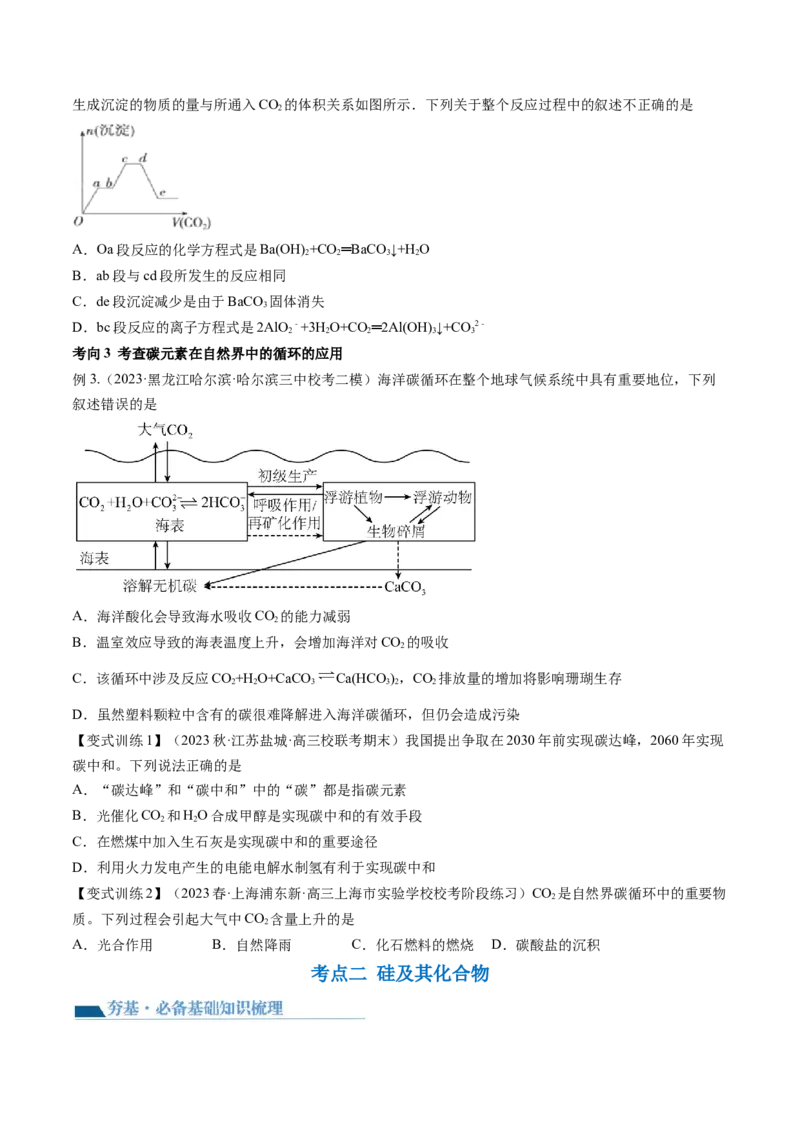
例3.(2023·黑龙江哈尔滨·哈尔滨三中校考二模)海洋碳循环在整个地球气候系统中具有重要地位,下列
叙述错误的是
A.海洋酸化会导致海水吸收CO 的能力减弱
2
B.温室效应导致的海表温度上升,会增加海洋对CO 的吸收
2
C.该循环中涉及反应CO+H O+CaCO Ca(HCO ),CO 排放量的增加将影响珊瑚生存
2 2 3 3 2 2
D.虽然塑料颗粒中含有的碳很难降解进入海洋碳循环,但仍会造成污染
【变式训练1】(2023秋·江苏盐城·高三校联考期末)我国提出争取在2030年前实现碳达峰,2060年实现
碳中和。下列说法正确的是
A.“碳达峰”和“碳中和”中的“碳”都是指碳元素
B.光催化CO 和HO合成甲醇是实现碳中和的有效手段
2 2
C.在燃煤中加入生石灰是实现碳中和的重要途径
D.利用火力发电产生的电能电解水制氢有利于实现碳中和
【变式训练2】(2023春·上海浦东新·高三上海市实验学校校考阶段练习)CO 是自然界碳循环中的重要物
2
质。下列过程会引起大气中CO 含量上升的是
2
A.光合作用 B.自然降雨 C.化石燃料的燃烧 D.碳酸盐的沉积
考点二 硅及其化合物知识点1 单质硅
1.硅的存在、结构与物理性质
(1)存在:单质硅有_________硅和_________硅两大类,自然界中无游离态硅——单质硅,硅以化合态存在,
主要以二氧化硅和硅酸盐的形式存在地壳中,含量仅次于氧,位列第二。
(2)单质硅结构:硅元素原子序数为14,基态原子的简化电子排布式为[Ne]_3s23p2,核外电子的空间运动状
态有8种,不成对电子数有2个;单晶硅为共价晶体,晶体中每个Si原子以sp3杂化,分别与4个相邻的
Si 原子形成4个σ键,Si原子的配位数为4,晶体中最小的环是6元环,1个环中平均含有0.5 Si原子,含
Si—Si键数为1。
(2)物理性质:灰黑色固体,有金属光泽,熔、沸点高,硬度大,有脆性,是常见的半导体材料和合金材料。
金刚石、晶体硅、碳化硅中熔点从高到低的顺序是金刚石、碳化硅、晶体硅。
2.单质硅化学性质
a.常温
①与氢氟酸反应的化学方程式:Si+4HF===SiF ↑+2H ↑;
4 2
②与NaOH溶液反应的化学方程式:Si+2NaOH+H O===Na SiO +2H ↑;
2 2 3 2
③与F 反应的化学方程式:Si+2F ===SiF
2 2 4
b.高温
①与O 反应:Si+O SiO 。
2 2 2
②与Cl 反应:Si+Cl SiCl
2 2 4
3.单质硅的工业制法
①原料:石英砂和焦炭
②制备:SiO+2C=====Si(粗)+2CO↑
2
③提纯:Si(粗)+2Cl SiCl ;SiCl +2H Si(纯)+4HCl
2 4 4 2
【特别提醒】①用焦炭还原SiO,产物是CO而不是CO。
2 2
②粗硅中含碳等杂质,与Cl 反应生成的SiCl 中含有CCl 等杂质,经过分馏提纯SiCl 后,再用H 还原,
2 4 4 4 2
得到高纯度硅。
4.单质硅的用途:半导体材料、太阳能电池、计算机芯片和耐酸设备等。
知识点2 二氧化硅
1.存在:硅石、石英、水晶、玛瑙、沙子等
2.二氧化硅的结构特点
在SiO 晶体中,每个Si周围结合4个O,Si在中心,O在4个顶角;许多这样的 四面体又通
2
过顶角的O相连接,每个O为两个四面体所共有,即每个O与2个Si相结合。实际上,SiO 晶体是由Si
2
和O按1∶2的比例所组成的立体网状结构的晶体。由结构可知,二氧化硅的化学性质很稳定。
3.物理性质:熔点高,硬度大,不溶于水
4.化学性质:a.酸性氧化物
①与碱反应: ___________________________;
②与CaO碱性氧化物反应:____________________________________;
③与盐反应:SiO+NaCO NaSiO+CO↑;SiO+CaCO CaSiO+CO↑(工业制玻璃)
2 2 3 2 3 2 2 3 3 2
b.氧化性:
①与碳反应:__________________ (制粗硅);SiO+3C SiC+2CO↑(制金刚砂);
2
②与Mg反应:4Mg+SiO 2MgSi+2MgO;MgSi+2HO=SiH↑+2Mg(OH) (制硅化氢);
2 2 2 2 4 2
c.特性:
与氢氟酸反应:___________________________
5.用途
①水晶可用于电子工业的部件、光学仪器、工艺品
②SiO 是制光导纤维的重要原料
2
③较纯的石英用于制造石英玻璃
④石英砂用于制玻璃的原料及建筑材料
【特别提醒】(1)由于玻璃的成分中含有SiO,故实验室盛放碱液的试剂瓶用橡皮塞而不用玻璃塞。
2
(2)未进行磨砂处理的玻璃,在常温下是不易被强碱腐蚀的。
(3)因为氢氟酸腐蚀玻璃,与玻璃中的SiO 反应,所以氢氟酸不能用玻璃瓶保存,而应保存在塑料瓶或
2
铅皿中。
(4)SiO 是HSiO 的酸酐,但SiO 不与水反应,不能用SiO 直接与水作用制备HSiO。
2 2 3 2 2 2 3
知识点3 硅酸
1.物理性质:硅酸是一种_________色胶状物质,_________溶于水,能形成胶体。新制备的硅酸为透明、
胶冻状,硅酸经干燥脱水形成硅酸干凝胶——“硅胶”。
2.化学性质:
a.弱酸性:硅酸的酸性很弱,比碳酸的酸性还弱,在与碱反应时只能与强碱反应。如 :
____________________________________。
b.不稳定性:硅酸的热稳定性很差,受热分解为SiO 和HO:HSiO=====SiO+HO。
2 2 2 3 2 2
3.制备:
由于SiO 不溶于水,所以硅酸是通过可溶性硅酸盐与其他酸反应制得的。
2
NaSiO+2HCl==H SiO↓+2NaCl,
2 3 2 3
NaSiO+CO +H O==H SiO↓+Na CO(证明酸性:HCO>HSiO)。
2 3 2 2 2 3 2 3 2 3 2 3
4.用途:硅胶可作催化剂的载体和袋装食品、瓶装药品的干燥剂。
知识点4 硅酸盐
1.概念:由_________和金属组成的化合物的总称,是构成地壳岩石的主要成分。
2.硅酸盐的氧化物表示方法——常用氧化物的形式表示:
氧化物的书写顺序:活泼金属氧化物→较活泼金属氧化物→二氧化硅→水,不同氧化物间以“·”隔开。
如硅酸钠(Na SiO)可表示为NaO·SiO ,长石(KAlSi O)可表示为KO·Al O·6SiO。
2 3 2 2 3 8 2 2 3 2【特别提醒】(1)氧化物之间以“· ”隔开;(2)计量数配置出现分数应化为整数。硅酸盐改写为氧化物
形式时,各元素的化合价保持不变,且满足化合价代数和为零,各元素原子个数比符合原来的组成。当系
数配置出现分数时一般应化为整数。如上例中KAlSi O,将KO·Al O·3SiO,要写成KO·Al O·6SiO。
3 8 2 2 3 2 2 2 3 2
3.硅酸钠(Na SiO)——又称泡花碱
2 3
①物理性质:白色、可溶于水的粉末状固体,其水溶液俗称_________,有黏性,水溶液显碱性。
②化学性质——与酸性较硅酸强的酸反应:
a.与盐酸反应的化学方程式:
NaSiO+2HCl===2NaCl+HSiO↓。
2 3 2 3
b.与CO 水溶液反应的化学方程式:
2
NaSiO+HO+CO===Na CO+HSiO↓。
2 3 2 2 2 3 2 3
③用途:黏合剂(矿物胶)、防腐剂和耐火阻燃材料。
【特别提醒】①NaSiO 的水溶液是一种黏合剂,是制备硅胶和木材防火剂等的原料;NaSiO 易与空气中
2 3 2 3
的CO、HO反应,要密封保存。
2 2
②可溶性碳酸盐、硅酸盐的水溶液呈碱性,保存该溶液的试剂瓶不能用玻璃塞,应用橡胶塞。
知识点5 碳、硅及其化合物性质“反常”小结
1.一般情况下,非金属元素单质熔、沸点低,硬度小,但晶体硅、金刚石熔、沸点高,硬度大,其中金刚
石为自然界中硬度最大的物质。
2.一般情况下,非金属单质为绝缘体,但硅为半导体,石墨为电的良导体。
3.Si的还原性强于C,但C在高温下能还原出Si:SiO+2C=====Si+2CO↑。
2
4.非金属单质与碱反应一般既作氧化剂又作还原剂,且无氢气放出,但硅与强碱溶液反应只作还原剂,且
放出氢气:Si+2NaOH+HO===Na SiO+2H↑。
2 2 3 2
5.非金属单质一般不与非氧化性酸反应,但硅能跟氢氟酸反应:Si+4HF===SiF ↑+2H↑。
4 2
6.一般情况下,碱性氧化物+酸―→盐+水,二氧化硅是酸性氧化物,却能与氢氟酸反应:SiO +
2
4HF===SiF ↑+2HO(SiF 不属于盐,故SiO 不是两性氧化物)。
4 2 4 2
7.一般情况下,无机酸能溶于水,但硅酸却难溶于水。
8.一般情况下,较强酸+较弱酸的盐―→较弱酸+较强酸的盐(溶液中的反应)。
因碳酸的酸性强于硅酸,所以水玻璃在空气中易变质:NaSiO+HO+CO===Na CO+HSiO(胶体)。
2 3 2 2 2 3 2 3
但在高温下,可发生反应NaCO+SiO=====NaSiO+CO↑(CO 离开反应体系促进反应的正向进行)。
2 3 2 2 3 2 2
9.一般情况下,金属(Na、K)能置换出水中的氢,但 C 在高温下也能置换出 HO 中的氢:C+
2
HO(g)=====H+CO。
2 2
10.一般情况下,酸性氧化物与水反应生成相应的含氧酸,但二氧化硅不溶于水,也不与水反应。
考向1 考查硅、二氧化硅的性质及其应用
例1.(2023·全国·高三专题练习)下列有关硅及其化合物的说法正确的是
A.在粗硅的制取中发生反应 ,硅被还原,所以碳的还原性大于硅的B.硅酸钠属于盐,不属于碱,所以硅酸钠可以保存在带磨口玻璃塞的试剂瓶中
C.用 制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后通入
D.由 可知,硅酸的酸性大于碳酸的
【变式训练】(2022·全国·高三专题练习)硅是构成无机非金属材料的一种主要元素,下列有关硅及其化
合物的叙述错误的是
A.氮化硅陶瓷是一种高温结构陶瓷,其化学式为Si N
3 4
B.高纯硅可以制成计算机、通信设备等的芯片
C.硅可以用来生产新型无机非金属材料——光导纤维
D.二氧化硅为立体网状结构,每个硅原子结合4个氧原子
考向2 考查硅的制备
例2.(2023·海南海口·统考模拟预测)设 为阿伏加德罗常数的值。工业上制备高纯度硅的反应有:
①
②
③
已知:H、Si的电负性依次为2.1、1.8.下列有关说法正确的是
A.①中,30g氧化剂含极性键数目为 B.②中,生成1g 时转移电子数为
C.②和③互为可逆反应 D.②和③的目的是除去粗硅中的杂质
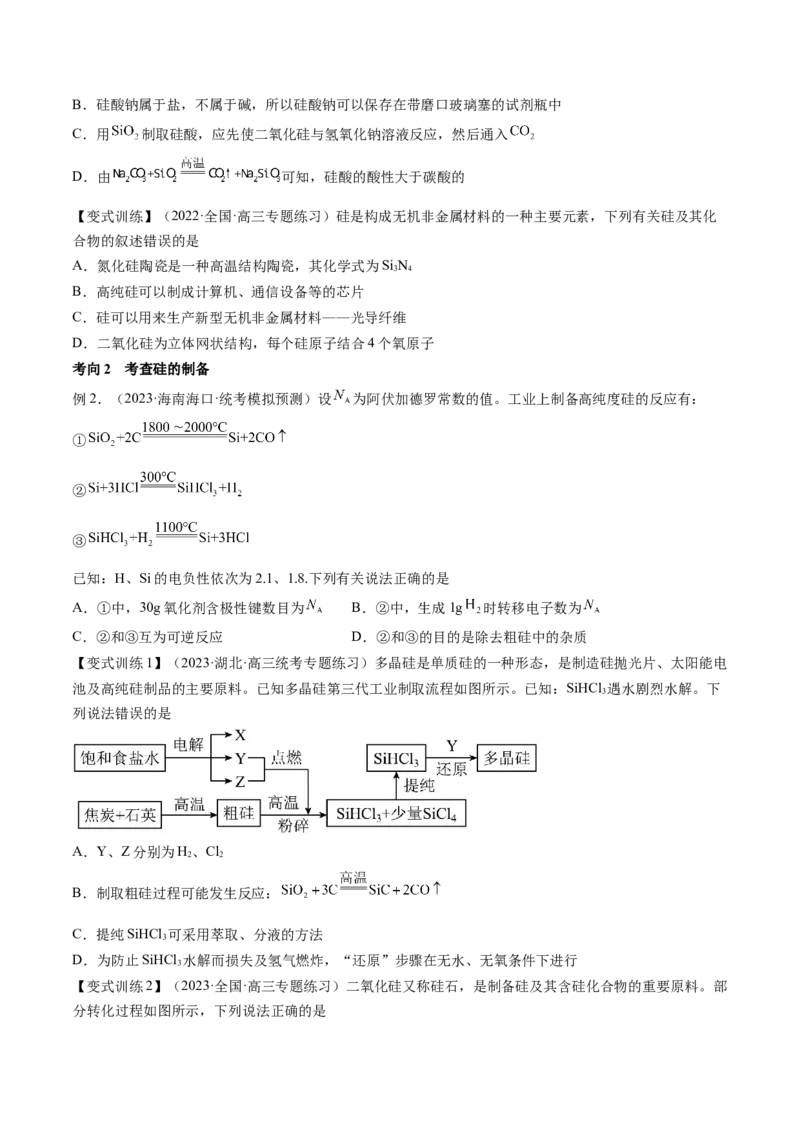
【变式训练1】(2023·湖北·高三统考专题练习)多晶硅是单质硅的一种形态,是制造硅抛光片、太阳能电
池及高纯硅制品的主要原料。已知多晶硅第三代工业制取流程如图所示。已知:SiHCl 遇水剧烈水解。下
3
列说法错误的是
A.Y、Z分别为H、Cl
2 2
B.制取粗硅过程可能发生反应:
C.提纯SiHCl 可采用萃取、分液的方法
3
D.为防止SiHCl 水解而损失及氢气燃炸,“还原”步骤在无水、无氧条件下进行
3
【变式训练2】(2023·全国·高三专题练习)二氧化硅又称硅石,是制备硅及其含硅化合物的重要原料。部
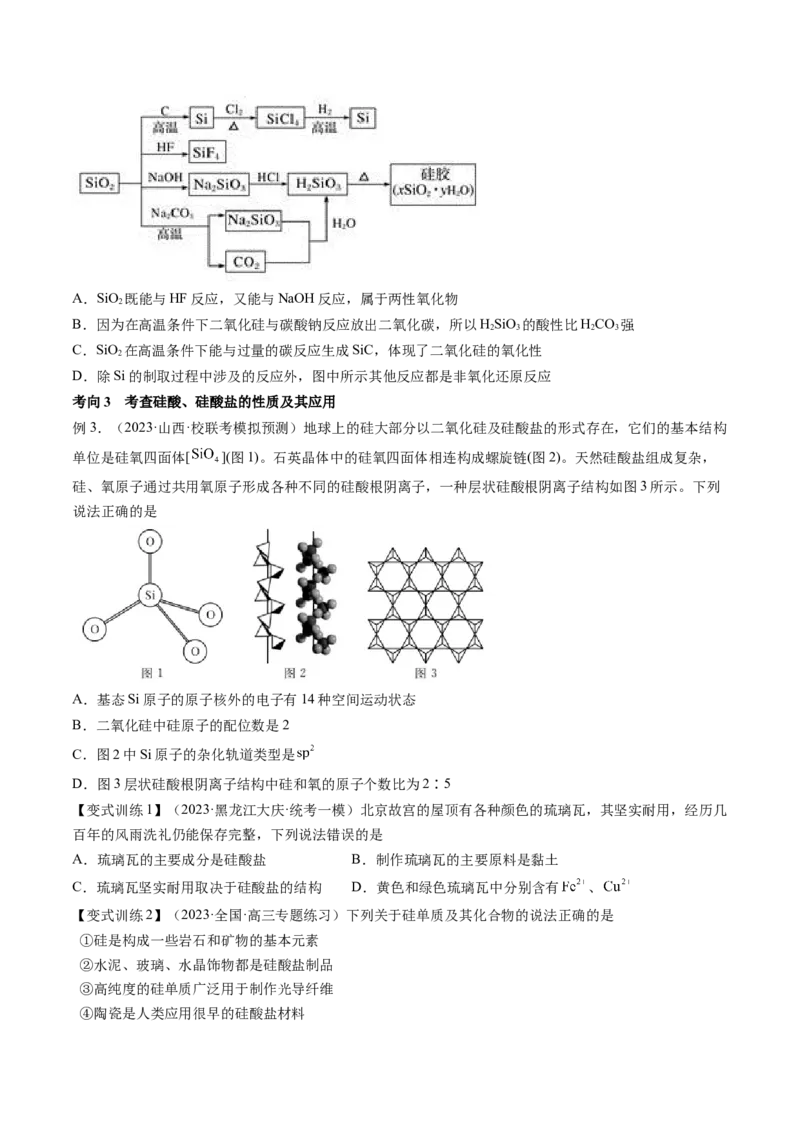
分转化过程如图所示,下列说法正确的是A.SiO 既能与HF反应,又能与NaOH反应,属于两性氧化物
2
B.因为在高温条件下二氧化硅与碳酸钠反应放出二氧化碳,所以HSiO 的酸性比HCO 强
2 3 2 3
C.SiO 在高温条件下能与过量的碳反应生成SiC,体现了二氧化硅的氧化性
2
D.除Si的制取过程中涉及的反应外,图中所示其他反应都是非氧化还原反应
考向3 考查硅酸、硅酸盐的性质及其应用
例3.(2023·山西·校联考模拟预测)地球上的硅大部分以二氧化硅及硅酸盐的形式存在,它们的基本结构
单位是硅氧四面体[ ](图1)。石英晶体中的硅氧四面体相连构成螺旋链(图2)。天然硅酸盐组成复杂,
硅、氧原子通过共用氧原子形成各种不同的硅酸根阴离子,一种层状硅酸根阴离子结构如图3所示。下列
说法正确的是
A.基态Si原子的原子核外的电子有14种空间运动状态
B.二氧化硅中硅原子的配位数是2
C.图2中Si原子的杂化轨道类型是
D.图3层状硅酸根阴离子结构中硅和氧的原子个数比为2∶5
【变式训练1】(2023·黑龙江大庆·统考一模)北京故宫的屋顶有各种颜色的琉璃瓦,其坚实耐用,经历几
百年的风雨洗礼仍能保存完整,下列说法错误的是
A.琉璃瓦的主要成分是硅酸盐 B.制作琉璃瓦的主要原料是黏土
C.琉璃瓦坚实耐用取决于硅酸盐的结构 D.黄色和绿色琉璃瓦中分别含有 、
【变式训练2】(2023·全国·高三专题练习)下列关于硅单质及其化合物的说法正确的是
①硅是构成一些岩石和矿物的基本元素
②水泥、玻璃、水晶饰物都是硅酸盐制品
③高纯度的硅单质广泛用于制作光导纤维
④陶瓷是人类应用很早的硅酸盐材料A.①② B.②③ C.①④ D.③④
考点三 无机非金属材料
知识点1 传统无机非金属材料
1.含义:传统的无机非金属材料多为硅酸盐材料,如水泥、玻璃、陶瓷等硅酸盐材料。
2.分类
(1)陶瓷:陶瓷以__________________为主要原料,经高温烧结而成的。
(2)玻璃:普通玻璃的主要成分为__________________,它是以__________________为主要原料,经混
合、粉碎,在玻璃窑中熔融,发生复杂的___________________________而制得的,玻璃可用于生产建筑
材料、光学仪器和各种器皿,还可制造玻璃纤维,用于高强度复合材料等。
(3)水泥:普通硅酸盐水泥的主要原料是__________________,二者与其他辅料经混合、研磨后在水泥
回转窑中煅烧,发生复杂的物理变化和化学变化,加入适量石膏调节水泥硬化速率,再研成细粉得到普通
水泥。_________是水泥、沙子和碎石等与水混合得到的。
3.传统无机非金属材料比较
水泥 玻璃 陶瓷
主要原料 黏土、石灰石、石膏 石灰石、石英砂、纯碱 黏土
主要设备 水泥回转窑 玻璃窑 陶瓷窑
复杂的物理、化学变 主要反应:NaCO+SiO=====NaSiO+ 复杂的物理、化
2 3 2 2 3
变化
化过程 CO↑、CaCO +SiO=====CaSiO +CO↑ 学变化过程
2 3 2 3 2
硅酸三钙(3CaO·SiO )
2
硅酸二钙(2CaO·SiO )
2
组成 硅酸钠、硅酸钙和二氧化硅 硅酸盐
铝酸三钙
3CaO·Al O)
2 3
在工农业、科
用途 重要的建筑材料 制化学实验用的玻璃仪器、窗玻璃等 技、生活、实验
室中使用广泛
知识点2 新型无机非金属材料
1.高纯度含硅元素的材料,如单晶硅、二氧化硅,具有特殊的光学和电学性能。
2.新型陶瓷
(1)含义:新型陶瓷在组成上不再限于传统的硅酸盐体系,在光学、热学、电学、磁学等方面具有很多
新的特性和功能。
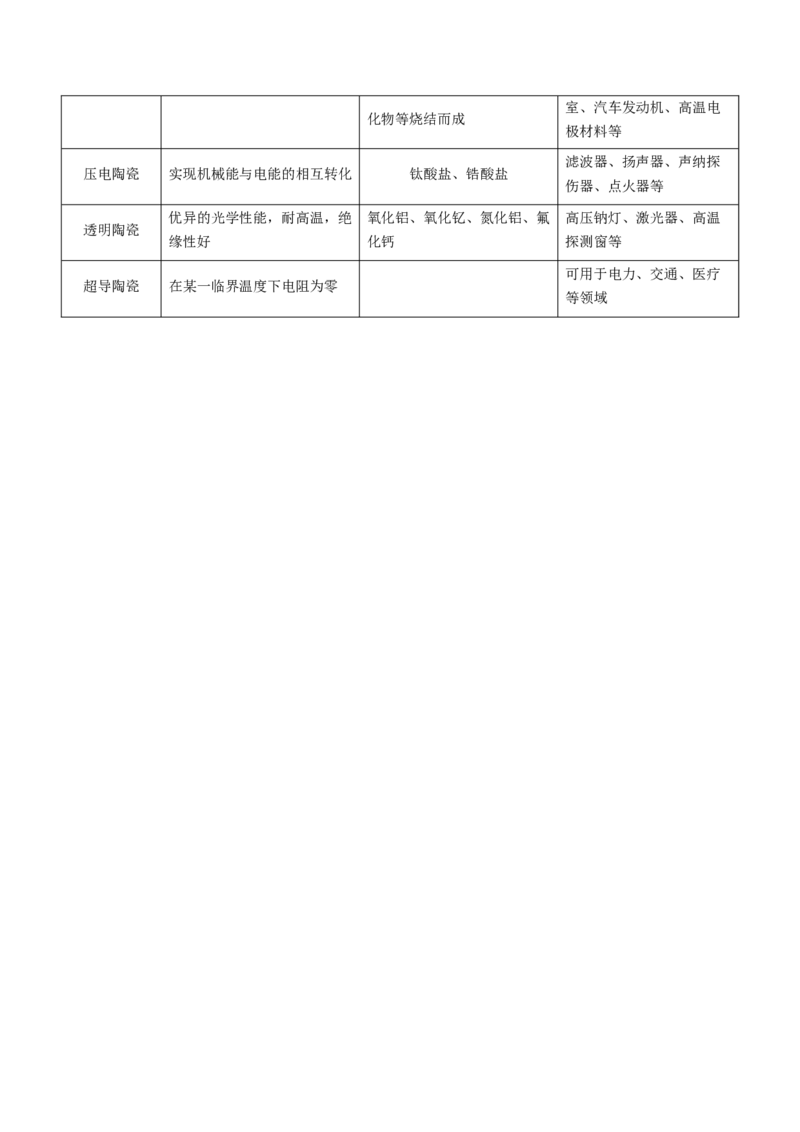
(2)新型陶瓷的种类与用途
材料类型 主要特性 示例 用途
高温结构陶瓷 耐高温、抗氧化、耐磨蚀 碳化硅、氮化硅与某些金属氧 火箭发动机的尾管及燃烧室、汽车发动机、高温电
化物等烧结而成
极材料等
滤波器、扬声器、声纳探
压电陶瓷 实现机械能与电能的相互转化 钛酸盐、锆酸盐
伤器、点火器等
优异的光学性能,耐高温,绝 氧化铝、氧化钇、氮化铝、氟 高压钠灯、激光器、高温
透明陶瓷
缘性好 化钙 探测窗等
可用于电力、交通、医疗
超导陶瓷 在某一临界温度下电阻为零
等领域3.碳纳米材料
(1)含义:碳纳米材料是一类新型的无机非金属材料。
(2)类型:富勒烯、碳纳米管、石墨烯等。
(3)用途:在能源、信息、医药等领域有广阔的应用前景。
材料类型 性能 用途
比表面积大,高强度,优良的电学性
碳纳米管 生产复合材料、电池和传感器等
能
电阻率低,热导率高,具有很高的强 用于光电器件、超级电容器、电池
石墨烯
度 和复合材料等
考向1 考查传统无机非金属材料的分类和应用
例1.(2023·全国·高三专题练习)下列关于无机非金属材料的说法不正确的是
A.传统无机非金属材料是指玻璃、水泥、陶瓷等硅酸盐材料
B.新型无机非金属材料虽然克服了传统无机非金属材料的缺点,但强度比较差
C.高温结构材料具有耐高温、耐酸碱腐蚀、硬度大、耐磨损、密度小等优点
D.传统无机非金属材料和新型无机非金属材料的主要成分不同
【变式训练】(2023·北京·高三专题练习)陶瓷版“冰墩墩”和“雪容融”均产自中国陶瓷之乡——福建
德化县。德化陶瓷早在宋元时期就是“海上丝绸之路”的重要出口商品。下列说法不正确的是
A.陶瓷、玻璃和水泥均属于传统无机非金属材料
B.陶瓷版“冰墩墩”上黑色涂料的主要成分为Fe O
2 3
C.高温结构陶瓷具有耐高温、耐氧化、耐磨蚀等优良性能
D.陶瓷是以粘土及天然矿物岩为原料,经加工烧制而成
考向2 考查新型无机非金属材料的分类和应用
例2.(2023·辽宁葫芦岛·统考二模)近年来,我国科技迅猛发展,下列科技成果中蕴含的化学知识叙述不
正确的是
A.建造港珠澳大桥所采用的高强抗震螺纹钢属于合金
B.中国天眼FAST用到的SiC是新型无机非金属材料
C.华为麒麟芯片的主要成分是单质硅
D.飞船返回舱使用氮化硅耐高温结构材料,Si N 属于分子晶体
3 4
【变式训练】(2023·安徽芜湖·统考二模)化学与生活、科技、社会发展息息相关。下列说法正确的是A.“天宫”空间站使用聚乳酸材料餐具,聚乳酸是化合物
B.富勒烯与石墨烯用途广泛,它们都属于新型无机非金属材料
C.冬奥场馆建筑使用碲化镉发电玻璃,碲和镉均属于主族元素
D.中国承建的卡塔尔首座光伏电站中的光伏材料为高纯度二氧化硅
1.(2023·山东·统考高考真题)下列之物具有典型的齐鲁文化特色,据其主要化学成分不能与其他三种归
为一类的是
A.泰山墨玉 B.龙山黑陶 C.齐国刀币 D.淄博琉璃
2.(2023·浙江·高考真题)下列物质中属于耐高温酸性氧化物的是
A. B. C. D.
3.(2023·湖北·统考高考真题)工业制备高纯硅的主要过程如下:
石英砂 粗硅 高纯硅
下列说法错误的是
A.制备粗硅的反应方程式为
B.1molSi含Si-Si键的数目约为
C.原料气HCl和 应充分去除水和氧气
D.生成 的反应为熵减过程
4.(2023·浙江·统考高考真题)材料是人类赖以生存和发展的物质基础,下列材料主要成分属于有机物的
是
A.石墨烯 B.不锈钢 C.石英光导纤维 D.聚酯纤维