文档内容
第 16 讲 原电池 新型电源
1.化学电源在生活中有广泛的应用,各种电池的示意图如图,下列有关说法正确的是
A.甲:电流由锌片经导线流向铜片
B.乙:负极的电极反应式为Zn-2e-=Zn2+
C.丙:锌筒作负极,发生氧化反应,使用一段时间锌筒会变薄
D.丁:使用一段时间后电解质溶液的酸性增强,导电能力增大
2.下列有关电化学知识的描述正确的是
A.锌、铜与稀硫酸组成的原电池,在工作过程中,电解质溶液的pH保持不变
B.用足量锌粒与稀硫酸反应制取 ,若要增大反应速率,可以滴入几滴 溶液
C.将铁、铜用导线连接后放入浓硝酸中组成原电池,铁作负极,铜作正极,其负极反应式为
D.燃料电池是利用燃料和氧化剂之间的氧化还原反应,将化学能转化为热能,然后再转化为电能的
化学电源
3.硫化氢(H S)是强烈的神经毒素,对黏膜有强烈的刺激作用。科研人员设计了如图装置,借助太阳
2
能,将HS再利用,变废为宝。下列叙述正确的是
2
A.b电极发生氧化反应
B.a电极区不可用NaOH溶液作电解质溶液
C. 的迁移方向为b电极→a电极D.每生成2g H ,负极区需消耗22.4 L H S
2 2
4.某储能电池原理如图1,其俯视图如图2,已知放电时N是负极(N 是阿伏加德罗常数的值)。下列
A
说法正确的是
A.放电时,每转移N 个电子,理论上CCl 吸收0.5N 个Cl
A 4 A 2
B.放电时,负极反应为NaTi (PO )-2e-=NaTi (PO )+2Na+
3 2 4 3 2 4 3
C.充电时,每转移1mol电子,N极理论质量减小23g
D.充电过程中,右侧储液器中NaCl溶液浓度增大
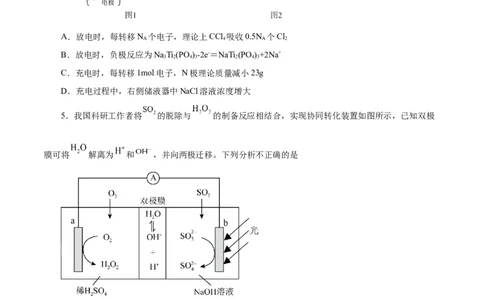
5.我国科研工作者将 的脱除与 的制备反应相结合,实现协同转化装置如图所示,已知双极
膜可将 解离为 和 ,并向两极迁移。下列分析不正确的是
A. 为正极,发生还原反应
B. 极电极反应式为:
C.双极膜的存在能保证两侧电解质溶液的浓度不变
D.协同转化总反应:
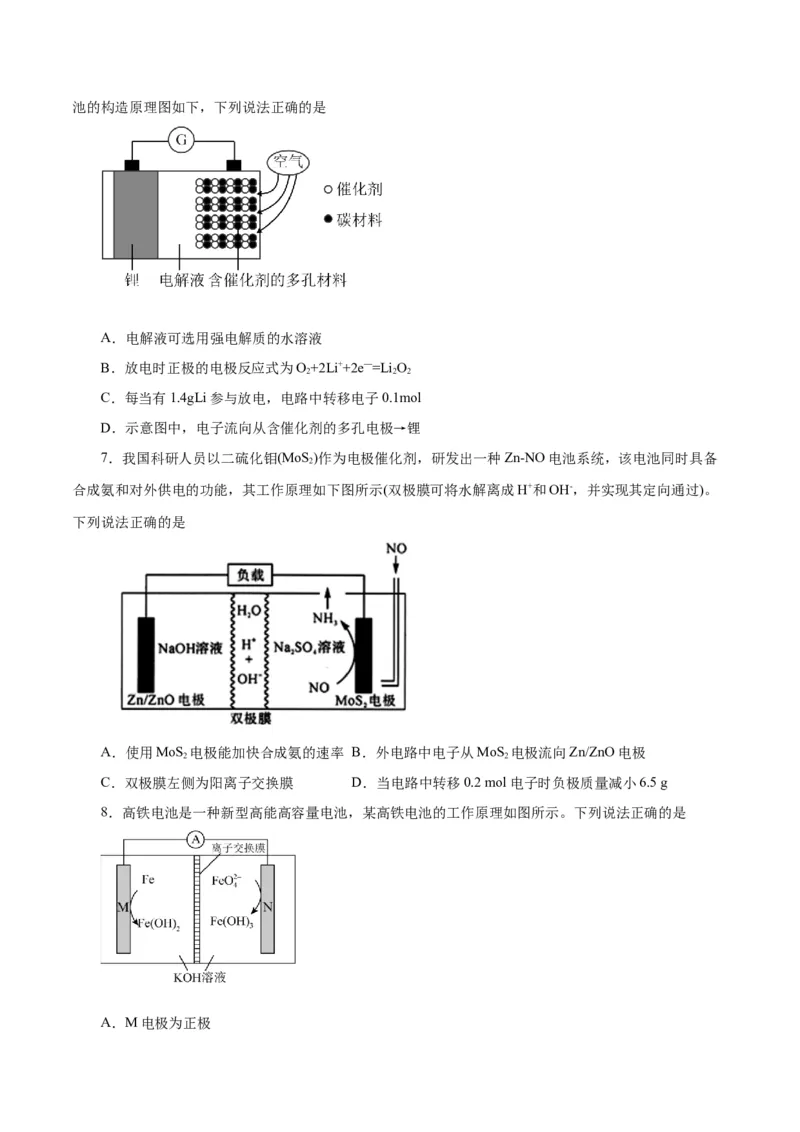
6.锂﹣空气电池是一种可充放电池,电池反应为2Li+O=Li O(已知LiO 是固体),某锂—空气电
2 2 2 2 2池的构造原理图如下,下列说法正确的是
A.电解液可选用强电解质的水溶液
B.放电时正极的电极反应式为O+2Li++2e—=Li O
2 2 2
C.每当有1.4gLi参与放电,电路中转移电子0.1mol
D.示意图中,电子流向从含催化剂的多孔电极→锂
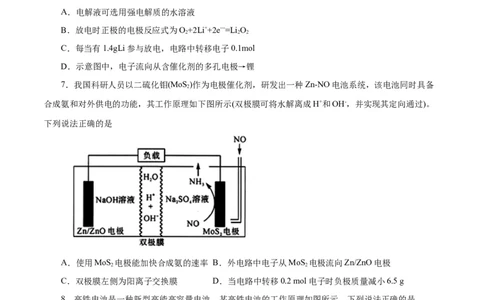
7.我国科研人员以二硫化钼(MoS )作为电极催化剂,研发出一种Zn-NO电池系统,该电池同时具备
2
合成氨和对外供电的功能,其工作原理如下图所示(双极膜可将水解离成H+和OH-,并实现其定向通过)。
下列说法正确的是
A.使用MoS 电极能加快合成氨的速率 B.外电路中电子从MoS 电极流向Zn/ZnO电极
2 2
C.双极膜左侧为阳离子交换膜 D.当电路中转移0.2 mol电子时负极质量减小6.5 g
8.高铁电池是一种新型高能高容量电池,某高铁电池的工作原理如图所示。下列说法正确的是
A.M电极为正极B.电池工作时,电流方向为:
C.N极的电极反应式为
D.电池工作一段时间后,正极区中 的浓度增大
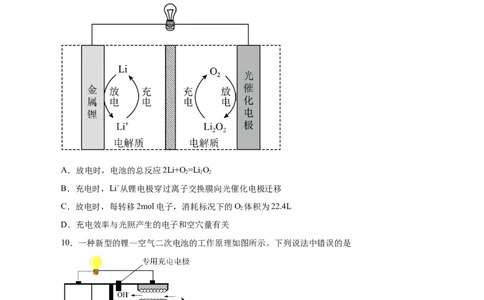
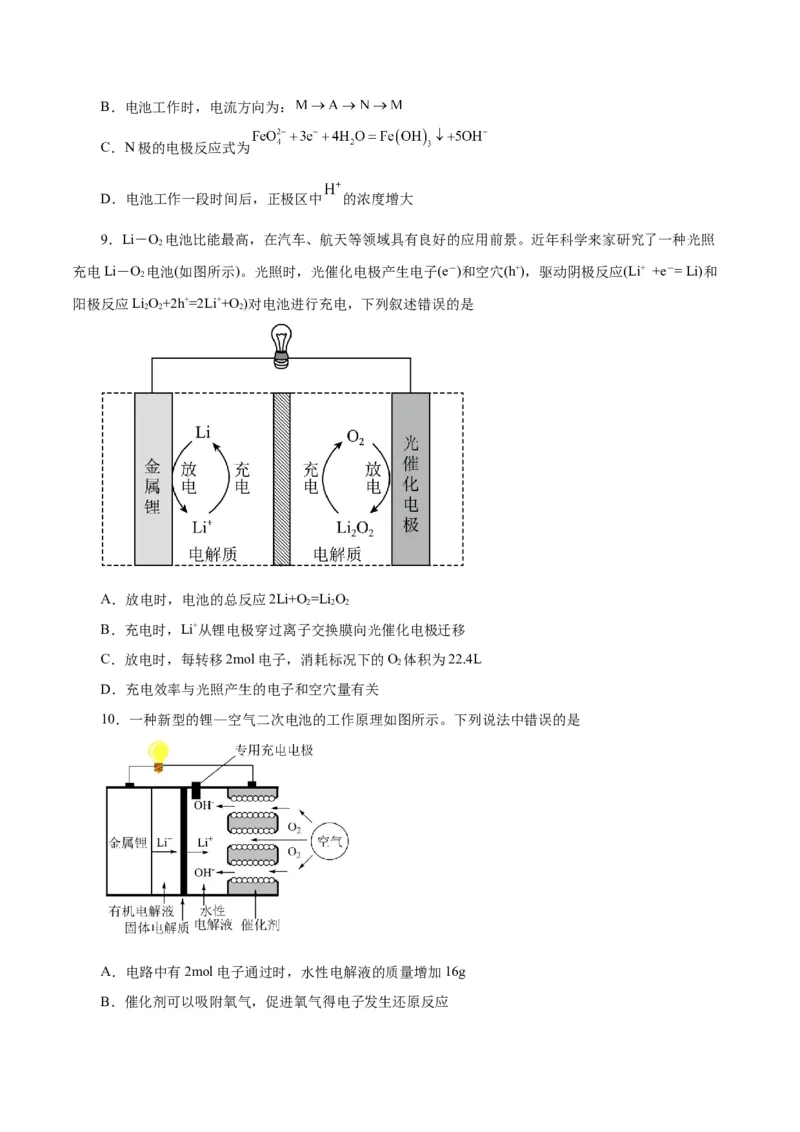
9.Li-O 电池比能最高,在汽车、航天等领域具有良好的应用前景。近年科学来家研究了一种光照
2
充电Li-O 电池(如图所示)。光照时,光催化电极产生电子(e-)和空穴(h+),驱动阴极反应(Li+ +e-= Li)和
2
阳极反应LiO+2h+=2Li++O )对电池进行充电,下列叙述错误的是
2 2 2
A.放电时,电池的总反应2Li+O=Li O
2 2 2
B.充电时,Li+从锂电极穿过离子交换膜向光催化电极迁移
C.放电时,每转移2mol电子,消耗标况下的O 体积为22.4L
2
D.充电效率与光照产生的电子和空穴量有关
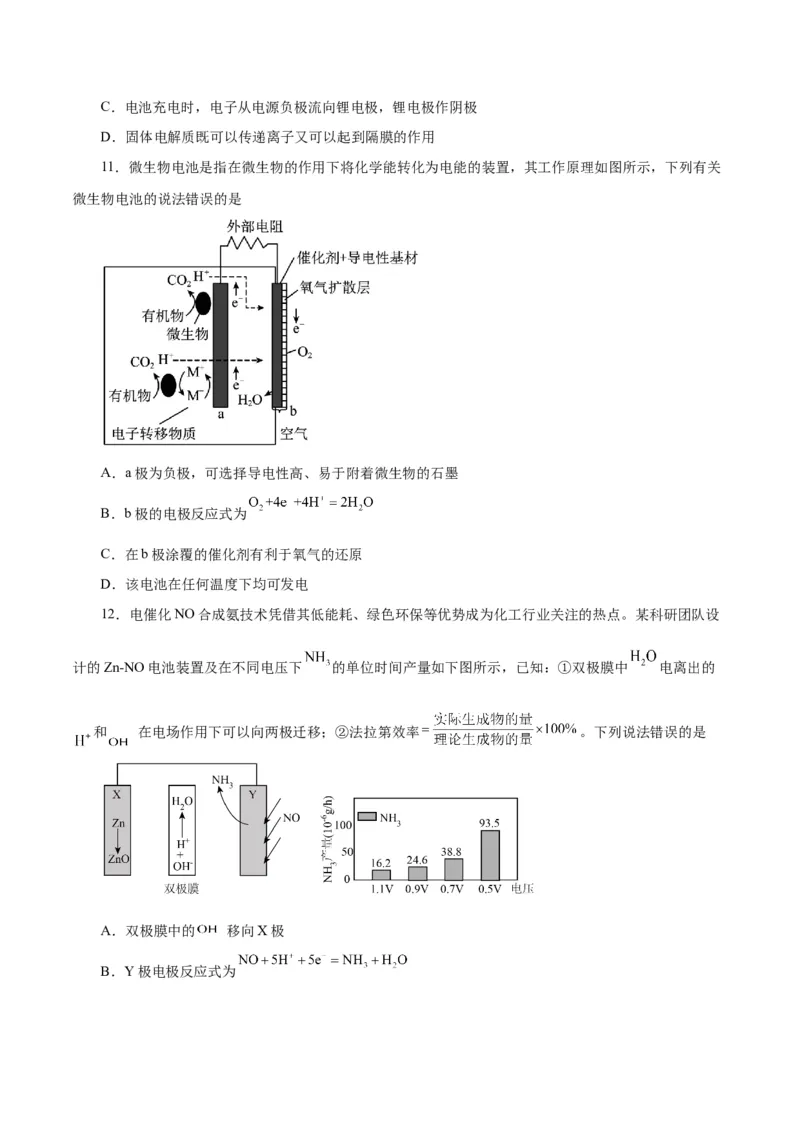
10.一种新型的锂—空气二次电池的工作原理如图所示。下列说法中错误的是
A.电路中有2mol电子通过时,水性电解液的质量增加16g
B.催化剂可以吸附氧气,促进氧气得电子发生还原反应C.电池充电时,电子从电源负极流向锂电极,锂电极作阴极
D.固体电解质既可以传递离子又可以起到隔膜的作用
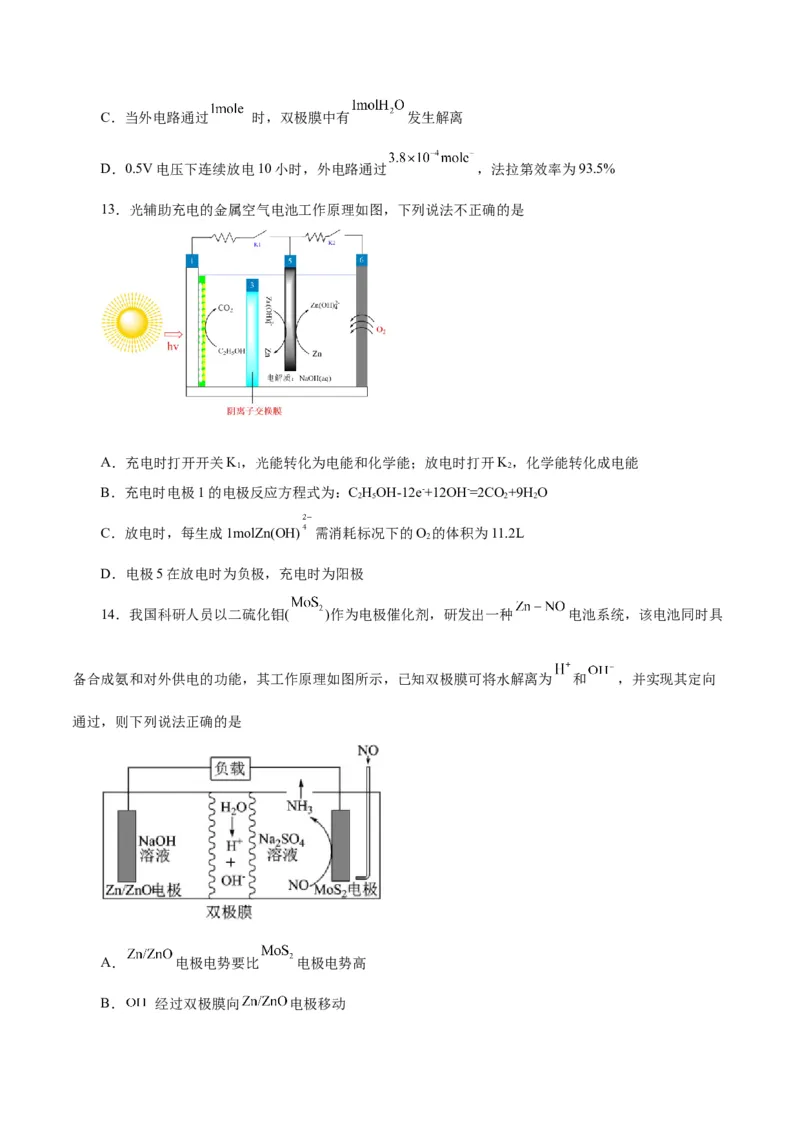
11.微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示,下列有关
微生物电池的说法错误的是
A.a极为负极,可选择导电性高、易于附着微生物的石墨
B.b极的电极反应式为
C.在b极涂覆的催化剂有利于氧气的还原
D.该电池在任何温度下均可发电
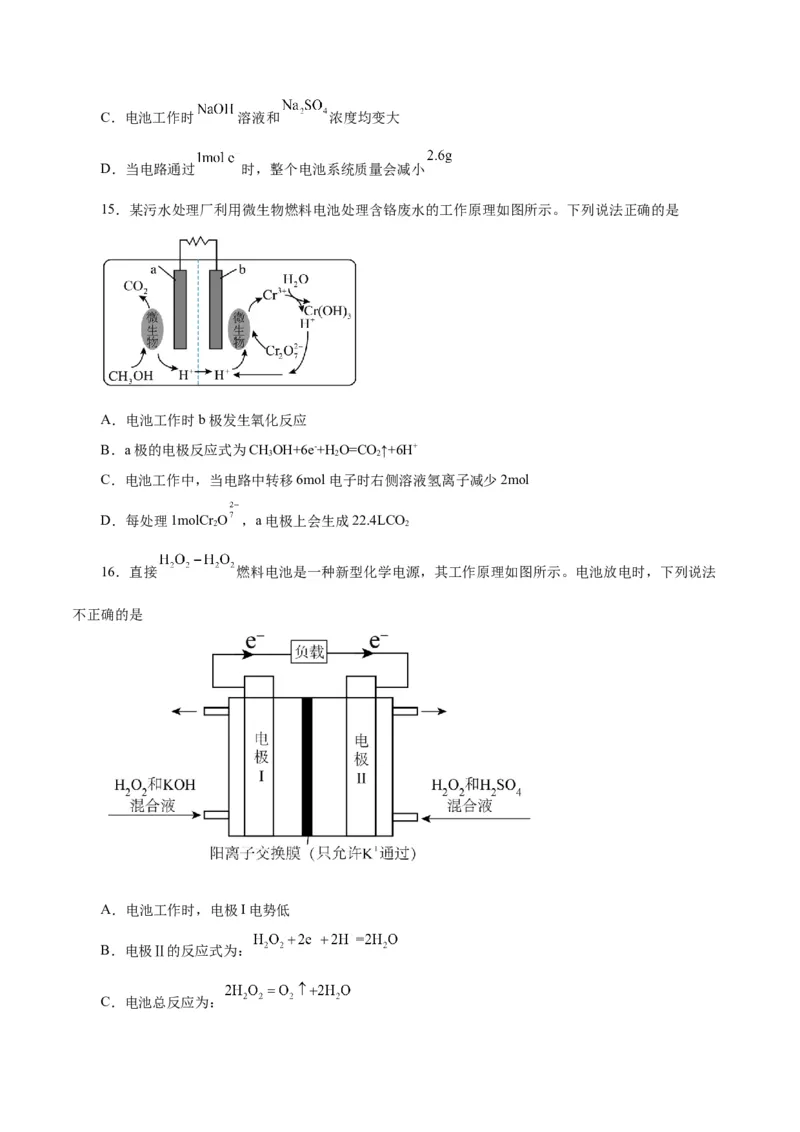
12.电催化NO合成氨技术凭借其低能耗、绿色环保等优势成为化工行业关注的热点。某科研团队设
计的Zn-NO电池装置及在不同电压下 的单位时间产量如下图所示,已知:①双极膜中 电离出的
和 在电场作用下可以向两极迁移;②法拉第效率 。下列说法错误的是
A.双极膜中的 移向X极
B.Y极电极反应式为C.当外电路通过 时,双极膜中有 发生解离
D.0.5V电压下连续放电10小时,外电路通过 ,法拉第效率为93.5%
13.光辅助充电的金属空气电池工作原理如图,下列说法不正确的是
A.充电时打开开关K,光能转化为电能和化学能;放电时打开K,化学能转化成电能
1 2
B.充电时电极1的电极反应方程式为:C HOH-12e-+12OH-=2CO +9H O
2 5 2 2
C.放电时,每生成1molZn(OH) 需消耗标况下的O 的体积为11.2L
2
D.电极5在放电时为负极,充电时为阳极
14.我国科研人员以二硫化钼( )作为电极催化剂,研发出一种 电池系统,该电池同时具
备合成氨和对外供电的功能,其工作原理如图所示,已知双极膜可将水解离为 和 ,并实现其定向
通过,则下列说法正确的是
A. 电极电势要比 电极电势高
B. 经过双极膜向 电极移动C.电池工作时 溶液和 浓度均变大
D.当电路通过 时,整个电池系统质量会减小
15.某污水处理厂利用微生物燃料电池处理含铬废水的工作原理如图所示。下列说法正确的是
A.电池工作时b极发生氧化反应
B.a极的电极反应式为CHOH+6e-+H O=CO↑+6H+
3 2 2
C.电池工作中,当电路中转移6mol电子时右侧溶液氢离子减少2mol
D.每处理1molCr O ,a电极上会生成22.4LCO
2 2
16.直接 燃料电池是一种新型化学电源,其工作原理如图所示。电池放电时,下列说法
不正确的是
A.电池工作时,电极I电势低
B.电极Ⅱ的反应式为:
C.电池总反应为:D.当电路中转移0.1mol电子时,通过阳离子交换膜的 为3.9g
17.我国科学家研究出一种新型水系 电池,其结构如下图,该电池既能实现乙炔加氢又能提
供电能,下列说法正确的是
A. 通过阴离子交换膜向a电极移动
B.左侧极室中 减小
C.a极的电极反应式为
D.每转移 ,右侧极室中溶液质量增大34g
18.一种具有高能量比的新型干电池示意图如图所示,石墨电极区发生的电极反应为MnO +e-
2
+H O=MnO(OH)+OH-。该装置工作时,下列叙述正确的是
2
A.石墨电极上的电势比Al电极上的低
B.每消耗27g Al,有3mol电子通过溶液转移到石墨电极上
C.若采用食盐水+NaOH溶液作电解质溶液,电极反应式相同
D.Al电极区的电极反应式: Al-3e- +3NH·H O =Al(OH) +3
3 2 3
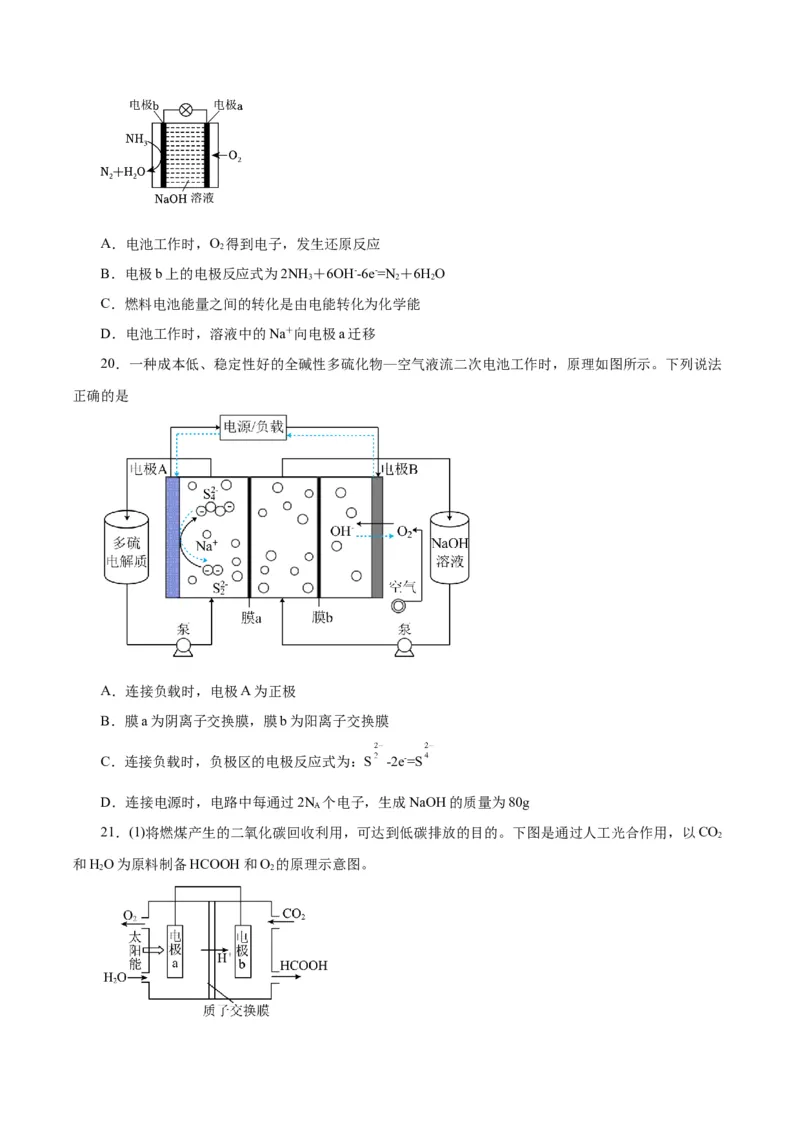
19.从节约能源和保护生态环境的角度来看,燃料电池是最具有发展前途的发电技术。NH ﹣O 燃料
3 2
电池装置如图所示,下列说法错误的是A.电池工作时,O 得到电子,发生还原反应
2
B.电极b上的电极反应式为2NH +6OH--6e-=N +6HO
3 2 2
C.燃料电池能量之间的转化是由电能转化为化学能
D.电池工作时,溶液中的Na+向电极a迁移
20.一种成本低、稳定性好的全碱性多硫化物—空气液流二次电池工作时,原理如图所示。下列说法
正确的是
A.连接负载时,电极A为正极
B.膜a为阴离子交换膜,膜b为阳离子交换膜
C.连接负载时,负极区的电极反应式为:S -2e-=S
D.连接电源时,电路中每通过2N 个电子,生成NaOH的质量为80g
A
21.(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。下图是通过人工光合作用,以CO
2
和HO为原料制备HCOOH和O 的原理示意图。
2 2①电极b为 极。
②电极b上的电极反应为 。
(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,该电池从浓
缩海水中提取LiCl的同时又获得了电能。
①X为 极,Y极的电极反应式为 。
②Y极生成1 mol Cl 时, mol Li+移向 (填“X”或“Y”)极。
2
(3)微生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇微生物燃料电池
中,电解质溶液为酸性,示意图如下:
①该电池中外电路电子的流动方向为 (填“从A到B”或“从B到A”)。
②A电极附近甲醇发生的电极反应为 。
22.为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。
回答下列问题:
(1)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并
且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择________作为电解质。
阳离子 u∞×108/(m2·s-1·V-1) 阴离子 u∞×108/(m2·s-1·V-1)Li+ 4.07 HCO 4.61
Na+ 5.19 NO 7.40
Ca2+ 6.59 Cl- 7.91
K+ 7.62 SO 8.27
(2)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入________电极溶液中。
(3)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未见Fe析出。可
知,石墨电极溶液中c(Fe2+)=________。
(4)根据(2)、(3)实验结果,可知石墨电极的电极反应式为____________________,铁电极的电极反应
式为________________________________。因此,验证了 Fe2+氧化性小于________、还原性小于
________。
(5)实验前需要对铁电极表面活化。在FeSO 溶液中加入几滴Fe (SO ) 溶液,将铁电极浸泡一段时间,
4 2 4 3
铁电极表面被刻蚀活化。检验活化反应完成的方法是____________________。