文档内容
化学实验基础和综合实验探究
第 1 讲 化学实验常用仪器及基本操作
课 程 标 准 知 识 建 构
1.了解化学实验室常用仪器的主要用途和使用方法。
2.掌握化学实验的基本操作。能识别化学用品标志。
3.了解实验室一般事故的预防和处理方法。
4.正确选用实验装置和仪器的连接。
一、常用仪器的识别与使用
1.加热仪器——热源
2.可加热的仪器
(1)(2)
3.计量仪器
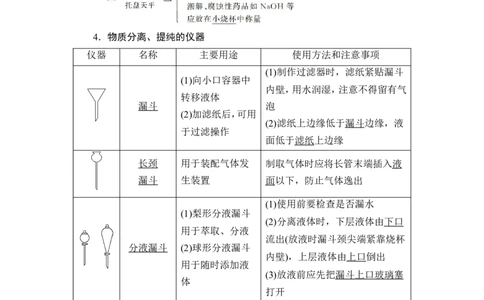
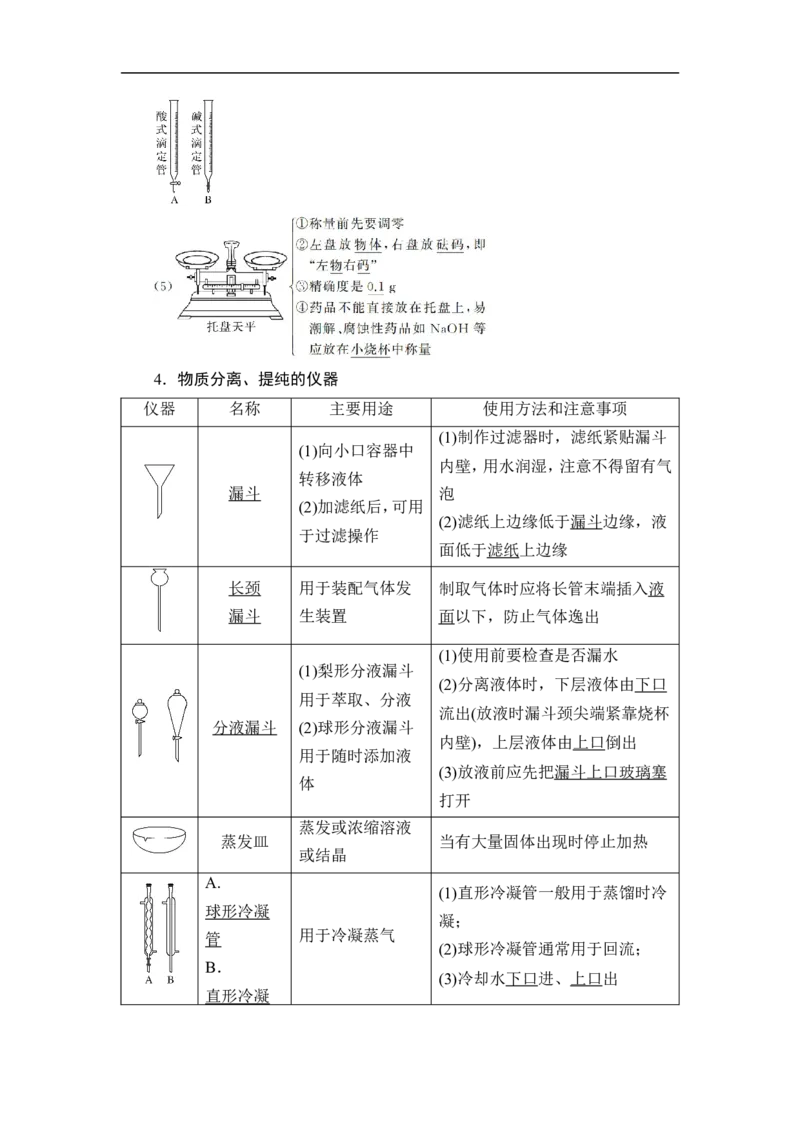
(4)4.物质分离、提纯的仪器
仪器 名称 主要用途 使用方法和注意事项
(1)制作过滤器时,滤纸紧贴漏斗
(1)向小口容器中
内壁,用水润湿,注意不得留有气
转移液体
漏斗 泡
(2)加滤纸后,可用
(2)滤纸上边缘低于漏斗边缘,液
于过滤操作
面低于滤纸上边缘
长颈 用于装配气体发 制取气体时应将长管末端插入液
漏斗 生装置 面以下,防止气体逸出
(1)使用前要检查是否漏水
(1)梨形分液漏斗
(2)分离液体时,下层液体由下口
用于萃取、分液
流出(放液时漏斗颈尖端紧靠烧杯
分液漏斗 (2)球形分液漏斗
内壁),上层液体由上口倒出
用于随时添加液
(3)放液前应先把漏斗上口玻璃塞
体
打开
蒸发或浓缩溶液
蒸发皿 当有大量固体出现时停止加热
或结晶
A.
(1)直形冷凝管一般用于蒸馏时冷
球形冷凝
凝;
管 用于冷凝蒸气
(2)球形冷凝管通常用于回流;
B.
(3)冷却水下口进、上口出
直形冷凝管
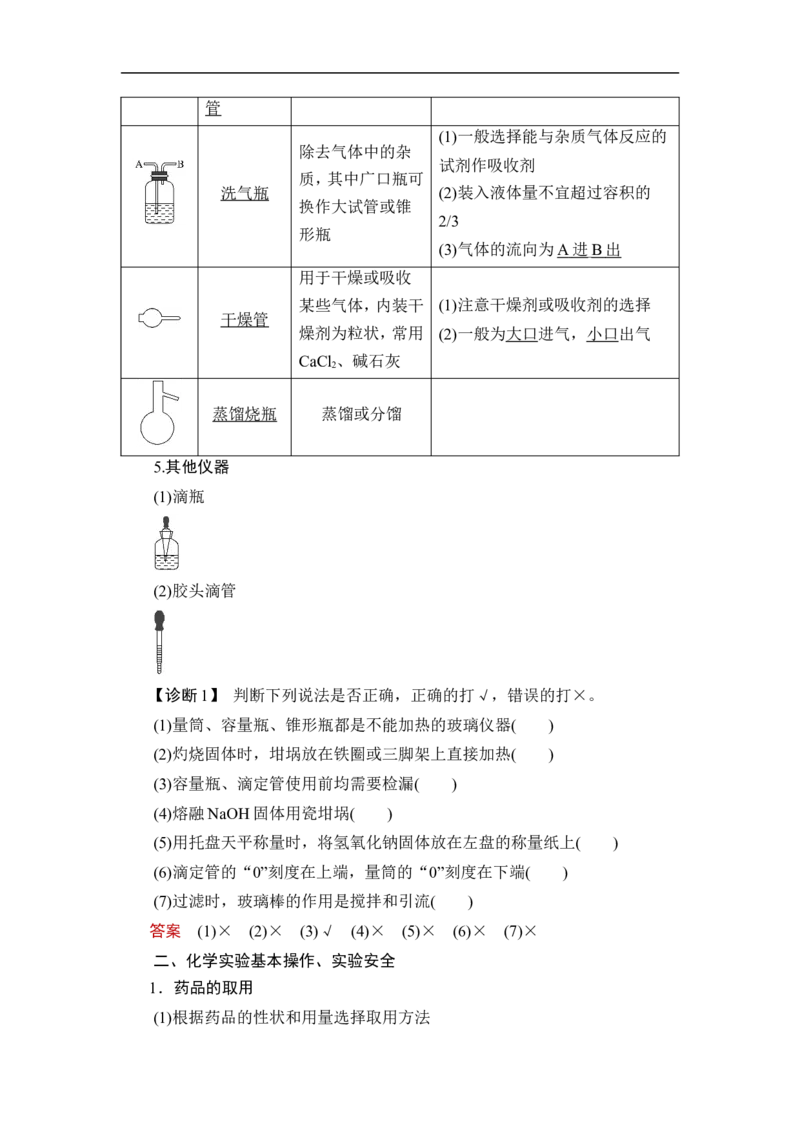
(1)一般选择能与杂质气体反应的
除去气体中的杂
试剂作吸收剂
质,其中广口瓶可
洗气瓶 (2)装入液体量不宜超过容积的
换作大试管或锥
2/3
形瓶
(3)气体的流向为 A 进 B 出
用于干燥或吸收
某些气体,内装干 (1)注意干燥剂或吸收剂的选择
干燥管
燥剂为粒状,常用 (2)一般为大口进气,小口出气
CaCl 、碱石灰
2
蒸馏烧瓶 蒸馏或分馏
5.其他仪器
(1)滴瓶
(2)胶头滴管
【诊断1】 判断下列说法是否正确,正确的打√,错误的打×。
(1)量筒、容量瓶、锥形瓶都是不能加热的玻璃仪器( )
(2)灼烧固体时,坩埚放在铁圈或三脚架上直接加热( )
(3)容量瓶、滴定管使用前均需要检漏( )
(4)熔融NaOH固体用瓷坩埚( )
(5)用托盘天平称量时,将氢氧化钠固体放在左盘的称量纸上( )
(6)滴定管的“0”刻度在上端,量筒的“0”刻度在下端( )
(7)过滤时,玻璃棒的作用是搅拌和引流( )
答案 (1)× (2)× (3)√ (4)× (5)× (6)× (7)×
二、化学实验基本操作、实验安全
1.药品的取用
(1)根据药品的性状和用量选择取用方法粉末状固体使用药匙(或纸槽),块状固体使用镊子;
少量液体使用胶头滴管,多量液体用试剂瓶倾倒。
(2)向仪器中加入药品的操作方法
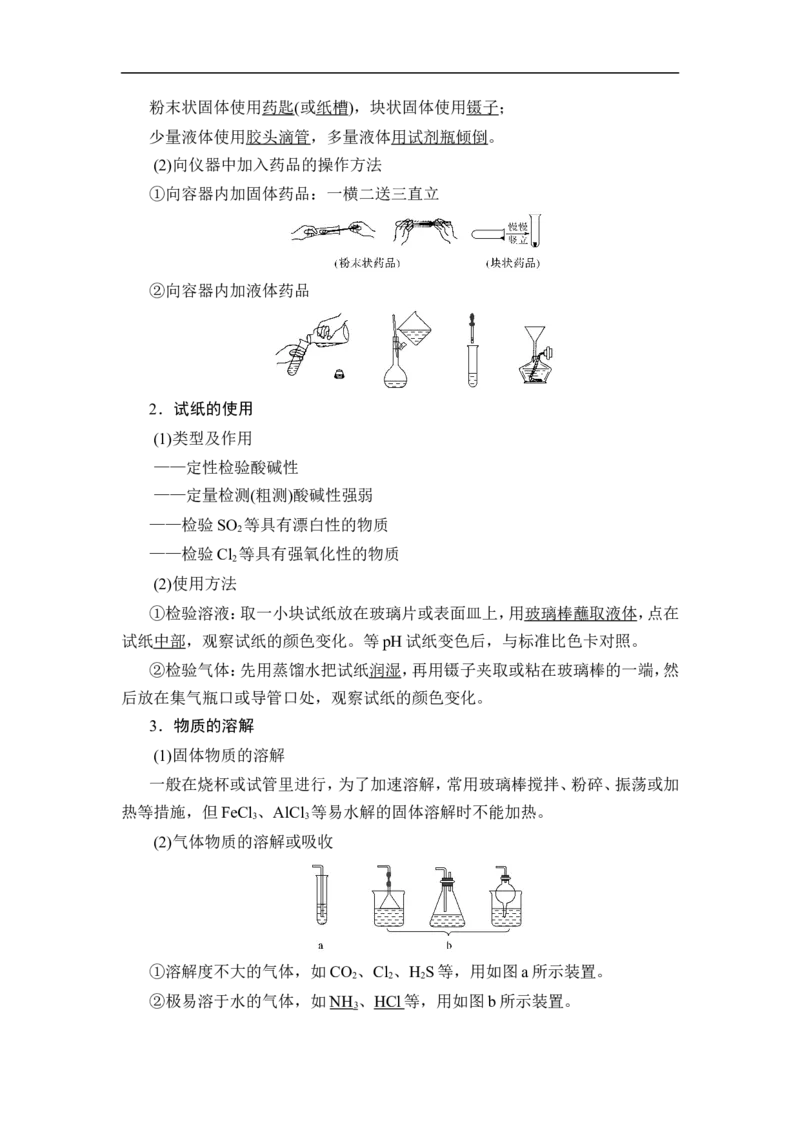
①向容器内加固体药品:一横二送三直立
②向容器内加液体药品
2.试纸的使用
(1)类型及作用
——定性检验酸碱性
——定量检测(粗测)酸碱性强弱
——检验SO 等具有漂白性的物质
2
——检验Cl 等具有强氧化性的物质
2
(2)使用方法
①检验溶液:取一小块试纸放在玻璃片或表面皿上,用玻璃棒蘸取液体,点在
试纸中部,观察试纸的颜色变化。等pH试纸变色后,与标准比色卡对照。
②检验气体:先用蒸馏水把试纸润湿,再用镊子夹取或粘在玻璃棒的一端,然
后放在集气瓶口或导管口处,观察试纸的颜色变化。
3.物质的溶解
(1)固体物质的溶解
一般在烧杯或试管里进行,为了加速溶解,常用玻璃棒搅拌、粉碎、振荡或加
热等措施,但FeCl 、AlCl 等易水解的固体溶解时不能加热。
3 3
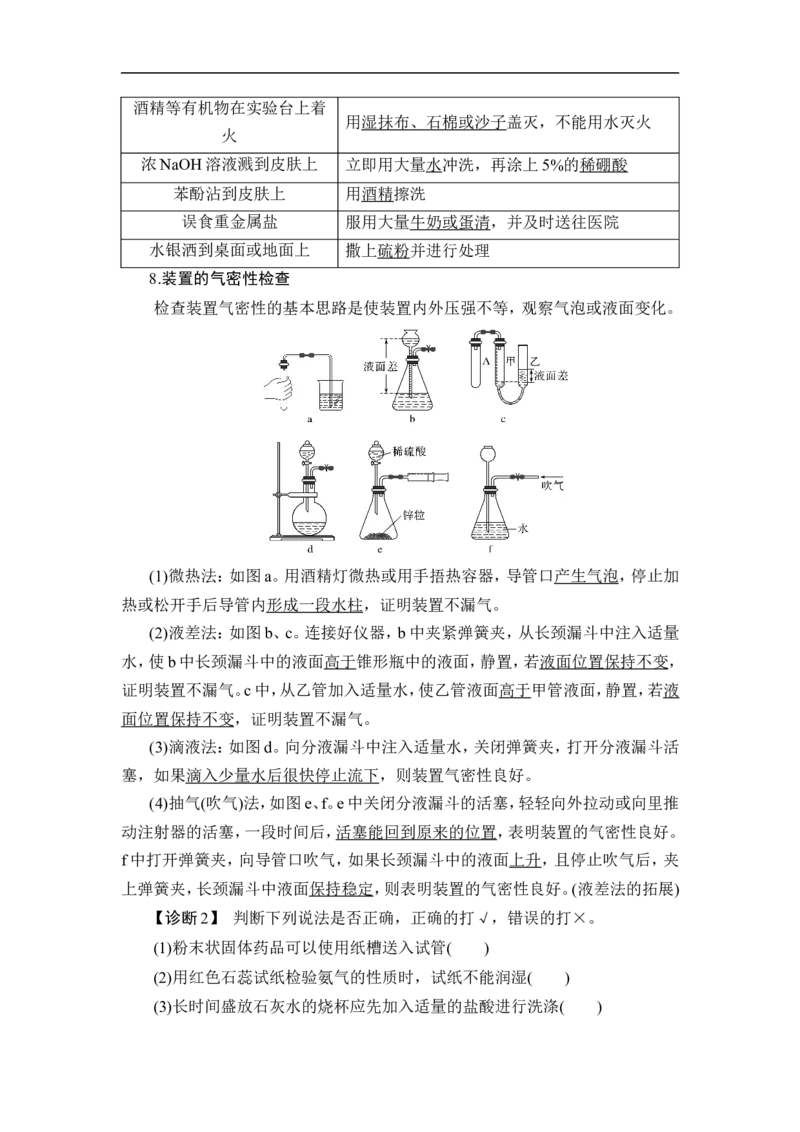
(2)气体物质的溶解或吸收
①溶解度不大的气体,如CO 、Cl 、H S等,用如图a所示装置。
2 2 2
②极易溶于水的气体,如NH 、HCl 等,用如图b所示装置。
3(3)液体物质的溶解(稀释):一般把密度较大的液体加入密度较小的液体中,
如浓硫酸的稀释、浓硫酸与浓硝酸的混合。
4.化学试剂的保存
(1)试剂瓶及瓶塞的选择
①根据药品状态
②根据见光是否分解
③根据酸碱性
(2)试剂的保存方法
化学试剂都应注意妥善密封保存于试剂瓶中。对于易变质、易挥发或有危险
性的化学试剂,还应根据性质采取特殊的保存方法。
5.玻璃仪器的洗涤
(1)洗净的标准:玻璃仪器内壁附着均匀的水膜,既不聚成滴,也不成股流下。
(2)常见残留物的洗涤
残留物 洗涤剂
容器里附有的油污 NaOH 溶液或热的纯碱溶液
容器壁上附着的硫 CS 或热的 NaOH 溶液
2
试管壁上附着的银镜 稀 HNO
3
AgCl 氨水
容器内残留的MnO 热的浓盐酸
2
6.物质的加热方式
加热方式 适用范围
直接加热 瓷质、金属质或小而薄的玻璃仪器(如试管)等
隔石棉网加热 较大的玻璃反应器(如烧杯、烧瓶等)
(1)需严格控制温度(如硝基苯的制备)
浴热(水浴、油浴、沙浴等) (2)需反应混合液静置(如银镜反应)
(3)蒸馏沸点差较小的混合液
7.常见实验事故的处理
实验事故 处理方法
立即用大量水冲洗,然后涂上3%~5%的碳酸
少量浓硫酸溅到皮肤上
氢钠溶液酒精等有机物在实验台上着
用湿抹布、石棉或沙子盖灭,不能用水灭火
火
浓NaOH溶液溅到皮肤上 立即用大量水冲洗,再涂上5%的稀硼酸
苯酚沾到皮肤上 用酒精擦洗
误食重金属盐 服用大量牛奶或蛋清,并及时送往医院
水银洒到桌面或地面上 撒上硫粉并进行处理
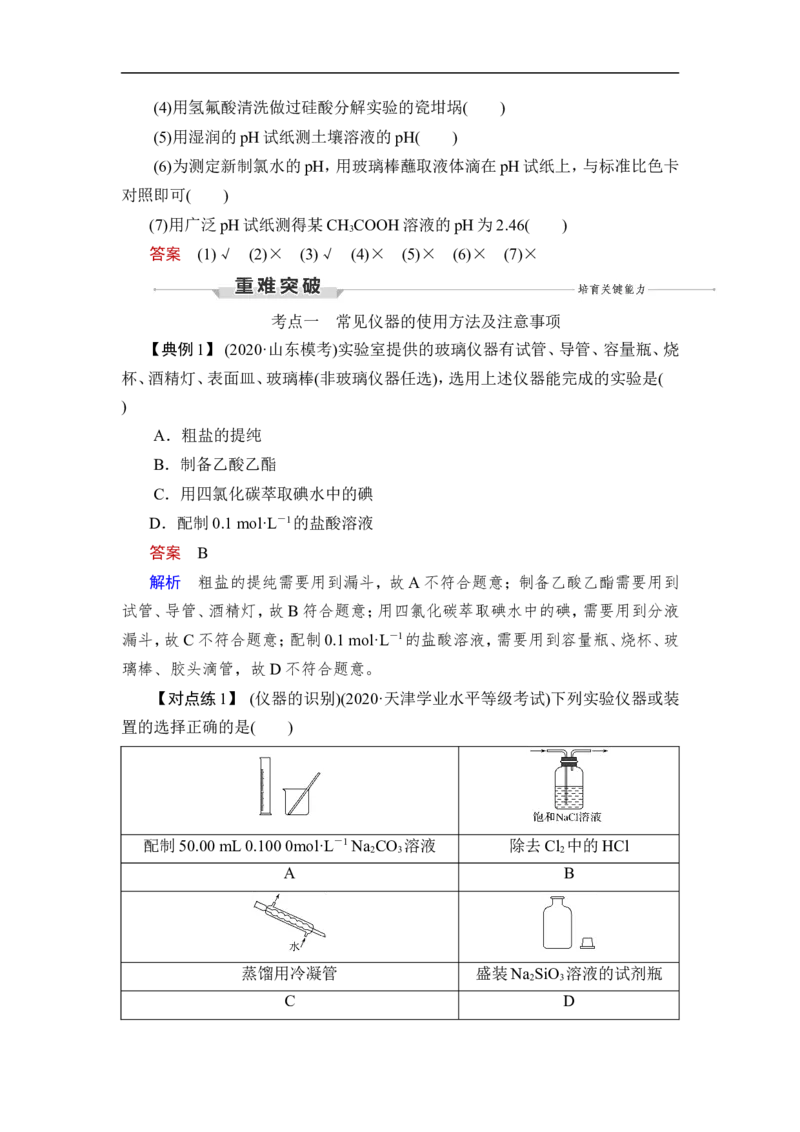
8.装置的气密性检查
检查装置气密性的基本思路是使装置内外压强不等,观察气泡或液面变化。
(1)微热法:如图a。用酒精灯微热或用手捂热容器,导管口产生气泡,停止加
热或松开手后导管内形成一段水柱,证明装置不漏气。
(2)液差法:如图b、c。连接好仪器,b中夹紧弹簧夹,从长颈漏斗中注入适量
水,使b中长颈漏斗中的液面高于锥形瓶中的液面,静置,若液面位置保持不变,
证明装置不漏气。c中,从乙管加入适量水,使乙管液面高于甲管液面,静置,若液
面位置保持不变,证明装置不漏气。
(3)滴液法:如图d。向分液漏斗中注入适量水,关闭弹簧夹,打开分液漏斗活
塞,如果滴入少量水后很快停止流下,则装置气密性良好。
(4)抽气(吹气)法,如图e、f。e中关闭分液漏斗的活塞,轻轻向外拉动或向里推
动注射器的活塞,一段时间后,活塞能回到原来的位置,表明装置的气密性良好。
f中打开弹簧夹,向导管口吹气,如果长颈漏斗中的液面上升,且停止吹气后,夹
上弹簧夹,长颈漏斗中液面保持稳定,则表明装置的气密性良好。(液差法的拓展)
【诊断2】 判断下列说法是否正确,正确的打√,错误的打×。
(1)粉末状固体药品可以使用纸槽送入试管( )
(2)用红色石蕊试纸检验氨气的性质时,试纸不能润湿( )
(3)长时间盛放石灰水的烧杯应先加入适量的盐酸进行洗涤( )(4)用氢氟酸清洗做过硅酸分解实验的瓷坩埚( )
(5)用湿润的pH试纸测土壤溶液的pH( )
(6)为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡
对照即可( )
(7)用广泛pH试纸测得某CH COOH溶液的pH为2.46( )
3
答案 (1)√ (2)× (3)√ (4)× (5)× (6)× (7)×
考点一 常见仪器的使用方法及注意事项
【典例1】 (2020·山东模考)实验室提供的玻璃仪器有试管、导管、容量瓶、烧
杯、酒精灯、表面皿、玻璃棒(非玻璃仪器任选),选用上述仪器能完成的实验是(
)
A.粗盐的提纯
B.制备乙酸乙酯
C.用四氯化碳萃取碘水中的碘
D.配制0.1 mol·L-1的盐酸溶液
答案 B
解析 粗盐的提纯需要用到漏斗,故A不符合题意;制备乙酸乙酯需要用到
试管、导管、酒精灯,故B符合题意;用四氯化碳萃取碘水中的碘,需要用到分液
漏斗,故C不符合题意;配制0.1 mol·L-1的盐酸溶液,需要用到容量瓶、烧杯、玻
璃棒、胶头滴管,故D不符合题意。
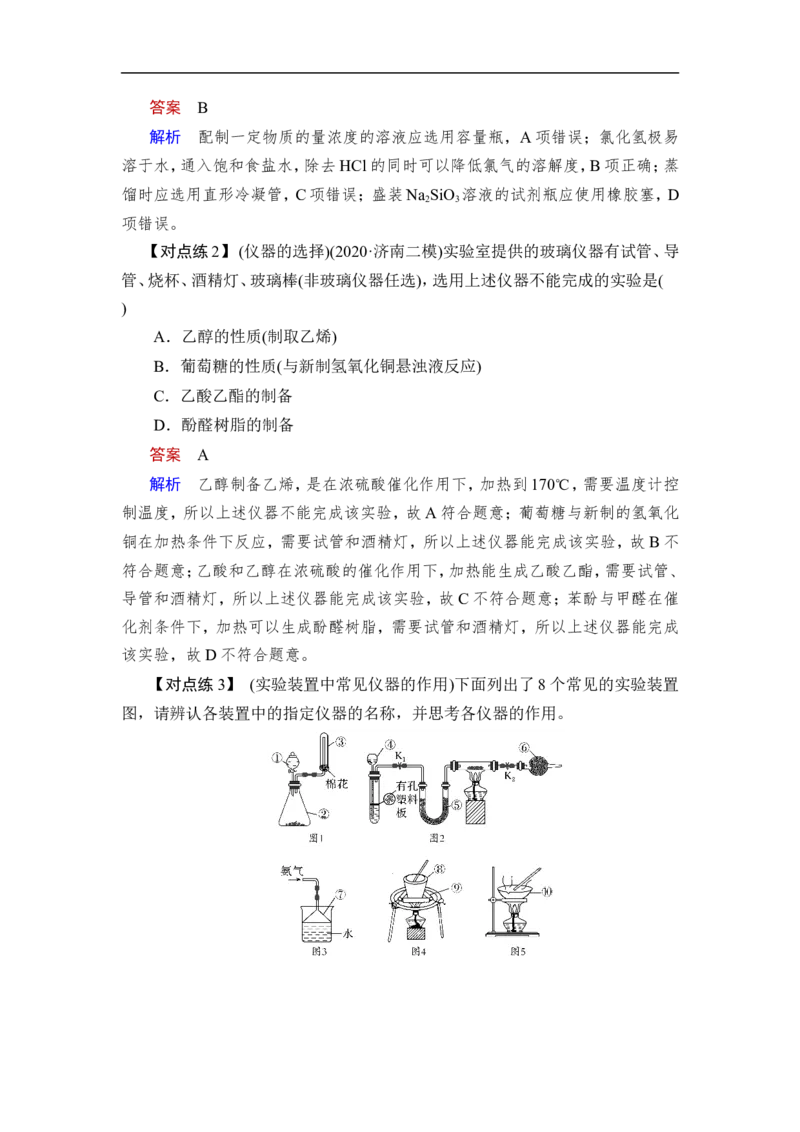
【对点练1】 (仪器的识别)(2020·天津学业水平等级考试)下列实验仪器或装
置的选择正确的是( )
配制50.00 mL 0.100 0mol·L-1 Na CO 溶液 除去Cl 中的HCl
2 3 2
A B
蒸馏用冷凝管 盛装Na SiO 溶液的试剂瓶
2 3
C D答案 B
解析 配制一定物质的量浓度的溶液应选用容量瓶,A项错误;氯化氢极易
溶于水,通入饱和食盐水,除去HCl的同时可以降低氯气的溶解度,B项正确;蒸
馏时应选用直形冷凝管,C项错误;盛装Na SiO 溶液的试剂瓶应使用橡胶塞,D
2 3
项错误。
【对点练2】 (仪器的选择)(2020·济南二模)实验室提供的玻璃仪器有试管、导
管、烧杯、酒精灯、玻璃棒(非玻璃仪器任选),选用上述仪器不能完成的实验是(
)
A.乙醇的性质(制取乙烯)
B.葡萄糖的性质(与新制氢氧化铜悬浊液反应)
C.乙酸乙酯的制备
D.酚醛树脂的制备
答案 A
解析 乙醇制备乙烯,是在浓硫酸催化作用下,加热到170℃,需要温度计控
制温度,所以上述仪器不能完成该实验,故A符合题意;葡萄糖与新制的氢氧化
铜在加热条件下反应,需要试管和酒精灯,所以上述仪器能完成该实验,故B不
符合题意;乙酸和乙醇在浓硫酸的催化作用下,加热能生成乙酸乙酯,需要试管、
导管和酒精灯,所以上述仪器能完成该实验,故C不符合题意;苯酚与甲醛在催
化剂条件下,加热可以生成酚醛树脂,需要试管和酒精灯,所以上述仪器能完成
该实验,故D不符合题意。
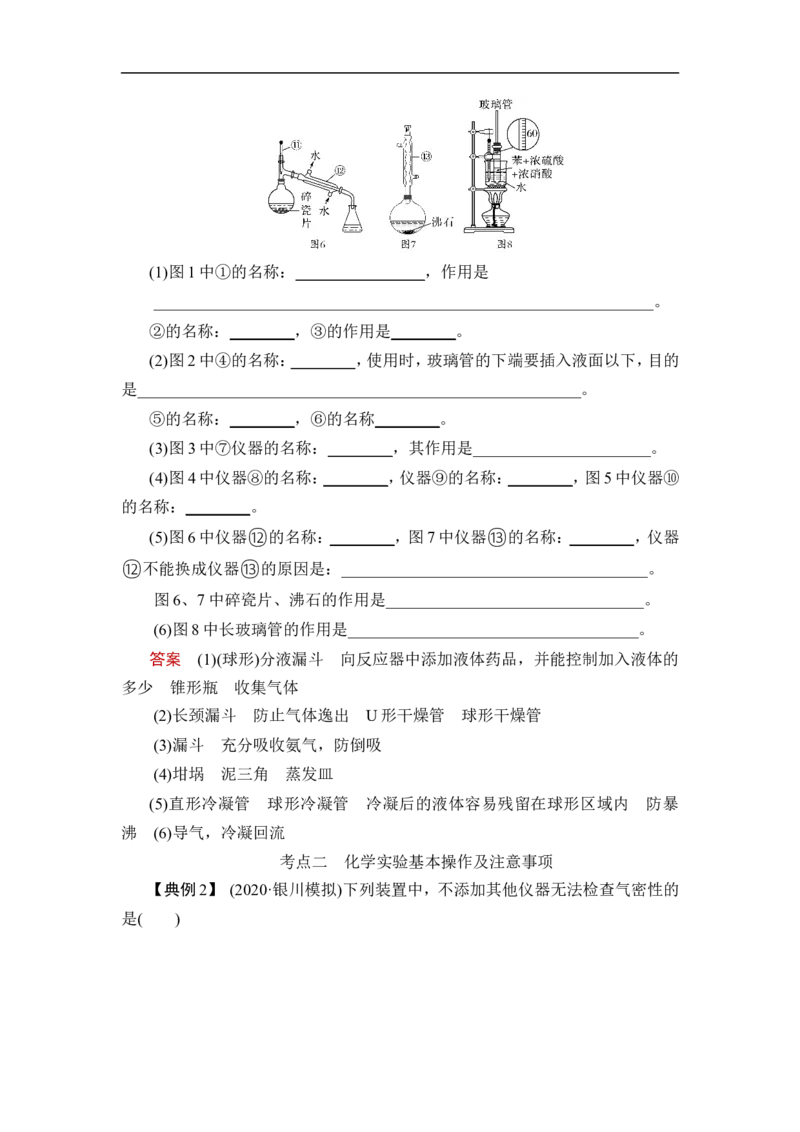
【对点练3】 (实验装置中常见仪器的作用)下面列出了8个常见的实验装置
图,请辨认各装置中的指定仪器的名称,并思考各仪器的作用。(1)图1中①的名称:________________,作用是
______________________________________________________________。
②的名称:________,③的作用是________。
(2)图2中④的名称:________,使用时,玻璃管的下端要插入液面以下,目的
是_______________________________________________________。
⑤的名称:________,⑥的名称________。
(3)图3中⑦仪器的名称:________,其作用是______________________。
(4)图4中仪器⑧的名称:________,仪器⑨的名称:________,图5中仪器⑩
的名称:________。
(5)图6中仪器⑫的名称:________,图7中仪器⑬的名称:________,仪器
⑫不能换成仪器⑬的原因是:______________________________________。
图6、7中碎瓷片、沸石的作用是________________________________。
(6)图8中长玻璃管的作用是____________________________________。
答案 (1)(球形)分液漏斗 向反应器中添加液体药品,并能控制加入液体的
多少 锥形瓶 收集气体
(2)长颈漏斗 防止气体逸出 U形干燥管 球形干燥管
(3)漏斗 充分吸收氨气,防倒吸
(4)坩埚 泥三角 蒸发皿
(5)直形冷凝管 球形冷凝管 冷凝后的液体容易残留在球形区域内 防暴
沸 (6)导气,冷凝回流
考点二 化学实验基本操作及注意事项
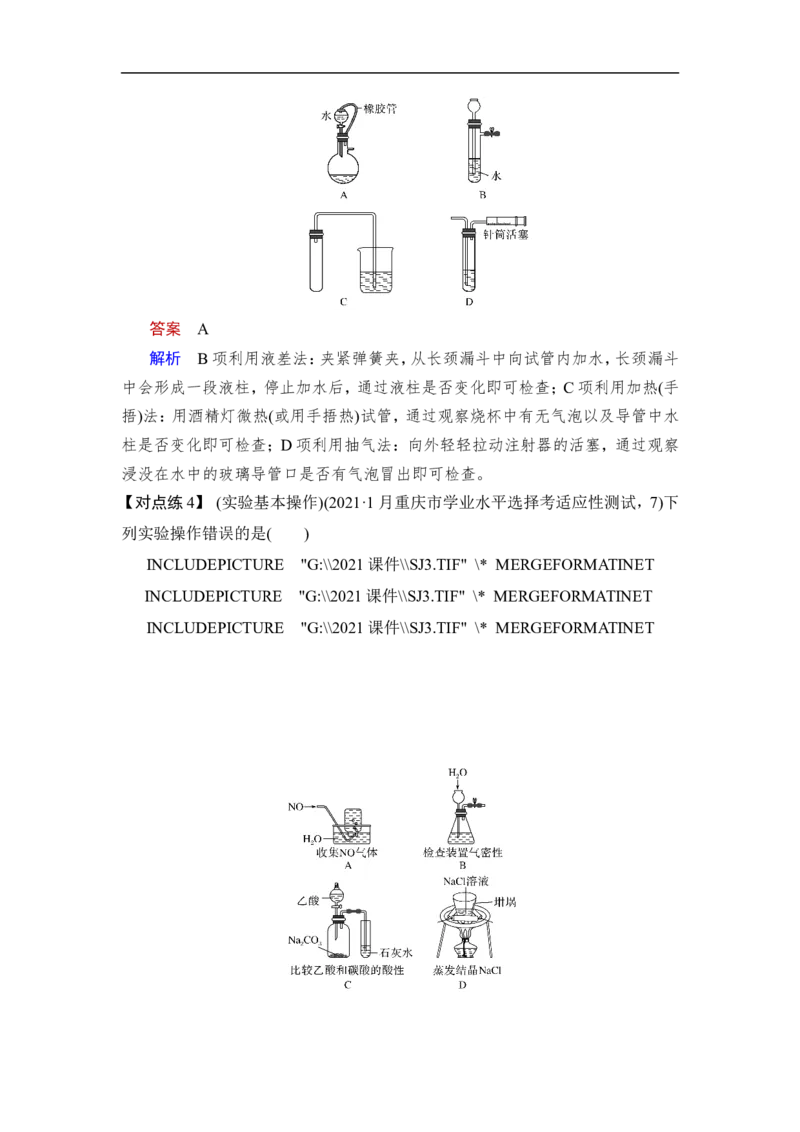
【典例2】 (2020·银川模拟)下列装置中,不添加其他仪器无法检查气密性的
是( )答案 A
解析 B项利用液差法:夹紧弹簧夹,从长颈漏斗中向试管内加水,长颈漏斗
中会形成一段液柱,停止加水后,通过液柱是否变化即可检查;C项利用加热(手
捂)法:用酒精灯微热(或用手捂热)试管,通过观察烧杯中有无气泡以及导管中水
柱是否变化即可检查;D项利用抽气法:向外轻轻拉动注射器的活塞,通过观察
浸没在水中的玻璃导管口是否有气泡冒出即可检查。
【对点练4】 (实验基本操作)(2021·1月重庆市学业水平选择考适应性测试,7)下
列实验操作错误的是( )
INCLUDEPICTURE "G:\\2021课件\\SJ3.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "G:\\2021课件\\SJ3.TIF" \* MERGEFORMATINET
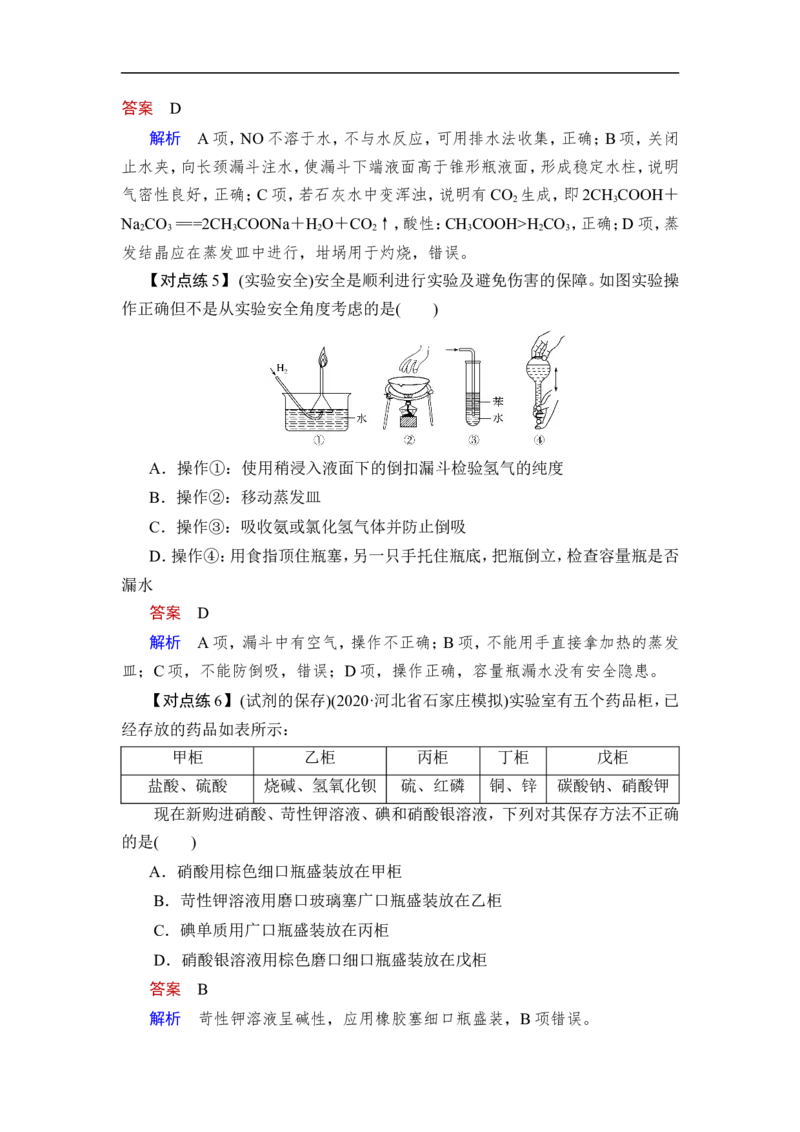
INCLUDEPICTURE "G:\\2021课件\\SJ3.TIF" \* MERGEFORMATINET答案 D
解析 A项,NO不溶于水,不与水反应,可用排水法收集,正确;B项,关闭
止水夹,向长颈漏斗注水,使漏斗下端液面高于锥形瓶液面,形成稳定水柱,说明
气密性良好,正确;C项,若石灰水中变浑浊,说明有CO 生成,即2CH COOH+
2 3
Na CO ===2CH COONa+H O+CO ↑,酸性:CH COOH>H CO ,正确;D项,蒸
2 3 3 2 2 3 2 3
发结晶应在蒸发皿中进行,坩埚用于灼烧,错误。
【对点练5】 (实验安全)安全是顺利进行实验及避免伤害的保障。如图实验操
作正确但不是从实验安全角度考虑的是( )
A.操作①:使用稍浸入液面下的倒扣漏斗检验氢气的纯度
B.操作②:移动蒸发皿
C.操作③:吸收氨或氯化氢气体并防止倒吸
D.操作④:用食指顶住瓶塞,另一只手托住瓶底,把瓶倒立,检查容量瓶是否
漏水
答案 D
解析 A项,漏斗中有空气,操作不正确;B项,不能用手直接拿加热的蒸发
皿;C项,不能防倒吸,错误;D项,操作正确,容量瓶漏水没有安全隐患。
【对点练6】 (试剂的保存)(2020·河北省石家庄模拟)实验室有五个药品柜,已
经存放的药品如表所示:
甲柜 乙柜 丙柜 丁柜 戊柜
盐酸、硫酸 烧碱、氢氧化钡 硫、红磷 铜、锌 碳酸钠、硝酸钾
现在新购进硝酸、苛性钾溶液、碘和硝酸银溶液,下列对其保存方法不正确
的是( )
A.硝酸用棕色细口瓶盛装放在甲柜
B.苛性钾溶液用磨口玻璃塞广口瓶盛装放在乙柜
C.碘单质用广口瓶盛装放在丙柜
D.硝酸银溶液用棕色磨口细口瓶盛装放在戊柜
答案 B
解析 苛性钾溶液呈碱性,应用橡胶塞细口瓶盛装,B项错误。试剂保存“八防”
依据 保存方法 典型实例
①密封或用后立即盖
①Na SO 、Na S、KI溶液等用后立即盖好
2 3 2
好
防氧化 ②FeSO 溶液中加少量铁屑
4
②加入还原剂
③K、Na保存在煤油里,Li保存在石蜡里
③隔绝空气
防与 密封保存,减少暴露时 NaOH、Na CO 溶液、石灰水、Na O 固体
2 3 2 2
CO 反应 间 等密封保存
2
①密封,置于阴凉处 ①浓盐酸、浓氨水等置于阴凉处
防挥发
②液封 ②液溴用水封
置于冷暗处,不与氧化
防燃烧 苯、汽油、酒精等
剂混合贮存,严禁火种
保存在棕色瓶中,并置 浓HNO 、KMnO 溶液、AgNO 溶液、氯水
3 4 3
防分解
于阴暗处 等
FeCl 溶液中加稀盐酸;
3
防水解 加入酸(碱)抑制水解
Na S溶液中加NaOH溶液
2
①腐蚀橡胶的物质用
①浓HNO 、酸性KMnO 溶液、氯水、溴水
3 4
玻璃塞或塑料盖
防腐蚀 等腐蚀橡胶
②腐蚀玻璃的物质用
②氢氟酸保存在塑料瓶中
塑料容器
防黏结 碱性溶液用橡胶塞 NaOH、Na CO 、Na SiO 溶液等
2 3 2 3
微专题39 仪器的组合与创新使用
一、广口瓶的创新使用
装置图 解读
收集密度比空气大的气体,如二氧化碳、氯气、氯化氢
等。操作要点是a进b出
集气瓶 收集密度比空气小的气体,如氢气、氨气等,操作要点
是b进a出
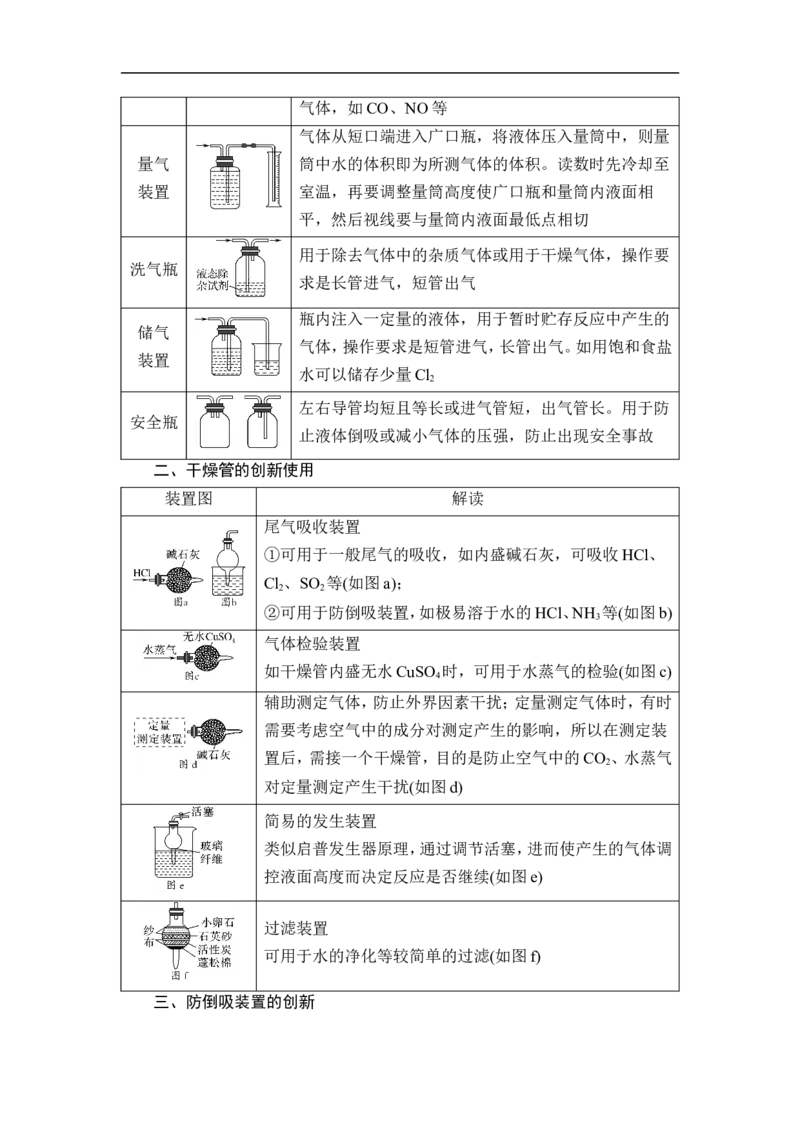
盛满水,“b进a出”可收集不溶于水且不与水反应的气体,如CO、NO等
气体从短口端进入广口瓶,将液体压入量筒中,则量
量气 筒中水的体积即为所测气体的体积。读数时先冷却至
装置 室温,再要调整量筒高度使广口瓶和量筒内液面相
平,然后视线要与量筒内液面最低点相切
用于除去气体中的杂质气体或用于干燥气体,操作要
洗气瓶
求是长管进气,短管出气
瓶内注入一定量的液体,用于暂时贮存反应中产生的
储气
气体,操作要求是短管进气,长管出气。如用饱和食盐
装置
水可以储存少量Cl
2
左右导管均短且等长或进气管短,出气管长。用于防
安全瓶
止液体倒吸或减小气体的压强,防止出现安全事故
二、干燥管的创新使用
装置图 解读
尾气吸收装置
①可用于一般尾气的吸收,如内盛碱石灰,可吸收HCl、
Cl 、SO 等(如图a);
2 2
②可用于防倒吸装置,如极易溶于水的HCl、NH 等(如图b)
3
气体检验装置
如干燥管内盛无水CuSO 时,可用于水蒸气的检验(如图c)
4
辅助测定气体,防止外界因素干扰;定量测定气体时,有时
需要考虑空气中的成分对测定产生的影响,所以在测定装
置后,需接一个干燥管,目的是防止空气中的CO 、水蒸气
2
对定量测定产生干扰(如图d)
简易的发生装置
类似启普发生器原理,通过调节活塞,进而使产生的气体调
控液面高度而决定反应是否继续(如图e)
过滤装置
可用于水的净化等较简单的过滤(如图f)
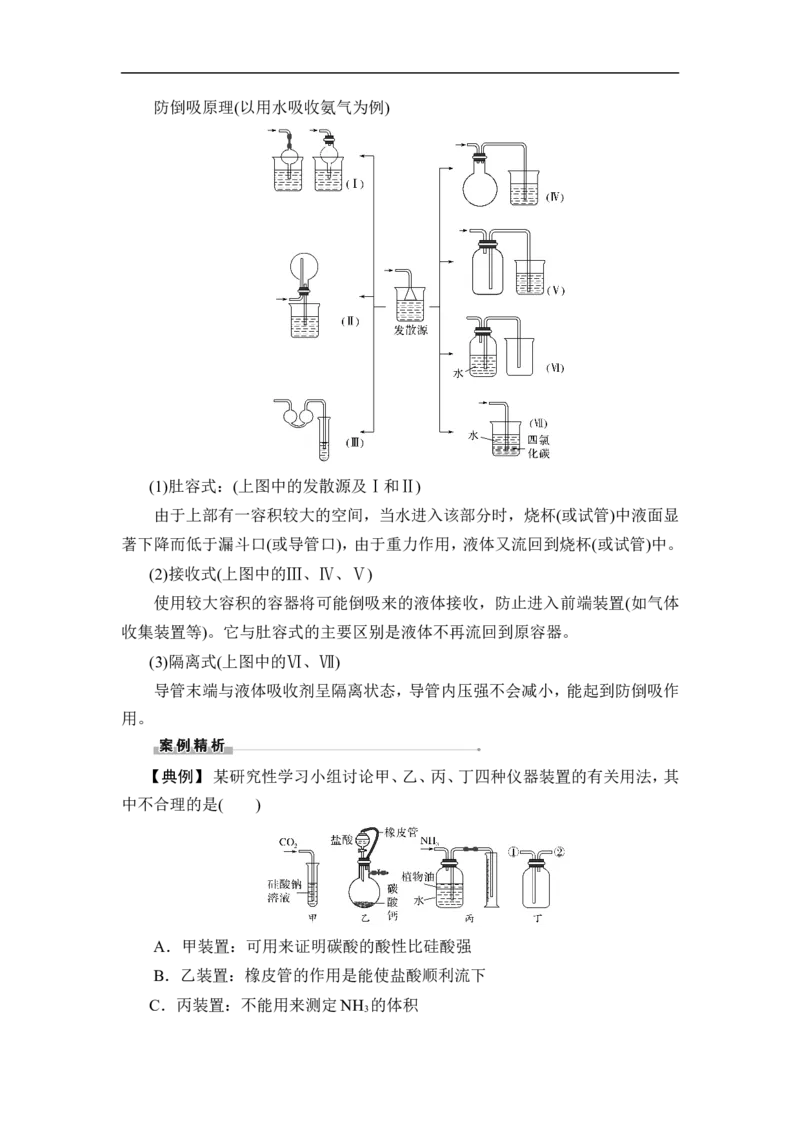
三、防倒吸装置的创新防倒吸原理(以用水吸收氨气为例)
(1)肚容式:(上图中的发散源及Ⅰ和Ⅱ)
由于上部有一容积较大的空间,当水进入该部分时,烧杯(或试管)中液面显
著下降而低于漏斗口(或导管口),由于重力作用,液体又流回到烧杯(或试管)中。
(2)接收式(上图中的Ⅲ、Ⅳ、Ⅴ)
使用较大容积的容器将可能倒吸来的液体接收,防止进入前端装置(如气体
收集装置等)。它与肚容式的主要区别是液体不再流回到原容器。
(3)隔离式(上图中的Ⅵ、Ⅶ)
导管末端与液体吸收剂呈隔离状态,导管内压强不会减小,能起到防倒吸作
用。
【典例】 某研究性学习小组讨论甲、乙、丙、丁四种仪器装置的有关用法,其
中不合理的是( )
A.甲装置:可用来证明碳酸的酸性比硅酸强
B.乙装置:橡皮管的作用是能使盐酸顺利流下
C.丙装置:不能用来测定NH 的体积
3D.丁装置:先从①口进气集满二氧化碳,再从②口进气,可收集氢气
答案 C
解析 植物油能隔离氨气与水的接触,可以将水排出,可以测定氨气的体积,
C错误;导管长进短出可收集密度比空气密度大的气体,短导管进气可收集密度
比空气小的气体,则从①口进气集满二氧化碳,再从②口进气,可收集氢气,D正
确。
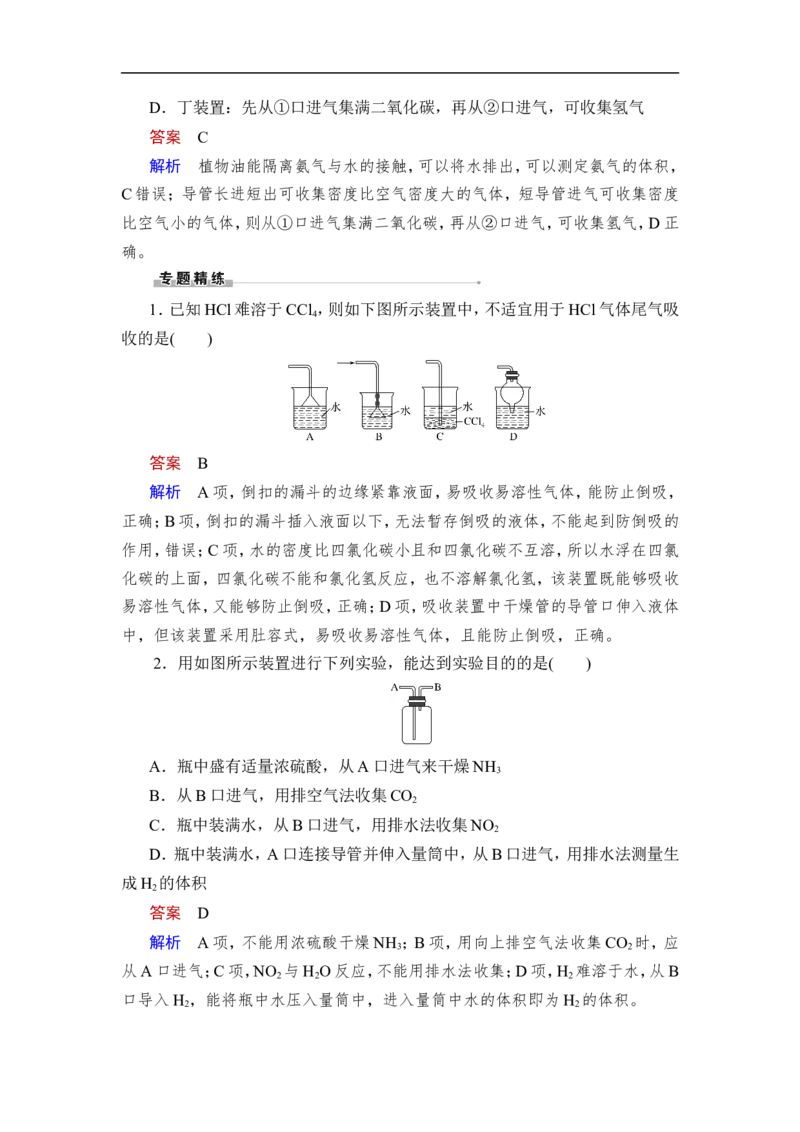
1.已知HCl难溶于CCl ,则如下图所示装置中,不适宜用于HCl气体尾气吸
4
收的是( )
答案 B
解析 A项,倒扣的漏斗的边缘紧靠液面,易吸收易溶性气体,能防止倒吸,
正确;B项,倒扣的漏斗插入液面以下,无法暂存倒吸的液体,不能起到防倒吸的
作用,错误;C项,水的密度比四氯化碳小且和四氯化碳不互溶,所以水浮在四氯
化碳的上面,四氯化碳不能和氯化氢反应,也不溶解氯化氢,该装置既能够吸收
易溶性气体,又能够防止倒吸,正确;D项,吸收装置中干燥管的导管口伸入液体
中,但该装置采用肚容式,易吸收易溶性气体,且能防止倒吸,正确。
2.用如图所示装置进行下列实验,能达到实验目的的是( )
A.瓶中盛有适量浓硫酸,从A口进气来干燥NH
3
B.从B口进气,用排空气法收集CO
2
C.瓶中装满水,从B口进气,用排水法收集NO
2
D.瓶中装满水,A口连接导管并伸入量筒中,从B口进气,用排水法测量生
成H 的体积
2
答案 D
解析 A项,不能用浓硫酸干燥NH ;B项,用向上排空气法收集CO 时,应
3 2
从A口进气;C项,NO 与H O反应,不能用排水法收集;D项,H 难溶于水,从B
2 2 2
口导入H ,能将瓶中水压入量筒中,进入量筒中水的体积即为H 的体积。
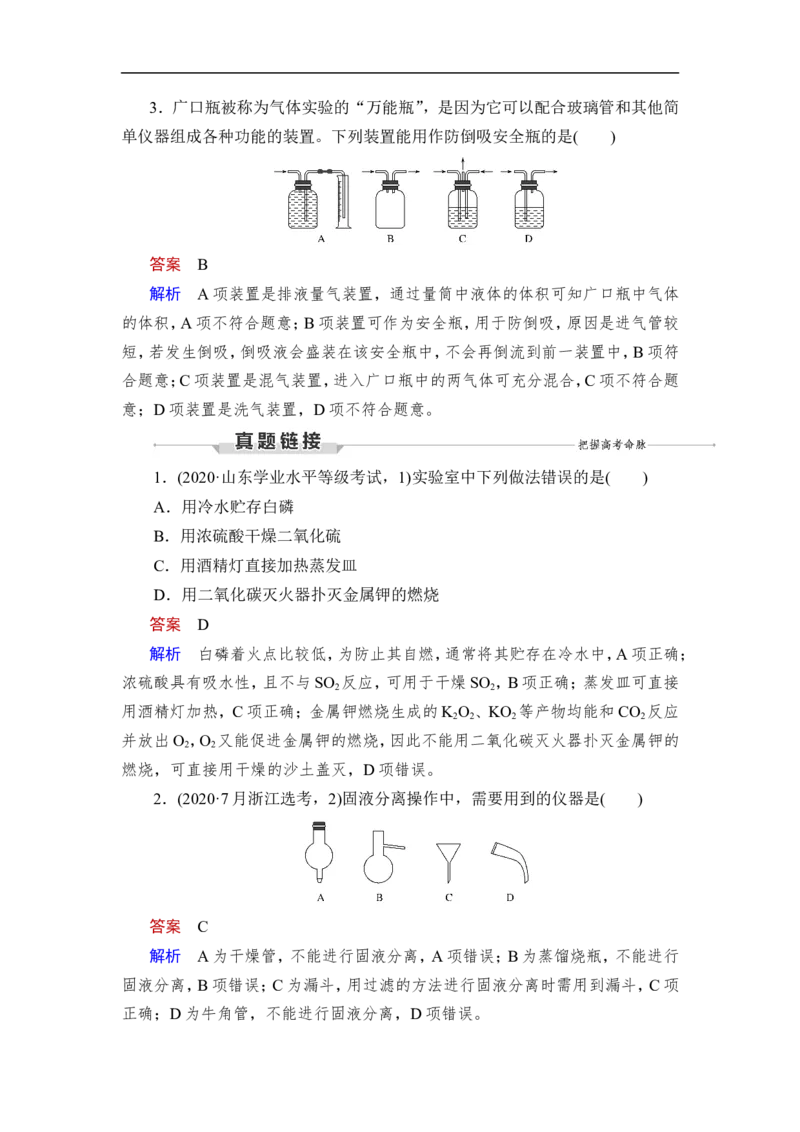
2 23.广口瓶被称为气体实验的“万能瓶”,是因为它可以配合玻璃管和其他简
单仪器组成各种功能的装置。下列装置能用作防倒吸安全瓶的是( )
答案 B
解析 A项装置是排液量气装置,通过量筒中液体的体积可知广口瓶中气体
的体积,A项不符合题意;B项装置可作为安全瓶,用于防倒吸,原因是进气管较
短,若发生倒吸,倒吸液会盛装在该安全瓶中,不会再倒流到前一装置中,B项符
合题意;C项装置是混气装置,进入广口瓶中的两气体可充分混合,C项不符合题
意;D项装置是洗气装置,D项不符合题意。
1.(2020·山东学业水平等级考试,1)实验室中下列做法错误的是( )
A.用冷水贮存白磷
B.用浓硫酸干燥二氧化硫
C.用酒精灯直接加热蒸发皿
D.用二氧化碳灭火器扑灭金属钾的燃烧
答案 D
解析 白磷着火点比较低,为防止其自燃,通常将其贮存在冷水中,A项正确;
浓硫酸具有吸水性,且不与SO 反应,可用于干燥SO ,B项正确;蒸发皿可直接
2 2
用酒精灯加热,C项正确;金属钾燃烧生成的K O 、KO 等产物均能和CO 反应
2 2 2 2
并放出O ,O 又能促进金属钾的燃烧,因此不能用二氧化碳灭火器扑灭金属钾的
2 2
燃烧,可直接用干燥的沙土盖灭,D项错误。
2.(2020·7月浙江选考,2)固液分离操作中,需要用到的仪器是( )
答案 C
解析 A为干燥管,不能进行固液分离,A项错误;B为蒸馏烧瓶,不能进行
固液分离,B项错误;C为漏斗,用过滤的方法进行固液分离时需用到漏斗,C项
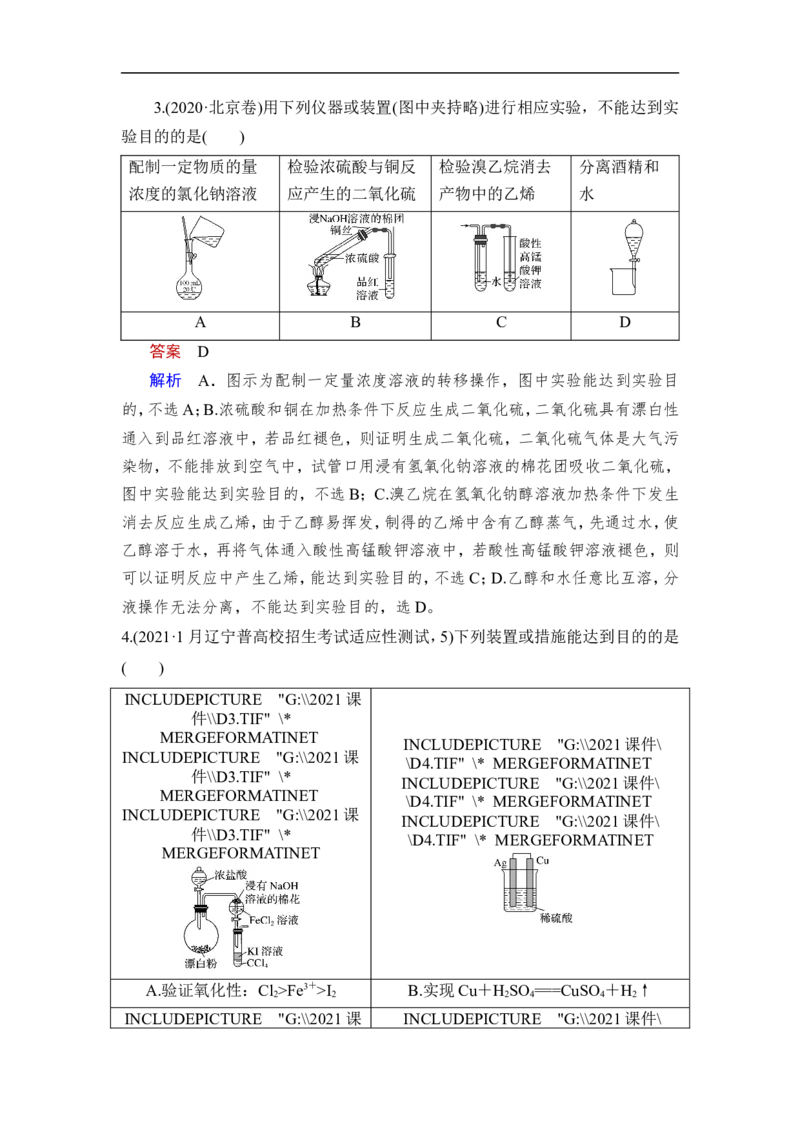
正确;D为牛角管,不能进行固液分离,D项错误。3.(2020·北京卷)用下列仪器或装置(图中夹持略)进行相应实验,不能达到实
验目的的是( )
配制一定物质的量 检验浓硫酸与铜反 检验溴乙烷消去 分离酒精和
浓度的氯化钠溶液 应产生的二氧化硫 产物中的乙烯 水
A B C D
答案 D
解析 A.图示为配制一定量浓度溶液的转移操作,图中实验能达到实验目
的,不选A;B.浓硫酸和铜在加热条件下反应生成二氧化硫,二氧化硫具有漂白性
通入到品红溶液中,若品红褪色,则证明生成二氧化硫,二氧化硫气体是大气污
染物,不能排放到空气中,试管口用浸有氢氧化钠溶液的棉花团吸收二氧化硫,
图中实验能达到实验目的,不选B;C.溴乙烷在氢氧化钠醇溶液加热条件下发生
消去反应生成乙烯,由于乙醇易挥发,制得的乙烯中含有乙醇蒸气,先通过水,使
乙醇溶于水,再将气体通入酸性高锰酸钾溶液中,若酸性高锰酸钾溶液褪色,则
可以证明反应中产生乙烯,能达到实验目的,不选C;D.乙醇和水任意比互溶,分
液操作无法分离,不能达到实验目的,选D。
4.(2021·1月辽宁普高校招生考试适应性测试,5)下列装置或措施能达到目的的是
( )
INCLUDEPICTURE "G:\\2021课
件\\D3.TIF" \*
MERGEFORMATINET
INCLUDEPICTURE "G:\\2021课件\
INCLUDEPICTURE "G:\\2021课
\D4.TIF" \* MERGEFORMATINET
件\\D3.TIF" \*
INCLUDEPICTURE "G:\\2021课件\
MERGEFORMATINET
\D4.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "G:\\2021课
INCLUDEPICTURE "G:\\2021课件\
件\\D3.TIF" \*
\D4.TIF" \* MERGEFORMATINET
MERGEFORMATINET
A.验证氧化性:Cl >Fe3+>I B.实现Cu+H SO ===CuSO +H ↑
2 2 2 4 4 2
INCLUDEPICTURE "G:\\2021课 INCLUDEPICTURE "G:\\2021课件\件\\D5.TIF" \*
MERGEFORMATINET
\D6.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "G:\\2021课
INCLUDEPICTURE "G:\\2021课件\
件\\D5.TIF" \*
\D6.TIF" \* MERGEFORMATINET
MERGEFORMATINET
INCLUDEPICTURE "G:\\2021课件\
INCLUDEPICTURE "G:\\2021课
\D6.TIF" \* MERGEFORMATINET
件\\D5.TIF" \*
MERGEFORMATINET
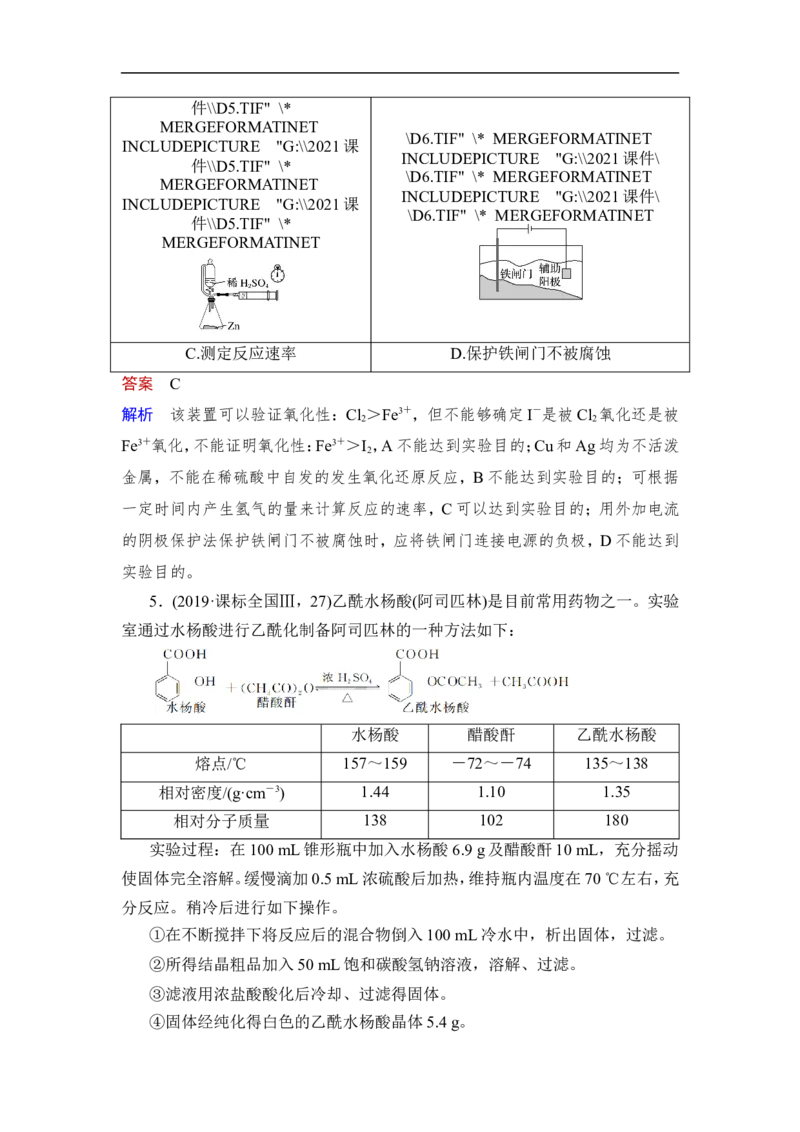
C.测定反应速率 D.保护铁闸门不被腐蚀
答案 C
解析 该装置可以验证氧化性:Cl >Fe3+,但不能够确定I-是被Cl 氧化还是被
2 2
Fe3+氧化,不能证明氧化性:Fe3+>I ,A不能达到实验目的;Cu和Ag均为不活泼
2
金属,不能在稀硫酸中自发的发生氧化还原反应,B不能达到实验目的;可根据
一定时间内产生氢气的量来计算反应的速率,C可以达到实验目的;用外加电流
的阴极保护法保护铁闸门不被腐蚀时,应将铁闸门连接电源的负极,D不能达到
实验目的。
5.(2019·课标全国Ⅲ,27)乙酰水杨酸(阿司匹林)是目前常用药物之一。实验
室通过水杨酸进行乙酰化制备阿司匹林的一种方法如下:
水杨酸 醋酸酐 乙酰水杨酸
熔点/℃ 157~159 -72~-74 135~138
相对密度/(g·cm-3) 1.44 1.10 1.35
相对分子质量 138 102 180
实验过程:在100 mL锥形瓶中加入水杨酸6.9 g及醋酸酐10 mL,充分摇动
使固体完全溶解。缓慢滴加0.5 mL浓硫酸后加热,维持瓶内温度在70 ℃左右,充
分反应。稍冷后进行如下操作。
①在不断搅拌下将反应后的混合物倒入100 mL冷水中,析出固体,过滤。
②所得结晶粗品加入50 mL饱和碳酸氢钠溶液,溶解、过滤。
③滤液用浓盐酸酸化后冷却、过滤得固体。
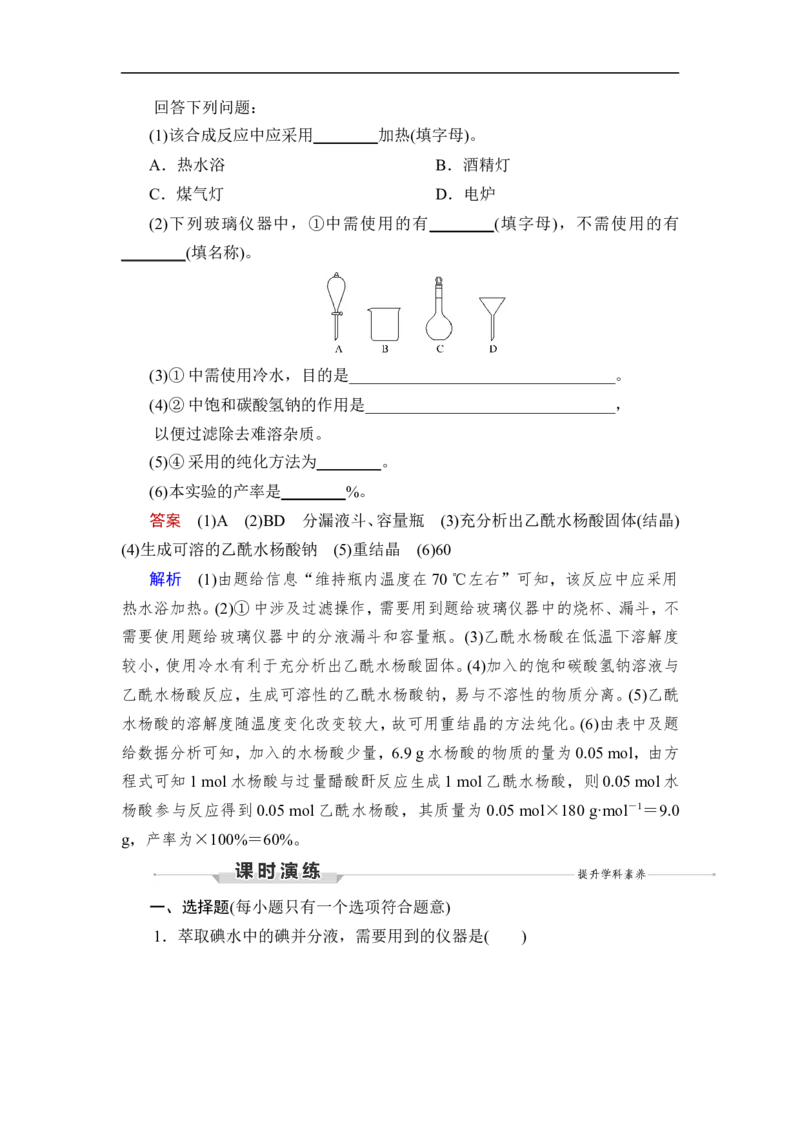
④固体经纯化得白色的乙酰水杨酸晶体5.4 g。回答下列问题:
(1)该合成反应中应采用________加热(填字母)。
A.热水浴 B.酒精灯
C.煤气灯 D.电炉
(2)下列玻璃仪器中,①中需使用的有________(填字母),不需使用的有
________(填名称)。
(3)①中需使用冷水,目的是_________________________________。
(4)②中饱和碳酸氢钠的作用是_______________________________,
以便过滤除去难溶杂质。
(5)④采用的纯化方法为________。
(6)本实验的产率是________%。
答案 (1)A (2)BD 分漏液斗、容量瓶 (3)充分析出乙酰水杨酸固体(结晶)
(4)生成可溶的乙酰水杨酸钠 (5)重结晶 (6)60
解析 (1)由题给信息“维持瓶内温度在70 ℃左右”可知,该反应中应采用
热水浴加热。(2)①中涉及过滤操作,需要用到题给玻璃仪器中的烧杯、漏斗,不
需要使用题给玻璃仪器中的分液漏斗和容量瓶。(3)乙酰水杨酸在低温下溶解度
较小,使用冷水有利于充分析出乙酰水杨酸固体。(4)加入的饱和碳酸氢钠溶液与
乙酰水杨酸反应,生成可溶性的乙酰水杨酸钠,易与不溶性的物质分离。(5)乙酰
水杨酸的溶解度随温度变化改变较大,故可用重结晶的方法纯化。(6)由表中及题
给数据分析可知,加入的水杨酸少量,6.9 g水杨酸的物质的量为0.05 mol,由方
程式可知1 mol水杨酸与过量醋酸酐反应生成1 mol乙酰水杨酸,则0.05 mol水
杨酸参与反应得到0.05 mol乙酰水杨酸,其质量为0.05 mol×180 g·mol-1=9.0
g,产率为×100%=60%。
一、选择题(每小题只有一个选项符合题意)
1.萃取碘水中的碘并分液,需要用到的仪器是( )答案 A
解析 A为分液漏斗,用于分离互不相溶的两种溶液,故选项A正确;B为容
量瓶,用于配制一定物质的量浓度的溶液,故B项错误;C为冷凝管,用于气体冷
凝成液体,多用于蒸馏,故C项错误;D为普通漏斗,用于分离不溶固体和液体,
即过滤,故D项错误。答案选A。
2.下列有关仪器用途的说法中正确的是( )
A.试管、烧杯均可用于给液体、固体加热
B.使食盐水中NaCl晶体析出时,常用到的仪器有坩埚、酒精灯、玻璃棒、泥
三角
C.区别NaCl、Na SO 时常用到胶头滴管、试管
2 4
D.漏斗可用于过滤及向滴定管中添加溶液
答案 C
3.下列保存物质的方法正确的是( )
A.液溴易挥发,存放在带橡胶塞的试剂瓶中,并加水封
B.波尔多液盛放在铁制容器中
C.氨水易挥发,应密封且在低温处保存
D.金属锂应保存在煤油中,防止被氧化
答案 C
解析 液溴能腐蚀橡胶,A错误;波尔多液中的CuSO 能与Fe发生置换反应
4
B错误;金属锂的密度比煤油小,会漂浮在煤油上面,锂和空气中的氧气、水蒸气
等均能发生反应,金属锂应保存在固体石蜡中,D错误。
4.某学生的实验报告中有如下数据:①用托盘天平称取21.7 g食盐;②用量
筒量取21.48 mL盐酸;③用容量瓶配制210 mL 1 mol·L-1的硫酸溶液;④用标准
NaOH溶液滴定未知浓度的盐酸,用去18.20 mL NaOH溶液,其中数据合理的是(
)
A.①④ B.②④
C.①③ D.②③
答案 A
解析 托盘天平的精确度为0.1 g,①正确;量筒精确度为0.1 mL,②错误;容量瓶的规格中有100 mL、250 mL、500 mL、1 000 mL等,没有210 mL的容量瓶,
③错误;中和滴定要用滴定管,滴定管的精确度为0.01 mL,题中18.20 mL的数
值合理,④正确。
5.(2020·河北五校联考)下列有关仪器的使用方法或实验操作正确的是(
)
A.用坩埚灼烧干海带制海带灰
B.蒸馏时,温度计水银球插入液面以下
C.用长颈漏斗分离CCl 萃取碘后的水层与有机层
4
D.用容量瓶配制溶液时,若加水超过刻度线,用胶头滴管吸出多余液体
答案 A
解析 A.灼烧干海带在坩埚中进行,故A正确;B.蒸馏时温度计测定馏分蒸
气的温度,温度计的水银球应在蒸馏烧瓶的支管口处,故B错误;C.萃取应选分
液漏斗,用分液漏斗分离CCl 萃取碘后的水层与有机层,故C错误;D.若加水超
4
过刻度线,配制失败,应重新配制,故D错误;故答案为A。
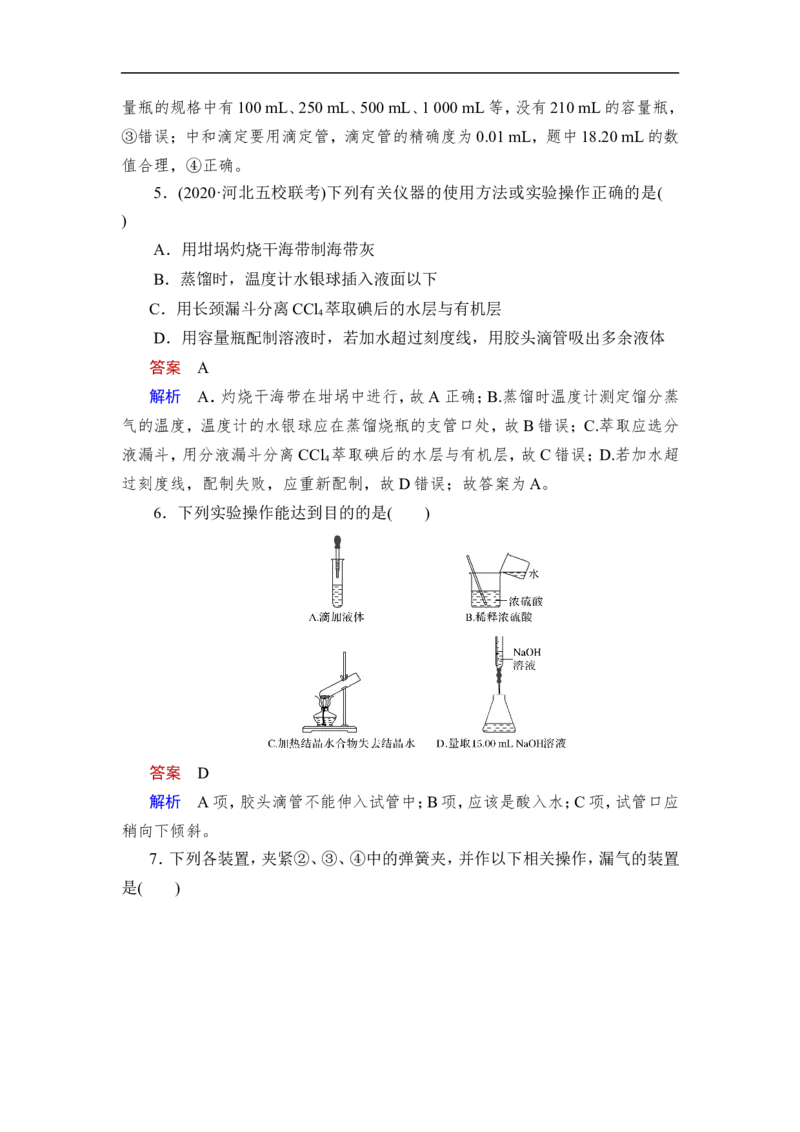
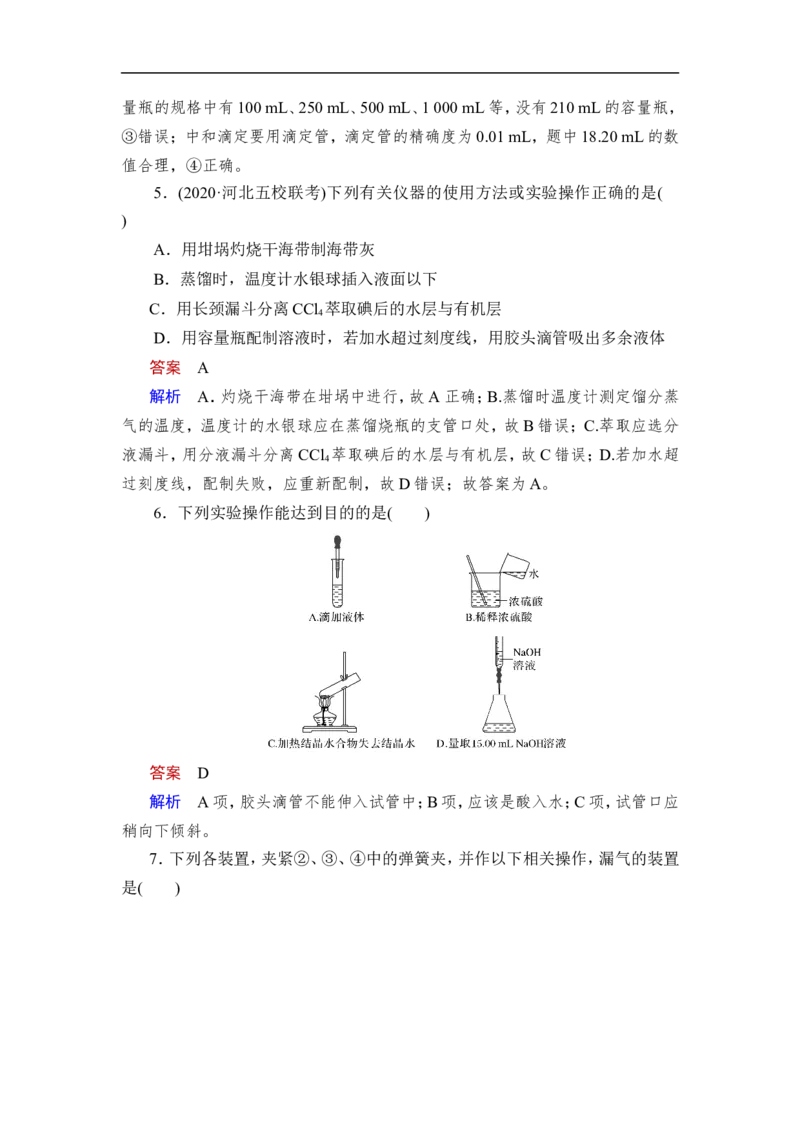
6.下列实验操作能达到目的的是( )
答案 D
解析 A项,胶头滴管不能伸入试管中;B项,应该是酸入水;C项,试管口应
稍向下倾斜。
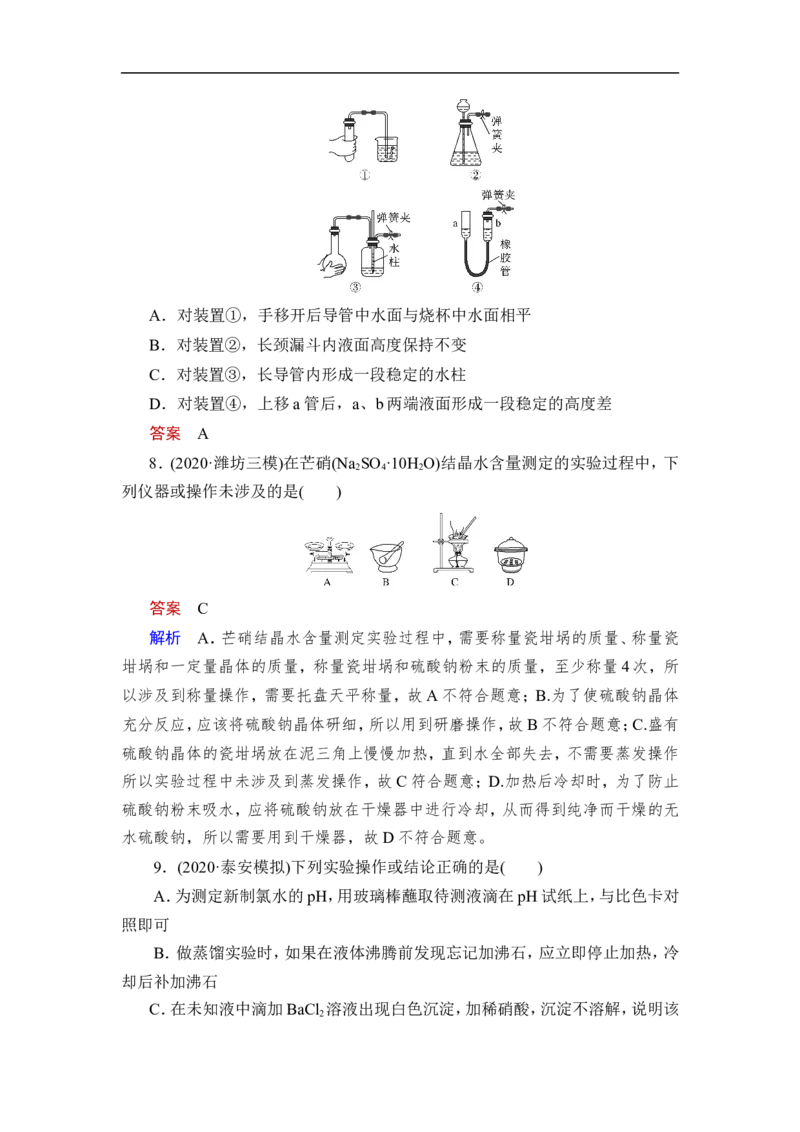
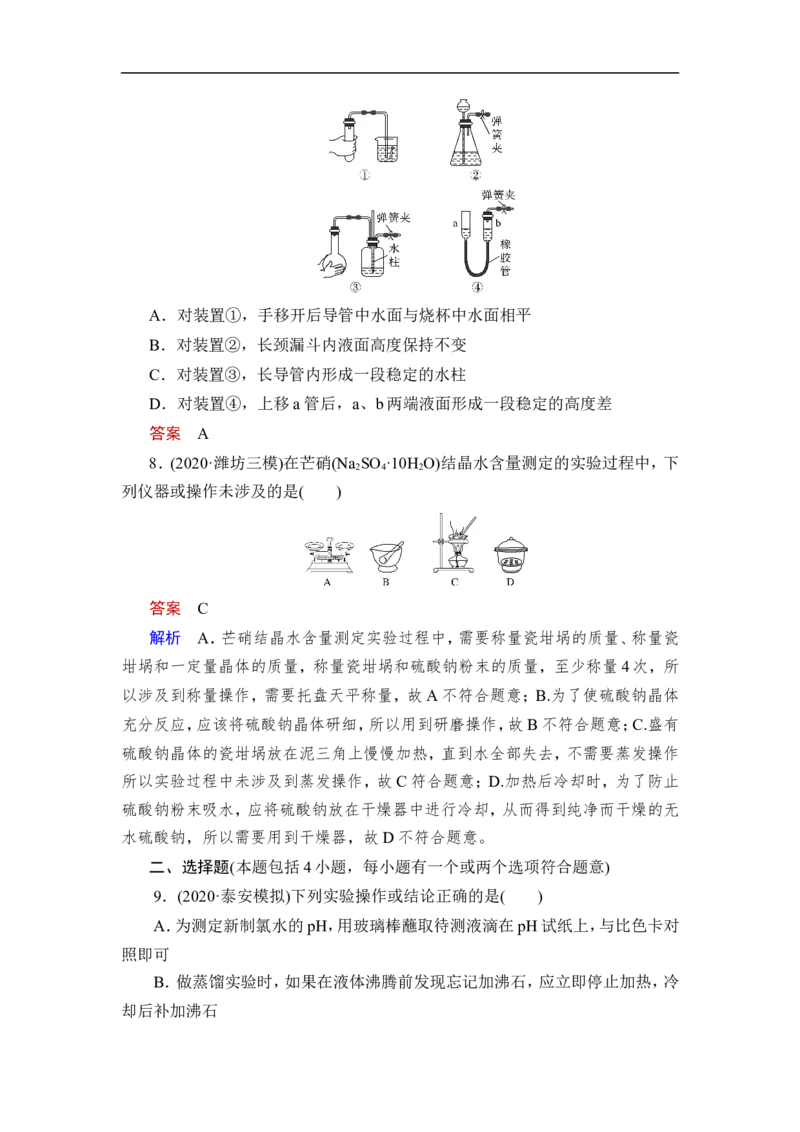
7.下列各装置,夹紧②、③、④中的弹簧夹,并作以下相关操作,漏气的装置
是( )A.对装置①,手移开后导管中水面与烧杯中水面相平
B.对装置②,长颈漏斗内液面高度保持不变
C.对装置③,长导管内形成一段稳定的水柱
D.对装置④,上移a管后,a、b两端液面形成一段稳定的高度差
答案 A
8.(2020·潍坊三模)在芒硝(Na SO ·10H O)结晶水含量测定的实验过程中,下
2 4 2
列仪器或操作未涉及的是( )
答案 C
解析 A.芒硝结晶水含量测定实验过程中,需要称量瓷坩埚的质量、称量瓷
坩埚和一定量晶体的质量,称量瓷坩埚和硫酸钠粉末的质量,至少称量4次,所
以涉及到称量操作,需要托盘天平称量,故A不符合题意;B.为了使硫酸钠晶体
充分反应,应该将硫酸钠晶体研细,所以用到研磨操作,故B不符合题意;C.盛有
硫酸钠晶体的瓷坩埚放在泥三角上慢慢加热,直到水全部失去,不需要蒸发操作
所以实验过程中未涉及到蒸发操作,故C符合题意;D.加热后冷却时,为了防止
硫酸钠粉末吸水,应将硫酸钠放在干燥器中进行冷却,从而得到纯净而干燥的无
水硫酸钠,所以需要用到干燥器,故D不符合题意。
9.(2020·泰安模拟)下列实验操作或结论正确的是( )
A.为测定新制氯水的pH,用玻璃棒蘸取待测液滴在pH试纸上,与比色卡对
照即可
B.做蒸馏实验时,如果在液体沸腾前发现忘记加沸石,应立即停止加热,冷
却后补加沸石
C.在未知液中滴加BaCl 溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该
2未知液中一定存在SO
D.提纯混有少量硝酸钾的氯化钠,采用在较高的温度下制成浓溶液再冷却
结晶、过滤、干燥的方法
答案 B
解析 氯水中的次氯酸能漂白pH试纸,不能用pH试纸测定新制氯水的pH,
A错误;液体加热要加沸石或碎瓷片,引入汽化中心,可防止溶液暴沸,如果加热
一段时间后发现忘记加碎瓷片,应该停止加热,待溶液冷却后重新添加碎瓷片,B
正确;硫酸钡和AgCl均为不溶于酸的白色沉淀,则向某溶液中加入BaCl 溶液生
2
成白色沉淀,继续加稀硝酸沉淀不消失,溶液中可能含Ag+、SO、SO,C错误;氯
化钠中混有少量的硝酸钾,氯化钠是大量的,制得的饱和溶液中硝酸钾量较少,
不能采取降温结晶的方法,D错误。
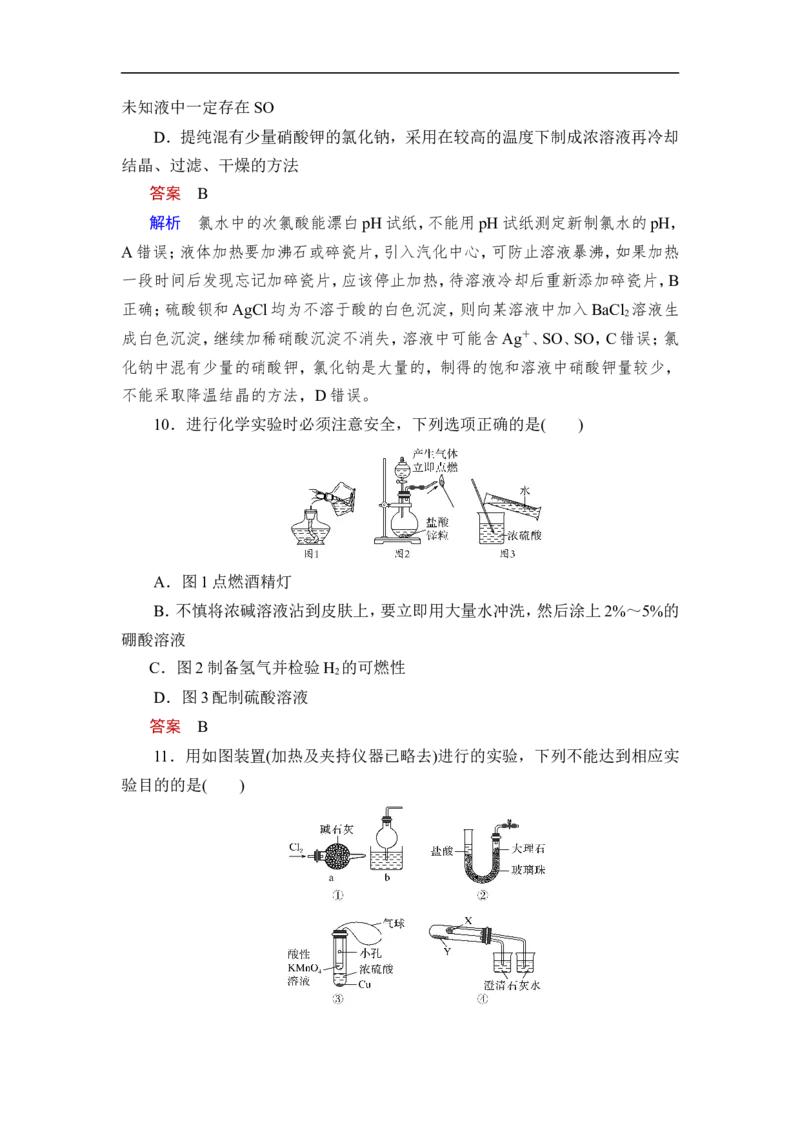
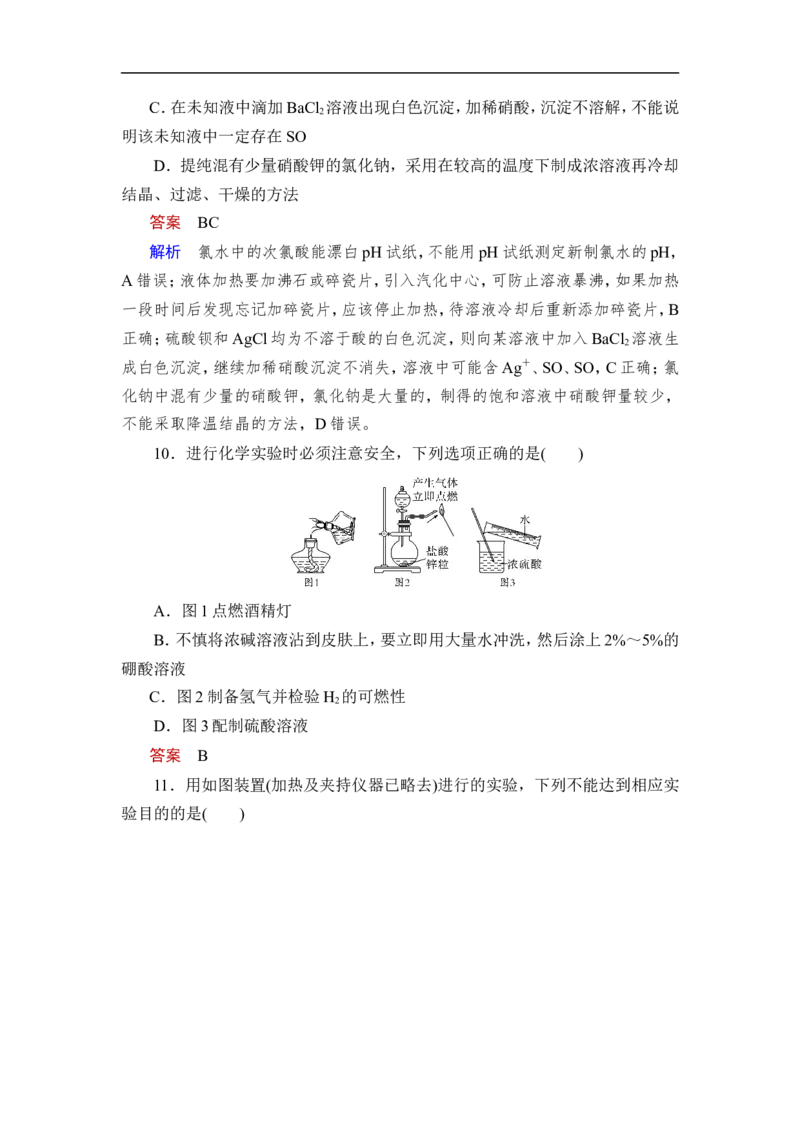
10.进行化学实验时必须注意安全,下列选项正确的是( )
A.图1点燃酒精灯
B.不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上2%~5%的
硼酸溶液
C.图2制备氢气并检验H 的可燃性
2
D.图3配制硫酸溶液
答案 B
11.用如图装置(加热及夹持仪器已略去)进行的实验,下列不能达到相应实
验目的的是( )A.装置①中的a可用于吸收尾气中的Cl ,b可用于吸收气体时防倒吸
2
B.装置②可实现制取CO 实验中的“即关即止,即开即用”的作用
2
C.利用装置③制取SO ,并验证其漂白性
2
D.利用装置④验证KHCO 和K CO 的热稳定性,X中应放的物质是KHCO
3 2 3 3
答案 C
解析 ①中碱石灰可吸收Cl ,b常用于防倒吸;②关闭止水夹时,产生的CO
2 2
将盐酸压入左侧,大理石与盐酸分离,反应停止,打开止水夹时,CO 气体排出,
2
压强减小,盐酸又流回右侧与大理石反应产生CO ;③中大试管中Cu与浓硫酸反
2
应生成SO 气体,若小试管中酸性KMnO 溶液褪色,则证明SO 具有还原性而不
2 4 2
是漂白性,C项不能达到实验目的;④中KHCO 受热不稳定,X中应放的物质是
3
KHCO 。
3
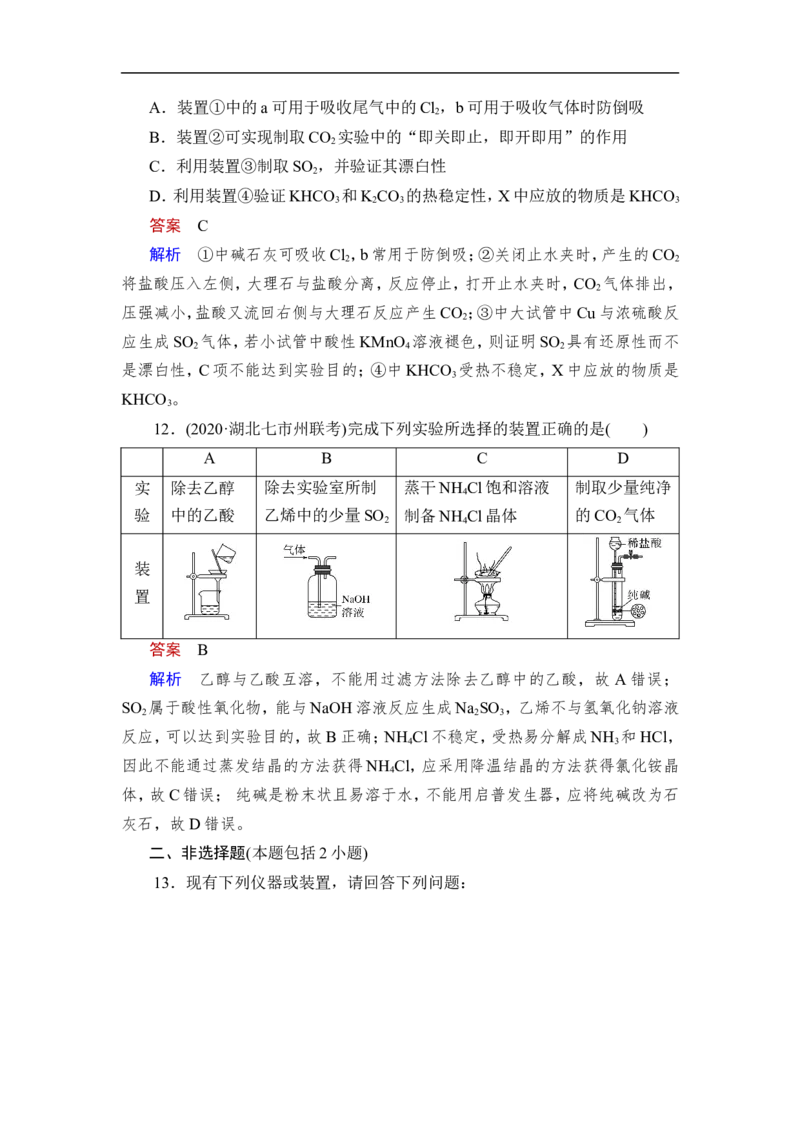
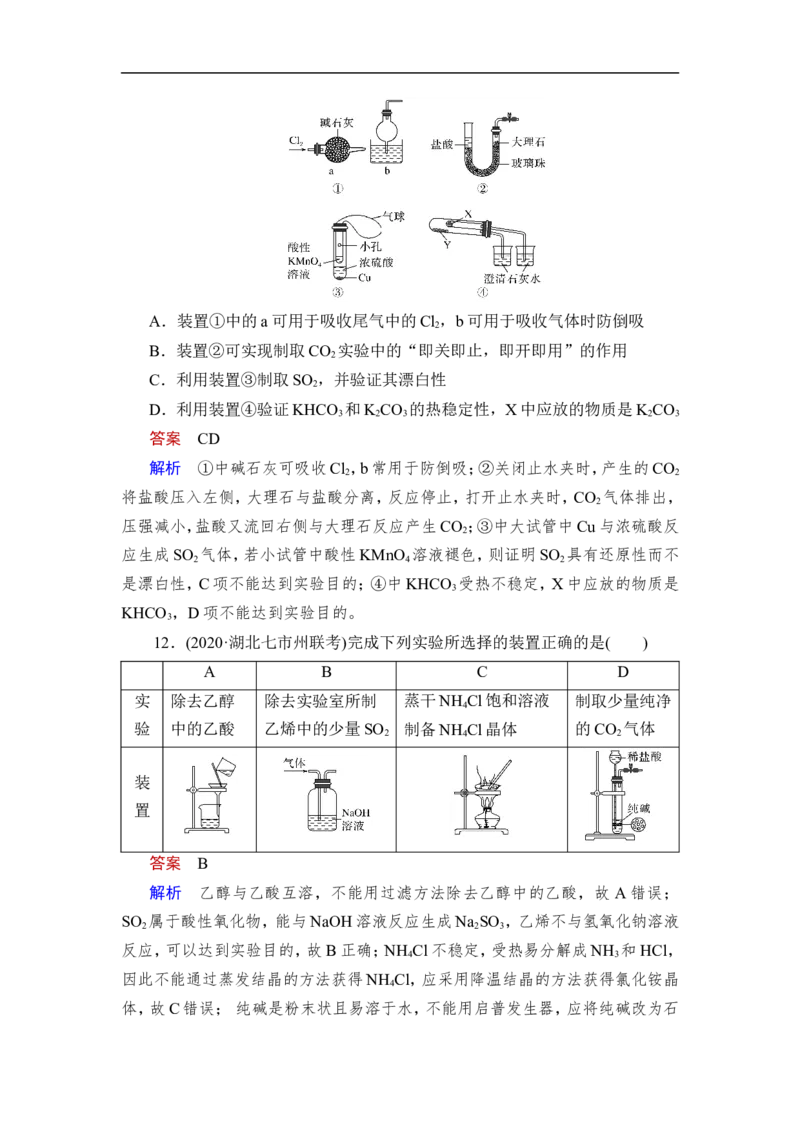
12.(2020·湖北七市州联考)完成下列实验所选择的装置正确的是( )
A B C D
实 除去乙醇 除去实验室所制 蒸干NH Cl饱和溶液 制取少量纯净
4
验 中的乙酸 乙烯中的少量SO 制备NH Cl晶体 的CO 气体
2 4 2
装
置
答案 B
解析 乙醇与乙酸互溶,不能用过滤方法除去乙醇中的乙酸,故 A错误;
SO 属于酸性氧化物,能与NaOH溶液反应生成Na SO ,乙烯不与氢氧化钠溶液
2 2 3
反应,可以达到实验目的,故B正确;NH Cl不稳定,受热易分解成NH 和HCl,
4 3
因此不能通过蒸发结晶的方法获得NH Cl,应采用降温结晶的方法获得氯化铵晶
4
体,故C错误; 纯碱是粉末状且易溶于水,不能用启普发生器,应将纯碱改为石
灰石,故D错误。
二、非选择题(本题包括2小题)
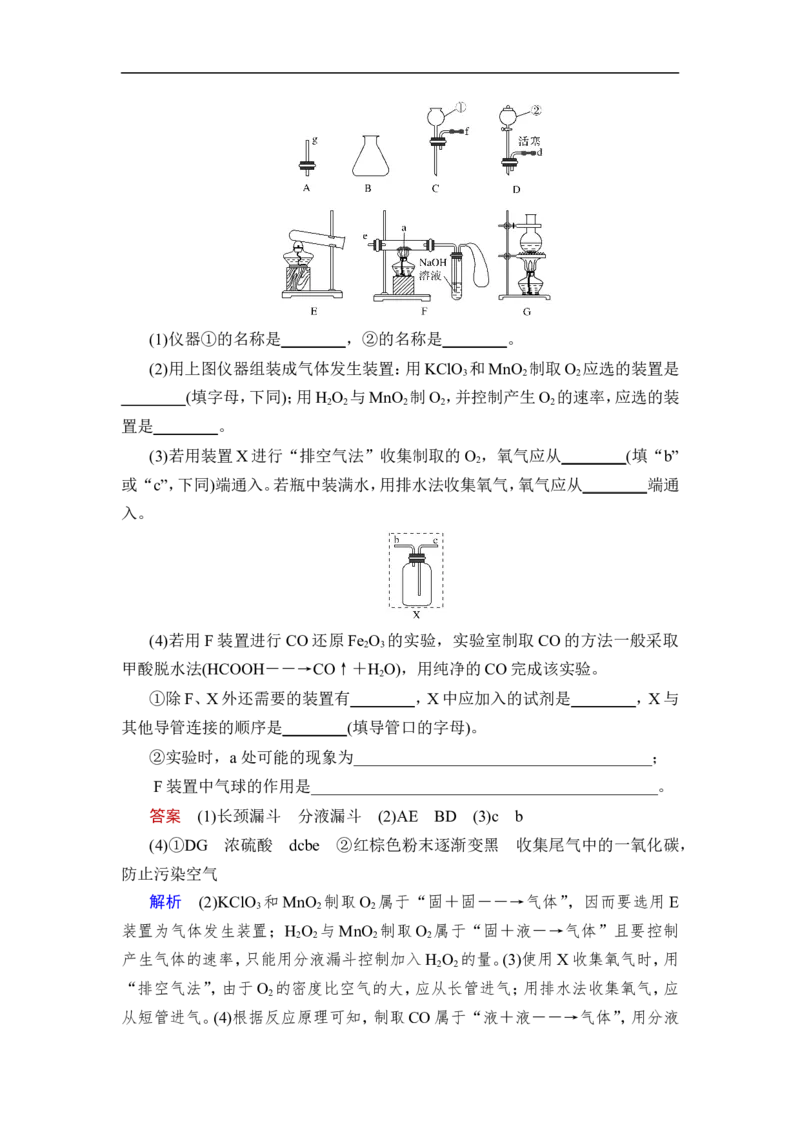
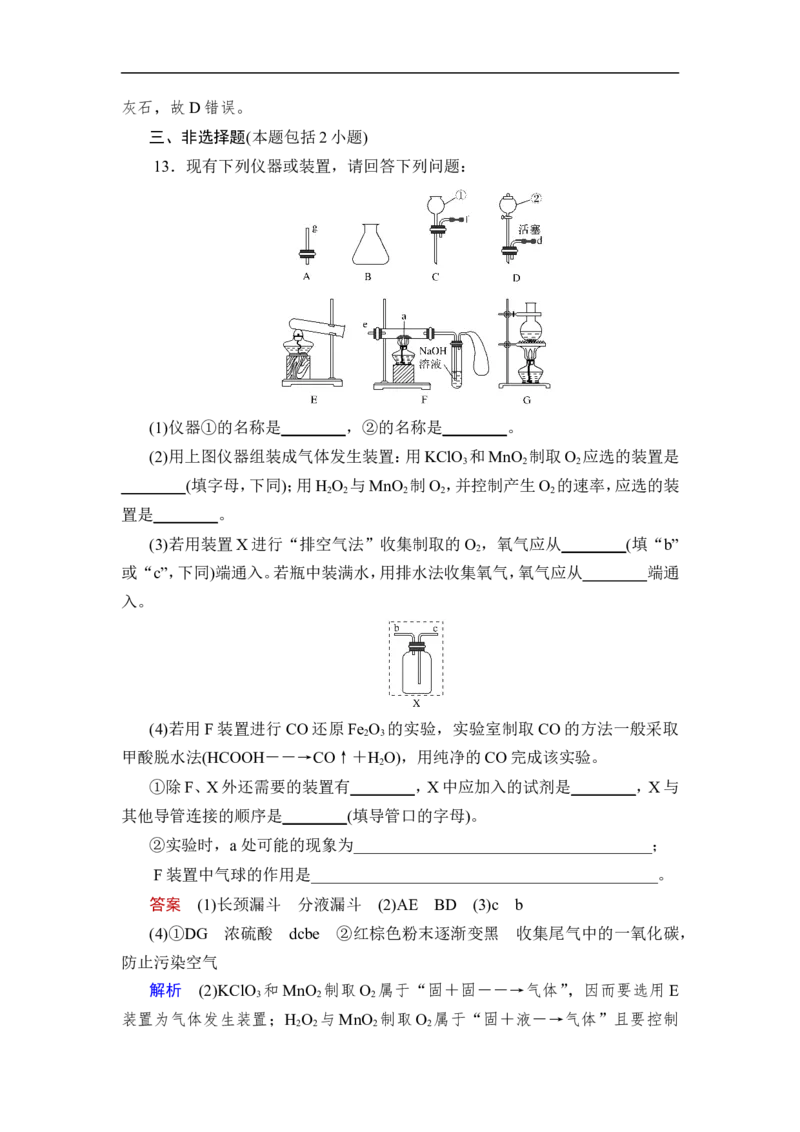
13.现有下列仪器或装置,请回答下列问题:(1)仪器①的名称是________,②的名称是________。
(2)用上图仪器组装成气体发生装置:用KClO 和MnO 制取O 应选的装置是
3 2 2
________(填字母,下同);用H O 与MnO 制O ,并控制产生O 的速率,应选的装
2 2 2 2 2
置是________。
(3)若用装置X进行“排空气法”收集制取的O ,氧气应从________(填“b”
2
或“c”,下同)端通入。若瓶中装满水,用排水法收集氧气,氧气应从________端通
入。
(4)若用F装置进行CO还原Fe O 的实验,实验室制取 CO的方法一般采取
2 3
甲酸脱水法(HCOOH――→CO↑+H O),用纯净的CO完成该实验。
2
①除F、X外还需要的装置有________,X中应加入的试剂是________,X与
其他导管连接的顺序是________(填导管口的字母)。
②实验时,a处可能的现象为_____________________________________;
F装置中气球的作用是___________________________________________。
答案 (1)长颈漏斗 分液漏斗 (2)AE BD (3)c b
(4)①DG 浓硫酸 dcbe ②红棕色粉末逐渐变黑 收集尾气中的一氧化碳,
防止污染空气
解析 (2)KClO 和MnO 制取O 属于“固+固――→气体”,因而要选用E
3 2 2
装置为气体发生装置;H O 与MnO 制取O 属于“固+液―→气体”且要控制
2 2 2 2
产生气体的速率,只能用分液漏斗控制加入H O 的量。(3)使用X收集氧气时,用
2 2
“排空气法”,由于O 的密度比空气的大,应从长管进气;用排水法收集氧气,应
2
从短管进气。(4)根据反应原理可知,制取CO属于“液+液――→气体”,用分液漏斗控制加入浓硫酸的量,应选D、G为气体发生装置,X的作用是除去CO中的
水蒸气,洗气时气体流向为“长进短出”。
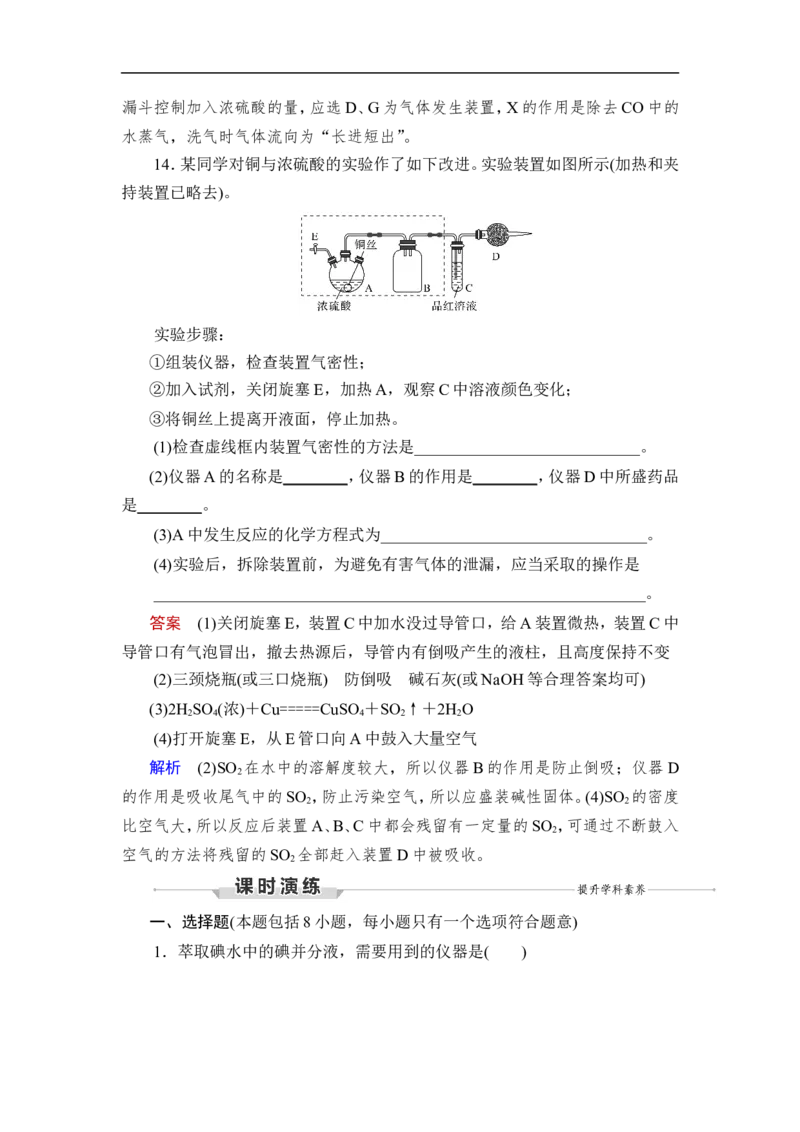
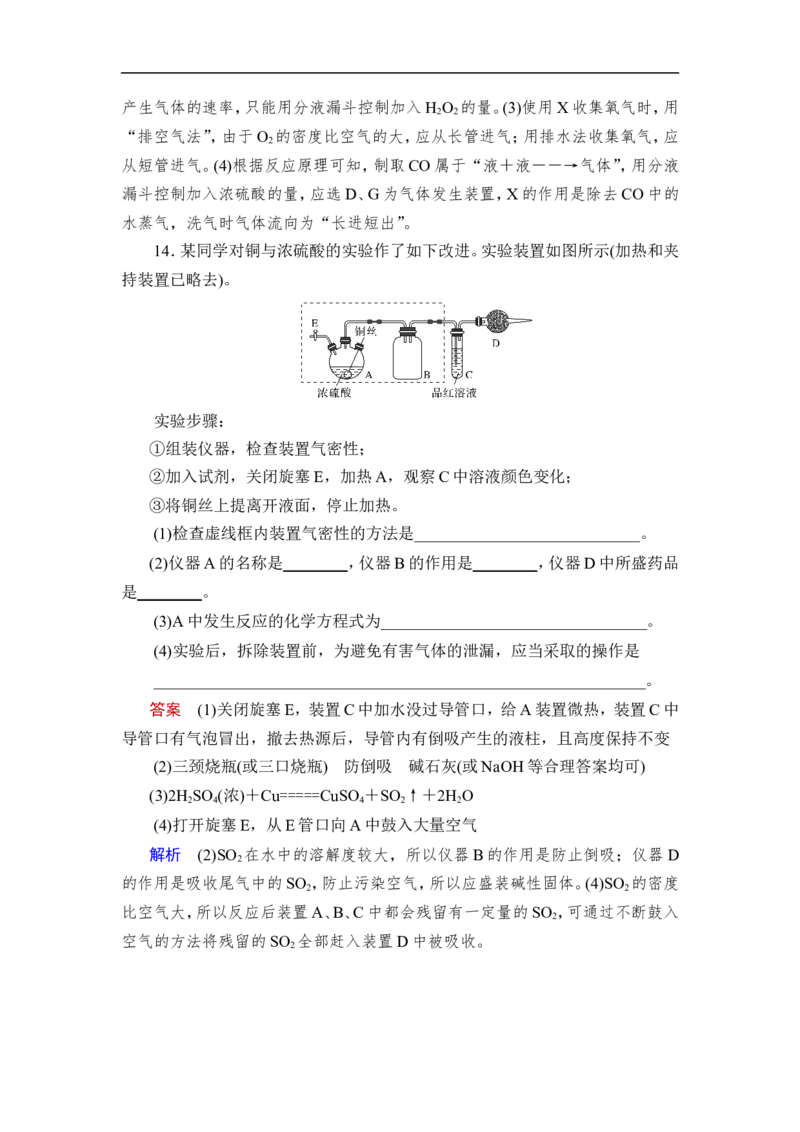
14.某同学对铜与浓硫酸的实验作了如下改进。实验装置如图所示(加热和夹
持装置已略去)。
实验步骤:
①组装仪器,检查装置气密性;
②加入试剂,关闭旋塞E,加热A,观察C中溶液颜色变化;
③将铜丝上提离开液面,停止加热。
(1)检查虚线框内装置气密性的方法是____________________________。
(2)仪器A的名称是________,仪器B的作用是________,仪器D中所盛药品
是________。
(3)A中发生反应的化学方程式为_________________________________。
(4)实验后,拆除装置前,为避免有害气体的泄漏,应当采取的操作是
_____________________________________________________________。
答案 (1)关闭旋塞E,装置C中加水没过导管口,给A装置微热,装置C中
导管口有气泡冒出,撤去热源后,导管内有倒吸产生的液柱,且高度保持不变
(2)三颈烧瓶(或三口烧瓶) 防倒吸 碱石灰(或NaOH等合理答案均可)
(3)2H SO (浓)+Cu=====CuSO +SO ↑+2H O
2 4 4 2 2
(4)打开旋塞E,从E管口向A中鼓入大量空气
解析 (2)SO 在水中的溶解度较大,所以仪器B的作用是防止倒吸;仪器D
2
的作用是吸收尾气中的SO ,防止污染空气,所以应盛装碱性固体。(4)SO 的密度
2 2
比空气大,所以反应后装置A、B、C中都会残留有一定量的SO ,可通过不断鼓入
2
空气的方法将残留的SO 全部赶入装置D中被吸收。
2
一、选择题(本题包括8小题,每小题只有一个选项符合题意)
1.萃取碘水中的碘并分液,需要用到的仪器是( )答案 A
解析 A为分液漏斗,用于分离互不相溶的两种溶液,故选项A正确;B为容
量瓶,用于配制一定物质的量浓度的溶液,故B项错误;C为冷凝管,用于气体冷
凝成液体,多用于蒸馏,故C项错误;D为普通漏斗,用于分离不溶固体和液体,
即过滤,故D项错误。答案选A。
2.下列有关仪器用途的说法中正确的是( )
A.试管、烧杯均可用于给液体、固体加热
B.使食盐水中NaCl晶体析出时,常用到的仪器有坩埚、酒精灯、玻璃棒、泥
三角
C.区别NaCl、Na SO 时常用到胶头滴管、试管
2 4
D.漏斗可用于过滤及向滴定管中添加溶液
答案 C
3.下列保存物质的方法正确的是( )
A.液溴易挥发,存放在带橡胶塞的试剂瓶中,并加水封
B.波尔多液盛放在铁制容器中
C.氨水易挥发,应密封且在低温处保存
D.金属锂应保存在煤油中,防止被氧化
答案 C
解析 液溴能腐蚀橡胶,A错误;波尔多液中的CuSO 能与Fe发生置换反应
4
B错误;金属锂的密度比煤油小,会漂浮在煤油上面,锂和空气中的氧气、水蒸气
等均能发生反应,金属锂应保存在固体石蜡中,D错误。
4.某学生的实验报告中有如下数据:①用托盘天平称取21.7 g食盐;②用量
筒量取21.48 mL盐酸;③用容量瓶配制210 mL 1 mol·L-1的硫酸溶液;④用标准
NaOH溶液滴定未知浓度的盐酸,用去18.20 mL NaOH溶液,其中数据合理的是(
)
A.①④ B.②④
C.①③ D.②③
答案 A
解析 托盘天平的精确度为0.1 g,①正确;量筒精确度为0.1 mL,②错误;容量瓶的规格中有100 mL、250 mL、500 mL、1 000 mL等,没有210 mL的容量瓶,
③错误;中和滴定要用滴定管,滴定管的精确度为0.01 mL,题中18.20 mL的数
值合理,④正确。
5.(2020·河北五校联考)下列有关仪器的使用方法或实验操作正确的是(
)
A.用坩埚灼烧干海带制海带灰
B.蒸馏时,温度计水银球插入液面以下
C.用长颈漏斗分离CCl 萃取碘后的水层与有机层
4
D.用容量瓶配制溶液时,若加水超过刻度线,用胶头滴管吸出多余液体
答案 A
解析 A.灼烧干海带在坩埚中进行,故A正确;B.蒸馏时温度计测定馏分蒸
气的温度,温度计的水银球应在蒸馏烧瓶的支管口处,故B错误;C.萃取应选分
液漏斗,用分液漏斗分离CCl 萃取碘后的水层与有机层,故C错误;D.若加水超
4
过刻度线,配制失败,应重新配制,故D错误;故答案为A。
6.下列实验操作能达到目的的是( )
答案 D
解析 A项,胶头滴管不能伸入试管中;B项,应该是酸入水;C项,试管口应
稍向下倾斜。
7.下列各装置,夹紧②、③、④中的弹簧夹,并作以下相关操作,漏气的装置
是( )A.对装置①,手移开后导管中水面与烧杯中水面相平
B.对装置②,长颈漏斗内液面高度保持不变
C.对装置③,长导管内形成一段稳定的水柱
D.对装置④,上移a管后,a、b两端液面形成一段稳定的高度差
答案 A
8.(2020·潍坊三模)在芒硝(Na SO ·10H O)结晶水含量测定的实验过程中,下
2 4 2
列仪器或操作未涉及的是( )
答案 C
解析 A.芒硝结晶水含量测定实验过程中,需要称量瓷坩埚的质量、称量瓷
坩埚和一定量晶体的质量,称量瓷坩埚和硫酸钠粉末的质量,至少称量4次,所
以涉及到称量操作,需要托盘天平称量,故A不符合题意;B.为了使硫酸钠晶体
充分反应,应该将硫酸钠晶体研细,所以用到研磨操作,故B不符合题意;C.盛有
硫酸钠晶体的瓷坩埚放在泥三角上慢慢加热,直到水全部失去,不需要蒸发操作
所以实验过程中未涉及到蒸发操作,故C符合题意;D.加热后冷却时,为了防止
硫酸钠粉末吸水,应将硫酸钠放在干燥器中进行冷却,从而得到纯净而干燥的无
水硫酸钠,所以需要用到干燥器,故D不符合题意。
二、选择题(本题包括4小题,每小题有一个或两个选项符合题意)
9.(2020·泰安模拟)下列实验操作或结论正确的是( )
A.为测定新制氯水的pH,用玻璃棒蘸取待测液滴在pH试纸上,与比色卡对
照即可
B.做蒸馏实验时,如果在液体沸腾前发现忘记加沸石,应立即停止加热,冷
却后补加沸石C.在未知液中滴加BaCl 溶液出现白色沉淀,加稀硝酸,沉淀不溶解,不能说
2
明该未知液中一定存在SO
D.提纯混有少量硝酸钾的氯化钠,采用在较高的温度下制成浓溶液再冷却
结晶、过滤、干燥的方法
答案 BC
解析 氯水中的次氯酸能漂白pH试纸,不能用pH试纸测定新制氯水的pH,
A错误;液体加热要加沸石或碎瓷片,引入汽化中心,可防止溶液暴沸,如果加热
一段时间后发现忘记加碎瓷片,应该停止加热,待溶液冷却后重新添加碎瓷片,B
正确;硫酸钡和AgCl均为不溶于酸的白色沉淀,则向某溶液中加入BaCl 溶液生
2
成白色沉淀,继续加稀硝酸沉淀不消失,溶液中可能含Ag+、SO、SO,C正确;氯
化钠中混有少量的硝酸钾,氯化钠是大量的,制得的饱和溶液中硝酸钾量较少,
不能采取降温结晶的方法,D错误。
10.进行化学实验时必须注意安全,下列选项正确的是( )
A.图1点燃酒精灯
B.不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上2%~5%的
硼酸溶液
C.图2制备氢气并检验H 的可燃性
2
D.图3配制硫酸溶液
答案 B
11.用如图装置(加热及夹持仪器已略去)进行的实验,下列不能达到相应实
验目的的是( )A.装置①中的a可用于吸收尾气中的Cl ,b可用于吸收气体时防倒吸
2
B.装置②可实现制取CO 实验中的“即关即止,即开即用”的作用
2
C.利用装置③制取SO ,并验证其漂白性
2
D.利用装置④验证KHCO 和K CO 的热稳定性,X中应放的物质是K CO
3 2 3 2 3
答案 CD
解析 ①中碱石灰可吸收Cl ,b常用于防倒吸;②关闭止水夹时,产生的CO
2 2
将盐酸压入左侧,大理石与盐酸分离,反应停止,打开止水夹时,CO 气体排出,
2
压强减小,盐酸又流回右侧与大理石反应产生CO ;③中大试管中Cu与浓硫酸反
2
应生成SO 气体,若小试管中酸性KMnO 溶液褪色,则证明SO 具有还原性而不
2 4 2
是漂白性,C项不能达到实验目的;④中KHCO 受热不稳定,X中应放的物质是
3
KHCO ,D项不能达到实验目的。
3
12.(2020·湖北七市州联考)完成下列实验所选择的装置正确的是( )
A B C D
实 除去乙醇 除去实验室所制 蒸干NH Cl饱和溶液 制取少量纯净
4
验 中的乙酸 乙烯中的少量SO 制备NH Cl晶体 的CO 气体
2 4 2
装
置
答案 B
解析 乙醇与乙酸互溶,不能用过滤方法除去乙醇中的乙酸,故 A错误;
SO 属于酸性氧化物,能与NaOH溶液反应生成Na SO ,乙烯不与氢氧化钠溶液
2 2 3
反应,可以达到实验目的,故B正确;NH Cl不稳定,受热易分解成NH 和HCl,
4 3
因此不能通过蒸发结晶的方法获得NH Cl,应采用降温结晶的方法获得氯化铵晶
4
体,故C错误; 纯碱是粉末状且易溶于水,不能用启普发生器,应将纯碱改为石灰石,故D错误。
三、非选择题(本题包括2小题)
13.现有下列仪器或装置,请回答下列问题:
(1)仪器①的名称是________,②的名称是________。
(2)用上图仪器组装成气体发生装置:用KClO 和MnO 制取O 应选的装置是
3 2 2
________(填字母,下同);用H O 与MnO 制O ,并控制产生O 的速率,应选的装
2 2 2 2 2
置是________。
(3)若用装置X进行“排空气法”收集制取的O ,氧气应从________(填“b”
2
或“c”,下同)端通入。若瓶中装满水,用排水法收集氧气,氧气应从________端通
入。
(4)若用F装置进行CO还原Fe O 的实验,实验室制取 CO的方法一般采取
2 3
甲酸脱水法(HCOOH――→CO↑+H O),用纯净的CO完成该实验。
2
①除F、X外还需要的装置有________,X中应加入的试剂是________,X与
其他导管连接的顺序是________(填导管口的字母)。
②实验时,a处可能的现象为_____________________________________;
F装置中气球的作用是___________________________________________。
答案 (1)长颈漏斗 分液漏斗 (2)AE BD (3)c b
(4)①DG 浓硫酸 dcbe ②红棕色粉末逐渐变黑 收集尾气中的一氧化碳,
防止污染空气
解析 (2)KClO 和MnO 制取O 属于“固+固――→气体”,因而要选用E
3 2 2
装置为气体发生装置;H O 与MnO 制取O 属于“固+液―→气体”且要控制
2 2 2 2产生气体的速率,只能用分液漏斗控制加入H O 的量。(3)使用X收集氧气时,用
2 2
“排空气法”,由于O 的密度比空气的大,应从长管进气;用排水法收集氧气,应
2
从短管进气。(4)根据反应原理可知,制取CO属于“液+液――→气体”,用分液
漏斗控制加入浓硫酸的量,应选D、G为气体发生装置,X的作用是除去CO中的
水蒸气,洗气时气体流向为“长进短出”。
14.某同学对铜与浓硫酸的实验作了如下改进。实验装置如图所示(加热和夹
持装置已略去)。
实验步骤:
①组装仪器,检查装置气密性;
②加入试剂,关闭旋塞E,加热A,观察C中溶液颜色变化;
③将铜丝上提离开液面,停止加热。
(1)检查虚线框内装置气密性的方法是____________________________。
(2)仪器A的名称是________,仪器B的作用是________,仪器D中所盛药品
是________。
(3)A中发生反应的化学方程式为_________________________________。
(4)实验后,拆除装置前,为避免有害气体的泄漏,应当采取的操作是
_____________________________________________________________。
答案 (1)关闭旋塞E,装置C中加水没过导管口,给A装置微热,装置C中
导管口有气泡冒出,撤去热源后,导管内有倒吸产生的液柱,且高度保持不变
(2)三颈烧瓶(或三口烧瓶) 防倒吸 碱石灰(或NaOH等合理答案均可)
(3)2H SO (浓)+Cu=====CuSO +SO ↑+2H O
2 4 4 2 2
(4)打开旋塞E,从E管口向A中鼓入大量空气
解析 (2)SO 在水中的溶解度较大,所以仪器B的作用是防止倒吸;仪器D
2
的作用是吸收尾气中的SO ,防止污染空气,所以应盛装碱性固体。(4)SO 的密度
2 2
比空气大,所以反应后装置A、B、C中都会残留有一定量的SO ,可通过不断鼓入
2
空气的方法将残留的SO 全部赶入装置D中被吸收。
2