文档内容
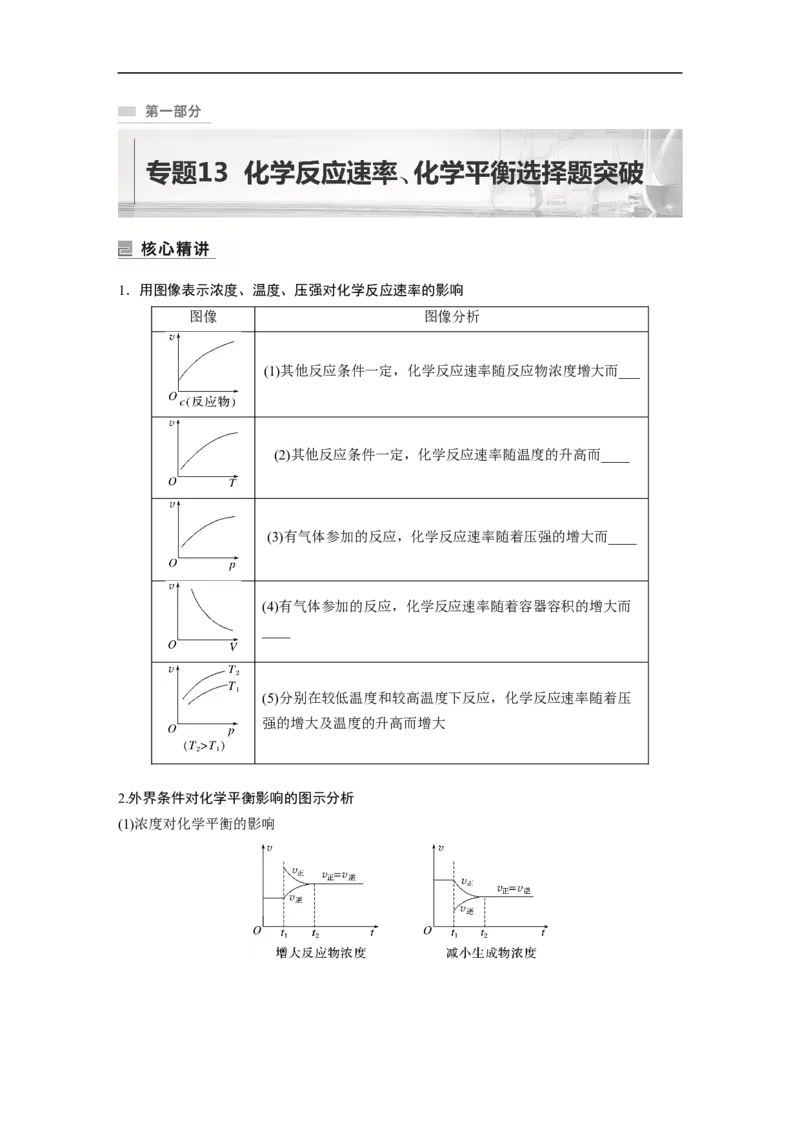
1.用图像表示浓度、温度、压强对化学反应速率的影响
图像 图像分析
(1)其他反应条件一定,化学反应速率随反应物浓度增大而___
(2)其他反应条件一定,化学反应速率随温度的升高而____
(3)有气体参加的反应,化学反应速率随着压强的增大而____
(4)有气体参加的反应,化学反应速率随着容器容积的增大而
____
(5)分别在较低温度和较高温度下反应,化学反应速率随着压
强的增大及温度的升高而增大
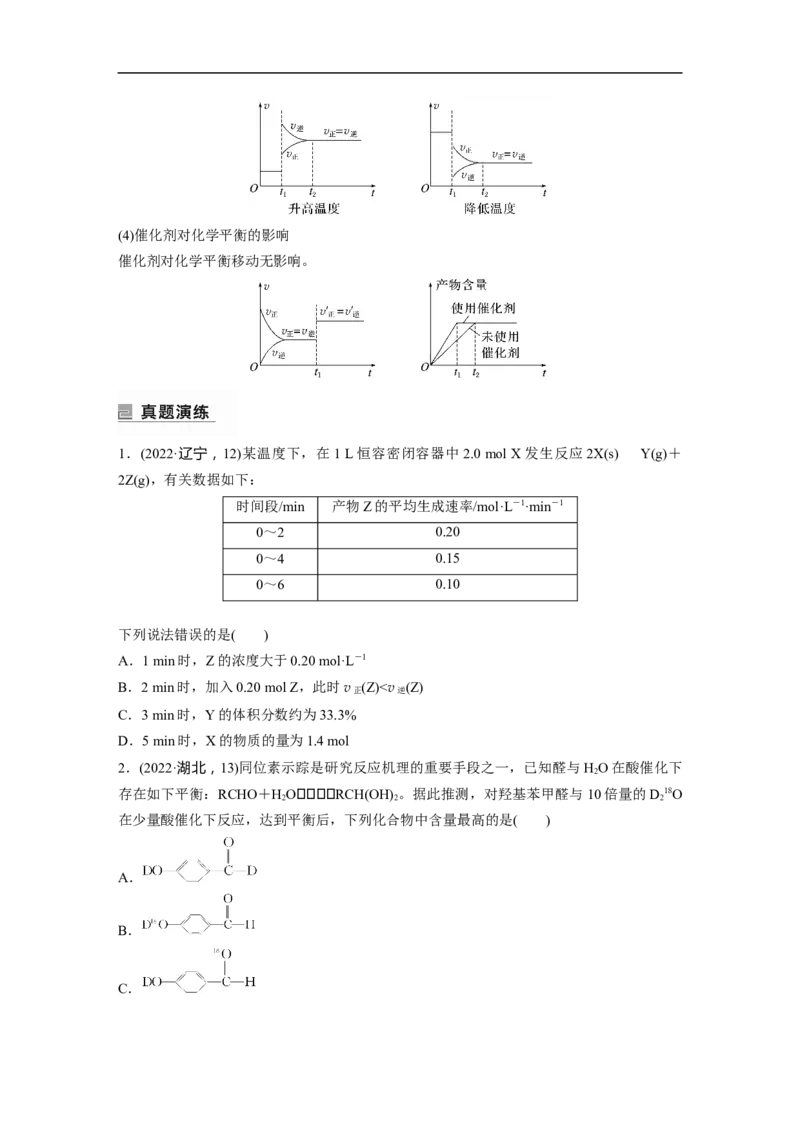
2.外界条件对化学平衡影响的图示分析
(1)浓度对化学平衡的影响(2)压强对化学平衡的影响
对于反应:mA(g)+nB(g)pC(g)+qD(g),若m+n>p+q,则图像对应图1、图2;若m+n
=p+q,则图像对应图3、图4。
说明:
①改变压强,相当于改变体积,也就相当于改变浓度。
②若反应前后气体体积无变化,改变压强,能同时改变正、逆反应速率,v正 =v逆 ,平衡不
移动。如H(g)+I(g)2HI(g)。
2 2
③压强变化是指平衡混合物体积变化而引起的总压强变化。若平衡混合物的体积不变,而加
入“惰性气体”,虽然总压强变化了,但平衡混合物的浓度仍不变,反应速率不变,平衡不
移动;若保持总压强不变加入“惰性气体”,此时增大了体系体积,这就相当于降低了平衡
体系的压强,平衡向气体体积增大的方向移动。
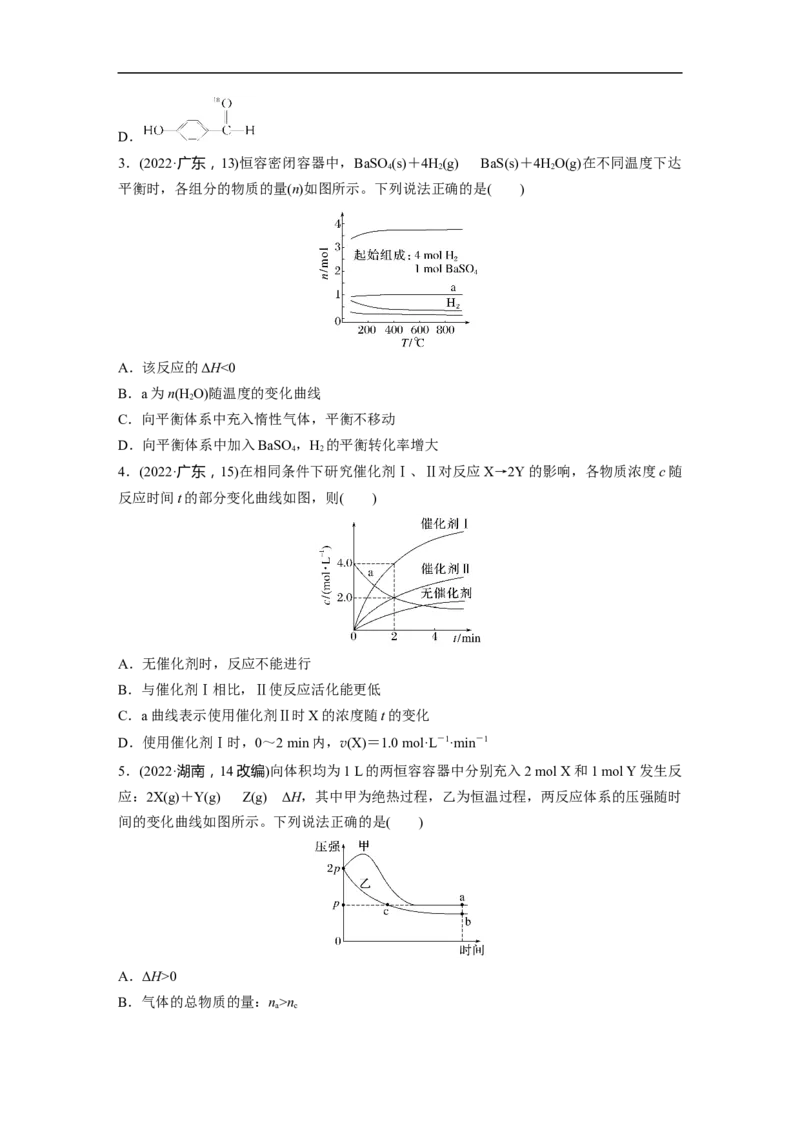
(3)温度对化学平衡的影响
在其他条件不变的情况下,升高温度,化学平衡向吸热反应方向移动;降低温度,化学平衡
向放热反应方向移动。
注意:
①升高温度,不管是吸热还是放热方向,反应速率均增大,但吸热方向速率增大的倍数大于
放热方向速率增大的倍数,使v(吸热)>v(放热),故平衡向吸热方向移动。
②只要是升高温度,新平衡状态的速率值一定大于原平衡状态的速率值;反之则小。v-t图
像[以N(g)+3H(g)2NH (g) ΔH<0为例]
2 2 3(4)催化剂对化学平衡的影响
催化剂对化学平衡移动无影响。
1.(2022·辽宁,12)某温度下,在1 L恒容密闭容器中2.0 mol X发生反应2X(s)Y(g)+
2Z(g),有关数据如下:
时间段/min 产物Z的平均生成速率/mol·L-1·min-1
0~2 0.20
0~4 0.15
0~6 0.10
下列说法错误的是( )
A.1 min时,Z的浓度大于0.20 mol·L-1
B.2 min时,加入0.20 mol Z,此时v正 (Z)0
B.气体的总物质的量:n>n
a cC.a点平衡常数:K>12
D.反应速率:v
a正
v逆 ,平衡常数增大
B.加入催化剂,平衡时CHCHOH(g)的浓度增大
3 2
C.恒容下,充入一定量的HO(g),平衡向正反应方向移动
2
D.恒容下,充入一定量的CH==CH(g),CH==CH(g)的平衡转化率增大
2 2 2 2
7.(2022·河北,13改编)恒温恒容条件下,向密闭容器中加入一定量X,发生反应的方程式
为①XY;②YZ。反应①的速率v =kc(X),反应②的速率v =kc(Y),式中k 、k
1 1 2 2 1 2
为速率常数。图甲为该体系中X、Y、Z浓度随时间变化的曲线,图乙为反应①和②的ln k
~曲线。下列说法错误的是( )
A.随c(X)的减小,反应①、②的速率均降低
B.体系中v(X)+v(Y)=v(Z)
C.欲提高Y的产率,需提高反应温度且控制反应时间
D.温度低于T 时,总反应速率由反应②决定
1
1.工业上用氨催化氧化法制硝酸的反应之一是4NH (g)+5O(g)4NO(g)+6HO(g),该反
3 2 2
应在任何温度下都能自发进行。下列说法正确的是( )
A.该反应的ΔS>0、ΔH>0
B.其他条件不变,加入催化剂,正反应速率增大,逆反应速率减小
C.其他条件不变,改变温度,平衡常数和NH 的平衡转化率一定都会变化
3
D.恒温恒容条件下,混合气体的密度不变时,反应达到平衡状态
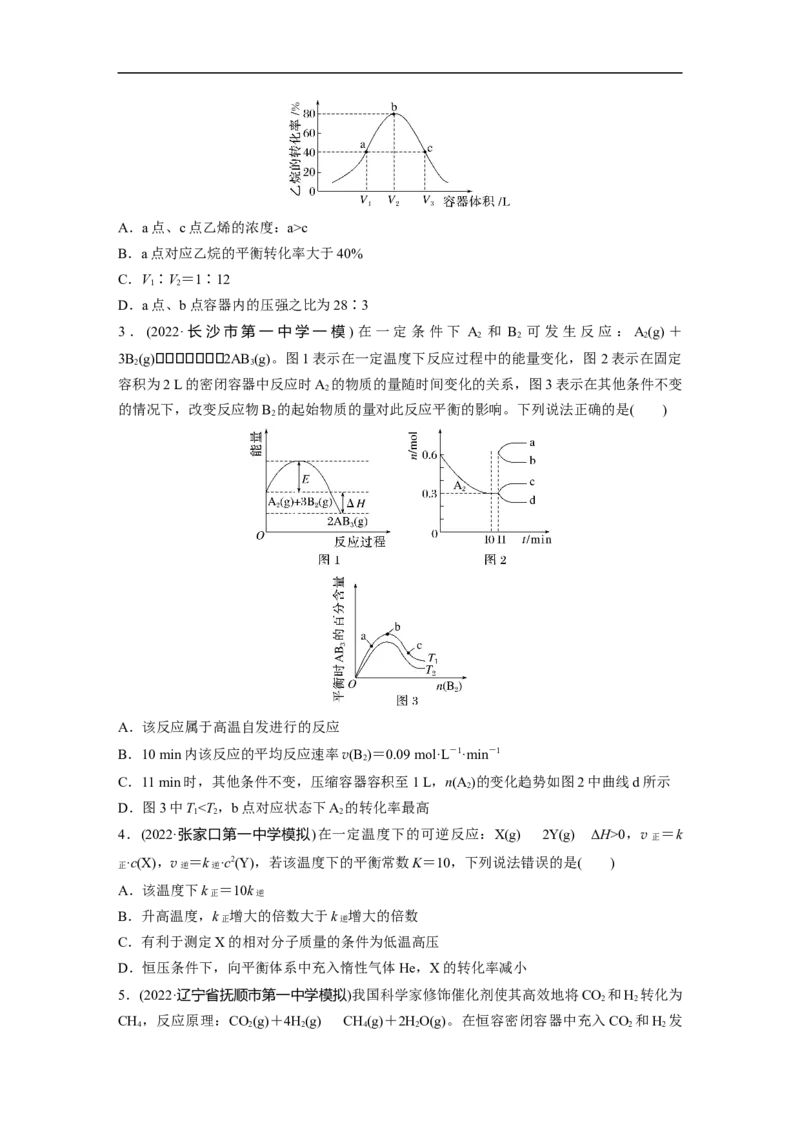
2.(2022·深圳市光明区高级中学联考)T ℃时,向体积不等的恒容密闭容器中均加入一定量
的PtSn-Mg(Zn)AlO催化剂和1 mol乙烷,发生乙烷脱氢反应:CHCH(g)CH==CH(g)
3 3 2 2
+H(g),反应相同时间,测得各容器中乙烷的转化率与容器体积的关系如图所示。下列说
2
法错误的是( )A.a点、c点乙烯的浓度:a>c
B.a点对应乙烷的平衡转化率大于40%
C.V∶V=1∶12
1 2
D.a点、b点容器内的压强之比为28∶3
3.(2022·长沙市第一中学一模)在一定条件下 A 和 B 可发生反应:A(g)+
2 2 2
3B (g)2AB (g)。图1表示在一定温度下反应过程中的能量变化,图 2表示在固定
2 3
容积为2 L的密闭容器中反应时A 的物质的量随时间变化的关系,图3表示在其他条件不变
2
的情况下,改变反应物B 的起始物质的量对此反应平衡的影响。下列说法正确的是( )
2
A.该反应属于高温自发进行的反应
B.10 min内该反应的平均反应速率v(B )=0.09 mol·L-1·min-1
2
C.11 min时,其他条件不变,压缩容器容积至1 L,n(A )的变化趋势如图2中曲线d所示
2
D.图3中T0,v正 =k
正
·c(X),v逆 =k
逆
·c2(Y),若该温度下的平衡常数K=10,下列说法错误的是( )
A.该温度下k =10k
正 逆
B.升高温度,k 增大的倍数大于k 增大的倍数
正 逆
C.有利于测定X的相对分子质量的条件为低温高压
D.恒压条件下,向平衡体系中充入惰性气体He,X的转化率减小
5.(2022·辽宁省抚顺市第一中学模拟)我国科学家修饰催化剂使其高效地将CO 和H 转化为
2 2
CH ,反应原理:CO(g)+4H(g)CH(g)+2HO(g)。在恒容密闭容器中充入CO 和H 发
4 2 2 4 2 2 2生上述反应。下列说法错误的是( )
A.达到平衡后,再充入少量H,CO 的平衡转化率增大
2 2
B.其他条件不变,加入催化剂,能同时增大正、逆反应速率
C.其他条件不变,充入氩气,能使平衡向正反应方向移动
D.其他条件不变,降低温度,能降低正、逆反应速率