文档内容
专题 13 化学反应速率、化学平衡选择题突破
1.丙烷脱氢是工业制丙烯的重要途径之一,反应原理为 2C H(g)+O(g)2C H(g)+
3 8 2 3 6
2HO(g) ΔH<0。下列说法正确的是( )
2
A.该反应的ΔS<0
B.选用合适的催化剂,能提高丙烯的生产效率
C.恒温恒容下,增大氧气的浓度,丙烯的体积分数一定增大
D.恒温下,减小压强,平衡正向移动,平衡常数增大
2.(2022·长沙长郡中学模拟)一定条件下:2NO (g)NO(g) ΔH<0,在测定NO 的相对
2 2 4 2
分子质量时,下列条件中,测定结果误差最小的是( )
A.温度0 ℃、压强50 kPa
B.温度130 ℃、压强300 kPa
C.温度25 ℃、压强100 kPa
D.温度130 ℃、压强50 kPa
3.向某密闭容器中充入NO ,发生反应:2NO (g)NO(g)(已知:NO 为无色气体)。其
2 2 2 4 2 4
他条件相同时,不同温度下平衡体系中各物质的物质的量分数如下表:
t/℃ 27 35 49 70
NO /% 20 25 40 66
2
NO/% 80 75 60 34
2 4
下列说法正确的是( )
A.平衡时,v(NO 消耗)=2v(N O 消耗)
2 2 4
B.27 ℃时,该平衡体系中NO 的转化率为80%
2
C.升高温度,该反应的化学平衡常数增大
D.温度不变,缩小容器体积,达到平衡时气体颜色变浅
4.(2022·大连一模)向恒容的密闭容器中充入a mol CO和b mol H S,发生反应:CO(g)+
2
HS(g)COS(g)+H(g),HS的平衡转化率如图所示,下列说法正确的是( )
2 2 2
A.150 ℃时,若该反应的平衡常数K=,则a∶b=6∶5
B.该反应为吸热反应C.若一段时间后,保持不变,则该反应达到平衡状态
D.平衡后,向容器中再通入a mol CO,v正 逐渐增大
5.(2022·广东省六校联考)已知反应A(g)+B(g)C(g)+D(g)的平衡常数K与温度的关系如
表所示。830 ℃时,向一个2 L的密闭容器中充入0.20 mol A和0.20 mol B,10 s末达到平衡。
下列说法不正确的是( )
温度/℃ 700 830 1 200
K 1.7 1.0 0.4
A.达到平衡后,B的转化率为50%
B.该反应为吸热反应,升高温度,平衡正向移动
C.反应初始至平衡,A的平均反应速率v(A)=0.005 mol·L-1·s-1
D.容器体积减小为原来的一半,平衡不移动,正、逆反应速率均增大
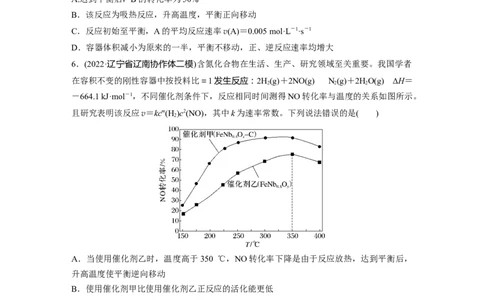
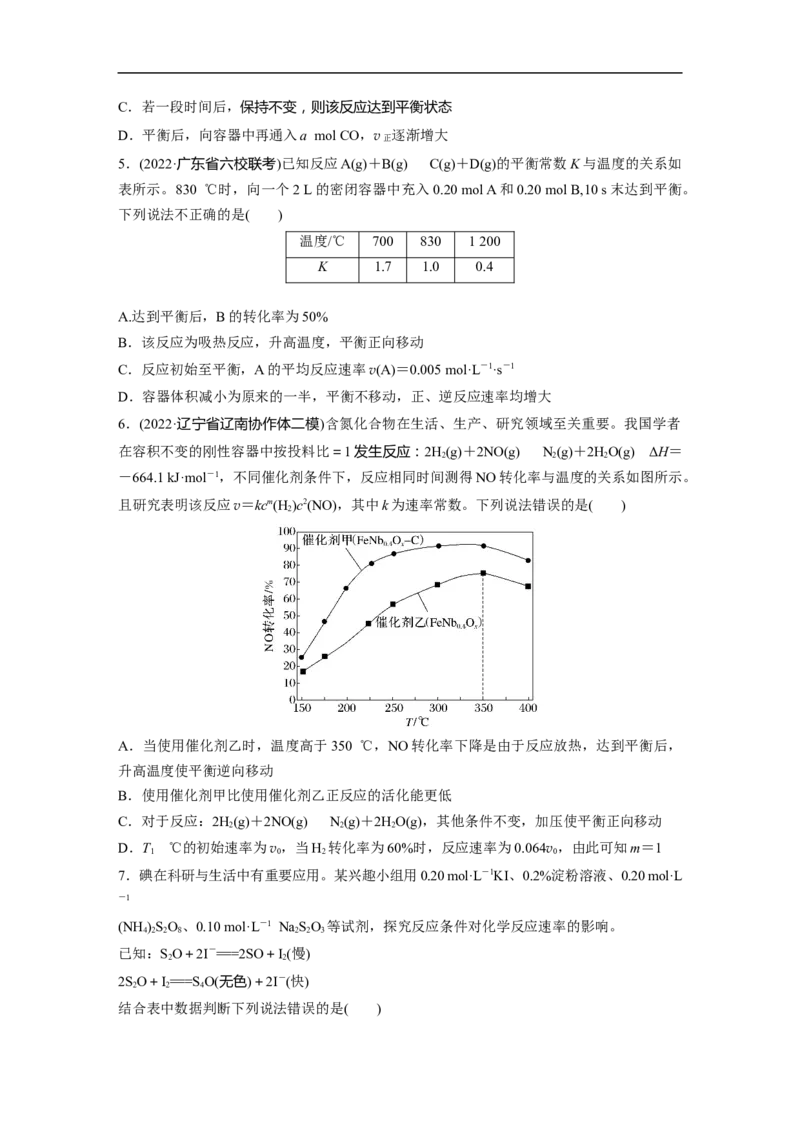
6.(2022·辽宁省辽南协作体二模)含氮化合物在生活、生产、研究领域至关重要。我国学者
在容积不变的刚性容器中按投料比=1发生反应:2H(g)+2NO(g)N(g)+2HO(g) ΔH=
2 2 2
-664.1 kJ·mol-1,不同催化剂条件下,反应相同时间测得NO转化率与温度的关系如图所示。
且研究表明该反应v=kcm(H )c2(NO),其中k为速率常数。下列说法错误的是( )
2
A.当使用催化剂乙时,温度高于350 ℃,NO转化率下降是由于反应放热,达到平衡后,
升高温度使平衡逆向移动
B.使用催化剂甲比使用催化剂乙正反应的活化能更低
C.对于反应:2H(g)+2NO(g)N(g)+2HO(g),其他条件不变,加压使平衡正向移动
2 2 2
D.T ℃的初始速率为v,当H 转化率为60%时,反应速率为0.064v,由此可知m=1
1 0 2 0
7.碘在科研与生活中有重要应用。某兴趣小组用0.20 mol·L-1KI、0.2%淀粉溶液、0.20 mol·L
-1
(NH )SO、0.10 mol·L-1 Na SO 等试剂,探究反应条件对化学反应速率的影响。
4 2 2 8 2 2 3
已知:SO+2I-===2SO+I(慢)
2 2
2SO+I===SO(无色)+2I-(快)
2 2 4
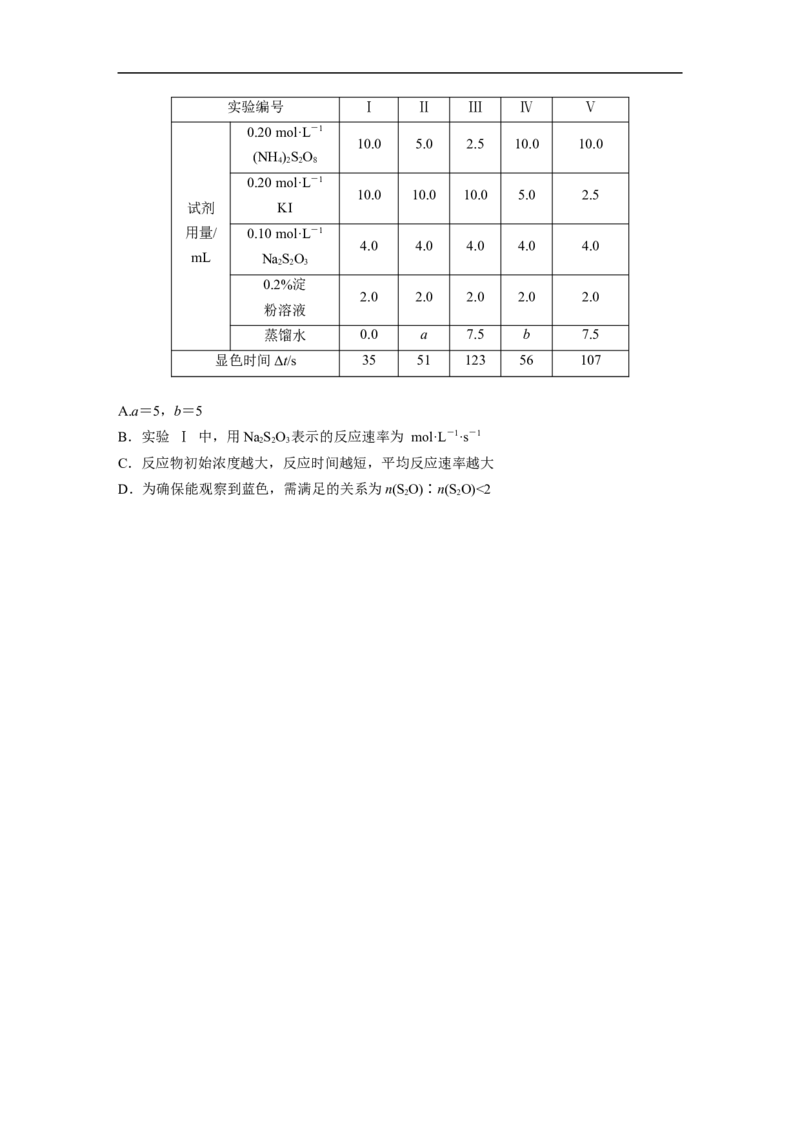
结合表中数据判断下列说法错误的是( )实验编号 Ⅰ Ⅱ Ⅲ Ⅳ Ⅴ
0.20 mol·L-1
10.0 5.0 2.5 10.0 10.0
(NH )SO
4 2 2 8
0.20 mol·L-1
10.0 10.0 10.0 5.0 2.5
试剂 KI
用量/ 0.10 mol·L-1
4.0 4.0 4.0 4.0 4.0
mL NaSO
2 2 3
0.2%淀
2.0 2.0 2.0 2.0 2.0
粉溶液
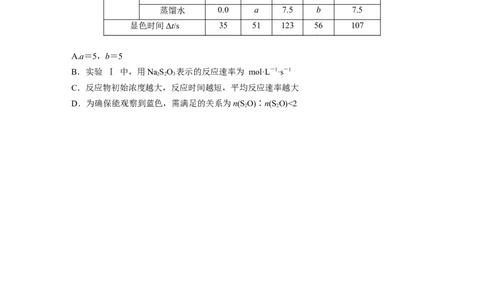
蒸馏水 0.0 a 7.5 b 7.5
显色时间Δt/s 35 51 123 56 107
A.a=5,b=5
B.实验 Ⅰ 中,用NaSO 表示的反应速率为 mol·L-1·s-1
2 2 3
C.反应物初始浓度越大,反应时间越短,平均反应速率越大
D.为确保能观察到蓝色,需满足的关系为n(S O)∶n(S O)<2
2 2