文档内容
第 22 讲 水的电离与溶液的 pH
1.认识水的电离,了解水的离子积常数,认识溶液的酸碱性及pH,掌握检测溶液pH的方法。
2.能进行溶液pH的简单计算,能正确测定溶液的pH,能调控溶液的酸、碱性。能选择实例说明溶
液pH的调控在工农业生产和科学研究中的重要作用。
【核心素养分析】
1.变化观念与平衡思想:认识水的电离有一定限度,是可以调控的。能多角度、动态地分析水的电离,
并运用平衡移动原理解决实际问题。
2.科学研究与创新意识:能发现并提出酸碱中和滴定中有探究价值的问题;能从问题和假设出发,确
定探究目的,设计探究方案,进行实验探究;在探究过程中学会合作,面对“异常”现象敢于提出自己的
见解,进行误差分析。
3.证据推理与模型认知:能从定性和定量上收集证据,能通过定性分析和定量计算推出合理的结论;
能运用pH计算模型进行pH的简单计算。
知识点一 水的电离与水的离子积常数
1.水的电离
水是极弱的电解质,水的电离方程式为HO+HO HO++OH-或HO H++OH-。
2 2 3 2
2.水的离子积常数
K =c(H+)·c(OH-)。
w
(1)室温下:K =1×10-14。
w
(2)影响因素:只与温度有关,升高温度,K 增大。
w
(3)适用范围:K 不仅适用于纯水,也适用于稀的电解质水溶液。
w
(4)K 揭示了在任何水溶液中均存在H+和OH-,只要温度不变,K 不变。
w w
3.影响水电离平衡的因素
体系变化
平衡移动方向 K 水的电离程度 c(OH-) c(H+)
w
条件
HCl 逆 不变 减小 减小 增大
NaOH 逆 不变 减小 增大 减小NaCO 正 不变 增大 增大 减小
2 3
可水解的盐
NH Cl 正 不变 增大 减小 增大
4
升温 正 增大 增大 增大 增大
温度
降温 逆 减小 减小 减小 减小
其他:如加入Na 正 不变 增大 增大 减小
知识点二 溶液的酸碱性和pH
1.溶液的酸碱性
溶液的酸碱性取决于溶液中c(H+)和c(OH-)的相对大小。
(1)酸性溶液:c(H+)>c(OH-),常温下,pH<7。
(2)中性溶液:c(H+)=c(OH-),常温下,pH=7。
(3)碱性溶液:c(H+)7。
2.pH及其测量
(1)计算公式:pH=-lg c(H+)。
(2)测量方法
①pH试纸法
用镊子夹取一小块试纸放在洁净的玻璃片或表面皿上,用玻璃棒蘸取待测液点在试纸的中央,变色后
与标准比色卡对照,即可确定溶液的pH。
②pH计测量法
(3)溶液的酸碱性与pH的关系
常温下:
3.溶液pH的计算
(1)单一溶液的pH计算
强酸溶液:如HA,设浓度为c mol·L-1,c(H+)=nc mol·L-1,pH=-lg c(H+)=-lg (nc)。
n
强碱溶液(25 ℃):如B(OH) ,设浓度为c mol·L-1,c(H+)= mol·L-1,pH=-lg c(H+)=14+lg
n
(nc)。
(2)混合溶液pH的计算类型
①两种强酸混合:直接求出c(H+) ,再据此求pH。c(H+) =。
混 混
②两种强碱混合:先求出c(OH-) ,再据K 求出c(H+) ,最后求pH。c(OH-) =。
混 w 混 混
③强酸、强碱混合:先判断哪种物质过量,再由下式求出溶液中H+或OH-的浓度,最后求pH。c(H+) 或c(OH-) =。
混 混
【方法规律】
1.稀释规律
酸、碱溶液稀释相同倍数时,强电解质溶液比弱电解质溶液的pH变化幅度大,但不管稀释多少倍,
最终都无限接近中性。
2.酸碱混合规律
(1)等浓度等体积一元酸与一元碱混合的溶液——“谁强显谁性,同强显中性”。
(2)25 ℃时,等体积pH之和等于14的一强一弱酸碱混合溶液——“谁弱谁过量,谁弱显谁性”。
(3)强酸、强碱等体积混合(25 ℃时)
①pH之和等于14呈中性;
②pH之和小于14呈酸性;
③pH之和大于14呈碱性。
知识点三 酸碱中和滴定
1.实验原理
利用酸碱中和反应,用已知浓度酸(或碱)来测定未知浓度的碱(或酸)的实验方法。以标准盐酸滴定待测
的NaOH溶液,待测的NaOH溶液的物质的量浓度为c(NaOH)=。
酸碱中和滴定的关键:
(1)准确测定标准液和待测液的体积;
(2)准确判断滴定终点。
2.实验用品
(1)仪器
图(A)是酸式滴定管、图(B)是碱式滴定管、滴定管夹、铁架台、锥形瓶。
(2)试剂:标准液、待测液、指示剂、蒸馏水。
(3)滴定管
①构造:“0”刻度线在上方,尖嘴部分无刻度。②精确度:读数可精确到0.01 mL。
③洗涤:先用蒸馏水洗涤,再用待装液润洗。
④排泡:酸、碱式滴定管中的液体在滴定前均要排出尖嘴中的气泡。
⑤使用注意事项:
试剂性质 滴定管 原因
酸性、氧化性 酸式滴定管 氧化性物质易腐蚀橡胶管
碱性 碱式滴定管 碱性物质易腐蚀玻璃,致使玻璃活塞无法打开
3.实验操作
以标准盐酸滴定待测NaOH溶液为例
(1)滴定前的准备
①滴定管:查漏→洗涤→润洗→装液→调液面→记录。
②锥形瓶:注碱液→记体积→加指示剂。
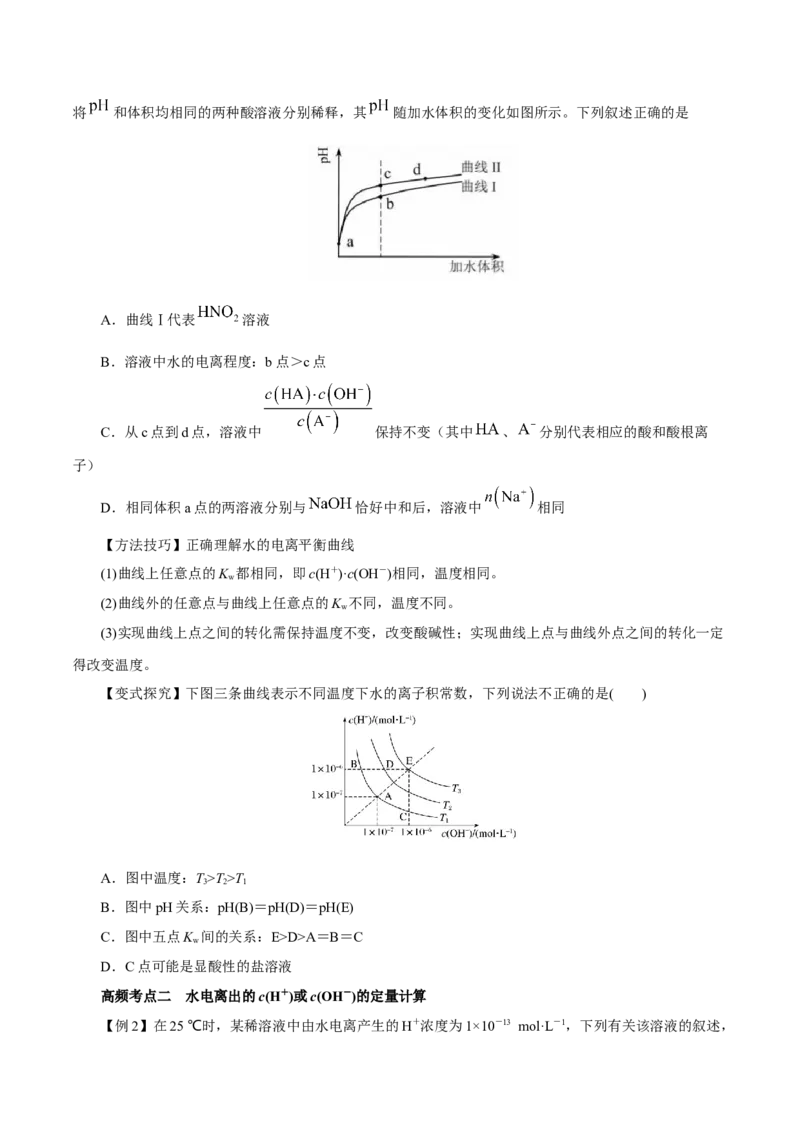
(2)滴定
(3)终点判断
等到滴入最后一滴标准液,指示剂变色,且在半分钟内不恢复原来的颜色,视为滴定终点并记录标准
液的体积。
(4)数据处理
按上述操作重复二至三次,求出用去标准盐酸体积的平均值,根据c(NaOH)=计算。
4.常用酸碱指示剂及变色范围
指示剂 变色范围的pH
石蕊 <5.0红色 5.0~8.0紫色 >8.0蓝色
甲基橙 <3.1红色 3.1~4.4橙色 >4.4黄色
酚酞 <8.2无色 8.2~10.0浅红色 >10.0红色
高频考点一 影响水电离平衡的因素及结果判断
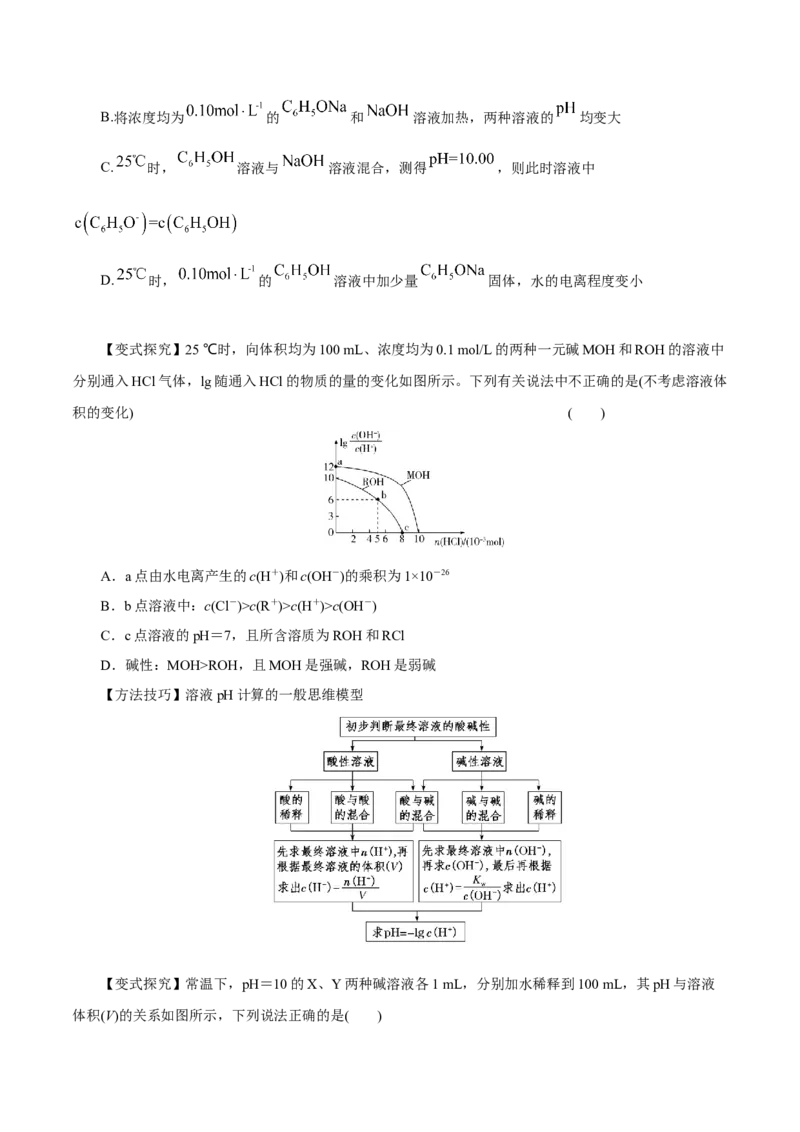
【例1】(2019·天津卷)某温度下, 和 的电离常数分别为 和 。将 和体积均相同的两种酸溶液分别稀释,其 随加水体积的变化如图所示。下列叙述正确的是
A.曲线Ⅰ代表 溶液
B.溶液中水的电离程度:b点>c点
C.从c点到d点,溶液中 保持不变(其中 、 分别代表相应的酸和酸根离
子)
D.相同体积a点的两溶液分别与 恰好中和后,溶液中 相同
【方法技巧】正确理解水的电离平衡曲线
(1)曲线上任意点的K 都相同,即c(H+)·c(OH-)相同,温度相同。
w
(2)曲线外的任意点与曲线上任意点的K 不同,温度不同。
w
(3)实现曲线上点之间的转化需保持温度不变,改变酸碱性;实现曲线上点与曲线外点之间的转化一定
得改变温度。
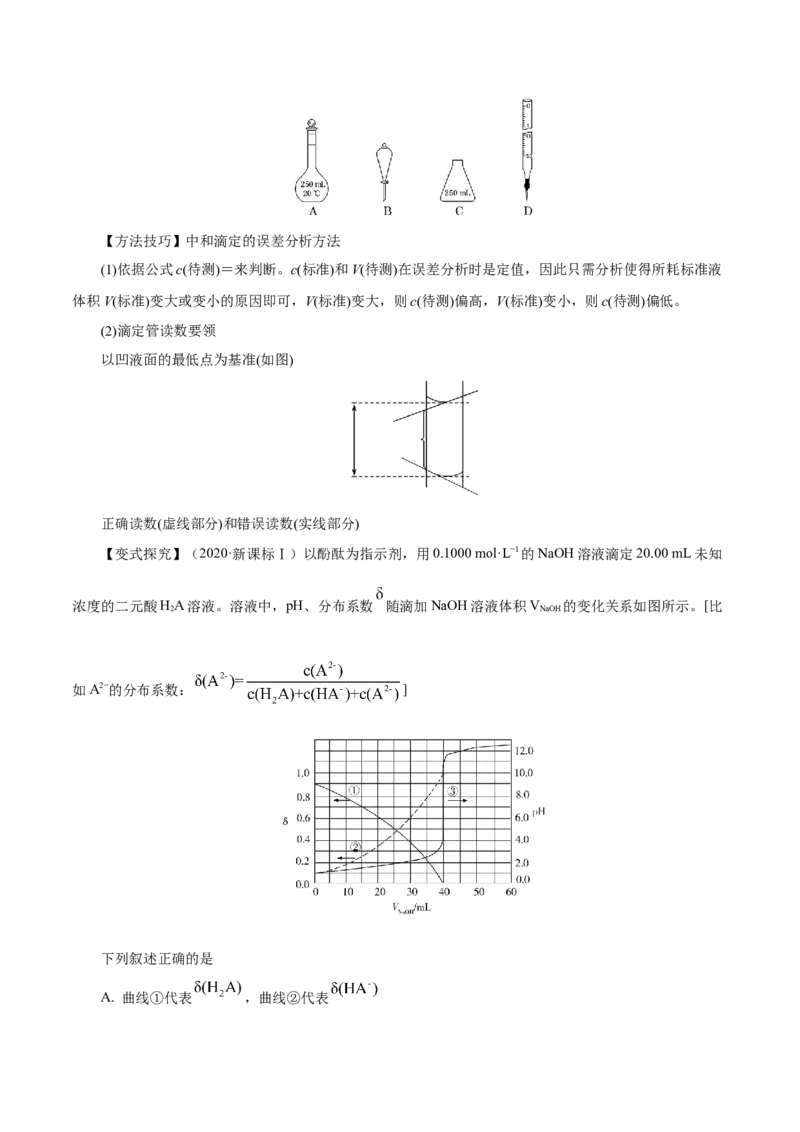
【变式探究】下图三条曲线表示不同温度下水的离子积常数,下列说法不正确的是( )
A.图中温度:T>T>T
3 2 1
B.图中pH关系:pH(B)=pH(D)=pH(E)
C.图中五点K 间的关系:E>D>A=B=C
w
D.C点可能是显酸性的盐溶液
高频考点二 水电离出的c(H+)或c(OH-)的定量计算
【例2】在25 ℃时,某稀溶液中由水电离产生的H+浓度为1×10-13 mol·L-1,下列有关该溶液的叙述,正确的是 ( )
A.该溶液可能呈酸性
B.该溶液一定呈碱性
C.该溶液的pH一定是1
D.该溶液的pH不可能为13
【方法技巧】水电离的c(H+)或c(OH-)的计算技巧(25 ℃时)
(1)中性溶液:c(H+)=c(OH-)=1.0×10-7 mol·L-1。
(2)酸或碱抑制水的电离,水电离出的c(H+)=c(OH-)<10-7 mol·L-1,当溶液中的c(H+)<10-7 mol·L
-1时就是水电离出的c(H+);当溶液中的c(H+)>10-7 mol·L-1时,就用10-14除以这个浓度即得到水电离
的c(H+)。
(3)可水解的盐促进水的电离,水电离的c(H+)或c(OH-)均大于10-7 mol·L-1。若给出的c(H+)>10-7
mol·L-1,即为水电离的c(H+);若给出的c(H+)<10-7 mol·L-1,就用10-14除以这个浓度即得水电离的c(H
+)。
【变式探究】下表是不同温度下水的离子积数据:
温度/℃ 25 t t
1 2
水的离子积常数 1×10-14 K 1×10-12
w
试回答下列问题:
(1)若 25<t <t ,则 K (填“>”“<”或“=”)1×10-14,做出此判断的理由是
1 2 w
。
(2)在t ℃时,测得纯水中的c(H+)=2.4×10-7 mol·L-1,则c(OH-)为 。该温度下,测得某
1
HSO 溶液中c(SO)=5×10-6 mol·L-1,该溶液中c(OH-)= mol·L-1。
2 4
高频考点三 pH的计算及其应用
【例3】(2022·浙江卷)已知25℃时二元酸HA的K =1.3×10-7,K =7.1×10-15。下列说法正确的是
2 a1 a2
A.在等浓度的NaA、NaHA溶液中,水的电离程度前者小于后者
2
B.向0.1mol·L-1的HA溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,则HA的电离度为0.013%
2 2
C.向HA溶液中加入NaOH溶液至pH=11,则c(A2-)>c(HA-)
2
D.取pH=a的HA溶液10mL,加蒸馏水稀释至100mL,则该溶液pH=a+1
2
【变式探究】(2022·浙江卷)25℃时,苯酚 的 ,下列说法正确的是
A.相同温度下,等 的 和 溶液中,B.将浓度均为 的 和 溶液加热,两种溶液的 均变大
C. 时, 溶液与 溶液混合,测得 ,则此时溶液中
D. 时, 的 溶液中加少量 固体,水的电离程度变小
【变式探究】25 ℃时,向体积均为100 mL、浓度均为0.1 mol/L的两种一元碱MOH和ROH的溶液中
分别通入HCl气体,lg随通入HCl的物质的量的变化如图所示。下列有关说法中不正确的是(不考虑溶液体
积的变化) ( )
A.a点由水电离产生的c(H+)和c(OH-)的乘积为1×10-26
B.b点溶液中:c(Cl-)>c(R+)>c(H+)>c(OH-)
C.c点溶液的pH=7,且所含溶质为ROH和RCl
D.碱性:MOH>ROH,且MOH是强碱,ROH是弱碱
【方法技巧】溶液pH计算的一般思维模型
【变式探究】常温下,pH=10的X、Y两种碱溶液各1 mL,分别加水稀释到100 mL,其pH与溶液
体积(V)的关系如图所示,下列说法正确的是( )A.稀释前,两种碱溶液中溶质的物质的量浓度一定相等
B.稀释后,X溶液的碱性比Y溶液的碱性强
C.完全中和X、Y溶液时,消耗同浓度盐酸的体积:V >V
X Y
D.若8