文档内容
第 23 讲 电解池 金属的腐蚀与防护
(模拟精练+真题演练)
完卷时间:50分钟
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Cu 64
一、选择题(每小题只有一个正确选项,共12×5分)
1.(2023·河南安阳·统考三模)二氧化氯(ClO )是一种安全的绿色消毒剂,实验室可用下列方法制备:
2
①电解NH Cl的盐酸溶液制得NCl (N元素为-3价)溶液;②将NCl 溶液与NaClO 溶液混合制得ClO 。
4 3 3 2 2
下列说法正确的是
A.①中在电解池的阴极得到NCl
3
B.组成①中的电解池除需要有电源、导线和大烧杯等,还必须有两个不同材质的电极
C.②中反应的氧化剂与还原剂的物质的量之比是6:1
D.②中反应后的溶液中主要存在的阳离子是Na+
【答案】D
【分析】氯化铵溶液加入盐酸后电解生成氢气、NCl 溶液,阴极生成氢气,阳极生成NCl ,电解方程式为
3 3
NH Cl+2HCl NCl +3H ↑,加入NaClO 溶液发生反应生成ClO 、NH 和X溶液,NCl 中N元素为-3价,
4 3 2 2 2 3 3
该反应中Cl元素化合价由+3价变为+4价,失电子发生氧化反应,则还存在Cl元素得电子发生还原反应,
所以溶液X中含Cl-,溶液呈碱性,所以还存在OH-,发生反应为:
NCl +6NaClO +3H O=6ClO +NH+3NaOH+3NaCl,据此分析解题。
3 2 2 2 3
【解析】A.由分析可知,①中氯化铵溶液加入盐酸后电解生成氢气、NCl 溶液,阴极生成氢气,阳极生
3
成NCl ,电解方程式为NH Cl+2HCl NCl +3H ↑,A错误;B.根据电解池的组成可知,组成①中的电
3 4 3 2
解池除需要有电源、导线和大烧杯等,还必须有两个惰性电极,可以是相同材质如均为石墨,也可以不同
材质如石墨作阳极,Cu作阴极等,B错误;C.由分析可知,②中反应方程式为
NCl +6NaClO +3H O=6ClO +NH+3NaOH+3NaCl,故氧化剂NCl 与还原剂NaClO 的物质的量之比是1:
3 2 2 2 3 3 2
6,C错误;D.由分析可知,②中反应方程式为NCl +6NaClO +3H O=6ClO +NH+3NaOH+3NaCl,故反应
3 2 2 2 3
后的溶液中主要存在的阳离子是Na+,D正确;故答案为:D。
2.(2023·浙江·校联考一模)利用电解池原理可将 转化为燃料或者化学品。下图通过将 与辛胺反
应耦合,实现了两电极体系中产物的高选择性合成。下列说法正确的是
A.装置中b电极为阴极,发生还原反应
B.电极a的电极反应可能为:
C.中间的离子交换膜一定是质子交换膜
D.电解过程中,a、b两极反应物物质的量之比为2∶1
【答案】B
【分析】利用电解池原理可将CO 转化为燃料或者化学品,反应过程中碳元素的化合价降低,得到电子,
2
则a极为阴极,CO 转化为燃料或者化学品,b极为阳极,辛胺转化为辛氰。
2
【解析】A.装置中b电极为阳极,失去电子,发生氧化反应,故A错误;B.电极a为阴极,电极反应可
能为: ,故B正确;C.若电解液中性时,中间的离子交换膜是质子交换
膜,若电解液碱性时,中间的离子交换膜是阴离子交换膜,故C错误;D.电解过程中,a极CO 转化为燃
2
料或者化学品,b极辛胺转化为辛氰,由于电极a的产物不确定,则反应物物质的量之比不确定,故D错
误;故选:B。
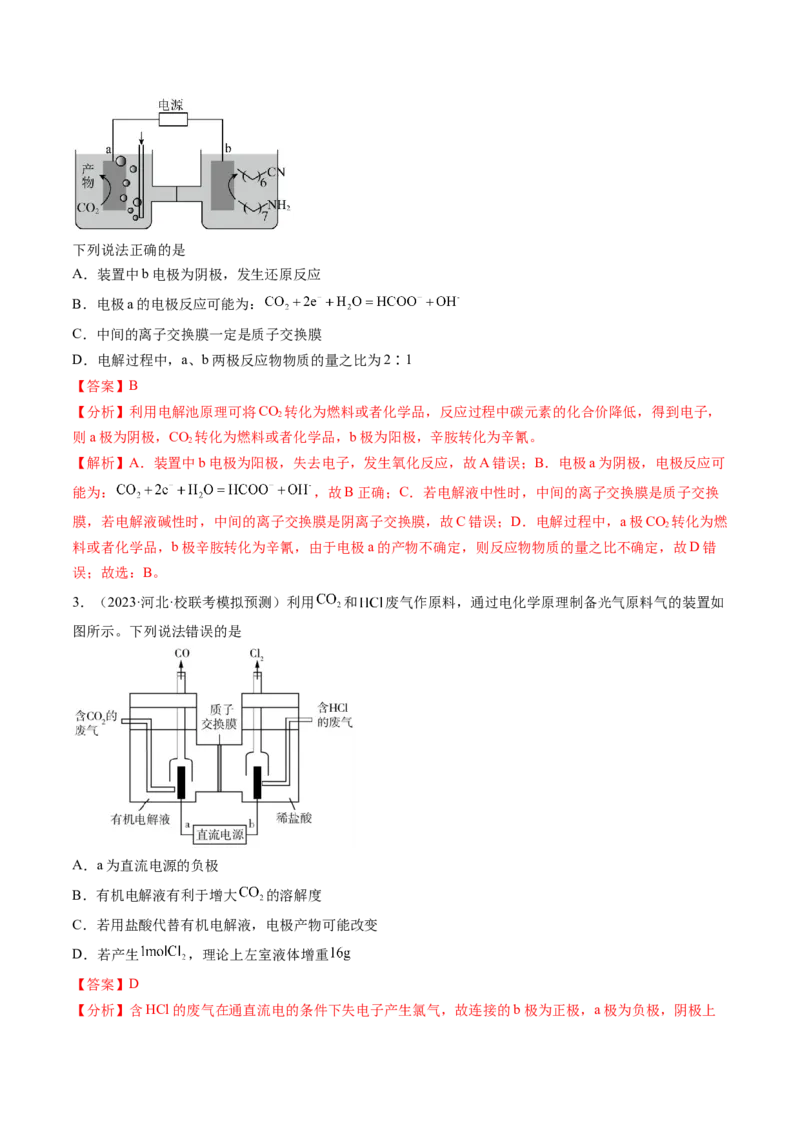
3.(2023·河北·校联考模拟预测)利用 和 废气作原料,通过电化学原理制备光气原料气的装置如
图所示。下列说法错误的是
A.a为直流电源的负极
B.有机电解液有利于增大 的溶解度
C.若用盐酸代替有机电解液,电极产物可能改变
D.若产生 ,理论上左室液体增重
【答案】D
【分析】含HCl的废气在通直流电的条件下失电子产生氯气,故连接的b极为正极,a极为负极,阴极上含有CO 的废气得电子产生CO;
2
【解析】A. 还原生成 ,该电极是阴极,故 为直流电源的负极,选项A正确;B. 为非极性
分子,在有机溶剂中的溶解度较大,有利于 在阴极放电,选项B正确;C.左室中的电极反应式为
,若用盐酸代替有机电解液,溶液中的 易在阴极放电产生 ,选项C正确;
D.若产生 ,电路中转移 电子,阴极产生 ,同时有 通过质子交换膜进入左室,
因此,左室增重: ,选项D错误;答案选D。
4.(2023·江苏南京·南京师大附中校考模拟预测)科研人员发现利用低温固体质子导体作电解质,催化合
成NH ,与传统的热催化合成氨相比,催化效率较高。其合成原理如图1所示,电源电压改变与生成NH
3 3
速率的关系如图2所示,下列说法不正确的是
A.Pt—C是该合成氨装置的阳极
B.Pt-C N 电极上发生的反应为N+6H++6e-=2NH
3 4 2 3
C.若H 的进出口流量差为22.4L/min,则固体质子导体中H+的流速为2mol/min
2
D.当电压高于1.2V时,混合气体中N 和NH 的体积分数之和小于100%
2 3
【答案】C
【分析】由图1可知,Pt—C电极是电解池的阳极,氢气在阳极失去电子发生氧化反应生成氢离子,电极
反应式为H-2e-=2H+,Pt-C N 电极为阴极,酸性条件下氮气在阴极得到电子发生还原反应生成氨气,电极
2 3 4
反应式为N+6H++6e-=2NH。
2 3
【解析】A.由分析可知,Pt—C电极是电解池的阳极,氢气在阳极失去电子发生氧化反应生成氢离子,故
A正确;B.由分析可知,Pt-C N 电极为阴极,酸性条件下氮气在阴极得到电子发生还原反应生成氨气,
3 4
电极反应式为N+6H++6e-=2NH,故B正确;C.缺标准状况下,无法计算22.4L氢气的物质的量和反
2 3
应生成氢离子的物质的量,则无法计算固体质子导体中氢离子的流速,故C错误;D.由图2可知,当电
压高于1.2V时,氨气反应速率变慢,说明氢离子在阴极得到电子生成氢气,导致混合气体中氮气和氨气的
体积分数之和小于100%,故D正确;故选C。
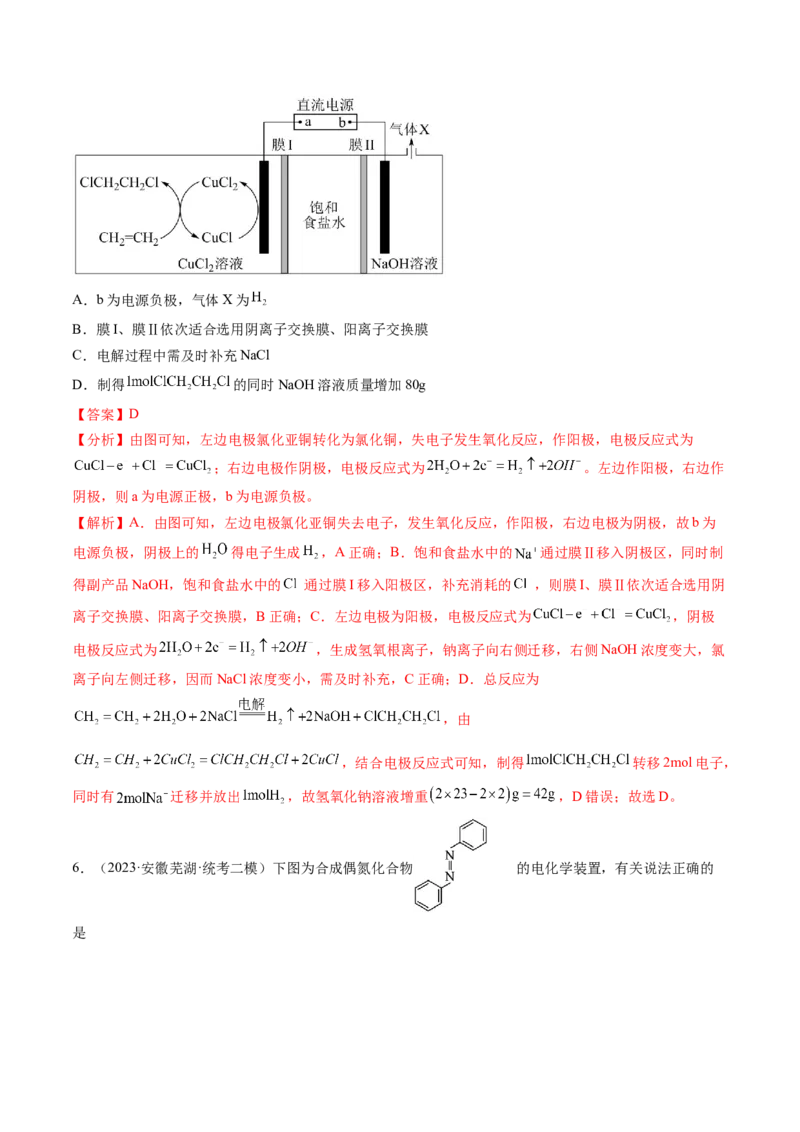
5.(2023·重庆沙坪坝·重庆八中校考二模)我国学者利用双膜三室电解法合成了 ,该方法的
优点是能耗低、原料利用率高,同时能得到高利用。价值的副产品,其工作原理如图所示。下列说法错误
的是A.b为电源负极,气体X为
B.膜I、膜Ⅱ依次适合选用阴离子交换膜、阳离子交换膜
C.电解过程中需及时补充NaCl
D.制得 的同时NaOH溶液质量增加80g
【答案】D
【分析】由图可知,左边电极氯化亚铜转化为氯化铜,失电子发生氧化反应,作阳极,电极反应式为
;右边电极作阴极,电极反应式为 。左边作阳极,右边作
阴极,则a为电源正极,b为电源负极。
【解析】A.由图可知,左边电极氯化亚铜失去电子,发生氧化反应,作阳极,右边电极为阴极,故b为
电源负极,阴极上的 得电子生成 ,A正确;B.饱和食盐水中的 通过膜Ⅱ移入阴极区,同时制
得副产品NaOH,饱和食盐水中的 通过膜I移入阳极区,补充消耗的 ,则膜I、膜Ⅱ依次适合选用阴
离子交换膜、阳离子交换膜,B正确;C.左边电极为阳极,电极反应式为 ,阴极
电极反应式为 ,生成氢氧根离子,钠离子向右侧迁移,右侧NaOH浓度变大,氯
离子向左侧迁移,因而NaCl浓度变小,需及时补充,C正确;D.总反应为
,由
,结合电极反应式可知,制得 转移2mol电子,
同时有 迁移并放出 ,故氢氧化钠溶液增重 ,D错误;故选D。
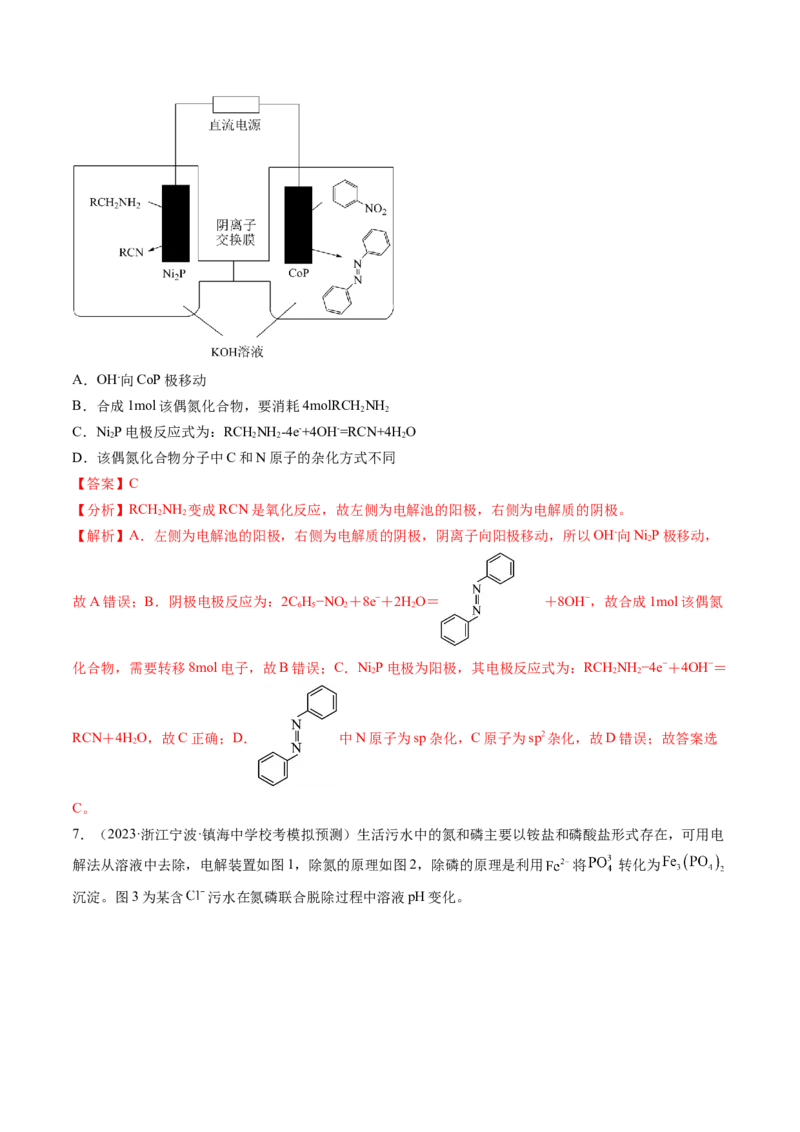
6.(2023·安徽芜湖·统考二模)下图为合成偶氮化合物 的电化学装置,有关说法正确的
是A.OH-向CoP极移动
B.合成1mol该偶氮化合物,要消耗4molRCH NH
2 2
C.Ni P电极反应式为:RCHNH -4e-+4OH-=RCN+4H O
2 2 2 2
D.该偶氮化合物分子中C和N原子的杂化方式不同
【答案】C
【分析】RCHNH 变成RCN是氧化反应,故左侧为电解池的阳极,右侧为电解质的阴极。
2 2
【解析】A.左侧为电解池的阳极,右侧为电解质的阴极,阴离子向阳极移动,所以OH-向Ni P极移动,
2
故A错误;B.阴极电极反应为:2C H−NO+8e−+2HO= +8OH−,故合成1mol该偶氮
6 5 2 2
化合物,需要转移8mol电子,故B错误;C.Ni P电极为阳极,其电极反应式为:RCHNH −4e−+4OH−=
2 2 2
RCN+4HO,故C正确;D. 中N原子为sp杂化,C原子为sp2杂化,故D错误;故答案选
2
C。
7.(2023·浙江宁波·镇海中学校考模拟预测)生活污水中的氮和磷主要以铵盐和磷酸盐形式存在,可用电
解法从溶液中去除,电解装置如图1,除氮的原理如图2,除磷的原理是利用 将 转化为
沉淀。图3为某含 污水在氮磷联合脱除过程中溶液pH变化。下列说法不正确的是
A.产生 的主要过程是:
B.除磷时阴极产物主要是
C.脱氮过程中阳极主要发生的反应为
D.在0-20min时脱除的元素是氮元素
【答案】C
【解析】A.由题干图1所示信息可知,当铁电极与电源正极相连作阳极时,即可产生Fe2+,该主要过程的
电极反应为:Fe-2e-=Fe2+,故A正确;B.除磷时,Fe作阳极,石墨作阴极,电极反应式为2H++2e-=H ↑,
2
除磷时阴极产物是H,故B正确;C.脱氮过程中产生N 和HClO,故脱氮过程中阳极主要发生的反应为
2 2
8ClO-+2 -6e-═N ↑+8HClO,故C错误;D.根据图3中0~20min溶液pH的变化可知,脱除的元素是
2
氮元素,故D正确;故选:C。
8.(2023·福建南平·统考三模)西北工业大学推出一种新型 电池。该电池能有效地捕获 ,
将其转化为 ,再将产生的 电解制氨,过程如图所示。下列说法错误的是
A.d电极为电解池的阳极
B. 电池总反应式为:
C.c极区溶液的pH升高
D.电路中转移 时,理论上能得到
【答案】D
【分析】由图可知,锌为活泼金属,失去电子发生氧化反应,a为负极、b为正极,则c为阴极、d为阳极;【解析】A.由分析可知,d电极为电解池的阳极,A正确;B. 电池总反应为锌和二氧化氮反应
生成亚硝酸锌: ,B正确;C.c极区为阴极区,亚硝酸根离子发生还原生成 ,
溶液碱性增强,故溶液的pH升高,C正确;D.c极区为阴极区,亚硝酸根离子发生还原生成 ,电子
转移为 ,则电路中转移 时,理论上能得到 ,D错误;故选D。
9.(2023·安徽·校联考三模)天津大学化学团队以CO 和辛胺为原料实现了甲酸和辛腈的高选择性合成,
2
工作原理如图(隔膜a只允许OH-通过)所示。下列说法错误的是
A.Ni P电极的电势比In/In O 电极的高
2 2 3-x
B.In/In O 电极上可能有副产物H 生成
2 3-x 2
C.电解过程中,OH-由In/In O 电极区向Ni P电极区迁移
2 3-x 2
D.电路中转移2mol电子时,阴极区溶液质量增加44g(不考虑气体的溶解)
【答案】D
【分析】由图中In/In O 电极上CO→HCOO-可知,CO 发生得电子的还原反应,In/In O 电极为阴极,
2 3-x 2 2 2 3-x
阴极反应为:CO+2e-+H O═HCOO-+OH-,则Ni P电极为阳极,辛胺在阳极上发生失电子的氧化反应生成
2 2 2
辛腈,电极反应为CH(CH)CHNH +4OH--4e-=CH (CH)CN+4HO。
3 2 6 2 2 3 2 6 2
【解析】A.根据分析,Ni P电极为阳极,连接电源的正极,电势比In/In O 电极的高,A正确;B.In/
2 2 3-x
InO 电极为阴极,阴极反应为:CO+2e-+H O═HCOO-+OH-,也可能发生2HO+2e-═2OH-+H ↑,B正确;
2 3-x 2 2 2 2
C.电解过程中,阴离子向阳极移动,则OH-由In/In O 电极区向Ni P电极区迁移,C正确;D.阴极反应
2 3-x 2
为:CO+2e-+H O═HCOO-+OH-,当电路中有2mol电子转移时,阴极区液体质量增加1mol CO 的质量,同
2 2 2
时减少2mol OH-的质量,则阴极区溶液质量增加44g-34g=10g,D错误;故选:D。
10.(2023·陕西榆林·统考模拟预测)电解HF和熔融KHF 的混合物(熔融混合物中常加入少量LiF或
2
AlF)制备单质氟,以电解槽内壁(镍铜合金)和石墨为电极,总反应为2KHF =2KF+F ↑+H ↑。下列有关电
3 2 2 2
解制备单质氟的说法正确的是
A.电解过程中,电解槽内壁与电源的正极相连
B.石墨电极发生的电极反应为2F- +2e- =F↑
2
C.电解过程中加入少量LiF或AlF 可以降低混合物的熔点,增强导电性
3
D.电解一段时间后,加入一定量的固体KHF 可还原混合物的组成
2【答案】C
【解析】A.电解槽内壁由Ni、Cu合金构成,若与电源正极相连,则为阳极,Ni、Cu失去电子与总反应
不符,A错误;B.石墨电极应为阳极,失去电子 ,B错误;C.LiF、AlF 的加入可降低混
3
合物熔点,增强导电性,C正确;D.从固体熔融物中析出后,H 气体则需要加HF还原混合物组成,D错
2
误;故答案为:C。
11.(2023·湖南长沙·长郡中学校考一模)“乌铜走银”是云南特有的中国传统铜制工艺品。它以铜为胎,
在胎上雕刻各种花纹图案,然后将熔化的银(或金)水填入花纹图案中,完成制作后需经常用汗湿的手摩擦
器物,使铜胎变为乌黑,透出银(或金)纹图案。下列有关该工艺的说法错误的是
A.用铜和少量的贵金属熔炼成的铜胎仍具有金属性能
B.熔化银(或金)时需破坏金属键
C.铜胎变乌黑的原因是汗液中存在氧化性物质使铜变成了氧化铜
D.“乌铜走银”工艺品最终呈现出黑白(或黑黄)分明的装饰效果
【答案】C
【解析】A.合金也具有金属性能,用铜和少量的贵金属熔炼成的铜胎仍具有金属性能,A正确;B.银
(或金)为金属晶体,熔化时需破坏金属键,B正确;C.汗液摩擦能提供电解质溶液,与铜和银(或
金)形成原电池,铜为负极,更容易被空气中的氧气所氧化,C错误;D.银为银白色,金为黄色,因此
“乌铜走银”工艺品呈现出黑白(或黑黄)分明的装饰效果,D正确;故答案选C。
12.(2023·辽宁鞍山·鞍山一中校考模拟预测)近日,清华大学王保国教授团队设计出了一种双极膜(将
解离成 和 )电解合成 的反应器,其简化模型如图所示,已知:法拉第常数 Cmol
(法拉第常数的物理意义:每摩尔电子携带的电荷量)。下列说法错误的是 ⋅
A.M极电势低于N极电势
B.电解合成过程中,N极附近电解质溶液的pH减小
C.阴极的电极反应式为
D.理论上产生0.02mol 时,外电路流过的电量为1930C
【答案】D
【分析】由图可知M极硝酸根离子转变为氨气,氮元素的化合价降低得到电子,是电解池的阴极与电源负
极相连,所以N极是电解池的阳极与电源正极相连,氢氧根离子失去电子生成氧气和水,以此分析。
【解析】A.左侧 发生还原反应生成 ,电极反应式为 ,该电极
为阴极,与电源负极相连,由于电源正极电极电势大于负极电势,故左边电极电势低于右边电极电势,A正确;B.电解合成过程中,N极氢氧根离子失去电子生成氧气和水,所以附近电解质溶液的pH减小,B
正确;C.根据分析阴极的电极反应式为 ,C正确;D.理论上产生
时,氧的化合价由-2价升高到零价转移 ,因此外电路流过的电量
,D错误;故选D。
二、主观题(共3小题,共40分)
13.(14分)钢铁工业是国家工业的基础,钢铁生锈现象却随处可见,为此每年国家损失大量资金。
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的正极电极反应式为:
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用图①所示的方案,其中焊接在铁闸门上的固体材料R
可以采用 。
A.铜 B.钠 C.锌 D.石墨
(3)图②所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的 极。
(4)钢铁的防护除了用电化学保护方法之外,在钢铁制品表面镀铜也可以有效地防止其腐蚀,电镀的装置如
图所示:
①电镀装置图的“直流电源”中, 填“a”或“b” 是正极。Fe电极反应式为 ;
②接通电源前,装置图中的铜、铁两个电极质量相等,电镀完成后,将两个电极取出,用水小心冲洗干净、
烘干,然后称量,二者质量之差为5.12g,由此计算电镀过程中电路中通过电子的物质的量为 。
③上述铁镀件破损后,铁更容易被腐蚀。请简要说明镀铜铁镀件破损后,铁更容易被腐蚀的原因:
。
【答案】(每空2分)(1)O +2H O+4e-==4OH-
2 2
(2)C
(3)负
(4)①a Cu2++2e-=Cu
②0.08mol
③铁比铜活泼,铁与铜构成原电池的两个电极,铁作负极,更易被腐蚀【解析】(1)钢铁腐蚀的吸氧腐蚀,是金属吸收空气中的氧气发生的反应,正极得电子,化合价降低,
故吸氧腐蚀过程中的正极电极反应式为:O+2H O+4e-==4OH-;
2 2
(2)图①所示的方案为牺牲阳极的阴极保护法,故添加的物质应该比铁更活泼,但钠易与水发生剧烈反
应,不安全,故焊接在铁闸门上的固体材料R可以采用锌,答案选C;
(3)图②所示的方案是外加电源的阴极保护法,故铁闸门应该连接在直流电源的负极,做阴极,答案为:
负;
(4))①电镀时电源正极连接的电极为阳极,故a为正极;铁连接负极,故Fe电极发生的电极反应为:
Cu2++2e-=Cu;②阳极溶解的铜的质量等于阴极上析出的铜的质量,故阳极溶解的铜为2.56 g,即0.04
mol,故电镀过程中电路中通过的电子的物质的量为0.08 mol;③镀件镀层破损后,镀层金属与镀件金属在
周围环境中形成原电池,活泼性较强的金属更容易被腐蚀;
故答案为:a;Cu2++2e-=Cu;0.08mol;铁比铜活泼,铁与铜构成原电池的两个电极,铁作负极,更易被腐
蚀。
14.(14分)Ⅰ.高铁酸盐在能源、环保等方面有着广泛的用途。高铁酸钾(K FeO)不仅是一种理想的水处
2 4
理剂,而且高铁电池的研制也在进行中。如图是高铁电池的模拟实验装置:
(1)该电池放电时正极的电极反应式为 。
(2)盐桥中盛有饱和KCl溶液,此盐桥中氯离子向 (填“左”或“右”)移动;若用阳离子交换膜代替盐桥,
则钾离子向 (填“左”或“右”)移动。
(3)如图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有 。
Ⅱ.二氧化氯(ClO )为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。如图是目
2
前已开发出用电解法制取ClO 的新工艺。
2(4)阳极产生ClO 的电极反应式: 。
2
(5)当阴极产生标准状况下112 mL气体时,通过阳离子交换膜离子的物质的量为 。
【答案】(除标注外,每空2分)(1)FeO +4H O+3e-=Fe(OH)↓+5OH-(3分)
2 3
(2)右 左
(3)使用时间长、工作电压稳定
(4)Cl--5e-+2H O=ClO ↑+4H+
2 2
(5)0.01mol(3分)
【解析】(1)根据电池装置,Zn做负极,C为正极,高铁酸钾的氧化性很强,正极上高铁酸钾发生还原
反应生成Fe(OH),正极电极反应式为:FeO +4H O+3e-=Fe(OH)↓+5OH-;
3 2 3
(2)盐桥中阴离子移向负极移动,盐桥起的作用是使两个半电池连成一个通路,使两溶液保持电中性,
起到平衡电荷,构成闭合回路,放电时盐桥中氯离子向右移动,用某种高分子材料制成阳离子交换膜代替
盐桥,则钾离子向左移动;
(3)由图可知高铁电池的优点有:使用时间长、工作电压稳定;
(4)由题意可知,氯离子放电生成ClO ,根据电子守恒和电荷守恒写出阳极的电极反应式为Cl--5e-
2
+2H O=ClO ↑+4H+;
2 2
(5)阴极产生标准状况下112mL是H,物质的量为0.005mol,阴极电极反应式为2H++2e-=H ↑,所以电
2 2
路中转移电子0.01mol,钠离子所带电荷与电子所带电荷数相同,所以通过阳离子交换膜的钠离子的物质
的量为0.01mol。
15.(12分)根据下列要求回答下列问题。
(1)次磷酸钴[Co(H PO )]广泛用于化学镀钴,以金属钴和次磷酸钠为原料,采用四室电渗析槽电解法制备,
2 2 2
原理如图:
则Co的电极反应式为 ,A、B、C为离子交换膜,其中B为 离子交换膜(填“阳”或“阴”)。
(2)我国科研人员研制出的可充电“NaCO”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应方
2程式为4Na+3CO 2NaCO+C.放电时该电池“吸入”CO,其工作原理如图所示:
2 2 3 2
①放电时,正极的电极反应式为 。
②若生成的NaCO 和C全部沉积在正极表面,当正极增加的质量为28g时,转移电子的物质的量为 。
2 3
③可选用高氯酸钠四甘醇二甲醚作电解液的理由是 。
【答案】(除标注外,每空2分)(1)Co-2e-=Co2+ 阴
(2)①3CO+4Na++4e-=2Na CO+C(3分)
2 2 3
②0.5mol(3分)
③导电性好、与金属钠不反应、难挥发等
【解析】(1)以金属钴和次磷酸钠为原料,用电解法制备次磷酸钴[Co(H PO )],Co的化合价从0升高到
2 2 2
+2,则Co的电极反应式为Co-2e-=Co2+,产品室可得到次磷酸钴的原因是阳极室中的Co2+通过阳离子交
换膜进入产品室,原料室中的HPO 通过阴离子交换膜进入产品室与Co2+结合生成Co(HPO ),所以B是
2 2 2 2
阴离子交换膜;
(2)①放电时,正极发生得到电子的还原反应,则根据总反应式可知电极反应式为3CO+4Na++4e-
2
=2Na CO+C;
2 3
②根据反应式可知每转移4mol电子,正极质量增加2×106g+12g=224g,所以当正极增加的质量为28g时,
转移电子的物质的量为 ×4mol=0.5mol;
③根据题干信息以及金属钠的化学性质可知可选用高氯酸钠四甘醇二甲醚作电解液的理由是其导电性好、
与金属钠不反应、难挥发等。
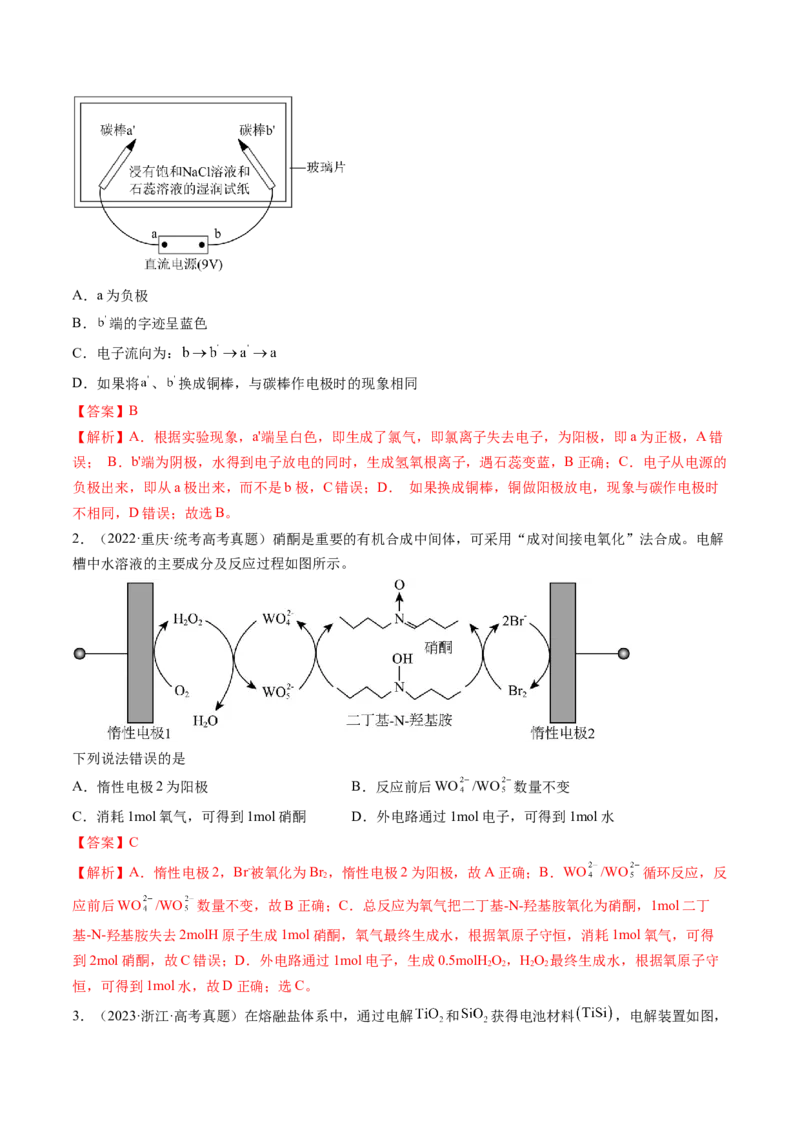
1.(2022·天津·统考高考真题)实验装置如图所示。接通电源后,用碳棒( 、 )作笔,在浸有饱和NaCl
溶液和石蕊溶液的湿润试纸上同时写字, 端的字迹呈白色。下列结论正确的是A.a为负极
B. 端的字迹呈蓝色
C.电子流向为:
D.如果将 、 换成铜棒,与碳棒作电极时的现象相同
【答案】B
【解析】A.根据实验现象,a'端呈白色,即生成了氯气,即氯离子失去电子,为阳极,即a为正极,A错
误; B.b'端为阴极,水得到电子放电的同时,生成氢氧根离子,遇石蕊变蓝,B正确;C.电子从电源的
负极出来,即从a极出来,而不是b极,C错误;D. 如果换成铜棒,铜做阳极放电,现象与碳作电极时
不相同,D错误;故选B。
2.(2022·重庆·统考高考真题)硝酮是重要的有机合成中间体,可采用“成对间接电氧化”法合成。电解
槽中水溶液的主要成分及反应过程如图所示。
下列说法错误的是
A.惰性电极2为阳极 B.反应前后WO /WO 数量不变
C.消耗1mol氧气,可得到1mol硝酮 D.外电路通过1mol电子,可得到1mol水
【答案】C
【解析】A.惰性电极2,Br-被氧化为Br ,惰性电极2为阳极,故A正确;B.WO /WO 循环反应,反
2
应前后WO /WO 数量不变,故B正确;C.总反应为氧气把二丁基-N-羟基胺氧化为硝酮,1mol二丁
基-N-羟基胺失去2molH原子生成1mol硝酮,氧气最终生成水,根据氧原子守恒,消耗1mol氧气,可得
到2mol硝酮,故C错误;D.外电路通过1mol电子,生成0.5molHO,HO 最终生成水,根据氧原子守
2 2 2 2
恒,可得到1mol水,故D正确;选C。
3.(2023·浙江·高考真题)在熔融盐体系中,通过电解 和 获得电池材料 ,电解装置如图,下列说法正确的是
A.石墨电极为阴极,发生氧化反应
B.电极A的电极反应:
C.该体系中,石墨优先于 参与反应
D.电解时,阳离子向石墨电极移动
【答案】C
【分析】由图可知,在外加电源下石墨电极上C转化为CO,失电子发生氧化反应,为阳极,与电源正极
相连,则电极A作阴极, 和 获得电子产生电池材料 ,电极反应为
。
【解析】A.在外加电源下石墨电极上C转化为CO,失电子发生氧化反应,为阳极,选项A错误;B.电
极A的电极反应为 ,选项B错误;C.根据图中信息可知,该体系中,石墨优
先于 参与反应,选项C正确;D.电解池中石墨电极为阳极,阳离子向阴极电极A移动,选项D错误;
答案选C。
4.(2022·辽宁·统考高考真题)镀锌铁钉放入棕色的碘水中,溶液褪色;取出铁钉后加入少量漂白粉,溶
液恢复棕色;加入 ,振荡,静置,液体分层。下列说法正确的是
A.褪色原因为 被 还原 B.液体分层后,上层呈紫红色
C.镀锌铁钉比镀锡铁钉更易生锈 D.溶液恢复棕色的原因为 被氧化
【答案】D
【解析】A. 比 活泼,更容易失去电子,还原性更强,先与 发生氧化还原反应,故溶液褪色原因为
被 还原,A项错误;B.液体分层后, 在 层, 的密度比水大,则下层呈紫红色,B项错误;
C.若镀层金属活泼性大于 ,则 不易生锈,反之,若 活泼性大于镀层金属,则 更易生锈,由于活
泼性: ,则镀锡铁钉更易生锈,C项错误;D.漂白粉的有效成分为 ,其具有强氧化性,
可将 氧化,D项正确;答案选D。
5.(2023·浙江·统考高考真题)氯碱工业能耗大,通过如图改进的设计可大幅度降低能耗,下列说法不正
确的是A.电极A接电源正极,发生氧化反应
B.电极B的电极反应式为:
C.应选用阳离子交换膜,在右室获得浓度较高的 溶液
D.改进设计中通过提高电极B上反应物的氧化性来降低电解电压,减少能耗
【答案】B
【解析】A.电极A是氯离子变为氯气,化合价升高,失去电子,是电解池阳极,因此电极A接电源正极,
发生氧化反应,故A正确;B.电极B为阴极,通入氧气,氧气得到电子,其电极反应式为:
,故B错误;C.右室生成氢氧根,应选用阳离子交换膜,左边的钠离子进入到右边,
在右室获得浓度较高的 溶液,故C正确;D.改进设计中增大了氧气的量,提高了电极B处的氧化
性,通过反应物的氧化性来降低电解电压,减少能耗,故D正确。综上所述,答案为B。
6.(2022·湖北·统考高考真题)下列实验装置(部分夹持装置略)或现象错误的是
A.滴入酚酞溶液 B.吸氧腐蚀 C.钠的燃烧 D.石蜡油的热分解
【答案】C
【解析】A.碳酸钠和碳酸氢钠都会因水解而使溶液显碱性,碳酸钠的碱性强于碳酸氢钠,滴入酚酞溶液
后,碳酸钠溶液呈现红色,碳酸氢钠的溶液呈现浅红色,A正确;B.食盐水为中性,铁钉发生吸氧腐蚀,
试管中的气体减少,导管口形成一段水柱,B正确;C.钠燃烧温度在400℃以上,玻璃表面皿不耐高温,
故钠燃烧通常载体为坩埚或者燃烧匙,C错误;D.石蜡油发生热分解,产生不饱和烃,不饱和烃与溴发
生加成反应,使试管中溴的四氯化碳溶液褪色,D正确;故答案选C。
7.(2021·湖南·统考高考真题)下列说法正确的是
A.糖类、蛋白质均属于天然有机高分子化合物
B. 粉末在空气中受热,迅速被氧化成
C. 可漂白纸浆,不可用于杀菌、消毒D.镀锌铁皮的镀层破损后,铁皮会加速腐蚀
【答案】B
【解析】A.糖类分为单糖、二糖和多糖,其中属于多糖的淀粉、纤维素的相对分子质量上万,属于天然
高分子化合物,蛋白质也属于天然有机高分子化合物,而单糖和二糖相对分子质量较小,不属于天然高分
子化合物,A错误;B.氧化亚铁具有较强的还原性,在空气中受热容易被氧气氧化为稳定的四氧化三铁,
B正确;C.二氧化硫除了具有漂白作用,可漂白纸浆、毛和丝等,还可用于杀菌消毒,例如,在葡萄酒
酿制过程中可适当添加二氧化硫,起到杀菌、抗氧化作用,C错误;D.镀锌的铁皮镀层破损后构成原电
池,锌作负极,铁作正极被保护,铁皮不易被腐蚀,D错误;故选B。