文档内容
专题 09 化学反应的热效应
第 25 练 反应热的计算
1.下列关于盖斯定律的说法不正确的是( )
A.不管反应是一步完成还是分几步完成,其反应热相同
B.反应热只与反应体系的始态和终态有关,而与反应的途径无关
C.有些反应的反应热不能直接测得,可通过盖斯定律间接计算得到
D.根据盖斯定律,热化学方程式中△H直接相加即可得总反应热
2.下列与化学反应能量变化相关的叙述正确的是( )
A. 为“-”时,表示该反应为吸热反应
B.反应热的大小与生成物所具有的能量与反应物所具有的能量无关
C.化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关
D.同温同压下,H(g)+Cl(g)=2HCl(g)在光照和点燃条件下的 不同
2 2
3.下列关于盖斯定律描述不正确的是( )
A.化学反应的反应热不仅与反应体系的始态和终态有关,也与反应的途径有关
B.盖斯定律遵守能量守恒定律
C.利用盖斯定律可间接计算通过实验难测定的反应的反应热
D.利用盖斯定律可以计算有副反应发生的反应的反应热
4.强酸与强碱的稀溶液发生中和反应的热效应H+(aq)+OH- (aq)=H O(aq) ΔH =-57.3 kJ•mol-1,向1L
2 1
0.5mol·L-1的NaOH溶液中加入下列物质:稀醋酸;浓硫酸;稀硝酸,恰好完全反应对应的热效应 H、
1
H、 H 的关系正确的是( )
2 3
A. H> H> H B. H< H< H
1 2 3 1 2 3
C. H= H> H D. H> H> H
1 3 2 1 3 2
5.已知:(1)2H (g)+O(g)=2HO(g) ΔH =a kJ•mol-1
2 2 2 1
(2)4H (g)+2O(g)=4HO(g) ΔH=b kJ•mol-1
2 2 2 2
(3)2H (g)+O(g)=2HO(l) ΔH=c kJ•mol-1
2 2 2 3
(4)4H (g)+2O(g)=4HO(l) ΔH=d kJ•mol-1
2 2 2 4
则a、b、c、d的关系正确的是( )A.2a=b<0 B.2c=d>0 C.a<c<0 D.b>d>0
6.天然气经O 和HO(g)重整制合成气,再由合成气制备甲醇的相关反应如下:
2 2
①主反应:CH(g)+ O(g)=CO(g)+2H(g) ∆H
4 2 2 1
②副反应:CH(g)+2O(g)=CO (g)+2HO(g) ∆H
4 2 2 2 2
③主反应:CH(g)+HO(g)=CO(g)+3H (g) ∆H=+206.1 kJ•mol-1
4 2 2 3
④主反应:CO(g)+2H(g)=CH OH(g) ∆H=-90.0 kJ•mol-1
2 3 4
⑤主反应:CO(g)+3H(g)=CH OH(g)+H O(g) ∆H=-49.0 kJ•mol-1
2 2 3 2 5
下列说法不正确的是( )
A.∆H 大于∆H
1 2
B.反应①为反应③提供能量
C.∆H-4∆H=659.3 kJ·mol-1
2 1
D.CO(g)+HO(g) CO(g)+H(g)的正反应为放热反应
2 2 2
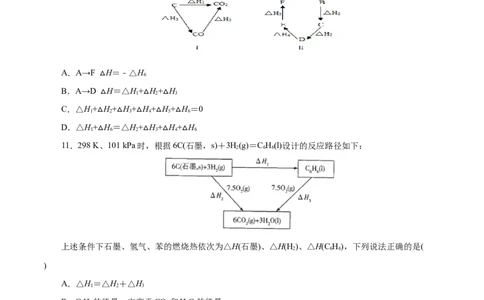
7.盖斯定律指出:化学反应的反应热只与反应的始态和终态有关,而与具体反应途径无关。物质A
在一定条件下可发生一系列转化,由图判断下列错误的是( )
A.ΔH+ΔH+ΔH+ΔH=1 B.A→D,ΔH=-ΔH
1 2 3 4 4
C.ΔH+ΔH =-ΔH-ΔH D.B→D ,ΔH=ΔH+ΔH
1 2 3 4 2 3
8.在1 200 ℃时,天然气脱硫工艺中会发生下列反应:
HS(g)+O(g)===SO(g)+HO(g) ΔH
2 2 2 2 1
2HS(g)+SO (g)===S(g)+2HO(g) ΔH
2 2 2 2 2
HS(g)+O(g)===S(g)+HO(g) ΔH
2 2 2 3
2S(g)===S (g) ΔH
2 4
则ΔH 的正确表达式为( )
4
A.ΔH=(ΔH+ΔH-3ΔH) B.ΔH=(3ΔH-ΔH-ΔH)
4 1 2 3 4 3 1 2
C.ΔH=(ΔH+ΔH-3ΔH) D.ΔH=(ΔH-ΔH-3ΔH)
4 1 2 3 4 1 2 3
9.假设反应体系的始态为甲,中间态为乙,终态为丙,它们之间的变化如图所示,则下列说法不正
确的是( )A.|ΔH|>|ΔH| B.|ΔH|<|ΔH|
1 2 1 3
C.ΔH+ΔH +ΔH =0 D.甲→丙的ΔH=ΔH+ΔH
1 2 3 1 2
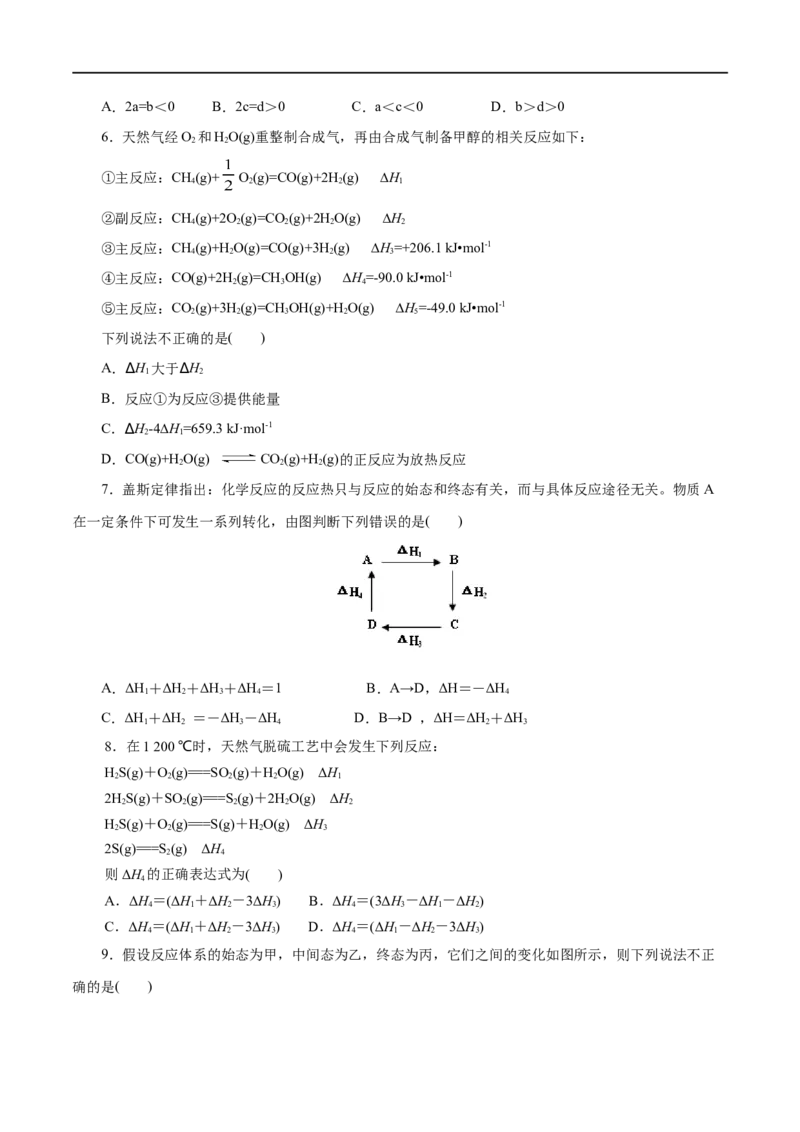
10.已知化学反应的热效应只与反应物的初始状态和生成物的最终状态有关,例如图(Ⅰ)所示:△H
1
=△H+ H,根据上述原理和图(Ⅱ)所示,判断各对应的反应热关系中不正确的是( )
2 3
△
A.A→F H=﹣△H
6
B.A→D △H=△H+ H+ H
1 2 3
C.△H+ △H+ H+ H△+ H△+ H=0
1 2 3 4 5 6
D.△H+△H=△△H△+ H△+ H△+ H
1 6 2 3 4 6
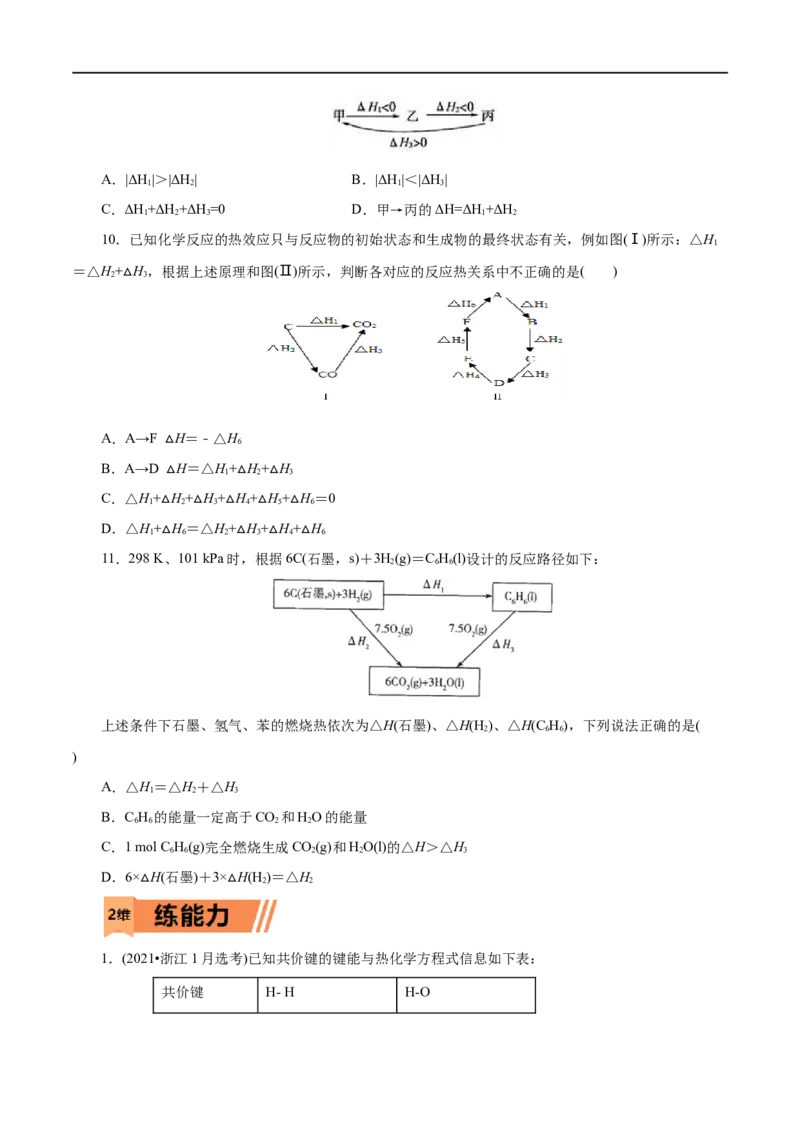
11.298 K△、101 kPa时△,根△据6C△(石墨,s)+3H(g)=C H(l)设计的反应路径如下:
2 6 6
上述条件下石墨、氢气、苯的燃烧热依次为△H(石墨)、△H(H )、△H(C H),下列说法正确的是(
2 6 6
)
A.△H=△H+△H
1 2 3
B.C H 的能量一定高于CO 和HO的能量
6 6 2 2
C.1 mol C H(g)完全燃烧生成CO(g)和HO(l)的△H>△H
6 6 2 2 3
D.6× H(石墨)+3× H(H )=△H
2 2
△ △
1.(2021•浙江1月选考)已知共价键的键能与热化学方程式信息如下表:
共价键 H- H H-O键能/(kJ·mol-1) 436 463
2H(g) + O (g)=2HO(g) ΔH=
热化学方程式 2 2 2
-482kJ·mol-1
则2O(g)=O (g)的ΔH为( )
2
A.428 kJ·mol-1 B.-428 kJ·mol-1 C.498 kJ·mol-1 D.-498 kJ·mol-1
2.已知:Fe O(s)+C(s)===CO(g)+2Fe(s) ΔH=234.1 kJ·mol-1 ①
2 3 2 1
C(s)+O(g)===CO (g) ΔH=-393.5 kJ·mol-1 ②
2 2 2
则2Fe(s)+O(g)===Fe O(s)的ΔH 是( )
2 2 3 3
A.-824.4 kJ·mol-1 B.-627.6 kJ·mol-1
C.-744.7 kJ·mol-1 D.-169.4 kJ·mol-1
3.在298K、100kPa时,有下列反应:O(g)+2H(g)=2HO(g)∆H;Cl(g)+H(g)=2HCl(g)∆H;2Cl(g)
2 2 2 1 2 2 2 2
+2H O(g)=4HCl(g)+O (g)∆H,则∆H 与∆H 和∆H 间的关系正确的是( )
2 2 3 3 1 2
A.∆H=∆H+∆H B.∆H=∆H+2∆H
3 1 2 3 1 2
C.∆H=2∆H-∆H D.∆H=∆H-∆H
3 2 1 3 1 2
4.已知:2C(s)+O(g)=2CO(g) H=-221.0 kJ·mol-1
2
① ②2H(g)+O(g)=2H△O(g) H=-483.6kJ·mol-1
2 2 2
则制备水煤气的反应C(s)+HO(g)=CO(g)+H△(g)的△H为( )
2 2
A.+262.6 kJ·mol-1 B.-131.3 kJ·mol-1
C.-352.3 kJ·mol-1 D.+131.3 kJ·mol-1
5.键能是指在25 ℃、1.01×105 Pa时,将1 mol理想气体分子AB拆开为中性气态原子A和B时所
需要的能量。已知键能:H—H为436 kJ·mol-1;Cl—Cl为243 kJ·mol-1;H—Cl为431 kJ·mol-1。下列说法
中不正确的是( )
A.1 mol H 中的化学键断裂时需要吸收436 kJ能量
2
B.2 mol HCl分子中的化学键形成时要释放862 kJ能量
C.此反应的热化学方程式为
H(g)+Cl(g)===2HCl(g) ΔH=183 kJ·mol-1
2 2
D.此反应的热化学方程式为H(g)+Cl(g)===HCl(g) ΔH=-91.5 kJ·mol-1
2 2
6.化学反应:C(s)+O(g)===CO(g) ΔH<0
2 1
CO(g)+O(g)===CO (g) ΔH<0
2 2 2
C(s)+O(g)===CO (g) ΔH<0;
2 2 3
下列说法中不正确的是(相同条件下)( )
A.56 g CO和32 g O 所具有的总能量大于88 g CO 所具有的总能量
2 2
B.12 g C所具有的能量一定大于28 g CO所具有的能量
C.ΔH+ΔH=ΔH
1 2 3D.将两份质量相等的碳燃烧,生成CO 的反应比生成CO的反应放出的热量多
2
7.用HO 和HSO 的混合溶液可溶出废旧印刷电路板上的铜。已知:
2 2 2 4
①Cu(s)+2H+(aq)=Cu2+(aq)+H (g) ΔH=+64.39 kJ·mol-1
2 2
②2HO(l)=2H O(l)+O(g) ΔH=-196.46 kJ·mol-1
2 2 2 2 2
② H(g)+ O(g)=HO(1) ΔH=-285.84 kJ·mol-1
2 2 2
在HSO 溶液中,1 mol Cu(s)与HO(l)反应生成Cu2+(aq)和HO(l)的反应热ΔH等于( )
2 4 2 2 2
A.-319.68 kJ·mol-1 B.-417.91 kJ·mol-1
C.-448.46 kJ·mol-1 D.+546.69 kJ·mol-1
8. SF 分子中只存在S-F键。已知:1moLS(s)转化为气态硫原子吸收能量280kJ,断裂1moLS-F键需
6
吸收330kJ能量。S(s)+3F (g)=SF(s) H= -1220kJ·mol-1,则断裂1moLF-F键需要的能量为( )
2 6
A.80kJ·mol-1 B.160kJ·mol-1△ C.240kJ·mol-1 D.320kJ·mol-1
9.氢气和氧气反应生成水的能量关系如图所示,下列说法不正确的是( )
A.∆H<0;∆H>0 B.∆H>∆H+∆H+∆H
2 5 1 2 3 4
C.∆H+∆H+∆H+∆H+∆H=0 D.O-H键键能为 |∆H|
1 2 3 4 5 1
10.NO催化O 分解的反应机理与总反应为:
3
第一步:O(g)+NO(g)→O (g)+NO g) ∆H
3 2 2( 1
第二步:NO (g)→NO(g)+O(g) ∆H
2 2
第三步:O(g)+O (g)→2O (g) ∆H
3 2 3
总反应:2O(g) →3Q (g) ∆H
3 2 4
其能量与反应历程的关系如图所示。下列叙述不正确的是( )A.∆H>0,∆H>0 B.∆H=∆H−∆H
1 2 2 3 1
C.∆H>∆H,∆H>∆H D.∆H=∆H−∆H−∆H
2 1 1 3 3 4 2 1
11.在一定条件下,S(s)和O(g)发生反应依次转化为SO (g)和SO (g)。反应过程和能量关系可用如图
8 2 2 3
简单表示(图中的ΔH表示生成1mol含硫产物的数据)。由图得出的结论正确的是( )
A.S(s)的燃烧热ΔH=-8(a+b)kJ·mol-1
8
B.2SO (g) 2SO (g)+O(g) ΔH=-2bkJ·mol-1
3 2 2
C.S(s)+8O(g)=8SO(g) ΔH=-akJ·mol-1
8 2 2
D.由1molS (s)生成SO 的反应热ΔH=-8(a+b)kJ·mol-1
8 3
12.在热的碱性水溶液1 molCl-、1 molClO - (x=1,2,3,4)的能量(kJ)相对大小如图所示。下列有关
x
说法正确的是( )2ClO- (aq)=Cl-(aq)+ClO -(aq) ΔH
2 1
3ClO- (aq)=2Cl-(aq)+ClO - (aq) ΔH
3 2
2ClO - (aq)=Cl-(aq)+ClO - (aq) ΔH
2 4 3
2ClO - (aq)=ClO-(aq)+ClO - (aq) ΔH
2 3 4
A.ΔH<0 ΔH>0 B.ΔH<ΔH C.ΔH<0 ΔH<0 D.ΔH>ΔH
1 2 1 2 3 4 3 4
13.生成水的能量关系如图所示:下列说法不正确的是( )
A.△H>0
2
B.若2H(g)+O(g)=2HO(l) H,则△H< H
2 2 2 4 4 1
C.一定条件下,气态原子生成1 m△ol H-O放出△a kJ热量,则该条件下△H=-4a kJ•mol-1
3
D.△H+△H+△H=0
1 2 3
14.根据下列能量变化示意图,说法不正确的是( )
A.破坏相同质量的NO (g)和NO(g)中的化学键,后者所需的能量较高
2 2 4
B.NH(l)+NO(g)=3/2N (g) +2 HO(l) ∆H;则∆H>∆H
2 4 2 2 2 4
C.2HO(g) 2H(g)+ O (g) ∆H<-∆H
2 2 2 6 5
D.∆H=∆H+∆H+∆H+∆H
5 1 2 3 4
1.(2021•浙江6月选考)相同温度和压强下,关于反应的 ,下列判断正确的是( )A.ΔH>0,ΔH>0 B.ΔH=ΔH+ΔH
1 2 3 1 2
C.ΔH>ΔH,ΔH>ΔH D.ΔH=ΔH+ΔH
1 2 3 2 2 3 4
2.(2022·浙江省1月选考)相关有机物分别与氢气发生加成反应生成1mol环己烷( )的能量变化如图
所示:
下列推理不正确的是( )
A.2ΔH≈ΔH,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比
1 2
B.ΔH<ΔH,说明单双键交替的两个碳碳双键间存在相互作用,有利于物质稳定
2 3
C.3ΔH<ΔH,说明苯分子中不存在三个完全独立的碳碳双键
1 4
D.ΔH-ΔH <0,ΔH-ΔH >0,说明苯分子具有特殊稳定性
3 1 4 3
3.(2022·浙江省6月选考)标准状态下,下列物质气态时的相对能量如下表:
物质(g) O H HO HOO H O HO HO
2 2 2 2 2
21
能量/ kJ·mol-l 249 39 10 0 0
8
可根据HO(g)+HO(g)= H O(g)计算出HO 中氧氧单键的键能为214 kJ·mol-l。下列说法不正确的是(
2 2 2 2
)
A.H 的键能为436 kJ·mol-l
2
B.O 的键能大于HO 中氧氧单键的键能的两倍
2 2 2
C.解离氧氧单键所需能量: HOO<HO
2 2
D.HO(g)+O(g)= H O(g) ΔH=-143kJ·mol−1
2 2 2
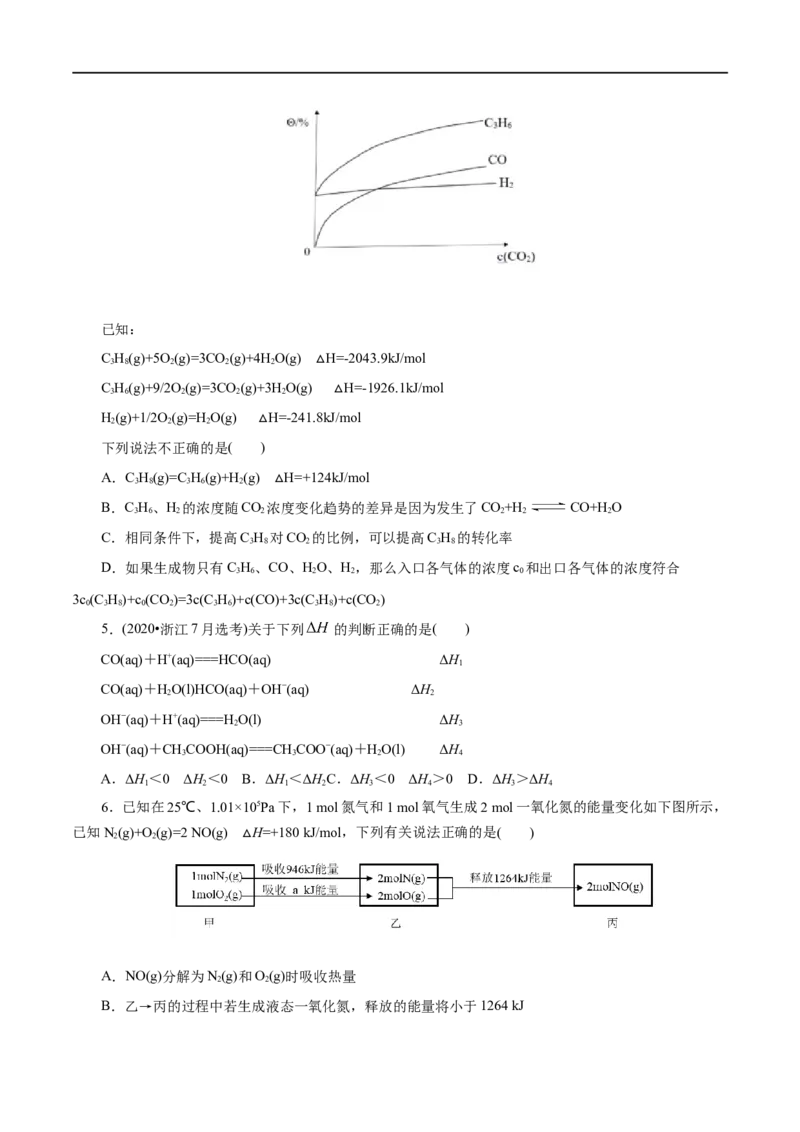
4.(2021•北京卷)已知C H 脱H 制烯烃的反应为C H = C H+H 。固定C H 浓度不变,提高CO 浓度,
3 8 2 3 8 3 6 2 3 8 2
测定出口处C H、H、CO浓度。实验结果如下图。
3 6 2已知:
C H(g)+5O(g)=3CO (g)+4HO(g) H=-2043.9kJ/mol
3 8 2 2 2
C 3 H 6 (g)+9/2O 2 (g)=3CO 2 (g)+3H 2 O(g) △ H=-1926.1kJ/mol
H
2
(g)+1/2O
2
(g)=H
2
O(g) H=-241.8kJ△/mol
下列说法不正确的是( △)
A.C H(g)=C H(g)+H(g) H=+124kJ/mol
3 8 3 6 2
B.C H、H 的浓度随CO 浓△度变化趋势的差异是因为发生了CO+H CO+HO
3 6 2 2 2 2 2
C.相同条件下,提高C H 对CO 的比例,可以提高C H 的转化率
3 8 2 3 8
D.如果生成物只有C H、CO、HO、H,那么入口各气体的浓度c 和出口各气体的浓度符合
3 6 2 2 0
3c(C H)+c (CO)=3c(C H)+c(CO)+3c(C H)+c(CO )
0 3 8 0 2 3 6 3 8 2
5.(2020•浙江7月选考)关于下列 的判断正确的是( )
CO(aq)+H+(aq)===HCO(aq) ΔH
1
CO(aq)+HO(l)HCO(aq)+OH−(aq) ΔH
2 2
OH−(aq)+H+(aq)===HO(l) ΔH
2 3
OH−(aq)+CHCOOH(aq)===CHCOO−(aq)+HO(l) ΔH
3 3 2 4
A.ΔH<0 ΔH<0 B.ΔH<ΔH C.ΔH<0 ΔH>0 D.ΔH>ΔH
1 2 1 2 3 4 3 4
6.已知在25℃、1.01×105Pa下,1 mol氮气和1 mol氧气生成2 mol一氧化氮的能量变化如下图所示,
已知N(g)+O(g)=2 NO(g) H=+180 kJ/mol,下列有关说法正确的是( )
2 2
△
A.NO(g)分解为N(g)和O(g)时吸收热量
2 2
B.乙→丙的过程中若生成液态一氧化氮,释放的能量将小于1264 kJC.O(g)=2O(g) H=+498 kJ/mol
2
D.甲、乙、丙中△物质所具有的总能量大小关系为:乙>甲>丙
7.已知室温下,将 CuSO ·5H O(s)溶于水会使溶液温度降低,将 CuSO (s)溶于水会使溶液温度升高。
4 2 4
则下列能量转化关系的判断不正确的是( )
A.△H>0 B.△H>△H C.△H>△H D.△H= H+ H
1 2 3 3 1 2 1 3
8.氢氟酸是一种弱酸,可用来刻蚀玻璃。 △ △
①HF(aq)+OH-(aq) = F-(aq)+H O(l) ΔH=a kJ·mol-1
2
②HO+(aq)+OH-(aq) = 2H O(l) ΔH=b kJ·mol-1
3 2
③HF(aq)+HO(l) HO+(aq)+F-(aq) ΔH=c kJ·mol-1
2 3
④F-(aq)+HO(l) ⇌HF(aq)+OH-(aq) ΔH=d kJ·mol-1
2
已知:a<b<0,⇌下列说法正确的是( )
A.HF的电离过程吸热 B.c=a-b,c<0
C.c>0,d<0 D.d=b+c,d<0