文档内容
第 28 讲 电离平衡
(模拟精练+真题演练)
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12×5分)
1.(2023·浙江金华·模拟预测)下列物质中属于强电解质且水溶液显酸性的是
A.盐酸 B.AlCl C.CHCOOH D.NaSiO
3 3 2 3
【答案】B
【解析】A.盐酸属于混合物,不属于电解质;故A不符合题意;B.AlCl 属于盐,是强电解质,而且电
3
解后溶液中Al3+水解使得溶液呈酸性;故B符合题意;C.CHCOOH属于弱电解质;故C不符合题意;
3
D.NaSiO 是强电解质, 水解呈碱性;故D不符合题意;故答案选B。
2 3
2.(2023·全国·模拟预测)实验测得浓度均为 的 溶液和 溶液的pH随温
度的变化情况如图所示。下列说法错误的是
A. 时, 的电离平衡常数约为
B. 后, 溶液的pH随温度的升高而增大的原因可能是 的挥发
C.升高温度, 溶液中 减小, 增大,pH减小
D. 溶液中存在:
【答案】C
【解析】A. 时, 的pH=a, 的电离平衡常数约为 ,故A正
确;B.升高温度,促进 电离,溶液中 增大, 后, 减小,说明醋酸的浓度降低,
的挥发会导致 降低,故B正确;C.升高温度,使 水解平衡正向移动,
溶液中 增大,故C错误;D.根据质子守恒, 溶液中
,故D正确;选C。3.(2023·浙江·校联考模拟预测)下列说法不正确的是
A.相同温度下, 相等的氨水、 溶液中, 相等
B. 的醋酸溶液的物质的量浓度大于 的醋酸溶液的10倍
C. 均为4的盐酸和氯化铵溶液等体积混合后,所得溶液的
D.用同浓度的 溶液分别与等体积、等 的盐酸和醋酸溶液恰好完全反应,盐酸消耗 溶液的
体积更大
【答案】D
【解析】A.相同温度下,水的离子积相等, 相等的氨水、 溶液中, 相等,则溶液中
相等,A正确;B.醋酸为弱酸,不能完全电离,浓度越大,电离程度越小, 的醋酸溶液的
物质的量浓度为 ( 为电离度), 的醋酸溶液的物质的量浓度为 ( 为电离度),
故前者比后者的10倍还大,B正确;C. 均为4的盐酸和氯化铵溶液等体积混合的瞬间,
,不发生变化,铵根离子和一水合氨的浓度瞬间变为原来的二分之一,则二者的
比值不变,故所得溶液中水的电离平衡没有移动,氯化铵的水解平衡没有移动,混合溶液中
, ,C正确;D.醋酸是弱酸,等体积、等 的盐酸和醋酸溶液中醋酸的
物质的量大于盐酸的物质的量,则用同浓度的 溶液分别与等体积、等 的盐酸和醋酸溶液恰好完
全反应,醋酸消耗 溶液的体积更大,D错误。故选D。
4.(2023·上海奉贤·统考二模)以下物质属于弱电解质的是
A.乙醇 B.乙酸 C.次氯酸钠 D.高锰酸钾
【答案】B
【解析】A.乙醇在水溶液和熔融状态下都无法导电,属于非电解质,A错误;B.乙酸在水中部分电离,
属于弱电解质,B正确;C.次氯酸钠在水中完全电离产生Na+和ClO-,是强电解质,C错误;D.高锰酸
钾在水中完全电离产生K+和 ,是强电解质,D错误;故答案选B。
5.(2023·江西宜春·江西省宜丰中学校考模拟预测)化学常用图像直观地描述化学反应的进程或结果。下
列图像描述不正确的是
A.图①表示弱电解质在水中建立电离平衡的过程
B.图②表示强碱滴定强酸的滴定曲线C.图③表示25℃时分别稀释pH=11的NaOH溶液和氨水时溶液pH的变化,曲线Ⅱ表示氨水
D.图④可表示 溶液中通入 至过量的过程中溶液导电性的变化
【答案】D
【解析】A.弱电解质存在电离平衡,平衡时正逆反应速率相等,图像符合电离特点,选项A正确;B.
强碱滴定强酸,溶液pH增大,存在pH的突变,图像符合,选项B正确;C.25℃时分别稀释pH=11的
NaOH溶液和氨水,弱碱溶液氨水的pH变化小,强碱NaOH的pH变化大,曲线Ⅱ表示氨水,图像符合,选
项C正确;D.向CHCOOH溶液中通入NH 生成醋酸铵,体积不变,自由移动离子浓度变大,导电性开
3 3
始应增强,而不是减弱,图像不符合,选项D错误;答案选D。
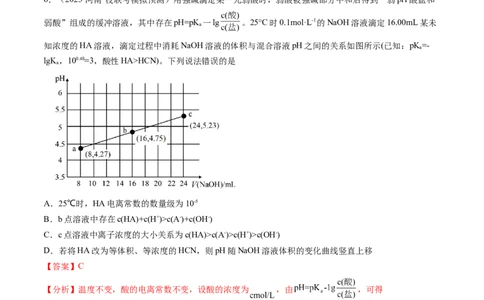
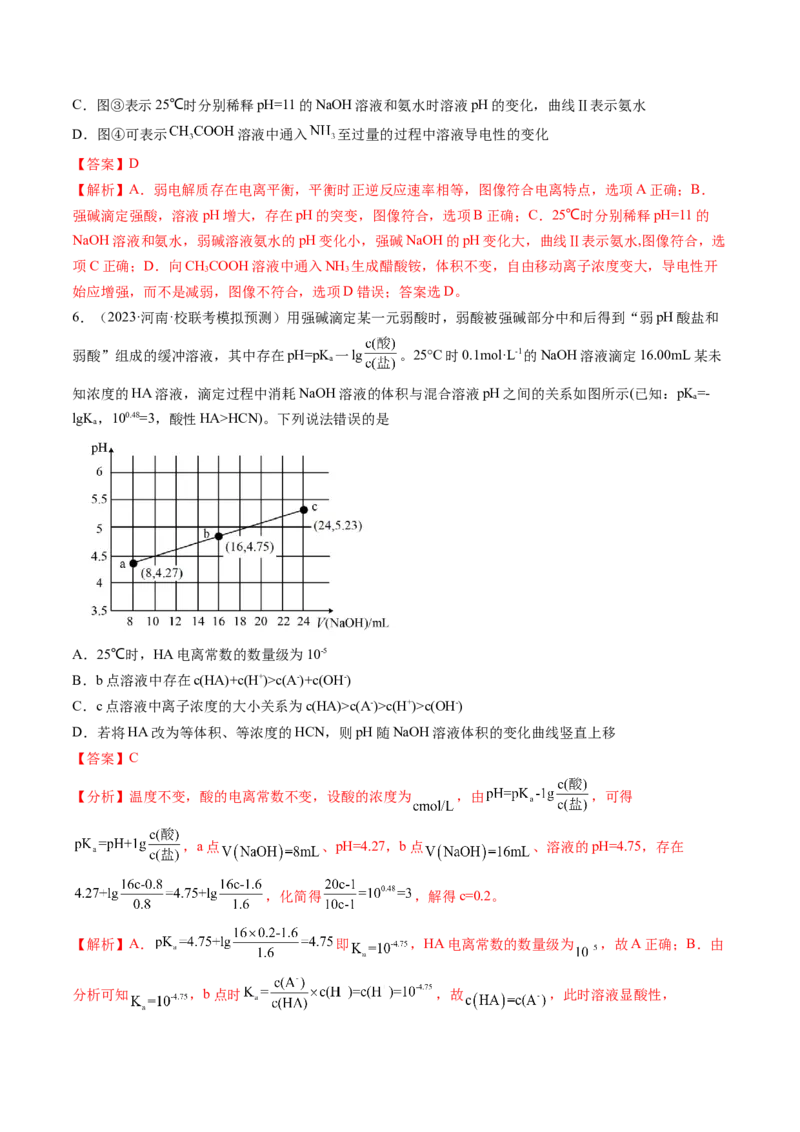
6.(2023·河南·校联考模拟预测)用强碱滴定某一元弱酸时,弱酸被强碱部分中和后得到“弱pH酸盐和
弱酸”组成的缓冲溶液,其中存在pH=pK 一lg 。25°C时0.1mol·L-1的NaOH溶液滴定16.00mL某未
a
知浓度的HA溶液,滴定过程中消耗NaOH溶液的体积与混合溶液pH之间的关系如图所示(已知:pK=-
a
lgK,100.48=3,酸性HA>HCN)。下列说法错误的是
a
A.25℃时,HA电离常数的数量级为10-5
B.b点溶液中存在c(HA)+c(H+)>c(A-)+c(OH-)
C.c点溶液中离子浓度的大小关系为c(HA)>c(A-)>c(H+)>c(OH-)
D.若将HA改为等体积、等浓度的HCN,则pH随NaOH溶液体积的变化曲线竖直上移
【答案】C
【分析】温度不变,酸的电离常数不变,设酸的浓度为 ,由 ,可得
,a点 、pH=4.27,b点 、溶液的pH=4.75,存在
,化简得 ,解得c=0.2。
【解析】A. 即 ,HA电离常数的数量级为 ,故A正确;B.由
分析可知 ,b点时 ,故 ,此时溶液显酸性,,故 ,故B正确;C.由B项分析可知b点时,故 ,
则随氢氧化钠溶液体积增大,c点时溶液 ,由图可知溶液呈酸性 ,酸电离程度
较小,所以离子浓度的大小关系为: ,故C错误;D.由HA的酸性强于HCN
可知,HA的电离常数大于HCN,由 可知,当 相等时,酸的电离常数越大,溶液
$pH$越小,则若将HA改为等体积等浓度的HCN,则pH随NaOH溶液体积的变化曲线竖直上移,故D正
确;故选C。
7.(2023·安徽安庆·安庆一中校考三模)常温下,二元酸HA的K (H A)= 1.0 ×10-2。 在某体系中,H+与
2 a2 2
A2-离子不能穿过隔膜,HA-可自由穿过该膜(如图所示)。溶液中c (H A)=c(HA-)+c(A2-),当达到平衡时,
总 2
下列叙述正确的是
A.溶液I中: c(H+)-c(OH-)=c (H A)
总 2
B.溶液II中: c (H A) >c(H+)>c(HA-) >c(OH-)
2
C.溶液I和II中的c (H A)不相等
总 2
D.溶液I和II中的c(A2-)之比为105
【答案】C
【分析】由c (H A)=c(HA-)+c(A2-)可知溶液中不存在HA分子,说明HA的第一步电离是完全电离,由
总 2 2 2
H+与A2-离子不能穿过隔膜,HA-可自由穿过该膜可知溶液I和溶液II中HA-的浓度相同。
【解析】A.溶液I中pH=7.0,c(H+)=c(OH-),A错误;B.HA的第一步电离是完全电离,所以溶液中不
2
存在HA分子,B错误;C.结合K (H A)=1.0 ×10-2可计算出c(A2-)= ,又因溶
2 a2 2
液I和溶液II中HA-的浓度相同而H+浓度不同,因此c(A2-)的浓度不同,又因c (H A) =c(HA-)+c(A2-),故
总 2
溶液I和II中的c (H A)不相等,C正确;D.由c(A2-)= 可计算出二者c(A2-)的
总 2
比值为10-1:10-7=106,D错误;故选C。
8.(2023·湖北荆州·统考模拟预测)1923年由布朗斯特和劳里提出酸碱质子理论认为,在反应过程中能给
出质子( )的分子或离子都是酸,凡是能接受质子的分子或离子都是碱。按照“酸碱质子理论”,下列叙
述错误的是
A.水既属于酸又属于碱
B.可以根据 的性质推断 的碱性较强
C.根据 ,则碱性:D. 是酸碱反应
【答案】B
【解析】A.根据酸碱质子理论可知,水能电离产生H+,为酸,水能和H+生成HO+,为碱,所以水既属
3
于酸又属于碱,A正确;B. 是强酸, 是弱碱 ,B错误;C.根据
,可知HO结合H+能力大于HC O 结合H+能量力,所以碱性:
2 2
,C正确;D. ,BrO-结合H+,HO给出H+,所以该反应是酸碱反
2
应,D正确;故答案选B。
9.(2023·河南郑州·郑州外国语学校校考模拟预测)已知电离常数:K(HCN)=5×10-10,HCO:
a 2 3
K =4.3×10-7,K =5.6×10-11,下列离子方程式书写正确的是
a1 a2
A.向KCN(aq)中通入少量的CO 气体:CO+H O+2CN-=2HCN+CO
2 2 2
B.少量SO 通入Ca(ClO) 溶液中:SO +H O+Ca2++2ClO-=CaSO ↓+2HClO
2 2 2 2 3
C.氢氧化铁沉淀溶解于过量氢碘酸溶液中:2Fe(OH) +6H++2I-=2Fe2++6H O+I
3 2 2
D.向Ba(OH) 溶液中加入少量的NaHCO 溶液:2HCO +Ba2++2OH-=BaCO ↓+CO +2H O
2 3 3 2
【答案】C
【解析】A.由电离常数可知酸性HCO>HCN>HCO ,则反应的离子方程式为CN﹣
2 3
+H O+CO=HCN+HCO ,故A错误;B.将少量SO 通入Ca(ClO) 溶液中,二者发生氧化还原反应,正确
2 2 2 2
的离子方程式为:Ca2++3ClO﹣+H O+SO ═CaSO ↓+2HClO+Cl﹣,故B错误;C.Fe(OH) 溶于HI,后生成的
2 2 4 3
Fe3+能将I﹣氧化为I,自身被还原为Fe2+,离子方程式为2Fe(OH) +6H++2I﹣=2Fe2++I +6H O,故C正确;
2 3 2 2
D.Ba(OH) 溶液中加入少量NaHCO 溶液,HCO 完全转化成BaCO 沉淀,正确的离子方程式为:HCO
2 3 3
+Ba2++OH﹣=BaCO ↓+H O,故D错误;故选C。
3 2
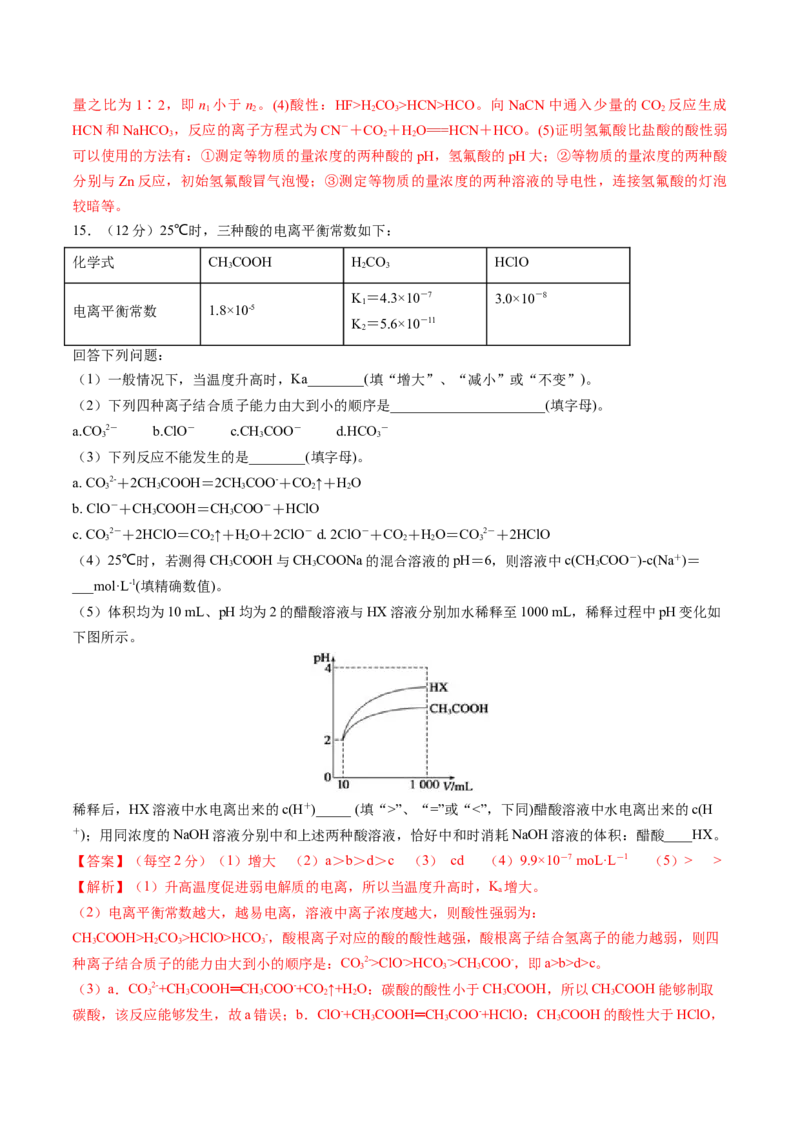
10.(2021·广东·校联考模拟预测)在25℃时,将1.0Lw 溶液与0.1molNaOH固体混合,
充分反应。向混合液中加入 或 固体(忽略体积和温度变化),溶液pH随加入
或 固体的物质的量的变化关系如图所示。下列叙述错误的是
A.b点混合液中B.加入 过程中, 减小
C.25℃时, 的电离平衡常数
D.a、b、c对应的混合液中,水的电离程度由大到小的顺序是b>a>c
【答案】D
【解析】A.b点溶液pH<7,溶液呈酸性,则c(H+)>c(OH-),溶液中存在电荷守恒c(Na+)+c(H+)=c(OH-)
+c(CH COO-),则c(Na+)<c(CHCOO-),所以c(Na+)<c(CHCOOH)+c(CH COO-),故A正确;B.加入
3 3 3 3
CHCOOH过程中c(Na+)不变,溶液中c(CHCOO-)增大,c(H+)增大,则c(OH-)= 减小,则
3 3
减小,故B正确;C.CHCOONa是弱酸强碱盐,溶液呈碱性,由图可知c点溶液呈中性,
3
则醋酸过量,c(H+)=c(OH-)=10-7mol/L,电荷守恒关系式为c(Na+)+c(H+)=c(OH-)+c(CH COO-),则
3
c(CHCOO-)=c(Na+)=0.2mol/L,但c点时c(CHCOOH)+c(CH COO-)=(w+0.1)mol/L,则c点溶液中剩余
3 3 3
c(CHCOOH)=wmol/L-c(CH COO-)=(w-0.1)mol/L,CHCOOH的电离平衡常数K(CHCOOH)=
3 3 3 a 3
,故C正确;D.CHCOOH抑制水电离,在b对应的混合液中加
3
入CHCOOH,水电离程度减小,CHCOO-促进水电离,在b对应的混合液中加入CHCOO-,水电离程度
3 3 3
增大,则水的电离程度由大到小的顺序是c>b>a,故D错误;故选:D。
11.(2023·安徽合肥·合肥市第六中学校考模拟预测)室温下,向20.00 mL0.1 mol·L-1的HAsO 溶液中滴
3 4
加等浓度的NaOH溶液。混合溶液中-lg X[表示 、 、 ]随溶液pH
的变化如图所示。
下列说法正确的是
A.曲线a表示 与溶液pH的关系
B.当消耗20.00 mL的NaOH溶液时,c(Na+ )> > >
C.pH=7.00时,c (Na+) = 3 +3
D.溶液中存在关系: >【答案】C
【解析】A.由题意的HAsO 属于三元弱酸,其三级电离中,电离常数逐渐减小。结合图像当-lg X =0时,
3 4
表示对应的两种离子浓度相等,且曲线a的PH最小,则电离出的氢离子浓度最大,故为第一步电离。结
合电离常数表达式,知曲线a表示 与溶液pH的关系,故A项错误;B.当消耗20.00 mL时,
等体积等浓度混合,溶液中溶质为 , 的电离平衡常数10-7大于水解平衡常数 ,故
> ,故B项错误;C.根据电荷守恒得,c(Na+ )+ c(H+ )= +3 +2
+ c(OH-),此时PH=7.00,c(H+ )= c(OH-),同时由曲线b可知, = ,故有
c(Na+ )= 3 +3 ,故C项正确;D.HAsO 的三级电离中,电离常数逐渐减小,
3 4
Ka>Ka ,则 < ,故D项错误。故答案选C。
2 3
12.(2023·河北衡水·衡水市第二中学校考三模)常温下,用 盐酸滴定 MOH溶液,
滴定曲线如图所示。下列叙述正确的是
A. 的数量级为
B.X→Y过程中,水的电离程度及 均逐渐增大
C.当滴定至溶液呈中性时,
D.Y点溶液中:
【答案】D
【解析】A.由图中X点可知,当中和百分数为50%时, ,此时 ,即
, , ,因此
的数量级为 ,A错误;B.Y点恰好完全反应生成正盐MCl,X→Y过程中碱的浓度逐渐减小,盐的浓
度逐渐增大,生成的强酸弱碱盐水解,促进水的电离,水的电离程度逐渐增大;温度不变, 保持不变,
B错误;C.当溶液呈中性时 ,根据电荷守恒可知 ,,C错误;D.根据质子守恒 ,则Y点溶液中
,D正确。 故选D。
二、主观题(共3小题,共40分)
13.(14分)(2023·四川成都·成都七中校考模拟预测)I.研究水溶液中的粒子行为在研究中具有重要价值。
根据下表所列三种溶液在25℃时的相关数据,按要求填空:
溶液 物质的量浓度 pH
(I)HAc 0.1 mol/L 2.86
(II) 0.1 mol/L 6.14
(III) 0.1 mol/L 1
(1)根据表中数据,写出HAc的电离方程式
(2)比较溶液(II)、(III)中 的大小关系是(II) (III)(填“>”、“<”或“=”)。
(3)溶液(I)和(II)中由水电离出的 之比是 。
II.某小组研究25℃下HAc电离平衡的影响因素。
提出假设 稀释HAc溶液或改变 浓度,HAc电离平衡会发生移动。
设计方案并完成实验 用浓度均为0.1 mol·L 的HAc和NaAc溶液,按下表配制总体积相同的系列溶液;
测定pH,记录数据。
序
V(HAc)/mL V(NaAc)/mL /mL pH
号
I 40.00 / / 0 2.86
II 4.00 / 36.00 0 3.36
VII 4.00 a b 3∶4 4.53
VIII 4.00 4.00 32.00 1∶1 4.65
(4)根据表中信息,补充数据:a= ,b= 。
(5)由实验I和II可知,稀释HAc溶液,电离平衡 (填“正”或“逆”)向移动;结合表中数据,给
出判断理由: 。由实验II~VIII可知,增大 浓度,HAc电离平衡逆向移动。
实验结论 假设成立。
【答案】(每空2分)(1)HAc Ac-+H+
(2)<
⇌
(3)1:105
(4)3.00 33.00(5)正 实验Ⅱ相较于实验Ⅰ,醋酸溶液稀释了10倍,而实验Ⅱ的pH增大值小于1
【解析】(1)0.1mol/L醋酸溶液的pH等于2.86,说明是弱电解质,则其电离方程式为HAc Ac-+H+;
(2)铵根水解显酸性,硫酸氢铵能电离出氢离子抑制铵根的水解,则溶液(Ⅱ)、(Ⅲ)中c( ⇌)的大小关系
是(Ⅱ)<(Ⅲ);
(3)醋酸电离出氢离子抑制水的电离,溶液中由水电离出的c(H+)与溶液中的c(OH-)相同,
1.0×10-11.14mol•L-1,氯化铵溶液中铵根水解促进水的电离,溶液中H+是由
水电离出的,c(H+)=1.0×10-6.14mol•L-1,则溶液(I)和(Ⅱ)中由水电离出的c(H+)之比是(1.0×10-11.14mol•L-1):
(1.0×10-6.14mol•L-1)=1:105;
(4)由表格中数据可知,保证醋酸钠和醋酸物质的量之比为3:4,二者浓度相等,则体积比为3:4,则
a=3.00mL,总体积是40ml,则b=(40-3.00-4.00)mL=33.00mL;
(5)加水稀释,体积增大,平衡向微粒数增多的方向移动,即向电离的正向移动,强酸溶液不存在电离
平衡,稀释10倍pH增大1,而比较实验I、II,醋酸稀释10倍,pH增大值小于1。
14.(14分)(2023·济南一模)常温下,部分酸的电离常数如表所示:
化学式 HF HCN HCO
2 3
电离 K= K= K =4.4×10-7
a a a1
常数 3.5×10-4 5.0×10-10 K =4.7×10-11
a2
(1)c(H+)相同的三种酸,其酸的浓度由大到小的顺序为_____________。
(2)若HCN的起始浓度为0.01 mol·L-1,平衡时c(H+)约为______________mol·L-1。若使此溶液中HCN的
电离程度增大且c(H+)也增大的方法是______________。
(3)中和等量的NaOH,消耗等pH的氢氟酸和硫酸的体积分别为 a L、b L,则a________b(填“大于”
“小于”或“等于”,下同)。
中和等物质的量浓度、等体积的氢氟酸和硫酸需要NaOH的物质的量为n、n,则n________n。
1 2 1 2
(4)向NaCN溶液中通入少量的CO,发生反应的离子方程式为_________________________。
2
(5)设计实验证明氢氟酸比盐酸的酸性弱:__________________________。
【答案】(每空2分)(1)c(HCN)>c(H CO)>c(HF)
2 3
(2)×10-6 升高温度
(3)小于 小于
(4)CN-+CO+HO===HCN+HCO
2 2
(5)测定等物质的量浓度的两种酸的pH,氢氟酸的pH大(其他合理答案均可)
【解析】(1)根据三种酸的电离常数可知,酸性:HF>H CO>HCN>HCO,因此c(H+)相同的三种酸,其酸
2 3
的浓度由大到小的顺序为c(HCN)>c(H CO)>c(HF)。(2)设c(H+)=x mol·L-1,根据HCNH++CN-,K
2 3 a
=5.0×10-10==,解得x≈×10-6;弱电解质的电离是吸热过程,升高温度,能够促进 HCN的电离,电离程
度增大,c(H+)也增大。(3)中和等量的NaOH,需要消耗等物质的量的H+,当氢氟酸和硫酸的pH相等时,
由于硫酸是强酸,氢氟酸为弱酸,氢氟酸浓度大于硫酸,需要氢氟酸的体积小于硫酸的体积,即 a小于
b。氢氟酸为一元酸、硫酸为二元酸,中和等物质的量浓度、等体积的氢氟酸和硫酸需要 NaOH的物质的量之比为1∶2,即n 小于n 。(4)酸性:HF>H CO>HCN>HCO。向NaCN中通入少量的 CO 反应生成
1 2 2 3 2
HCN和NaHCO ,反应的离子方程式为CN-+CO +HO===HCN+HCO。(5)证明氢氟酸比盐酸的酸性弱
3 2 2
可以使用的方法有:①测定等物质的量浓度的两种酸的pH,氢氟酸的pH大;②等物质的量浓度的两种酸
分别与Zn反应,初始氢氟酸冒气泡慢;③测定等物质的量浓度的两种溶液的导电性,连接氢氟酸的灯泡
较暗等。
15.(12分)25℃时,三种酸的电离平衡常数如下:
化学式 CHCOOH HCO HClO
3 2 3
K=4.3×10-7 3.0×10-8
1
电离平衡常数 1.8×10-5
K=5.6×10-11
2
回答下列问题:
(1)一般情况下,当温度升高时,Ka________(填“增大”、“减小”或“不变”)。
(2)下列四种离子结合质子能力由大到小的顺序是______________________(填字母)。
a.CO 2- b.ClO- c.CH COO- d.HCO-
3 3 3
(3)下列反应不能发生的是________(填字母)。
a. CO2-+2CHCOOH=2CHCOO-+CO↑+HO
3 3 3 2 2
b. ClO-+CHCOOH=CHCOO-+HClO
3 3
c. CO2-+2HClO=CO↑+HO+2ClO- d. 2ClO-+CO+HO=CO2-+2HClO
3 2 2 2 2 3
(4)25℃时,若测得CHCOOH与CHCOONa的混合溶液的pH=6,则溶液中c(CHCOO-)-c(Na+)=
3 3 3
___mol·L-1(填精确数值)。
(5)体积均为10 mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000 mL,稀释过程中pH变化如
下图所示。
稀释后,HX溶液中水电离出来的c(H+)_____ (填“>”、“=”或“<”,下同)醋酸溶液中水电离出来的c(H
+);用同浓度的NaOH溶液分别中和上述两种酸溶液,恰好中和时消耗NaOH溶液的体积:醋酸____HX。
【答案】(每空2分)(1)增大 (2)a>b>d>c (3) cd (4)9.9×10-7 moL·L-1 (5)> >
【解析】(1)升高温度促进弱电解质的电离,所以当温度升高时,K 增大。
a
(2)电离平衡常数越大,越易电离,溶液中离子浓度越大,则酸性强弱为:
CHCOOH>H CO>HClO>HCO -,酸根离子对应的酸的酸性越强,酸根离子结合氢离子的能力越弱,则四
3 2 3 3
种离子结合质子的能力由大到小的顺序是:CO2->ClO->HCO->CH COO-,即a>b>d>c。
3 3 3
(3)a.CO2-+CH COOH═CH COO-+CO ↑+H O:碳酸的酸性小于CHCOOH,所以CHCOOH能够制取
3 3 3 2 2 3 3
碳酸,该反应能够发生,故a错误;b.ClO-+CH COOH═CH COO-+HClO:CHCOOH的酸性大于HClO,
3 3 3CHCOOH能够制取HClO,该反应能够发生,故b错误;c.CO2-+HClO═CO ↑+H O+ClO-:HClO的酸性
3 3 2 2
小于碳酸,该反应无法发生,故c正确;故选cd。d.2ClO-+CO +H O═CO 2-+2HClO:由于酸性
2 2 3
HCO>HClO>HCO -,则碳酸与次氯酸根离子反应只能生成碳酸氢根离子,不会生成CO2-,该反应不能发
2 3 3 3
生,故d正确;
(4)根据电荷守恒得c(CHCOO-)-c(Na+)=c(H+)-c(OH-)=(10-6-10-8)mol·L-1=
3
9.9×10-7mol·L-1。
(5)加水稀释促进弱酸电离,pH相同的不同酸稀释相同的倍数,pH变化大的酸酸性强,变化小的酸酸性
弱;酸或碱抑制水电离,酸中氢离子或碱中氢氧根离子浓度越大其抑制水电离程度越大,根据图知,pH相
同的醋酸和HX稀释相同的倍数,HX的pH变化大,则HX的酸性大于醋酸,所以HX的电离平衡常数大
于常数,稀释后醋酸中氢离子浓度大于HX,所以醋酸抑制水电离程度大于HX,则HX溶液中水电离出来
的c(H+)大于醋酸溶液水电离出来c(H+);溶液中氢离子浓度越小,对的抑制程度越小,水的电离程度
越大,稀释后HX溶液中的c(H+)小于CHCOOH溶液中的c(H+),它对水的电离的抑制能力减弱。
3
1.(2023·浙江·高考真题)硫酸铜应用广泛,下列说法不正确的是
A. 元素位于周期表p区 B.硫酸铜属于强电解质
C.硫酸铜溶液呈酸性 D.硫酸铜能使蛋白质变性
【答案】A
【解析】A.Cu为29号元素,位于IB族,属于ds区元素,故A错误;B.硫酸铜属于盐类,在水溶液中
能完全电离,属于强电解质,故B正确;C.硫酸铜为强酸弱碱盐,铜离子水解使溶液呈酸性,故C正确;
D.铜离子为重金属离子,能使蛋白质变性,故D正确;故选:A。
2.(2022·浙江·统考高考真题)下列物质属于强电解质的是
A. B. C. D.
【答案】C
【解析】A. 是弱酸,在水溶液中只能部分电离,属于弱电解质,A不合题意;B. 是单质,不
是电解质,B不合题意;C. 是盐,在水溶液中能够完全电离,故属于强电解质,C符合题意;
D. 是有机物,在水溶液和熔融状态下均不导电,属于非电解质,D不合题意;故答案为:C。
3.(2022·浙江·统考高考真题)已知25℃时二元酸HA的K =1.3×10-7,K =7.1×10-15。下列说法正确的是
2 a1 a2
A.在等浓度的NaA、NaHA溶液中,水的电离程度前者小于后者
2
B.向0.1mol·L-1的HA溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,则HA的电离度为0.013%
2 2
C.向HA溶液中加入NaOH溶液至pH=11,则c(A2-)>c(HA-)
2
D.取pH=a的HA溶液10mL,加蒸馏水稀释至100mL,则该溶液pH=a+1
2
【答案】B
【解析】A.在等浓度的NaA、NaHA溶液中,A2-的水解程度大于HA-,水的电离程度前者大于后者,故
2
A错误;B.溶液中c(H+)=10-3mol/L,HA电离程度较小,溶液中c(HA)≈0.1mol/L,K =
2 2 a1,c(HA-)=1.3×10-5mol/L,c(HA-)≈c(HA) ,则HA的电离度
2 电离 2
0.013%,故B正确;C.向HA溶液中加入NaOH溶液至pH=11,
2
,则c(A2-)