文档内容
第 28 讲 电离平衡
(模拟精练+真题演练)
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12×5分)
1.(2023·浙江金华·模拟预测)下列物质中属于强电解质且水溶液显酸性的是
A.盐酸 B.AlCl C.CHCOOH D.NaSiO
3 3 2 3
2.(2023·全国·模拟预测)实验测得浓度均为 的 溶液和 溶液的pH随温
度的变化情况如图所示。下列说法错误的是
A. 时, 的电离平衡常数约为
B. 后, 溶液的pH随温度的升高而增大的原因可能是 的挥发
C.升高温度, 溶液中 减小, 增大,pH减小
D. 溶液中存在:
3.(2023·浙江·校联考模拟预测)下列说法不正确的是
A.相同温度下, 相等的氨水、 溶液中, 相等
B. 的醋酸溶液的物质的量浓度大于 的醋酸溶液的10倍
C. 均为4的盐酸和氯化铵溶液等体积混合后,所得溶液的
D.用同浓度的 溶液分别与等体积、等 的盐酸和醋酸溶液恰好完全反应,盐酸消耗 溶液的
体积更大
4.(2023·上海奉贤·统考二模)以下物质属于弱电解质的是
A.乙醇 B.乙酸 C.次氯酸钠 D.高锰酸钾
5.(2023·江西宜春·江西省宜丰中学校考模拟预测)化学常用图像直观地描述化学反应的进程或结果。下
列图像描述不正确的是
1A.图①表示弱电解质在水中建立电离平衡的过程
B.图②表示强碱滴定强酸的滴定曲线
C.图③表示25℃时分别稀释pH=11的NaOH溶液和氨水时溶液pH的变化,曲线Ⅱ表示氨水
D.图④可表示 溶液中通入 至过量的过程中溶液导电性的变化
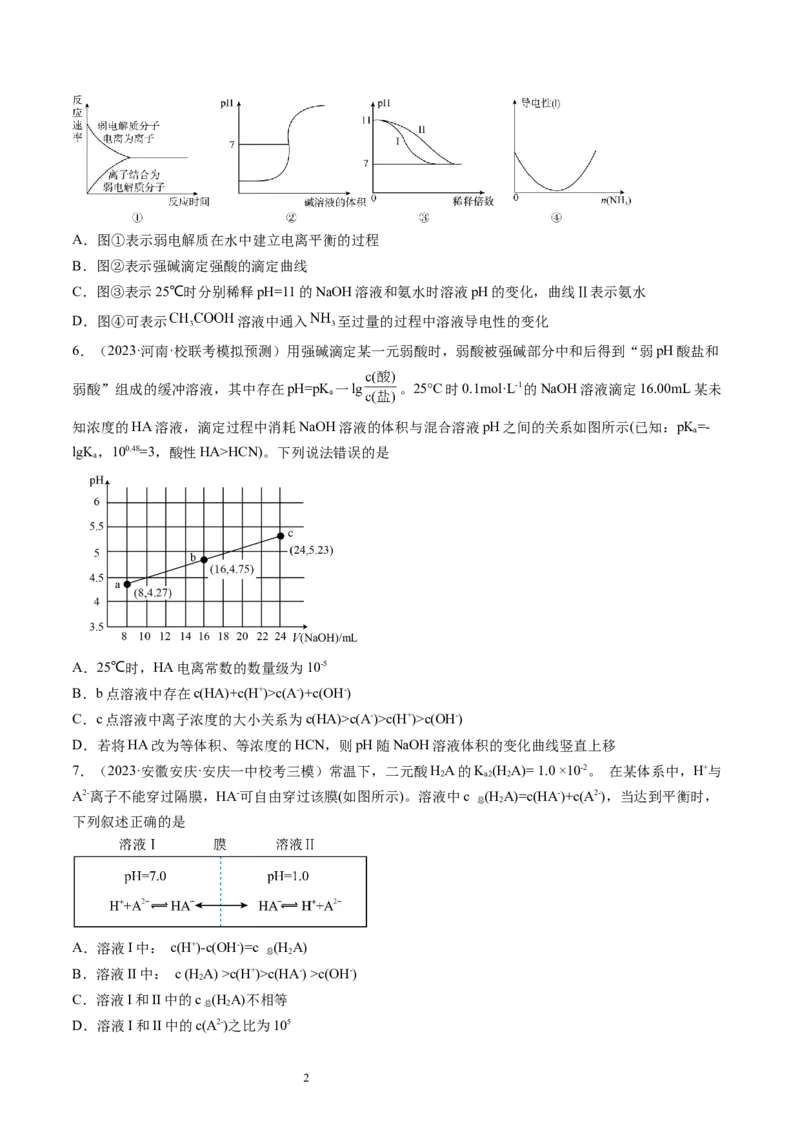
6.(2023·河南·校联考模拟预测)用强碱滴定某一元弱酸时,弱酸被强碱部分中和后得到“弱pH酸盐和
弱酸”组成的缓冲溶液,其中存在pH=pK 一lg 。25°C时0.1mol·L-1的NaOH溶液滴定16.00mL某未
a
知浓度的HA溶液,滴定过程中消耗NaOH溶液的体积与混合溶液pH之间的关系如图所示(已知:pK=-
a
lgK,100.48=3,酸性HA>HCN)。下列说法错误的是
a
A.25℃时,HA电离常数的数量级为10-5
B.b点溶液中存在c(HA)+c(H+)>c(A-)+c(OH-)
C.c点溶液中离子浓度的大小关系为c(HA)>c(A-)>c(H+)>c(OH-)
D.若将HA改为等体积、等浓度的HCN,则pH随NaOH溶液体积的变化曲线竖直上移
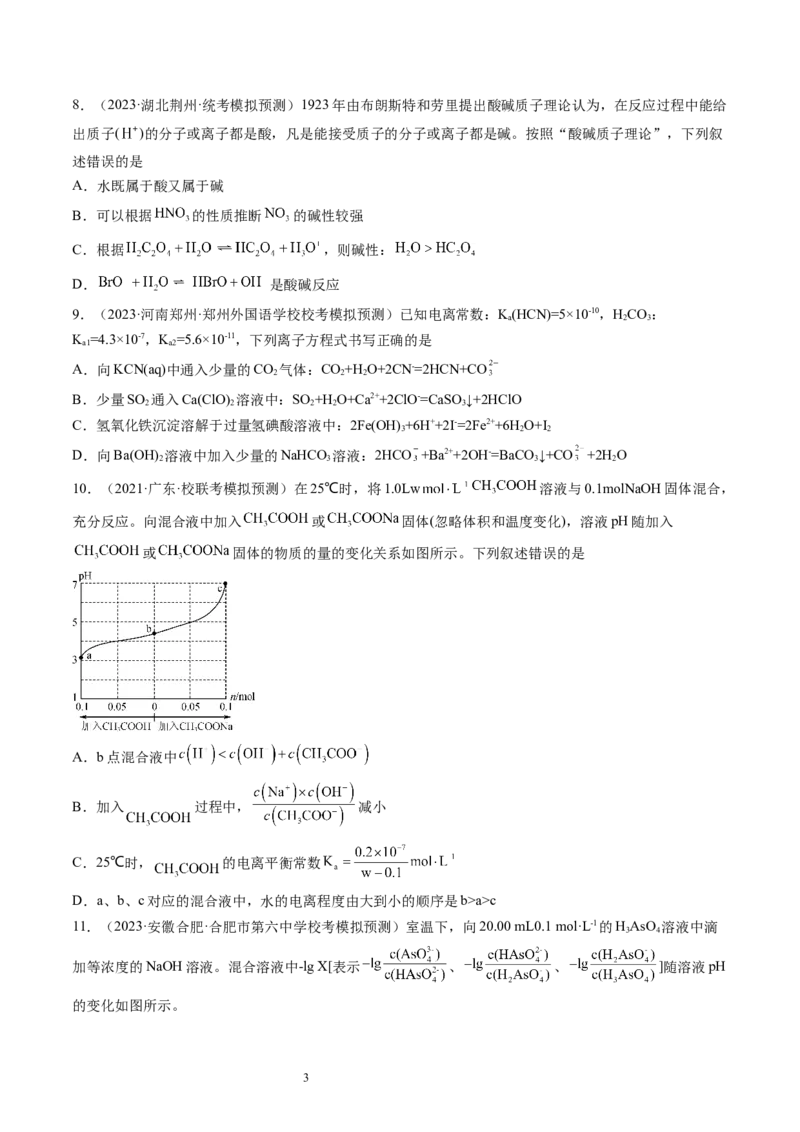
7.(2023·安徽安庆·安庆一中校考三模)常温下,二元酸HA的K (H A)= 1.0 ×10-2。 在某体系中,H+与
2 a2 2
A2-离子不能穿过隔膜,HA-可自由穿过该膜(如图所示)。溶液中c (H A)=c(HA-)+c(A2-),当达到平衡时,
总 2
下列叙述正确的是
A.溶液I中: c(H+)-c(OH-)=c (H A)
总 2
B.溶液II中: c (H A) >c(H+)>c(HA-) >c(OH-)
2
C.溶液I和II中的c (H A)不相等
总 2
D.溶液I和II中的c(A2-)之比为105
28.(2023·湖北荆州·统考模拟预测)1923年由布朗斯特和劳里提出酸碱质子理论认为,在反应过程中能给
出质子( )的分子或离子都是酸,凡是能接受质子的分子或离子都是碱。按照“酸碱质子理论”,下列叙
述错误的是
A.水既属于酸又属于碱
B.可以根据 的性质推断 的碱性较强
C.根据 ,则碱性:
D. 是酸碱反应
9.(2023·河南郑州·郑州外国语学校校考模拟预测)已知电离常数:K(HCN)=5×10-10,HCO:
a 2 3
K =4.3×10-7,K =5.6×10-11,下列离子方程式书写正确的是
a1 a2
A.向KCN(aq)中通入少量的CO 气体:CO+H O+2CN-=2HCN+CO
2 2 2
B.少量SO 通入Ca(ClO) 溶液中:SO +H O+Ca2++2ClO-=CaSO ↓+2HClO
2 2 2 2 3
C.氢氧化铁沉淀溶解于过量氢碘酸溶液中:2Fe(OH) +6H++2I-=2Fe2++6H O+I
3 2 2
D.向Ba(OH) 溶液中加入少量的NaHCO 溶液:2HCO +Ba2++2OH-=BaCO ↓+CO +2H O
2 3 3 2
10.(2021·广东·校联考模拟预测)在25℃时,将1.0Lw 溶液与0.1molNaOH固体混合,
充分反应。向混合液中加入 或 固体(忽略体积和温度变化),溶液pH随加入
或 固体的物质的量的变化关系如图所示。下列叙述错误的是
A.b点混合液中
B.加入 过程中, 减小
C.25℃时, 的电离平衡常数
D.a、b、c对应的混合液中,水的电离程度由大到小的顺序是b>a>c
11.(2023·安徽合肥·合肥市第六中学校考模拟预测)室温下,向20.00 mL0.1 mol·L-1的HAsO 溶液中滴
3 4
加等浓度的NaOH溶液。混合溶液中-lg X[表示 、 、 ]随溶液pH
的变化如图所示。
3下列说法正确的是
A.曲线a表示 与溶液pH的关系
B.当消耗20.00 mL的NaOH溶液时,c(Na+ )> > >
C.pH=7.00时,c (Na+) = 3 +3
D.溶液中存在关系: >
12.(2023·河北衡水·衡水市第二中学校考三模)常温下,用 盐酸滴定 MOH溶液,
滴定曲线如图所示。下列叙述正确的是
A. 的数量级为
B.X→Y过程中,水的电离程度及 均逐渐增大
C.当滴定至溶液呈中性时,
D.Y点溶液中:
二、主观题(共3小题,共40分)
13.(14分)(2023·四川成都·成都七中校考模拟预测)I.研究水溶液中的粒子行为在研究中具有重要价值。
根据下表所列三种溶液在25℃时的相关数据,按要求填空:
溶液 物质的量浓度 pH
(I)HAc 0.1 mol/L 2.86
(II) 0.1 mol/L 6.14
(III) 0.1 mol/L 1
(1)根据表中数据,写出HAc的电离方程式
4(2)比较溶液(II)、(III)中 的大小关系是(II) (III)(填“>”、“<”或“=”)。
(3)溶液(I)和(II)中由水电离出的 之比是 。
II.某小组研究25℃下HAc电离平衡的影响因素。
提出假设 稀释HAc溶液或改变 浓度,HAc电离平衡会发生移动。
设计方案并完成实验 用浓度均为0.1 mol·L 的HAc和NaAc溶液,按下表配制总体积相同的系列溶液;
测定pH,记录数据。
序
V(HAc)/mL V(NaAc)/mL /mL pH
号
I 40.00 / / 0 2.86
II 4.00 / 36.00 0 3.36
VII 4.00 a b 3∶4 4.53
VIII 4.00 4.00 32.00 1∶1 4.65
(4)根据表中信息,补充数据:a= ,b= 。
(5)由实验I和II可知,稀释HAc溶液,电离平衡 (填“正”或“逆”)向移动;结合表中数据,给
出判断理由: 。由实验II~VIII可知,增大 浓度,HAc电离平衡逆向移动。
实验结论 假设成立。
14.(14分)(2023·济南一模)常温下,部分酸的电离常数如表所示:
化学式 HF HCN HCO
2 3
电离 K= K= K =4.4×10-7
a a a1
常数 3.5×10-4 5.0×10-10 K =4.7×10-11
a2
(1)c(H+)相同的三种酸,其酸的浓度由大到小的顺序为_____________。
(2)若HCN的起始浓度为0.01 mol·L-1,平衡时c(H+)约为______________mol·L-1。若使此溶液中HCN的
电离程度增大且c(H+)也增大的方法是______________。
(3)中和等量的NaOH,消耗等pH的氢氟酸和硫酸的体积分别为 a L、b L,则a________b(填“大于”
“小于”或“等于”,下同)。
中和等物质的量浓度、等体积的氢氟酸和硫酸需要NaOH的物质的量为n、n,则n________n。
1 2 1 2
(4)向NaCN溶液中通入少量的CO,发生反应的离子方程式为______________________________________
2
_________________________________。
(5)设计实验证明氢氟酸比盐酸的酸性弱:__________________________。
15.(12分)25℃时,三种酸的电离平衡常数如下:
化学式 CHCOOH HCO HClO
3 2 3
电离平衡常数 1.8×10-5 K=4.3×10-7 3.0×10-8
1
5K=5.6×10-11
2
回答下列问题:
(1)一般情况下,当温度升高时,Ka________(填“增大”、“减小”或“不变”)。
(2)下列四种离子结合质子能力由大到小的顺序是______________________(填字母)。
a.CO 2- b.ClO- c.CH COO- d.HCO-
3 3 3
(3)下列反应不能发生的是________(填字母)。
a. CO2-+2CHCOOH=2CHCOO-+CO↑+HO
3 3 3 2 2
b. ClO-+CHCOOH=CHCOO-+HClO
3 3
c. CO2-+2HClO=CO↑+HO+2ClO- d. 2ClO-+CO+HO=CO2-+2HClO
3 2 2 2 2 3
(4)25℃时,若测得CHCOOH与CHCOONa的混合溶液的pH=6,则溶液中c(CHCOO-)-c(Na+)=
3 3 3
___mol·L-1(填精确数值)。
(5)体积均为10 mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000 mL,稀释过程中pH变化如
下图所示。
稀释后,HX溶液中水电离出来的c(H+)_____ (填“>”、“=”或“<”,下同)醋酸溶液中水电离出来的c(H
+);用同浓度的NaOH溶液分别中和上述两种酸溶液,恰好中和时消耗NaOH溶液的体积:醋酸____HX。
1.(2023·浙江·高考真题)硫酸铜应用广泛,下列说法不正确的是
A. 元素位于周期表p区 B.硫酸铜属于强电解质
C.硫酸铜溶液呈酸性 D.硫酸铜能使蛋白质变性
2.(2022·浙江·统考高考真题)下列物质属于强电解质的是
A. B. C. D.
3.(2022·浙江·统考高考真题)已知25℃时二元酸HA的K =1.3×10-7,K =7.1×10-15。下列说法正确的是
2 a1 a2
A.在等浓度的NaA、NaHA溶液中,水的电离程度前者小于后者
2
B.向0.1mol·L-1的HA溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,则HA的电离度为0.013%
2 2
C.向HA溶液中加入NaOH溶液至pH=11,则c(A2-)>c(HA-)
2
D.取pH=a的HA溶液10mL,加蒸馏水稀释至100mL,则该溶液pH=a+1
2
4.(2018·浙江·校联考高考真题)相同温度下,关于盐酸和醋酸两种溶液的比较,下列说法正确的是
A.pH相等的两溶液中:
B.分别中和pH相等、体积相等的两溶液,所需NaOH的物质的量相同
6C.相同浓度的两溶液,分别与NaOH固体反应后呈中性的溶液中
D.相同浓度的两溶液,分别与金属镁反应,反应速率相同
5.(2021·浙江·高考真题)下列物质属于弱电解质的是
A.CO B.HO C.HNO D.NaOH
2 2 3
6.(2021·浙江·统考高考真题)25℃时,下列说法正确的是
A.NaHA溶液呈酸性,可以推测HA为强酸
2
B.可溶性正盐BA溶液呈中性,可以推测BA为强酸强碱盐
C.0.010 mol·L-1、0.10mol·L-1的醋酸溶液的电离度分别为α 、α ,则α <α
1 2 1 2
D.100 mL pH=10.00的NaCO 溶液中水电离出H+的物质的量为1.0×10-5mol
2 3
7