文档内容
第 38 讲 卤代烃 醇 酚
目录
考情分析
考点二 醇、酚、醚
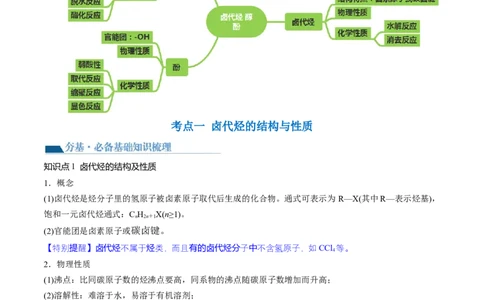
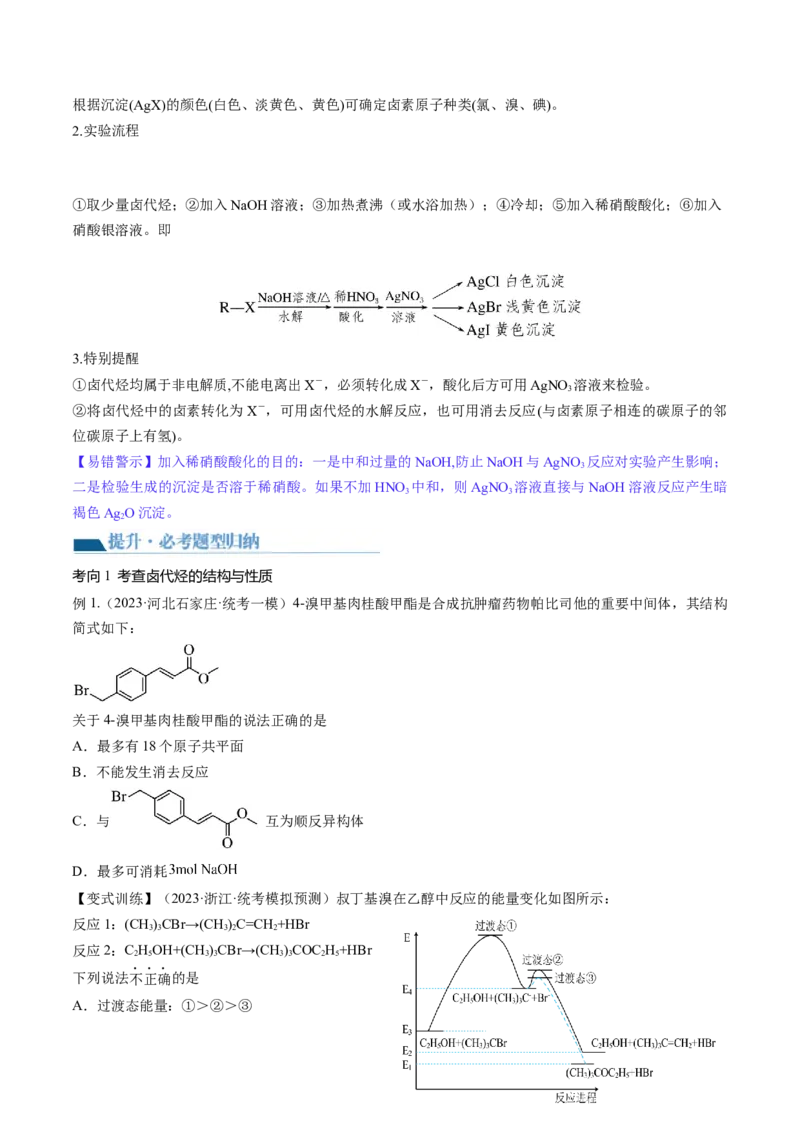
网络构建
【夯基·必备基础知识梳理】
考点一 卤代烃的结构与性质 知识点1 醇、酚、醚的结构
【夯基·必备基础知识梳理】 知识点2 醇、酚、醚的性质
知识点1 卤代烃的结构及性质 【提升·必考题型归纳】
知识点2 卤代烃的检验 考向1 考查醇的结构与性质
【提升·必考题型归纳】 考向2 考查酚的结构与性质
考向1 考查卤代烃的结构与性质
真题感悟
考向2 考查卤代烃的检验
考向3 考查卤代烃在有机合成中的作用
考点要求 考题统计 考情分析
2023海南卷11题,3分 一、分析近三年高考试题,高考命题在本讲有以下规律:
卤代烃的结构与 2022北京卷3题,3分 1.从考查题型和内容上看,高考命题以选择题和非选择题
性质 2021湖南卷13题,3分 呈现,考查内容主要有以下两个方面:
(1)卤代烃的组成、结构特点和性质。
(2)考查卤代烃、醇、酚、醚的性质与结构的关系;
(3)考查卤代烃、醇、酚、醚的同分异构体等。
2.从命题思路上看,侧重
(1)卤代烃在有机合成中的应用考查。
2023湖北卷4题,3分
醇、酚、醚的结 (2)以陌生有机物的结构简式为情境载体考查醇、酚
2022浙江6月卷15题,2分
构与性质 的重要性质。
2021全国甲卷10题,6分
二、根据高考命题的特点和规律,复习时要注意以下几
个方面:
(1)卤代烃、醇、酚、醚的官能团;
(2)卤代烃、醇、酚、醚的典型代表物的性质及检
验;(3)卤代烃、醇、酚、醚的同分异构体的书写规律;
(4)卤代烃、醇、酚、醚之间的相互转化。
考点一 卤代烃的结构与性质
知识点1 卤代烃的结构及性质
1.概念
(1)卤代烃是烃分子里的氢原子被卤素原子取代后生成的化合物。通式可表示为 R—X(其中R—表示烃基),
饱和一元卤代烃通式:C H X(n≥1)。
n 2n+1
(2)官能团是卤素原子或碳卤键。
【特别提醒】卤代烃不属于烃类,而且有的卤代烃分子中不含氢原子,如CCl 等。
4
2.物理性质
(1)沸点:比同碳原子数的烃沸点要高,同系物的沸点随碳原子数增加而升高;
(2)溶解性:难溶于水,易溶于有机溶剂;
(3)密度:一般一氟代烃、一氯代烃比水小,其余比水大。
(4)常温常压下,除CHCl、CHCHCl等少数为气体外,其余为液体或固体。
3 3 2
3.化学性质
(1)水解反应
①反应条件:氢氧化钠的水溶液、加热。
②C HBr在碱性条件下水解的化学方程式为C HBr+NaOH――→C HOH+NaBr。
2 5 2 5 2 5
③用R—CH—X表示卤代烃,碱性条件下水解的化学方程式为
2
R—CH—X+NaOH――→R—CHOH+NaX。
2 2(2)消去反应
①概念:有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(如HO、HBr等),而生成含不
2
饱和键化合物的反应。
②卤代烃消去反应条件:氢氧化钠的醇溶液、加热。
③溴乙烷发生消去反应的化学方程式为CHCHBr+NaOH――→CH===CH ↑+NaBr+HO。
3 2 2 2 2
④用R—CH—CH—X表示卤代烃,消去反应的化学方程式为
2 2
R—CH—CH—X+NaOH――→R—CH==CH +NaX+HO。
2 2 2 2
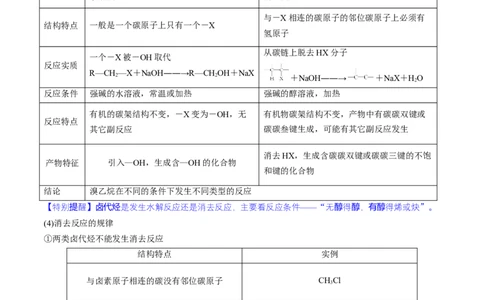
(3)卤代烃的水解反应和消去反应的比较
反应类型 水解反应 消去反应
与-X相连的碳原子的邻位碳原子上必须有
结构特点 一般是一个碳原子上只有一个-X
氢原子
从碳链上脱去HX分子
一个-X被-OH取代
反应实质
R—CH—X+NaOH――→R—CHOH+NaX
2 2 +NaOH――→ +NaX+HO
2
反应条件 强碱的水溶液,常温或加热 强碱的醇溶液,加热
有机的碳架结构不变,-X变为-OH,无 有机物碳架结构不变,产物中有碳碳双键或
反应特点
其它副反应 碳碳叁键生成,可能有其它副反应发生
消去HX,生成含碳碳双键或碳碳三键的不饱
产物特征 引入—OH,生成含—OH的化合物
和键的化合物
结论 溴乙烷在不同的条件下发生不同类型的反应
【特别提醒】卤代烃是发生水解反应还是消去反应,主要看反应条件——“无醇得醇,有醇得烯或炔”。
(4)消去反应的规律
①两类卤代烃不能发生消去反应
结构特点 实例
与卤素原子相连的碳没有邻位碳原子 CHCl
3
与卤素原子相连的碳有邻位碳原子,但邻位
碳原子上无氢原子
、
②有两种或三种邻位碳原子,且碳原子上均带有氢原子时,发生消去反应可生成不同的产物。例如:
+NaOH――→CH==CH—CH —CH(或CH—CH==CH—CH )+NaCl+HO
2 2 3 3 3 2③ 型卤代烃,发生消去反应可以生成R—C≡C—R,如
BrCHCHBr+2NaOH――→CH≡CH↑+2NaBr+2HO
2 2 2
4.获取方法
(1)取代反应,如:
①苯与Br 反应的化学方程式:
2
。
②C HOH与HBr反应的化学方程式:
2 5
C HOH+HBr――→C HBr+HO。
2 5 2 5 2
(2)不饱和烃的加成反应,如:
①丙烯与Br 反应的化学方程式:
2
CH===CHCH+Br ――→CHBrCHBrCH
2 3 2 2 3
②丙烯与 HBr反应的化学方程式:
CH—CH===CH +HBr――→CH—CHBr—CH (或CH—CH—CHBr)。
3 2 3 3 3 2 2
③乙炔与HCl制氯乙烯的化学方程式:
CH≡CH+HCl――→CH===CHCl。
2
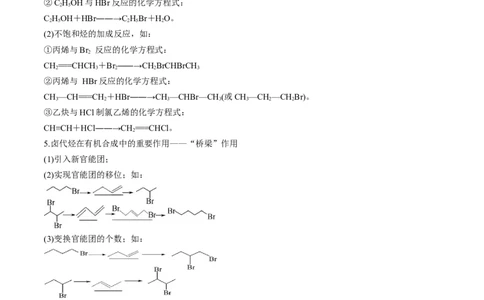
5.卤代烃在有机合成中的重要作用——“桥梁”作用
(1)引入新官能团;
(2)实现官能团的移位;如:
(3)变换官能团的个数;如:
(4)增长碳链;
(5)成环等。
6.卤代烃对环境、健康产生的影响
氟氯烃在大气平流层中会破坏臭氧层,是造成臭氧空洞的主要原因。
知识点2 卤代烃的检验
1.实验原理:
R—X+HO R—OH +HX、HX+NaOH=NaX+H O HNO+NaOH=NaNO +H O、
2 2 3 3 2
AgNO+NaX=AgX↓+NaNO
3 3根据沉淀(AgX)的颜色(白色、淡黄色、黄色)可确定卤素原子种类(氯、溴、碘)。
2.实验流程
①取少量卤代烃;②加入NaOH溶液;③加热煮沸(或水浴加热);④冷却;⑤加入稀硝酸酸化;⑥加入
硝酸银溶液。即
3.特别提醒
①卤代烃均属于非电解质,不能电离出X-,必须转化成X-,酸化后方可用AgNO 溶液来检验。
3
②将卤代烃中的卤素转化为X-,可用卤代烃的水解反应,也可用消去反应(与卤素原子相连的碳原子的邻
位碳原子上有氢)。
【易错警示】加入稀硝酸酸化的目的:一是中和过量的NaOH,防止NaOH与AgNO 反应对实验产生影响;
3
二是检验生成的沉淀是否溶于稀硝酸。如果不加HNO 中和,则AgNO 溶液直接与NaOH溶液反应产生暗
3 3
褐色Ag O沉淀。
2
考向1 考查卤代烃的结构与性质
例1.(2023·河北石家庄·统考一模)4-溴甲基肉桂酸甲酯是合成抗肿瘤药物帕比司他的重要中间体,其结构
简式如下:
关于4-溴甲基肉桂酸甲酯的说法正确的是
A.最多有18个原子共平面
B.不能发生消去反应
C.与 互为顺反异构体
D.最多可消耗
【变式训练】(2023·浙江·统考模拟预测)叔丁基溴在乙醇中反应的能量变化如图所示:
反应1:(CH)CBr→(CH)C=CH +HBr
3 3 3 2 2
反应2:C HOH+(CH )CBr→(CH)COC H+HBr
2 5 3 3 3 3 2 5
下列说法不正确的是
A.过渡态能量:①>②>③B.(CH)COC H 可以逆向转化为(CH)CBr,但不会转化为(CH)C=CH
3 3 2 5 3 3 3 2 2
C.若将上述反应体系中的叔丁基溴改为叔丁基氯,则E—E 的值增大
4 3
D.向(CH)CBr的乙醇溶液中加入NaOH并适当升温,可以得到较多的(CH)C=CH
3 3 3 2 2
考向2 考查卤代烃的检验
例2.(2023·全国·高三)为检验某卤代烃(R-X)中的X元素,有下列实验操作:①加热煮沸;②加入
AgNO 溶液;③取少量卤代烃;④加入稀硝酸酸化;⑤加入氢氧化钠溶液;⑥冷却。正确操作的先后顺序
3
是
A.③①⑤⑥②④ B.③②①⑥④⑤ C.③⑤①⑥④② D.③⑤①⑥②④
【变式训练】(2023·广东佛山·统考二模)卤代烃的水解反应常伴随消去反应的发生。溴乙烷与NaOH水
溶液共热一段时间后,下列实验设计能达到对应目的的是
A.观察反应后溶液的分层现象,检验溴乙烷是否完全反应
B.取反应后溶液滴加 溶液,检验是否有 生成
C.取反应后溶液加入一小块金属Na,检验是否有乙醇生成
D.将产生的气体通入酸性 溶液,检验是否有乙烯生成
考向3 考查卤代烃在有机合成中的作用
例3.(2023秋·江苏苏州·高三统考开学考试)格氏试剂(RMgX)与醛、酮反应是制备醇的重要途径。化合
物Y的一种制备方法如下:
已知:CHCHMgBr易水解,反应X→Z需在无水条件下进行。下列说法正确的是
3 2
A.X、Y、Z分子中均含有手性碳原子
B.CHCHMgBr水解可生成CHCH 与Mg(OH)Br
3 2 3 3
C.Z在NaOH醇溶液中加热能发生消去反应
D.以CHCOCH 、CHMgBr和水为原料也可制得Y
3 3 3
【变式训练】(2023·安徽黄山·统考三模)化合物3是一种药物合成的重要中间体,其合成路线如图所示。
下列说法错误的是
A.化合物1中所有的碳原子可能共面B.化合物2能发生消去反应生成双键
C.化合物3中存在两个手性碳
D.化合物1、2、3均能在碱性条件下水解生成酚类物质
考点二 醇、酚、醚
知识点1 醇、酚、醚的结构
1.醇、酚、醚的概念
(1)醇是羟基与链烃基或苯环侧链上的碳原子相连的化合物,饱和一元醇的分子通式为C H OH(n≥1)。
n 2n+1
(2)酚是羟基与苯环直接相连而形成的化合物,最简单的酚为苯酚或 。
(3)醚是由一个氧原子连接两个烷基或芳基所形成,醚的通式为:R–O–R。醚类化合物都含有醚键。它还可
看作是醇或酚羟基上的氢被烃基所取代的化合物。
2.醇的分类
(1)分类:
(2)几种常见的醇
名称 甲醇 乙二醇 丙三醇
俗称 木精、木醇 甘油
结构简式 CHOH
3
状态 无色液体,有毒 无色黏稠液体 无色黏稠液体
熔沸点、 沸点低易挥发、易
与水和乙醇互溶
溶解性 溶于水
化工生产、车用燃 发动机防冻液、合成 制造化妆品、三硝
用途
料 高分子的原料 酸甘油酯
3.醚的分类
(1)根据烃基是否相同可以分为:
①两个烃基相同的醚成为对称醚,也叫简单醚。
②两个烃基不相同的醚称为不对称醚,也叫混合醚。(2)根据两个烃基的类别,醚还可以分为脂肪醚和芳香醚。在脂肪醚中,分子中不是由氧原子和碳原子
结合成环状醚结构的醚称为无环醚。还可细分为饱和醚和不饱和醚。有氧原子和碳原子结合成环状醚结构
的醚称为环醚。环上含氧的醚称为内醚或环氧化合物。含有多个氧的大环醚因形如皇冠称之为冠醚。
4.醇、酚、醚的命名
1)醇的命名
①选择含有与-OH相连的碳原子的最长碳链为主链,根据碳原子数目称某醇;
②从距离-OH最近的一端给主链碳原子依次编号;
③醇的名称前面要用阿拉伯数字标出羟基的位置;羟基的个数用“二”“三”等表示。
2)酚的命名
①去除酚羟基,留下苯环或苯的同系物,先命名上述名称,例如,甲(基)苯,乙(基)苯。
②加上酚羟基,看在苯环的什么位置,共有邻、间、对三个位置,例如甲苯,在除甲基外的正六边形上依
次分别标上12345,共5个位置,其中15,24位置相同,则1位为邻位,2位为间位,3位为对位,那么酚
羟基在哪个位置上,就叫X甲苯酚。以此类推。
【易错警示】(1)从物质分类看,石炭酸不属于羧酸。
(2)酚羟基的氢原子比醇羟基的氢原子易电离,是因为苯环对羟基产生影响。
3)醚的命名
一般醚以与氧相连的烃基加醚字命名,例如,C H─O─C H 称二乙基醚,简称乙醚,CH─O─C H 称
2 5 2 5 3 2 5
甲基乙基醚,简称甲乙醚。环醚一般用俗名。
知识点2 醇、酚、醚的性质
1.醇类、苯酚、醚的物理性质
1)醇类物理性质的变化规律
(1)溶解性:低级脂肪醇易溶于水。饱和一元醇的溶解度随着分子中碳原子数的递增而逐渐减小
(2)密度:一元脂肪醇的密度一般小于1 g·cm-3。
(3)沸点
①直链饱和一元醇的沸点随着分子中碳原子数的递增而逐渐升高。
②醇分子间存在氢键,所以相对分子质量相近的醇和烷烃相比,醇的沸点远远高于烷烃。
【易错警示】醇羟基是亲水基,多羟基化合物如丙三醇等都易溶于水或与水以任意比例互溶。碳原子数多的
一元醇水溶性差。
2)苯酚的物理性质
(1)纯净的苯酚是无色晶体,有特殊气味,易被空气氧化呈粉红色。
(2)苯酚常温下在水中的溶解度不大,当温度高于65℃时,能与水混溶,苯酚易溶于酒精。
(3)苯酚有毒,对皮肤有强烈的腐蚀作用,如果不慎沾到皮肤上应立即用酒精洗涤。
3)醚的物理性质
(1)多数醚是易挥发、易燃的无色液体,有香味,沸点低,比水轻,性质稳定。与醇不同,醚分子之间不能
形成氢键,所以沸点比同组分醇的沸点低得多,如乙醇的沸点为 78.4℃,甲醚的沸点为-24.9℃;正丁醇的沸
点为117.8℃,乙醚的沸点为34.6℃。
(2)多数醚不溶于水,但环状醚类如常用的四氢呋喃和1,4-二氧六环却能和水完全互溶,这是由于二者和水形成氢键。乙醚的碳氧原子数虽然和四氢呋喃的相同,但因后者的氧和碳架共同形成环,氧原子突出在外,
容易和水形成氢键,而乙醚中的氧原子"被包围"在分子之中,难以和水形成氢键,所以乙醚只能稍溶于水。
2.醇类、苯酚的化学性质
1)由断键方式理解醇的化学性质(以乙醇为例)
反应物
断键位置 反应类型 化学方程式
及条件
Na ① 置换反应 2CHCHOH+2Na―→2CHCHONa+H↑
3 2 3 2 2
HBr,△ ② 取代反应 CHCHOH+HBr――→CHCHBr+HO
3 2 3 2 2
O
2
①③ 氧化反应 2CHCHOH+O――→2CHCHO+2HO
3 2 2 3 2
(Cu,△)
浓硫酸,
②⑤ 消去反应 CHCHOH――→CH===CH ↑+HO
3 2 2 2 2
170 ℃
浓硫酸,
①② 取代反应 2CHCHOH――→CHCHOCH CH+HO
3 2 3 2 2 3 2
140 ℃
CHCOOH
3
① 酯化反应 CHCOOH+CHCHOH――→CHCOOCH CH+HO
3 3 2 3 2 3 2
(浓硫酸)
【特别提醒】 (1)醇能否发生催化氧化及氧化产物类型取决于醇分子中是否有α-H及其个数:
(2)醇能否发生消去反应取决于醇分子中是否有β-H,若β碳原子上没有氢原子,则不能发生消去反应。
2)由基团之间的相互影响理解酚的化学性质
(1)苯环对羟基的影响——弱酸性
由于苯环对羟基的影响,使酚羟基比醇羟基更活泼,可以发生电离。①苯酚的电离方程式为C HOH C HO-+H+。苯酚俗称石炭酸,但酸性很弱,不能使石蕊溶液变红。
6 5 6 5
②与碱的反应:苯酚的浑浊液――→现象为液体变澄清――→现象为溶液又变浑浊。
该过程中发生反应的化学方程式分别为
。
。
③与活泼金属反应:
(2)羟基对苯环的影响——苯环上邻对位氢原子的取代反应
由于羟基对苯环的影响,使苯酚中苯环上的氢比苯分子中的氢活泼。苯酚稀溶液中滴入过量的浓溴水中产
生现象为:产生白色沉淀。其化学方程式为:
。
【易错警示】①在苯酚与溴水的取代反应实验中,苯酚取少量,滴入的溴水要过量。这是因为生成的三溴苯
酚易溶于苯酚等有机溶剂,使沉淀溶解,不利于观察实验现象。②苯酚分子中羟基邻对位的H原子易被取代,
是因为羟基对苯环产生影响。
(3)显色反应:苯酚溶液中滴如FeCl 溶液,溶液变为紫色。
3
(4)氧化反应:苯酚易被空气中的氧气氧化而显粉红色,易被酸性KMnO 溶液氧化,易燃烧。
4
(5)缩聚反应:苯酚与甲醛在催化剂作用下,可发生缩聚反应,化学方程式是:
+(n-1)H O。
2
【特别提醒】苯酚是重要的医用消毒剂和化工原料,广泛用于制造酚醛树脂、染料、医药、农药等。酚类
化合物均有毒,是重点控制的水污染物之一。苯酚有毒,浓溶液对皮肤有强腐蚀性,如皮肤不慎沾上苯酚
溶液,应立即用酒精洗涤,再用水冲洗。
3)醇和酚的性质比较
类别 脂肪醇 芳香醇 酚
实例 CHCHOH C HCHCHOH C HOH
3 2 6 5 2 2 6 5
官能团 —OH —OH —OH—OH与芳香烃侧链
结构特点 —OH与链烃基相连 —OH与苯环直接相连
上的碳原子相连
(1)弱酸性
(1)与钠反应;(2)取代反应;(3)脱水反应;
主要化学性质 (2)取代反应
(4)氧化反应;(5)酯化反应
(3)显色反应
将红热的铜丝插入醇中有刺激性气味产生
特性 遇FeCl 溶液显紫色
3
(生成醛或酮)
考向1 考查醇的结构与性质
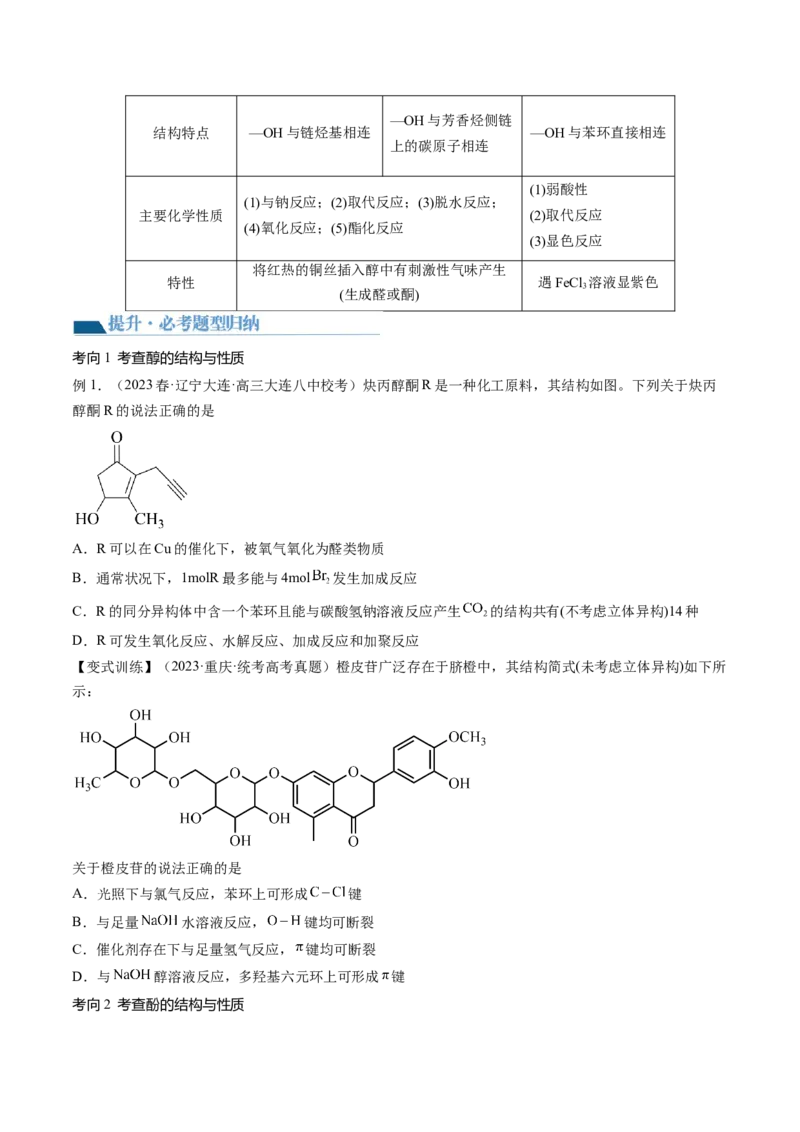
例1.(2023春·辽宁大连·高三大连八中校考)炔丙醇酮R是一种化工原料,其结构如图。下列关于炔丙
醇酮R的说法正确的是
A.R可以在Cu的催化下,被氧气氧化为醛类物质
B.通常状况下,1molR最多能与4mol 发生加成反应
C.R的同分异构体中含一个苯环且能与碳酸氢钠溶液反应产生 的结构共有(不考虑立体异构)14种
D.R可发生氧化反应、水解反应、加成反应和加聚反应
【变式训练】(2023·重庆·统考高考真题)橙皮苷广泛存在于脐橙中,其结构简式(未考虑立体异构)如下所
示:
关于橙皮苷的说法正确的是
A.光照下与氯气反应,苯环上可形成 键
B.与足量 水溶液反应, 键均可断裂
C.催化剂存在下与足量氢气反应, 键均可断裂
D.与 醇溶液反应,多羟基六元环上可形成 键
考向2 考查酚的结构与性质例2.(2023·四川成都·石室中学校考模拟预测)某种兴奋剂的结构简式如图所示。下列有关该化合物的说
法正确的是
A.该化合物的分子式为C H O
15 14 3
B.分子中所有碳原子一定在个平面上
C.该化合物的同分异构体中一定有苯环
D.该化合物可以发生加成、加聚、氧化、还原、取代反应
【变式训练】(2023·黑龙江哈尔滨·哈师大附中校考模拟预测)大豆素为主要成分的大豆异黄酮及其衍生
物,因其具有优良的生理活性而备受关注,其结构简式如图所示。下列说法正确的是
A.含有三种官能团
B.分子式为C H O
15 12 4
C.可以发生加成、氧化和取代反应
D.1mol该物质最多可以与4mol Br 反应
2
1.(2022·北京·高考真题)利用如图所示装置(夹持装置略)进行实验,b中现象不能证明a中产物生成的是
a中反应 b中检测试剂及现象
A 浓 分解生成 淀粉 溶液变蓝
B 与浓 生成 品红溶液褪色
C 浓 与 溶液生成 酚酞溶液变红
D 与 乙醇溶液生成丙 溴水褪色烯
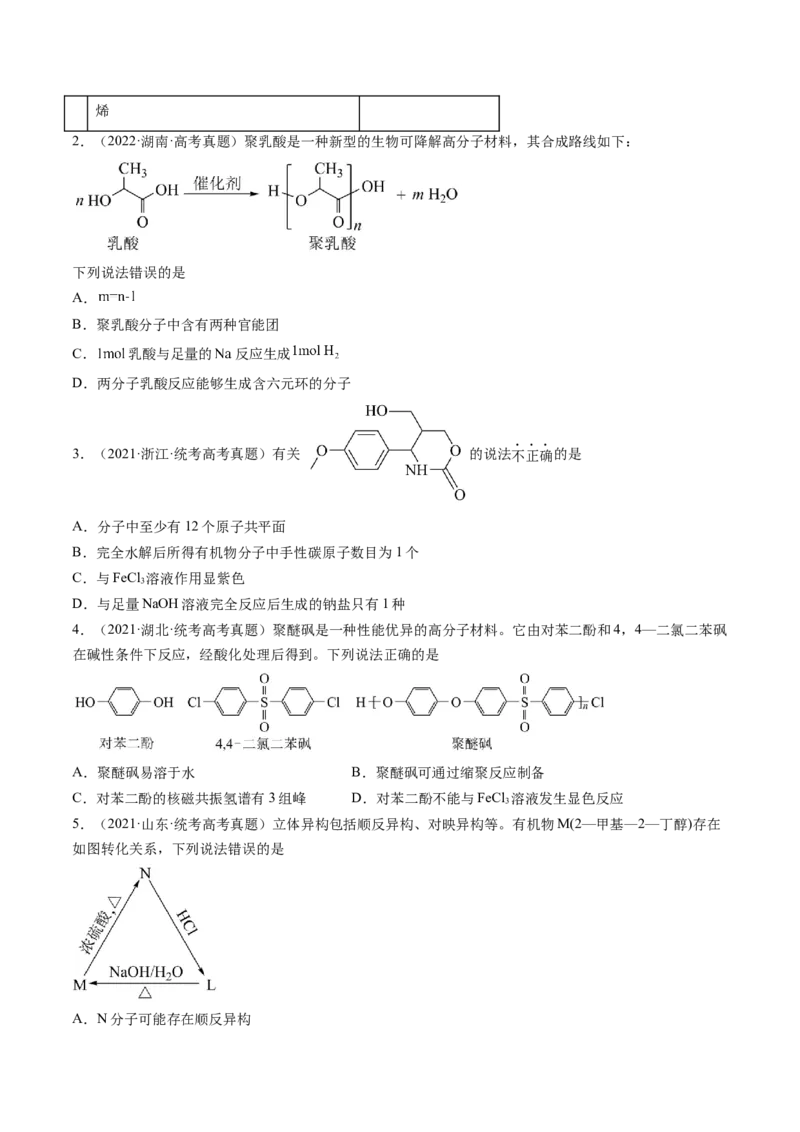
2.(2022·湖南·高考真题)聚乳酸是一种新型的生物可降解高分子材料,其合成路线如下:
下列说法错误的是
A.
B.聚乳酸分子中含有两种官能团
C. 乳酸与足量的 反应生成
D.两分子乳酸反应能够生成含六元环的分子
3.(2021·浙江·统考高考真题)有关 的说法不正确的是
A.分子中至少有12个原子共平面
B.完全水解后所得有机物分子中手性碳原子数目为1个
C.与FeCl 溶液作用显紫色
3
D.与足量NaOH溶液完全反应后生成的钠盐只有1种
4.(2021·湖北·统考高考真题)聚醚砜是一种性能优异的高分子材料。它由对苯二酚和4,4—二氯二苯砜
在碱性条件下反应,经酸化处理后得到。下列说法正确的是
A.聚醚砜易溶于水 B.聚醚砜可通过缩聚反应制备
C.对苯二酚的核磁共振氢谱有3组峰 D.对苯二酚不能与FeCl 溶液发生显色反应
3
5.(2021·山东·统考高考真题)立体异构包括顺反异构、对映异构等。有机物M(2—甲基—2—丁醇)存在
如图转化关系,下列说法错误的是
A.N分子可能存在顺反异构B.L的任一同分异构体最多有1个手性碳原子
C.M的同分异构体中,能被氧化为酮的醇有4种
D.L的同分异构体中,含两种化学环境氢的只有1种
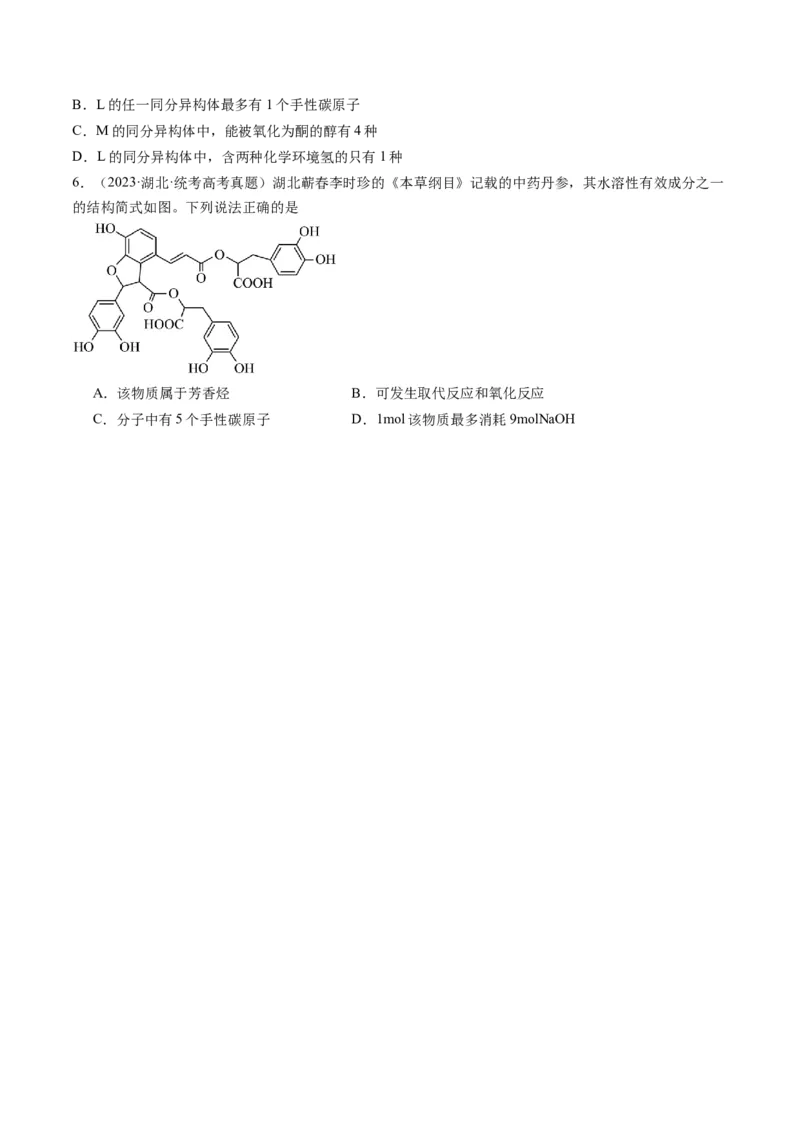
6.(2023·湖北·统考高考真题)湖北蕲春李时珍的《本草纲目》记载的中药丹参,其水溶性有效成分之一
的结构简式如图。下列说法正确的是
A.该物质属于芳香烃 B.可发生取代反应和氧化反应
C.分子中有5个手性碳原子 D.1mol该物质最多消耗9molNaOH