文档内容
专题 15 晶体结构与性质
第 44 练 金属晶体与离子晶体
1.构成金属晶体的基本微粒是( )
A.分子 B.原子
C.阳离子与阴离子 D.阳离子与自由电
子
2.从严格意义上讲石墨属于( )
A.分子晶体 B.原子晶体 C.金属晶体 D.混合型晶体
3.下列各类物质中,固态时只能形成离子晶体的是( )
A.非金属氧化物 B.非金属单质 C.强酸 D.强碱
4.下列性质中,可以较充分说明某晶体是离子晶体的是( )
A.具有较高的熔点 B.固态不导电,水溶液能导电
C.可溶于水 D.固态不导电,熔融状态能导电
5.离子晶体不可能具有的性质是( )
A.较高的熔、沸点 B.良好的导电性
C.溶于极性溶剂 D.坚硬而易粉碎
6.下列说法正确的是( )
A.晶体中若存在阴离子,就一定存在阳离子
B.离子晶体不一定是化合物
C.离子晶体都易溶于水
D.离子晶体一定是由活泼金属和活泼非金属形成的
7.Al O 的下列性质能用晶格能解释的是( )
2 3
A.Al O 可用作耐火材料 B.固态时不导电,熔融时能导电
2 3
C.Al O 是两性氧化物 D.晶体Al O 可以作宝石
2 3 2 3
8.下列有关离子晶体的数据大小比较,不正确的是( )
A.熔点:NaF>MgF >AlF B.晶格能:NaF>NaCl>NaBr
2 3
C.阴离子的配位数:CsCl>NaCl>CaF D.硬度:MgO>CaO>BaO
2
9.下列生活中的问题,不能用电子气理论知识解释的是( )
A.铁易生锈 B.用金属铝制成导线
C.用金箔做外包装 D.用铁制品做炊具10.物质结构理论推出:金属键越强,其金属的硬度越大,熔、沸点越高。且研究表明,一般来说,
金属阳离子半径越小,所带电荷越多,则金属键越强,由此判断下列说法错误的是( )
A.硬度:Mg>Al B.熔、沸点:Mg>Ca
C.硬度:Mg>K D.熔、沸点:Ca>K
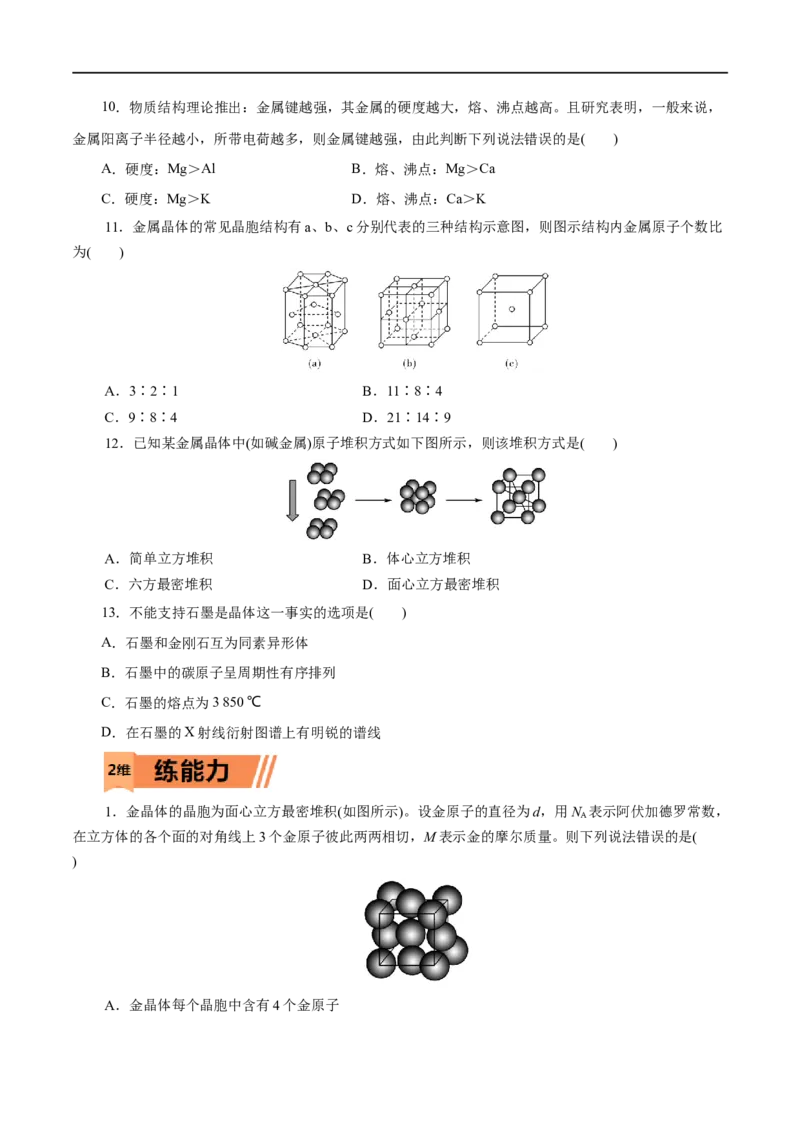
11.金属晶体的常见晶胞结构有a、b、c分别代表的三种结构示意图,则图示结构内金属原子个数比
为( )
A.3∶2∶1 B.11∶8∶4
C.9∶8∶4 D.21∶14∶9
12.已知某金属晶体中(如碱金属)原子堆积方式如下图所示,则该堆积方式是( )
A.简单立方堆积 B.体心立方堆积
C.六方最密堆积 D.面心立方最密堆积
13.不能支持石墨是晶体这一事实的选项是( )
A.石墨和金刚石互为同素异形体
B.石墨中的碳原子呈周期性有序排列
C.石墨的熔点为3 850 ℃
D.在石墨的X射线衍射图谱上有明锐的谱线
1.金晶体的晶胞为面心立方最密堆积(如图所示)。设金原子的直径为d,用N 表示阿伏加德罗常数,
A
在立方体的各个面的对角线上3个金原子彼此两两相切,M表示金的摩尔质量。则下列说法错误的是(
)
A.金晶体每个晶胞中含有4个金原子B.金属键无方向性,金属原子尽可能采取密堆积
C.一个晶胞的体积是16d3
D.金晶体的密度是
2.关于体心立方堆积型晶体(如图)的结构的叙述中正确的是( )
A.是密置层的一种堆积方式 B.晶胞是六棱柱
C.每个晶胞内含2个原子 D.每个晶胞内含6个原子
3.教材中给出了几种晶体的晶胞如图所示:
所示晶胞分别表示的物质正确的排序是( )
A.碘、锌、钠、金刚石 B.金刚石、锌、碘、钠
C.钠、锌、碘、金刚石 D.锌、钠、碘、金刚石
4.下列说法正确的是( )
A.第三周期主族元素从左到右,最高价氧化物中离子键的百分数逐渐增大
B.大多数晶体都是过渡晶体
C.过渡晶体是指某些物质的晶体通过改变条件,转化为另一种晶体
D.NaO 是纯粹的离子晶体,SiO 是纯粹的共价晶体
2 2
5.NaF、NaI、和MgO均为离子晶体,有关数据如下表:
物质 ①NaF ②NaI ③MgO
离子电荷数 1 1 2
键长(10-10m) 2.31 3.18 2.10
试判断,这三种化合物的熔点由高到低的顺序是( )
A.①>②>③ B.③>①>②
C.③>②>① D.②>①>③
6.下列性质适合于离子晶体的是( )
A.熔点1 070 ℃,易溶于水,水溶液能导电
B.熔点10.31 ℃,液态不导电,水溶液能导电
C.能溶于CS,熔点112.8 ℃,沸点444.6 ℃
2
D.熔点97.81 ℃,质软,导电,密度0.97 g·cm-37.有一种蓝色晶体,化学式可表示为M[Fe(CN) ],经X射线研究发现,它的结构特征是Fe3+和Fe2
x y 6
+分别占据立方体互不相邻的顶点,而CN-位于立方体的棱上。其晶体中阴离子的最小结构单元如图所示。
下列说法正确的是( )
A.该晶体的化学式为M[Fe (CN) ]
2 2 6
B.该晶体属于离子晶体,M呈+1价
C.该晶体属于离子晶体,M呈+2价
D.晶体中与每个Fe3+距离最近且相等的CN-有3个
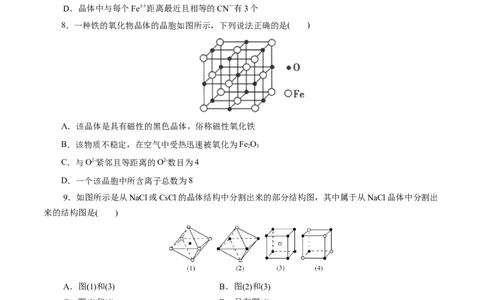
8.一种铁的氧化物晶体的晶胞如图所示,下列说法正确的是( )
A.该晶体是具有磁性的黑色晶体,俗称磁性氧化铁
B.该物质不稳定,在空气中受热迅速被氧化为Fe O
2 3
C.与O2-紧邻且等距离的O2-数目为4
D.一个该晶胞中所含离子总数为8
9.如图所示是从NaCl或CsCl的晶体结构中分割出来的部分结构图,其中属于从NaCl晶体中分割出
来的结构图是( )
A.图(1)和(3) B.图(2)和(3)
C.图(1)和(4) D.只有图(4)
1.金属钠晶体为体心立方晶胞(如图),实验测得钠的密度为ρ(g·cm-3)。已知钠的相对原子质量为a,
阿伏加德罗常数为N (mol-1),假定金属钠原子为等径的钢性球且处于体对角线上的三个球相切。则钠原子
A
的半径r(cm)为( )A. B.·
C.· D.·
2.如图,铁有δ、γ、α三种同素异形体,三种晶体在不同温度下能发生转化。下列说法不正确的是
( )
δFe γ Fe αFe
A.δFe晶体中与每个铁原子等距离且最近的铁原子有8个
B.αFe晶体中与每个铁原子等距离且最近的铁原子有6个
C.若δFe晶胞边长为a cm,αFe晶胞边长为b cm,则两种晶体密度比为2b3∶a3
D.将铁加热到1 500 ℃分别急速冷却和缓慢冷却,得到的晶体类型相同
3. 是第四周期元素,其原子最外层只有 个电子,次外层的所有原子轨道均充满电子。元素 的负
一价离子的最外层电子数与次外层电子数相同。下列说法错误的是( )
A.单质 的晶体类型为金属晶体
B.已知单质 是面心立方最密堆积,其中 原子的配位数为
C.元素 的基态原子的核外电子排布式为
D. 与 形成的一种化合物的立方晶胞如图所示。该化合物的化学式为
4.有四种不同堆积方式的金属晶体的晶胞如图所示,下列有关说法正确的是( )A.图1和图4为非密置层堆积,图2和图3为密置层堆积
B.图1~图4分别是简单立方堆积、六方最密堆积、面心立方最密堆积、体心立方堆积
C.图1~图4每个晶胞所含有原子数分别为1、2、2、4
D.图1~图4堆积方式的空间利用率大小关系是图1<图2<图3=图4
4.有四种不同堆积方式的金属晶体的晶胞如图所示(原子半径为rcm),下列叙述错误的是( )
A.晶胞中原子的配位数分别为:①6,②8,③12,④12
B.晶胞①的空间利用率:
C.晶胞中含有的原子数分别为:③2,④4,
D.金属晶体是一种“巨分子”,可能存在分子间作用力
5.已知金属钠和氦可形成化合物,该化合物晶胞如下图所示,其结构中Na+按简单立方分布,形成
Na 立方体空隙,电子对(2e-)和氮原子交替分布填充在小立方体的中心。下列说法中错误的是( )
8
A.该晶胞中的Na+数为8
B.该化合物的化学式 [ Na+]He [e ]2-
2 2
C.若将原子放在晶胞顶点,则所有电子对(2e-)在晶胞的体心
D.该晶胞中 最近的He原子数目为4
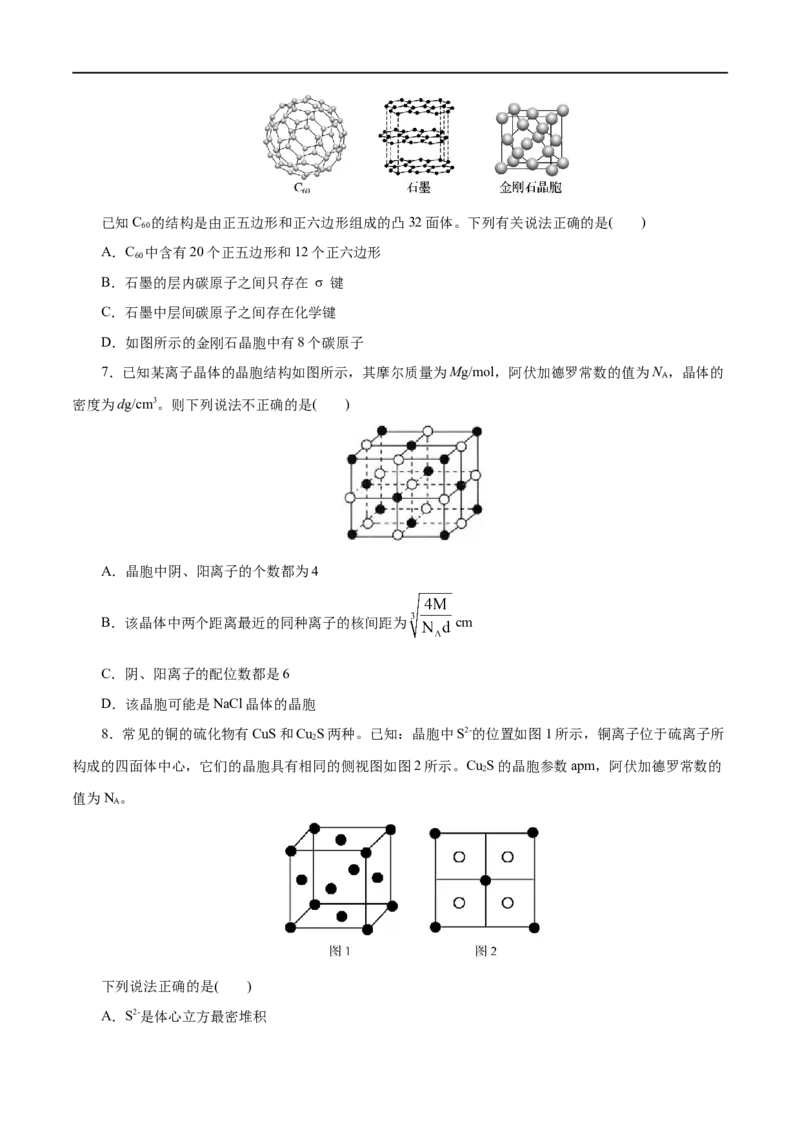
6.碳元素有多种同素异形体,其中C 、石墨与金刚石的结构如图所示。
60已知C 的结构是由正五边形和正六边形组成的凸32面体。下列有关说法正确的是( )
60
A.C 中含有20个正五边形和12个正六边形
60
B.石墨的层内碳原子之间只存在 σ 键
C.石墨中层间碳原子之间存在化学键
D.如图所示的金刚石晶胞中有8个碳原子
7.已知某离子晶体的晶胞结构如图所示,其摩尔质量为Mg/mol,阿伏加德罗常数的值为N ,晶体的
A
密度为dg/cm3。则下列说法不正确的是( )
A.晶胞中阴、阳离子的个数都为4
B.该晶体中两个距离最近的同种离子的核间距为 cm
C.阴、阳离子的配位数都是6
D.该晶胞可能是NaCl晶体的晶胞
8.常见的铜的硫化物有CuS和Cu S两种。已知:晶胞中S2-的位置如图1所示,铜离子位于硫离子所
2
构成的四面体中心,它们的晶胞具有相同的侧视图如图2所示。Cu S的晶胞参数apm,阿伏加德罗常数的
2
值为N 。
A
下列说法正确的是( )
A.S2-是体心立方最密堆积B.Cu S晶胞中,Cu+填充了晶胞中一半四面体空隙
2
C.CuS晶胞中,S2-配位数为8
D.Cu S晶胞的密度为
2